145、合欢花165-288,其该中药组合物可以增加脑组织5-羟色胺的含量。
8.本发明还提供了该中药组合物在增加超氧化歧化酶含量中的应用。
9.本发明还提供了该中药组合物在上调脑干及海马区神经生长因子、上调血管活性肠肽表达中的应用。
10.本发明还保护该中药组合物在该组合物在抑制促肾上腺皮质激素释放激素、促肾上腺皮质激素、肾上腺皮质激素中的应用。
11.本发明中药组合物可以由如下重量份比例的原料药制成的:何首乌158酸枣仁270桑椹165灵芝135百合80知母110丹参125菊花118茯苓80合欢花280。
12.本发明中药组合物也可以由如下重量份比例的原料药制成的:何首乌265酸枣仁147桑椹250灵芝81百合158知母55丹参188菊花50茯苓145合欢花170。
13.本发明中药组合物还可以由如下重量份比例的原料药制成的:何首乌225酸枣仁163桑椹220灵芝83百合113知母50丹参193菊花45茯苓113合欢花178。
14.本发明中药组合物也可由如下重量份比例的原料药制成的:何首乌200酸枣仁200桑椹200灵芝100百合100知母66.7丹参166.7菊花66.7茯苓100合欢花200。
15.本发明所述的中药组合物制剂剂型为胶囊剂、片剂、散剂、口服液、丸剂或注射剂。
16.其片剂是由如下步骤组成:a)按比例称取选净的何首乌、知母及选净粗碎的酸枣仁,加6-12倍量30%-70%乙醇,加热回流提取1-3次,每次1-3小时,提取液过滤,合并,减压回收乙醇,浓缩至在60℃测定相对密度为1.10-1.15,得醇提浸膏,备用;b)按比例称取选净的桑椹、茯苓、灵芝、丹参、合欢花、菊花,加10-15倍量水提取1-3次,每次提取1-3小时,提取液滤过,合并,浓缩至在60℃测定相对密度约为1.10-1.15,得水提浸膏,备用;c)按比例称取选净的百合,粉碎成100目粉,备用;d)将步骤a)所得醇提浸膏和步骤b)的水提浸膏及步骤c)所得百合细粉干燥制粒,整粒后,加入适当辅料,混匀,压片,包衣,即得。
附图说明
17.图1:ngf的表达,注control、m、as、es、h、m、l分别表示正常对照组、模型组、安神补脑液组、艾司唑仑片组、本发明药物组合物高剂量组、本发明药物组合物中剂量组、本发明药物组合物低剂量组。
18.图2:vip的表达,注control、m、as、es、h、m、l分别表示正常对照组、模型组、安神补脑液组、艾司唑仑片组、本发明药物组合物高剂量组、本发明药物组合物中剂量组、本发明药物组合物低剂量组。
具体实施方式
19.下面结合具体实施方式对本发明做进一步详细说明:实施例1:原料药配方为:何首乌200克酸枣仁200克桑椹200克灵芝100克百合100克知母66.7克丹参166.7克菊花66.7克茯苓100克合欢花200克中药组合物片剂的制备方法为:a)按比例称取选净的何首乌、知母及选净粗碎的酸枣仁,加60%乙醇,加热回流提取2次,第一次加10倍量,提取2小时,第二次加8倍量,提取1小时,提取液过滤,合并,减压回收乙醇,浓缩至在60℃测定相对密度为1.10,得醇提浸膏,备用;b)按比例称取选净的桑椹、茯苓、灵芝、丹参、合欢花、菊花,加11倍量水提取2次,每次1.5小时,提取液过滤,合并,浓缩至在60℃测定相对密度约为1.10,得水提浸膏,备用;c)按比例称取选净的百合,粉碎成100目粉,备用;d)将步骤c)所得百合细粉加入喷雾干燥制粒机原料容器内,将步骤a)所得醇提浸膏和步骤b)的水提浸膏喷入,喷雾制粒,整粒后,加入0.5%硬脂酸镁,混匀,压片,包衣,即得。
20.实施例2:原料药配方为:何首乌158克酸枣仁270克桑椹165克灵芝135克百合80克知母110克丹参125克菊花118克茯苓80克合欢花280克。
21.中药组合物胶囊剂的制备方法为:a)按比例称取选净的何首乌、知母及选净粗碎的酸枣仁,加6倍量30%乙醇,加热回流提取3次,每次3小时,提取液过滤,合并,减压回收乙醇,浓缩至在60℃测定相对密度为1.15,得醇提浸膏,备用;b)按比例称取选净的桑椹、茯苓、灵芝、丹参、合欢花、菊花,加10倍量水提取3次,每次提取3小时,提取液滤过,合并,浓缩至在60℃测定相对密度约为1.15,得水提浸膏,备用;c)按比例称取选净的百合,粉碎成100目粉,备用;d)将步骤a)所得醇提浸膏和步骤b)的水提浸膏及步骤c)所得百合细粉干燥制粒,整粒后,加入适当辅料,混匀,填充胶囊,即得。
22.实施例3:原料药配方为:何首乌265克酸枣仁147克桑椹250克灵芝81克百合158克知母55克丹参188克菊花50克茯苓145克合欢花170克。
23.中药组合物丸剂的制备方法为:a)按比例称取选净的何首乌、知母及选净粗碎的酸枣仁,加12倍量70%乙醇,加热回流提取2次,每次2小时,提取液过滤,合并,减压回收乙醇,浓缩至在60℃测定相对密度为1.12,得醇提浸膏,备用;b)按比例称取选净的桑椹、茯苓、灵芝、丹参、合欢花、菊花,加15倍量水提取2次,
每次提取2小时,提取液滤过,合并,浓缩至在60℃测定相对密度约为1.12,得水提浸膏,备用;c)按比例称取选净的百合,粉碎成100目粉,备用;d)将步骤a)所得醇提浸膏和步骤b)的水提浸膏及步骤c)所得百合细粉按照常规方法制成丸剂,即得。
24.试验例取按照实施例1制得的本发明药物组合物压片前的颗粒进行如下研究。
25.方法:取检疫合格的spf级sd大鼠120只,雌雄各半,体重150-200g,采用咖啡因与环磷酰胺腹腔注射同时配合水环境法干预制作大鼠失眠模型,共计4周。 取失眠模型的大鼠,按体重顺序随机分为6个组,14只/组,雌雄各半,分别为供试品高剂量组(7.2g生药/kg)、 供试品中剂量组(3.6g生药/kg)、 供试品低剂量组(1.8g生药/kg)、 阳性对照1组(给予艾司唑仑片,给药剂量为0.6mg/kg)、 阳性对照2组(给予安神补脑液,给药剂量为2ml/kg)和模型组。 再取检疫合格 未造模的sd大鼠14只作为正常对照组。模型组和正常对照组给予0.5 % (g/ml) 的羧甲基纤维素钠溶液。各组动物连续给药28d,1次/d。 每日进行一般症状观察。 试验结束后采用morris水迷宫分析学习记忆及空间认知功能的变化,elisa检测血清中下丘脑-垂体-肾上腺轴的激素水平以及脑组织中5-羟色胺(5-ht)含量、超氧化物岐化酶(sod)活力的变化;荧光定量rt-pcr和免疫组化法检测脑干及海马部位神经生长因子(ngf)和血管活性肠肽(vip)的表达;he染色观察 脑 、脑垂体、肾上腺组织病理形态学改变。
26.结果:睡眠剥夺大鼠在morris水迷宫中穿越平台次数增多,探索时间百分比增加,hpa轴较正常组明显活跃,血清中促肾上腺皮质激素释放激素(crh)、促肾上腺皮质激素(acth)、肾上腺皮质激素(ach)均不同程度升高,脑干及海马组织中5-ht含量明显减少,脑组织中sod活力降低,海马区ngf和vip表达下降。与模型组比较,本发明药物组合物高、中、低剂量组均能不同程度减少morris水迷宫的穿越平台次数,降低探索时间百分比,抑制hpa轴激素水平,增加脑内5-ht、sod含量,促进海马区ngf和vip的表达。
27.结论:本发明药物组合物对咖啡因与环磷酰胺腹腔注射同时配合水环境法所致失眠大鼠具有调控ach、acth、 crh、 5-ht、 sod、 vip和ngf等关键因子的作用。
28.1材料与方法1.1供试品名称:本发明药物组合物颗粒规格/含量:0.4 g/片;3.64 g生药/g颗粒批号:b1904001。
29.性状:棕褐色颗粒, 气微, 味苦。
30.生产日期:2019.04.09有效期至:2022.04.08保存条件:密封保存。
31.2实验系统2.1实验动物2.1.1名称:大鼠 。
32.2.1.2种系:sd。
33.2.1.3实验动物数量:实验使用数量为134只。
34.2.1.4实验动物性别:雌雄各半。
35.2.1.5实验动物体重范围:150-200g 。
36.2.1.6实验动物等级:spf级。
37.2.1.7实验动物来源:长沙天勤生物技术有限公司。
38.2.1.8实验动物生产许可证号:scxk(湘)2014-0011。
39.2.1.9实验动物质犹合格证:n21107261911000053 。
40.2.1.10实验动物使用许可证号:syxk(琼)2016-0013。
41.2.1.11实验动物采购、运输及接收实验动物采购、运输与接收具体操作按中心“sop-04-ma-020-00实验动物采购、运输及接收“执行。
42.2.1.11.1实验动物的采购经中心动物伦理委员会同意,并在“实验动物使用审核表”上签字,请购者填写“form-04-ma-o 10-00实验动物请购单”注明请购动物的种类、品系、日龄或/和体重、性别、数量、动物级别及专题代号等信息。
43.2.1.11.2实验动物的运输和接收不同种类和等级的动物分开装运。spf级大鼠的接收按spf级实验动物的接收标准执行,填写“form-04-ma-o 12-00实验动物接收单”,门口相应位置处放置动物实验室(饲养室)管理卡,并注明相关信息。实验动物接收时间: 2019.08.27。
44.2. 2动物饲料2.2.1名称:spf级鼠料。
45.2.2.2配制标准:符合gb-14924.3-2010标准。
46.2.2.3饲料合格证号:11002900022860。
47.2.2.4主要成分:spf级鼠料主要原料为玉米、面粉、麸皮、秘鲁鱼粉、豆粕、磷酸氢钙、石粉、植物油、盐、赖氨酸、蛋氨酸、维生素和复合矿物质等。
48.2.2.5包装:2kg/袋,6袋/箱,钴60辐照(25kgy)灭菌。
49.2.2.6存储条件:放置于阴凉、干燥、隔热、通风处,环境温度低于25
°
c,湿度70%以内,保质期为6个月。
50.2.2.7生产厂家:广东省医学实验动物中心2.3实验动物饮水实验动物饮用中心自制的灭菌水,进行理化指标及微生物指标检测,所检测项目结果均符合现行国家《生活饮用水卫生标准》(gb5749-2006)规定的限值要求。
51.2.4方法2.4.1动物分组和给药方法取检疫合格的spf级sd大鼠120只,雌雄各半,体重150~200g,采用咖啡因与环磷酰胺腹腔注射同时配合水环境法干预制作大鼠失眠模型,共计4周。取造模成功的大鼠,按体重顺序随机分为6个组,14只/组,雌雄各半。分别为供试品高剂量组(给药剂量为7.2g生药/kg)、供试品中剂量组(给药剂量为3.6g生药/kg)、供试品低剂量组(给药剂量为1.8g生药/kg)、阳性对照1 组(给予艾司唑仑片,给药剂量为0.6mg/kg)、阳性对照2组(给予安神补脑液,给药剂量为2ml/kg)和模型组,再取检疫合格未造模的spf级sd大鼠14只作为正常对照组。模型组和正常对照组给予0.5% (g/ml)的羧甲基纤维素钠溶液。
52.2.4.2剂量设计2.4.2.1失眠造模剂量设计咖啡因:购自北京中科华标生物技术研究院。按60mg/kg/d腹腔注射造模,共计4周。
53.注射用环磷酰胺,按100mg/kg/d进行腹腔注射造模,共计4周。
54.2.4.2.2本发明药物组合物给药组剂量设计本发明药物组合物委拟人临床用剂量为17.0g生药/天,即0.28 g生药/kg体重(标准体重60kg),本实验设本发明药物组合物高剂量、中、低剂量组,给药剂量分别7.2g生药/kg、3.6g生药/kg、1.8g生药/kg(分别相当于临床剂量的26、13、6.5倍),给药浓度分别为200、100、50mg药粉/ml。
55.2.4.2.3阳性对照品剂量设计艾司唑仑片临床常用堂为6mg/日,按成人标准体重60kg计算,临床给药剂量为0.1mg/kg,换算为大鼠等效剂量为0.6mg/kg。本实验以0.6mg/kg作为阳性对照品艾司唑仑片的给药剂量。给药浓度为0.06mg/ml。
56.安神补脑液临床常用量为20ml/日,按成人标准体重60kg计算, 临床给药剂量为0.33ml/kg, 换算为大鼠等效剂量为2ml/kg。 本实验以2ml/kg作为阳性对照品安神补脑液的给药剂量。 试验时将原液稀释5倍灌胃给药。
57.2.4.3给药途径采用灌胃给药途径,按
ꢀ“
sop-04-gs-011-00大鼠灌胃给药”执行。
58.2.4.4给药体积供试品和溶媒对照品给药体积为10ml/kg。
59.2.4.5给药频率和给药周期连续给药28d,1次/d。
60.2.4.6模型的制备造模方法为复合造模法,即咖啡因与环磷酰胺腹腔注射同时配合水环境法干预,共计4周。在进行水环境剥夺前1周,每天定时对造模动物分别进行咖啡因及环磷酰胺腹腔注射,空白组注射等量生理盐水。 第2周开始到第四周结束,进行水环境睡眠剥夺(每天18h)。 将空白组置于有铁丝网覆盖的剥夺箱内,箱内灌有水,水面距离圆台2cm, 其余各组直接放置在圆形平台上,无铁丝网覆盖,水面距离平台1cm,大鼠因害怕落入水中而时刻保持清醒,不能入睡,每个剥夺箱放大鼠5只。每天定期打扫箱体,将大鼠放回饲养笼休息6h后再放入剥夺箱内,及时添加饲料及饮水。
61.造模成功后进行大鼠行为学评定,行为学表现积分的标准为:a精神状态、对外界的刺激反应性;b嗜睡情况;c面部、口鼻、粘膜、耳朵和尾、爪;d进食及消瘦程度;e皮毛光泽度。按照五个等级进行积分,状态好的为高分,状态不好为低分,最高5分,最低 1分,共计25分。批表评分与对照组有统计学差异即为造模成功。
62.2.4.7检测末次给药后24h, 进行大鼠水迷宫检测。末次给药后48h, 通过水合氯醛麻醉实验动物,股动脉取血,置于离心管中,静置约0.5 h后 3000r/min 离心20min, 收集血清,-80℃保存。取血完毕后,解剖分离出部分脑组织,-80℃保存,做酶联免疫法检测;海马及脑干
组织一部分-80℃保存用于荧光定量rt-pcr检测,剩余部分与垂体和肾上腺用4%的中性甲醛固定,he染色,进行组织病理学态学检查。
63.2.4.7.1药物对中枢睡眠-觉醒周期调节采用elisa试剂盒检测脑干及海马部位5-羟色胺(5-ht)神经递质含量。
64.2.4.7.2药物对下丘脑-垂体-肾上腺轴(hpa轴)的神经内分泌活动的影响采用elisa试剂盒检测血清中促肾上腺皮质激素释放激素(crh)、 促肾上腺皮质激素(acth)和肾上腺皮质激素(ach)的含量。
65.2.4.7.3药物对睡眠剥夺引起的脑损伤保护作用采用elisa试剂盒检测脑组织超氧化物岐化酶(sod)的含量。
66.2.4.7.4药物对睡眠剥夺动物模型中神经细胞保护及再生的影响采用免疫组化法及荧光定量rt-pcr法检测神经生长因子(ngf)和血管活性肠肽(vip)的表达。
67.2.4.7.4.1免疫组织化学染色石蜡切片脱蜡至水:依次将切片放入二甲苯i 15min-二甲苯ii 15min-二甲苯iii 15min-无水乙醇i 5min-无水乙醇ii 5min
ꢀ‑
85%酒精5min
ꢀ‑
75%酒精5min-蒸馏水洗。 抗原修复:组织切片置盛满柠檬酸抗原修复缓冲液(ph6.0)的修复盒中于微波炉内进行抗原修复,中火8min至沸,停火8min保温再转中低火7min,此过程中应防止缓冲液过度蒸发,切勿干片。自然冷却后将玻片置于pbs(ph7.4) 中在脱色摇床上晃动洗涤3次,每次5min。阻断内源性过氧化物酶:切片放入3%双氧水溶液,室温避光孵育25 min, 将玻片置于pbs(ph7.4)中在脱色摇床上晃动洗涤3次,每次5min。血清封闭:在组化圈内滴加3%bsa均匀覆盖组织,室温封闭30min。( 一抗是山羊来源的用兔血清封闭,其他来源的用bsa封闭), 加一抗:轻轻甩掉封闭液,在切片上滴加pbs按一定比例配好的一抗(vip: 1:200: ngf: 1:500), 切片平放于湿盒内4℃孵育过夜。(湿盒内加少量水防止抗体蒸发) ,加二抗: 玻片置于pbs(ph7.4)中在脱色摇床上晃动洗涤3次,每次 5min。切片稍甩干后在圈内滴加与一抗相应种属的二抗(hrp标记)覆盖组织,室温孵育50min。dab显色:玻片置于pbs(ph7.4)中在脱色摇床上晃动洗涤 3次,每次5min。切片稍甩干后在圈内滴加新鲜配制的dab显色液,显微镜下控制显色时间,阳性为棕黄色,自来水冲洗切片终止显色。复染细胞核:苏木素复染3min左右,自来水洗,苏木素分化液分化数秒,自来水冲洗,苏木素返蓝液返蓝,流水冲洗。脱水封片:将切片依次放入75%酒精5min-85%酒精5min-无水乙醇i 5min-无水乙醇ii 5min-二甲苯i 5min 中脱水透明,将切片从二甲苯拿出来稍晾干,中性树胶封片。显微镜镜检,图像采集分析。
68.2.4.7.4.2荧光定量rt-pcr试验(1)总rna抽提:取匀浆管,加入1ml的 trizolreagent, 置冰上预冷。取100mg组织,加入到匀浆管中。匀浆仪充分研磨直至无可见组织块。12000rpm 离心10min取上清。加入250
ꢀµ
l三氯甲烷颠倒离心管15s,充分混匀,静置3min。4度下12000rpm离心10min。将上清液转移到一新的离心管中,加入0.8倍体积的异丙醇,颠倒混匀。-20℃放置15min。4℃下12000rpm离心10min, 管底的白色沉淀即为rna。吸除液体,加入75%乙醇1.5ml洗涤沉淀。4℃下12000rpm 离心5min。将液体吸除干净,将离心管置于超净台上吹3min。加入15
µ
l无rna酶的水溶解rna。55℃孵育5min。使用nanodrop 2000检测rna浓度及纯度:仪器空白调零后
取2.5
µ
l待测rna溶液于检测基座上,放下样品臂,使用电脑上的软件开始吸光值检测。将浓度过高的rna进行适当比例的稀释,使其终浓度为200ng/
µ
l。
69.(2)反转录:取一pcr管,加入含2
µ
grna的溶液。加入1
µ
loligo(dt)18。用无核糖核酸酶的去离子水补足至12
µ
l。于pcr仪上65℃保温5min,迅速置冰上冷却。依次加入4
µ
l5xreactionbuffer,2
µ
ll0mmdntpmix,1ulribolockrnaase抑制剂(20u/
µ
l))和1
µ
lrevertaim-mulv逆转录酶(200u/
µ
l),用枪抽吸混匀。于pcr仪上42℃保温60min,结束后10℃保温5min灭活反转录酶。
70.(3)定量pcr1)取0.2mlpcr管,配制如下反应体系,每个反转录产物配制3管。
71.2xqpcrmix12.5
µ
l;7.5
µ
m基因引物2.0
µ
l;反转录产物2.5
µ
l;ddh208.0
µ
l;2)pcr扩增预变性95℃,10min;循环(40次)95℃,15s一60℃,60s;熔解曲线60℃
‑‑
95℃,每20s升温1度;(4)结果处理
△△
ct法:a=ct(目的基因,待测样本)-ct(内标基因,待测样本)b=ct(目的基因,对照样本)-ct(内标基因,对照样本)k=a-b表达倍数=2-k
2.4.8统计分析实验相关数据用spss统计分析软件进行方差分析。
72.3结果3.1大鼠水迷宫检测水迷宫实验中大鼠穿越平台和在目标象限探索的时间(目标象限游泳时间/总时间)表现上具有致性,此实验表明各组别中药干预后睡眠剥夺大鼠的记忆能力有明显提升。
73.3.2药物对中枢睡眠-觉醒周期调节的影响3.2.1海马区he染色结果(400x)正常对照组海马区细胞染色深,细胞密集,排列整齐;模型组海马区神经元细胞出现形态不规则,间隙增宽,有凋亡小体形成;其余供试品组及安神补脑液组、艾司嗤仑片组海马区神经元细胞形态出现不同程度的改变,间隙增宽,及凋亡小体形成,各给药处理组病变程度较模型组得以改善。
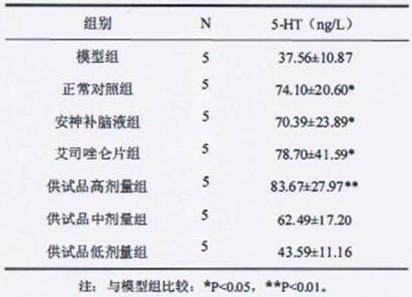
74.3.2.2中枢神经递质含量检测elisa试剂盒检测脑干及海马部位5-ht神经递质含量,结果见表1。与模型组比较,各实验组脑组织5-ht含量明显升高,其中正常对照组、安神补脑液组、艾司唑仑片组、供试品高剂量组尤为显著(p《0.05,p《0.01),供试品中剂量、低剂量组高于模型组但无统计学差异(p》0.05)。
75.表1 试验各组5-ht含量3.3药物对下丘脑-垂体-肾上腺轴(hpa轴)的神经内分泌活动的影响3.3.1 hpa轴激素含量检测采用elisa试剂盒检测血清中促肾上腺皮质激素释放激素(crh)、促肾上腺皮质激素(acth)、肾上腺皮质激素(ach)的含量。结果见表2。各实验组血清中acth和crh含量均低于模型组(p《0.05, p《0.01) 。与模型组比较,安神补脑液组及供试品中剂量组ach含量显著低于模型组(p《0.05) ,其余组也低于模型组但差异均无统计学差异(p》0.05) 。
76.表2实验各组hpa轴激素的含量3.4药物对睡眠剥夺因引起的脑损伤保护作用采用elisa试剂盒检测脑组织超氧化物岐化酶(sod)的含最,结果见表3。各实验组脑组织中sod含量均高于模型组。其中正常对照组、艾司唑仑片组、供试品高、中剂量组sod含量均显著高于模型组 (p《0.01) ,低剂量组、安神补脑液组sod含量高于模型组但差异均无统计学差异 (p》0.05) 。
77.3.5药物对睡眠剥夺动物模型中神经细胞保护及再生的影响采用免疫组化法和荧光定量rt-pcr检查脑干及海马部位神经生长因子 (ngf)、血管活性肠肤(vip)的表达。
78.3.5.2荧光定量ri-pcr试验正常对照组海马区神经元细胞胞浆内有神经生长因子(ngf) 和血管活性肠肽(vip) 表达,其它组别均出现不同程度的表达减弱。其中模型组海马区神经元细胞表达最弱,而供试品高、中、低组、安神补脑液组及艾司唑仑片组相对模型组神经元胞浆内 ngf和 vip的表达出现不同程度的增强,以供试品高剂量、安神补脑液及艾司唑仑片组表达增强最多。
79.表4 引物序列。
80.4结论本发明药物组合物可以调控抑制促肾上腺皮质激素释放激素、促肾上腺皮质激素、肾上腺皮质激素的分泌与释放;增加脑组织5-羟色胺、超氧化物歧化酶含量、上调脑干及海马区神经生长因子、血管活性肠肽表达。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。