1.相关申请的交叉引用
2.本技术要求基于在2020年12月31日提交的韩国专利申请第10-2020-0189140号的优先权,并且相应韩国专利申请的文件中公开的所有内容通过引用并入本说明书的一部分。
3.本发明涉及包括五氟苯基酯的聚合物以及包括该聚合物的电化学生物传感器,该聚合物可用于将电子转移介体和氧化还原酶固定在装置(比如电化学生物传感器)中的电极表面上。
4.糖尿病是一种当高血糖水平长期维持时发生的疾病,并引起并发症,如心血管疾病、中风和肾疾病等。响应于高血糖水平,需要通过胰岛素注射来降低血糖水平,但如果过量注射胰岛素,可能会发生低血糖症,从而导致休克或死亡。为了防止这种情况,对于糖尿病患者来说,为了保持适当的血糖水平,使用血糖传感器连续测量体内的血糖浓度是必要的。
5.最近,已对应用连续葡萄糖监测系统(cgms)的血糖传感器进行了研究并商业化。cgms传感器是一种插入皮下组织并且通过细胞间流体而不是血液来连续测量葡萄糖浓度的装置。在手指采血方法的情况下,很难通过每天测量血糖5至6次来检查血糖水平的准确变化,而cgms具有检查一天内血糖水平的变化和趋势的优点。由此,患者可以快速识别高血糖或低血糖,并且管理血糖的能力可以进一步得到改善。
6.生物传感器是指选择性检测生物样品并将其转化为具体信号的装置。尤其,使用电化学方法的酶类生物传感器是优选的,因为其改善了选择性、微型化和测量准确度。使用电化学方法的血糖生物传感器主要分为第一代方法和第二代方法。第一代血糖传感器首先由clark和lyon开发,并且是一种通过酶的酶氧化还原反应产生的氧浓度降低和过氧化氢浓度变化来测量血糖水平的方法,并且第二代血糖传感器是一种通过电子转移介体将通过酶的氧化还原反应产生的电子转移到电极的方法。与第一代传感器相比,第二代传感器在以下方面具有许多优点:依赖于氧浓度的误差较小,并且通过介体的电子转移反应高效且快速。为此,包括电子转移介体的第二代传感器方法正在被应用于cgms血糖传感器。
7.电化学方法的酶类血糖生物传感器通常由酶、电子转移介体和电极组成。首先,葡萄糖被酶氧化成葡糖酸内酯,并且然后被还原的酶被氧化并向电子传递介体提供电子。然后,被还原的介质被氧化,并经历将电子转移到电极的过程。从这一系列过程中,可以将血糖水平确认为电信号。
8.在血糖传感器的生产中,将电子转移介体和酶固定在电极表面上的方法非常重要。迄今为止,已经研究了通过与酶混合并添加交联剂来将包含电子转移介体的氧化还原水合聚合物固定在电极上的方法。其中,聚乙烯基吡啶和聚乙烯基咪唑作为氧化还原聚合物基质是众所周知的。然而,这些常规氧化还原聚合物的问题在于,最终材料的合成步骤长且复杂,表现出过渡金属复合物的低固定效率,并且也难以将其它官能团引入聚合物中。所
以,即使现在,为了开发具有卓越性能的氧化还原聚合物,需要开发超越常规材料限制的新材料。
9.在此背景下,本发明人反复研究了用于固定用于电化学生物传感器的电子转移介体和酶的聚合物,结果,他们证实了当使用包含五氟苯基(pfp)酯的聚合物时,其具有与胺官能团的高反应性、较少的水解和在有机溶剂中通常良好的溶解性,并且与具有类似结构的聚合物相比,其具有较小的空间位阻和毒性,并且特别是,他们已经证实,这对于将传感器的一部分插入人体的可植入装置(例如连续血糖监测传感器)是有用的,从而完成了本发明。
技术实现要素:
10.【技术问题】
11.本发明的目的是提供包括五氟苯基酯的用于制造氧化还原聚合物材料的聚合物。
12.本发明的另一目的是提供包括用于制造过渡金属复合物和氧化还原聚合物材料的聚合物的氧化还原聚合物材料薄膜和电化学生物传感器。
13.【技术解决方案】
14.作为解决上述目的的一个方面,本发明涉及包括五氟苯基酯的用于制造氧化还原聚合物材料的聚合物,包含该聚合物和过渡金属配合物的用于电化学生物传感器的氧化还原聚合物,包括用于由其制备的电化学生物传感器的氧化还原聚合物的氧化还原聚合物材料薄膜,以及包括其的电化学生物传感器,例如,血糖传感器。
15.【有益效果】
16.当用于电化学传感器时,根据本发明的聚五氟苯基酯类聚合物具有与胺官能团的高反应性、较少的水解、在有机溶剂中的高溶解性以及低空间位阻和毒性或副作用,并且因此,特别地,其可用于其中传感器的一部分置于人体内的可植入装置,例如连续血糖监测传感器。
附图说明
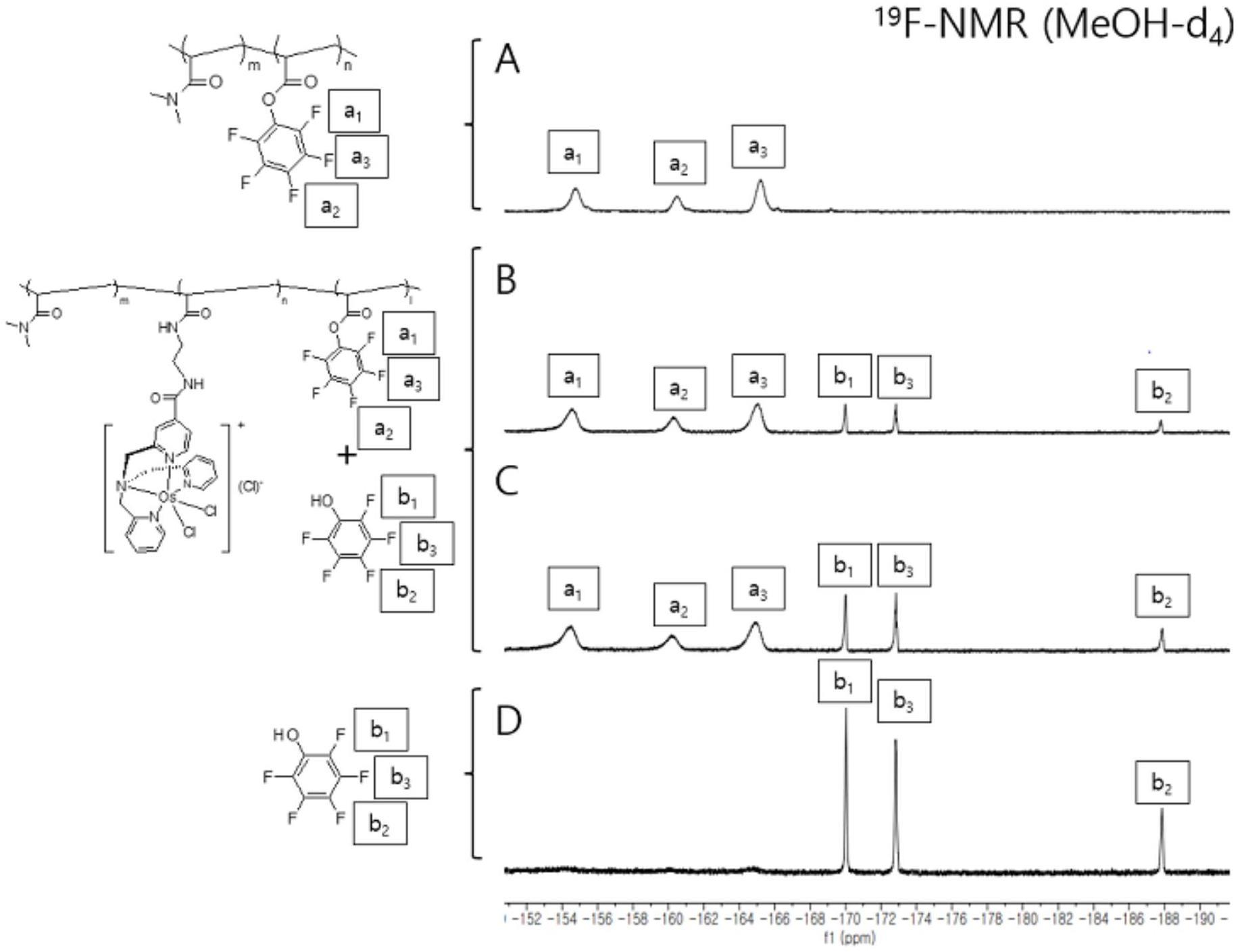
17.图1为示出向根据本发明的pfp聚合物p1中添加锇复合物22后通过
19
f nmr的反应监测结果的曲线图。
18.图2为当pfp聚合物(36)和锇复合物(22,33)的最终反应进行时确认
19
f nmr的曲线图,以及通过该曲线图预测的氧化还原聚合物(37,38)的比例。
19.图3是确认实施例1-4的包括包含c-n配体的过渡金属复合物和pfp聚合物的氧化还原聚合物的合成的
19
f nmr数据。
20.图4为确认实施例1-5的包括包含c-n配体的过渡金属复合物和pfp聚合物的氧化还原聚合物的合成的
19
f nmr数据。
21.图5为氧化还原聚合物和酶的组合物以及在spces电极表面上的交联方法的示意图。
22.图6a为示出当根据本发明的氧化还原聚合物(37和38)中的葡萄糖浓度增加至每200秒0.01、0.05、0.1、0.5、1、2、4、8、16、32、64、100mm时的电流的变化(上部),根据葡萄糖浓度的电流的变化(下部),左侧为低浓度部分(0~1mm),而右侧为总部分(0~100mm)的曲
线图。
23.图6b为示出当根据本发明的氧化还原聚合物(包括包含c-n配体的过渡金属复合物和pfp聚合物的氧化还原聚合物1)中的葡萄糖浓度增加至每200秒0.01、0.05、0.1、0.5mm时的电流的变化(上部-左),根据葡萄糖浓度的电流的变化(上部-右)以及葡萄糖浓度增加至每200秒0、1、5、10、50、100mm时的电流的变化(下部-左)和根据葡萄糖浓度的电流的变化(下部-右)的曲线图。
24.图6c为示出当根据本发明的氧化还原聚合物(包括包含c-n配体的过渡金属复合物和pfp聚合物的氧化还原聚合物1)中的葡萄糖浓度增加至每200秒0.01、0.05、0.1、0.5mm时的电流的变化(上部-左),根据葡萄糖浓度的电流的变化(上部-右)以及葡萄糖浓度增加至每200秒0、1、5、10、50、100mm时的电流的变化(下部-左)和根据葡萄糖浓度的电流的变化(下部-右)的曲线图。
25.图7a至图7d为示出根据本发明的氧化还原聚合物(37、38以及包括包含c-n配体的过渡金属复合物和pfp聚合物的氧化还原聚合物1和氧化还原聚合物2)的循环伏安法测试之前和之后的电流的变化的测量结果的曲线图。在图7a至7d中,cv表示完成电极后立即测量的值,并且cv后代表在pbs溶液中搅拌1小时后测量的值。
具体实施方式
26.下文,将更详细描述本发明。
27.根据本发明的用于制造氧化还原聚合物材料的聚合物是基于聚五氟苯基酯的聚合物,并且具体地,用作氧化还原聚合物材料的聚合物前体,包括衍生自五氟苯基酯的重复单元。优选地,聚合物可以与具有包括胺基和过渡金属复合物的反应基团的交联材料形成用于电子转移介体氧化还原聚合物材料。
28.作为一个示例,根据本发明的用于制造氧化还原聚合物材料的聚合物可为用于制造氧化还原聚合物材料的聚合物,该氧化还原聚合物材料通过氨解将作为包含胺基的交联材料的伯胺类化合物和仲胺类化合物引入聚五氟苯基酯中来制备。
29.用于氧化还原聚合物材料的聚合物的非限制示例可为一种或多种选自由下述组成的组中的聚合物:聚丙烯酸五氟苯酯(ppfpa)均聚物、聚甲基丙烯酸五氟苯酯(ppfpm)均聚物、聚丙烯酸五氟苯酯-聚二甲基丙烯酰胺(ppfpa-pdma)共聚物、聚甲基丙烯酸五氟苯酯-聚二甲基丙烯酰胺(ppfpm-pdma)共聚物、聚丙烯酸五氟苯酯-聚丙烯酰胺(ppfpa-paa)共聚物、聚甲基丙烯酸五氟苯酯-聚丙烯酰胺(ppfpm-paa)共聚物,但是不限于此。
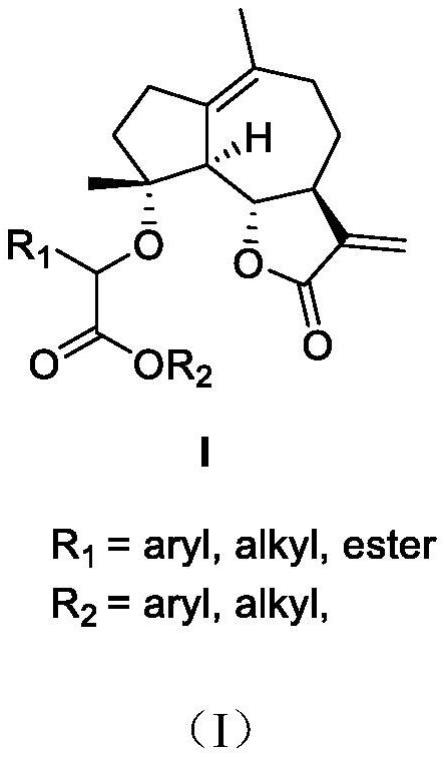
30.在一个示例中,根据本发明的用于制造氧化还原聚合物材料的聚合物可具有下面的化学式1或化学式2的结构:
31.[化学式1]
[0032]
[0033]
[化学式2]
[0034][0035]
在化学式1或化学式2中,
[0036]rt
和r
l
各自独立地选自由下述组成的组中:取代或未取代的具有1至20个碳原子的亚烷基、取代或未取代的具有1至20个碳原子的亚环烷基、取代或未取代的具有3至30个碳原子的乙二醇基、取代或未取代的具有6至30个碳原子的亚芳基、取代或未取代的具有3至30个碳原子的亚杂芳基、取代或未取代的具有2至40个碳原子的烯基和取代或未取代的具有2至40个碳原子的炔基;并且
[0037]
n为10至300的整数。
[0038]
在本发明中,“取代”可为至少一个氢原子选自由下述组成的组中的1种至3种:卤原子(例如、f、cl、br或i)、氰基、羟基、硫醇基、硝基、氨基、亚氨基、叠氮基、脒基、肼基、腙基、氧代基、羰基、氨甲酰基、酯基、醚基、羧酸基或其盐、磺酸基或其盐、磷酸盐或其盐、具有1-6个碳原子的烷基、具有1-6个碳原子的卤代烷基、具有2至6个碳原子的烯基、具有2至6个碳原子的卤代烯基、具有2至6个碳原子的炔基、具有2至6个碳原子的卤代炔基、具有1至6个碳原子的烷氧基、具有1至6个碳原子的卤代烷氧基、具有1至6个碳原子的烷硫基、具有1至9个碳环的杂环烷基、具有6至10个碳原子的芳基、具有6至10个碳原子的芳氧基、具有6至10个碳原子的芳基硫醇基、具有1至9个碳环的杂烷基、具有1至9个碳环的杂芳氧基和具有含有1至9个碳原子的碳环的杂芳硫基,除非以其他方式提到。
[0039]
优选地,r
t
和r
l
可各自独立地选自由下述组成的组中:聚二甲基丙烯酰胺(pdma)、聚丙烯酰胺(paa)、聚苯乙烯(ps)、聚乙二醇(peg)、聚环氧乙烷(peo)、聚甲基丙烯酸甲酯(pmma)、聚乙烯基咪唑(pvi)、聚乙烯基吡啶(pvp)和分子量为1,000g/mol~50,000g/mol的聚硅氧烷(pdms)。
[0040]
作为一个示例,根据本发明的用于制造氧化还原聚合物材料的聚合物可具有范围为1,000g/mol至500,000g/mol的重均分子量,但是不限于此。
[0041]
作为另一方面,本发明涉及用于电化学传感器的氧化还原聚合物材料,其中将过渡金属复合物引入聚五氟苯基酯类聚合物。
[0042]
例如,该氧化还原聚合物材料可通过如下制备:引入包括选自由胺基、铵基、卤基、环氧基、叠氮化物基、丙烯酸酯基、烯基、炔基、硫醇基、异氰酸酯、醇基和硅烷基组成的组中的官能团的化合物来将聚五氟苯基酯类聚合物官能化,并且将过渡金属复合物结合到如此官能化的聚合物。
[0043]
另外,氧化还原聚合物材料可通过如下制备:通过取代反应和加成反应将官能团比如交联材料(比如胺基、铵基、硫醇基和醇基等)引入过渡金属复合物的配体,并且将如此官能化的过渡金属复合物和根据本发明的聚合物结合,从而将聚五氟苯基酯类聚合物官能化,而不是将聚合物官能化。
[0044]
另外,聚合物材料可通过如下制备:使用包括选自由胺基、铵基、卤基、环氧基、叠氮化物基、丙烯酸酯基、烯基、炔基、硫醇基、异氰酸酯、醇基和硅烷基组成的组中的官能团的交联材料将所有的聚五氟苯基酯类聚合物和过渡金属复合物官能化,并且将它们彼此结合。
[0045]
优选地,在根据本发明的氧化还原聚合物材料中,将选自由伯胺和仲胺基以及铵基组成的组中的官能团和过渡金属复合物结合到聚五氟苯基酯类聚合物。
[0046]
具体地,过渡金属复合物可具有下面的化学式3或化学式4的结构。
[0047]
[化学式3]
[0048][0049]
[化学式4]
[0050][0051]
在化学式3或化学式4中,
[0052]
m为一种选自由下述组成的组中的过渡金属:os、rh、ru、ir、fe和co;并且
[0053]
在化学式3中,l
g1
和l
g2
彼此结合以形成选自下面的化学式5至化学式6的二齿配体;并且
[0054]
l
g3
和l
g4
彼此结合以形成选自下面的化学式5至化学式6的二齿配体;并且l
g5
和l
g6
彼此结合以形成选自下面的化学式5至化学式6的二齿配体;并且
[0055]
[化学式5]
[0056][0057]
[化学式6]
[0058][0059]
在化学式5中,lc为包括一个或多个氮原子的杂环化合物,并且在2位与苯的化学式连接;并且
[0060]
在化学式6中,ln为包括一个或多个氮原子的杂环化合物,并且l
n1
和l
n2
分别在2位彼此连接。
[0061]rl
为杂环化合物lc、l
n1
和l
n2
的所有官能团。
[0062]
在一个方面中,r1、r2、r3、r4、r5和r
l
可各自独立地选自由以下组成的组中:取代或未取代的具有1至10个碳原子的烷基、取代或未取代的具有2至20个碳原子的乙二醇基、取代或未取代的具有1至20个碳原子的醇基、取代或未取代的具有1至20个碳原子的卤烷基、取代或未取代的具有1至20个碳原子的硫醇基、取代或未取代的具有3至20个碳原子的烷基叠氮化物基、取代或未取代的具有7至30个碳原子的芳基叠氮化物基、取代或未取代的具有2至40个碳原子的烯基、取代或未取代的具有2至40个碳原子的炔基、氰基、卤基、重氢和氢。
[0063]
在一个方面中,化学式4的l
h1
、l
h3
和l
h4
可以l
h2
为中心彼此结合,以形成由下面的化学式7表示的四齿配体。
[0064]
然后,l
h5
和l
h6
可分别形成如化学式8表示的过渡金属m的单齿配体;或l
h5
和l
h6
可彼此结合以分别形成如由下面的化学式9表示的过渡金属m的二齿配体;并且
[0065]
[化学式7]
[0066][0067]
在化学式7中,
[0068]
ca、cb和cc为包括一个或多个氮原子的杂环化合物,并且优选地,该杂环化合物可在其2位连接至甲胺,并且三个杂环的3个氮和在连接三个杂环的中心的1个氮可连接至过渡金属m。
[0069]
r1、r2、r3意指杂环化合物ca、cb、cc的所有官能团。
[0070]
在一个方面中,r1、r2和r3可各自独立地选自由下述组成的组:取代或未取代的具有1至10个碳原子的烷基、取代或未取代的具有2至20个碳原子的乙二醇基、取代或未取代的具有1至20个碳原子的醇基、取代或未取代的具有1至20个碳原子的卤烷基、取代或未取代的具有1至20个碳原子的硫醇基、取代或未取代的具有3至20个碳原子的烷基叠氮化物基、取代或未取代的具有7至30个碳原子的芳基叠氮化物基、取代或未取代的具有2至40个碳原子的烯基、取代或未取代的具有2至40个碳原子的炔基、氰基、卤基、重氢和氢。优选地,可各自独立地引入能够连接至聚合物的反应基团。
[0071]
[化学式8]
[0072][0073]
[化学式9]
[0074][0075]
在化学式8中,
[0076]
l
h5
和l
h6
可独立地为单齿配体,并且各自独立地为包括一个或多个-h、-f、-cl、-br、-i、-no2、-ncch3、-co、-oh2、-nh3或氮原子的杂环化合物。
[0077]
在化学式9中,
[0078]
l
h5-l
h6
可为二齿配体,并且为儿茶酚、乙酰丙酮、2-吡啶甲酸、2-吡啶甲酰胺、2,2-联吡啶或2,2-联噻唑。
[0079]
l1可独立地选自由下述组成的组中:取代或未取代的具有1至20个碳原子的亚烷基、取代或未取代的具有1至20个碳原子的亚环烷基、取代或未取代的具有2至30个碳原子的乙二醇基、取代或未取代的具有6至30个碳原子的亚芳基和取代或未取代的具有3至30个碳原子的亚杂芳基;并且
[0080]aa
选自由胺基和铵基组成的组中。
[0081]
本发明的一个方面涉及:用于制备氧化还原聚合物材料薄膜的方法,其包括将包含聚合物的氧化还原聚合物材料涂覆至电极上,并且然后硬化涂覆的电极;以及由此制备的氧化还原聚合物材料薄膜和包括该薄膜的电化学生物传感器。
[0082]
另外,本发明的一个另外方面涉及用于电化学生物传感器的传感层,其包括能够氧化还原液体生物样品的c酶;和包括过渡金属复合物的电子转移介体。
[0083]
氧化还原酶是指在活体中催化氧化还原反应的酶,并且在本发明中,在待测目标材料(例如,生物传感器)的情况下,是指通过与待测目标材料反应而被还原的酶。如此还原的酶与电子转移介体反应,并且然后,通过测量信号(如生成的电流变化)来量化目标材料。本发明中可用的氧化还原酶可为选自由各种脱氢酶、氧化酶和酯酶等组成的组中的一种或多种,并且可以根据氧化还原或检测目标材料,通过在属于酶组的酶中选择使用目标材料作为底物的酶来使用。
[0084]
更具体地,氧化还原酶可为选自由下述组成的组中的一种或多种:葡萄糖脱氢酶、谷氨酸脱氢酶、葡萄糖氧化酶、胆固醇氧化酶、胆固醇酯酶、乳酸盐氧化酶、抗坏血酸氧化酶、醇氧化酶、醇脱氢酶和胆红素氧化酶等。
[0085]
另一方面,氧化还原酶可包括辅助因子,该辅助因子起到将氧化还原酶从待测目标材料(例如,目标材料)窃取的氢存储在一起的作用,并且例如,其可为选自由下述组成的组中的一种或多种:黄素腺嘌呤二核苷酸(fad)、烟酰胺腺嘌呤二核苷酸(nad)和吡咯并喹啉醌(pqq)等。
[0086]
例如,当要测量血糖浓度时,葡萄糖脱氢酶(gdh)可用作氧化还原酶,并且葡萄糖脱氢酶可为包括fad作为辅助因子的黄素腺嘌呤二核苷酸-葡萄糖脱氢酶(fad-gdh),和/或包括fad-gdh作为辅助因子的烟酰胺腺嘌呤二核苷酸-葡萄糖脱氢酶。
[0087]
在具体的实施方式中,可用的氧化还原酶可为选自由下述组成的组中的一种或多种:fad-gdh(例如,ec 1.1.99.10等)、nad-gdh(例如,ec 1.1.1.47等)、pqq-gdh(例如,ec1.1.5.2等)、谷氨酸脱氢酶(例如,ec 1.4.1.2等)、葡萄糖氧化酶(例如,ec 1.1.3.4等)、胆固醇氧化酶(例如,ec 1.1.3.6等)、胆固醇酯酶(例如,ec 3.1.1.13等)、乳酸盐氧化酶
(例如,ec 1.1.3.2等)、抗坏血酸氧化酶(例如,ec 1.10.3.3等)、醇氧化酶(例如,ec 1.1.3.13等)、醇脱氢酶(例如,ec 1.1.1.1等)和胆红素氧化酶(例如,ec 1.3.3.5等)等。
[0088]
最优选地,氧化还原酶为能够在37℃的缓冲溶液中保持70%或更高的活性1周的葡萄糖脱氢酶。
[0089]
基于100重量份的氧化还原酶,根据本发明的传感层可含有20重量份至700重量份,例如,60重量份至700重量份,或30重量份至340重量份的氧化还原聚合物。氧化还原聚合物的含量可根据氧化还原酶的活性来适当地调整。
[0090]
而且,根据本发明的传感层可进一步包括用于增加膜性能的碳纳米管。具体地,当过渡金属复合物(特别是锇)一起使用时,随着电子转移速率增加,碳纳米管可进一步增加传感层的性能。
[0091]
另外,根据本发明的传感层可进一步包括交联剂。
[0092]
另一方面,根据本发明的传感层可进一步包括选自由表面活性剂、水性聚合物、叔铵盐、脂肪酸和增稠剂等组成的组中的一种或多种的添加剂,用于在试剂溶解期间充当分散剂,在试剂制备期间充当粘合剂和用于长时间段存储的稳定剂等。
[0093]
可当等分组合物时,表面活性剂可起到将组合物均匀分布在电极上以均匀厚度等分的作用。作为表面活性剂,可使用选自由triton x-100、十二烷基硫酸钠、全氟辛烷磺酸酯和硬脂酸钠等组成的组中的一种或多种。基于100重量份的氧化还原酶,根据本发明的试剂组合物可含有3重量份至5重量份,例如,10重量份至25重量份的量的表面活性剂,以便当等分试剂时,适当地起到将试剂均匀分布在电极上以均匀厚度等分的作用。例如,当使用具有700u/mg活性的氧化还原酶时,基于100重量份的氧化还原酶,可包含10重量份至25重量份的表面活性剂,并且当氧化还原酶的活性高于700u/mg时,可以将表面活性剂的含量调节至低于上述含量。
[0094]
水性聚合物为试剂组合物的聚合物载体,其起到帮助酶稳定和分散的作用。作为水性聚合物,可使用选自由下述组成的组中的一种或多种:聚乙烯吡咯烷酮(pvp)、聚乙烯醇(pva)、聚全氟磺酸酯、羟乙基纤维素(hec)、羟丙基纤维素(hpc)、羧酸基甲基纤维素(cmc)、乙酸纤维素和聚酰胺等。基于100重量份的氧化还原酶,根据本发明的试剂组合物可含有10重量份至70重量份,例如,30重量份至70重量份的水性聚合物,以便充分且适当地展示有助于氧化还原酶的稳定和分散的作用。例如,当使用具有700u/mg活性的氧化还原酶时,基于100重量份的氧化还原酶,可包含30至70重量份的水性聚合物,并且当氧化还原酶的活性高于700u/mg时,可以将水性聚合物的含量调节至低于上述含量。
[0095]
水性聚合物可具有约2,500g/mol至3,000,000g/mol,例如,5,000g/mol至1,000,000g/mol的重均分子量,以便有效地起到帮助载体和酶的稳定和分散的作用。
[0096]
增稠剂起到将试剂牢固附着到电极上的作用。作为增稠剂,可使用一种或多种选自natrosol和二乙氨基乙基-葡聚糖盐酸盐(deae-葡聚糖盐酸盐)等的物质。基于100重量份的氧化还原酶,根据本发明的电化学传感器可包含10重量份至90重量份,例如30重量份至90重量份的量的增稠剂,以便将根据本发明的氧化还原聚合物牢固地附接至电极。例如,当使用具有700u/mg活性的氧化还原酶时,基于100重量份的氧化还原酶,可包含30重量份至90重量份的增稠剂,并且当氧化还原酶的活性高于700u/mg时,可以将增稠剂的含量调节至低于上述含量。
[0097]
作为另一方面,本发明可为一种装置,优选地,可插入装置,例如,可插入人体的装置,其包括该有机电子转移介体。另外,优选地,装置可为电化学生物传感器,更优选地,电化学葡萄糖(血糖)传感器。
[0098]
具体地,对电化学生物传感器的类型没有限制,但是其可为连续血糖监测传感器。
[0099]
作为该连续血糖监测传感器的组成,本发明可包括例如,电极、绝缘体、基板、包括氧化还原聚合物和氧化还原酶的传感层、扩散层和保护层等。在电极的情况下,可包括两种电极比如工作电极和对电极,并且可包括三种电极,比如工作电极、对电极和参比电极。在一个实施方式中,根据本发明的生物传感器可为电化学生物传感器,其通过将包含氧化还原聚合物的试剂组合物施加至具有至少两个、优选两个或三个电极的基板并干燥而产生,该氧化还原聚合物包含化学式1的有机系列电子转移介体和能够氧化还原液体生物样品的酶。例如,在电化学生物传感器中,提供了平面的电化学生物传感器,其中工作电极和对电极装配在彼此相对的两侧,并且包含具有根据本发明的有机系列电子转移介体的氧化还原聚合物的传感层层压在工作电极上,并且绝缘体、扩散层和保护层依次层叠在配备有工作电极和对电极的基板的两侧上。
[0100]
作为具体的方面,基板可由选自由pet(聚对苯二甲酸乙二醇酯)、pc(聚碳酸酯)和pi(聚酰亚胺)组成的组中的一种或多种制成。
[0101]
另外,工作电极可使用碳、金、铂、银或银/氯化银电极。
[0102]
此外,在具有2个电极的电化学生物传感器的情况下,对电极也起到参比电极的作用,因此,作为对电极,可使用金、铂、银或银/氯化银电极,并且在包括参比电极的三个电极的电化学生物传感器的情况下,作为参比电极,可使用金、铂、银或银/氯化银电极,并且作为对电极,可使用碳电极。
[0103]
可使用nafion、乙酸纤维素和硅酮橡胶作为扩散层,并且可使用硅酮橡胶、聚氨酯和聚氨酯类共聚物等作为保护层,但不限于此。
[0104]
作为非限制性实例,在两个电极的情况下,对电极也起到参比电极的作用,因此,可使用氯化银或银,并且在三个电极的情况下,可使用氯化银或银作为参比电极,并且可使用碳电极作为对电极。
[0105]
本发明的具体的实施方式阐释用于测量葡萄糖的生物传感器作为电化学生物传感器的适用示例,但通过改变本发明的试剂组合物中包含的酶的类型,其可应用于用于量化各种物质(比如胆固醇、乳酸盐、肌酸酐、过氧化氢、醇、氨基酸和谷氨酸)的生物传感器。
[0106]
【发明方式】
[0107]
下文,将通过下述实施例更详细描述本发明。然而,下述实施例仅阐释本发明,但是本发明的内容不受下述实施例限制。
[0108]
[实施例]
[0109]
实验材料
[0110]
参考实施例1.试剂和样品
[0111]
使用从aldrich公司和acros公司、tci公司和alfa aesar公司商购的试剂,无需特别纯化,并且通过将碱性氧化铝填充到10ml移液管中然后过滤,使用乙二胺、吡啶、1-甲基咪唑和三乙胺。纯化并使用从daejung和samchun购买的如下几种溶剂。无水二氯甲烷和无水n,n-二甲基甲酰胺通过添加氢化钙并且蒸馏来获得,并且无水乙腈通过使用p2o5蒸馏来
获得。二乙基醚使用钠和二苯甲酮来蒸馏。对于用于分析的薄层色谱,使用merck硅胶60f
254
玻璃板,并且使用双短波长(254nm)/长波长(365nm)uv灯观察荧光。对于柱色谱,使用aldrich碱性氧化铝或alfa中性氧化铝。作为丝网印刷碳电极(spces),使用zensor公司的se102产品。
[0112]
参考实施例2.设备
[0113]
使用varian inova 400(对于1h为400mhz,并且对于
13
c为100mhz)分光计获得氢核磁共振(1h nmr)、碳核磁共振(
13
c nmr)和氟核磁共振(
19
f nmr)光谱。基于四甲基硅烷(δ0.00)或氘化的氯仿(1h nmr中对于cdcl3的δ7.26,
13
c nmr中对于cdcl3为δ77.2)、氘化的二甲亚砜(1h nmr中对于dmso为δ2.50,
13
c nmr中对于dmso为δ39.52)和氘化乙腈(1h nmr中对于cd3cn为δ1.94),所有化学位移均以ppm单位表示。在氟核磁共振(
19
f nmr)的情况下,将少量三氟甲苯(cf
3-ar,
19
f nmr中对于cd3od为δ-69.27)添加到氘化甲醇并基于此,以ppm单位表示。通过ch instruments公司的chi1040c型进行循环伏安图(cv)的测量。使用清洗干净的直径为3mm的碳玻璃电极作为工作电极,ag/agcl电极作为参比电极,并且pt电极作为对电极,以10~50mv/s的扫描速率进行测量。在sogang大学有机化学研究中心的thermofisher scientific公司的ltq xl模型中,在低分辨率的情况下,通过esi-iontrap获得质谱,并且在高分辨率的情况下,通过esi-orbitrap获得质谱。单晶x射线衍射分析委托韩国化学技术研究所进行,并且晶体结构可使用bruker smart apex ii模型进行鉴定。
[0114]
实施例1.使用pfp聚合物基质的氧化还原聚合物合成
[0115]
该实验的目的是通过与末端包含胺基(-nh2)的电子转移介体的反应,由丙烯酸五氟苯酯(pfpa)类聚合物基质合成氧化还原聚合物。首先,使用aibn,通过丙烯酸五氟苯酯(pfpa)和二甲基丙烯酰胺(dma)以5:5的比例进行自由基聚合来合成dma:pfpa聚合物(p1)。
[0116]
1-1.聚(n,n-二甲基丙烯酰胺-共-丙烯酸五氟苯酯)(p1)的合成
[0117][0118]
[dma:pfp聚合物的合成]
[0119]
将n,n-二甲基丙烯酰胺(150mg,1.51mmol)、丙烯酸五氟苯酯(360mg,1.51mmol)、偶氮二异丁腈(aibn,7mg,0.043mmol)添加至玻璃培养管中,并且添加乙腈(8ml)以制备混合溶液。之后,吹入氩气10分钟以在玻璃培养管中产生氩气氛,并且然后在80℃回流12小时。反应完成后,用旋转蒸发器去除溶剂,并且加入ch2cl2以制备混合溶液。将通过重复将混合溶液缓慢滴加到正己烷中三次以获得沉淀而产生的聚合物进行纯化。通过干燥经过滤沉淀物并用正己烷在真空中洗涤6小时或更长时间而获得的聚合物,获得白色固体形式的产物p1。(482mg,95%)1h nmr(400mhz,cdcl3)δ2.81~3.34ppm(br,7h,ppfpa的骨架中的-ch-和来自pdma的-n(ch3)2),2.47至2.65ppm(br,1h,pdma的骨架中的-ch-),1.13至2.22ppm(br,4h,pdma和ppfpa的骨架中的-ch
2-),
19
f nmr(400mhz,cdcl3)δ-152.90(br,邻位),-157.21(br,对位),-162.15(br,间位)
[0120]
合成的聚合物在甲醇、乙腈、丙酮和二氯甲烷中展示良好的溶解性,但是在水和二乙醚中完全不溶。
[0121]
1-2.确认pfp聚合物是否可用作能够固定电子转移介体和gdh的聚合物基质
[0122]
为了确认在实施例1-1中合成的聚合物p1和在末端包括胺基的锇复合物22之间的反应是否进行,通过
19
f nmr进行了观察。
[0123][0124]
复合物22以其中两性离子为cl-的形式反应,并且在能够溶解复合物和聚合物的氘化甲醇溶剂下确认nmr峰。另外,当复合物22的胺基以铵(-nh
4
)形式存在时,其不能与pfp酯反应,所以加入与复合物等量的三乙胺(tea)。结果如图1中示出。如可由图1中确认,最初,通过
19
f nmr只确认了聚合物p1,结果,示出了对应于pfpa的三个宽峰。然后,一旦加入复合物22,就观察到另外示出尖锐点形式的五氟苯酚(pfpoh)的三个峰。这些是pfpoh的峰,pfpoh是通过在复合物22的末端的胺的反应而产生的副产物。随着时间的推移,pfpoh的峰逐渐增加并且pfpa的峰逐渐减少,约36小时后,pfpa的所有峰消失,仅保留pfpoh的峰。通过该结果,确定了pfp酯可与包含tpma类锇复合物的胺基反应,并且pfpa聚合物可用作能够固定电子转移介体和gdh的聚合物基质。
[0125]
1-3.氧化还原聚合物(氧化还原聚合物(36)和(37))的合成
[0126]
通过包含胺官能团的tpma类锇复合物22和33与pfpa聚合物36反应,合成了氧化还原聚合物(图2)。为了获得在整个聚合物链中包含约25%~30%锇复合物的氧化还原聚合物,通过计算当量比来进行反应。
[0127]
1)氧化还原聚合物(36)的合成
[0128][0129]
在nmr管中将起始材料22(6mg,0.009mmol)溶解在氘代的甲醇(0.5ml)中。将溶解的溶液添加到溶解在氘代的甲醇(0.5ml)中的起始材料p1(5mg)中,并且然后添加三乙胺(1.24μl,0.009mmol)。在通过
19
f nmr确认反应进程后,纯化通过重复将反应溶液缓慢滴入二乙醚中三次以获得沉淀而产生的聚合物。过滤产生的沉淀物并用二乙醚洗涤,然后在真空中干燥4小时或更长时间,以获得棕色固体形式的产物36。(6mg,64%)
19
f nmr(400mhz,cd3od)δ-153.38(br,邻位),-159.74(br,对位),-163.53(br,间位)
[0130]
2)氧化还原聚合物(37)的合成
[0131][0132]
在nmr管中将起始材料33(6.5mg,0.009mmol)溶解在氘化甲醇(0.5ml)中。将溶解的溶液添加到溶解于氘化甲醇(0.5ml)中的起始材料p1(5mg),并且然后添加三乙胺(1.22μl,0.009mmol)。通过
19
f nmr确认反应进程后,纯化通过重复将反应溶液缓慢滴入二乙醚中三次以获得沉淀而产生的聚合物。过滤产生的沉淀物并用二乙醚洗涤,然后在真空中干燥4小时或更长时间,以获得棕色固体形式的产物37。(7.2mg,73%)
19
f nmr(400mhz,cd3od)δ-154.57(br,邻位),-160.27(br,对位),-164.95(br,间位)
[0133]
通过
19
f nmr确认添加的复合物和pfpa聚合物之间的反应,直到峰不再变化,并确定氧化还原聚合物的比例。所有加入的锇复合物反应大约需要24~36小时。作为通过
19
f nmr确认两种氧化还原聚合物的比例的结果,可以间接确定在氧化还原聚合物37的情况下,pfpa:pfpoh的比例示出为2∶3,锇复合物占据总链的30%,并且在38的情况下,pfpa∶pfpoh的比例示出为2.2∶2.8,并且28%的锇复合物包含在聚合物基质中。两种聚合物都是通过在二乙醚中沉淀得到的,并且与起始材料36聚合物不同,所有的氧化还原聚合物都溶于水。另外,如下面所确认,当测量cv时,展示出类似于锇复合物单体的氧化还原电势。通过该结果,确定成功地合成了包含tpma类锇复合物的氧化还原聚合物。
[0134]
1-4.包括包含c-n配体的过渡金属复合物和pfp聚合物的氧化还原聚合物1的合成
[0135][0136]
作为起始材料,在nmr管中将包括c-n配体的锇复合物[os(2-(2-吡啶基-κn)-5-甲烷胺-苯基-κc)(4,4
’‑
二甲基-2,2
’‑
联吡啶)2]cl2(11mg,0.014mmol)溶解在氘化甲醇(0.5ml)中。将溶解的溶液添加至溶解在氘化甲醇(0.5ml)中的起始材料pfp聚合物(7:3)(17mg)中,并且然后添加三乙胺(3.8μl,0.028mmol)。在通过
19
f nmr(图3)确认反应的进程后,纯化通过重复将反应溶液缓慢滴入二乙醚中三次以获得沉淀物而产生的聚合物。过滤产生的沉淀物并用二乙醚洗涤,然后在真空中干燥4小时或更长时间,以获得棕色固体形式的产物。
[0137]
1-5.包括包含c-n配体的过渡金属复合物的氧化还原聚合物2的合成
[0138][0139]
在nmr管中将起始材料[os(2-(2-吡啶基-κn)-5-甲烷胺-苯基-κc)(4,4
’‑
二甲氧基-2,2
’‑
联吡啶)2]cl2(9.7mg,0.012mmol)溶解在氘化甲醇(0.5ml)中。将溶解的溶液添加至溶解在氘化甲醇(0.5ml)中的起始材料pfp聚合物(7:3)(15mg)中,并且然后添加三乙胺(3.1μl,0.024mmol)。在通过
19
f nmr确认反应的进展后(图4),纯化通过重复将反应溶液缓慢滴入二乙醚中三次以获得沉淀物而产生的聚合物。过滤产生的沉淀物并用二乙醚洗涤,然后在真空中干燥4小时或更长时间,以获得棕色固体形式的产物。
[0140]
实施例2.氧化还原聚合物和酶的固定化以及对葡萄糖的响应测试
[0141]
将混合了包含锇复合物和葡萄糖脱氢酶(gdh)的氧化还原聚合物的溶液固定在spces电极上,并且为了确认取决于葡萄糖浓度的响应,进行下述测试。
[0142]
2-1.其中固定有氧化还原聚合物和葡萄糖脱氢酶的电极的制备
[0143]
通过混合将氧化还原聚合物0.4mg溶解在蒸馏水50μl中而成的溶液和将葡萄糖脱氢酶(gdh)0.8mg溶解在蒸馏水50μl(v/v 1:1)中而成的溶液来制备混合溶液。在氧化还原聚合物37和氧化还原聚合物38的情况下的0.83μl以及在包含包含c-n配体的过渡金属复合物的氧化还原聚合物1和氧化还原聚合物2的情况下的1μl的该混合溶液被均匀地放置在spces上,并且在室温下缓慢干燥。完成干燥后,再次放置在氧化还原聚合物37和氧化还原聚合物38的情况下的0.83μl和在包括包含c-n配体的过渡金属复合物的氧化还原聚合物1和氧化还原聚合物2的情况下的1μl的混合溶液,并且该过程重复两次以上。将其上有总共2.5μl(聚合物37和聚合物38)和3μl(包括包含c-n配体的过渡金属复合物的氧化还原聚合物1和氧化还原聚合物2)的混合溶液的电极在室温下干燥12小时或更长时间以制备电极。图5示意性地示出了介体和酶的组成以及在spces电极表面上的交联方法。
[0144]
2-2.根据葡萄糖浓度的电流测量
[0145]
在将搅拌棒添加到50ml的10mm pbs溶液后,在以150rpm搅拌实施例2-1中制备的固定有氧化还原聚合物和葡萄糖脱氢酶的电极的同时,测量i-t曲线。每200秒加入一定量的葡萄糖溶解在10mm pbs中而成的溶液,并在0.01、0.05、0.1、0.5、1、2、4、8、16、32、64、100mm的浓度下测量电流以确认电流的变化。结果在图6a中示出。
[0146]
作为测试的结果,当电极中葡萄糖浓度逐渐增加时,电流逐渐增加,其中氧化还原聚合物37和氧化还原聚合物38分别与酶交联。首先,在电流-时间图中,两个电极都示出逐步增加,直到100mm的浓度,并且即使在低浓度部分(0~1mm)变化也是明显的。另外,当对根据浓度产生的电流进行平均并绘制电流-浓度图时,确认了与每种葡萄糖浓度产生的电流的大小的相关性。在低浓度段,恒定电流量线性增加,但随着浓度逐渐增加,在16mm或更高的高浓度段,电流增加逐渐减少,示出电流值出现恒定。可见,这达到了葡萄糖在电极中可以被氧化的最大值,并且电流增加逐渐减少,并且达到了极限催化电流(i
max
)。此外,用氧化还原聚合物37交联的电极示出约1.5μa的最大电流,而用氧化还原聚合物38交联的电极示
出约0.5μa的最大电流,比37类电极低1/3。
[0147]
在将搅拌棒添加到50ml的10mm pbs溶液后,在以150rpm搅拌实施例2-1中制备的固定有氧化还原聚合物和葡萄糖脱氢酶的电极的同时,测量i-t曲线。在包括包含c-n配体的过渡金属配合物的氧化还原聚合物1和氧化还原聚合物2用酶交联的电极中,每200秒添加一定量的葡萄糖溶解在10mm pbs中而成的溶液,并分别在增加到0.01、0.05、0.1、0.5mm的低浓度段和增加到1、5、10、50、100mm的高浓度段测量电流,以确认电流的变化。结果如图6b至图6c中示出。
[0148]
作为测试的结果,在低浓度段(0~0.5mm)和高浓度段(0~100mm)中,两个电极中的电流逐步增加。在低浓度段,恒定电流量线性增加,而在高浓度段,浓度逐渐增加,示出电流值从50mm或更高的浓度开始呈现恒定。这达到葡萄糖在电极中可被氧化的最大值,并且其中包括包含c-n配体的过渡金属复合物的氧化还原聚合物1被交联的电极示出约1.0μa的最大电流,并且包括包含c-n配体的过渡金属复合物的氧化还原聚合物2被交联的电极示出约0.2μa的最大电流。
[0149]
此外,测量了循环伏安法测试前后的电流变化。具体地,对于电流的变化,在10mm pbs中在-0.5至 0.1v下测量,并且在氧化还原聚合物1和氧化还原聚合物2包括包含c-n配体和pfpa的电子转移介体的情况下,在-0.3至 0.4v下测量,并且结果在图7a至图7d中示出。在图7a至图7d中,cv表示完成电极后立即测量的值,并且cv后表示在pbs溶液中搅拌1小时后测量的值。
[0150]
如上所述,包含pfpa的氧化还原聚合物被良好地固定到酶和电极表面,并且即使在低浓度段也示出清晰的响应,并且即使在一定浓度下也可以确认线性电流变化。另外,交联电极的极限催化电流分别为1.5μa、0.5μa、1.0μa和0.2μa。由此,证明了使用tpma-锇复合物类电子转移介体或c-n配体-锇复合物类电子转移介体和pfp聚合物基质的固定方法可用作血糖传感器。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。