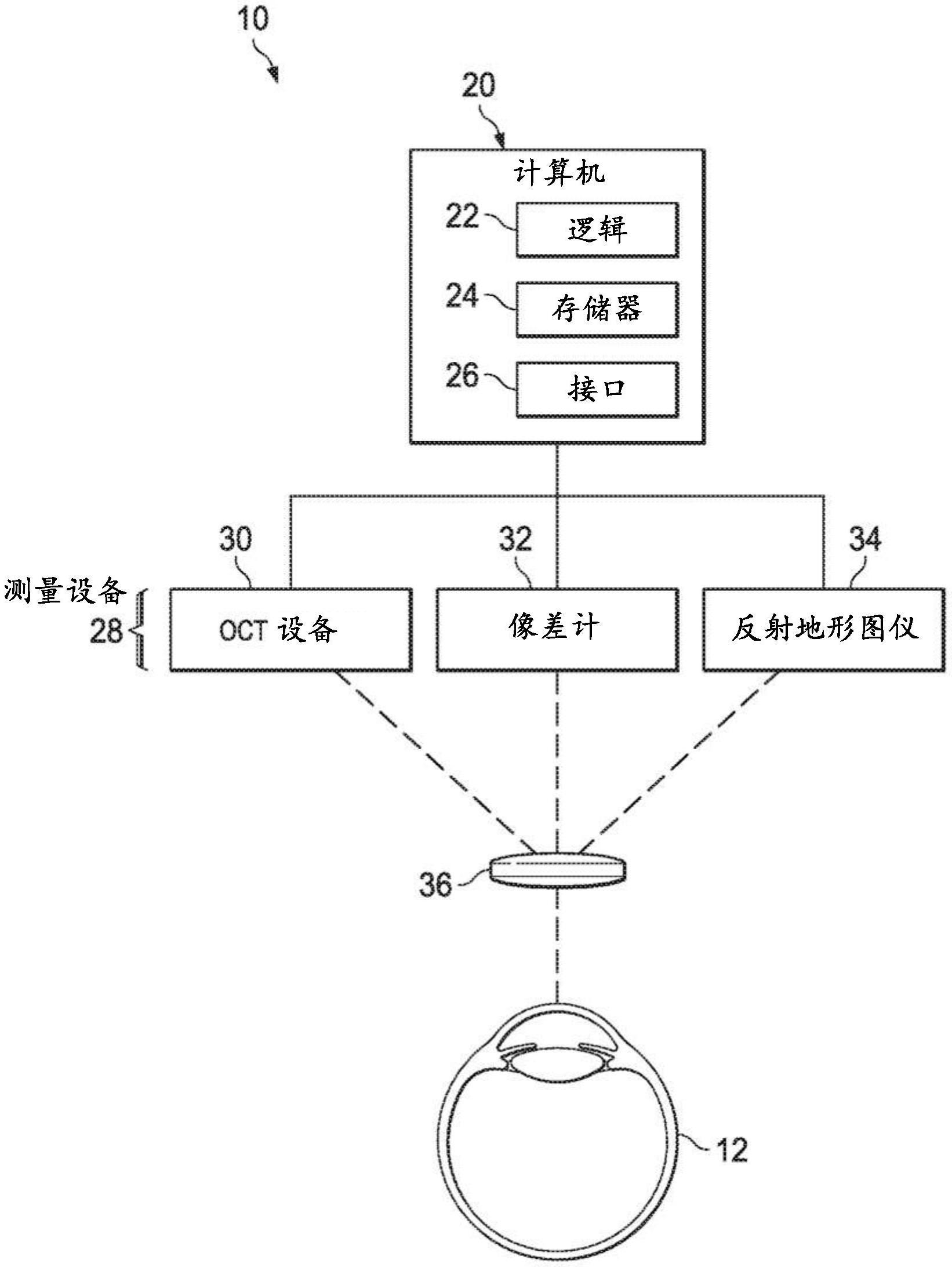
1.本发明属于制药技术领域,具体涉及一种自组装微沉淀组合物及其皮肤用凝胶、制备方法和应用。
背景技术:
2.皮炎发病率高,主要表现为红斑、潮红、脱屑等损害,自觉瘙痒,严重影响患者的正常生活。临床治疗多以激素及免疫抑制类药物为主,不良反应明显且患者极易产生耐受性,从而导致皮肤病反复发作,中药在治疗皮肤病方面有较好的应用前景。
3.近年来,在中医理论指导下常以龙胆泻肝汤化裁方治疗带状疱疹、接触性皮炎、急性湿疹等,获得了显著的治疗效果。其中君药龙胆,对于多种致病菌都有不同程度的抑制作用,抗过敏和抗炎作用显著。佐使药物甘草在各皮肤用经典方剂中广泛使用,甘草具有解毒,调和诸药,祛风止痒的功效。皮炎湿敷散为空军特色医学中心的军队医疗机构制剂,由龙胆、甘草两味药材组成,具有清热燥湿,抗敏止痒的功效,用于各种皮炎的治疗。
4.由于散剂有效成分难以溶出释放,中药难溶性成分生物利用度差,易损失,转移率低。长期以来,研究者们尝试应用多种制剂技术来解决这些难题,大量证据显示中药水煎煮过程形成的自组装体是决定其性质的关键因素,它的形成不仅能够促进活性成分的吸收及靶组织分布,还表现出更强的生物活性。但传统的水煎煮过程,往往只能提取部分水溶性成分,难溶性成分不易提取和保留;且水煎煮形成的自组装体易受多种因素影响,产率低,稳定性较差。
技术实现要素:
5.本团队首次构建基于反溶剂法的新型自组装微沉淀关键技术,获得的新型自组装微沉淀组合物可提高有效成分的经皮渗透能力,使药物到达皮肤更深层,前期实验证明,该组合物凝胶在体内外均具有较好的生物活性,因此,该技术对中药新药的开发应用具有重要意义。
6.本发明的第一个目的在于公开了一种自组装微沉淀组合物及其制备方法。
7.本发明第二个目的在于公开了上述自组装微沉淀组合物皮肤用凝胶及其制备方法。
8.本发明第三个目的在于公开了上述自组装微沉淀组合物的应用和自组装微沉淀组合物皮肤用凝胶的应用。
9.本发明的目的是通过以下技术方案实现的:
10.一种自组装微沉淀组合物,其特征在于,所述自组装微沉淀组合物通过下述方法制备:
11.(1)、按照重量比为龙胆:甘草=2.5:1称取原料龙胆和甘草;
12.(2)、取龙胆,加水浸泡0.5h,煎煮0.5~2h,过滤,重复煎煮0.5~2h,过滤,滤液合并,备用;
13.(3)、取甘草,加水浸泡0.5h,煎煮0.5~2h,过滤,重复煎煮0.5~2h,过滤,滤液合并,药渣备用;
14.(4)、取步骤(3)中甘草水煎煮剩余的药渣,加80%乙醇,提取0.5~2h,过滤,备用;
15.(5)、将步骤(4)制备的甘草药渣醇提液缓慢加入到步骤(2)制备的龙胆水煎液和步骤(3)制备的甘草水煎液中,混合后旋蒸快速除醇,得到0.25g生药/ml的混合提取液,即得自组装微沉淀组合物。
16.上述技术方案所述的自组装微沉淀组合物,其中:自组装微沉淀组合物平均粒径为100~800nm,pdi为0.05-0.40,电位绝对值为20~60mv;sem显示其形态为球形。
17.一种自组装微沉淀组合物的制备方法,其中,所述制备方法为自组装微沉淀技术,自组装微沉淀技术是基于反溶剂沉淀法,将适当浓度的中药醇提溶液加入至水煎煮液中,控制条件,使形成自组装微沉淀。
18.上述技术方案所述的制备方法,其中,所述方法包括以下步骤:
19.(1)、按照重量比为龙胆:甘草=2.5:1称取原料龙胆和甘草;
20.(2)、取龙胆,加水浸泡0.5h,煎煮0.5~2h,过滤,重复煎煮0.5~2h,过滤,滤液合并,备用;
21.(3)、取甘草,加水浸泡0.5h,煎煮0.5~2h,过滤,重复煎煮0.5~2h,过滤,滤液合并,药渣备用;
22.(4)、取步骤(3)中甘草水煎煮剩余的药渣,加80%乙醇,提取0.5~2h,过滤,备用;
23.(5)、将步骤(4)制备的甘草药渣醇提液缓慢加入到步骤(2)制备的龙胆水煎液和步骤(3)制备的甘草水煎液中,混合后旋蒸快速除醇,得到0.25g生药/ml的混合提取液,即得自组装微沉淀组合物。
24.一种自组装微沉淀组合物皮肤用凝胶,其中:自组装微沉淀组合物皮肤用凝胶由以下重量百分数的组分组成:自组装微沉淀组合物含量为30~50%;凝胶保湿剂为丙二醇和甘油,含量各为20~30%;增稠剂为丙烯酸钠/丙烯酰二甲基牛磺酸钠共聚物/异十六烷/聚山梨醇酯-80(sepineo p600)含量为3~5%;丁二醇含量为3~5%;羟苯乙酯含量为0.5~1%和1,2-己二醇含量为1~1.5%;
25.所述有效成分为上述技术方案所述的自组装微沉淀组合物。
26.上述技术方案所述自组装微沉淀组合物皮肤用凝胶的制备方法,其中:所述制备方法包括下述步骤:
27.(1)、根据上述技术方案的方法制备自组装微沉淀组合物;
28.(2)、称取以下重量百分数的原料:30~50%的自组装微沉淀组合物、3~5%的sepineo p600、3~5%的丁二醇、20~30%的甘油、20~30%的丙二醇、0.5~1%的羟苯乙酯和1~1.5%的1,2-己二醇;
29.(3)、取自组装微沉淀组合物、sepineo p600和丁二醇于烧杯中,在80℃条件下,以100-300r/min的转速,1000-1500rpm的均质条件下,均质搅拌20min,再加入甘油和丙二醇,持续均质搅拌20min,将温度降至65℃,继续以100~300r/min的转速加入羟苯乙酯和1,2-己二醇,均质搅拌10min,使混合均匀,分装,即得自组装微沉淀组合物皮肤用凝胶。
30.上述技术方案所述的自组装微沉淀组合物或自组装微沉淀组合物皮肤用凝胶在制备治疗皮肤病药物中的应用。
31.上述技术方案所述的应用,其中:所述皮肤病为特应性皮炎。
32.上述技术方案所述的应用,其中:所述应用为通过调控il-6/jak2/stat3信号通路,从而抑制炎性细胞增殖。
33.传统方式将醇提取液直接除醇,浓缩,进一步制备,整个过程中难溶性成分不稳定而析出,转移率极低;本发明改变了传统方式,采用基于反溶剂沉淀法的自组装微沉淀技术,将适当浓度的中药醇提溶液加入至水煎煮液中,控制条件,使形成自组装微沉淀;具体的技术是将甘草水提液、龙胆水提液与醇提液混合,温度升高使药物在混合溶剂中的溶解度变大,促使比表面积大的小粒子溶解;同时对药材醇提液、水提液生药浓度、混合加入方式等条件进行控制,旋蒸混合液,快速挥发乙醇,微粒来不及附着在已有粒子表面生长,便会析出很多独立的小粒子,得到一个多分散的微沉淀组合物体系,即为自组装微沉淀组合物。
34.本发明具有以下有益效果:
35.1、本发明制备的自组装微沉淀组合物粒径分布较为均一,体系较为稳定;其平均粒径为100~800nm,pdi为0.05-0.40,电位绝对值为20~60mv;sem显示其形态为球形。
36.2、本发明的自组装微沉淀组合物皮肤用凝胶具有较好的生物相容性,凝胶中的中药微沉淀组合物可通过调控il-6/jak2/stat3信号通路,从而抑制炎性细胞增殖。
附图说明:
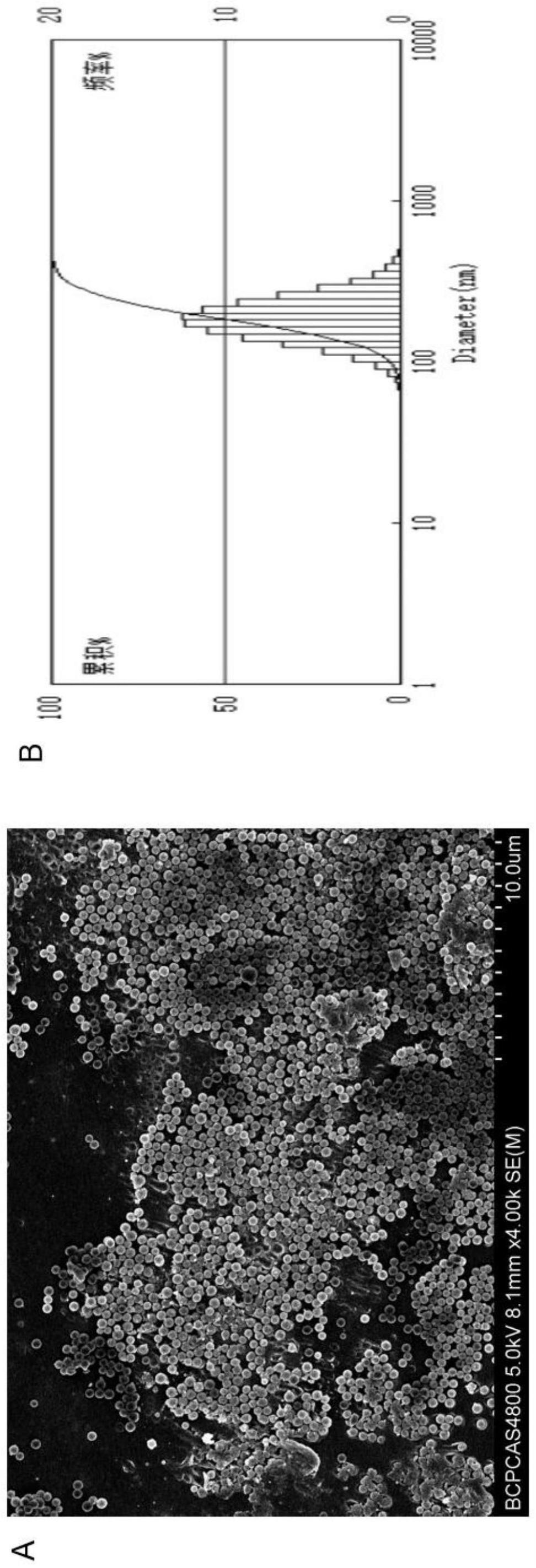
37.1、图1为是自组装微沉淀组合物的表征图,其中a为扫描电镜、透射电镜图片;b为粒径分布结果图。
38.2、图2为cck8增殖实验结果图,其中a为cck8检测不同提取物的细胞毒性;b为不同提取物对10ng/mltnf-α/ifn-γ诱导的hacat炎性细胞增殖抑制作用。
39.3、图3为rt-pcr检测相关mrna表达图;pcr检测结果表明甘草水提液、甘草醇提物、龙胆水提物、自组装微沉淀组合物可显著降低炎症细胞jak2、stat1、stat3、il-6的mrna的表达。
40.4、图4为试验例3中给药组的给药方法图。
41.5、图5为各组特应性皮炎模型小鼠皮损情况;其中:a.空白组;b.模型组;c.阳性药组;自组装微沉淀组合物凝胶低浓度(d)、中浓度(e)、高浓度(f)组。
具体实施方式:
42.为使本发明的技术方案便于理解,以下结合具体实施例对本发明一种自组装微沉淀组合物及其皮肤用凝胶、制备方法和应用作进一步的说明。
43.实施例1:自组装微沉淀组合物的制备:
44.自组装微沉淀的制备采用经典的反溶剂沉淀法,即将适当浓度的中药醇提溶液加入至水煎煮液中,控制条件,使形成自组装微沉淀组合物,具体操作步骤如下:
45.(1)、称取原料龙胆1428.5g和甘草571.4g;
46.(2)、取龙胆,加水浸泡0.5h,煎煮0.5~2h,过滤,重复煎煮0.5~2h,过滤,滤液合并,备用;
47.(3)、取甘草,加水浸泡0.5h,煎煮0.5~2h,过滤,重复煎煮0.5~2h,过滤,滤液合
己二醇,均质搅拌10min,使混合均匀,分装,即得自组装微沉淀组合物皮肤用凝胶。
67.实施例5:自组装微沉淀组合物皮肤用凝胶的制备:
68.本实施例的制备步骤与实施例4相同,区别仅在于各原料的重量:700g的自组装微沉淀组合物、70g的sepineo p600、90g的丁二醇、450g的甘油、550g的丙二醇、12g的羟苯乙酯和28g的1,2-己二醇。
69.实施例6:自组装微沉淀组合物皮肤用凝胶的制备:
70.本实施例的制备步骤与实施例4相同,区别仅在于各原料的重量:900g的自组装微沉淀组合物、90g的sepineo p600、70g的丁二醇、600g的甘油、400g的丙二醇、18g的羟苯乙酯和22g的1,2-己二醇。
71.实施例7:自组装微沉淀组合物皮肤用凝胶的含量测定:
72.(1)、hplc法测定龙胆苦苷含量:
73.仪器与试药:
74.lcms-2010ev高效液相色谱仪,日本岛津公司;甲醇为色谱纯;其他试剂为分析纯。
75.色谱条件:
76.色谱柱:diamonsil(2)-c
18
色谱柱(4.6
×
250mm,5μm);预柱:gl-cartridge c18柱;流动相:乙腈-0.2%磷酸水(15:85);流速:1.0ml/min;检测波长:270nm;柱温:30℃;进样量:10μl。
77.对照品溶液的制备:取龙胆苦苷对照品适量,精密称定,加70%乙醇溶液制成1ml含0.28mg的溶液,即得。
78.供试品溶液的制备:取实施例4制备的凝胶样品适量,置25ml容量瓶中,加入70%乙醇溶液适量,超声将其溶解,加70%乙醇溶液定容至刻度,摇匀、滤过,取续滤液,即得供试品溶液。
79.测定法分别精密吸取龙胆苦苷对照品溶液与供试品溶液各10μl,注入液相色谱仪,测定,即得。
80.(2)、hplc方法测定甘草酸、甘草查尔酮a:
81.色谱柱:diamonsil(2)-c
18
色谱柱(4.6
×
250mm,5μm);预柱为gl-cartridge c18柱;流动相a:乙腈,流动相b:0.05%磷酸溶液;流速:1.0ml/min;进样量:20μl;检测波长:250nm/370nm;柱温:30℃;按下表中的规定进行梯度洗脱。
82.表1梯度洗脱表
[0083][0084]
对照品溶液的制备:取甘草酸、甘草查尔酮a对照品适量,精密称定,加70%甲醇制成每1ml含0.2mg的溶液,即得对照品溶液。
[0085]
供试品溶液制备:取实施例4制备的凝胶样品适量,置25ml容量瓶中,加入70%乙
醇溶液适量,超声将其溶解,加70%乙醇溶液定容至刻度,摇匀、滤过,取续滤液,即得供试品溶液。
[0086]
测定法分别精密吸取甘草酸对照品溶液与供试品溶液各20μl,注入液相色谱仪,测定,即得。
[0087]
(3)、上述方法对凝胶样品的含量测定结果重复性好、准确度高,可用于凝胶样品的含量测定。最终确定每支凝胶(20g)中含有主要有效成分的量分别为:甘草酸不少于10mg,甘草查尔酮a不少于0.7mg,龙胆苦苷不少于40mg。
[0088]
以下通过具体试验例来说明本发明所具有的有益效果:
[0089]
试验例1:自组装微沉淀组合物的表征:
[0090]
一、取实施例1制备的自组装微沉淀组合物,加蒸馏水稀释20倍,采用纳米粒度仪测定粒径与pdi,重复测定3次,取平均值;
[0091]
二、对实施例1制备的自组装微沉淀组合物,加蒸馏水稀释20倍,用电位仪(上海中晨数字技术设备有限公司的js94k2电位仪)测定自组装微沉淀组合物的电位;
[0092]
三、sem观察自组装微沉淀组合物的形态,将样品用蒸馏水稀释20倍后滴在锡纸上,然后在20ma电流下用金钯导电层溅射镀膜1min,并在10kv的加速激励电压下进行观察。
[0093]
自组装微沉淀组合物的粒径分布、形态分析如图1所示(图1为是自组装微沉淀组合物的表征,其中a为扫描电镜、透射电镜图片,b为粒径分布结果图)。由图1可知,sem显示其形态为球形,自组装微沉淀组合物粒径分布较为均一,体系较为稳定。其平均粒径为100~800nm,pdi为0.05-0.40,电位绝对值为20~60mv(该数据可间接反应微沉淀组合物的稳定性,结果表明该微沉淀组合物分散体系的稳定性良好)。
[0094]
试验例2:自组装微沉淀组合物细胞药效学研究:
[0095]
1、细胞:hacat细胞
[0096]
2、试剂与器材:dmem培养基、高灭活胎牛血清、青链霉素混合液、cck-8试剂盒。
[0097]
3、实验方法:
[0098]
(1)、cck8增殖实验:
[0099]
取生长状态良好且处于对数生长期的hacat细胞,接种于96孔板,每个孔细胞密度保持在1
×
104个,将96孔板置于37℃,5%co2恒温培养箱中进行贴壁培养。以不同浓度梯度甘草水提物(gw:1600、800、400、200、100、50、25、12.5、6.25μg/ml)、甘草醇提物(ga:800、400、200、100、50、25、12.5、6.25、3.125μg/ml)、龙胆水提物(rw:2000、1000、500、250、125、62.5、31.25、15.625、7.8125μg/ml),自组装微沉淀组合物(sam:3200、1600、800、400、200、100、50、25、12.5μg/ml)分别作用于诱导的hacat炎症细胞24h。
[0100]
(2)、pcr法检测hacat细胞炎症相关细胞因子的表达水平:
[0101]
取对数生长期hacat细胞,接种于6孔板中,待细胞完全贴壁后,加入不同药物(gw:50、100μg/ml,ga:12.5、25μg/ml,rw:6.25、12.5μg/ml,sam:400、800μg/ml)处理24h。收集细胞,加入trizol试剂提取总rna。反转录制备cdna,除去培养基,pbs洗1次,除去pbs,每组加入1mltrizol后放置于冰面,轻摇使trizol试剂充分接触5min。rt-qpcr检测tnf-a、il-6等在细胞中的的mrna的表达,采用2
‑△△
ct
法计算mrna相对表达量。
[0102]
4、实验结果:cck8结果表明,四种不同浓度药物细胞生物相容性较好,结果见图2a。细胞增殖实验表明,不同浓度药物可显著抑制tnf-α和ifn-γ诱导的hacat炎症细胞的
增殖,结果见图2b。
[0103]
pcr结果表明,三种提取物及自组装微沉淀组可显著抑制jak2、stat1、stat3、il-6表达(图3),以上结果表明其通过调控il-6/jak2/stat3通路抑制tnf-α和ifn-γ诱导的hacat炎症细胞增殖。
[0104]
试验例3:自组装微沉淀组合物皮肤用凝胶(以下称:自组装微沉淀组合物凝胶)抗特应性皮炎的药效学研究:
[0105]
1、动物:雄性balb/c小鼠48只,spf级,8周龄,体重25-30g。
[0106]
2、试剂与器材:2,4-二硝基氯苯(dncb)(美国sigma公司,批号:2508193);il-6、tnf-α的水平和酶联免疫吸附(elisa)试剂盒。
[0107]
3、实验方法:
[0108]
(1)、模型建立与给药:
[0109]
将经检疫合格的spf级balb/c小鼠,随机分组,每组6只,分别为空白组;dcnb模型组;自组装微沉淀组合物凝胶组(1、2、4g
·
kg-1
以生药量计,下同);地塞米松乳膏阳性对照组(1.0g
·
kg-1
)。
[0110]
小鼠经两天适应性喂养后,在实验前一天使用脱毛膏脱去背部毛发(约2cm
×
2cm面积)。1d和4d模型组和各给药组于背部脱毛区涂抹含5%2,4-二硝基氯苯(dncb)的基质溶液(丙酮∶橄榄油溶液=3:1配制)100μl。空白对照组小鼠相应部位涂抹等体积空白基质溶液。空白组涂抹等量基质、给药组:方法见图4。前期高剂量的dncb刺激后小鼠背部皮肤出现水肿、红斑、结痂,后期0.5%dncb刺激后出现暗红斑及鳞屑,表明小鼠造模成功。
[0111]
(2)、相关指标观察:(一)小鼠皮炎评分:观察皮肤组织病理形态学变化。(二)皮肤组织中il-6、tnf-α等因子检测:称取创面皮肤及正常组皮肤500mg,用0.5mlph为7.4的pbs匀浆后,在4℃,12000r/min条件下离心20min。收集上清用elisa试剂盒检测。
[0112]
4、实验结果:
[0113]
各组小鼠背部皮损情况比较:各组小鼠第28天皮损情况见图5。由图5可知,模型组与正常组小鼠相比,背部皮肤大面积泛红增厚,表明造模成功。阳性药组虽红肿破损消失,但皮肤出现明显皱缩,自组装微沉淀组合物凝胶组小鼠皮损显著改善,且随着给药浓度增大,治疗效果越明显。
[0114]
表4为各组小鼠皮损组织中炎症因子il-6、tnf-α的含量。由表可知,与正常组相比,模型组小鼠的炎症因子含量均显著增加(p《0.05),说明造模成功。除低剂量组的il-6、tnf-α含量外,其余各给药组炎症因子含量与模型组相比,差异均具有统计学意义。
[0115]
表4不同组对炎症小鼠主要炎症因子分泌的影响(x
±
sd,n=8)
[0116][0117]
注:与空白组比较,
*
p《0.05,
**
p《0.01;与模型组比较,
#
p《0.05,
##
p《0.01
[0118]
以上所述,仅为本发明的较佳实施例,并非对本发明作任何形式上和实质上的限
制,凡熟悉本专业的技术人员,在不脱离本发明技术方案范围内,当可利用以上所揭示的技术内容,而作出的些许更动、修饰与演变的等同变化,均为本发明的等效实施例;同时,凡依据本发明的实质技术对以上实施例所作的任何等同变化的更动、修饰与演变,均仍属于本发明的技术方案的范围内。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。