1.本技术属于生物药物制剂技术领域,尤其涉及一种抗肿瘤药物制剂及其制备方法和应用。
背景技术:
2.肿瘤一直是危害人类健康的一个重大疾病,会造成人体正常组织器官结构和功能的破坏,严重的可引起患者死亡。化疗是目前治疗肿瘤的主要方式之一。
3.目前,临床上主要用于化疗的药物包括:硼替佐米、阿霉素以及顺铂等。通常情况下,由于化疗过程所采取的药物用量大,因此,大量的化疗药物会在一定程度上对患者造成胃肠不适、细胞受损、骨髓抑制的副作用。然而,减少药物用量会让肿瘤清除不彻底甚至会让肿瘤产生耐药性,并且这些药物价格高昂,治疗周期长,会给患者在精神和物质上造成巨大压力。
4.因此,亟需提供一种既可以使得化疗药物的用量减小,又能够增强化疗药物对于肿瘤的治疗效果的抗肿瘤药物制剂。
技术实现要素:
5.有鉴于此,本技术实施例提供了一种抗肿瘤药物制剂及其制备方法和应用。该抗肿瘤药物制剂能够通过增强广谱抗肿瘤药物的治疗效果来抑制肿瘤细胞的活性,并且能够有效减小实体肿瘤的大小。
6.本技术实施例的第一方面提供了一种抗肿瘤药物制剂,该抗肿瘤药物制剂为硅矿抗肿瘤药物制剂,该抗肿瘤药物制剂包括:含有一种或者多种的硅离子的硅酸盐矿物以及至少一种广谱抗肿瘤药物;其中,硅离子的浓度范围为0.25~120ppm。
7.结合第一方面,在第一方面的第一种可能实现方式中,广谱抗肿瘤药物包括:硼替佐米、顺铂、阿霉素、pd-l1、紫杉醇、异长春花碱、奥沙利铂、多西他赛以及吉西他滨中的一种或者多种。
8.结合第一方面,在第一方面的第二种可能实现方式中,硅酸盐矿物包括硅酸钙、硅酸钠、镁黄长石、锌黄长石、铜硅钙石、硅酸锌、硅酸铜、生物玻璃以及铜或锌掺杂介孔二氧化硅中的一种或多种。
9.结合第一方面,在第一方面的第三种可能实现方式中,抗肿瘤药物制剂包括:含有硅离子浓度为30ppm的硅酸盐矿物、阿霉素、顺铂以及硼替佐米;其中,阿霉素的浓度为0~20μm,顺铂的浓度为0~10μm,硼替佐米的浓度为0~500nm。
10.结合第一方面,在第一方面的第四种可能实现方式中,抗肿瘤药物制剂包括:硅离子/硼替佐米组合抗肿瘤药物制剂、硅酸钙/阿霉素复合抗肿瘤药物制剂以及阿霉素/镁黄长石/锌黄长石/铜硅钙石粉体复合抗肿瘤药物制剂。
11.本技术实施例的第二方面提供了一种抗肿瘤药物制剂的制备方法,包括:将硅酸盐矿物制备为硅离子的浓度范围在0.5~120ppm的硅离子制剂;配置广谱抗肿瘤药物的药
物制剂,该广谱抗肿瘤药物的药物制剂中包括至少一种广谱抗肿瘤药物所对应的预设浓度的药物制剂;按照预设比例将硅离子制剂以及广谱抗肿瘤药物的药物制剂进行混合,得到抗肿瘤药物制剂。
12.结合第二方面,在第二方面的第一种可能实现方式中,硅离子制剂是通过灭菌水、pbs、生理盐水或细胞培养基制备的。
13.结合第二方面,在第二方面的第二种可能实现方式中,该方法还包括:将硅离子制剂所对应的硅酸盐矿物的一种或多种,与广谱抗肿瘤药物,溶于高分子溶液,制备材料形式包括微针、水凝胶或者电纺丝的产品;其中,高分子溶液包括海藻酸钠溶液、透明质酸溶液或者结冷胶中的至少一种。
14.本技术实施例的第三方面提供了一种抗肿瘤药物制剂的应用,该应用包括第一方面所述的抗肿瘤药物制剂在耐药性肿瘤中的应用。
15.结合第三方面,在第三方面的第一种可能实现方式中,耐药性肿瘤包括急性白血病(淋巴细胞性和粒细胞性)所引起的肿瘤、恶性淋巴瘤、乳腺癌、支气管肺癌(未分化小细胞性和非小细胞性)、卵巢癌、软组织肉瘤、成骨肉瘤、横纹肌肉瘤、尤文肉瘤、母细胞瘤、神经母细胞瘤、膀胱癌、甲状腺癌、前列腺癌、头颈部鳞癌、睾丸癌、胃癌、肝癌等中的一种或多种。
16.本技术实施例与现有技术相比存在的有益效果是:
17.本技术实施例提供一种抗肿瘤药物制剂及其制备方法和应用。该抗肿瘤药物制剂为硅矿抗肿瘤药物制剂,该抗肿瘤药物制剂包括:含有一种或者多种的硅离子的硅酸盐矿物以及至少一种广谱抗肿瘤药物;其中,硅离子的浓度范围为0.25~120ppm。该抗肿瘤药物制剂能够通过增强广谱抗肿瘤药物的治疗效果来抑制肿瘤细胞的活性,并且能够有效减小实体肿瘤的大小,且该种抗肿瘤药物制剂能够在增强化疗药物的治疗效果的同时减少药物的使用量,在一定程度上减轻患者的负担。
附图说明
18.为了更清楚地说明本技术实施例中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本技术的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动性的前提下,还可以根据这些附图获得其他的附图。
19.图1是本技术实施例提供的硅离子增强硼替佐米诱导的人多发性骨髓瘤细胞系的凋亡的实验结果示意图;
20.图2是本技术实施例提供的硅离子联合硼替佐米诱导新诊断多发性骨髓瘤细胞的凋亡的实验结果示意图;
21.图3是本技术实施例提供的硅离子联合硼替佐米诱导难治性或复发性多发性骨髓瘤细胞的凋亡的实验结果示意图;
22.图4是本技术实施例提供的硅离子增强了硼替佐米对人多发性骨髓瘤细胞系的g2/m细胞周期阻滞的实验结果示意图;
23.图5是本技术实施例提供的硅离子增强了硼替佐米对nf-κb通路的抑制的实验结果示意图;
24.图6是本技术实施例提供的硅离子联合阿霉素和顺铂对骨肉瘤细胞、乳腺癌瘤细胞、黑色素瘤细胞活性的影响的示意图;
25.图7是本技术实施例提供的不同种类的硅矿联合阿霉素对黑色素瘤细胞的影响的示意图;
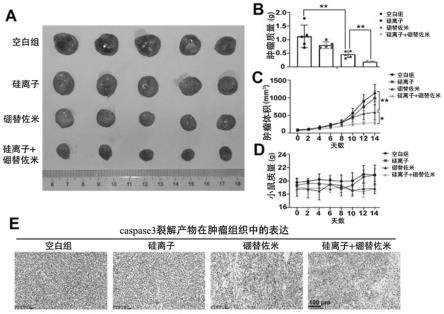
26.图8是本技术实施例提供的硅离子联合硼替佐米在小鼠体内骨髓瘤作用过程的示意图。
具体实施方式
27.以下描述中,为了说明而不是为了限定,提出了诸如特定系统结构、技术之类的具体细节,以便透彻理解本技术实施例。然而,本领域的技术人员应当清楚,在没有这些具体细节的其它实施例中也可以实现本技术。在其它情况中,省略对众所周知的系统、装置、电路以及方法的详细说明,以免不必要的细节妨碍本技术的描述。
28.以下结合具体的实施例对本技术提供的技术方案进行详细的解释说明。
29.本技术实施例提供了一种抗肿瘤药物制剂,该抗肿瘤药物制剂包括:含有硅离子的硅酸盐矿物以及至少一种广谱抗肿瘤药物;其中,含有硅离子的硅酸盐矿物中硅离子的浓度范围为0.5~120ppm。
30.在本实施例中提供的抗肿瘤药物制剂中,广谱抗肿瘤药物包括:硼替佐米、顺铂、阿霉素、紫杉醇、异长春花碱、奥沙利铂、多西他赛以及吉西他滨中的一种或者多种。具体在制备抗肿瘤药物制剂时可以根据实际需求进行选择,本实施例中不做具体限制。
31.在一些实施例中,硅酸盐矿物包括硅酸钙、硅酸钠、镁黄长石、锌黄长石、铜硅钙石、硅酸锌、硅酸铜、生物玻璃以及铜或锌掺杂介孔二氧化硅中的一种或多种。
32.作为本技术提供的抗肿瘤药物制剂的一个实施例,该抗肿瘤药物制剂包括:含有硅离子浓度为30ppm的硅酸盐矿物、阿霉素、顺铂以及硼替佐米。其中,阿霉素的浓度为0.5~20μm,优选为10μm;顺铂的浓度为0.5~10μm,优选为5μm;硼替佐米的浓度为0.5~500nm,优选为50nm。
33.本实施例中所提供的抗肿瘤药物制剂,应用于耐药性肿瘤,该耐药性肿瘤
34.包括急性白血病(淋巴细胞性和粒细胞性)所引起的肿瘤、恶性淋巴瘤、乳腺5癌、支气管肺癌(未分化小细胞性和非小细胞性)、卵巢癌、软组织肉瘤、成
35.骨肉瘤、横纹肌肉瘤、尤文肉瘤、母细胞瘤、神经母细胞瘤、膀胱癌、甲状腺癌、前列腺癌、头颈部鳞癌、睾丸癌、胃癌、肝癌等中的一种或多种。
36.以下对本技术实施例中提供的抗肿瘤药物制剂的制备方法进行详细的解释说明。
37.0本技术实施例提供的抗肿瘤药物制剂的制备方法包括以下步骤s101~s105。
38.s101、将硅酸盐矿物制备为硅离子的浓度范围在0.5~120ppm的硅离子制剂。
39.s102、配置广谱抗肿瘤药物的药物制剂,该广谱抗肿瘤药物的药物制剂中包括至少一种广谱抗肿瘤药物所对应的预设浓度的药物制剂。
40.5s103、按照预设比例将硅离子制剂以及广谱抗肿瘤药物的药物制剂进行混
41.合,得到抗肿瘤药物制剂。
42.s104、将硅离子制剂所对应的硅酸盐矿物的一种或多种,与广谱抗肿瘤药物,溶于高分子溶液,制备材料形式包括微针、水凝胶或者电纺丝的产品;
43.其中,高分子溶液包括海藻酸钠溶液、透明质酸溶液或者结冷胶中的至少0一种。
44.以下以具体的实例对上述抗肿瘤药物制剂的制备方法作进一步的解释说明。
45.作为本技术提供的抗肿瘤药物制剂的制备方法的一个实施例,制备硅离子/
46.硼替佐米(bor)组合抗肿瘤药物制剂。具体包括,硅离子制剂的配置方法如
47.下:将硅酸钙粉末以1mg/ml的固体/液体比率溶解于去离子水中,按照一定的5比例加入至rpmi-1640培养液中,配置成浓度为0.25-120ppm(μg/ml)的离
48.子制剂;bor制剂的配置方法如下:将bor以1mm的固体/液体比率溶解于磷酸缓冲盐溶液(pbs)中,按一定比例加入rpmi-1640培养液中,配置成浓度为0-500nm的药物制剂;硅离子/硼替佐米(bor)组合抗肿瘤药物制剂配置方法如下:按照预设比例将上述硅离子制剂和bor药物制剂混合,其中硅离子制剂浓度为0.25-120ppm(μg/ml),bor药物制剂的浓度为0-100nm。
49.作为本技术提供的抗肿瘤药物制剂的制备方法的一个实施例,制备一种含有硅酸钙/广谱抗肿瘤药物复合制剂。具体包括,广谱抗肿瘤药制剂的配置方法如下:将阿霉素、顺铂中的任意一种以1mm的固体/液体比率溶解于pbs中,按一定的比例加入肿瘤培养基中,配置成浓度为0-20μm的广谱抗肿瘤药物制剂;硅酸钙制剂的配置方法如下:将硅酸钙粉末以1mg/ml的固体/液体比率溶解于去离子水中,按照一定的比例加入至耐药肿瘤细胞专用细胞培养液中,配置成浓度为0.25-120ppm(μg/ml)的离子制剂;硅酸钙增强广谱抗肿瘤药制剂的配置方法如下:按照预设比例将上述几种制剂混合,其中广谱抗肿瘤药的浓度为0-20μm,硅酸钙的浓度为0.25-120ppm(μg/ml)。
50.此外,在一些实施方案中,本实施例还提供了一种制备广谱抗肿瘤药物/多种硅矿复合药物制剂。具体包括,广谱抗肿瘤药制剂的配置方法如下:将阿霉素以1mm的固体/液体比率溶解于pbs中,按一定的比例加入肿瘤培养基中,配置成浓度为0-20μm的广谱抗肿瘤药物制剂;多种硅矿制剂的配置方法如下:根据iso/en 10993-12,制备一系列镁黄长石/锌黄长石/铜硅钙石粉体的稀释离子提取物。首先,将镁黄长石/锌黄长石/铜硅钙石粉体加入到无血清肿瘤细胞培养液中,在200mg/ml的固体/液体比率下,在37℃孵育24小时,将混合物以4000rpm离心10分钟,然后将上清液通过过滤膜(millipore,0.22μm)灭菌并收集以获得储备溶液。然后,采用肿瘤细胞培养液稀释储备溶液以制备合适的离子提取物;多种硅矿增强广谱抗肿瘤药制剂的配置方法如下:按照预设比例将上述几种制剂混合,其中阿霉素的浓度为0-20μm,硅矿的浓度为0.25-120ppm(μg/ml)。
51.通过以上方式则可以制备出如硅离子/硼替佐米(bor)组合抗肿瘤药物制剂、硅酸钙/广谱抗肿瘤药物复合制剂以及广谱抗肿瘤药物/多种硅矿复合药物制剂等抗肿瘤药物制剂。通过本技术实施例中的制备方法制备的抗肿瘤药物制剂能够通过增强广谱抗肿瘤药物的治疗效果来抑制肿瘤细胞的活性。
52.以下则以具体的实验实例对通过本技术实施例提供的抗肿瘤药物制剂的制备方法所制得的抗肿瘤药物制剂,对增强广谱抗肿瘤药物的治疗效果进行详细的解释说明。
53.首先是硅离子增强硼替佐米诱导的人多发性骨髓瘤细胞系(hmcls)细胞凋亡的影响。具体的,在本技术的一个实施方案中,采用硅离子/硼替佐米组合抗肿瘤药物制剂,对hmcls细胞凋亡和细胞周期进行评价。首先采用硅离子/硼替佐米组合抗肿瘤药物制剂处理hmcls并培养24小时,根据制造商的说明用膜联蛋白v-fitc/pi(dojindo,kumamoto,japan)
染色,然后通过流式细胞仪(bd biosciences)分析以检测细胞凋亡。使用flow jo软件(v10,tree star,ashland,united states)评估凋亡数据。用上述配置的溶液,处理hmcls并培养24小时,根据制造商的说明用pi染色(multi-sciences,lianke bio,china)染色,然后通过流式细胞仪(bd biosciences)分析以检测细胞周期。mod-fit lt软件(v3.1,verity software house,inc.,topsham,me,united states)用于评估细胞周期数据。
54.然后是硅离子增强硼替佐米对新诊断的多发性骨髓瘤(ndmm)和难治性或复发性多发性骨髓瘤(rrmm)的影响。在本技术的一个实施方案中,用硅离子/硼替佐米组合抗肿瘤药物制剂对人的外周血单个核细胞(pbmc)、从ndmm患者分离的原代ndmm细胞和从rrmm患者分离出的原代rrmm细胞进行评价。
55.再是硅酸钙增强阿霉素/顺铂制剂对于耐药性肿瘤细胞活性的影响。在本技术的一个实施方案中,本实验选取三种耐药性肿瘤细胞,mnng(骨肉瘤细胞),4t1(乳腺癌细胞),b16f10(黑色素瘤细胞),药物选取盐酸阿霉素和顺铂(临床上典型广谱抗肿瘤药物),硅离子溶液用硅酸钙配置,浓度选用为0,cs/1/8,cs/1/4,cs/1/2。将养好的肿瘤细胞,吸去培养基,滴入1~2ml胰酶,然后放培养箱中1min,再加入等量的培养基中和,离心(1000r,3min),再吸取上层清液,加入5ml培养基,吹打,每个孔板放入约1000个细胞,放在培养箱中一天,待肿瘤细胞完全贴壁,再吸取掉培养基,加入100μl含有硅离子的药物溶液(过滤菌膜后的溶液),放入培养箱中培养2d,取出后,吸掉废液,再加入100μlcck8溶液,再放入培养箱中培养2h,用酶标仪测试得出结果。
56.进而是si/bor联合治疗对在小鼠体内多发性骨髓瘤(arp-1)的功效。在本技术的一个实施方案中,将6周大的nod-scid(非肥胖糖尿病-先天性突变免疫缺陷)小鼠皮下注射arp-1(5
×
106)细胞至左右两侧,以建立mm(多发性骨髓瘤)异种移植模型。7天后,当肿块形成时,将小鼠随机分为四组(每组n=6),包括载体、bor、si和si/bor组合组。bor(1mg/kg)每三天腹腔注射一次,连续2周,si(200ul)瘤周皮下注射,每天一次,持续2周。每两天用卡尺监测肿瘤大小。肿瘤组织取自荷瘤nod/scid小鼠,肿瘤块在4%多聚甲醛中固定,然后在切片前包埋在石蜡中。最后,进行免疫组织化学染色以分析裂解的半胱氨酸蛋白酶-3(caspase3)。
57.以下则对上述实验过程以具体实施过程的方式进行解释说明。
58.实例1:硅离子(si)增强硼替佐米(bor)诱导的人多发性骨髓瘤细胞系(hmcls)细胞凋亡的影响。
59.硅酸钙制剂的配置方法如下:将硅酸钙粉末以1mg/ml的固体/液体比率溶解于去离子水中,按照一定的比例加入至rpmi-1640培养液中,配置成浓度为0.25-120ppm(μg/ml)的离子制剂。
60.bor制剂的配置方法如下:将bor以1mm的固体/液体比率溶解于pbs中,按合适比例加入rpmi-1640培养液中,配置成浓度为0-500nm的药物制剂。
61.si增强bor制剂的配置方法如下:按照特定比例将上述几种制剂混合,其中硅酸钙制剂浓度为0.25-120ppm(μg/ml),bor制剂浓度为0-100nm
62.基于上述配置的溶液,对hmcls进行处理并培养24小时,然后采用膜联蛋白v-fitc/pi(dojindo,kumamoto,japan)对其进行染色,再通过流式细胞仪(bd biosciences)分析以检测细胞凋亡。使用flow jo软件(v10,tree star,ashland,united states)评估凋
亡数据。
63.基于上述配置的溶液,处理hmcls并培养24小时,然后采用pi染色(multi-sciences,lianke bio,china)进行染色,再通过流式细胞仪(bd biosciences)分析以检测细胞周期。mod-fit lt软件(v3.1,verity software house,inc.,topsham,me,united states)用于评估细胞周期数据。
64.首先,根据数据显示判断si是否对mm细胞具有细胞毒性:基于不同浓度的cs处理hmcls(arp-1、cag、nci-h929、jjn3、lp1、mm1.s、u266、u266/bor(bor抗性细胞)和rpmi-8226)24小时,然后使用流式细胞术分析细胞凋亡。结果表明,不同浓度的si不会增加mm细胞的凋亡。然后,判断si/bor组合对不同mm细胞的协同作用:将包括arp-1、u266和u266/bor的hmcls与si、bor和si/bor组合孵育24小时,并通过流式细胞术分析细胞凋亡。从q4象限的细胞存活率可以得出,如图1中a部分所示,未经任何处理的mm细胞具有更高的存活率(arp-1:90.3%;u266:90.0%;u266/bor:82.5%),而单用si对细胞存活率没有任何影响(arp-2:88.2%;u264:92.4%;u266/bor:81.1%)。当两个非耐药mm细胞用低剂量的bor(arp-1:2nm;u266:5nm)处理时,细胞存活率略有下降(arp1:84.0%;u26:81.2%),而si/bor组合显著降低了细胞存活率(arp-1:259.2%;u266:52.2%)。对于耐药mm细胞(u266/bor),观察到用高剂量50nm bor治疗u266/bor导致56.1%的细胞存活率,而用相同bor剂量(50nm)的si/bor组合显著降低细胞存活率至36.5%。此外,根据流式细胞术的结果计算bor的半最大抑制浓度(ic50)。可见,u266/bor中bor的ic50(ic50:65.58nm)远高于bor敏感细胞系(arp-1和u266;ic50:5.31nm和7.87nm)。另外,研究数据表明:si/bor组合处理明显降低了bor的ic50,特别是对于bor抗性细胞系(arp-1,ic50:3.01nm;u266,ic50:4.59nm;u266/bor,ic50:18.44nm),如图1中b部分所示。为了对上述结果进行证实,本实施例中以蛋白质印迹来评估凋亡相关蛋白的表达。如图1中c部分所示,联合治疗显著增加了裂解的caspase-3和裂解的parp1的表达。综上,本实验表明si作为敏化剂,可增加bor对hmcls(包括bor抗性细胞系)的细胞毒性作用。
65.实例2:硅离子(si)增强硼替佐米(bor)治疗新诊断的多发性骨髓瘤(ndmm)和难治性或复发性多发性骨髓瘤(rrmm)。
66.骨髓瘤样本获取:从mm患者处获取骨髓样本,并从健康捐赠者处获取外周血。
67.骨髓瘤细胞培养:用淋巴细胞分离液(corning,usa)分离骨髓单核细胞(bmc)和外周血单个核细胞(pbmc),然后在含有20%fbs的rpmi-1640培养基中在37℃、5%co2气氛下培养。原代ndmm和rrmm细胞用cd138flow抗体标记。
68.为了进一步验证si/bor组合的活性和安全性,本实施例中特别选择了健康人的外周血单个核细胞(pbmc)、从ndmm患者分离的原代ndmm细胞和从rrmm患者分离出的原代rrmm细胞。采用一系列浓度的bor和/或1/2浓度的cs进行体外治疗无法诱导从健康供体分离的pbmc凋亡。对于原代ndmm细胞,单独用bor处理导致细胞凋亡显著增加,其特征为cd138 免疫表型,而单独用1/2浓度的si溶液处理不能诱导凋亡(p《0.05)。与单独的bor治疗相比,si/bor组合治疗导致细胞凋亡显著增加,如图2中a部分和b部分所示。然后,本实施例中进一步评估si/bor组合是否仍诱导从rrmm患者分离的原代rrmm细胞凋亡。如图3中a部分和b部分所示,在5个rrmm患者样本中,与单独的bor相比,si/bor组合治疗导致cd38 细胞凋亡显著增加。这些结果表明,si与bor联合不仅有效杀死了从ndmm患者分离的原代ndmm细胞,
而且显著抑制了从rrmm患者分离出的rrmm细胞,参见图2和图3所示。更重要的是,si/bor不杀死正常造血干细胞,这表明其具有良好的生物安全性。
69.实例3si增强bor诱导的hmcls的g2/m细胞周期阻滞。
70.采用si/bor组合药物处理hmcls细胞24小时。
71.采用pi对细胞染色(multi-sciences,lianke bio,china)染色。
72.通过流式细胞仪(bd biosciences)分析以检测细胞周期。
73.mod-fit lt软件(v3.1,verity software house,inc.,topsham,me,united states)用于评估细胞周期数据。
74.g2/m细胞周期阻滞是bor诱导的主要细胞变化之一。为了进一步研究si/bor组合疗法的作用机制,本实施例中评估了细胞周期状态。如图4所示,在u266/bor细胞系中,单独暴露于bor 24小时后,g2/m期的细胞百分比显著增加,g1期的比例相应降低,但也明显降低了s相。对于arp-1和u266细胞,bor处理导致g2/m和g1期增加,但s期减少。而si/bor组合处理导致hmcls中g2/m期的细胞周期停滞比单独的bor更显著,这可能与诱导多发性骨髓瘤凋亡的协同作用有关。相比之下,单用si处理不会影响细胞周期的分布。
75.实例4si增强bor对nf-κb通路的抑制。
76.用pbs冲洗细胞并使用ripa裂解缓冲液分离蛋白。
77.蛋白质含量通过bca试剂盒(上海epizyme biomedical technology,china)测定。
78.将20mg样品的总蛋白装载在4%-20%聚丙烯酰胺凝胶上,并转移至pvdf膜(默克millipore,达姆施塔特,德国)。室温下在封闭缓冲液中浸泡1小时后,将膜与各种一级抗体在4℃下孵育过夜,然后与二级抗体孵育1小时。
79.研究表明,核因子κb(nf-κb)的激活导致mm患者的愈后不佳。bor通过抑制蛋白酶体介导的κ,其中iκba与活化的b细胞中磷酸化的核因子-κ轻链增强子结合,防止其转位到细胞核。因此,本实施例中进一步探讨了si/bor组合对nf-κb信号传导的影响。如图5所示,本实施例中的结果表明在hmcls中单独用bor治疗明显增加了iκba和磷酸化iκb的表达,并抑制了nf-κb通路的激活,表现为磷酸化p65、p105和p50的表达减少,而未观察到对磷酸化的p65、p105和p50的调节作用。这一结果表明,si单独对nf-κb通路的抑制能力非常弱。可见,si/bor组合治疗导致nf-κb相关蛋白表达的抑制显著高于单独bor治疗,这表明si和bor对hmcls的协同作用
80.实例5:硅酸钙增强阿霉素/顺铂制剂的制备及其对于耐药性肿瘤细胞活性的影响。
81.广谱抗肿瘤药制剂的配置方法如下:将阿霉素、顺铂中的任意一种以1mm的固体/液体比率溶解于pbs中,按一定的比例加入肿瘤培养基中,配置成浓度为0-20μm的广谱抗肿瘤药物制剂。
82.硅酸钙制剂的配置方法如下:将硅酸钙粉末以1mg/ml的固体/液体比率溶解于去离子水中,按照一定的比例加入至耐药肿瘤细胞专用细胞培养液中,配置成浓度为0.25-120ppm(μg/ml)的离子制剂。
83.硅酸钙增强广谱抗肿瘤药制剂的配置方法如下:按照特定的比例将上述几种制剂混合,其中广谱抗肿瘤药的浓度为0-20μm,硅酸钙的浓度为0.25-120ppm(μg/ml)。
84.取上述配置好的溶液,按照比例加入胎牛血清,生长补充剂与青霉素和链霉素。将
耐药性肿瘤细胞接种于96孔培养板中,初始密度为每孔1
×
103个细胞,培养24小时后,将细胞培养基更换为配置好的硅酸钙/抗肿瘤药制剂。再次培养48小时后,通过cck-8(细胞计数试剂盒-8)在酶标仪450nm下测量所有样品的吸光度来评估细胞的活性。
85.参见图6所示,根据cck8的数据可知,当不加任何药物时,细胞的存活率不受到si浓度的影响,因此本实施例中所选用的si浓度是一个安全的浓度。在不添加si的时候,阿霉素等于5μm的时候对mnng,4t1,b16f10肿瘤细胞均有抑制功能,但只有20%~30%的抑制率,而随着si浓度的增加,si与阿霉素结合,三种肿瘤细胞的存活率不断降低,当si浓度等于cs/1/2时,三种肿瘤细胞的抑制率达到了40%~50%,提升了近一倍,说明si可以有效增强阿霉素的治疗效果。在阿霉素等于10μm时,si浓度等于0时与si浓度等于cs/1/2时,4t1细胞组的细胞存活率显著降低至21%。当顺铂浓度为5μm时,顺铂对三种肿瘤的抑制率达到了50%~60%,而随着si浓度的提高,肿瘤的抑制率不断增加,当si浓度等于cs/1/2时,三种肿瘤的抑制率达到了70%~80%,当顺铂浓度在10μm时就可以将肿瘤细胞完全抑制,三种肿瘤细胞的存活率均在20%以下(此时默认肿瘤细胞已被完全杀死,故引入si没有进一步提升治疗效果)。
86.实例6:多种硅矿增强阿霉素制剂的制备及其对于黑色素瘤细胞活性的影响。
87.广谱抗肿瘤药制剂的配置方法如下:将阿霉素以1mm的固体/液体比率溶解于pbs中,按一定的比例加入肿瘤培养基中,配置成浓度为0-20μm的广谱抗肿瘤药物制剂。
88.硅矿制剂的配置方法如下:根据iso/en 10993-12,制备了一系列镁黄长石/锌黄长石/铜硅钙石粉体的稀释离子提取物。首先,将镁黄长石/锌黄长石/铜硅钙石粉体加入到无血清肿瘤细胞培养液中,在200mg/ml的固体/液体比率下,在37℃孵育24小时,将混合物以4000rpm离心10分钟,然后上清液通过过滤膜(millipore,0.22μm)灭菌并收集以获得储备溶液。随后,用黑色素瘤细胞培养液稀释储备溶液以制备合适的离子提取物。
89.多种硅矿增强广谱抗肿瘤药制剂的配置方法如下:按照预设比例将上述几种制剂混合,其中阿霉素的浓度为0-20μm,硅矿的浓度为0.25-120ppm(μg/ml)。
90.取上述配置好的溶液,按照比例加入胎牛血清,生长补充剂与青霉素和链霉素。将黑色素瘤细胞接种于96孔培养板中,初始密度为每孔1
×
103个细胞,培养24小时后,将细胞培养基更换为配置好的硅酸钙/阿霉素制剂。再次培养48小时后,通过cck-8(细胞计数试剂盒-8)在酶标仪450nm下测量所有样品的吸光度来评估黑色素瘤细胞的活性。
91.参见图7中所示,根据cck8的数据可以发现,当不加阿霉素时,细胞的存活率不受到任一种类硅矿浓度的影响,因此本实施例中选用的硅矿浓度是一个安全的浓度。在不添加硅矿的时候,阿霉素等于5μm、10μm的时候对黑色素瘤细胞均有抑制功能,但只有20%~30%的抑制率,而随着不同种类硅矿浓度的增加,硅矿释放si和金属离子与阿霉素结合,让黑色素瘤细胞的存活率不断降低。当si浓度等于cs/1/2,阿霉素的浓度等于10μm时,镁黄长石组的75%肿瘤细胞抑制率,参见图8中a部分所示;当si浓度等于cs/1/8,阿霉素的浓度等于10μm时,铜硅钙石组肿瘤细胞抑制率等于85%,参见图8中c部分所示。因此铜硅钙石中的铜离子对肿瘤细胞的抑制作用要优于镁黄长石中的镁离子。当镁黄长石和锌黄长石浓度等于cs/1/2,铜硅钙石浓度等于cs/1/8时,不同硅矿的三组肿瘤细胞抑制率均达到了70%~80%,可以发现不同种类的硅矿结合阿霉素也会增强药物活性。
92.实例7:si/bor联合治疗对在小鼠体内多发性骨髓瘤(arp-1)的功效。
93.建立多发性骨髓瘤异种移植模型:将6周大的nod-scid小鼠皮下注射arp-1(5
×
106)细胞至左右两侧,以建立多发性骨髓瘤异种移植模型。7天后,当肿块形成时,将小鼠随机分为四组(每组n=6),包括载体对照组、si组、bor组以及si和bor组合的组。bor(1mg/kg)每三天腹腔注射一次,连续2周,将si(200μl)瘤周皮下注射,每天一次,持续2周。每两天用卡尺监测肿瘤大小。
94.肿瘤组织切片分析:肿瘤组织取自荷瘤nod/scid小鼠,肿瘤块在4%多聚甲醛中固定,然后在切片前包埋在石蜡中。最后,进行免疫组织化学染色以分析裂解的caspase3。
95.如图8所示,与载体对照组、si组和bor组相比,联合治疗导致肿瘤负担更明显的减少,表现为肿瘤体积和肿瘤重量的减少图8中a、b和c部分所示参见。此外,在接受联合治疗的小鼠中未观察到显著的毒性,因为在治疗期间小鼠的体重没有显著下降,参见图8中d部分所示。接下来,本实施例中使用免疫组织化学来验证裂解的caspase-3的表达。结果表明硅酸钙和bor联合治疗增加了裂解的caspase-3的表现,参见图8中e部分所示。综上,本实施例中的实验表明si/bor组合疗法在体内非常有效。
96.综上可知,本技术实施例提供一种抗肿瘤药物制剂及其制备方法和应用。该抗肿瘤药物制剂为硅矿抗肿瘤药物制剂,该抗肿瘤药物制剂包括:含有一种或者多种的硅离子的硅酸盐矿物以及至少一种广谱抗肿瘤药物;其中,硅离子的浓度范围为0.25~120ppm。该抗肿瘤药物制剂能够通过增强广谱抗肿瘤药物的治疗效果来抑制肿瘤细胞的活性,并且能够有效减小实体肿瘤的大小,且该种抗肿瘤药物制剂能够在增强化疗药物的治疗效果的同时减少药物的使用量,在一定程度上减轻患者的负担。
97.需要说明的是,诸如“第一”和“第二”等之类的关系术语仅仅用来将一个实体或者操作与另一个实体或操作区分开来,而不一定要求或者暗示这些实体或操作之间存在任何这种实际的关系或者顺序。而且,术语“包括”、“包含”或者其任何其他变体意在涵盖非排他性的包含,从而使得包括一系列要素的物品或者设备不仅包括那些要素,而且还包括没有明确列出的其他要素,或者是还包括为这种过程、方法、物品或者设备所固有的要素。在没有更多限制的情况下,由语句“包括一个
……”
限定的要素,并不排除在包括所述要素的过程、方法、物品或者设备中还存在另外的相同要素。
98.以上所述实施例仅用以说明本技术的技术方案,而非对其限制;尽管参照前述实施例对本技术进行了详细的说明,本领域的普通技术人员应当理解:其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分技术特征进行等同替换;而这些修改或者替换,并不使相应技术方案的本质脱离本技术各实施例技术方案的精神和范围,均应包含在本技术的保护范围之内。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。