1.本发明涉及生物医药技术领域,具体涉及一种靶向纳米分子探针及其在制备肿瘤治疗药物中的应用。
背景技术:
2.胰腺癌是属于消化系统的恶性肿瘤,具有发病隐匿、生存率低等特点,大多数患者确诊时已经处于进展期。目前,对胰腺癌的治疗常常以手术治疗、放疗、化疗、靶向药物治疗和免疫治疗为主。胰腺癌组织纤维成分丰厚、血管成分功能失调,缺乏组织靶向性及胰腺癌细胞固有的化疗抵抗特性,单一的治疗手段难以有效的实现胰腺癌细胞的杀伤。使得吉西他滨(gemcitabine,gem)、奥沙利铂(oxaliplatin)等胰腺癌一线治疗药物的临床效果不尽如人意。而现有的联合治疗手段如吉西他滨联合白紫杉醇,奥沙利铂、伊立替康联合5-氟尿嘧啶等因为严重的副作用而不能被患者所耐受。
3.免疫治疗作为最有可能治愈肿瘤的手段,得到临床和基础研究的广泛关注,在黑色素瘤和乳腺癌的治疗中显示出广阔的应用前景。然而,因胰腺癌细胞表面表达一系列免疫抑制分子(如lgals9),致使胰腺癌免疫治疗的效果不佳。因此,急需形成一种具有高靶向性、低毒性的新型治疗手段。
技术实现要素:
4.本发明针对现有技术中存在的缺陷,改善目前常用治疗方案对胰腺癌治疗效果上的不足,提供一种靶向纳米分子探针及其在制备肿瘤治疗药物中的应用,本发明提供的靶向纳米分子探针具有荧光标记的免疫检查点受体,可以通过π-π作用结合装载药物,增强药物在胰腺癌组织靶向聚集。
5.本发明的上述目的是通过以下技术方案实现:在某一具体实施例中,本发明提供了一种靶向纳米分子探针,所述探针包括过表达免疫检查点对应受体的细胞膜纳米囊泡,以及聚乙二醇(peg)修饰的黑色素纳米颗粒;所述的peg带有羧基,所述的细胞膜纳米囊泡表面标记有mcherry。
6.所述的免疫检查点对应受体为pd1、lag3、tigit、cd38、cd39或tim3。
7.所述黑色素纳米颗粒包载有吉西他滨或奥沙利铂。
8.黑色素纳米颗粒作为磁共振t1加权成像的增强造影剂,提高肿瘤组织监测的敏感性和治疗效果。所述的peg为硫辛酸-聚乙二醇-羧基,peg修饰的黑色素纳米颗粒具有较高的生物安全性、低免疫原性以及延长纳米载体的半衰期。
9.本发明还提供了一种靶向纳米分子探针的制备方法,所述方法包括:(1)将荧光标记的免疫检查点对应受体质粒和慢病毒包装质粒转染细胞系,裂解、挤压过滤得到细胞膜纳米囊泡;(2)将氨水、去离子水、无水乙醇混合均匀,在搅拌条件下加入盐酸多巴胺水溶液,反应后离心、洗涤得到黑色素纳米球,将其与聚乙二醇水溶液混合,加入氨水后摇床反应,
洗涤后得到聚乙二醇修饰的黑色素纳米球(mns-peg);(3)将步骤(1)获得的细胞膜纳米囊泡和步骤(2)获得的mns-peg混合后利用电击法获得靶向纳米分子探针。
10.进一步地,步骤(1)中所述的免疫检查点对应受体质粒和慢病毒包装质粒的用量比为1:1,所述的慢病毒包装质粒为pspax2和pmd2g。
11.步骤(1)中所述的免疫检查点对应受体为pd1、lag3、tigit、cd38、cd39或tim3。
12.步骤(1)中所述的细胞系为hek293t、panc02或kpc细胞。
13.步骤(2)中所述的mns-peg可包载治疗肿瘤的药物,所述的药物为吉西他滨或奥沙利铂。
14.步骤(3)中所述的电极法为300 mv电击两次,冰上复苏30 min,12000 g,4 ℃离心10分钟。
15.本发明还提供了上述靶向纳米分子探针在制备胰腺癌治疗药物中的应用。
16.进一步地,所述的靶向纳米分子探针包载有吉西他滨或奥沙利铂。
17.与现有技术相比,本发明的有益效果是:本发明首次合成过表达有免疫检查点对应受体且带有mcherry标记的细胞膜纳米囊泡,同时联合黑色素包载治疗药物制备靶向纳米分子探针。本发明mcherry标记的过表达免疫检查点受体能够通过识别肿瘤表面的lgals9,更好的将化疗药物递送至肿瘤组织,实现肿瘤细胞聚集及有效杀伤,改善胰腺癌免疫治疗缺陷。具有减少给药次数、提高疗效、改善耐受性等优点,增加了药物在体内的保留时间、提高半衰期、延长吸收时间以及提高肿瘤靶向性。同时利用磁共振成像实现胰腺癌诊断和联合治疗的双重效应。在肿瘤药物靶向递送、疗效实时、动态监测中具有巨大的优势。
18.本发明以tim3细胞膜纳米囊泡为例,将其与黑色素-吉西他滨联用制备的靶向纳米分子探针。经过实施例证明,制备的纳米探针经过血液循环到达肿瘤处,能够识别肿瘤细胞表面的lgals9并与其结合,实现在肿瘤处的富集,破坏tim3/lgals9免疫检查点抑制轴,避免杀伤性cd8
t细胞的耗竭,实现对胰腺癌精准靶向免疫治疗的目的。同时,可利用黑色素纳米颗粒进行磁共振t1加权成像,检测胰腺癌的治疗效果,从而实现诊疗胰腺癌和激活细胞毒性t细胞的双重功能。
附图说明
19.图1是hek293t细胞系的激光共聚焦对比图;图2是mcherry-tim3在细胞膜表达的效率验证图;图3是mns包载吉西他滨的包封率验证图;图中,左图是吉西他滨的标准曲线;右图是根据标准曲线得到的包封率;图4是囊泡的扫描电镜对比图;图5是动态光散射分析对比图;图6是mns@tim3 nvs、tim3 nvs及mns的zeta电位对比图;图7是tim3 nvs组在胰腺癌panc02细胞中的定位图;图8是6 h后各组模型小鼠中囊泡在胰腺癌中的聚集定位图;图9是各组小鼠的胰腺癌磁共振成像图;
图10是各组小鼠的肿瘤组织图像对比图;图11是各组小鼠的肿瘤体积变化图;图12是各组小鼠的肿瘤重量图;图13是各组小鼠的肿瘤组织中ki-67的表达情况图;图14是各组小鼠脾脏及肿瘤中cd8
t细胞ifnγ的表达图;图中,a是脾脏中cd8
t细胞中ifng表达情况,b是肿瘤中cd8
t细胞中ifng表达情况。
具体实施方式
20.本发明公开了一种靶向纳米分子探针及其在制备肿瘤治疗药物中的应用。本领域技术人员可以借鉴本文内容,适当改进工艺参数实现。特别需要指出的是,所有类似的替换和改动对本领域技术人员来说是显而易见的,它们都被视为包括在本发明。本发明的方法及应用已经通过较佳实施例进行了描述,相关人员明显能在不脱离本发明内容、精神和范围内对本文所述的方法和应用进行改动或适当变更与组合,来实现和应用本发明技术。
21.本领域技术人员清楚,在下文中,如果未特别说明,本发明所用材料和操作方法是本领域公知的,所使用的实验方法均为常规方法,所用材料、试剂等均可从化学试剂公司购买。本发明所涉及的mcherry-tim3质粒、pspax2质粒和pmd2g质粒均购买于广州基旦生物科技有限公司。
22.实施例1:细胞膜纳米囊泡(tim3 nvs)的构建将免疫检查点对应受体质粒mcherry-tim3质粒和慢病毒包装质粒pspax2 和 pmd2g以2:1:1的比例混合后转染hek293t细胞,72h后制备得到慢病毒悬液感染hek293t细胞,2μg/ml嘌呤霉素筛选72h,构建稳定表达mcherry-tim3的hek293t细胞系。
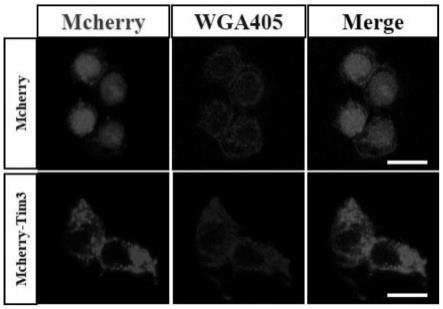
23.对构建的表达mcherry-tim3的hek293t细胞系进行表征:将构建的过表达mcherry-tim3的hek293t细胞铺板于有圆玻片的12孔板中培养过夜,使用5μg/ml浓度的细胞膜染料wga405避光染色30 min,pbs清洗2遍后加入4 %多聚甲醛固定10min,通过激光共聚焦观察荧光情况;同时以只表达mcherry的hek293t细胞作为对照。图1是hek 293t细胞系的激光共聚焦对比图;如图1所示,过表达mcherry-tim3的hek293t细胞系的细胞膜表面带有荧光的tim3,而对照组只表达mcherry的hek293t整个细胞呈现荧光。
24.将过表达mcherry-tim3的hek293t细胞收集后使用hm buffer裂解10分钟,研磨棒冰上研磨使细胞彻底破裂。随后5000 g/min,4℃离心10分钟,弃去下层的细胞核及胞质蛋白,收集上清液12000 g/min,4℃离心10分钟,将下层沉淀物(即细胞膜)用pbs重悬并合,依次挤压过0.45μm,0.22μm和0.1μm滤网,得到细胞膜纳米囊泡(tim3 nvs)。
25.图2是mcherry-tim3在细胞膜表达的效率验证图;图中,atpase为细胞膜标志蛋白,β-actin为胞质标志蛋白。如图2所示,在hek293t细胞的细胞膜上可以稳定表达mcherry-tim3。
26.实施例2:黑色素-吉西他滨(mns-gem)的合成(1)黑色素纳米球的合成将3.6 ml 氨水、54 ml 去离子水、24 ml无水乙醇混合均匀,30℃,500 rpm搅拌30 min。在搅拌条件下加入6 ml 50 mg/ml的盐酸多巴胺水溶液;恒温反应18 h,经过9000 rpm离心15 min,并用去离子水洗涤三次后,收集得到黑色素纳米球,将其分散至30 ml去离子
水中得到浓度为 2 mg/ml的黑色素纳米球水溶液,4℃保存备用。
27.(2)聚乙二醇的修饰将1 ml 5 mg/ml 的聚乙二醇(peg)水溶液与 5 ml步骤(1)得到的黑色素纳米球水溶液混合,加入 0.5 ml 氨水,室温摇床反应 6 h。用水洗涤数3次,得到聚乙二醇修饰的黑色素纳米球(mns-peg),分散于5 ml水。
28.(3)装载吉西他滨1 mg 吉西他滨(gem)加入至1 ml 步骤(2)制备的mns-peg水溶液中震荡混匀后,避光摇床 100 rpm 反应 12 h,9000 rpm 离心 15 min 得到mns包载吉西他滨(记为mns-gem)。用去离子水洗涤 2 次去除未被装载的 gem。随后以吉西他滨为标准品,检测不同浓度吉西他滨的吸光度,通过分光光度计检测在268 nm波峰的数值,得到标准曲线y=32.737x 0.3245,r2=0.9993。图3是mns包载吉西他滨的包封率验证图;图中,左图是吉西他滨的标准曲线;右图是根据标准曲线得到的包封率;如图3所示,得到mns包载吉西他滨的包封率为18.025
ꢀ±ꢀ
1.065 %。
29.实施例3:tim3 nvs包载黑色素将1 mg mns-peg 与1 mg实施例1制备的细胞膜纳米囊泡(tim3 nvs)混合均匀后,300 mv电击两次,冰上复苏30 min,12000 g,4 ℃离心10分钟,弃去上清,重新加入pbs后,-80 ℃保存备用,制备得到浓度为1mg/ml 的mns@tim3-nvs。采用相同方法用tim3 nvs装载mns-gem制备,区别在于用等量的mns-gem替换mns-peg,制备得到gem-mns@tim3-nvs。
30.测量所制备的获得mns@tim3-nvs的电势和扫描电镜图,并以tim3 nvs、mns作为对照。图4是囊泡的扫描电镜对比图;如图4可见,tim3 nvs、mns及mns@tim3 nvs均呈现100-120 nm左右的圆球状,可以看到tim3 nvs具有明显的膜结构,黑色素mns仅呈现球形结构,不能看到细胞膜,而mns@tim3-nvs可以看到有mns包裹在细胞膜里面,说明制备的细胞膜纳米囊泡tim3 nvs可以实现mns的包载。
31.利用动态光散射法分别测量mns@tim3-nvs、tim3 nvs、mns的粒径大小。图5是动态光散射分析对比图;由图5可见,tim3 nvs、mns及mns@tim3-nvs呈现均匀的正态分布,粒径皆约为120 nm左右,此结果与透射电镜的结果一致。图6是mns@tim3-nvs、tim3 nvs及mns的zeta电位对比图;由图6可见,tim3 nvs、mns及mns@tim3-nvs的表面电势分别为-14.2
±
2.95 mv、-25.9
±
4.15 mv及-35.7
±
4.02 mv。
32.实施例4:tim3 nvs在胰腺癌细胞及胰腺癌皮下模型中的定位情况将实施例1制备的表达tim3的细胞膜纳米囊泡tim3 nvs与胰腺癌panc02细胞共孵育30分钟,利用激光共聚焦观察tim3 nvs在panc02细胞中的定位情况。图7是tim3 nvs组在胰腺癌panc02细胞中的定位图;如图7所示,细胞膜纳米囊泡tim3 nvs能定位在panc02细胞的表面。
33.分别将过表达tim3的hek293t细胞的细胞膜纳米囊泡(tim3 nvs)与只表达mcherry的hek293t细胞的囊泡(mcherry nvs)进行dio细胞膜染色,dio的浓度为30μm,取1 ml的dio染液分别与上述各囊泡(100μg)混合,37℃孵育30 min,12000 rpm,4 ℃离心10 min,弃去上清,加入200μl pbs重悬后备用,分别记为tim3 nvs组和mcherry nvs组,同时设置pbs组作为对照。在c57b/l6小鼠皮下构建胰腺癌模型小鼠,分别在每组老鼠尾静脉注射200μl备好的pbs悬液,在6 h、24 h时,用小动物成像仪在700 nm的波长处观察囊泡在小鼠
皮下肿瘤处的聚集情况。图8是6 h后各组模型小鼠中囊泡在胰腺癌中的聚集定位图;图中,圆圈内的方型区域代表肿瘤部位,如图8所示,与其他组相比,tim3 nvs组可以实现在肿瘤部位的靶向聚集,其聚集程度高,聚集量多。
34.实施例5:纳米探针的靶向聚集将100μg的细胞膜纳米囊泡tim3 nvs与100μg聚乙二醇修饰的黑色素纳米球(mns-peg)通过电穿孔仪电击连接,加入200μl pbs重悬后得到200μl的pbs悬液,记为mns@tim3-nvs。基于mns具有磁共振成像功能,通过磁共振观察制备的mns@tim3 nvs在动物模型中的靶向情况。以mns组为对照;分别在胰腺癌模型小鼠尾静脉注射200μl备好的pbs悬液,并在0 h、6 h、12 h进行磁共振成像,所用序列为ti加权像。图9是各组小鼠的胰腺癌磁共振成像图;图中,箭头代表肿瘤部位,颜色越白显示黑色素纳米颗粒探针聚集越多。如图9所示,负载有黑色素的细胞膜纳米囊泡mns@tim3-nvs具有很好的靶向性,将黑色素靶靶向到肿瘤的部位。
35.实施例6 :tim3纳米囊泡包载黑色素吉西他滨对胰腺癌的治疗效果本实施例中分别以pbs组、mcherry nvs组、tim3 nvs组、mns组、gem组、gem-mns组、gem-mns@ mcherry nvs组和gem-mns@tim3-nvs组为治疗药物,对胰腺癌小鼠模型注射治疗,分析纳米囊泡包载的黑色素吉西他滨对胰腺癌的治疗效果,每组三个平行,动物实验在江苏大学动物实验伦理委员会批准下进行。具体为将2
×
106个panc02小鼠胰腺癌细胞注入c57bl/6小鼠皮下,待肿瘤大小长至50 mm3时,开始尾静脉注射药物治疗,每2天通过尾静脉注射一次,并且记录小鼠的体重和存活情况;到第14天时,将所有小鼠处死,收取肿瘤组织和脾脏组织,拍摄肿瘤照片。
36.图10是各组小鼠的肿瘤组织图像对比图;图11是各组小鼠的肿瘤体积变化图;图12是各组小鼠的肿瘤重量图;由图10~12可见,gem-mns@tim3-nvs组在肿瘤形态大小、体积变化及肿瘤重量上都小于其他的组别,可见,纳米囊泡包载的黑色素吉西他滨起到良好的抑制胰腺癌生长的治疗效果。
37.将肿瘤组织石蜡包埋、切片,并通过免疫组织染色分析ki-67的表达分析肿瘤的增值情况。图13是各组小鼠的肿瘤组织中ki-67的表达情况图;由图13所示,gem-mns@tim3-nvs组中的ki-67表达明显低于其他组别,具有很好的抑制肿瘤增殖的性能。
38.为了观察gem-mns@tim3-nvs是否具有增强cd8
细胞功能,本实施例对cd8
t细胞活化的指标ifnγ进行检测。分别将收取的肿瘤组织和脾脏组织充分研磨并通过100目筛网过滤器过滤,获得单细胞悬液,与apc-cd3、fitc-cd8、percp-ifnγ流式抗体孵育后检测cd8
t细胞中ifnγ表达水平。图14是各组小鼠脾脏及肿瘤中cd8
t细胞ifnγ的表达图;图中,a是脾脏中cd8
t细胞中ifng表达情况,b是肿瘤中cd8
t细胞中ifng表达情况;如图14所示,tim3 nvs及gem-mns@tim3-nvs组的脾脏及肿瘤中的cd8
t细胞中的ifnγ皆高于其他组别,可见,tim3囊泡可以增强cd8
细胞功能,避免杀伤性cd8
t细胞的耗竭,增加吉西他滨在肿瘤组织聚集,增强对胰腺癌的杀伤效果。
39.综合以上结果,以tim3细胞膜纳米囊泡包载黑色素-吉西他滨为例证实本发明提供的靶向纳米分子探针对胰腺癌具有很好的诊疗效果。
40.以上显示和描述了本发明的基本原理、主要特征以及本发明的优点。本行业的技术人员应该了解,本发明不受上述实施例的限制,上述实施例和说明书中描述的只是说明
本发明的原理,在不脱离本发明精神和范围的前提下,本发明还会有各种变化和改进,这些变化和改进都落入要求保护的本发明范围内。本发明要求保护范围由所附的权利要求书及其等效物界定。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。