一种25-羟基维生素d的检测方法及试剂盒
技术领域
1.本发明属于25-羟基维生素d检测相关技术领域,具体涉及一种25-羟基维生素d的检测方法及试剂盒。
背景技术:
2.维生素d是人体不可缺少的维生素,它有以下生理功能:1提高肌体对钙、磷的吸收;2、促进生长和骨骼钙化,促进牙齿健全;3、通过肠壁增加磷的吸收,并通过肾小管增加磷的再吸收;4、防止氨基酸通过肾脏损失。人体缺乏维生素d会引起佝偻病、手足抽搐和软骨病。长期摄入过多的维生素d(5000iu/日),将引起高血钙和高尿钙。
3.维生素d在肝脏和肾脏转化成为有生物活性的25-羟基维生素d(25-ohd)和25-二羟基维生素d。由于25-羟基维生素d是人体内维生素d的主要储存形式。因此通过检测25-羟基维生素d(包括25-羟基维生素d2与25-羟基维生素d3)可以评估人体维生素d水平,进而评价钙吸收水平、协助临床疾病的诊断和监测并确定钙和维生素d的补充方案。
4.25-ohd的主要理化检测方法有高效液相色谱法(high performance liquid chromatography,hplc)和液相色谱质谱法(liquid chromatography mass spectrometry,lc-ms)。hplc技术具有良好的精密度和准确度,但由于其操作复杂,反应时间长,所需样本量大,故不适于临床应用。lc-ms是在hplc基础上发展起来的一项新的检测技术,现为色谱法中最为常用的25-ohd检测方法。lc-ms技术可完全满足临床检测方法要求的准确性,灵敏度,特异性,该方法已经被美国国家疾控中心采用的参考方法,被认为是检测25-ohd的金标准。虽然lc-ms具有以上优点,但同时也存在着样品前处理繁琐,技术操作复杂,需要专业人员,仪器昂贵,检测周期长,自动化程度不高等缺点,限制着lc-ms在临床检测中的应用。
5.因此,当前亟需设计一种操作简便、特异性高、灵敏度好的用于检测人血清中25-羟基维生素d的方法。
技术实现要素:
6.本发明的目的在于提供一种25-羟基维生素d的检测方法及试剂盒,其采用化学发光竞争法,操作简便、特异性高、灵敏度好,能够满足现有的检测需求。
7.为实现上述目的,本发明提供如下技术方案。
8.一种25-羟基维生素d的检测方法,其特征在于:所述检测方法包括以下步骤:
9.步骤1、进行第一次孵育:加入30μl被测样本和150μl孵育缓冲液到化学发光微孔板中一起孵育,使与维生素d结合蛋白结合的25-羟基维生素d转换成游离态,并与化学发光微孔板中的固相抗体结合;
10.步骤2、进行第一次清洗:吸取350μl清洗液加入到化学发光微孔板中,清洗4次,洗去未结合在固相上的物质;
11.步骤3、进行第二次孵育:加入100μl的酶结合物溶液一起孵育,与化学发光微孔板上尚未结合的25-羟基维生素d抗体结合;
12.步骤4、进行第二次清洗:吸取350μl清洗液加入到化学发光微孔板中,清洗4次,洗去未结合在固相上的物质;
13.步骤5、进行读数,加入化学发光底物a、化学发光底物b,酶催化底物发光,通过光电倍增器测量发光强度;
14.步骤6、利用已知浓度的定标品绘制发光强度标准曲线,根据步骤5得到的发光强度对照所述发光强度标准曲线,计算得出待测样本中的25-羟基维生素d含量。
15.进一步的,所述孵育缓冲液的配置方式为:取9.55ml卡松、38.2g牛血清白蛋白、133.64ml丙二醇加入1l水中,调ph为7.0进行配制。
16.进一步的,所述化学发光微孔板为包被有25-羟基维生素d抗体。
17.进一步的,所述25-羟基维生素d抗体的浓度为3μg/ml。
18.进一步的,所述酶结合物溶液的配置方式为:取60.55g蔗糖、6.05g 2-氯乙酰胺、1.21g牛血清白蛋白、0.12g铁氰化钾、1.21ml proclin300,调ph为7.0进行配置,再加入0.25%25-羟基维生素d-hrp偶联物。
19.进一步的,所述化学发光底物a为含有0.4%鲁米诺,ph9.0的水溶液;所述化学发光底物b为含有0.06%四硼酸钠,ph5.0的水溶液;所述清洗液为含1%吐温20和0.1%proclin300的0.05m、ph值为7.5的tris-hcl溶液。
20.进一步的,所述定标品的配置方式为:将25-羟基维生素d抗原添加至马血清中,配置成浓度约为0ng/ml、7.5ng/ml、15ng/ml、30ng/ml、60ng/ml和120ng/ml的定标品。
21.进一步的,所述步骤1和步骤3中的孵育时间均为15分钟。
22.基于上述检测方法,本发明还提供了一种25-羟基维生素d的检测试剂盒,其特征在于:所述试剂盒包括化学发光微孔板、孵育缓冲液、酶结合物溶液、定标品、化学发光底物a、化学发光底物b和清洗液。
23.进一步的,所述化学发光底物a、化学发光底物b和清洗液均为独立包装。
24.与现有技术相比,本发明具备以下有益效果:
25.1、本发明检测样品中25-羟基维生素d的免疫学方法为化学发光竞争法。首先用纯化的25-羟基维生素d抗体包被化学发光微孔板制成固相抗体,然后往化学发光微孔板的微孔中依次加入样本与孵育缓冲液,使与维生素d结合蛋白结合的25-羟基维生素d转换成游离态,游离态的25-羟基维生素d与微孔中的固相抗体结合;洗涤除去未结合物质后加入浓度一定的hrp标记过的25-羟基维生素d偶联物,与微孔中未与样本中25-羟基维生素d结合的抗体结合;洗涤除去未结合物质后加入化学发光底物a和b。化学发光底物在hrp酶的催化下发光,然后用化学发光免疫分析仪读取相对发光强度(rlu),最后通过校准曲线计算样品中25-羟基维生素d的浓度,实现了检测样品中25-羟基维生素d含量的功能。
26.2、本发明采用将样本与释放剂同时加入微孔板中的方法,使样本、释放剂与微孔板中的抗体同时孵育,以便于样本中的25-羟基维生素d释放出来后直接与固相抗体结合,省去了样本单独处理的过程,节约了时间,操作简便、特异性高、灵敏度好,能够满足现有的检测需求。
附图说明
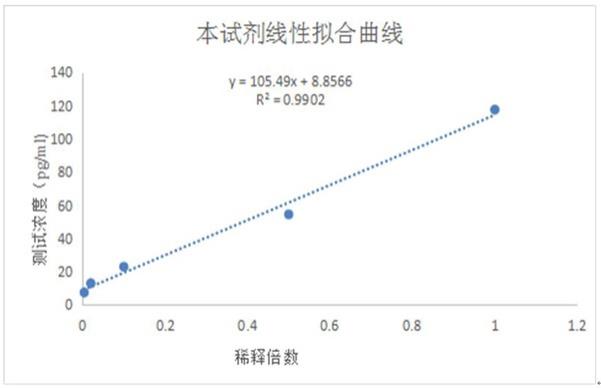
27.图1为计算本试剂的线性拟合曲线。
28.图2为计算对比试剂的线性拟合曲线。
具体实施方式
29.实施例:基于本发明的检测方法,制作试剂盒进行以下各种性能指标的检测。将本试剂盒作为实验组,对比试剂为市售试剂盒。
30.性能指标1、最低检测限:
31.用零浓度稀释液作为样本进行检测,重复测定20次,计算其rlu值(相对发光值)平均值(m)和标准差(sd),得出m 2sd。利用剂量-反应曲线计算出(m 2sd)对应的浓度值为最低检测限。
32.表1最低检测限结果
33.[0034][0035]
通过检测数据可知,本试剂盒具有较好的最低检测线且设定的最低检测限6ng/ml合理。
[0036]
性能指标2、准确度:
[0037]
各重复检测3次,将每次检测结果记为(mi),分别计算每次检测结果的相对偏差(bi)。如果3次结果的相对偏差都在
±
10%范围内,即判定为符合要求;如果大于等于2次结果的相对偏差不在
±
10%范围内,即判定为不符合要求;如果有1次结果的相对偏差不在
±
10%范围内,则应重新连续测试20次,并分别计算相对偏差,如果大于等于19次结果的相对
偏差在
±
10%范围内,即判定为符合要求。
[0038]
表2本试剂准确度测试
[0039][0040]
表3对比试剂准确度测试
[0041][0042]
由结果可知,本试剂盒测定质控品的结果更接近于标识浓度,证明本试剂的相对偏差均小于对比试剂盒,因此本试剂的准确度更好,更能准确测定出样本中待测物的真实浓度。
[0043]
性能指标3、精密度:
[0044]
以本试剂盒对比试剂各重复检测10次,计算各参考品10次测量浓度结果的平均值m和标准差sd,根据公式cv=sd/m
×
100%,计算变异系数。
[0045]
表4精密度测试
[0046][0047]
本试剂盒测定控品1和质控品2的cv分别为2.80%和5.61%,均小于对比试剂盒的5.90%和7.05%,证明本试剂的精密度更高,测定样本的重复性更好。性能指标4、线性范围:
[0048]
取接近线性范围上限的高值样本按一定比例稀释为5种浓度,其中低值浓度的样本须接近线性范围的下限。对每一浓度的样本均重复检测3次,计算其平均值,将结果平均值和稀释比例用最小二乘法进行直线拟合,并计算线性相关系数r,r不小于0.99。
[0049]
表5线性范围测试
[0050][0051]
如图1和图2所示,试剂盒获得的拟合直线线性相关系数r2大于0.990,并且高于对比试剂的0.98,因此本试剂盒线满足预期设定的线性范围。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。