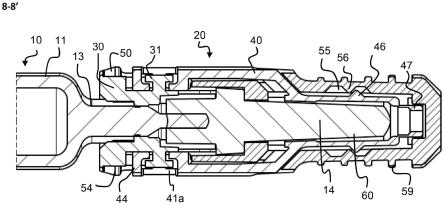
用于tg2相关疾病的吡啶酮衍生物的全身性制剂
技术领域
1.本发明涉及用于预防和/或治疗tg2相关疾病诸如纤维化、特别是肾病、纤维化肝病(包括非酒精性脂肪肝疾病(nafld)和非酒精性脂肪性肝炎(nash))、特发性肺纤维化(ipf)和囊性纤维化的全身性制剂、特别是口服制剂,及其在预防和/或治疗纤维化、特别是肾病、纤维化肝病(包括nafld和nash)、特发性肺纤维化和囊性纤维化中的用途。
2.进一步,本技术也涉及(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯作为肝保护剂(即作为肝保护性药剂)的用途。
3.另外,本发明涉及包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯的药物组合物,其用作肝保护剂和用于保护肝脏免于肝毒性,改善肝功能和/或修复肝损伤,或用于预防或治疗肝疾病或肝障碍,如通过降低肝酶的血清水平所证明的。
背景技术:
4.脂肪性肝炎是脂肪肝疾病的一种类型,其特征在于肝脏炎症并同时在肝细胞中积累脂肪。仅脂肪在肝脏中的沉积被称为脂肪变性,并且这些一起构成脂肪肝变化。
5.脂肪肝疾病有两种主要类型:酒精相关性脂肪肝疾病和非酒精性脂肪肝疾病(nafld)。nafld的危险因素包括糖尿病、肥胖和代谢综合征。当存在炎症时,它被称为酒精性脂肪性肝炎和非酒精性脂肪性肝炎(nash)。任何一种未经治疗的脂肪性肝炎都可能造成发展为纤维化和随后的肝硬化,并且现在认为nash是无法解释的肝硬化的常见原因。
6.糖尿病性肾病是作为糖尿病(dm)的结果而发生的肾脏疾病。糖尿病和2型糖尿病(t2dm)是终末期肾病(esrd)的最常见原因。糖尿病性肾病通常导致肾功能的慢性和进行性退化,达到患者必须接受透析或接受移植才能存活的程度。肾小球的细微形态变化的初始阶段之后是微白蛋白尿。这与适度升高的血压和心血管疾病的发病率增加相关。随后尿蛋白排泄和确定的肾小球滤过率持续增加。糖尿病性肾病具有许多可能的潜在病理生理学原因,包括代谢、蛋白糖基化、血液动力学、改变的肾小球流量/压力、高血压的发展和细胞因子产生;所有这些都与细胞外基质的发展和血管渗透性增加相关,从而导致肾小球损伤和蛋白尿。
7.huang等人(kidney international 2009,76,383-394)将二肽衍生物(ntu281)描述为不可逆的tg2抑制剂。所述二肽衍生物的缺点之一是,必须通过植入式渗透泵将二肽衍生物局部应用到肾脏中。基于该教导,无法想象根据johnson的二肽衍生物的全身性制剂,因为tg2在几乎所有细胞类型和细胞区室中普遍表达,存在于细胞表面上并分泌到细胞外基质中,并且存在于各种器官中,因此通过应用tg2抑制剂,最可能出现不需要的脱靶效应。
8.huang等人描述了一种植入式渗透泵,其含有在作为媒介物的磷酸盐缓冲盐水中的局部制剂ntu281(药物)(50mmol/l)。由此,渗透泵必须通过与麻醉相关的外科手术干预来植入。尽管麻醉在医学领域中是常用的,但并发症的显著风险总是相关的,特别是在对儿
童和老年人等弱势群体进行治疗时。将渗透泵植入患者体内会给患者带来额外的风险,因为像泵这样的电子设备在生理条件下是敏感的并且可能例如爆裂,并因此并不总是可靠的。此外,必须维护泵,这会给患者带来额外的痛苦。此外,由于消除了外科手术干预的障碍,可以显著提高患者顺应性。含有局部制剂的植入式渗透泵不可用于人体。
9.lauzier等人(arthritis research therapy 2012,14,r159)描述了胱胺或rna衍生物通过胱胺(转谷氨酰胺酶的一种竞争性抑制剂)对tg2的抑制对关节炎中的侵袭性伪足形成和软骨破坏的影响。胱胺是具有两个氨基部分的二硫化物。
10.luciani等人(nature cell biology 2010,12,863-875)描述了胱胺和sirna对囊性纤维化中的肺部炎症的影响。
11.luo等人(journal of the american heart association,2016,1-12)公开了1,3-二甲基-2-[(2-氧代丙基)-硫基]-咪唑鎓(r283)或卤代-二氢异噁唑衍生物转谷氨酰胺酶抑制剂(kcc009)对囊性纤维化中的炎症的影响。
[0012]
olsen等人(american journal of respiratory cell and molecular biology 2014,50,737-747)公开了两种不同的小亲电子化合物2-氰基-3,12-二氧代齐墩果-1,9-二烯-28-酸(dioxoolean-1,9-dien-28-oic acid)和15-脱氧δ-12,14-前列腺素j2对肺纤维化的影响。
[0013]
sanchez-lara等人(veterinary pathology 2015,第52(3)卷513-523)描述了1,3-二甲基-2[(氧代丙基)硫基]-咪唑鎓氯化物(d003,zedira)(非选择性的tg抑制剂ntu281)或单克隆抗体bb7对慢性肾脏疾病的影响。
[0014]
在生理条件下,特别是在全身疗法(systemic therapy,或译为系统疗法)的情况下,建立药物的适当生物利用度仍然是药学领域中的一个重大问题。
[0015]
本发明的目的是提供用于治疗糖尿病性肾病和/或非酒精性脂肪性肝炎的方式,其表现出生物利用度和高抗纤维化作用以及低副作用。
[0016]
本发明的另一个目的是提供一种化合物,其用于用作肝保护剂(即肝保护性药剂),和用于保护肝脏免于肝毒性,改善肝功能,保护/修复肝损伤,和/或预防或治疗肝脏疾病。
[0017]
独立权利要求的教导解决了本发明的目的。根据本技术的从属权利要求、说明书、附图和实施例,本发明的其它有利特征、方面和细节是显而易见的。
技术实现要素:
[0018]
本发明的目的由一种制剂、优选全身性制剂解决,所述制剂含有式(i)的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯:
[0019][0020]
或式(i)的对映异构体、溶剂化物、水合物或药学上可接受的盐。在本文中,式(i)的化合物也被称作化合物1(compound 1或comp1)。
[0021]
出乎意料地发现,根据式(i)的化合物可以用于减少纤维化,特别是由糖尿病性肾病和非酒精性脂肪性肝炎造成的纤维化。该化合物含有吡啶酮部分作为主要结构元件。此外,令人惊讶的是,根据式(i)的化合物可以作为全身性制剂用于预防和治疗肾病、特别是糖尿病性肾病,肝纤维化和囊性纤维化,即药物通过遍布全身的血液或淋巴系统进行分布。这尤其令人惊讶,因为实际上tg2在几乎所有细胞类型和细胞区室中普遍表达,存在于细胞表面上并分泌到细胞外基质中,并且存在于各种器官中,因此可以设想脱靶效应最可能发生。nash-和小鼠模型研究证实了通过施用含有根据式(i)的化合物的全身性制剂(实施例2和3)实现了对肝脏和肾脏的抗纤维化作用。此外,在小鼠中的生物利用度研究的阳性数据(实施例4)也通过体内全身施用证实了化合物(i)的生物利用度。令人惊讶的是,发现可以通过应用全身性制剂(实施例7)在人体中大大增加化合物(i)的生物利用度。
[0022]
此外,全身性制剂避免了诸如johnson等人使用的渗透泵之类的方式,并且可以完全避免所述装置的植入,并从而使药物的施用客观地便利化,更可靠,更安全,并且可以显著地和客观地减轻患者的痛苦。可以比现有技术的制剂更容易地施用根据本发明的制剂。此外,根据本发明的制剂表现出更高的抗纤维化作用和因此更好的治疗效果。
[0023]
糖尿病也经常与nash(非酒精性脂肪性肝炎)相关,这是无法解释的肝硬化的常见原因。显然,经常同时需要nash和糖尿病性肾病的治疗。根据本发明的全身性制剂可用于同时靶向肝脏(nash)和肾脏(糖尿病性肾病)。同样,胆汁淤积性肝疾病诸如psc(原发性硬化性胆管炎)和pbc(原发性胆汁性胆管炎)是经常与胆血症性肾病有关的纤维化肝病,胆血症性肾病是由向内源性胆汁酸的高暴露引起的肾脏的慢性和纤维化炎症。也可能同时治疗肾脏和预防性治疗肝脏,反之亦然。因此,显然根据本发明的全身性制剂能够将其用于新的临床情况。此外,囊性纤维化经常与糖尿病有关。可以证实,含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯的全身性制剂在肝脏中和在肾脏中表现出相同的抗纤维化作用(实施例5)。
[0024]
发明描述
[0025]
术语“全身性制剂”表示这样的药物组合物:其适合施用使得药物或活性剂在整个生物体中全身施用,例如,用于循环系统的药物形式,从而影响整个身体。施用可以通过肠内施用(药物通过胃肠道吸收)或胃肠外施用(例如肺、鼻、注射或输注)进行。优选地,术语“全身性制剂”不包括用于静脉内应用的制剂。循环系统(也被称作心血管系统或血管系统)是允许血液循环并向和从身体中的细胞运输营养物(诸如氨基酸和电解质)、氧、二氧化碳、
激素和血细胞以提供营养并帮助对抗疾病、稳定温度和ph、以及维持体内稳态的器官系统。
[0026]
循环系统包括循环淋巴的淋巴系统。例如,淋巴的通过时间比血液的通过时间长得多。因此,术语“全身性制剂”表示一种制剂,其中药物分布在整个生物体中,例如通过遍布全身的血液或淋巴系统,例如,在静脉内或肌肉内注射或服用片剂以后,即在肠内以后,特别是在口服或胃肠外施用以后。
[0027]
如本文所公开的全身性制剂优选为片剂、包衣片剂、包衣片剂、胶囊剂、粉末剂或颗粒剂的形式。
[0028]
与此相反,“局部制剂”是应用于其应该起作用的身体表面或内部的特定位置的制剂。局部的意思是“地方”、“局部”、“在特定部位”、“外部”或“被限制到身体的特定部位”。因此,可以降低在生物体其它区域中可能出现的不希望的副作用的风险。最常见的局部施用是指通过包括乳膏剂、泡沫、凝胶、洗剂和软膏剂在内的多种类别应用于身体表面(诸如皮肤或粘膜)来治疗疾病。许多局部药物是皮内的,这意味着,它们直接应用于皮肤。局部药物也可以是吸入的,诸如哮喘药物,或应用于皮肤以外的组织表面,诸如应用于结膜的滴眼剂,或滴入耳朵的滴耳剂,应用于牙齿表面的药物,或借助于泵诸如渗透泵来应用药物。
[0029]
局部制剂包括耳、含服、支气管内、皮内、吸入、关节内、进入臀大肌、心内、皮内、腰椎内、淋巴管内、乳房内、鼻内、神经元内、眼内、眶内、骨内、心包内、肺内、鞘内、气管内、尿道内、子宫内、心室内、膀胱内、玻璃体内、结膜、皮肤(cutan)、鼻、神经周、眼球后、结膜下、阴道和睫毛(ciliary)制剂。
[0030]
本文中使用的术语“胃肠外制剂”表示通常通过注射或输注施用的制剂,包括、但不限于硬膜外、动脉内、静脉内、脉管内(intravasal)、血管内(intravascular)、肌肉内、腹膜内、胸膜内、皮下、表皮下和透皮注射和输注。优选地,胃肠外制剂选自包含以下成员或由以下成员组成的集合:硬膜外、脉管内、血管内、肌肉内、腹膜内、胸膜内、皮下、表皮下和透皮注射和输注。优选地,动脉内和静脉内制剂被排除在胃肠外制剂之外。
[0031]
本文中使用的“肠内制剂”表示通常是经口吸收的药物的制剂(口服(per os、orally、perorally)):片剂、糖衣丸、胶囊剂、汁液、滴剂等。这些药物在胃肠道被吸收到血液中,并然后通过门静脉系统进入肝脏中,并然后通过肝静脉进入血流中。本文中使用的该术语表示这样的制剂:其通常施用方式包括、但不限于肠内、胃内、舌下、口服(经口)和直肠。优选地,肠内制剂由特定制剂组成,所述特定制剂选自包含以下成员或由以下成员组成的集合:肠内、胃内、舌下、口服(经口)和直肠。
[0032]
本文中使用的“口服制剂”表示是经口吸收的药物的制剂(口服(per os、orally、perorally)):片剂、糖衣丸、胶囊剂、汁液、滴剂等。这些药物在胃肠道被吸收到血液中,并然后通过门静脉系统进入肝脏中,并然后通过肝静脉进入血流中。本文中使用的该术语表示口服施用的制剂。
[0033]
所述全身性制剂可以是液体或固体形式,包括溶液、口服滴剂、混悬液、乳剂、粉剂和颗粒诸如泡腾颗粒、片剂诸如未包衣片剂、包衣片剂、泡腾片剂、可溶性片剂、咀嚼片剂、口服冻干粉剂、锭剂、软锭剂、压缩锭剂、舌下片剂、含服片剂、颗粒、泡腾颗粒和胶囊剂。具体地,所述全身性制剂可以是液体制剂,包括口服溶液、混悬液、乳剂、用于口服溶液和混悬液的粉末和颗粒、口服滴剂、用于口服滴剂的粉末、糖浆剂以及用于糖浆剂的粉末和颗粒,或固体形式,包括未包衣片剂、包衣片剂、泡腾片剂、可溶性片剂、咀嚼片剂、口服冻干粉剂、
锭剂、软锭剂、压缩锭剂、舌下片剂、含服片剂、颗粒、泡腾颗粒和胶囊剂。未包衣和包衣片剂以及硬或软胶囊剂是优选的药物制剂。最优选地,所述制剂是片剂或胶囊剂。作为一个例子,可以提及用于胃肠外注射的水或水/丙二醇溶液,或用于口服溶液、混悬液和乳剂的甜味剂和遮光剂的添加。优选地,所述全身性制剂是固体制剂,更优选固体肠内制剂,且最优选固体口服制剂。
[0034]
本文中使用的“局部施用”表示局部制剂的施用。
[0035]
本文中使用的“全身施用”表示全身性制剂的施用。
[0036]
本文中使用的“局部利用度”表示药物从其制剂诸如从制剂的媒介物或从片剂释放到所述药物应该被特定组织或器官吸收的位置,从而药物可以完全发挥作用。
[0037]
本文中使用的“全身利用度”表示在通过静脉内以外的途径施用后完整地到达全身循环的药物的剂量比例。术语“全身利用度”也表示药物或其它物质在施用后被特定组织或器官吸收的程度。例如,口服施用并克服肠道上皮屏障的药物存在于肠道组织中,且因此它具有全身利用度,或者换句话说,它是全身可用的。“全身利用度”和“全身可用的”是“生物利用度”或“可生物利用的”的同义词。因此,局部施用的化合物也可以表现出全身利用度。
[0038]
术语“药物水平”表示药物在血浆、组织或器官中的水平,且短语“在靶部位处的全身利用度”表示相同方面。
[0039]
本文中使用的术语“药学上可接受的盐”表示某种(些)成分的盐,其具有与未修饰的化合物相同的活性并且其在生物学上或在其它方面都不是不希望的。
[0040]
药学上可接受的盐可以与例如有机或无机酸形成。合适的酸包括乙酸、乙酰基水杨酸,有机二羧酸诸如草酸、丙二酸、琥珀酸、戊二酸、酒石酸、富马酸、马来酸、苹果酸、己二酸或谷氨酸,和有机三羧酸诸如柠檬酸或柠檬酸氢钠、海藻酸、抗坏血酸、天冬氨酸、苯甲酸、苯磺酸、亚硫酸(bisulfic acid)、硼酸、丁酸、樟脑酸、樟脑磺酸、碳酸、柠檬酸、环戊烷丙酸、二葡糖酸、十二烷基硫酸(dodecylsulfic acid)、乙磺酸、甲酸、富马酸、甘油酸、甘油磷酸、甘氨酸、葡萄糖庚酸、葡糖酸、谷氨酸、戊二酸、羟乙酸、半硫酸(hemisulfic acid)、庚酸、己酸、马尿酸、氢溴酸、盐酸、氢碘酸、羟基乙磺酸、乳酸、马来酸、苹果酸、丙二酸、扁桃酸、甲磺酸、粘酸、萘磺酸(naphthylanesulfonic acid)、萘酸(naphthylic acid)、烟酸、亚硝酸、草酸、壬酸、磷酸、丙酸、糖精、水杨酸、山梨酸、琥珀酸、硫酸、酒石酸、硫氰酸、巯基乙酸、硫代硫酸、甲苯磺酸、十一烯酸、以及天然地和合成地衍生出的氨基酸。优选地,所述酸是己二酸。
[0041]
因此,本发明的一个优选实施方案涉及式(i)的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯和己二酸的盐:
咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯:
[0053][0054]
此外,所述全身性制剂可以是肠内或胃肠外制剂。因此,根据本发明的一个实施方案涉及一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐,其中所述全身性制剂是肠内或胃肠外制剂的形式。
[0055]
优选的是,所述全身性制剂是口服制剂形式。口服制剂是肠内制剂的特定形式。因此,本发明的一个优选实施方案涉及一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐,其中所述全身性制剂是口服制剂形式。
[0056]
此外,可以以其药学上有活性的盐、溶剂化物或水合物的形式施用(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯,任选地使用基本上无毒的药学上可接受的赋形剂。以已知方式在常规固体或流体载体中使用常规的药学上可接受的赋形剂以合适的剂量制备制剂。
[0057]
因此,根据本发明的全身性制剂可以进一步包含赋形剂。因此,根据本发明的一个实施方案涉及一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和至少一种赋形剂,或由它们组成。
[0058]
在施用全身性制剂以后,施用的药物剂量必须快速地和完全地溶解。必须调节口服施用后胃中的ph变化,并应确保所施用的药物剂量溶解。与小肠中的粘膜释放相关的全身利用度(auc)越大,预期的药理学作用越高。
[0059]
赋形剂可以是酸化剂。术语“酸化剂”表示当溶解在水中时产生小于7.0的ph水平的物质。因此,根据本发明的全身性制剂可以包含酸化剂。酸化剂包括有机酸诸如抗坏血酸、有机二羧酸诸如草酸、丙二酸、琥珀酸、戊二酸、酒石酸、富马酸、马来酸、苹果酸、肥酸(己二酸)或谷氨酸、和有机三羧酸诸如柠檬酸或柠檬酸氢钠。优选地,所述酸化剂是己二酸。
[0060]
用于如本文所公开的全身性制剂的优选“酸化剂”选自由以下成员组成的集合:抗坏血酸、有机二羧酸诸如草酸、丙二酸、琥珀酸、戊二酸、酒石酸、富马酸、马来酸、苹果酸、己二酸、谷氨酸、和有机三羧酸、柠檬酸和柠檬酸氢钠。
[0061]
用于如本文所公开的全身性制剂的更优选“酸化剂”选自由以下成员组成的集合:己二酸、富马酸、戊二酸。
[0062]
因此,根据本发明的全身性制剂可以包含酸化剂。
[0063]
根据本发明的一个优选实施方案涉及一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和至少一种赋形剂,或由它们组成,其中所述至少一种赋形剂是酸化剂。
[0064]
根据本发明的另一个优选实施方案涉及一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和至少一种酸化剂,或由它们组成。
[0065]
根据本发明的一个优选实施方案涉及一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和至少一种赋形剂,或由它们组成,其中所述至少一种赋形剂是酸化剂,且其中至少一种酸化剂选自包含以下成员或由以下成员组成的集合:有机二羧酸和有机三羧酸。优选地,至少一种酸化剂选自由以下成员组成的集合:有机二羧酸和有机三羧酸。更优选地,所述至少一种酸化剂选自包含以下成员或由以下成员组成的集合:有机二羧酸和有机三羧酸。甚至更优选地,所述至少一种酸化剂选自由有机二羧酸和有机三羧酸组成的集合。
[0066]
因此,根据本发明的一个优选实施方案涉及一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和至少一种酸化剂,或由它们组成,其中至少一种酸化剂选自包含以下成员或由以下成员组成的集合:有机二羧酸和有机三羧酸。
[0067]
根据本发明的一个优选实施方案涉及一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和至少一种赋形剂,或由它们组成,其中所述至少一种赋形剂是酸化剂,且其中至少一种酸化剂选自包含以下成员或由以下成员组成的集合:草酸、丙二酸、琥珀酸、戊二酸、酒石酸、富马酸、马来酸、苹果酸、肥酸(己二酸)或谷氨酸。优选地,至少一种酸化剂选自由以下成员组成的集合:草酸、丙二酸、琥珀酸、戊二酸、酒石酸、富马酸、马来酸、苹果酸、肥酸(己二酸)或谷氨酸。更优选地,所述至少一种酸化剂选自包含以下成员或由以下成员组成的集合:草酸、丙二酸、琥珀酸、戊二酸、酒石酸、富马酸、马来酸、苹果酸、肥酸(己二酸)或谷氨酸。甚至更优选地,所述至少一种酸化剂选自由以下成员组成的集合:草酸、丙二酸、琥珀酸、戊二酸、酒石酸、富马酸、马来酸、苹果酸、肥酸(己二酸)或谷氨酸。
[0068]
根据本发明的一个优选实施方案涉及一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和至少一种酸化剂,或由它们组成,其中至少一种酸化剂选自包含以下成员或由以
下成员组成的集合:草酸、丙二酸、琥珀酸、戊二酸、酒石酸、富马酸、马来酸、苹果酸、肥酸(己二酸)或谷氨酸。
[0069]
根据本发明的一个更优选实施方案涉及一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和至少一种赋形剂,或由它们组成,其中所述至少一种赋形剂是酸化剂,其中所述酸化剂是己二酸、富马酸、戊二酸。
[0070]
根据本发明的一个特别优选的实施方案涉及一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和至少一种赋形剂,或由它们组成,其中所述至少一种赋形剂是酸化剂,其中所述酸化剂是己二酸。
[0071]
根据本发明的一个特别优选的实施方案涉及一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和至少一种酸化剂,或由它们组成,其中至少一种酸化剂是己二酸。
[0072]
根据本发明的一个特别优选的实施方案涉及一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和己二酸或由它们组成。
[0073]
药物溶液在胃通过后输送至小肠。至少在禁食状态下,这段通道与从约2至约6的ph增加相关。药物剂量必须保留在溶液中,即药物不应沉淀。这种效果可以通过添加聚合物沉淀抑制剂来实现。因此,所述聚合物沉淀抑制剂抑制(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐的结晶,并作为结晶抑制剂起作用。
[0074]
聚合物沉淀抑制剂是能够稳定药物的过饱和阶段的聚合物,即它们能够阻止药物分子的成核或最初形成的药物颗粒的生长,这通过覆盖药物颗粒的表面从而阻止颗粒-颗粒相互作用来实现,或通过提高悬浮介质的粘度来实现。沉淀抑制剂在动力学上稳定药物的过饱和状态的能力被认为是由于溶液中药物和聚合物之间的分子间相互作用(例如通过氢键合或疏水相互作用)、聚合物在空间上阻碍结晶过程的能力或增加悬浮介质的粘度,而不是通过增加药物的溶解度,即通过增加平衡溶解度。
[0075]
所述化合物的饱和溶解度在小肠中的ph值是低的(实施例10和图11)。通过添加也可以作为粘合剂的聚合物沉淀抑制剂来稳定溶液。当药物暴露于水性介质时,聚合物沉淀抑制剂减缓药物的沉淀或结晶,优选地通过络合作用。
[0076]
除此之外,聚合物沉淀抑制剂增加了介质中的粘度,这进一步增强了效果。
[0077]
因此,根据本发明的全身性制剂可以进一步包含聚合物沉淀抑制剂。因此,所述赋形剂可以是聚合物沉淀抑制剂。
[0078]
术语“聚合物沉淀抑制剂”表示减缓药物的沉淀或结晶的物质。
[0079]“聚合物沉淀抑制剂”包括纤维素衍生物、淀粉衍生物、葡聚糖/糊精衍生物、聚醚衍生物、聚乙烯基衍生物、聚丙烯酸衍生物和聚胺衍生物、聚磺酸衍生物和它们的组合。
[0080]
在某些实施方案中“聚合物沉淀抑制剂”选自包含以下成员或由以下成员组成的集合:
[0081]
纤维素衍生物,包括、但不限于微晶纤维素(mcc)、醋酸邻苯二甲酸纤维素(cap)、醋酸对苯二甲酸纤维素、醋酸间苯二甲酸纤维素、醋酸丁酸纤维素(cab)、醋酸偏苯三酸纤维素(cat)、甲基纤维素(mc)、醋酸邻苯二甲酸甲基纤维素、乙基纤维素(ec)、羧甲基纤维素(cmc)、羧甲基纤维素钠、羧甲基乙基纤维素(cmec)、羟基甲基纤维素(hmc)、羟乙基纤维素(hec)、羟丙基纤维素(hpc或羟丙纤维素)、l-羟丙基纤维素、羟丙基甲基纤维素(hpmc或羟丙甲纤维素)、羧甲基羟乙基纤维素(cmhec)、羧甲基羟乙基纤维素钠(nacmhec)、邻苯二甲酸羟丙基甲基纤维素(hpmcp,邻苯二甲酸酯羟丙甲纤维素)、醋酸羟丙甲纤维素琥珀酸酯(hpmcas,醋酸羟丙甲基纤维素琥珀酸酯);
[0082]
淀粉衍生物,包括、但不限于羟乙基淀粉、羟丙基淀粉(hps)和预胶化淀粉;
[0083]
葡聚糖/糊精衍生物,包括、但不限于环葡聚糖(cyclodextran)(即,环异麦芽(cycloisomalto)-七糖(ci-7)、环异麦芽-八糖(ci-8)、环异麦芽-九糖(ci-9))、羟丙基葡聚糖、麦芽糊精、α-/β-/γ-环糊精、2-羟乙基-β-环糊精、2-羟丙基-β-环糊精(hpβcd)、磺基丁醚-β-环糊精钠盐、甲基化-β-环糊精、2-羟丙基-γ-环糊精;
[0084]
聚醚衍生物,包括、但不限于聚乙二醇(peg)、聚环氧乙烷(peo)、聚醚多元醇、聚(丙二醇)双(2-氨基丙基醚)(ppgae)、聚(环氧乙烷)-聚(环氧丙烷)-聚(环氧乙烷)(peo-ppo-peo,泊洛沙姆)诸如泊洛沙姆188和泊洛沙姆407,
[0085]
聚乙烯基衍生物,包括、但不限于聚乙烯醇(pva)、聚醋酸乙烯邻苯二甲酸酯(pvap)、聚乙烯吡咯烷酮(pvp)、聚乙烯吡咯烷酮-共聚-聚乙酸乙烯酯(pvpva)、聚乙烯基己内酰胺-聚乙酸乙烯酯-聚乙二醇接枝共聚物
[0086]
聚丙烯酸衍生物,包括、但不限于聚(丙烯酸)(paa)、聚(丙烯酰胺/丙烯酸)(pac-ac)、聚甲基丙烯酸酯(pma)、聚甲基丙烯酸、聚(甲基丙烯酸/甲基丙烯酸甲酯)、聚(甲基丙烯酸/丙烯酸酯乙酯);
[0087]
聚胺衍生物,包括、但不限于聚乙烯亚胺(pei)、聚烯丙胺氯化氢、聚二烯丙基二甲基氯化铵和聚(2-乙基-2-噁唑啉);
[0088]
聚磺酸衍生物,包括、但不限于聚苯乙烯磺酸(pssa);和
[0089]
至少两种上述聚合物沉淀抑制剂的组合。
[0090]
优选地,所述“聚合物沉淀抑制剂”选自包含以下成员或由以下成员组成的集合:微晶纤维素(mcc)、醋酸邻苯二甲酸纤维素(cap)、醋酸对苯二甲酸纤维素、醋酸间苯二甲酸纤维素、醋酸丁酸纤维素(cab)、醋酸偏苯三酸纤维素(cat)、甲基纤维素(mc)、醋酸邻苯二甲酸甲基纤维素、乙基纤维素(ec)、羧甲基纤维素(cmc)、羧甲基纤维素钠、羧甲基乙基纤维素(cmec)、羟基甲基纤维素(hmc)、羟乙基纤维素(hec)、羟丙基纤维素(hpc或羟丙纤维素)、l-羟丙基纤维素、羟丙基甲基纤维素(hpmc或羟丙甲纤维素)、羧甲基羟乙基纤维素(cmhec)、羧甲基羟乙基纤维素钠(nacmhec)、邻苯二甲酸羟丙基甲基纤维素(hpmcp,邻苯二甲酸酯羟丙甲纤维素)、醋酸羟丙甲纤维素琥珀酸酯(hpmcas,醋酸羟丙甲基纤维素琥珀酸酯)、羟乙基淀粉、羟丙基淀粉(hps)和预胶化淀粉、环葡聚糖(即,环异麦芽-七糖(ci-7)、环
异麦芽-八糖(ci-8)、环异麦芽-九糖(ci-9))、羟丙基葡聚糖、麦芽糊精、α-/β-/γ-环糊精、2-羟乙基-β-环糊精、2-羟丙基-β-环糊精(hpβcd)、磺基丁醚-β-环糊精钠盐、甲基化-β-环糊精、2-羟丙基-γ-环糊精、聚乙二醇(peg)、聚环氧乙烷(peo)、聚醚多元醇、聚(丙二醇)双(2-氨基丙基醚)(ppgae)、聚(环氧乙烷)-聚(环氧丙烷)-聚(环氧乙烷)(peo-ppo-peo,泊洛沙姆)诸如泊洛沙姆188和泊洛沙姆407、聚乙烯醇(pva)、聚醋酸乙烯邻苯二甲酸酯(pvap)、聚乙烯吡咯烷酮(pvp)、聚乙烯吡咯烷酮-共聚-聚乙酸乙烯酯(pvpva)、聚乙烯基己内酰胺-聚乙酸乙烯酯-聚乙二醇接枝共聚物聚(丙烯酸)(paa)、聚(丙烯酰胺/丙烯酸)(pac-ac)、聚甲基丙烯酸酯(pma)、聚甲基丙烯酸、聚(甲基丙烯酸/甲基丙烯酸甲酯)、聚(甲基丙烯酸/丙烯酸酯乙酯)、聚乙烯亚胺(pei)、聚烯丙胺氯化氢、聚二烯丙基二甲基氯化铵、聚(2-乙基-2-噁唑啉)、聚苯乙烯磺酸(pssa);和
[0091]
至少两种上述聚合物沉淀抑制剂的组合。
[0092]
更优选地,所述“聚合物沉淀抑制剂”选自包含以下成员或由以下成员组成的集合:微晶纤维素(mcc)、醋酸邻苯二甲酸纤维素(cap)、醋酸对苯二甲酸纤维素、醋酸间苯二甲酸纤维素、醋酸丁酸纤维素(cab)、醋酸偏苯三酸纤维素(cat)、甲基纤维素(mc)、醋酸邻苯二甲酸甲基纤维素、乙基纤维素(ec)、羧甲基纤维素(cmc)、羧甲基纤维素钠、羧甲基乙基纤维素(cmec)、羟基甲基纤维素(hmc)、羟乙基纤维素(hec)、羟丙基纤维素(hpc或羟丙纤维素)、l-羟丙基纤维素、羟丙基甲基纤维素(hpmc或羟丙甲纤维素)、羧甲基羟乙基纤维素(cmhec)、羧甲基羟乙基纤维素钠(nacmhec)、邻苯二甲酸羟丙基甲基纤维素(hpmcp,邻苯二甲酸酯羟丙甲纤维素)、醋酸羟丙甲纤维素琥珀酸酯(hpmcas,醋酸羟丙甲基纤维素琥珀酸酯)、聚乙二醇(peg)、聚环氧乙烷(peo)、聚醚多元醇、聚(丙二醇)双(2-氨基丙基醚)(ppgae)、聚(环氧乙烷)-聚(环氧丙烷)-聚(环氧乙烷)(peo-ppo-peo,泊洛沙姆)诸如泊洛沙姆188和泊洛沙姆407、聚乙烯醇(pva)、聚醋酸乙烯邻苯二甲酸酯(pvap)、聚乙烯吡咯烷酮(pvp)、聚乙烯吡咯烷酮-共聚-聚乙酸乙烯酯(pvpva)、聚乙烯基己内酰胺-聚乙酸乙烯酯-聚乙二醇接枝共聚物聚(丙烯酸)(paa)、聚(丙烯酰胺/丙烯酸)(pac-ac)、聚甲基丙烯酸酯(pma)、聚甲基丙烯酸、聚(甲基丙烯酸/甲基丙烯酸甲酯)、聚(甲基丙烯酸/丙烯酸酯乙酯)和
[0093]
至少两种上述聚合物沉淀抑制剂的组合。
[0094]
更优选地,合适的聚合物沉淀抑制剂包括l-羟丙基纤维素、羟丙基纤维素、l-羟丙基纤维素和羟丙基纤维素的组合、聚乙二醇(peg)、聚(环氧乙烷)-聚(环氧丙烷)-聚(环氧乙烷)(=泊洛沙姆)、聚乙烯醇(pva)、聚乙烯吡咯烷酮(pvp)、羧甲基纤维素(cmc)、甲基纤维素(mc)、羟乙基纤维素(hec)、羟丙基甲基纤维素(hpmc)、乙基纤维素(ec)、聚乙烯基己内酰胺-聚乙酸乙烯酯-聚乙二醇接枝共聚物和/或羧甲基纤维素钠。更优选地,所述聚合物沉淀抑制剂选自包含以下成员或由以下成员组成的集合:聚乙烯醇(pva)、聚乙烯基己内酰胺-聚乙酸乙烯酯-聚乙二醇接枝共聚物纤维素和纤维素衍生物。更优选地,所述聚合物沉淀抑制剂是聚乙烯醇(pva)、聚乙烯基己内酰胺-聚乙酸乙烯酯-聚乙二醇接枝共聚物纤维素、纤维素衍生物、或纤维素和纤维素衍生物的组合。
[0095]
优选地,所述纤维素是微晶纤维素(mcc)且所述纤维素衍生物选自由以下成员组成的集合:微晶纤维素(mcc)、醋酸邻苯二甲酸纤维素(cap)、醋酸对苯二甲酸纤维素、醋酸间苯二甲酸纤维素、醋酸丁酸纤维素(cab)、醋酸偏苯三酸纤维素(cat)、甲基纤维素(mc)、醋酸邻苯二甲酸甲基纤维素、乙基纤维素(ec)、羧甲基纤维素(cmc)、羧甲基纤维素钠、羧甲基乙基纤维素(cmec)、羟基甲基纤维素(hmc)、羟乙基纤维素(hec)、羟丙基纤维素(hpc或羟丙纤维素)、l-羟丙基纤维素、羟丙基甲基纤维素(hpmc或羟丙甲纤维素)、羧甲基羟乙基纤维素(cmhec)、羧甲基羟乙基纤维素钠(nacmhec)、邻苯二甲酸羟丙基甲基纤维素(hpmcp,邻苯二甲酸酯羟丙甲纤维素)、醋酸羟丙甲纤维素琥珀酸酯(hpmcas,醋酸羟丙甲基纤维素琥珀酸酯)。
[0096]
甚至更优选地,所述聚合物沉淀抑制剂选自包含以下成员或由以下成员组成的集合:聚乙烯醇(pva)、聚乙烯基己内酰胺-聚乙酸乙烯酯-聚乙二醇接枝共聚物l-羟丙基纤维素和羟丙基纤维素。最优选地,所述聚合物沉淀抑制剂是聚乙烯醇(pva)、聚乙烯基己内酰胺-聚乙酸乙烯酯-聚乙二醇接枝共聚物l-羟丙基纤维素、羟丙基纤维素、或l-羟丙基纤维素和羟丙基纤维素的组合。所述l-羟丙基纤维素和羟丙基纤维素的组合充当聚合物沉淀抑制剂和崩解剂使得可以减少崩解剂的量。
[0097]
如本文所公开的全身性制剂和特别是用于口服施用的全身性制剂最优选地含有作为聚合物沉淀抑制剂的聚乙烯醇(pva)、聚乙烯基己内酰胺-聚乙酸乙烯酯-聚乙二醇接枝共聚物l-羟丙基纤维素、羟丙基纤维素、或l-羟丙基纤维素和羟丙基纤维素的组合。
[0098]
如本文所公开的全身性制剂和特别是用于口服施用的全身性制剂最优选地包含至少一种酸化剂和/或至少一种聚合物沉淀抑制剂。
[0099]
如本文所公开的全身性制剂和特别是用于口服施用的全身性制剂最优选地含有己二酸作为酸化剂和l-羟丙基纤维素、羟丙基纤维素、聚乙烯醇(pva)、聚乙烯基己内酰胺-聚乙酸乙烯酯-聚乙二醇接枝共聚物或l-羟丙基纤维素和羟丙基纤维素的组合作为聚合物沉淀抑制剂。
[0100]
因此,本发明的一个实施方案涉及一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和至少一种赋形剂,或由它们组成,其中所述至少一种赋形剂是聚合物沉淀抑制剂。
[0101]
因此,本发明的一个实施方案涉及一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和至少一种聚合物沉淀抑制剂或由它们组成。
[0102]
优选地所述“聚合物沉淀抑制剂”选自包含以下成员或由以下成员组成的集合:
[0103]
纤维素衍生物,包括、但不限于微晶纤维素(mcc)、醋酸邻苯二甲酸纤维素(cap)、醋酸对苯二甲酸纤维素、醋酸间苯二甲酸纤维素、醋酸丁酸纤维素(cab)、醋酸偏苯三酸纤维素(cat)、甲基纤维素(mc)、醋酸邻苯二甲酸甲基纤维素、乙基纤维素(ec)、羧甲基纤维素(cmc)、羧甲基纤维素钠、羧甲基乙基纤维素(cmec)、羟基甲基纤维素(hmc)、羟乙基纤维素
(hec)、羟丙基纤维素(hpc或羟丙纤维素)、l-羟丙基纤维素、羟丙基甲基纤维素(hpmc或羟丙甲纤维素)、羧甲基羟乙基纤维素(cmhec)、羧甲基羟乙基纤维素钠(nacmhec)、邻苯二甲酸羟丙基甲基纤维素(hpmcp,邻苯二甲酸酯羟丙甲纤维素)、醋酸羟丙甲纤维素琥珀酸酯(hpmcas,醋酸羟丙甲基纤维素琥珀酸酯);
[0104]
淀粉衍生物,包括、但不限于羟乙基淀粉、羟丙基淀粉(hps)和预胶化淀粉;
[0105]
葡聚糖/糊精衍生物,包括、但不限于环葡聚糖(即,环异麦芽-七糖(ci-7)、环异麦芽-八糖(ci-8)、环异麦芽-九糖(ci-9))、羟丙基葡聚糖、麦芽糊精、α-/β-/γ-环糊精、2-羟乙基-β-环糊精、2-羟丙基-β-环糊精(hpβcd)、磺基丁醚-β-环糊精钠盐、甲基化-β-环糊精、2-羟丙基-γ-环糊精;
[0106]
聚醚衍生物,包括、但不限于聚乙二醇(peg)、聚环氧乙烷(peo)、聚醚多元醇、聚(丙二醇)双(2-氨基丙基醚)(ppgae)、聚(环氧乙烷)-聚(环氧丙烷)-聚(环氧乙烷)(peo-ppo-peo,泊洛沙姆)诸如泊洛沙姆188和泊洛沙姆407,
[0107]
聚乙烯基衍生物,包括、但不限于聚乙烯醇(pva)、聚醋酸乙烯邻苯二甲酸酯(pvap)、聚乙烯吡咯烷酮(pvp)、聚乙烯吡咯烷酮-共聚-聚乙酸乙烯酯(pvpva)、聚乙烯基己内酰胺-聚乙酸乙烯酯-聚乙二醇接枝共聚物
[0108]
聚丙烯酸衍生物,包括、但不限于聚(丙烯酸)(paa)、聚(丙烯酰胺/丙烯酸)(pac-ac)、聚甲基丙烯酸酯(pma)、聚甲基丙烯酸、聚(甲基丙烯酸/甲基丙烯酸甲酯)、聚(甲基丙烯酸/丙烯酸酯乙酯);
[0109]
聚胺衍生物,包括、但不限于聚乙烯亚胺(pei)、聚烯丙胺氯化氢、聚二烯丙基二甲基氯化铵和聚(2-乙基-2-噁唑啉);
[0110]
聚磺酸衍生物,包括、但不限于聚苯乙烯磺酸(pssa);和
[0111]
至少两种上述聚合物沉淀抑制剂的组合。
[0112]
更优选地,所述“聚合物沉淀抑制剂”选自包含以下成员或由以下成员组成的集合:微晶纤维素(mcc)、醋酸邻苯二甲酸纤维素(cap)、醋酸对苯二甲酸纤维素、醋酸间苯二甲酸纤维素、醋酸丁酸纤维素(cab)、醋酸偏苯三酸纤维素(cat)、甲基纤维素(mc)、醋酸邻苯二甲酸甲基纤维素、乙基纤维素(ec)、羧甲基纤维素(cmc)、羧甲基纤维素钠、羧甲基乙基纤维素(cmec)、羟基甲基纤维素(hmc)、羟乙基纤维素(hec)、羟丙基纤维素(hpc或羟丙纤维素)、l-羟丙基纤维素、羟丙基甲基纤维素(hpmc或羟丙甲纤维素)、羧甲基羟乙基纤维素(cmhec)、羧甲基羟乙基纤维素钠(nacmhec)、邻苯二甲酸羟丙基甲基纤维素(hpmcp,邻苯二甲酸酯羟丙甲纤维素)、醋酸羟丙甲纤维素琥珀酸酯(hpmcas,醋酸羟丙甲基纤维素琥珀酸酯)、聚乙二醇(peg)、聚环氧乙烷(peo)、聚醚多元醇、聚(丙二醇)双(2-氨基丙基醚)(ppgae)、聚(环氧乙烷)-聚(环氧丙烷)-聚(环氧乙烷)(peo-ppo-peo,泊洛沙姆)诸如泊洛沙姆188和泊洛沙姆407、聚乙烯醇(pva)、聚醋酸乙烯邻苯二甲酸酯(pvap)、聚乙烯吡咯烷酮(pvp)、聚乙烯吡咯烷酮-共聚-聚乙酸乙烯酯(pvpva)、聚乙烯基己内酰胺-聚乙酸乙烯酯-聚乙二醇接枝共聚物聚(丙烯酸)(paa)、聚(丙烯酰胺/丙烯酸)(pac-ac)、聚甲基丙烯酸酯(pma)、聚甲基丙烯酸、聚(甲基丙烯酸/甲基丙烯酸甲酯)、聚(甲基丙烯酸/丙烯酸酯乙酯)和
[0113]
至少两种上述聚合物沉淀抑制剂的组合。
[0114]
本发明的一个优选实施方案涉及一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和至少一种赋形剂,或由它们组成,其中所述至少一种赋形剂是聚合物沉淀抑制剂,且其中所述聚合物沉淀抑制剂选自包含以下成员或由以下成员组成的集合:聚乙烯醇(pva)、聚乙烯基己内酰胺-聚乙酸乙烯酯-聚乙二醇接枝共聚物纤维素和纤维素衍生物。
[0115]
本发明的一个优选实施方案涉及一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和至少一种聚合物沉淀抑制剂或由它们组成,所述聚合物沉淀抑制剂选自包含以下成员或由以下成员组成的集合:聚乙烯醇(pva)、聚乙烯基己内酰胺-聚乙酸乙烯酯-聚乙二醇接枝共聚物纤维素和纤维素衍生物。
[0116]
优选地,所述纤维素是微晶纤维素(mcc)且所述纤维素衍生物选自由以下成员组成的集合:微晶纤维素(mcc)、醋酸邻苯二甲酸纤维素(cap)、醋酸对苯二甲酸纤维素、醋酸间苯二甲酸纤维素、醋酸丁酸纤维素(cab)、醋酸偏苯三酸纤维素(cat)、甲基纤维素(mc)、醋酸邻苯二甲酸甲基纤维素、乙基纤维素(ec)、羧甲基纤维素(cmc)、羧甲基纤维素钠、羧甲基乙基纤维素(cmec)、羟基甲基纤维素(hmc)、羟乙基纤维素(hec)、羟丙基纤维素(hpc或羟丙纤维素)、l-羟丙基纤维素、羟丙基甲基纤维素(hpmc或羟丙甲纤维素)、羧甲基羟乙基纤维素(cmhec)、羧甲基羟乙基纤维素钠(nacmhec)、邻苯二甲酸羟丙基甲基纤维素(hpmcp,邻苯二甲酸酯羟丙甲纤维素)、醋酸羟丙甲纤维素琥珀酸酯(hpmcas,醋酸羟丙甲基纤维素琥珀酸酯)。
[0117]
因此,本发明的一个实施方案涉及一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和至少一种赋形剂,或由它们组成,其中所述至少一种赋形剂是聚合物沉淀抑制剂,且其中所述聚合物沉淀抑制剂是聚乙烯醇(pva)、聚乙烯基己内酰胺-聚乙酸乙烯酯-聚乙二醇接枝共聚物l-羟丙基纤维素和/或羟丙基纤维素。
[0118]
因此,本发明的一个实施方案涉及一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和至少一种聚合物沉淀抑制剂或由它们组成,所述聚合物沉淀抑制剂选自包含以下成员或由以下成员组成的集合:聚乙烯醇(pva)、聚乙烯基己内酰胺-聚乙酸乙烯酯-聚乙二醇接枝共聚物l-羟丙基纤维素和/或羟丙基纤维素。
[0119]
因此,本发明的一个实施方案涉及一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和聚乙烯醇(pva)、聚乙烯基己内酰胺-聚乙酸乙烯酯-聚乙二醇接枝共聚物
l-羟丙基纤维素和/或羟丙基纤维素或由它们组成。
[0120]
根据本发明的全身性制剂可以包含粘合剂。因此,所述赋形剂可以是粘合剂。粘合剂被表征为将粉末彼此结合或“粘合”在一起的物质,且因此它们在制剂中充当“胶水”。换而言之,粘合剂是一种材料,其机械地、化学地、通过粘合或粘结力将其它材料保持或拉到一起以形成一个内聚性整体。合适的粘合剂包括糖,诸如蔗糖;多糖诸如黄原胶、瓜尔胶、角叉菜胶、从小麦、玉米、大米和马铃薯衍生出的淀粉、和从小麦、玉米、大米和马铃薯衍生出的预凝(改性)淀粉、淀粉羟乙酸钠;天然树胶诸如金合欢胶、明胶和黄蓍胶;海藻的衍生物诸如海藻酸、海藻酸钠和海藻酸钙铵,纤维素或其衍生物诸如羟丙基纤维素、l-羟丙基纤维素、低取代的羟丙基纤维素、甲基纤维素、羧甲基纤维素钠、羟丙基甲基纤维素和聚乙烯吡咯烷酮(交聚维酮)特别是聚维酮k25。优选地所述粘合剂是聚合物,更优选凝胶形成聚合物,更优选地所述粘合剂是纤维素或其衍生物,更优选l-羟丙基纤维素,且最优选l-羟丙基纤维素和羟丙基纤维素的组合。
[0121]
羟丙基纤维素是纤维素的部分地取代的聚(羟丙基)醚。它可以含有不超过0.6%的硅胶或另一种合适的防结块剂。羟丙基纤维素以许多具有各种溶液粘度的不同等级商购可得。分子量范围为50000-1250000。羟丙基纤维素是部分地o-(2-羟丙基化的)纤维素。相对于干燥物,它含有53.4%至80.5%的羟基丙氧基基团。平均聚合度范围为200-300。摩尔取代度为约4。
[0122]“低取代的羟丙基纤维素”(l-hpc或lhpc)是纤维素的低取代的聚(羟丙基)醚。它以许多具有不同粒度和取代水平的不同等级商购可得。
[0123]
相对于干燥物,低取代的羟丙基纤维素含有5%至16%羟基丙氧基基团。摩尔取代度《1。特别地,低取代的羟丙基纤维素是低取代的o-(2-羟丙基化的)纤维素,以干燥基础计算,其含有不小于5.0%且不超过16.0%的羟基丙氧基基团(-och2chohch3)。
[0124]
低取代的羟丙基纤维素是低取代的o-(2-羟丙基化的)纤维素,以干燥基础计算,其含有不小于5.0%且不超过16.0%的羟基丙氧基基团(-och2chohch3)。
[0125]“聚乙烯基己内酰胺-聚乙酸乙烯酯-聚乙二醇接枝共聚物(pcl-pvac-peg)”具有以下化学结构:
(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和至少一种赋形剂,或由它们组成,其中所述至少一种赋形剂是粘合剂,其中所述粘合剂是聚乙烯吡咯烷酮,且其中所述聚乙烯吡咯烷酮是聚维酮k25。
[0134]
因此,本发明的一个优选实施方案涉及一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和聚维酮k25或由它们组成。
[0135]
此外,根据本发明的全身性制剂可以包含粘合剂和/或聚合物沉淀抑制剂。
[0136]
因此,本发明的一个优选实施方案涉及一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和至少一种赋形剂,或由它们组成,其中至少一种赋形剂选自包含以下成员或由以下成员组成的集合:粘合剂和聚合物沉淀抑制剂。
[0137]
因此,本发明的一个优选实施方案涉及一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和至少一种粘合剂和/或至少一种聚合物沉淀抑制剂或由它们组成。
[0138]
因此,本发明的一个优选实施方案涉及一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和至少一种赋形剂,或由它们组成,其中所述至少一种赋形剂是粘合剂和聚合物沉淀抑制剂。优选地,至少一种赋形剂同时作为粘合剂和聚合物沉淀抑制剂起作用。因此,至少一种赋形剂是粘合剂和聚合物沉淀抑制剂。
[0139]
因此,本发明的一个优选实施方案涉及一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和至少一种化合物或由它们组成,所述化合物是粘合剂和聚合物沉淀抑制剂。
[0140]
因此,本发明的一个优选实施方案涉及一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、至少一种粘合剂和至少一种聚合物沉淀抑制剂或由它们组成。
[0141]
优选地,所述“粘合剂”选自包含以下成员或由以下成员组成的集合:糖,诸如蔗糖;多糖诸如黄原胶、瓜尔胶、角叉菜胶、从小麦、玉米、大米和马铃薯衍生出的淀粉、和从小麦、玉米、大米和马铃薯衍生出的预凝(改性)淀粉、淀粉羟乙酸钠;天然树胶诸如金合欢胶、明胶和黄蓍胶;海藻的衍生物诸如海藻酸、海藻酸钠和海藻酸钙铵,纤维素或其衍生物诸如羟丙基纤维素、l-羟丙基纤维素、低取代的羟丙基纤维素、甲基纤维素、羧甲基纤维素钠、羟丙基甲基纤维素和聚乙烯吡咯烷酮(交聚维酮)特别是聚维酮k25;且
[0142]“聚合物沉淀抑制剂”选自包含以下成员或由以下成员组成的集合:微晶纤维素
(mcc)、醋酸邻苯二甲酸纤维素(cap)、醋酸对苯二甲酸纤维素、醋酸间苯二甲酸纤维素、醋酸丁酸纤维素(cab)、醋酸偏苯三酸纤维素(cat)、甲基纤维素(mc)、醋酸邻苯二甲酸甲基纤维素、乙基纤维素(ec)、羧甲基纤维素(cmc)、羧甲基纤维素钠、羧甲基乙基纤维素(cmec)、羟基甲基纤维素(hmc)、羟乙基纤维素(hec)、羟丙基纤维素(hpc或羟丙纤维素)、l-羟丙基纤维素、羟丙基甲基纤维素(hpmc或羟丙甲纤维素)、羧甲基羟乙基纤维素(cmhec)、羧甲基羟乙基纤维素钠(nacmhec)、邻苯二甲酸羟丙基甲基纤维素(hpmcp,邻苯二甲酸酯羟丙甲纤维素)、醋酸羟丙甲纤维素琥珀酸酯(hpmcas,醋酸羟丙甲基纤维素琥珀酸酯)、聚乙二醇(peg)、聚环氧乙烷(peo)、聚醚多元醇、聚(丙二醇)双(2-氨基丙基醚)(ppgae)、聚(环氧乙烷)-聚(环氧丙烷)-聚(环氧乙烷)(peo-ppo-peo,泊洛沙姆)诸如泊洛沙姆188和泊洛沙姆407、聚乙烯醇(pva)、聚醋酸乙烯邻苯二甲酸酯(pvap)、聚乙烯吡咯烷酮(pvp)、聚乙烯吡咯烷酮-共聚-聚乙酸乙烯酯(pvpva)、聚乙烯基己内酰胺-聚乙酸乙烯酯-聚乙二醇接枝共聚物聚(丙烯酸)(paa)、聚(丙烯酰胺/丙烯酸)(pac-ac)、聚甲基丙烯酸酯(pma)、聚甲基丙烯酸、聚(甲基丙烯酸/甲基丙烯酸甲酯)、聚(甲基丙烯酸/丙烯酸酯乙酯)和至少两种上述聚合物沉淀抑制剂的组合。
[0143]
本发明的一个优选实施方案涉及一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和至少一种赋形剂,或由它们组成,其中至少一种赋形剂选自包含以下成员或由以下成员组成的集合:粘合剂和聚合物沉淀抑制剂,且其中所述聚合物沉淀抑制剂是聚乙烯醇(pva)、聚乙烯基己内酰胺-聚乙酸乙烯酯-聚乙二醇接枝共聚物纤维素、纤维素衍生物、纤维素和衍生物的组合或纤维素衍生物的组合。
[0144]
本发明的一个优选实施方案涉及一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和至少一种粘合剂和/或至少一种聚合物沉淀抑制剂或由它们组成,其中所述聚合物沉淀抑制剂是聚乙烯醇(pva)、聚乙烯基己内酰胺-聚乙酸乙烯酯-聚乙二醇接枝共聚物纤维素、纤维素衍生物、纤维素和衍生物的组合或纤维素衍生物的组合。
[0145]
本发明的一个优选实施方案涉及一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和至少一种赋形剂,或由它们组成,其中至少一种赋形剂选自包含以下成员或由以下成员组成的集合:粘合剂和聚合物沉淀抑制剂,且其中所述聚合物沉淀抑制剂是聚乙烯醇(pva)、聚乙烯基己内酰胺-聚乙酸乙烯酯-聚乙二醇接枝共聚物l-羟丙基纤维素、羟丙基纤维素、或l-羟丙基纤维素和羟丙基纤维素的组合。
[0146]
本发明的一个优选实施方案涉及一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和至少一种粘合剂和/或至少一种聚合物沉淀抑制剂或由它们组成,其中所述聚合物沉淀抑
制剂是聚乙烯醇(pva)、聚乙烯基己内酰胺-聚乙酸乙烯酯-聚乙二醇接枝共聚物l-羟丙基纤维素、羟丙基纤维素、或l-羟丙基纤维素和羟丙基纤维素的组合。
[0147]
本发明的一个实施方案涉及一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和至少一种赋形剂,或由它们组成,其中至少一种赋形剂选自包含以下成员或由以下成员组成的集合:粘合剂和聚合物沉淀抑制剂,其中所述聚合物沉淀抑制剂是聚乙烯醇(pva)、聚乙烯基己内酰胺-聚乙酸乙烯酯-聚乙二醇接枝共聚物l-羟丙基纤维素、羟丙基纤维素或l-羟丙基纤维素的组合,且其中所述粘合剂是l-羟丙基纤维素、羟丙基纤维素、l-羟丙基纤维素和羟丙基纤维素的组合和/或聚乙烯吡咯烷酮。
[0148]
本发明的一个实施方案涉及一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和至少一种聚合物沉淀抑制剂和至少一种粘合剂或由它们组成,所述聚合物沉淀抑制剂选自包含以下成员或由以下成员组成的集合:聚乙烯醇(pva)、聚乙烯基己内酰胺-聚乙酸乙烯酯-聚乙二醇接枝共聚物l-羟丙基纤维素和羟丙基纤维素,所述粘合剂选自集合:l-羟丙基纤维素、羟丙基纤维素和羟丙基纤维素和/或聚乙烯吡咯烷酮。
[0149]
本发明的一个优选实施方案涉及一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和至少一种赋形剂,或由它们组成,其中所述至少一种赋形剂是粘合剂和/或至少一种赋形剂是聚合物沉淀抑制剂,且其中所述聚合物沉淀抑制剂是聚乙烯醇(pva)、聚乙烯基己内酰胺-聚乙酸乙烯酯-聚乙二醇接枝共聚物纤维素、纤维素衍生物、纤维素和纤维素衍生物的组合或纤维素衍生物的组合,且所述粘合剂是纤维素、纤维素衍生物、纤维素和衍生物的组合或纤维素衍生物的组合和/或聚维酮k25。
[0150]
本发明的一个优选实施方案涉及一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和至少一种粘合剂和/或至少一种聚合物沉淀抑制剂或由它们组成,且其中所述聚合物沉淀抑制剂是聚乙烯醇(pva)、聚乙烯基己内酰胺-聚乙酸乙烯酯-聚乙二醇接枝共聚物纤维素、纤维素衍生物、纤维素和衍生物的组合或纤维素衍生物的组合,且所述粘合剂是纤维素、纤维素衍生物、纤维素和衍生物的组合或纤维素衍生物的组合和/或聚维酮k25。
[0151]
本发明的另一个优选实施方案涉及一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐
和至少一种赋形剂,或由它们组成,其中所述至少一种赋形剂是粘合剂和/或至少一种赋形剂是聚合物沉淀抑制剂,其中所述聚合物沉淀抑制剂是聚乙烯醇(pva)、聚乙烯基己内酰胺-聚乙酸乙烯酯-聚乙二醇接枝共聚物l-羟丙基纤维素、羟丙基纤维素或l-羟丙基纤维素的组合,且其中所述粘合剂是l-羟丙基纤维素、羟丙基纤维素、l-羟丙基纤维素和羟丙基纤维素的组合和/或聚维酮k25。
[0152]
本发明的另一个优选实施方案涉及一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和至少一种粘合剂和/或至少一种聚合物沉淀抑制剂或由它们组成,其中所述聚合物沉淀抑制剂是聚乙烯醇(pva)、聚乙烯基己内酰胺-聚乙酸乙烯酯-聚乙二醇接枝共聚物l-羟丙基纤维素、羟丙基纤维素或l-羟丙基纤维素的组合,且其中所述粘合剂是l-羟丙基纤维素、羟丙基纤维素、l-羟丙基纤维素和羟丙基纤维素的组合和/或聚维酮k25。
[0153]
本发明的一个优选实施方案涉及一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和至少一种赋形剂,或由它们组成,其中所述至少一种赋形剂是粘合剂和/或至少一种赋形剂是聚合物沉淀抑制剂,其中所述聚合物沉淀抑制剂是聚乙烯醇(pva)、聚乙烯基己内酰胺-聚乙酸乙烯酯-聚乙二醇接枝共聚物l-羟丙基纤维素、羟丙基纤维素、或l-羟丙基纤维素和羟丙基纤维素的组合,其中所述粘合剂是聚维酮k25。
[0154]
本发明的一个优选实施方案涉及一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和至少一种粘合剂和/或至少一种聚合物沉淀抑制剂或由它们组成,其中所述聚合物沉淀抑制剂是聚乙烯醇(pva)、聚乙烯基己内酰胺-聚乙酸乙烯酯-聚乙二醇接枝共聚物l-羟丙基纤维素、羟丙基纤维素、或l-羟丙基纤维素和羟丙基纤维素的组合,其中所述粘合剂是聚维酮k25。
[0155]
在人中的药代动力学研究的积极数据证实了化合物(i)的高生物利用度。必须与之前已经进行的动物研究相比来理解在该背景下的高生物利用度。
[0156]
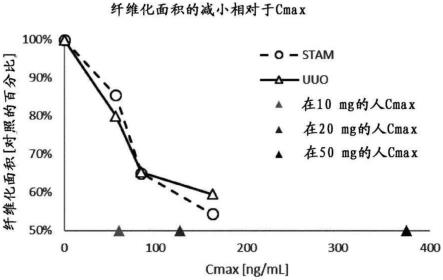
stam-和uuo小鼠模型研究证实,通过施用含有根据式(i)的化合物的全身性制剂实现了对肝脏和肾脏的抗纤维化作用。因此,全身施用的式(i)的药物在靶部位显示出高抗纤维化作用,并从而指示全身生物利用度。因此,含有式(i)的药物的口服制剂的施用在靶部位表现出高抗纤维化作用,并因此可以获得全身利用度(生物利用度),即药物在靶组织处被吸收。
[0157]
酸化剂的添加确保(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯在胃中的完全溶解,但在小肠中的ph从2增加到6,因此所述药物在它可以被小肠吸收之前可以沉淀。为了确保所述化合物在小肠中的完全溶解,根据本发明的制剂优选含有酸化剂和/或聚
合物沉淀抑制剂。此外,在实施例9中可以证实,在人体中仅20mg的剂量就足以达到血浆中的药物浓度,并从而达到全身利用度。
[0158]
药代动力学研究表明,(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯在小肠中被吸收,并需要20-50mg的低剂量才能在人体中达到治疗有效的药物浓度(实施例7、图6)。此外,用20mg的人剂量已经可以实现抗纤维化作用(实施例9和图9)。
[0159]
此外,没有观察到脱靶效应。如前所述,这尤其令人惊讶,因为实际上tg2在几乎所有细胞类型和细胞区室中普遍表达,它存在于细胞表面上并分泌到细胞外基质中,并存在于各种器官中,且因此可以设想最可能发生脱靶效应。
[0160]
因此,根据本发明的全身性制剂可以包含酸化剂和/或聚合物沉淀抑制剂。优选地,所述全身性制剂包含酸化剂和聚合物沉淀抑制剂。
[0161]
根据本发明的一个优选实施方案涉及一种全身性制剂,其含有本发明所述化合物或其对映异构体、溶剂化物、水合物或药学上可接受的盐和至少一种赋形剂,或由它们组成,其中至少一种赋形剂选自包含以下成员或由以下成员组成的集合:酸化剂和聚合物沉淀抑制剂。
[0162]
本发明的一个优选实施方案涉及一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、至少一种酸化剂和至少一种聚合物沉淀抑制剂或由它们组成。
[0163]
因此,本发明的一个优选实施方案涉及一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、至少一种选自己二酸、富马酸和戊二酸的酸化剂和至少一种聚合物沉淀抑制剂或由它们组成。
[0164]
因此,本发明的一个优选实施方案涉及一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、己二酸和至少一种聚合物沉淀抑制剂或由它们组成。
[0165]
根据本发明的一个优选实施方案涉及一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和至少一种赋形剂,或由它们组成,其中至少一种赋形剂选自包含以下成员或由以下成员组成的集合:酸化剂和聚合物沉淀抑制剂,且其中所述酸化剂选自包含以下成员或由以下成员组成的集合:己二酸、富马酸和戊二酸;且所述聚合物沉淀抑制剂选自包含以下成员或由以下成员组成的集合:聚乙烯醇(pva)、聚乙烯基己内酰胺-聚乙酸乙烯酯-聚乙二醇接枝共聚物纤维素和纤维素衍生物。
[0166]
根据本发明的一个优选实施方案涉及一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接
受的盐和至少一种赋形剂,或由它们组成,其中至少一种赋形剂选自包含以下成员或由以下成员组成的集合:酸化剂和聚合物沉淀抑制剂,且其中所述酸化剂是己二酸,且所述聚合物沉淀抑制剂选自包含以下成员或由以下成员组成的集合:聚乙烯醇(pva)、聚乙烯基己内酰胺-聚乙酸乙烯酯-聚乙二醇接枝共聚物纤维素和纤维素衍生物。
[0167]
根据本发明的一个优选实施方案涉及一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和至少一种酸化剂和至少一种聚合物沉淀抑制剂或由它们组成,其中所述酸化剂是己二酸,且所述聚合物沉淀抑制剂选自包含以下成员或由以下成员组成的集合:聚乙烯醇(pva)、聚乙烯基己内酰胺-聚乙酸乙烯酯-聚乙二醇接枝共聚物纤维素和纤维素衍生物。
[0168]
因此,本发明的一个优选实施方案涉及一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、至少一种酸化剂和至少一种聚合物沉淀抑制剂或由它们组成,所述聚合物沉淀抑制剂选自包含以下成员或由以下成员组成的集合:聚乙烯醇(pva)、聚乙烯基己内酰胺-聚乙酸乙烯酯-聚乙二醇接枝共聚物l-羟丙基纤维素和羟丙基纤维素。
[0169]
因此,本发明的一个优选实施方案涉及一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、己二酸和至少一种聚合物沉淀抑制剂或由它们组成,所述聚合物沉淀抑制剂选自包含以下成员或由以下成员组成的集合:聚乙烯醇(pva)、聚乙烯基己内酰胺-聚乙酸乙烯酯-聚乙二醇接枝共聚物l-羟丙基纤维素和羟丙基纤维素。
[0170]
根据本发明的一个优选实施方案涉及一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和至少一种赋形剂,或由它们组成,其中至少一种赋形剂选自包含以下成员或由以下成员组成的集合:酸化剂和聚合物沉淀抑制剂,且其中所述酸化剂是己二酸,且所述聚合物沉淀抑制剂是聚乙烯醇(pva)、聚乙烯基己内酰胺-聚乙酸乙烯酯-聚乙二醇接枝共聚物l-羟丙基纤维素、羟丙基纤维素、或l-羟丙基纤维素和羟丙基纤维素的组合。
[0171]
根据本发明的一个优选实施方案涉及一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和至少一种酸化剂和/或至少一种聚合物沉淀抑制剂或由它们组成,且其中所述酸化剂是己二酸,且所述聚合物沉淀抑制剂是聚乙烯醇(pva)、聚乙烯基己内酰胺-聚乙酸乙烯酯-聚乙二醇接枝共聚物l-羟丙基纤维素、羟丙基纤维素、或l-羟丙基纤
维素和羟丙基纤维素的组合。
[0172]
一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐,其中所述全身性制剂进一步包含至少一种赋形剂,其中至少一种赋形剂选自包含以下成员或由以下成员组成的集合:酸化剂和聚合物沉淀抑制剂,其中所述酸化剂选自由以下成员组成的集合:抗坏血酸、有机二羧酸诸如草酸、丙二酸、琥珀酸、戊二酸、酒石酸、富马酸、马来酸、苹果酸、己二酸或谷氨酸、和有机三羧酸诸如柠檬酸或柠檬酸氢钠。
[0173]
一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐,其中所述全身性制剂进一步包含至少一种赋形剂,其中至少一种赋形剂选自包含以下成员或由以下成员组成的集合:酸化剂和粘合剂,其中所述酸化剂选自由以下成员组成的集合:抗坏血酸、有机二羧酸诸如草酸、丙二酸、琥珀酸、戊二酸、酒石酸、富马酸、马来酸、苹果酸、己二酸或谷氨酸、和有机三羧酸诸如柠檬酸或柠檬酸氢钠,且其中所述粘合剂选自由以下成员组成的集合:糖,诸如蔗糖;多糖诸如黄原胶、瓜尔胶、角叉菜胶、从小麦、玉米、大米和马铃薯衍生出的淀粉,和从小麦、玉米、大米和马铃薯衍生出的预凝淀粉、淀粉羟乙酸钠;聚丙烯酸;天然树胶诸如金合欢胶、明胶和黄蓍胶;海藻的衍生物诸如海藻酸、海藻酸钠和海藻酸钙铵,纤维素或其衍生物诸如羟丙基纤维素、l-羟丙基纤维素、甲基纤维素和羧甲基纤维素钠和羟丙基甲基纤维素、或聚乙烯吡咯烷酮。
[0174]
根据本发明的全身性制剂可以包含酸化剂、聚合物沉淀抑制剂和/或粘合剂。
[0175]
根据本发明的一个实施方案涉及一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和至少一种赋形剂,或由它们组成,其中至少一种赋形剂选自包含以下成员或由以下成员组成的集合:酸化剂、聚合物沉淀抑制剂和粘合剂。
[0176]
根据本发明的一个优选实施方案涉及一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、至少一种酸化剂、至少一种酸化剂、至少一种聚合物沉淀抑制剂和至少一种粘合剂或由它们组成。
[0177]
根据本发明的一个更优选实施方案涉及一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、至少一种酸化剂、至少一种酸化剂、至少一种聚合物沉淀抑制剂和至少一种粘合剂或由它们组成,其中所述酸化剂是己二酸,所述聚合物沉淀抑制剂是聚乙烯醇(pva)、聚乙烯基己内酰胺-聚乙酸乙烯酯-聚乙二醇接枝共聚物l-羟丙基纤维素、羟丙基纤维素、或l-羟丙基纤维素和羟丙基纤维素的组合,且其中所述粘合剂是聚乙烯吡咯烷酮。
[0178]
根据本发明的全身性制剂可以包含崩解剂。
[0179]
因此,所述赋形剂可以是崩解剂。术语“崩解剂”表示添加到组合物中以支持制剂的崩解和活性药物成分的释放的材料。合适的崩解剂包括淀粉,可溶于冷水中的变性淀粉,诸如羧甲基淀粉钠;纤维素衍生物诸如甲基纤维素和羧甲基纤维素钠、微晶纤维素和交联微晶纤维素诸如交联羧甲基纤维素钠;海藻酸盐诸如海藻酸和海藻酸钠;粘土诸如皂粘土和泡沫混合物;泡腾化合物诸如柠檬酸、酒石酸、柠檬酸钠、柠檬酸氢二钠、柠檬酸单钠、碳酸氢钠和/或碳酸氢钾的组合,其在有水存在下反应以产生二氧化碳。优选地,所述崩解剂是交联羧甲基纤维素钠。
[0180]
微晶纤维素是一种纯化的、部分地解聚的纤维素,其作为由多孔颗粒组成的白色、无臭、无味、结晶性粉末存在。它通过用无机酸处理α-纤维素(从纤维性植物材料作为浆获得)而制成。几种不同等级是商购可得的,它们的差别在于它们的制造方法、粒度、水分、流动和其它物理性能。较大粒度等级通常提供较好的流动性能。低水分等级与水分敏感材料一起使用。较高密度等级具有改善的流动性。
[0181]
本文使用的微晶纤维素可以具有100μm的标称平均粒度和≤5.0%的水分含量。
[0182]
因此,本发明的一个实施方案涉及一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和至少一种赋形剂,或由它们组成,其中所述至少一种赋形剂是崩解剂。
[0183]
因此,本发明的一个实施方案涉及一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和至少一种崩解剂或由它们组成。
[0184]
根据本发明的全身性制剂可以包含酸化剂、聚合物沉淀抑制剂、粘合剂和/或崩解剂。
[0185]
根据本发明的一个实施方案涉及一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和至少一种赋形剂,或由它们组成,其中至少一种赋形剂选自包含以下成员或由以下成员组成的集合:酸化剂、聚合物沉淀抑制剂、粘合剂和崩解剂。
[0186]
根据本发明的全身性制剂可以包含润滑剂/助流剂。因此,所述赋形剂可以是润滑剂/助流剂。润滑剂/助流剂是这样的材料:其阻止结块、改善颗粒的流动特征,使得流动平滑和均匀,并减少直接接触的表面之间的摩擦,以使片剂、颗粒等从铸造模具或压制模具(在压制后)释放。润滑剂/助流剂包括苯甲酸钠、金属硬脂酸盐诸如硬脂酸镁、硬脂酸钙或硬脂酸钾、硬脂酸、高熔点蜡类、无机润滑剂/助流剂诸如二氧化硅和滑石粉和其它润滑剂/助流剂诸如油酸钠和聚乙二醇。优选地,所述润滑剂/助流剂是滑石粉或二氧化硅。由于润滑剂/助流剂必须存在于颗粒表面上以及颗粒与设备部件之间的事实,通常在封装或压制之前的最后一步中添加它们。
[0187]
因此,本发明的一个优选实施方案涉及一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪
唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和至少一种赋形剂,或由它们组成,其中所述至少一种赋形剂是润滑剂/助流剂。
[0188]
因此,本发明的一个优选实施方案涉及一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和至少一种润滑剂/助流剂或由它们组成。
[0189]
根据本发明的全身性制剂可以包含酸化剂、聚合物沉淀抑制剂、粘合剂和/或润滑剂/助流剂或由它们组成。
[0190]
根据本发明的一个优选实施方案涉及一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和至少一种赋形剂,或由它们组成,其中至少一种赋形剂选自包含以下成员或由以下成员组成的集合:酸化剂、聚合物沉淀抑制剂、粘合剂和润滑剂/助流剂。
[0191]
根据本发明的一个优选实施方案涉及一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和至少一种赋形剂,或由它们组成,其中至少一种赋形剂选自包含以下成员或由以下成员组成的集合:酸化剂、聚合物沉淀抑制剂、粘合剂和润滑剂/助流剂。
[0192]
根据本发明的全身性制剂可以包含酸化剂、聚合物沉淀抑制剂、粘合剂、崩解剂和/或润滑剂/助流剂或由它们组成。
[0193]
根据本发明的一个优选实施方案涉及一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和至少一种赋形剂,或由它们组成,其中至少一种赋形剂选自包含以下成员或由以下成员组成的集合:酸化剂、聚合物沉淀抑制剂、粘合剂、崩解剂和润滑剂/助流剂。
[0194]
此外,根据本发明的全身性制剂也可以包含稀释剂/填充剂/粘合剂、甜味剂、矫味剂、缓冲剂、抗氧化剂、乳化剂、增溶剂/润湿剂和/或防腐剂作为赋形剂。
[0195]
合适的稀释剂/填充剂/粘合剂是经常形成组合物或剂型的最大部分的物质。合适的稀释剂/填充剂/粘合剂包括糖诸如乳糖、蔗糖、甘露醇和山梨醇;从小麦、玉米、大米和马铃薯衍生出的淀粉;和纤维素诸如微晶纤维素、磷酸氢钙二水合物和硫酸钙。优选地,所述稀释剂/填充剂/粘合剂是纤维素和/或甘露醇。最优选地,所述稀释剂/填充剂/粘合剂是微晶纤维素和/或甘露醇。优选地,当所述制剂是片剂时,所述稀释剂/填充剂/粘合剂是微晶纤维素,且当所述制剂是胶囊剂时,所述稀释剂/填充剂/粘合剂是甘露醇。
[0196]
甘露醇的添加进一步增加颗粒的孔隙率并因此增加润湿性。因此,本发明的一个优选实施方案涉及一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和至少一种赋形剂,或由它们组成,其中所述至少一种赋形剂是稀释剂/填充剂/粘合剂。
[0197]
根据本发明的全身性制剂可以包含酸化剂、聚合物沉淀抑制剂、粘合剂、崩解剂、
润滑剂/助流剂和/或稀释剂/填充剂/粘合剂或由它们组成。
[0198]
本发明的一个实施方案涉及一种制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和至少一种赋形剂,或由它们组成,其中至少一种赋形剂选自包含以下成员或由以下成员组成的集合:酸化剂、聚合物沉淀抑制剂、粘合剂、崩解剂、润滑剂/助流剂和稀释剂/填充剂/粘合剂。
[0199]
本发明的一个实施方案涉及一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、至少一种酸化剂、至少一种聚合物沉淀抑制剂、至少一种粘合剂、至少一种崩解剂、至少一种润滑剂/助流剂和至少一种稀释剂/填充剂/粘合剂或由它们组成。
[0200]
以适合于口服应用的可施用形式提供所述优选制剂,诸如片剂如未包衣片剂、包衣片剂、泡腾片剂、可溶性片剂、咀嚼片剂、口服冻干粉剂、锭剂、软锭剂、压缩锭剂、舌下片剂、含服片剂、颗粒、泡腾颗粒和胶囊剂。更优选地,所述口服制剂是片剂或胶囊剂。未包衣和包衣片剂、以及硬或软胶囊剂是最优选的药物制剂。
[0201]
本发明的一个实施方案涉及一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐,其中所述全身性制剂是片剂、胶囊剂、粉剂或颗粒剂。
[0202]
根据本发明的全身性制剂可以包含其它成分诸如不可避免的杂质、用于胶囊剂的成分,包括胶囊剂的着色剂。在片剂中也可以存在着色剂作为其它成分。
[0203]
此外,用于包衣片剂的组分也被术语“其它成分”包括。
[0204]
胶囊剂的外壳可以包含着色剂。本文中使用的术语“着色剂”包括颜料诸如白色颜料。所述着色剂尤其可以是氧化铁、特别是氧化铁(iii)、氧化铁(ii、iii)或水合的氧化铁、或二氧化钛。
[0205]“片剂”是指含有至少一种活性药物成分和合适的赋形剂的压缩固体剂型。通过压制经本领域技术人员已知的湿法制粒、干法制粒或压实获得的混合物或颗粒,可以生产片剂。
[0206]
术语“胶囊”表示由甲基纤维素、聚乙烯醇或明胶或变性明胶或淀粉组成的特殊容器或壳,在其中可以包封活性剂。通常,硬壳胶囊由羟丙基甲基纤维素或由具有较高凝胶强度的猪骨和皮明胶的混合物制备。胶囊剂的壳可以含有少量的着色剂、遮光剂、软化剂和防腐剂。“软壳胶囊”含有明胶作为基本聚合物、较高量的一种或多种软化剂诸如甘油或山梨醇以及水。一般而言,软化剂的量是胶囊壳的20-30重量%,明胶的量是胶囊壳的40-45重量%,且水的量是胶囊壳的30-35重量%。在胶囊干燥后,水的量是胶囊壳的7-8重量%。
[0207]
胶囊壳可以包含明胶、羟丙基甲基纤维素(hmpc)、多糖诸如淀粉和角叉菜胶;和/或合成的聚合物诸如聚乙烯醇的共聚合物(compolymers)。此外,胶囊的壳可以包含着色剂。本文中使用的术语“着色剂”包括颜料诸如白色颜料。所述着色剂尤其可以是氧化铁、特别是氧化铁(iii)、氧化铁(ii、iii)或水合的氧化铁、二氧化钛、天然染料、偶氮(azo)和苍耳烷化合物。此外,胶囊壳可以包含防腐剂诸如对羟基苯甲酸酯或改善风味的物质诸如乙
香草醛。另外,胶囊壳可以包含表面活性剂诸如月桂基硫酸钠。
[0208]
用于组合物的“粉末”表示含有活性组分和合适赋形剂的粉末混合物/掺合物,其可以在使用前悬浮在水或汁液中。球形颗粒也表示弹丸或珠子。
[0209]“颗粒”表示干燥和固体颗粒。每个颗粒代表粉末颗粒的附聚物。
[0210]
当用包覆或包埋方法处理药物颗粒时,包衣方法与剂型本身有关。片剂、糖衣丸的中心或胶囊被包衣层包裹,其中赋形剂是诸如纤维素的衍生物、纤维素醚诸如羟丙基甲基纤维素(hmpc)、合成的聚合物、紫胶、玉米蛋白玉蜀黍蛋白或其它多糖以及甲基丙烯酸和甲基丙烯酸甲酯的阴离子共聚物。所述包衣可以进一步包含着色剂诸如二氧化钛、氧化铁(iii)、氧化铁(ii、iii)或水合的氧化铁、乳糖一水合物和/或巴西棕榈蜡。胶囊也可以包衣。
[0211]
持续释放型制剂在现有技术中已知用于提供任何一种或多种组分或活性组分的受控释放速率,以优化治疗效果,即抑制活性等。保证药理学最佳浓度在一定时间内在单次剂量的作用期以上。用于持续释放的合适剂型包括分层片剂,其含有具有不同降解速率的多个层或浸渍有活性组分的控释聚合物基质,并且呈含有这样的浸渍或包封的多孔聚合物基质的片剂或胶囊剂的形式。持续释放型制剂会阻碍化合物的快速释放。在本文中,希望在施用后向靶部位快速地释放高浓度的药物。因此,为了本发明的目的,持续释放型制剂不是优选的并且实际上应该避免,因为初步结果指示,这样的制剂不可提供根据本发明的所需的高药物浓度。
[0212]
根据本发明的全身性制剂可以呈胶囊剂或片剂的形式,即活性剂和赋形剂可以填充在胶囊中。根据本发明的一个实施方案是全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐或由它们组成,其中所述全身性制剂是胶囊剂或片剂的形式。
[0213]
根据本发明的一个优选实施方案是全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和至少一种赋形剂,或由它们组成,其中至少一种赋形剂选自包含以下成员或由以下成员组成的集合:酸化剂和聚合物沉淀抑制剂,其中所述全身性制剂是胶囊剂或片剂的形式。
[0214]
根据本发明的一个优选实施方案是全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、至少一种酸化剂和至少一种聚合物沉淀抑制剂或由它们组成,其中所述全身性制剂是胶囊剂或片剂的形式。
[0215]
根据本发明的另一个优选实施方案是全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和至少一种赋形剂,或由它们组成,其中至少一种赋形剂选自包含以下成员或由以下成员组成的集合:酸化剂、聚合物沉淀抑制剂和粘合剂,其中所述全身性制剂是胶囊剂或片剂的形式。
[0216]
根据本发明的另一个优选实施方案是全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、至少一种酸化剂、至少一种聚合物沉淀抑制剂和至少一种粘合剂或由它们组成,其中所述全身性制剂是胶囊剂或片剂的形式。
[0217]
根据本发明的另一个优选实施方案涉及一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和至少一种赋形剂,或由它们组成,其中至少一种赋形剂选自包含以下成员或由以下成员组成的集合:酸化剂、聚合物沉淀抑制剂、粘合剂、崩解剂和润滑剂/助流剂,其中所述全身性制剂是胶囊剂或片剂的形式。
[0218]
根据本发明的另一个优选实施方案涉及一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、至少一种酸化剂、至少一种聚合物沉淀抑制剂、至少一种粘合剂、至少一种崩解剂和至少一种润滑剂/助流剂或由它们组成,其中所述全身性制剂是胶囊剂或片剂的形式。
[0219]
根据本发明的另一个优选实施方案涉及一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和至少一种赋形剂,或由它们组成,其中至少一种赋形剂选自包含以下成员或由以下成员组成的集合:酸化剂、聚合物沉淀抑制剂、稀释剂/填充剂/粘合剂、崩解剂、润滑剂/助流剂和稀释剂/填充剂/粘合剂,其中所述全身性制剂是胶囊剂或片剂的形式。
[0220]
根据本发明的另一个优选实施方案涉及一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、至少一种酸化剂、至少一种聚合物沉淀抑制剂、至少一种粘合剂、至少一种崩解剂、至少一种润滑剂/助流剂和至少一种稀释剂/填充剂/粘合剂或由它们组成,其中所述全身性制剂是胶囊剂或片剂的形式。
[0221]
优选的药物制剂是用于口服施用。因此,优选的药物制剂是用于口服施用的肠内或胃肠外制剂形式的全身性制剂。所以,特别地胶囊剂和片剂是用于口服施用的最优选肠内或胃肠外制剂,且特别地这些胶囊剂和片剂确保(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯的快速释放,并且由此确保高药物浓度。因此,持续释放制剂不是合适的并且实际上不应用于本发明的目的。
[0222]
此外,含有己二酸的用于口服施用的药物制剂是优选的。更优选的是含有己二酸的用于口服施用的肠内或胃肠外制剂形式的全身性制剂。最优选的是含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和己二酸的用于口服施用的胶囊剂和片剂。
[0223]
此外,为了进一步改善制剂的性能,可以调整特定psd(粒度分布)和/或psr(粒度范围)。
[0224]
因此,根据本发明的一个实施方案涉及一种全身性制剂,其含有式(i)的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯:
[0225][0226]
或式(i)的溶剂化物、水合物或药学上可接受的盐,其中(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯颗粒具有从0.1至100μm的粒度范围。
[0227]
进一步更优选的是,(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐的粒度是在0.1μm至100μm的范围内,优选地在0.5μm至50μm的范围内,且更优选地在1.0μm至20μm的范围内。因此,(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐的粒度范围(psr)是从0.1μm至100μm、从0.5μm至50μm或从1.0μm至20μm。优选地,根据式(i)的药物的粒度≤10μm。
[0228]
根据本发明的另一个优选实施方案是一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、己二酸和l-羟丙基纤维素或由它们组成,其中(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯颗粒具有从0.1μm至100μm的粒度范围。
[0229]
因此,根据本发明的一个实施方案涉及一种全身性制剂,其含有式(i)的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯:
[0230]
[0231]
或式(i)的对映异构体、溶剂化物、水合物或药学上可接受的盐,其中(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯颗粒具有由d(0.95)≤25μm定义的粒度分布,其中(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐优选地被微粉化。
[0232]
此外,优选的是,(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐的粒度分布的特征在于从0.1至5μm的d(0.1)、从0.3至10μm的d(0.5)、从3至25μm的d(0.95),更优选从0.2至3μm的d(0.1)、从0.4至7.5μm的d(0.5)和从2至15μm的d(0.95),且最优选从0.3至3μm的d(0.1)、从0.5至5μm的d(0.5)和从1至10μm的d(0.95)。
[0233]
通过激光衍射(malvern分析,样品分散在正己烷和脱水山梨糖醇单油酸酯中)测量粒度分布。因此,激光根据粒度被散射。从依赖于角度的散射光强度产生衍射图样,可以计算粒度。
[0234]
参数d(0.1)表示,当通过激光衍射(malvern分析,样品分散在正己烷和脱水山梨糖醇单油酸酯中)分析时,样品中颗粒的总体积的10%由具有小于指定值或值范围的直径的颗粒构成时的直径。因此,d(0.1)=0.1至5μm是指,限定样品中最小颗粒的10%的粒度范围的上限是在0.1μm至5μm之间。因此,总颗粒的10%具有不超过d(0.1)的粒度,在该情况下意味着,它们具有0.1μm至5μm的最大尺寸。
[0235]
相应地,参数d(0.5)表示,当通过激光衍射(malvern分析,样品分散在正己烷和脱水山梨糖醇单油酸酯中)分析时,样品中颗粒的总体积的50%由具有小于指定值或值范围的直径的颗粒构成时的直径。因此,d(0.5)=0.3至10μm是指,限定样品中最小颗粒的50%的粒度范围的上限是在0.3μm至10μm之间。因此,总颗粒的50%具有不超过d(0.5)的粒度,在该情况下意味着,它们具有0.3μm至10μm的最大尺寸。
[0236]
相应地,参数d(0.95)表示,当通过激光衍射(malvern分析,样品分散在正己烷和脱水山梨糖醇单油酸酯中)分析时,样品中颗粒的总体积的95%由具有小于指定值或值范围的直径的颗粒构成时的直径。因此,d(0.95)=3-25μm是指,限定样品中最小颗粒的95%的粒度范围的上限是在3μm至25μm之间。因此,总颗粒的95%具有不超过d(0.95)的粒度,在该情况下意味着,它们具有3μm至25μm的最大尺寸。
[0237]
本发明的另一个实施方案涉及一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、己二酸和l-羟丙基纤维素,其中(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯颗粒具有由d(0.95)≤25μm定义的粒度分布。
[0238]
本发明的一个优选实施方案涉及一种全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐,
(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯:
[0245][0246]
或式(i)的对映异构体、溶剂化物、水合物或药学上可接受的盐,其中(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯颗粒具有从0.1至100μm的粒度范围和由d(0.95)≤25μm限定的粒度分布。
[0247]
因此,优选的是全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐,其中所述(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐呈颗粒的形式,所述颗粒具有由d(0.95)≤25μm限定的粒度分布。
[0248]
根据本发明的一个优选实施方案是一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、己二酸和l-羟丙基纤维素或由它们组成,其中(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯颗粒具有从0.1至100μm的粒度范围和由d(0.95)≤25μm限定的粒度分布。
[0249]
根据本发明的一个更优选实施方案是一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、己二酸、l-羟丙基纤维素、羟丙基纤维素、甘露醇、交联羧甲基纤维素钠和滑石粉或由它们组成,其中(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯颗粒具有从0.1至100μm的粒度范围和由d(0.95)≤25μm限定的粒度分布。
[0250]
根据本发明的一个特别优选的实施方案是一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、己二酸、l-羟丙基纤维素、羟丙基纤维素、甘露醇、交联羧甲基纤维素钠、滑石粉、明胶和二氧化钛或由它们组成,其中(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯颗粒具有从0.1至100μm的粒度范围和由d(0.95)≤25μm限定的粒度分布。
[0251]
本发明的另一个特别优选的实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、己二酸、l-羟丙基纤维素、聚维酮k25、交联羧甲基纤维素钠、微晶纤维素和二氧化硅或由它们组成,其中(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯颗粒具有从0.1至100μm的粒度范围和由d(0.95)≤25μm限定的粒度分布。
[0252]
所述全身性制剂可以含有以下量的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或对映异构体、溶剂化物、水合物或药学上可接受的盐:每个制剂至少0.01mg,优选至少0.1mg,更优选至少0.5mg,甚至更优选至少1mg,甚至更优选至少2mg,甚至更优选至少3mg,甚至更优选至少4mg,甚至更优选至少5mg,甚至更优选0.01mg至1000mg,甚至更优选0.05mg至900mg,甚至更优选0.10mg至800mg,更优选0.2mg至700mg,更优选0.3mg至600mg,更优选0.4mg至500mg,更优选0.5mg至500mg,更优选0.6mg至450mg,更优选0.7mg至400mg,更优选0.8mg至375mg,更优选0.9mg至350mg,更优选1.0mg至300mg,更优选1.25mg至300mg,更优选1.5mg至275mg,更优选1.75mg至250mg,更优选2.0mg至225mg,mg,更优选2.25至220mg,更优选2.5至220mg,更优选2.75mg至215mg,更优选3.0mg至210mg,更优选3.75mg至205mg,更优选4.0mg至205mg,4.5mg至200mg,最优选5mg至200mg。
[0253]
所述全身性制剂可以含有以下量的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或对映异构体、溶剂化物、水合物或药学上可接受的盐、溶剂化物或水合物:0.1重量%至99重量%,优选0.2重量%至90重量%,更优选0.3重量%至85重量%,甚至更优选0.4重量%至80重量%,甚至更优选0.5重量%至75重量%,甚至更优选0.6重量%至70重量%,甚至更优选0.7重量%至65重量%,甚至更优选0.8重量%至60重量%,甚至更优选0.9重量%至55重量%,甚至更优选1重量%至50重量%,甚至更优选1重量%至45重量%,甚至更优选1.25重量%至45重量%,甚至更优选1.5重量%至40重量%,甚至更优选1.75重量%至35重量%,甚至更优选2重量%至34重量%,甚至更优选2.25重量%至33重量%,甚至更优选2.5重量%至32重量%,且最优选2.5重量%至31重量%,甚至更优选2.5重量%至30.5重量%,且甚至更优选2.6重量%至30.3重量%,甚至更优选3重量%至30重量%,甚至更优选3.5重量%至29重量%,甚至更优选4重量%至28重量%,甚至更优选4重量%至27重量%,甚至更优选4.5重量%至27重量%,且最优选5重量%至27重量%。“重量%”(重量百分比)表示在组合物中的重量百分比。
[0254]
所述酸化剂的量的范围可以为从0.1重量%至80重量%,优选从0.5重量%至77.5重量%,更优选从1重量%至75重量%,更优选从1.5重量%至72.5重量%,更优选从2重量%至70重量%,更优选从2.5重量%至62.5重量%,更优选从3重量%至57.5重量%,更优选从3.5重量%至55重量%,甚至更优选从4重量%至55重量%,甚至更优选从4.5重量%至55重量%,甚至更优选从5重量%至54重量%,甚至更优选从5.5重量%至53重量%,甚至更优选从6重量%至52重量%,甚至更优选从6.5重量%至51重量%,甚至更优选从7重量%至50重量%,甚至更优选从8重量%至49重量%,甚至更优选从8.5重量%至49重量%,且最优
选从9重量%至49重量%。
[0255]
此外,所述酸化剂的量的范围可以为从1.00mg至500mg,更优选从1.25mg 495mg,更优选从1.50mg至490mg,更优选从1.75mg至485mg,更优选从2.00mg至480mg,更优选从2.25mg至475mg,更优选从2.50mg至470mg,更优选从3.0mg至465mg,更优选从3.25mg至460mg,更优选从3.5mg至455mg,甚至更优选从3.75mg至450mg,甚至更优选从4.00mg至445mg,甚至更优选从4.25mg至440mg,更优选从4.5mg至435mg,更优选从4.75mg至430mg,更优选从5.0mg至425mg,更优选从5.25mg至420mg,更优选从5.5mg至415mg,更优选从5.75mg至410mg,更优选从6.0mg至410mg,更优选从6.25mg至405mg,更优选从6.5mg至400mg,更优选从6.75mg至395mg,更优选从7.0mg至390mg,更优选从7.5mg至390mg,更优选从7.75mg至385mg,更优选从8.0mg至380mg,更优选从8.5mg至375mg,更优选从9mg至370mg,更优选从9mg至365mg,更优选从9mg至360mg,更优选从9mg至350mg,更优选从9mg至325mg,更优选从9mg至300mg,更优选从9mg至250mg,更优选从9mg至200mg,且最优选从9mg至180mg。
[0256]
此外,所述酸化剂相对于(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐的质量的质量比的范围可以为从15至0.1质量/质量,优选从14.5至0.2质量/质量,更优选从14.0至0.3质量/质量,更优选从13.5至0.4质量/质量,更优选从13.0至0.5质量/质量,更优选从12.5至0.6质量/质量,更优选从12.0至0.7质量/质量,更优选从11.75至0.8质量/质量,更优选从11.5至0.9质量/质量,更优选从11.5至1.0质量/质量,更优选从11.5至1.1质量/质量,更优选从11.5至1.2质量/质量,更优选从11.5至1.3质量/质量,更优选从11.5至1.4质量/质量,更优选从11.5至1.5质量/质量,更优选从11.5至1.6质量/质量,更优选从11.5至1.7质量/质量,且最优选地优选从11.5至1.8质量/质量。
[0257]
所述聚合物沉淀抑制剂的量可以从0.1重量%至40重量%变化,优选0.5重量%至39重量%,更优选1重量%至38重量%,更优选1.25重量%至38重量%,更优选1.5重量%至37重量%,更优选1.75重量%至36重量%,更优选2重量%至35重量%,更优选1.5重量%至34重量%,更优选1.6重量%至33重量%,更优选1.7重量%至32重量%,更优选1.8重量%至31重量%,更优选3.5重量%至30重量%,更优选4重量%至29重量%,更优选4.5重量%至28.5重量%,最优选5重量%至28.5重量%。
[0258]
此外,所述聚合物沉淀抑制剂的量的范围可以为从1mg至100mg,优选从1.5mg至95mg,更优选从2mg至92.5mg,更优选2.5mg至90mg,更优选3mg至87.5mg,更优选3.5mg至85mg,更优选4mg至82.5mg,更优选4.5mg至80mg,更优选5mg至77.5mg,更优选5.5mg至75mg,6mg至72.5mg,更优选6.5mg至70mg,更优选7mg至65mg,更优选7.5mg至62.5mg,更优选8mg至60mg,甚至更优选从8.5mg至57.5mg,甚至更优选从9mg至55mg,甚至更优选从9.5mg至52.5mg,甚至更优选从9.75mg至52.5mg,且最优选从10mg至50mg。
[0259]
此外,所述聚合物沉淀抑制剂相对于(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐的质量的质量比的范围可以为从0.05至10质量/质量,优选从0.06至9.5质量/质量,更优选从0.07至9.00质量/质量,更优选从0.08至8.50质量/质量,更优选从0.09至8.00质量/质量,更优选从0.1至7.5
质量/质量,更优选从0.11至7.25质量/质量,更优选从0.12至7质量/质量,更优选从0.13至6.75质量/质量,更优选从0.14至6.5质量/质量,更优选从0.15至6.25质量/质量,甚至更优选从0.16至6质量/质量,甚至更优选从0.17至5.75质量/质量,甚至更优选从0.18至5.5质量/质量,甚至更优选从0.19至5.25质量/质量,且最优选从0.20至5质量/质量。
[0260]
所述粘合剂的量可以从0重量%至40重量%变化,优选从0重量%至35重量%,更优选从0重量%至30重量%,更优选从0重量%至25重量%,更优选从0重量%至20重量%,更优选从0重量%至15重量%,更优选从0重量%至12重量%,且最优选从0重量%至8.5重量%。
[0261]
此外,所述粘合剂的量的范围可以为从1.00mg至100mg,优选从1.50mg至95mg,更优选从2.00mg至92.5mg,更优选2.50mg至90mg,更优选3.00mg至87.5mg,更优选3.50mg至85mg,更优选4.00mg至82.5mg,更优选4.50mg至80mg,更优选5.00mg至77.5mg,更优选5.50mg至75mg,6.00mg至72.5mg,更优选6.50mg至70mg,更优选7.00mg至65mg,更优选7.50mg至62.5mg,更优选8.00mg至60mg,甚至更优选从8.50mg至57.5mg,甚至更优选从9.00mg至55.0mg,甚至更优选从9.50mg至52.5mg,甚至更优选从9.75mg至52.5mg,且最优选从10mg至50mg。
[0262]
此外,所述粘合剂相对于(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐的质量的质量比的范围可以为从0-10质量/质量,优选从0.05至9.5质量/质量,更优选从0.06至9.00质量/质量,更优选从0.07至8.50质量/质量,更优选从0.08至8.00质量/质量,更优选从0.09至7.5质量/质量,更优选从0.1至7.25质量/质量,更优选从0.11至7.00质量/质量,更优选从0.12至6.75质量/质量,更优选从0.13至6.50质量/质量,更优选从0.14至6.25质量/质量,甚至更优选从0.15至6.00质量/质量,甚至更优选从0.16至5.75质量/质量,甚至更优选从0.17至5.50质量/质量,甚至更优选从0.18至5.25质量/质量,甚至更优选从0.19至5.5质量/质量,甚至更优选从0.20至5质量/质量,甚至更优选从0.20至4.5质量/质量,甚至更优选从0.20至4质量/质量,甚至更优选从0.20至3.5质量/质量,甚至更优选从0.20至3质量/质量,甚至更优选从0.20至2.5质量/质量,且甚至更优选从0.20至2质量/质量。
[0263]
所述崩解剂的量可以从0.1重量%至40重量%变化,优选从1重量%至35重量%,甚至更优选从2重量%至30重量%,甚至更优选从2.5重量%至29重量%,甚至更优选从3.0重量%至28重量%,甚至更优选从3.5重量%至27重量%,且最优选从3.5重量%至26.5重量%。
[0264]
另外,所述崩解剂的量可以从0.1mg至150mg变化,优选从0.50mg至145mg,更优选从0.75mg至140mg,更优选从1.00mg至135mg,更优选从1.25mg至130mg,更优选从1.50mg至125mg,更优选从1.75mg至120mg,更优选从2.00mg至115mg,更优选从2.25mg至110mg,更优选从2.50mg至105mg,更优选从2.75mg至100mg,更优选从3.00mg至95mg,甚至更优选从3.25mg至90mg,甚至更优选从3.50mg至85mg,甚至更优选从3.75mg至80mg,甚至更优选从4.00mg至75mg,甚至更优选从4.25mg至70mg,甚至更优选4.50mg至65mg,甚至更优选4.75mg至60mg,甚至更优选5.00mg至55mg,甚至更优选5.50mg至50mg,甚至更优选6.00mg至45mg,甚至更优选6.50mg至42.5mg,甚至更优选7.00mg至40mg,甚至更优选7.50mg至40mg,甚至更
优选8.00mg至40mg,甚至更优选8.50mg至40mg,甚至更优选9.00mg至40mg,甚至更优选9.50mg至40mg,且最优选从10mg至40mg。
[0265]
此外,所述崩解剂相对于(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐的质量的质量比的范围可以为从0.05至12质量/质量,优选从0.06至11.5质量/质量,更优选从0.07至11质量/质量,更优选从0.08至10.5质量/质量,更优选从0.09至10质量/质量,更优选从0.1至9.5质量/质量,更优选从0.11至9质量/质量,更优选从0.12至8.5质量/质量,更优选从0.13至8质量/质量,更优选从0.14至7.5质量/质量,更优选从0.15至7质量/质量,甚至更优选从0.16至6.5质量/质量,甚至更优选从0.17至5.5质量/质量,甚至更优选从0.18至5质量/质量,甚至更优选从0.19至5质量/质量,且最优选0.2至5质量/质量。
[0266]
所述润滑剂/助流剂的量的范围可以为从0.1重量%至10重量%,优选从0.25重量%至9.5重量%,更优选从0.5重量%至9重量%,更优选从0.75重量%至8.5重量%,更优选从1重量%至8重量%,更优选从1.25重量%至7.5重量%,更优选从1.5重量%至7重量%,且甚至更优选1.5重量%至6.5重量%。
[0267]
此外,所述润滑剂/助流剂的量的范围可以为从0.01mg至100mg,优选从0.05mg至95mg,更优选从0.1mg至90mg,更优选从0.3mg至85mg,更优选从0.4mg至80mg,更优选从0.5mg至0.6mg,更优选从0.7mg至70mg,更优选从0.8mg至65mg,更优选从0.9mg至60mg,更优选从1mg至55mg,更优选从1.1mg至50mg,更优选从1.2mg至45mg,更优选从1.3mg至40mg,更优选从1.4mg至35mg,更优选从1.5mg至30mg,更优选从1.6mg至25mg,更优选从1.7mg至20mg,甚至更优选从1.8mg至20mg,甚至更优选从1.9mg至20mg,甚至优选从2mg至20mg,甚至优选从3mg至20mg,甚至优选从4mg至20mg,且最优选地甚至优选从5mg至20mg。
[0268]
此外,所述润滑剂/助流剂相对于(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐的质量的质量比的范围可以为从0.05至2质量/质量,优选从0.06至1.8质量/质量,更优选从0.07至1.6质量/质量,0.08至1.4质量/质量,更优选从0.09至1.3质量/质量,且最优选从0.1至1.2质量/质量。
[0269]
所述组合物中稀释剂/填充剂/粘合剂的量的范围可以为从0重量%至50%重量%,优选从1重量%至47.5%重量%,更优选从1.5重量%至45%重量%,更优选从2重量%至42.5%重量%,更优选从2.5至40重量%,更优选从3重量%至38%重量%,更优选3.5重量%至38重量%,更优选4重量%至38重量%,更优选至重量%,更优选4.5重量%至38重量%,且甚至更优选5重量%至38重量%
[0270]
此外,所述稀释剂/填充剂/粘合剂的量的范围可以为从1mg至290mg,优选从2mg至280mg,更优选从3mg至270mg,甚至更优选从4mg至260mg,甚至更优选从5mg至250mg,甚至更优选从6mg至240mg,甚至更优选从7mg至230mg,甚至更优选从8mg至220mg,甚至更优选从9mg至210mg,甚至更优选从10mg至200mg,甚至更优选从11mg至190mg,甚至更优选从12mg至180mg,甚至更优选从13mg至170mg,甚至更优选从14mg至160mg,甚至更优选从15mg至150mg,甚至更优选从16mg至140mg,甚至更优选从17mg至130mg,甚至更优选从18mg至120mg,甚至更优选从19mg至110mg,甚至更优选从19mg至100mg,甚至更优选从20mg至90mg,
更优选从21mg至80mg,甚至更优选从22mg至70mg,甚至更优选从23mg至60mg,甚至更优选从24mg至55mg,且最优选25mg至50mg。
[0271]
此外,所述稀释剂/填充剂/粘合剂相对于(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐的质量的质量比的范围可以为从0质量/质量至20质量/质量,更优选0.01质量/质量至17.5质量/质量,更优选0.05质量/质量至15质量/质量,更优选0.1质量/质量至0.125质量/质量,更优选0.15质量/质量至10质量/质量,更优选0.175质量/质量至7.5质量/质量,更优选0.2质量/质量至6,更优选0.2质量/质量至5.5,更优选0.2质量/质量至5质量/质量。
[0272]
相对于剂型,其它成分的量的范围可以为从5重量%至60重量%,优选从6重量%至57.5重量%,更优选7重量%至55重量%,甚至更优选从8重量%至52.5重量%,甚至更优选从9重量%至51重量%,且最优选10重量%至50重量%。
[0273]
另外,其它成分的量的范围可以为从50mg至200mg,优选从55mg至190mg,更优选从60mg至180mg,更优选从65mg至170mg,更优选从70mg至160mg,更优选从75mg至150mg,更优选从80mg至140mg,更优选从90mg至130mg,甚至更优选从90mg至120mg,甚至更优选从90mg至110mg,且最优选从90mg至100mg。
[0274]
此外,其它成分相对于(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐的质量的质量比的范围可以为从0-30质量/质量,优选从0.2至27.5质量/质量,更优选从0.3至25质量/质量,更优选从0.35至22.5质量/质量,甚至更优选从0.4至21质量/质量,且最优选从0.45至20质量/质量。
[0275]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐或由它们组成。
[0276]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐或由它们组成。
[0277]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐或由它们组成。
[0278]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和1重量%至75重量%的酸化剂或由它们组成。
[0279]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨
基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和3重量%至75重量%的酸化剂或由它们组成。
[0280]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和4.5重量%至55重量%的酸化剂或由它们组成。
[0281]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和1重量%至75重量%的酸化剂或由它们组成。
[0282]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和3重量%至75重量%的酸化剂或由它们组成。
[0283]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和4.5重量%至55重量%的酸化剂或由它们组成。
[0284]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和1重量%至75重量%的酸化剂或由它们组成。
[0285]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和3重量%至75重量%的酸化剂或由它们组成。
[0286]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和4.5重量%至55重量%的酸化剂或由它们组成。
[0287]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和1重量%至75重量%的酸化剂或由它们组成。
[0288]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和3重量%至75重量%的酸化剂或由它们组成。
[0289]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的
(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和4.5重量%至55重量%的酸化剂或由它们组成。
[0290]
本发明的一个优选实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和1重量%至75重量%的己二酸或由它们组成。
[0291]
本发明的一个优选实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和3重量%至75重量%的己二酸或由它们组成。
[0292]
本发明的一个优选实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和4.5重量%至55重量%的己二酸或由它们组成。
[0293]
本发明的一个更优选实施方案涉及一种全身性制剂,其包含0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和1重量%至75重量%的己二酸或由它们组成。
[0294]
本发明的一个更优选实施方案涉及一种全身性制剂,其包含0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和3重量%至75重量%的己二酸或由它们组成。
[0295]
本发明的一个更优选实施方案涉及一种全身性制剂,其包含0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和4.5重量%至55重量%的己二酸或由它们组成。
[0296]
本发明的一个优选实施方案涉及一种全身性制剂,其包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和1重量%至75重量%的己二酸或由它们组成。
[0297]
本发明的一个优选实施方案涉及一种全身性制剂,其包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和3重量%至75重量%的己二酸或由它们组成。
[0298]
本发明的一个优选实施方案涉及一种全身性制剂,其包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和4.5重量%至55重量%的己二酸或由它们组成。
[0299]
本发明的一个优选实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和1重量%至75重量%的己二酸或由它们组成。
[0300]
本发明的一个优选实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和3重量%至75重量%的己二酸或由它们组成。
[0301]
本发明的一个优选实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和4.5重量%至55重量%的己二酸或由它们组成。
[0302]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和0.1重量%至40重量%的聚合物沉淀抑制剂或由它们组成。
[0303]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和2重量%至35重量%的聚合物沉淀抑制剂或由它们组成。
[0304]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和3.5重量%至30重量%的聚合物沉淀抑制剂或由它们组成。
[0305]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和0.1重量%至40重量%的聚合物沉淀抑制剂或由它们组成。
[0306]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和3.5重量%至35重量%的聚合物沉淀抑制剂或由它们组成。
[0307]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和2重量%至30重量%的聚合物沉淀抑制剂或由它们组成。
[0308]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或
药学上可接受的盐和0.1重量%至40重量%的聚合物沉淀抑制剂或由它们组成。
[0309]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和2重量%至35重量%的聚合物沉淀抑制剂或由它们组成。
[0310]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和3.5重量%至30重量%的聚合物沉淀抑制剂或由它们组成。
[0311]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和0.1重量%至40重量%的聚合物沉淀抑制剂或由它们组成。
[0312]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和2重量%至35重量%的聚合物沉淀抑制剂或由它们组成。
[0313]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和3.5重量%至30重量%的聚合物沉淀抑制剂或由它们组成。
[0314]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和0.1重量%至40重量%的l-羟丙基纤维素和/或羟丙基纤维素或由它们组成。
[0315]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和2重量%至35重量%的l-羟丙基纤维素和/或羟丙基纤维素或由它们组成。
[0316]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和3.5重量%至30重量%的l-羟丙基纤维素和/或羟丙基纤维素或由它们组成。
[0317]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和0.1重量%至40重量%的l-羟丙基纤维素和/或羟丙基纤维素或由它们组成。
[0318]
本发明的一个优选实施方案涉及一种全身性制剂,其包含0.1重量%至80重量%
的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和2重量%至35重量%的l-羟丙基纤维素和/或羟丙基纤维素或由它们组成。
[0319]
本发明的一个优选实施方案涉及一种全身性制剂,其包含0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和3.5重量%至30重量%的l-羟丙基纤维素和/或羟丙基纤维素或由它们组成。
[0320]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和0.1重量%至40重量%的l-羟丙基纤维素和/或羟丙基纤维素或由它们组成。
[0321]
本发明的一个优选实施方案涉及一种全身性制剂,其包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和2重量%至35重量%的l-羟丙基纤维素和/或羟丙基纤维素或由它们组成。
[0322]
本发明的一个优选实施方案涉及一种全身性制剂,其包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和3.5重量%至30重量%的l-羟丙基纤维素和/或羟丙基纤维素或由它们组成。
[0323]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和0.1重量%至40重量%的l-羟丙基纤维素和/或羟丙基纤维素或由它们组成。
[0324]
本发明的一个优选实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和2重量%至35重量%的l-羟丙基纤维素和/或羟丙基纤维素或由它们组成。
[0325]
本发明的一个优选实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和3.5重量%至30重量%的l-羟丙基纤维素和/或羟丙基纤维素或由它们组成。
[0326]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的酸化剂和0.1重量%至40重量%的聚合物沉淀抑制剂或由它们组成。
[0327]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的酸化剂以及2重量%至35重量%的聚合物沉淀抑制剂或由它们组成。
[0328]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的酸化剂和3.5重量%至30重量%的聚合物沉淀抑制剂或由它们组成。
[0329]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的酸化剂和0.1重量%至40重量%的聚合物沉淀抑制剂或由它们组成。
[0330]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的酸化剂和2重量%至35重量%的聚合物沉淀抑制剂或由它们组成。
[0331]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的酸化剂和3.5重量%至30重量%的聚合物沉淀抑制剂或由它们组成。
[0332]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的酸化剂和0.1重量%至40重量%的聚合物沉淀抑制剂或由它们组成。
[0333]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的酸化剂和2重量%至35重量%的聚合物沉淀抑制剂或由它们组成。
[0334]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的酸化剂和3.5重量%至30重量%的聚合物沉淀抑制剂或由它们组成。
[0335]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或
甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的酸化剂和3.5重量%至30重量%的聚合物沉淀抑制剂或由它们组成。
[0344]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的酸化剂和0.1重量%至40重量%的聚合物沉淀抑制剂或由它们组成。
[0345]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的酸化剂和2重量%至35重量%的聚合物沉淀抑制剂或由它们组成。
[0346]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的酸化剂和3.5重量%至30重量%的聚合物沉淀抑制剂或由它们组成。
[0347]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的酸化剂和0.1重量%至40重量%的聚合物沉淀抑制剂或由它们组成。
[0348]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的酸化剂和2重量%至35重量%的聚合物沉淀抑制剂或由它们组成。
[0349]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的酸化剂和3.5重量%至30重量%的聚合物沉淀抑制剂或由它们组成。
[0350]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的酸化剂和0.1重量%至40重量%的聚合物沉淀抑制剂或由它们组成。
[0351]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至45重量%的(s,
e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的酸化剂和2重量%至35重量%的聚合物沉淀抑制剂或由它们组成。
[0352]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的酸化剂和3.5重量%至30重量%的聚合物沉淀抑制剂或由它们组成。
[0353]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的酸化剂和0.1重量%至40重量%的聚合物沉淀抑制剂或由它们组成。
[0354]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的酸化剂和2重量%至35重量%的聚合物沉淀抑制剂或由它们组成。
[0355]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的酸化剂和3.5重量%至30重量%的聚合物沉淀抑制剂或由它们组成。
[0356]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的酸化剂和0.1重量%至40重量%的聚合物沉淀抑制剂或由它们组成。
[0357]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的酸化剂和2重量%至35重量%的聚合物沉淀抑制剂或由它们组成。
[0358]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的酸化剂和3.5重量%至30重量%的聚合物沉淀抑制剂或由它们组成。
[0359]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的酸化剂和0.1重量%至40重量%的聚合物沉淀抑制剂或由它们组成。
[0360]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的酸化剂和2重量%至35重量%的聚合物沉淀抑制剂或由它们组成。
[0361]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的酸化剂和3.5重量%至30重量%的聚合物沉淀抑制剂或由它们组成。
[0362]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的己二酸和0.1重量%至40重量%的l-羟丙基纤维素和/或羟丙基纤维素或由它们组成。
[0363]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的己二酸和2重量%至35重量%的l-羟丙基纤维素和/或羟丙基纤维素或由它们组成。
[0364]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的己二酸和3.5重量%至30.5重量%的l-羟丙基纤维素和/或羟丙基纤维素或由它们组成。
[0365]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的己二酸和0.1重量%至40重量%的l-羟丙基纤维素和/或羟丙基纤维素或由它们组成。
[0366]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的己二酸和2重量%至35重量%的l-羟丙基纤维素和/或羟丙基纤维素或
由它们组成。
[0367]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的己二酸和3.5重量%至30.5重量%的l-羟丙基纤维素和/或羟丙基纤维素或由它们组成。
[0368]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的己二酸和0.1重量%至40重量%的l-羟丙基纤维素和/或羟丙基纤维素或由它们组成。
[0369]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的己二酸和2重量%至35重量%的l-羟丙基纤维素和/或羟丙基纤维素或由它们组成。
[0370]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的己二酸和3.5重量%至30.5重量%的l-羟丙基纤维素和/或羟丙基纤维素或由它们组成。
[0371]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的己二酸和0.1重量%至40重量%的l-羟丙基纤维素和/或羟丙基纤维素或由它们组成。
[0372]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的己二酸和2重量%至35重量%的l-羟丙基纤维素和/或羟丙基纤维素或由它们组成。
[0373]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的己二酸和3.5重量%至30.5重量%的l-羟丙基纤维素和/或羟丙基纤维素或由它们组成。
[0374]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或
甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的己二酸和3.5重量%至30.5重量%的l-羟丙基纤维素和/或羟丙基纤维素或由它们组成。
[0383]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的己二酸和0.1重量%至40重量%的l-羟丙基纤维素和/或羟丙基纤维素或由它们组成。
[0384]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的己二酸和2重量%至35重量%的l-羟丙基纤维素和/或羟丙基纤维素或由它们组成。
[0385]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的己二酸和3.5重量%至30.5重量%的l-羟丙基纤维素和/或羟丙基纤维素或由它们组成。
[0386]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的己二酸和0.1重量%至40重量%的l-羟丙基纤维素和/或羟丙基纤维素或由它们组成。
[0387]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的己二酸和2重量%至35重量%的l-羟丙基纤维素和/或羟丙基纤维素或由它们组成。
[0388]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的己二酸和3.5重量%至30.5重量%的l-羟丙基纤维素和/或羟丙基纤维素或由它们组成。
[0389]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的己二酸和0.1重量%至40重量%的l-羟丙基纤维素和/或羟丙基纤维素或由它们组成。
[0390]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的
(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的己二酸和2重量%至35重量%的l-羟丙基纤维素和/或羟丙基纤维素或由它们组成。
[0391]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的己二酸和3.5重量%至30.5重量%的l-羟丙基纤维素和/或羟丙基纤维素或由它们组成。
[0392]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的己二酸和0.1重量%至40重量%的l-羟丙基纤维素和/或羟丙基纤维素或由它们组成。
[0393]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的己二酸和2重量%至35重量%的l-羟丙基纤维素和/或羟丙基纤维素或由它们组成。
[0394]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的己二酸和3.5重量%至30.5重量%的l-羟丙基纤维素和/或羟丙基纤维素或由它们组成。
[0395]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的己二酸和0.1重量%至40重量%的l-羟丙基纤维素和/或羟丙基纤维素或由它们组成。
[0396]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的己二酸和2重量%至35重量%的l-羟丙基纤维素和/或羟丙基纤维素或由它们组成。
[0397]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的己二酸和3.5重量%至30.5重量%的l-羟丙基纤维素和/或羟丙基纤维素或由它们组成。
[0398]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的酸化剂、0.1重量%至40重量%的聚合物沉淀抑制剂和0重量%至15重量%的粘合剂或由它们组成。
[0399]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的酸化剂、0.1重量%至40重量%的聚合物沉淀抑制剂和0重量%至12重量%的粘合剂或由它们组成。
[0400]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的酸化剂、2重量%至35重量%的聚合物沉淀抑制剂和0重量%至12重量%的粘合剂或由它们组成。
[0401]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的酸化剂、3.5重量%至30重量%的聚合物沉淀抑制剂和0重量%至12重量%的粘合剂或由它们组成。
[0402]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的酸化剂、0.1重量%至40重量%的聚合物沉淀抑制剂和0重量%至12重量%的粘合剂或由它们组成。
[0403]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的酸化剂、2重量%至35重量%的聚合物沉淀抑制剂和0重量%至12重量%的粘合剂或由它们组成。
[0404]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的酸化剂、3.5重量%至30重量%的聚合物沉淀抑制剂和0重量%至12重量%的粘合剂或由它们组成。
[0405]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的酸化剂、0.1重量%至40重量%的聚合物沉淀抑制剂和0重量%至12重
量%的粘合剂或由它们组成。
[0406]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的酸化剂、2重量%至35重量%的聚合物沉淀抑制剂和0重量%至12重量%的粘合剂或由它们组成。
[0407]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的酸化剂、3.5重量%至30重量%的聚合物沉淀抑制剂和0重量%至12重量%的粘合剂或由它们组成。
[0408]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的酸化剂、0.1重量%至40重量%的聚合物沉淀抑制剂和0重量%至12重量%的粘合剂或由它们组成。
[0409]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的酸化剂、2重量%至35重量%的聚合物沉淀抑制剂和0重量%至12重量%的粘合剂或由它们组成。
[0410]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的酸化剂、3.5重量%至30重量%的聚合物沉淀抑制剂和0重量%至12重量%的粘合剂或由它们组成。
[0411]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的酸化剂、0.1重量%至40重量%的聚合物沉淀抑制剂和0重量%至12重量%的粘合剂或由它们组成。
[0412]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的酸化剂、2重量%至35重量%的聚合物沉淀抑制剂和0重量%至12重量%的粘合剂或由它们组成。
[0413]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或
甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的酸化剂、2重量%至35重量%的聚合物沉淀抑制剂和0重量%至12重量%的粘合剂或由它们组成。
[0422]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的酸化剂、3.5重量%至30重量%的聚合物沉淀抑制剂和0重量%至12重量%的粘合剂或由它们组成。
[0423]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的酸化剂、0.1重量%至40重量%的聚合物沉淀抑制剂和0重量%至12重量%的粘合剂或由它们组成。
[0424]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的酸化剂、2重量%至35重量%的聚合物沉淀抑制剂和0重量%至12重量%的粘合剂或由它们组成。
[0425]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的酸化剂、3.5重量%至30重量%的聚合物沉淀抑制剂和0重量%至12重量%的粘合剂或由它们组成。
[0426]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的酸化剂、0.1重量%至40重量%的聚合物沉淀抑制剂和0重量%至12重量%的粘合剂或由它们组成。
[0427]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的酸化剂、2重量%至35重量%的聚合物沉淀抑制剂和0重量%至12重量%的粘合剂或由它们组成。
[0428]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的酸化剂、3.5重量%至30重量%的聚合物沉淀抑制剂和0重量%至12重量%的粘合剂或由它们组成。
[0429]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至30.5重量%的
(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的酸化剂、0.1重量%至40重量%的聚合物沉淀抑制剂和0重量%至12重量%的粘合剂或由它们组成。
[0430]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的酸化剂、2重量%至35重量%的聚合物沉淀抑制剂和0重量%至12重量%的粘合剂或由它们组成。
[0431]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的酸化剂、3.5重量%至30重量%的聚合物沉淀抑制剂和0重量%至12重量%的粘合剂或由它们组成。
[0432]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的酸化剂、0.1重量%至40重量%的聚合物沉淀抑制剂和0重量%至12重量%的粘合剂或由它们组成。
[0433]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的酸化剂、2重量%至35重量%的聚合物沉淀抑制剂和0重量%至12重量%的粘合剂或由它们组成。
[0434]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的酸化剂、3.5重量%至30重量%的聚合物沉淀抑制剂和0重量%至12重量%的粘合剂或由它们组成。
[0435]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的己二酸、0.1重量%至40重量%的l-羟丙基纤维素和/或羟丙基纤维素和0重量%至15重量%的聚维酮k25或由它们组成。
[0436]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的己二酸、0.1重量%至40重量%的l-羟丙基纤维素和/或羟丙基纤维素和0重量%至12重量%的聚维酮k25或由它们组成。
[0437]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的己二酸、2重量%至35重量%的l-羟丙基纤维素和/或羟丙基纤维素和0重量%至12重量%的聚维酮k25或由它们组成。
[0438]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的己二酸、3.5重量%至30.5重量%的l-羟丙基纤维素和/或羟丙基纤维素和0重量%至12重量%的聚维酮k25或由它们组成。
[0439]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的己二酸、0.1重量%至40重量%的l-羟丙基纤维素和/或羟丙基纤维素和0重量%至12重量%的聚维酮k25或由它们组成。
[0440]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的己二酸、2重量%至35重量%的l-羟丙基纤维素和/或羟丙基纤维素和0重量%至12重量%的聚维酮k25或由它们组成。
[0441]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的己二酸、3.5重量%至30.5重量%的l-羟丙基纤维素和/或羟丙基纤维素和0重量%至12重量%的聚维酮k25或由它们组成。
[0442]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的己二酸、0.1重量%至40重量%的l-羟丙基纤维素和/或羟丙基纤维素和0重量%至12重量%的聚维酮k25或由它们组成。
[0443]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的己二酸、2重量%至35重量%的l-羟丙基纤维素和/或羟丙基纤维素和0重量%至12重量%的聚维酮k25或由它们组成。
[0444]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的己二酸、3.5重量%至30.5重量%的l-羟丙基纤维素和/或羟丙基纤维素
和0重量%至12重量%的聚维酮k25或由它们组成。
[0445]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的己二酸、0.1重量%至40重量%的l-羟丙基纤维素和/或羟丙基纤维素和0重量%至12重量%的聚维酮k25或由它们组成。
[0446]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的己二酸和2重量%至35重量%的l-羟丙基纤维素和/或羟丙基纤维素或由它们组成。
[0447]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的己二酸、3.5重量%至30.5重量%的l-羟丙基纤维素和/或羟丙基纤维素和0重量%至12重量%的聚维酮k25或由它们组成。
[0448]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的己二酸、0.1重量%至40重量%的l-羟丙基纤维素和/或羟丙基纤维素和0重量%至12重量%的聚维酮k25或由它们组成。
[0449]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的己二酸、2重量%至35重量%的l-羟丙基纤维素和/或羟丙基纤维素和0重量%至12重量%的聚维酮k25或由它们组成。
[0450]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的己二酸、3.5重量%至30.5重量%的l-羟丙基纤维素和/或羟丙基纤维素和0重量%至12重量%的聚维酮k25或由它们组成。
[0451]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的己二酸、0.1重量%至40重量%的l-羟丙基纤维素和/或羟丙基纤维素和0重量%至12重量%的聚维酮k25或由它们组成。
[0452]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或
甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的己二酸、0.1重量%至40重量%的l-羟丙基纤维素和/或羟丙基纤维素和0重量%至12重量%的聚维酮k25或由它们组成。
[0461]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的己二酸、2重量%至35重量%的l-羟丙基纤维素和/或羟丙基纤维素和0重量%至12重量%的聚维酮k25或由它们组成。
[0462]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的己二酸、3.5重量%至30.5重量%的l-羟丙基纤维素和/或羟丙基纤维素和0重量%至12重量%的聚维酮k25或由它们组成。
[0463]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的己二酸、0.1重量%至40重量%的l-羟丙基纤维素和/或羟丙基纤维素和0重量%至12重量%的聚维酮k25或由它们组成。
[0464]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的己二酸、2重量%至35重量%的l-羟丙基纤维素和/或羟丙基纤维素和0重量%至12重量%的聚维酮k25或由它们组成。
[0465]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的己二酸和3.5重量%至30.5重量%的l-羟丙基纤维素和/或羟丙基纤维素和0重量%至12重量%的聚维酮k25或由它们组成。
[0466]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的己二酸、0.1重量%至40重量%的l-羟丙基纤维素和/或羟丙基纤维素和0重量%至12重量%的聚维酮k25或由它们组成。
[0467]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的己二酸、2重量%至35重量%的l-羟丙基纤维素和/或羟丙基纤维素和0重量%至12重量%的聚维酮k25或由它们组成。
[0468]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的
(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的己二酸、3.5重量%至30.5重量%的l-羟丙基纤维素和/或羟丙基纤维素和0重量%至12重量%的聚维酮k25或由它们组成。
[0469]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的己二酸、0.1重量%至40重量%的l-羟丙基纤维素和/或羟丙基纤维素和0重量%至12重量%的聚维酮k25或由它们组成。
[0470]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的己二酸、2重量%至35重量%的l-羟丙基纤维素和/或羟丙基纤维素和0重量%至12重量%的聚维酮k25或由它们组成。
[0471]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的己二酸、3.5重量%至30.5重量%的l-羟丙基纤维素和/或羟丙基纤维素和0重量%至12重量%的聚维酮k25或由它们组成。
[0472]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的酸化剂、0.1重量%至40重量%的聚合物沉淀抑制剂、0重量%至15重量%的粘合剂、0.1重量%至35重量%的崩解剂和0.1重量%至10重量%的润滑剂/助流剂或由它们组成。
[0473]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的酸化剂、0.1重量%至40重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂和1重量%至9重量%的润滑剂/助流剂或由它们组成。
[0474]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的酸化剂、0.1重量%至40重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂和1重量%至9重量%的润滑剂/助流剂或由它们组成。
[0475]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨
基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的酸化剂、2重量%至35重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂和1重量%至9重量%的润滑剂/助流剂或由它们组成。
[0476]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的酸化剂、3.5重量%至30重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂和1重量%至9重量%的润滑剂/助流剂或由它们组成。
[0477]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的酸化剂、0.1重量%至40重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂和1重量%至9重量%的润滑剂/助流剂或由它们组成。
[0478]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的酸化剂、2重量%至35重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂和1重量%至9重量%的润滑剂/助流剂或由它们组成。
[0479]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的酸化剂、3.5重量%至30重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂和1重量%至9重量%的润滑剂/助流剂或由它们组成。
[0480]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的酸化剂、0.1重量%至40重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂和1重量%至9重量%的润滑剂/助流剂或由它们组成。
[0481]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的酸化剂、2重量%至35重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂和1重量%至9重量%的润滑剂/助流剂或由它们组
成。
[0482]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的酸化剂、3.5重量%至30重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂和1重量%至9重量%的润滑剂/助流剂或由它们组成。
[0483]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的酸化剂、0.1重量%至40重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂、1重量%至9重量%的润滑剂/助流剂、2重量%至35重量%的崩解剂和1重量%至9重量%的润滑剂/助流剂或由它们组成。
[0484]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的酸化剂、2重量%至35重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂、1重量%至9重量%的润滑剂/助流剂、2重量%至35重量%的崩解剂和1重量%至9重量%的润滑剂/助流剂或由它们组成。
[0485]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的酸化剂、3.5重量%至30重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂、1重量%至9重量%的润滑剂/助流剂、2重量%至35重量%的崩解剂和1重量%至9重量%的润滑剂/助流剂或由它们组成。
[0486]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的酸化剂、0.1重量%至40重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂和1重量%至9重量%的润滑剂/助流剂或由它们组成。
[0487]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的酸化剂、2重量%至35重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂和1重量%至9重量%的润
甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的酸化剂、3.5重量%至30重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂和1重量%至9重量%的润滑剂/助流剂或由它们组成。
[0495]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的酸化剂、0.1重量%至40重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂和1重量%至9重量%的润滑剂/助流剂或由它们组成。
[0496]
本发明的一个优选实施方案涉及一种全身性制剂,其包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的酸化剂、2重量%至35重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂和1重量%至9重量%的润滑剂/助流剂或由它们组成。
[0497]
本发明的一个非常优选的实施方案涉及一种全身性制剂,其包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的己二酸、2重量%至35重量%的l-羟丙基纤维素和/或羟丙基纤维素、0重量%至12重量%的聚维酮k25、2重量%至35重量%的交联羧甲基纤维素钠和1重量%至9重量%的滑石粉或二氧化硅或由它们组成。
[0498]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的酸化剂、3.5重量%至30重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂和1重量%至9重量%的润滑剂/助流剂或由它们组成。
[0499]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的酸化剂、0.1重量%至40重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂和1重量%至9重量%的润滑剂/助流剂或由它们组成。
[0500]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的酸化剂、2重量%至35重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂和1重量%至9重量%的
润滑剂/助流剂或由它们组成。
[0501]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的酸化剂、3.5重量%至30重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂和1重量%至9重量%的润滑剂/助流剂或由它们组成。
[0502]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的酸化剂、0.1重量%至40重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂和1重量%至9重量%的润滑剂/助流剂或由它们组成。
[0503]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的酸化剂、2重量%至35重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂和1重量%至9重量%的润滑剂/助流剂或由它们组成。
[0504]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的酸化剂、3.5重量%至30重量%的聚合物沉淀抑制剂和0重量%至12重量%的粘合剂或由它们组成。
[0505]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的酸化剂、0.1重量%至40重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂和1重量%至9重量%的润滑剂/助流剂或由它们组成。
[0506]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的酸化剂、2重量%至35重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂和1重量%至9重量%的润滑剂/助流剂或由它们组成。
[0507]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物
或药学上可接受的盐、3重量%至75重量%的酸化剂、3.5重量%至30重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂和1重量%至9重量%的润滑剂/助流剂或由它们组成。
[0508]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的酸化剂、0.1重量%至40重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂和1重量%至9重量%的润滑剂/助流剂或由它们组成。
[0509]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的酸化剂、2重量%至35重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂和1重量%至9重量%的润滑剂/助流剂或由它们组成。
[0510]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的酸化剂、3.5重量%至30重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂和1重量%至9重量%的润滑剂/助流剂或由它们组成。
[0511]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的己二酸、0.1重量%至40重量%的l-羟丙基纤维素和/或羟丙基纤维素、0重量%至15重量%的聚维酮k25、0.1重量%至35重量%的交联羧甲基纤维素钠和0.1重量%至10重量%的滑石粉或二氧化硅或由它们组成。
[0512]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的己二酸、0.1重量%至40重量%的l-羟丙基纤维素和/或羟丙基纤维素、0重量%至12重量%的聚维酮k25、2重量%至35重量%的交联羧甲基纤维素钠和1重量%至9重量%的滑石粉或二氧化硅或由它们组成。
[0513]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的己二酸、2重量%至35重量%的l-羟丙基纤维素和/或羟丙基纤维素、0重量%至12重量%的聚维酮k25、2重量%至35重量%的交联羧甲基纤维素钠和1重量%至9重量%的滑石粉或二氧化硅或由它们组成。
[0514]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的己二酸、3.5重量%至30.5重量%的l-羟丙基纤维素和/或羟丙基纤维素、0重量%至12重量%的聚维酮k25、2重量%至35重量%的交联羧甲基纤维素钠和1重量%至9重量%的滑石粉或二氧化硅或由它们组成。
[0515]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的己二酸、0.1重量%至40重量%的l-羟丙基纤维素和/或羟丙基纤维素、0重量%至12重量%的聚维酮k25、2重量%至35重量%的交联羧甲基纤维素钠和1重量%至9重量%的滑石粉或二氧化硅或由它们组成。
[0516]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的己二酸、2重量%至35重量%的l-羟丙基纤维素和/或羟丙基纤维素、0重量%至12重量%的聚维酮k25、2重量%至35重量%的交联羧甲基纤维素钠和1重量%至9重量%的滑石粉或二氧化硅或由它们组成。
[0517]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的己二酸、3.5重量%至30.5重量%的l-羟丙基纤维素和/或羟丙基纤维素、0重量%至12重量%的聚维酮k25、2重量%至35重量%的交联羧甲基纤维素钠和1重量%至9重量%的滑石粉或二氧化硅或由它们组成。
[0518]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的己二酸、0.1重量%至40重量%的l-羟丙基纤维素和/或羟丙基纤维素、0重量%至12重量%的聚维酮k25、2重量%至35重量%的交联羧甲基纤维素钠和1重量%至9重量%的滑石粉或二氧化硅或由它们组成。
[0519]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的己二酸、2重量%至35重量%的l-羟丙基纤维素和/或羟丙基纤维素、0重量%至12重量%的聚维酮k25、2重量%至35重量%的交联羧甲基纤维素钠和1重量%至9重量%的滑石粉或二氧化硅或由它们组成。
[0520]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重
量%至55重量%的己二酸、3.5重量%至30.5重量%的l-羟丙基纤维素和/或羟丙基纤维素、0重量%至12重量%的聚维酮k25、2重量%至35重量%的交联羧甲基纤维素钠和1重量%至9重量%的滑石粉或二氧化硅或由它们组成。
[0521]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的己二酸、0.1重量%至40重量%的l-羟丙基纤维素和/或羟丙基纤维素、0重量%至12重量%的聚维酮k25、2重量%至35重量%的交联羧甲基纤维素钠和1重量%至9重量%的滑石粉或二氧化硅或由它们组成。
[0522]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的己二酸、2重量%至35重量%的l-羟丙基纤维素和/或羟丙基纤维素、2重量%至35重量%的交联羧甲基纤维素钠和1重量%至9重量%的滑石粉或二氧化硅或由它们组成。
[0523]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的己二酸、3.5重量%至30.5重量%的l-羟丙基纤维素和/或羟丙基纤维素、0重量%至12重量%的聚维酮k25、2重量%至35重量%的交联羧甲基纤维素钠和1重量%至9重量%的滑石粉或二氧化硅或由它们组成。
[0524]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的己二酸、0.1重量%至40重量%的l-羟丙基纤维素和/或羟丙基纤维素、0重量%至12重量%的聚维酮k25、2重量%至35重量%的交联羧甲基纤维素钠和1重量%至9重量%的滑石粉或二氧化硅或由它们组成。
[0525]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的己二酸、2重量%至35重量%的l-羟丙基纤维素和/或羟丙基纤维素、0重量%至12重量%的聚维酮k25、2重量%至35重量%的交联羧甲基纤维素钠和1重量%至9重量%的滑石粉或二氧化硅或由它们组成。
[0526]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的己二酸、3.5重量%至30.5重量%的l-羟丙基纤维素和/或羟丙基纤维素、0重量%至12重量%的聚维酮k25、2重量%至35重量%的交联羧甲基纤维素钠和1重量%至9重量%的滑石粉或二氧化硅或由它们组成。
[0527]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的己二酸、0.1重量%至40重量%的l-羟丙基纤维素和/或羟丙基纤维素和0重量%至12重量%的聚维酮k25或由它们组成。
[0528]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的己二酸、2重量%至35重量%的l-羟丙基纤维素和/或羟丙基纤维素、0重量%至12重量%的聚维酮k25、2重量%至35重量%的交联羧甲基纤维素钠和1重量%至9重量%的滑石粉或二氧化硅或由它们组成。
[0529]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的己二酸、3.5重量%至30.5重量%的l-羟丙基纤维素和/或羟丙基纤维素、0重量%至12重量%的聚维酮k25、2重量%至35重量%的交联羧甲基纤维素钠和1重量%至9重量%的滑石粉或二氧化硅或由它们组成。
[0530]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的己二酸、0.1重量%至40重量%的l-羟丙基纤维素和/或羟丙基纤维素、0重量%至12重量%的聚维酮k25、2重量%至35重量%的交联羧甲基纤维素钠和1重量%至9重量%的滑石粉或二氧化硅或由它们组成。
[0531]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的己二酸、2重量%至35重量%的l-羟丙基纤维素和/或羟丙基纤维素和0重量%至12重量%的聚维酮k25或由它们组成。
[0532]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的己二酸、3.5重量%至30.5重量%的l-羟丙基纤维素和/或羟丙基纤维素和0重量%至12重量%的聚维酮k25或由它们组成。
[0533]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的己二酸、0.1重量%至40重量%的l-羟丙基纤维素和/或羟丙基纤维素、0重量%至12重量%的聚维酮k25、2重量%至35重量%的交联羧甲基纤维素钠和1重量%至9重量%的滑石粉或二氧化硅或由它们组成。
[0534]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的己二酸、2重量%至35重量%的l-羟丙基纤维素和/或羟丙基纤维素、0重量%至12重量%的聚维酮k25、2重量%至35重量%的交联羧甲基纤维素钠和1重量%至9重量%的滑石粉或二氧化硅或由它们组成。
[0535]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的己二酸、3.5重量%至30.5重量%的l-羟丙基纤维素和/或羟丙基纤维素、0重量%至12重量%的聚维酮k25、2重量%至35重量%的交联羧甲基纤维素钠和1重量%至9重量%的滑石粉或二氧化硅或由它们组成。
[0536]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的己二酸、0.1重量%至40重量%的l-羟丙基纤维素和/或羟丙基纤维素、0重量%至12重量%的聚维酮k25、2重量%至35重量%的交联羧甲基纤维素钠和1重量%至9重量%的滑石粉或二氧化硅或由它们组成。
[0537]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的己二酸、2重量%至35重量%的l-羟丙基纤维素和/或羟丙基纤维素、0重量%至12重量%的聚维酮k25、2重量%至35重量%的交联羧甲基纤维素钠和1重量%至9重量%的滑石粉或二氧化硅或由它们组成。
[0538]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的己二酸、3.5重量%至30.5重量%的l-羟丙基纤维素和/或羟丙基纤维素、0重量%至12重量%的聚维酮k25、2重量%至35重量%的交联羧甲基纤维素钠和1重量%至9重量%的滑石粉或二氧化硅或由它们组成。
[0539]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的己二酸、0.1重量%至40重量%的l-羟丙基纤维素和/或羟丙基纤维素、0重量%至12重量%的聚维酮k25、2重量%至35重量%的交联羧甲基纤维素钠和1重量%至9重量%的滑石粉或二氧化硅或由它们组成。
[0540]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物
或药学上可接受的盐、1重量%至75重量%的己二酸、2重量%至35重量%的l-羟丙基纤维素和/或羟丙基纤维素、0重量%至12重量%的聚维酮k25、2重量%至35重量%的交联羧甲基纤维素钠和1重量%至9重量%的滑石粉或二氧化硅或由它们组成。
[0541]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的己二酸和3.5重量%至30.5重量%的l-羟丙基纤维素和/或羟丙基纤维素、0重量%至12重量%的聚维酮k25、2重量%至35重量%的交联羧甲基纤维素钠和1重量%至9重量%的滑石粉或二氧化硅或由它们组成。
[0542]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的己二酸、0.1重量%至40重量%的l-羟丙基纤维素和/或羟丙基纤维素、0重量%至12重量%的聚维酮k25、2重量%至35重量%的交联羧甲基纤维素钠和1重量%至9重量%的滑石粉或二氧化硅或由它们组成。
[0543]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的己二酸、2重量%至35重量%的l-羟丙基纤维素和/或羟丙基纤维素、0重量%至12重量%的聚维酮k25、2重量%至35重量%的交联羧甲基纤维素钠和1重量%至9重量%的滑石粉或二氧化硅或由它们组成。
[0544]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的己二酸、3.5重量%至30.5重量%的l-羟丙基纤维素和/或羟丙基纤维素、0重量%至12重量%的聚维酮k25、2重量%至35重量%的交联羧甲基纤维素钠和1重量%至9重量%的滑石粉或二氧化硅或由它们组成。
[0545]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的己二酸、0.1重量%至40重量%的l-羟丙基纤维素和/或羟丙基纤维素、0重量%至12重量%的聚维酮k25、2重量%至35重量%的交联羧甲基纤维素钠和1重量%至9重量%的滑石粉或二氧化硅或由它们组成。
[0546]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的己二酸、2重量%至35重量%的l-羟丙基纤维素和/或羟丙基纤维素、0重量%至12重量%的聚维酮k25、2重量%至35重量%的交联羧甲基纤维素钠和1重量%至9重量%的滑石粉或二氧化硅或由它们组成。
[0547]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的己二酸、3.5重量%至30重量%的l-羟丙基纤维素和/或羟丙基纤维素、0重量%至12重量%的聚维酮k25、2重量%至35重量%的交联羧甲基纤维素钠和1重量%至9重量%的滑石粉或二氧化硅或由它们组成。
[0548]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的酸化剂、0.1重量%至40重量%的聚合物沉淀抑制剂、0重量%至15重量%的粘合剂、0.1重量%至35重量%的崩解剂、0.1重量%至10重量%的润滑剂/助流剂和0重量%至50重量%的稀释剂/填充剂/粘合剂或由它们组成。
[0549]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的酸化剂、0.1重量%至40重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂、1重量%至9重量%的润滑剂/助流剂和0重量%至50重量%的稀释剂/填充剂/粘合剂或由它们组成。
[0550]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的酸化剂、0.1重量%至40重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂、1重量%至9重量%的润滑剂/助流剂和0重量%至50重量%的稀释剂/填充剂/粘合剂或由它们组成。
[0551]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的酸化剂、2重量%至35重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂、1重量%至9重量%的润滑剂/助流剂和0重量%至50重量%的稀释剂/填充剂/粘合剂或由它们组成。
[0552]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的酸化剂、3.5重量%至30重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂、1重量%至9重量%的润滑剂/助流剂和0重量%至50重量%的稀释剂/填充剂/粘合剂或由它们组成。
[0553]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重
量%至75重量%的酸化剂、0.1重量%至40重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂、1重量%至9重量%的润滑剂/助流剂和0重量%至50重量%的稀释剂/填充剂/粘合剂或由它们组成。
[0554]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的酸化剂、2重量%至35重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂、1重量%至9重量%的润滑剂/助流剂和0重量%至50重量%的稀释剂/填充剂/粘合剂或由它们组成。
[0555]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的酸化剂、3.5重量%至30重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂、1重量%至9重量%的润滑剂/助流剂和0重量%至50重量%的稀释剂/填充剂/粘合剂或由它们组成。
[0556]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的酸化剂、0.1重量%至40重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂、1重量%至9重量%的润滑剂/助流剂和0重量%至50重量%的稀释剂/填充剂/粘合剂或由它们组成。
[0557]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的酸化剂、2重量%至35重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂、1重量%至9重量%的润滑剂/助流剂和0重量%至50重量%的稀释剂/填充剂/粘合剂或由它们组成。
[0558]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的酸化剂、3.5重量%至30重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂、1重量%至9重量%的润滑剂/助流剂和0重量%至50重量%的稀释剂/填充剂/粘合剂或由它们组成。
[0559]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的酸化剂、0.1重量%至40重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂、1重量%至9重量%的润滑剂/助流剂、2重量%至35重量%的崩解剂、1重量%至9重量%的润滑剂/助流剂和0重
量%至50重量%的稀释剂/填充剂/粘合剂或由它们组成。
[0560]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的酸化剂、2重量%至35重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂、1重量%至9重量%的润滑剂/助流剂、2重量%至35重量%的崩解剂、1重量%至9重量%的润滑剂/助流剂和0重量%至50重量%的稀释剂/填充剂/粘合剂或由它们组成。
[0561]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的酸化剂、3.5重量%至30重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂、1重量%至9重量%的润滑剂/助流剂、2重量%至35重量%的崩解剂、1重量%至9重量%的润滑剂/助流剂和0重量%至50重量%的稀释剂/填充剂/粘合剂或由它们组成。
[0562]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的酸化剂、0.1重量%至40重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂、1重量%至9重量%的润滑剂/助流剂和0重量%至50重量%的稀释剂/填充剂/粘合剂或由它们组成。
[0563]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的酸化剂、2重量%至35重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂、1重量%至9重量%的润滑剂/助流剂和0重量%至50重量%的稀释剂/填充剂/粘合剂或由它们组成。
[0564]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的酸化剂、3.5重量%至30重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂、1重量%至9重量%的润滑剂/助流剂和0重量%至50重量%的稀释剂/填充剂/粘合剂或由它们组成。
[0565]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的酸化剂、0.1重量%至40重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂、1重量%至9重量%的润滑剂/助流剂和0重量%至50重量%的稀释剂/填充剂/粘合剂或由它们组成。
[0566]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的酸化剂、2重量%至35重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂、1重量%至9重量%的润滑剂/助流剂和0重量%至50重量%的稀释剂/填充剂/粘合剂或由它们组成。
[0567]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的酸化剂、3.5重量%至30重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂、1重量%至9重量%的润滑剂/助流剂和0重量%至50重量%的稀释剂/填充剂/粘合剂或由它们组成。
[0568]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的酸化剂、0.1重量%至40重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂、1重量%至9重量%的润滑剂/助流剂和0重量%至50重量%的稀释剂/填充剂/粘合剂或由它们组成。
[0569]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的酸化剂、2重量%至35重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂、1重量%至9重量%的润滑剂/助流剂或由它们组成。
[0570]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的酸化剂、3.5重量%至30重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂、1重量%至9重量%的润滑剂/助流剂和0重量%至50重量%的稀释剂/填充剂/粘合剂或由它们组成。
[0571]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的酸化剂、0.1重量%至40重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂、1重量%至9重量%的润滑剂/助流剂和0重量%至50重量%的稀释剂/填充剂/粘合剂或由它们组成。
[0572]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或
药学上可接受的盐、3重量%至75重量%的酸化剂、2重量%至35重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂、1重量%至9重量%的润滑剂/助流剂和0重量%至50重量%的稀释剂/填充剂/粘合剂或由它们组成。
[0573]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的酸化剂、3.5重量%至30重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂、1重量%至9重量%的润滑剂/助流剂和0重量%至50重量%的稀释剂/填充剂/粘合剂或由它们组成。
[0574]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的酸化剂、0.1重量%至40重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂、1重量%至9重量%的润滑剂/助流剂和0重量%至50重量%的稀释剂/填充剂/粘合剂或由它们组成。
[0575]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的酸化剂、2重量%至35重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂、1重量%至9重量%的润滑剂/助流剂和0重量%至50重量%的稀释剂/填充剂/粘合剂或由它们组成。
[0576]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的酸化剂、3.5重量%至30重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂、1重量%至9重量%的润滑剂/助流剂和0重量%至50重量%的稀释剂/填充剂/粘合剂或由它们组成。
[0577]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的酸化剂、0.1重量%至40重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂、1重量%至9重量%的润滑剂/助流剂和0重量%至50重量%的稀释剂/填充剂/粘合剂或由它们组成。
[0578]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的酸化剂、2重量%至35重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂、1重量%至9重量%的润滑剂/助流剂和0重量%至50重量%的稀释剂/填充剂/粘合剂或由它们组成。
[0579]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的酸化剂、3.5重量%至30重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂和0重量%至50重量%的稀释剂/填充剂/粘合剂或由它们组成。
[0580]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的酸化剂、0.1重量%至40重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂、1重量%至9重量%的润滑剂/助流剂和0重量%至50重量%的稀释剂/填充剂/粘合剂或由它们组成。
[0581]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的酸化剂、2重量%至35重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂、1重量%至9重量%的润滑剂/助流剂和0重量%至50重量%的稀释剂/填充剂/粘合剂或由它们组成。
[0582]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的酸化剂、3.5重量%至30重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂、1重量%至9重量%的润滑剂/助流剂和0重量%至50重量%的稀释剂/填充剂/粘合剂或由它们组成。
[0583]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的酸化剂、0.1重量%至40重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂、1重量%至9重量%的润滑剂/助流剂和0重量%至50重量%的稀释剂/填充剂/粘合剂或由它们组成。
[0584]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的酸化剂、2重量%至35重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂、1重量%至9重量%的润滑剂/助流剂和0重量%至50重量%的稀释剂/填充剂/粘合剂或由它们组成。
[0585]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物
或药学上可接受的盐、4.5重量%至55重量%的酸化剂、3.5重量%至30重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂、1重量%至9重量%的润滑剂/助流剂和0重量%至50重量%的稀释剂/填充剂/粘合剂或由它们组成。
[0586]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的己二酸、0.1重量%至40重量%的l-羟丙基纤维素和/或羟丙基纤维素、0重量%至15重量%的聚维酮k25、0.1重量%至35重量%的交联羧甲基纤维素钠、0.1重量%至10重量%的滑石粉或二氧化硅和0重量%至50重量%的甘露醇和/或微晶纤维素或由它们组成。
[0587]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的己二酸、0.1重量%至40重量%的l-羟丙基纤维素和/或羟丙基纤维素、0重量%至12重量%的聚维酮k25、2重量%至35重量%的交联羧甲基纤维素钠、1重量%至9重量%的滑石粉或二氧化硅和0重量%至50重量%的甘露醇和/或微晶纤维素或由它们组成。
[0588]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的己二酸、2重量%至35重量%的l-羟丙基纤维素和/或羟丙基纤维素、0重量%至12重量%的聚维酮k25、2重量%至35重量%的交联羧甲基纤维素钠、1重量%至9重量%的滑石粉或二氧化硅和0重量%至50重量%的甘露醇和/或微晶纤维素或由它们组成。
[0589]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的己二酸、3.5重量%至30.5重量%的l-羟丙基纤维素和/或羟丙基纤维素、0重量%至12重量%的聚维酮k25、2重量%至35重量%的交联羧甲基纤维素钠、1重量%至9重量%的滑石粉或二氧化硅和0重量%至50重量%的甘露醇和/或微晶纤维素或由它们组成。
[0590]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的己二酸、0.1重量%至40重量%的l-羟丙基纤维素和/或羟丙基纤维素、0重量%至12重量%的聚维酮k25、2重量%至35重量%的交联羧甲基纤维素钠、1重量%至9重量%的滑石粉或二氧化硅和0重量%至50重量%的甘露醇和/或微晶纤维素或由它们组成。
[0591]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨
甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的己二酸、2重量%至35重量%的l-羟丙基纤维素和/或羟丙基纤维素、2重量%至35重量%的交联羧甲基纤维素钠、1重量%至9重量%的滑石粉或二氧化硅和0重量%至50重量%的甘露醇和/或微晶纤维素或由它们组成。
[0598]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的己二酸、3.5重量%至30.5重量%的l-羟丙基纤维素和/或羟丙基纤维素、0重量%至12重量%的聚维酮k25、2重量%至35重量%的交联羧甲基纤维素钠、1重量%至9重量%的滑石粉或二氧化硅和0重量%至50重量%的甘露醇和/或微晶纤维素或由它们组成。
[0599]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的己二酸、0.1重量%至40重量%的l-羟丙基纤维素和/或羟丙基纤维素、0重量%至12重量%的聚维酮k25、2重量%至35重量%的交联羧甲基纤维素钠、1重量%至9重量%的滑石粉或二氧化硅和0重量%至50重量%的甘露醇和/或微晶纤维素或由它们组成。
[0600]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的己二酸、2重量%至35重量%的l-羟丙基纤维素和/或羟丙基纤维素、0重量%至12重量%的聚维酮k25、2重量%至35重量%的交联羧甲基纤维素钠、1重量%至9重量%的滑石粉或二氧化硅和0重量%至50重量%的甘露醇和/或微晶纤维素或由它们组成。
[0601]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的己二酸、3.5重量%至30.5重量%的l-羟丙基纤维素和/或羟丙基纤维素、0重量%至12重量%的聚维酮k25、2重量%至35重量%的交联羧甲基纤维素钠、1重量%至9重量%的滑石粉或二氧化硅和0重量%至50重量%的甘露醇和/或微晶纤维素或由它们组成。
[0602]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的己二酸、0.1重量%至40重量%的l-羟丙基纤维素和/或羟丙基纤维素、0重量%至12重量%的聚维酮k25、2重量%至35重量%的交联羧甲基纤维素钠、1重量%至9重量%的滑石粉或二氧化硅和0重量%至50重量%的甘露醇和/或微晶纤维素或由它们组成。
[0603]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的己二酸、2重量%至35重量%的l-羟丙基纤维素和/或羟丙基纤维素、0重量%至12重量%的聚维酮k25、2重量%至35重量%的交联羧甲基纤维素钠、1重量%至9重量%的滑石粉或二氧化硅和0重量%至50重量%的甘露醇和/或微晶纤维素或由它们组成。
[0604]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的己二酸、3.5重量%至30.5重量%的l-羟丙基纤维素和/或羟丙基纤维素、0重量%至12重量%的聚维酮k25、2重量%至35重量%的交联羧甲基纤维素钠、1重量%至9重量%的滑石粉或二氧化硅和0重量%至50重量%的甘露醇和/或微晶纤维素或由它们组成。
[0605]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的己二酸、0.1重量%至40重量%的l-羟丙基纤维素和/或羟丙基纤维素、0重量%至12重量%的聚维酮k25、2重量%至35重量%的交联羧甲基纤维素钠、1重量%至9重量%的滑石粉或二氧化硅和0重量%至50重量%的甘露醇和/或微晶纤维素或由它们组成。
[0606]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的己二酸、2重量%至35重量%的l-羟丙基纤维素和/或羟丙基纤维素、0重量%至12重量%的聚维酮k25、1重量%至9重量%的滑石粉或二氧化硅和0重量%至50重量%的甘露醇和/或微晶纤维素或由它们组成。
[0607]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的己二酸、3.5重量%至30.5重量%的l-羟丙基纤维素和/或羟丙基纤维素、0重量%至12重量%的聚维酮k25、2重量%至35重量%的交联羧甲基纤维素钠、1重量%至9重量%的滑石粉或二氧化硅和0重量%至50重量%的甘露醇和/或微晶纤维素或由它们组成。
[0608]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的己二酸、0.1重量%至40重量%的l-羟丙基纤维素和/或羟丙基纤维素、0重量%至12重量%的聚维酮k25、2重量%至35重量%的交联羧甲
(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的己二酸、0.1重量%至40重量%的l-羟丙基纤维素和/或羟丙基纤维素、0重量%至12重量%的聚维酮k25、2重量%至35重量%的交联羧甲基纤维素钠、1重量%至9重量%的滑石粉或二氧化硅和0重量%至50重量%的甘露醇和/或微晶纤维素或由它们组成。
[0615]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的己二酸、2重量%至35重量%的l-羟丙基纤维素和/或羟丙基纤维素、0重量%至12重量%的聚维酮k25、2重量%至35重量%的交联羧甲基纤维素钠、1重量%至9重量%的滑石粉或二氧化硅和0重量%至50重量%的甘露醇和/或微晶纤维素或由它们组成。
[0616]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的己二酸、3.5重量%至30.5重量%的l-羟丙基纤维素和/或羟丙基纤维素、0重量%至12重量%的聚维酮k25、2重量%至35重量%的交联羧甲基纤维素钠、1重量%至9重量%的滑石粉或二氧化硅和0重量%至50重量%的甘露醇和/或微晶纤维素或由它们组成。
[0617]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的己二酸、0.1重量%至40重量%的l-羟丙基纤维素和/或羟丙基纤维素、0重量%至12重量%的聚维酮k25、2重量%至35重量%的交联羧甲基纤维素钠、1重量%至9重量%的滑石粉或二氧化硅和0重量%至50重量%的甘露醇和/或微晶纤维素或由它们组成。
[0618]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的己二酸、2重量%至35重量%的l-羟丙基纤维素和/或羟丙基纤维素、0重量%至12重量%的聚维酮k25、2重量%至35重量%的交联羧甲基纤维素钠、1重量%至9重量%的滑石粉或二氧化硅和0重量%至50重量%的甘露醇和/或微晶纤维素或由它们组成。
[0619]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的己二酸、3.5重量%至30.5重量%的l-羟丙基纤维素和/或羟丙基纤维素、0重量%至12重量%的聚维酮k25、2重量%至35重量%的交联羧甲基纤维素钠、1重量%至9重量%的滑石粉或二氧化硅和0重量%至50重量%的甘露醇
和/或微晶纤维素或由它们组成。
[0620]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的己二酸、0.1重量%至40重量%的l-羟丙基纤维素和/或羟丙基纤维素、0重量%至12重量%的聚维酮k25、2重量%至35重量%的交联羧甲基纤维素钠、1重量%至9重量%的滑石粉或二氧化硅和0重量%至50重量%的甘露醇和/或微晶纤维素或由它们组成。
[0621]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的己二酸、2重量%至35重量%的l-羟丙基纤维素和/或羟丙基纤维素、0重量%至12重量%的聚维酮k25、2重量%至35重量%的交联羧甲基纤维素钠、1重量%至9重量%的滑石粉或二氧化硅和0重量%至50重量%的甘露醇和/或微晶纤维素或由它们组成。
[0622]
本发明的一个实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的己二酸、3.5重量%至30.5重量%的l-羟丙基纤维素和/或羟丙基纤维素、0重量%至12重量%的聚维酮k25、2重量%至35重量%的交联羧甲基纤维素钠、1重量%至9重量%的滑石粉或二氧化硅和0重量%至50重量%的甘露醇和/或微晶纤维素或由它们组成。
[0623]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的酸化剂、0-50重量%的稀释剂/填充剂/粘合剂、0.1重量%至40重量%的聚合物沉淀抑制剂、0重量%至15重量%的粘合剂、0.1重量%至35重量%的崩解剂和0.1重量%至10重量%的润滑剂/助流剂或由它们组成。
[0624]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1重量%至75重量%的酸化剂、0-50重量%的稀释剂/填充剂/粘合剂、0.1重量%至40重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂和1重量%至9重量%的润滑剂/助流剂或由它们组成。
[0625]
根据本发明的一个更优选实施方案涉及一种全身性制剂,其包含0.1重量%至35重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、0重量%至50重量%的稀释剂/填充剂/粘合剂、1重量%至75重量%的酸化剂、2重量%至25重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合
剂、2重量%至35重量%的崩解剂和1重量%至9重量%的润滑剂/助流剂或由它们组成。
[0626]
根据本发明的一个更优选实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、0重量%至50重量%的稀释剂/填充剂/粘合剂、1重量%至75重量%的酸化剂、2重量%至25重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂和1重量%至9重量%的润滑剂/助流剂或由它们组成。
[0627]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、3重量%至75重量%的酸化剂、0-50重量%的稀释剂/填充剂/粘合剂、0.1重量%至40重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂和1重量%至9重量%的润滑剂/助流剂或由它们组成。
[0628]
根据本发明的一个更优选实施方案涉及一种全身性制剂,其包含0.1重量%至35重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、0重量%至50重量%的稀释剂/填充剂/粘合剂、3重量%至75重量%的酸化剂、2重量%至25重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂和1重量%至9重量%的润滑剂/助流剂或由它们组成。
[0629]
根据本发明的一个更优选实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、0重量%至50重量%的稀释剂/填充剂/粘合剂、3重量%至75重量%的酸化剂、2重量%至25重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂和1重量%至9重量%的润滑剂/助流剂或由它们组成。
[0630]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、4.5重量%至55重量%的酸化剂、0-50重量%的稀释剂/填充剂/粘合剂、0.1重量%至40重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂和1重量%至9重量%的润滑剂/助流剂或由它们组成。
[0631]
根据本发明的一个更优选实施方案涉及一种全身性制剂,其包含0.1重量%至35重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、0重量%至50重量%的稀释剂/填充剂/粘合剂、4.5重量%至55重量%的酸化剂、2重量%至25重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂和1重量%至9重量%的润滑剂/助流剂或由它们组成。
[0632]
根据本发明的一个更优选实施方案涉及一种全身性制剂,其包含2.5重量%至30.5重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、0重量%至50重量%的稀释剂/填充剂/粘合剂、4.5重量%至55重量%的酸化剂、2重量%至25重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂和1重量%至9重量%的润滑剂/助流剂或由它们组成。
[0633]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、0-50重量%的微晶纤维素、5重量%至75重量%的己二酸、0.1重量%至40重量%的l-羟丙基纤维素和/或羟丙基纤维素、0重量%至15重量%的聚维酮k25、0.1重量%至35重量%的交联羧甲基纤维素钠和0.1重量%至9重量%的滑石粉或二氧化硅或由它们组成。
[0634]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、0-50重量%的微晶纤维素、1重量%至75重量%的己二酸、0.1重量%至40重量%的l-羟丙基纤维素和/或羟丙基纤维素、0重量%至15重量%的聚维酮k25、2重量%至35重量%的交联羧甲基纤维素钠和1重量%至9重量%的滑石粉或二氧化硅或由它们组成。
[0635]
根据本发明的一个更优选实施方案涉及一种全身性制剂,其包含0.1重量%至35重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、0-50重量%的微晶纤维素、1重量%至75重量%的己二酸、0.1重量%至40重量%的l-羟丙基纤维素和/或羟丙基纤维素,0重量%至15重量%的聚维酮k25、2重量%至35重量%的交联羧甲基纤维素钠和1重量%至9重量%的滑石粉或二氧化硅或由它们组成。
[0636]
如果所述全身性制剂被公开为由一定量(重量百分比、质量比和/或绝对质量)的成分组成的制剂,则其余为其它成分,即用其它成分平衡至100重量%。上面描述了其它成分。
[0637]
本发明的一个实施方案涉及一种用于预防和/或治疗本文中公开的疾病的全身性制剂,其包含至少0.01mg(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1mg至500mg己二酸和1mg至100mg l-羟丙基纤维素或由它们组成。
[0638]
本发明的一个优选实施方案涉及一种全身性制剂,其包含0.01mg至500mg(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药
学上可接受的盐、1mg至500mg己二酸和1mg至100mg l-羟丙基纤维素和/或羟丙基纤维素和至多100mg聚维酮k25或由它们组成。
[0639]
本发明的一个实施方案涉及一种全身性制剂,其包含0.01mg至500mg(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1mg至500mg己二酸、1mg至100mg l-羟丙基纤维素和羟丙基纤维素、至多100mg聚维酮k25、1mg至100mg交联羧甲基纤维素钠和1mg至50mg滑石粉或二氧化硅或由它们组成。
[0640]
本发明的一个实施方案涉及一种全身性制剂,其包含0.01mg至500mg(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1mg至360mg己二酸、10mg至40mg l-羟丙基纤维素、10mg至40mg交联羧甲基纤维素钠和1mg至20mg滑石粉或二氧化硅或由它们组成。
[0641]
本发明的一个实施方案涉及一种全身性制剂,其包含至少0.1mg(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1mg至500mg己二酸和1mg至100mg l-羟丙基纤维素或由它们组成。
[0642]
本发明的一个优选实施方案涉及一种全身性制剂,其包含0.1mg至500mg(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1mg至500mg己二酸和1mg至100mg l-羟丙基纤维素和/或羟丙基纤维素和至多100mg聚维酮k25或由它们组成。
[0643]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1mg至500mg(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1mg至500mg己二酸、1mg至100mg l-羟丙基纤维素和羟丙基纤维素、至多100mg聚维酮k25、1mg至100mg交联羧甲基纤维素钠和1mg至50mg滑石粉或二氧化硅或由它们组成。
[0644]
本发明的一个实施方案涉及一种全身性制剂,其包含0.1mg至500mg(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1mg至360mg己二酸、10mg至40mg l-羟丙基纤维素、10mg至40mg交联羧甲基纤维素钠和1mg至20mg滑石粉或二氧化硅或由它们组成。
[0645]
本发明的一个优选实施方案涉及一种全身性制剂,其包含0.5mg至500mg(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1mg至500mg己二酸和1mg至100mg l-羟丙基纤维素和/或羟丙基纤维素和至多100mg聚维酮k25或由它们组成。
[0646]
本发明的一个实施方案涉及一种全身性制剂,其包含0.5mg至500mg(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可
接受的盐、1mg至500mg己二酸、1mg至100mg l-羟丙基纤维素和羟丙基纤维素、至多100mg聚维酮k25、1mg至100mg交联羧甲基纤维素钠和1mg至50mg滑石粉或二氧化硅或由它们组成。
[0647]
本发明的一个实施方案涉及一种全身性制剂,其包含0.5mg至500mg(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1mg至360mg己二酸、10mg至40mg l-羟丙基纤维素、10mg至40mg交联羧甲基纤维素钠和1mg至20mg滑石粉或二氧化硅或由它们组成。
[0648]
本发明的一个优选实施方案涉及一种全身性制剂,其包含1mg至500mg(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1mg至500mg己二酸和1mg至100mg l-羟丙基纤维素和/或羟丙基纤维素和至多100mg聚维酮k25或由它们组成。
[0649]
本发明的一个实施方案涉及一种全身性制剂,其包含1mg至500mg(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1mg至500mg己二酸、1mg至100mg l-羟丙基纤维素和羟丙基纤维素、至多100mg聚维酮k25、1mg至100mg交联羧甲基纤维素钠和1mg至50mg滑石粉或二氧化硅或由它们组成。
[0650]
本发明的一个实施方案涉及一种全身性制剂,其包含1mg至500mg(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1mg至360mg己二酸、10mg至40mg l-羟丙基纤维素、10mg至40mg交联羧甲基纤维素钠和1mg至20mg滑石粉或二氧化硅或由它们组成。
[0651]
本发明的一个实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和1-15质量/质量的酸化剂或由它们组成,其中相对于(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐的质量计算所述化合物的质量/质量(质量比)。
[0652]
本发明的一个优选实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和11.5至1.5质量/质量的酸化剂或由它们组成,其中相对于(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐的质量计算所述化合物的质量/质量(质量比)。
[0653]
本发明的一个优选实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和
11.5至1.8质量/质量的酸化剂或由它们组成,其中相对于(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐的质量计算所述化合物的质量/质量(质量比)。
[0654]
本发明的一个优选实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和0.1至7质量/质量的聚合物沉淀抑制剂或由它们组成,其中相对于(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐的质量计算所述化合物的质量/质量(质量比)。
[0655]
本发明的一个优选实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和0.2至5质量/质量的聚合物沉淀抑制剂或由它们组成,其中相对于(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐的质量计算所述化合物的质量/质量(质量比)。
[0656]
本发明的一个优选实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1-15质量/质量的酸化剂和0.1至7质量/质量的聚合物沉淀抑制剂或由它们组成,其中相对于(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐的质量计算所述化合物的质量/质量(质量比)。
[0657]
本发明的一个优选实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、11.5至1.5质量/质量的酸化剂和0.1至7质量/质量的聚合物沉淀抑制剂或由它们组成,其中相对于(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐的质量计算所述化合物的质量/质量(质量比)。
[0658]
本发明的一个优选实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、11.5至1.8质量/质量的酸化剂和0.1至7质量/质量的聚合物沉淀抑制剂或由它们组成,其中相对于(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐的质量计算所述化合物的质量/质量(质量比)。
[0659]
本发明的一个优选实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1-15质量/质量的酸化剂和0.2至5质量/质量的聚合物沉淀抑制剂或由它们组成,其中相对于(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐的质量计算所述化合物的质量/质量(质量比)。
[0660]
本发明的一个优选实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、11.5至1.5质量/质量的酸化剂和0.2至5质量/质量的聚合物沉淀抑制剂或由它们组成,其中相对于(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐的质量计算所述化合物的质量/质量(质量比)。
[0661]
本发明的一个优选实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、11.5至1.8质量/质量的酸化剂和0.2至5质量/质量的聚合物沉淀抑制剂或由它们组成,其中相对于(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐的质量计算所述化合物的质量/质量(质量比)。
[0662]
本发明的一个优选实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1-15质量/质量的酸化剂、0.1至7质量/质量的聚合物沉淀抑制剂、0-5质量/质量的粘合剂、0.1至7质量/质量的崩解剂和0.05至2质量/质量的润滑剂/助流剂或由它们组成,其中相对于(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐的质量计算所述化合物的质量/质量(质量比)。
[0663]
本发明的一个优选实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、11.5至1.5质量/质量的酸化剂、0.1至7质量/质量的聚合物沉淀抑制剂、0-5质量/质量的粘合剂、0.1至7质量/质量的崩解剂和0.05至2质量/质量的润滑剂/助流剂或由它们组成,其中相对于(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐的质量计算所述化合物的质量/质量(质量比)。
[0664]
本发明的一个优选实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲
酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、11.5至1.8质量/质量的酸化剂、0.1至7质量/质量的聚合物沉淀抑制剂、0-5质量/质量的粘合剂、0.1至7质量/质量的崩解剂和0.05至2质量/质量的润滑剂/助流剂或由它们组成,其中相对于(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐的质量计算所述化合物的质量/质量(质量比)。
[0665]
本发明的一个优选实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1-15质量/质量的酸化剂、0.2至5质量/质量的聚合物沉淀抑制剂、0-5质量/质量的粘合剂、0.1至7质量/质量的崩解剂和0.05至2质量/质量的润滑剂/助流剂或由它们组成,其中相对于(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐的质量计算所述化合物的质量/质量(质量比)。
[0666]
本发明的一个优选实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、11.5至1.5质量/质量的酸化剂、0.2至5质量/质量的聚合物沉淀抑制剂、0-5质量/质量的粘合剂、0.1至7质量/质量的崩解剂和0.05至2质量/质量的润滑剂/助流剂或由它们组成,其中相对于(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐的质量计算所述化合物的质量/质量(质量比)。
[0667]
本发明的一个优选实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、11.5至1.8质量/质量的酸化剂、0.2至5质量/质量的聚合物沉淀抑制剂、0-5质量/质量的粘合剂、0.1至7质量/质量的崩解剂和0.05至2质量/质量的润滑剂/助流剂或由它们组成,其中相对于(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐的质量计算所述化合物的质量/质量(质量比)。
[0668]
本发明的一个优选实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1-15质量/质量的酸化剂、0.1至7质量/质量的聚合物沉淀抑制剂、0-2质量/质量的粘合剂、0.1至7质量/质量的崩解剂和0.05至2质量/质量的润滑剂/助流剂或由它们组成,其中相对于(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐的质量计算所述化合物的质量/质量(质量比)。
[0669]
本发明的一个优选实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙
基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、11.5至1.5质量/质量的酸化剂、0.1至7质量/质量的聚合物沉淀抑制剂、0-2质量/质量的粘合剂、0.1至7质量/质量的崩解剂和0.05至2质量/质量的润滑剂/助流剂或由它们组成,其中相对于(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐的质量计算所述化合物的质量/质量(质量比)。
[0670]
本发明的一个优选实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、11.5至1.8质量/质量的酸化剂、0.1至7质量/质量的聚合物沉淀抑制剂、0-2质量/质量的粘合剂、0.1至7质量/质量的崩解剂和0.05至2质量/质量的润滑剂/助流剂或由它们组成,其中相对于(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐的质量计算所述化合物的质量/质量(质量比)。
[0671]
本发明的一个优选实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1-15质量/质量的酸化剂、0.1至7质量/质量的聚合物沉淀抑制剂、0-5质量/质量的粘合剂、0.1至7质量/质量的崩解剂和0.1至1.5质量/质量的润滑剂/助流剂或由它们组成,其中相对于(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐的质量计算所述化合物的质量/质量(质量比)。
[0672]
本发明的一个优选实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、11.5至1.5质量/质量的酸化剂、0.1至7质量/质量的聚合物沉淀抑制剂、0-5质量/质量的粘合剂、0.1至7质量/质量的崩解剂和0.1至1.5质量/质量的润滑剂/助流剂或由它们组成,其中相对于(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐的质量计算所述化合物的质量/质量(质量比)。
[0673]
本发明的一个优选实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、11.5至1.8质量/质量的酸化剂、0.1至7质量/质量的聚合物沉淀抑制剂、0-5质量/质量的粘合剂、0.1至7质量/质量的崩解剂和0.1至1.5质量/质量的润滑剂/助流剂或由它们组成,其中相对于(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐的质量计算所述化合物的质量/质量(质量比)。
[0674]
本发明的一个优选实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1-15质量/质量的酸化剂、0.1至7质量/质量的聚合物沉淀抑制剂、0-5质量/质量的粘合剂、0.2至5质量/质量的崩解剂和0.05至2质量/质量的润滑剂/助流剂或由它们组成,其中相对于(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐的质量计算所述化合物的质量/质量(质量比)。
[0675]
本发明的一个优选实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、11.5至1.5质量/质量的酸化剂、0.1至7质量/质量的聚合物沉淀抑制剂、0-5质量/质量的粘合剂、0.2至5质量/质量的崩解剂和0.05至2质量/质量的润滑剂/助流剂或由它们组成,其中相对于(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐的质量计算所述化合物的质量/质量(质量比)。
[0676]
本发明的一个优选实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、11.5至1.8质量/质量的酸化剂、0.1至7质量/质量的聚合物沉淀抑制剂、0-5质量/质量的粘合剂、0.2至5质量/质量的崩解剂和0.05至2质量/质量的润滑剂/助流剂或由它们组成,其中相对于(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐的质量计算所述化合物的质量/质量(质量比)。
[0677]
本发明的一个优选实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1-15质量/质量的酸化剂、0.1至7质量/质量的聚合物沉淀抑制剂、0-5质量/质量的粘合剂、0.1至7质量/质量的崩解剂、0.05至2质量/质量的润滑剂/助流剂、0-5质量/质量的稀释剂/填充剂/粘合剂和0质量/质量至25质量/质量的其它成分或由它们组成,其中相对于(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐的质量计算所述化合物的质量/质量(质量比)。
[0678]
本发明的一个优选实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、11.5至1.8质量/质量的酸化剂、0.2至5质量/质量的聚合物沉淀抑制剂、0-2质量/质量的粘合剂、0.2至5质量/质量的崩解剂和0.05至2质量/质量的润滑剂/助流剂或由它们组成,其中相对于(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基
咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、11.5至1.8质量/质量的己二酸和0.2至5质量/质量的l-羟丙基纤维素和/或羟丙基纤维素或由它们组成,其中相对于(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐的质量计算所述化合物的质量/质量(质量比)。
[0684]
本发明的另一个优选实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、1-15质量/质量的己二酸、0.1至7质量/质量的l-羟丙基纤维素和/或羟丙基纤维素、0-2质量/质量的聚维酮k25、0.2至5质量/质量的交联羧甲基纤维素钠和0.05至2质量/质量的滑石粉或二氧化硅或由它们组成,其中相对于(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐的质量计算所述化合物的质量/质量(质量比)。
[0685]
本发明的另一个特别优选的实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、11.5至1.8质量/质量的己二酸、0.2至5质量/质量的l-羟丙基纤维素和/或羟丙基纤维素、0至1.5质量/质量的聚维酮k25、0.2至5质量/质量的交联羧甲基纤维素钠和0.1至1.2质量/质量的滑石粉或二氧化硅或由它们组成,其中相对于(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐的质量计算所述化合物的质量/质量(质量比)。
[0686]
优选的是,所述酸化剂相对于(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐的质量的质量比的范围为从11.5至1质量/质量,且所述聚合物沉淀抑制剂相对于(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐的质量的质量比的范围为从0.2至5质量/质量。
[0687]
更优选的是,所述酸化剂相对于(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐的质量的质量比的范围为从11.5至1.8质量/质量,且所述聚合物沉淀抑制剂相对于(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐的质量的质量比的范围为从0.2至5质量/质量。
[0688]
所述酸化剂和所述聚合物沉淀抑制剂之间的质量比可以从0.01质量/质量至20质
量/质量变化,优选从0.02质量/质量至15质量/质量,更优选从0.03质量/质量至12.5质量/质量,甚至更优选从0.04质量/质量至10质量/质量,甚至更优选从0.05质量/质量,甚至更优选从0.06质量/质量至9质量/质量,甚至更优选从0.07质量/质量至8质量/质量,甚至更优选从0.08质量/质量至7质量/质量,甚至更优选从0.09质量/质量至6质量/质量,甚至更优选从0.1质量/质量至5质量/质量,甚至更优选从0.1质量/质量至4.5质量/质量,甚至更优选从0.1质量/质量至4质量/质量,甚至更优选从0.1质量/质量至3.5质量/质量,且最优选从0.1质量/质量至3质量/质量,其中相对于所述制剂中的酸化剂的质量计算所述质量比。
[0689]
本发明的一个优选实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、酸化剂和聚合物沉淀抑制剂或由它们组成,其中所述溶液稳定剂和所述酸化剂之间的质量比的范围为从0.01至6质量/质量,且其中相对于所述酸化剂的质量计算所述化合物的质量/质量(质量比)。
[0690]
优选地,根据本发明的制剂未被包括在可植入泵中。通过渗透泵的施用不适用于人。
[0691]
本发明的一个优选实施方案涉及一种全身性制剂,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、酸化剂和聚合物沉淀抑制剂或由它们组成,其中所述溶液稳定剂和所述酸化剂之间的质量比的范围为从0.05至3.5质量/质量,且其中相对于所述酸化剂的质量计算所述化合物的质量/质量(质量比)。
[0692]
优选地,根据本发明的制剂未被包括在可植入泵中。通过渗透泵的施用不适用于人。
[0693]
优选地,在施用后(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐在血浆或组织中的最大浓度(cmax-值)是0.2ng/ml至2000ng/ml,且其中通过与质谱法偶联的液相色谱法测量在血浆样品中的cmax-值。
[0694]
抑制作用依赖于最大血浆或组织浓度(cmax-值)。
[0695]
本发明的另一个方面涉及用于用作药物的根据本发明的制剂,优选用于哺乳动物,且最优选用于人。
[0696]
本发明的一个优选实施方案涉及用于预防和/或治疗tg2相关疾病的全身性制剂。优选地所述tg2相关疾病选自包含以下成员或由以下成员组成的集合:肾病、纤维化肝病(包括nafld、nash)、肝硬化、胆汁淤积性肝疾病诸如原发性硬化性胆管炎(psc)和原发性胆汁性胆管炎(pbc)、自身免疫性肝炎(aih)、酒精性脂肪性肝炎(ash)、囊性纤维化、肺纤维化、特发性肺纤维化、辐射诱导的肺损伤、桥接纤维化、心脏纤维化、全身性硬化症、胶原诱发的关节炎(cia)、类风湿性关节炎(ra)、心房纤维化、心内膜心肌纤维化、陈旧性心肌梗塞、血管硬化、血管钙化、纤维增生性疾病、血压升高、胶质瘢痕、动脉僵硬、关节纤维化、杜
普伊特伦氏挛缩、瘢痕疙瘩、纵隔纤维化、骨髓纤维化、佩罗尼氏病、肾原性全身性纤维化、iga肾病、进行性块状纤维化、腹膜后纤维化、全身性硬化症和粘连性囊炎(adhersisve capsulitis),优选地在人中。最优选地所述tg2相关疾病选自肾病、nash、囊性纤维化和糖尿病有关的纤维化。
[0697]
本发明的一个更优选实施方案涉及用于预防和/或治疗中的全身性制剂,其中所述tg2相关疾病选自包含以下成员或由以下成员组成的集合:肾病、纤维化肝病(包括nafld、nash)、肝硬化、胆汁淤积性肝疾病诸如原发性硬化性胆管炎(psc)和原发性胆汁性胆管炎(pbc)、自身免疫性肝炎(aih)、酒精性脂肪性肝炎(ash)和/或囊性纤维化、肺纤维化、特发性肺纤维化、心脏纤维化、全身性硬化症、胶原诱发的关节炎(cia)、类风湿性关节炎(ra)、iga肾病(iga-n)、血管硬化、血管钙化、纤维增生性疾病和血压升高,优选地在人中。
[0698]
根据本发明的一个优选实施方案涉及用于预防和/或治疗纤维化的全身性制剂,优选地在人中。
[0699]
因此,本发明的另一个方面涉及用于预防和/或治疗纤维化的式(i)的化合物,优选地在人中。
[0700]
本发明的另一个方面涉及用于预防和/或治疗纤维化的式(i)的化合物的盐,优选地在人中。
[0701]
本发明的再另一个方面涉及用于预防和/或治疗纤维化的式(i)的化合物和己二酸的盐,优选地在人中。
[0702]
纤维化更优选地与糖尿病病症背景下的纤维化变化有关。因此,本发明的一个特别优选的实施方案涉及一种制剂,优选全身性制剂,更优选肠内制剂,且最优选根据本发明的口服制剂,其用于预防和/或治疗糖尿病性肾病、糖尿病相关的非酒精性脂肪性肝炎和/或囊性纤维化有关的糖尿病。因此,在本发明的一个优选实施方案中,所述tg2相关疾病选自由以下成员组成的集合:肾病、nash和/或囊性纤维化。在本发明的另一个优选实施方案中,所述tg2相关疾病包含糖尿病有关的纤维化或由它们组成。
[0703]
本发明的一个实施方案涉及用于预防和/或治疗疾病的根据本发明的制剂,所述疾病选自包含以下成员或由以下成员组成的集合:肾病、nash和/或囊性纤维化。
[0704]
本发明的另一个方面涉及一种用于制备根据本发明的制剂的方法,所述方法包含以下步骤:
[0705]
a-1)提供(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐。
[0706]
在上面提及了在步骤a-1)中提供的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐的量。
[0707]
因此,本发明的一个实施方案涉及一种用于制备根据本发明的制剂的方法,所述方法包含以下步骤:
[0708]
a-1)提供1mg至500g(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对
映异构体、溶剂化物、水合物或药学上可接受的盐。
[0709]
因此,本发明的一个实施方案涉及一种用于制备根据本发明的制剂的方法,所述方法包含以下步骤:
[0710]
a-1)提供1mg至500g(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐。
[0711]
本发明的另一个实施方案涉及一种用于制备根据本发明的制剂的方法,所述方法包含以下步骤:
[0712]
a-1)提供0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐。
[0713]
显然,所述药物的量还可以被上面提及的另一个量替代。
[0714]
在步骤a-2)中,加入至少一种如本文中所述的赋形剂。优选地,至少一种赋形剂是聚合物沉淀抑制剂优选l-羟丙基纤维素、崩解剂或稀释剂/填充剂/粘合剂。
[0715]
因此,根据本发明的一个实施方案涉及一种用于制备根据本发明的制剂的方法,所述方法包含以下步骤:
[0716]
a-1)提供(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐,和
[0717]
a-2)加入至少一种赋形剂。
[0718]
在步骤a-2’)中,将(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、聚合物沉淀抑制剂优选l-羟丙基纤维素和崩解剂优选交联羧甲基纤维素钠以干燥状态过筛,优选地分开过筛。
[0719]
因此,根据本发明的一个实施方案涉及一种用于制备根据本发明的制剂的方法,所述方法包含以下步骤:
[0720]
a-1)提供(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐,和
[0721]
a-2’)将(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、聚合物沉淀抑制剂和崩解剂以干燥状态过筛,优选地分开过筛。
[0722]
在上面提及了在步骤a-2’)中的崩解剂、聚合物沉淀抑制剂和崩解剂的量。
[0723]
因此,根据本发明的一个实施方案涉及一种用于制备根据本发明的制剂的方法,所述方法包含以下步骤:
[0724]
a-1)提供1mg至500mg(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐,和
[0725]
a-2’)将(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、10mg至50mg聚合物沉淀抑制剂和10mg至40mg崩解剂以干燥状态过筛,优选地分开过筛。
[0726]
根据本发明的一个优选实施方案涉及一种用于制备根据本发明的制剂的方法,所述方法包含以下步骤:
[0727]
a-1)提供1mg至500mg(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐,和
[0728]
a-2’)将(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、10mg至50mg l-羟丙基纤维素和10mg至40mg交联羧甲基纤维素钠以干燥状态过筛,优选地分开过筛。
[0729]
根据本发明的另一个优选实施方案涉及一种用于制备根据本发明的制剂的方法,所述方法包含以下步骤:
[0730]
a-1)提供0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐,和
[0731]
a-2’)将(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、0.1重量%至40重量%的聚合物沉淀抑制剂和2重量%至15重量%的崩解剂以干燥状态过筛,优选地分开过筛。
[0732]
根据本发明的另一个更优选的实施方案涉及一种用于制备根据本发明的制剂的方法,所述方法包含以下步骤:
[0733]
a-1)提供0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐,和
[0734]
a-2’)将(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、0.1重量%至40重量%的l-羟丙基纤维素和/聚维酮k25和2重量%至15重量%的交联羧甲基纤维素钠以干燥状态过筛,优选地分开过筛。
[0735]
显然,所述赋形剂和所述药物的量还可以被上面提及的另一个量替代。
[0736]
在步骤a-3)中,可以加入溶剂,其导致颗粒团聚和颗粒结构的形成。优选地,所述溶剂是乙醇。
[0737]
因此,根据本发明的一个实施方案涉及一种用于制备根据本发明的制剂的方法,所述方法包含以下步骤:
[0738]
a-1)提供(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐,
[0739]
a-2)加入至少一种赋形剂,和
[0740]
a-3)加入溶剂,其导致颗粒团聚和颗粒结构的形成。
[0741]
因此,根据本发明的一个实施方案涉及一种用于制备根据本发明的制剂的方法,所述方法包含以下步骤:
[0742]
a-1)提供(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐,和
[0743]
a-2’)将(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、聚合物沉淀抑制剂和崩解剂以干燥状态过筛,和
[0744]
a-3)加入溶剂,其导致颗粒团聚和颗粒结构的形成。
[0745]
在步骤a-4)中,可以将颗粒块以湿状态过筛,优选步骤a-3)的颗粒块。
[0746]
因此,根据本发明的一个实施方案涉及一种用于制备根据本发明的制剂的方法,所述方法包含以下步骤:
[0747]
a-1)提供(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐,和
[0748]
a-2’)将(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、聚合物沉淀抑制剂和崩解剂以干燥状态过筛,
[0749]
a-3)加入溶剂,其导致颗粒团聚和颗粒结构的形成,和
[0750]
a-4)将步骤a-3)的颗粒块以湿状态过筛。
[0751]
在步骤a-5)中,将处于湿状态的颗粒块干燥,其中接收干燥的颗粒。
[0752]
因此,根据本发明的一个实施方案涉及一种用于制备根据本发明的制剂的方法,所述方法包含以下步骤:
[0753]
a-1)提供(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐,和
[0754]
a-2’)将(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、聚合物沉淀抑制剂和崩解剂以干燥状态过筛,
[0755]
a-3)加入溶剂,其导致颗粒团聚和颗粒结构的形成,
[0756]
a-4)将步骤a-3)的颗粒块以湿状态过筛,和
[0757]
a-5)干燥处于湿状态的颗粒块。
[0758]
在步骤b-1)中,可以将赋形剂优选己二酸和/或滑石粉加入干燥的颗粒,并优选地在干燥的混合器中混合,从而形成粉末混合物。
[0759]
因此,根据本发明的一个实施方案涉及一种用于制备根据本发明的制剂的方法,所述方法包含以下步骤:
[0760]
a-1)提供(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡
啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐,和
[0761]
b-1)加入至少一种赋形剂。
[0762]
因此,根据本发明的一个实施方案涉及一种用于制备根据本发明的制剂的方法,所述方法包含以下步骤:
[0763]
a-1)提供(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐,
[0764]
a-2)加入至少一种赋形剂,和
[0765]
a-3)加入溶剂,其导致颗粒团聚和颗粒结构的形成。
[0766]
b-1)加入至少一种赋形剂。
[0767]
因此,根据本发明的一个实施方案涉及一种用于制备根据本发明的制剂的方法,所述方法包含以下步骤:
[0768]
a-1)提供(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐,和
[0769]
a-2’)将(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、聚合物沉淀抑制剂和崩解剂以干燥状态过筛,
[0770]
a-3)加入溶剂,其导致颗粒团聚和颗粒结构的形成,
[0771]
a-4)将步骤a-3)的颗粒块以湿状态过筛,
[0772]
a-5)干燥处于湿状态的颗粒块,和
[0773]
b-1)将至少一种赋形剂诸如酸化剂优选己二酸和/或润滑剂/助流剂优选滑石粉或二氧化硅加入干燥的颗粒。
[0774]
因此,根据本发明的一个实施方案涉及一种用于制备根据本发明的制剂的方法,所述方法包含以下步骤:
[0775]
a-1)提供1mg至500mg(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐,和
[0776]
a-2’)将(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、10mg至50mg聚合物沉淀抑制剂和10mg至40mg崩解剂以干燥状态过筛,
[0777]
a-3)加入溶剂,其导致颗粒团聚和颗粒结构的形成,
[0778]
a-4)将步骤a-3)的颗粒块以湿状态过筛,
[0779]
a-5)干燥处于湿状态的颗粒块,和
[0780]
b-1)将10-360mg酸化剂和/或1mg至20mg润滑剂/助流剂优选滑石粉或二氧化硅加入干燥的颗粒。
[0781]
因此,根据本发明的一个实施方案涉及一种用于制备根据本发明的制剂的方法,
所述方法包含以下步骤:
[0782]
a-1)提供0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐,和
[0783]
a-2’)将(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、0.1重量%至40重量%的聚合物沉淀抑制剂和2重量%至15重量%的崩解剂以干燥状态过筛,
[0784]
a-3)加入溶剂,其导致颗粒团聚和颗粒结构的形成,
[0785]
a-4)将步骤a-3)的颗粒块以湿状态过筛,
[0786]
a-5)干燥处于湿状态的颗粒块,和
[0787]
b-1)将5重量%至75重量%的酸化剂和/或0.1重量%至10重量%的润滑剂/助流剂优选滑石粉或二氧化硅加入干燥的颗粒。
[0788]
根据本发明的一个优选实施方案涉及一种用于制备根据本发明的制剂的方法,所述方法包含以下步骤:
[0789]
a-1)提供1mg至500mg(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐,和
[0790]
a-2’)将(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、10mg至50mg l-羟丙基纤维素和/或聚维酮k25和10mg至40mg交联羧甲基纤维素钠以干燥状态过筛,优选地分开过筛。
[0791]
a-3)加入溶剂,其导致颗粒团聚和颗粒结构的形成,
[0792]
a-4)将步骤a-3)的颗粒块以湿状态过筛,
[0793]
a-5)干燥处于湿状态的颗粒块,和
[0794]
b-1)将10-360mg己二酸和1mg至20mg滑石粉或二氧化硅加入干燥的颗粒。
[0795]
根据本发明的另一个更优选的实施方案涉及一种用于制备根据本发明的制剂的方法,所述方法包含以下步骤:
[0796]
a-1)提供0.1重量%至80重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐,和
[0797]
a-2’)将(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、0.1重量%至40重量%的l-羟丙基纤维素和/或聚维酮k25和2重量%至15重量%的交联羧甲基纤维素钠以干燥状态过筛,优选地分开过筛。
[0798]
a-3)加入溶剂,其导致颗粒团聚和颗粒结构的形成,
[0799]
a-4)将步骤a-3)的颗粒块以湿状态过筛,
[0800]
a-5)干燥处于湿状态的颗粒块,和
[0801]
b-1)将5重量%至75重量%的己二酸和0.1重量%至10重量%的滑石粉或二氧化
硅加入干燥的颗粒。
[0802]
在步骤b-1’)中,优选地可以将赋形剂酸化剂和/或润滑剂/助流剂过筛,如果将两种赋形剂过筛,优选地分开过筛。
[0803]
因此,根据本发明的一个实施方案涉及一种用于制备根据本发明的制剂的方法,所述方法包含以下步骤:
[0804]
a-1)提供(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐,和
[0805]
a-2’)将(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、聚合物沉淀抑制剂和崩解剂以干燥状态过筛,
[0806]
a-3)加入溶剂,其导致颗粒团聚和颗粒结构的形成,
[0807]
a-4)将步骤a-3)的颗粒块以湿状态过筛,
[0808]
a-5)干燥处于湿状态的颗粒块,
[0809]
b-1’)将酸化剂和润滑剂/助流剂诸如滑石粉或二氧化硅过筛,和
[0810]
b-1)将过筛的酸化剂和润滑剂/助流剂加入干燥的颗粒。
[0811]
根据本发明的一个优选实施方案涉及一种用于制备根据本发明的制剂的方法,所述方法包含以下步骤:
[0812]
a-1)提供1mg至500mg化合物(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐,和
[0813]
a-2’)将(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、10mg至50mg聚合物沉淀抑制剂和10mg至40mg崩解剂以干燥状态过筛,
[0814]
a-3)加入溶剂,其导致颗粒团聚和颗粒结构的形成,
[0815]
a-4)将步骤a-3)的颗粒块以湿状态过筛,
[0816]
a-5)干燥处于湿状态的颗粒块,
[0817]
b-1’)将10-360mg酸化剂和1mg至20mg润滑剂/助流剂诸如滑石粉或二氧化硅过筛,和
[0818]
b-1)将过筛的酸化剂和润滑剂/助流剂加入干燥的颗粒。
[0819]
根据本发明的另一个优选实施方案涉及一种用于制备根据本发明的制剂的方法,所述方法包含以下步骤:
[0820]
a-1)提供0.1重量%至80重量%的化合物(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐,和
[0821]
a-2’)将(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、0.1重量%至40重量%的聚合物沉淀抑制剂和2重
1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯的药物组合物,其用作肝保护剂和用于保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤,和/或用于预防或治疗肝障碍/疾病,如通过降低肝酶的血清水平所证明的。
[0843]
发明背景
[0844]
肝脏不仅参与代谢和解毒,而且参与先天性免疫功能,并因此经常暴露于可能导致躯体损伤的有害影响。令人感兴趣的是,肝脏具有独特的再生能力并从最急性、非反复的情况中完全恢复。但是,包括病毒性肝炎、非酒精性脂肪肝疾病、长期酒精滥用和药物长期使用在内的多种情况可以造成持续性损伤,其中再生能力最终变得功能失调,从而导致肝瘢痕和肝硬化。尽管现代医学不断取得治疗进步和发展,但肝病仍然是世界范围内的健康问题。
[0845]
肝脏是参与食物和药物的生物转化的主要器官。肝病是一个世界性的重大问题。由于过量的药物或外源性物质,肝毒性的最常见形式是肝脏的机能障碍或损伤。肝毒物是具有临床关联性的外源性试剂,其可能包括某些药物化合物、工业化学品等的剂量过量,这会造成肝损伤。
[0846]
药物诱发的肝损伤的确切机制仍然在很大程度上是未知的,但它似乎涉及两种途径——直接的肝毒性(a型或dili1(药物诱发的肝损伤1),内在的或可预测的药物反应)和间接的肝毒性(b型或dili2(药物诱发的肝损伤2),不可预测的或特殊的药物反应)或不利的免疫反应。
[0847]
肝毒性可能导致细胞毒性效应(坏死、细胞凋亡)、胆汁淤积、脂肪变性、纤维化、肝硬化、肝炎和肝肿瘤。肝毒性相关症状可能包括黄疸(jaundice或icterus)外观(从而造成皮肤、眼睛的变黄)和严重腹部疼痛、恶心或呕吐、虚弱、严重疲劳、持续出血、皮疹、全身瘙痒、脚和/或腿的肿胀、在短时间内的异常和快速体重增加、尿色深、大便颜色浅。血清中各种肝酶的增加被认为是肝毒性的标志。
[0848]
本发明的另一个目的是提供一种化合物,其用于用作肝保护剂(即肝保护性药剂),和用于保护肝脏免于肝毒性,改善肝功能,保护/修复肝损伤,和/或预防或治疗肝障碍/疾病。
[0849]
独立权利要求的教导解决了本发明的目的。根据从属权利要求、说明书、附图和本技术的实施例,本发明的其它有利特征、方面和细节是显而易见的。
[0850]
发明内容
[0851]
本发明的目的通过式(i)的化合物(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或式(i)的对映异构体、溶剂化物、水合物或药学上可接受的盐作为肝保护剂(即作为肝保护性药剂)的用途得到解决:
[0852][0853]
在一个实施方案中,本发明涉及用于保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤和/或预防或治疗肝障碍/疾病的式(i)的化合物。
[0854]
在一个实施方案中,本发明涉及用于保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤和/或预防或治疗肝障碍/疾病的式(i)的化合物,其中所述化合物降低至少一种肝酶的血清水平,优选地所述至少一种肝酶选自丙氨酸氨基转移酶(alt)、天冬氨酸氨基转移酶(ast)和碱性磷酸酶(alp)。
[0855]
在一个实施方案中,本发明涉及用于预防或治疗肝障碍/疾病的式(i)的化合物,其中所述肝障碍/疾病是肝纤维化、酒精性肝炎、非酒精性脂肪性肝炎(nash)、非酒精性脂肪肝疾病(nafld)、肝硬化、胆汁淤积性肝疾病诸如原发性硬化性胆管炎(psc)和原发性胆汁性胆管炎(pbc)、自身免疫性肝炎(aih)、酒精性脂肪性肝炎(ash)或肝炎症。
[0856]
在一个实施方案中,本发明涉及用于保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤和/或预防或治疗肝障碍/疾病的式(i)的化合物,其中所述肝毒性、所述肝损伤或所述肝障碍/疾病由至少一种肝毒物造成,优选地所述至少一种肝毒物选自包含以下成员或由以下成员组成的集合:有毒的化学物质、外源性物质、抗癌药物、免疫抑制药物、镇痛药物、抗炎药物、抗结核药物、生物制品、辐射、重金属、真菌毒素、半乳糖胺和脂多糖。
[0857]
在一个实施方案中,本发明涉及与一种或多种治疗剂联合用于预防或治疗肝障碍/疾病的式(i)的化合物,其中所述肝障碍/疾病是肝纤维化。
[0858]
在一个实施方案中,本发明涉及用于所述用途的式(i)的化合物,其中口服施用所述化合物。
[0859]
本发明的另一个方面涉及一种用于用作肝保护剂的药物组合物,其包含
[0860]
式(i)的化合物(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯:
[0861][0862]
或其对映异构体、溶剂化物、水合物或药学上可接受的盐。
[0863]
优选地,所述药物组合物可用于保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤和/或预防或治疗肝障碍/疾病。
[0864]
优选地,所述肝毒性或所述肝损伤、所述肝障碍/疾病由至少一种肝毒物、乳糜泻或病毒感染造成。
[0865]
具体地,所述至少一种肝毒物选自包含以下成员或由以下成员组成的集合:有毒的化学物质、外源性物质、抗癌药物、免疫抑制药物、镇痛药物、抗炎药物、抗结核药物、生物制品、辐射、重金属、真菌毒素、半乳糖胺和脂多糖;与特定遗传表型(hla dq2/dq8)和由转谷氨酰胺酶2(tg2)促进的病理学相关的乳糜泻;和/或甲型、乙型、丙型肝炎病毒的病毒感染。
[0866]
在一个实施方案中,本发明涉及所述用于保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤和/或预防或治疗肝障碍/疾病的药物组合物,其中所述化合物降低至少一种肝酶的血清水平,优选地所述至少一种肝酶选自丙氨酸氨基转移酶(alt)、天冬氨酸氨基转移酶(ast)和碱性磷酸酶(alp)。
[0867]
在一个实施方案中,本发明涉及所述用于保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤和/或预防或治疗肝障碍/疾病的药物组合物,其中所述肝障碍/疾病是肝纤维化、酒精性肝炎、非酒精性脂肪性肝炎(nash)、非酒精性脂肪肝疾病(nafld)、肝硬化、胆汁淤积性肝疾病诸如原发性硬化性胆管炎(psc)和原发性胆汁性胆管炎(pbc)、自身免疫性肝炎(aih)、酒精性脂肪性肝炎(ash)或肝炎症。
[0868]
在一个实施方案中,本发明涉及所述用于保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤和/或预防或治疗肝障碍/疾病的药物组合物,其中所述药物组合物进一步包含至少一种聚合物沉淀抑制剂。
[0869]
优选地,所述至少一种聚合物沉淀抑制剂选自由以下成员组成的集合:l-羟丙基纤维素、羟丙基纤维素、l-羟丙基纤维素和羟丙基纤维素的组合、聚乙二醇、聚(环氧乙烷)-聚(环氧丙烷)-聚(环氧乙烷)、聚乙烯醇、聚乙烯吡咯烷酮、羧甲基纤维素、甲基纤维素、羟乙基纤维素、羟丙基甲基纤维素、乙基纤维素、聚乙烯醇(pva)、聚乙烯基己内酰胺-聚乙酸乙烯酯-聚乙二醇接枝共聚物和羧甲基纤维素钠。
[0870]
在一个实施方案中,本发明涉及用于所述用途的药物组合物,其中所述药物组合物进一步包含至少一种酸化剂和/或至少一种粘合剂。
[0871]
在一个优选实施方案中,本发明涉及所述用于保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤和/或预防或治疗肝障碍/疾病的药物组合物,其中所述至少一种酸化剂选自由以下成员组成的集合:抗坏血酸、有机二羧酸诸如草酸、丙二酸、琥珀酸、戊二酸、酒石酸、富马酸、马来酸、苹果酸、己二酸或谷氨酸、和有机三羧酸诸如柠檬酸或柠檬酸氢钠。
[0872]
在一个优选实施方案中,本发明涉及所述用于保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤和/或预防或治疗肝障碍/疾病的药物组合物,其中所述至少一种粘合剂选自由以下成员组成的集合:糖、蔗糖、多糖、黄原胶、瓜尔胶、角叉菜胶、从小麦、玉米、大米和马铃薯衍生出的淀粉、从小麦、玉米、大米和马铃薯衍生出的预凝(改性)淀粉、淀粉羟乙酸钠、天然树胶、金合欢胶、明胶、黄蓍胶、海藻的衍生物、海藻酸、海藻酸钠、海藻酸钙铵、纤维素、纤维素衍生物、羟丙基纤维素、l-羟丙基纤维素、低取代的羟丙基纤维素、甲基纤维素、羧甲基纤维素钠、羟丙基甲基纤维素、聚乙烯吡咯烷酮、聚维酮k25。
[0873]
在一个实施方案中,本发明涉及所述用于保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤和/或预防或治疗肝障碍/疾病的药物组合物,其中(s,e)-7-(1-(2-(2-乙基
丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯颗粒具有由d(0.95)≤25μm定义的粒度分布。
[0874]
在某些实施方案中,本发明涉及所述用于保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤和/或预防或治疗肝障碍/疾病的药物组合物,其中所述药物组合物是口服制剂,优选地所述口服制剂是片剂、胶囊剂、粉剂或颗粒剂。
[0875]
在一个优选实施方案中,本发明涉及所述用于保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤和/或预防或治疗肝障碍/疾病的药物组合物,其中所述药物组合物包含1-15质量/质量的酸化剂、0.1至7质量/质量的聚合物沉淀抑制剂,其中相对于(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯的质量计算所述化合物的质量/质量(质量比)。
[0876]
在一个优选实施方案中,本发明涉及用于保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤和/或预防或治疗肝障碍/疾病的药物组合物,其中所述药物组合物包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯、3重量%至75重量%的酸化剂、2重量%至35重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂和1重量%至9重量%的润滑剂/助流剂。
[0877]
在一个优选实施方案中,本发明涉及用于保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤和/或预防或治疗肝障碍/疾病的药物组合物,其中所述药物组合物包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯、3重量%至75重量%的己二酸、2重量%至35重量%的l-羟丙基纤维素和/或羟丙基纤维素、0重量%至12重量%的聚维酮k25、2重量%至35重量%的交联羧甲基纤维素钠和1重量%至9重量%的滑石粉或二氧化硅。
[0878]
在一个优选实施方案中,本发明涉及用于预防或治疗肝障碍/疾病的药物组合物,其中所述肝障碍/疾病是肝纤维化。
[0879]
发明描述
[0880]
本文中使用的术语“药学上可接受的盐”表示某种(些)成分的盐,其具有与未修饰的化合物相同的活性并且其在生物学上或在其它方面都不是不希望的。
[0881]
药学上可接受的盐可以与例如有机或无机酸形成。合适的酸包括乙酸、乙酰基水杨酸,有机二羧酸诸如草酸、丙二酸、琥珀酸、戊二酸、酒石酸、富马酸、马来酸、苹果酸、己二酸或谷氨酸,和有机三羧酸诸如柠檬酸或柠檬酸氢钠、海藻酸、抗坏血酸、天冬氨酸、苯甲酸、苯磺酸、亚硫酸(bisulfic acid)、硼酸、丁酸、樟脑酸、樟脑磺酸、碳酸、柠檬酸、环戊烷丙酸、二葡糖酸、十二烷基硫酸(dodecylsulfic acid)、乙磺酸、甲酸、富马酸、甘油酸、甘油磷酸、甘氨酸、葡萄糖庚酸、葡糖酸、谷氨酸、戊二酸、羟乙酸、、庚酸、己酸、半硫酸(hemisulfic acid)、马尿酸、氢溴酸、盐酸、氢碘酸、羟基乙磺酸、乳酸、马来酸、苹果酸、丙二酸、扁桃酸、甲磺酸、粘酸、萘磺酸(naphthylanesulfonic acid)、萘酸(naphthylic acid)、烟酸、亚硝酸、草酸、壬酸、磷酸、丙酸、糖精、水杨酸、山梨酸、琥珀酸、硫酸、酒石酸、硫氰酸、巯基乙酸、硫代硫酸、甲苯磺酸、十一烯酸、以及天然地和合成地衍生出的氨基酸。优选地,所述酸是己二酸、富马酸、戊二酸,更优选地,所述酸是己二酸。
[0882]
因此,一种优选的药学上可接受的盐是式(i)的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯和己二酸的盐
[0883][0884]
本文中使用的术语“溶剂化物”表示通过与溶剂分子配位形成复合物的化合物、特别是(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯的那些形式。
[0885]
本文中使用的术语“水合物”表示通过与水分子配位形成复合物的化合物、特别是(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯的那些形式。
[0886]
本文中使用的术语活性剂或药学活性剂或药物或活性药物成分(它们在本文中是同义的)的“有效量”或“治疗有效量”表示足以具有积极作用的活性剂或药学活性剂或药物或活性药物成分的量。因此,这些量对于治疗疾病是有效的,但足够低以避免严重的副作用。治疗有效量的药学活性剂在随时间重复应用时将造成症状的实质缓解。药学活性剂的有效量将随所治疗的一种或多种特定病症、病症的严重程度、治疗的持续时间、所使用的组合物的具体组分以及类似因素而变化。
[0887]
本文中使用的术语“活性剂”、“药学活性剂”、“药物”或“活性药物成分”、“治疗剂”(它们在本文中同义地使用)表示对哺乳动物、特别是人表现出治疗效果的化合物。
[0888]
本文中使用的术语“治疗”、“处理”或类似的语言表示这样的过程:(1)延迟正在造成临床症状的疾病的发作;(2)抑制疾病,即阻止临床症状的发展;和/或(3)缓解疾病,即造成临床症状或其严重程度的消退。
[0889]
本文中使用的术语“药物组合物”表示在施用后对哺乳动物表现出治疗效果的组合物。
[0890]
本文中使用的“口服制剂”表示是经口吸收的药物的制剂(口服(per os、orally、perorally)):片剂、糖衣丸、胶囊剂、汁液、滴剂等。这些药物在胃肠道被吸收到血液中,并然后通过门静脉系统进入肝脏中,并然后通过肝静脉进入血流中。本文中使用的该术语表示口服施用的制剂。
[0891]
肝障碍在本文中主要由肝毒物造成。“肝毒物”包括、但不限于有毒的化学物质(醇类)、外源性物质(四氯化碳、氯化烃、异氰酸盐、杀虫剂诸如杀昆虫剂、杀真菌剂、除草剂和去污剂诸如胆汁酸盐)、抗癌药物(硫唑嘌呤、多柔比星、顺铂)、免疫抑制药物(环孢菌素)、镇痛抗炎药物(对乙酰氨基酚、硫代乙酰胺)、抗结核药物(异烟肼、利福平)、生物制品(卡介苗疫苗)、辐射(γ辐射)、重金属(镉、砷)、真菌毒素(黄曲霉毒素)、半乳糖胺和脂多糖。肝损伤的各种危险因素包括伴随的肝疾病、年龄、性别、酒精中毒、营养物和细胞色素p
450
酶的遗
传多态性也已经被强调。
[0892]
评估肝保护活性的最常用参数是形态,例如肝脏重量和体积,生化估算诸如转氨酶活性、sgpt、scot、碱性磷酸酶、血清胆红素、总血清蛋白、白蛋白、球蛋白和凝血酶原时间、功能参数、戊巴比妥和海索比妥睡眠时间的测量,最后是关于坏死、脂肪变性和肝硬化的存在的组织病理学研究。
[0893]
为了鉴定各种与肝脏有关的疾病,几个试验项目被统称为肝功能试验。主要试验包括肝酶的血清水平的活性,包括丙氨酸转氨酶(alt)或血清谷氨酸-丙酮酸转氨酶(sgpt)、天冬氨酸转氨酶(ast)或血清谷氨酸草酰乙酸转氨酶(sgot)、γ-谷氨酰基转移酶(ggt)和碱性磷酸酶(alp)和胆红素。此外,有时试验总蛋白、白蛋白、ldh(乳酸脱氢酶)、氨等。
[0894]
在它们中,ast(got)和alt(gpt)是存在于肝细胞中的酶,并主要在肝细胞受损时释放到血液中。因此,血液ast和alt水平可以用作肝损伤的标志物。在急性肝细胞损伤的早期,ast(其具有高肝细胞浓度)比alt升高更多,但在24-48小时以后,和在慢性肝细胞损伤中,具有更长半衰期的alt通常更高。在酒精性肝炎中,ast进一步升高。
[0895]
令人惊讶的是,如在实施例14中的表4所示,证实了式(i)的化合物可以以剂量依赖性的方式降低血清中的丙氨酸氨基转移酶(alt)和天冬氨酸氨基转移酶(ast)、碱性磷酸酶(alp)浓度。这些结果指示,式(i)的化合物对肝损伤具有保护作用,并具有治疗肝损伤的潜力。
[0896]
乳糜泻的特征在于由转谷氨酰胺酶2(tg2)驱动的谷蛋白相关的病理学。但是,乳糜泻(一种谷蛋白不耐受症)是最普遍的胃肠道适应症之一。乳糜泻的特征在于小肠粘膜的慢性炎症。在相关患者中,在摄入含谷蛋白的食物后,肠上皮接连地被破坏,导致营养吸收减少,这再次对相关患者产生巨大影响,并且例如与诸如体重减轻、贫血、腹泻、恶心、食欲不振和疲劳等症状相关。
[0897]
对乳糜泻中肝损伤的潜在机制知之甚少。但是,氨基转移酶水平的升高是乳糜泻患者的特征性表现。在体内,用化合物1(作为转谷氨酰胺酶2(tg2)的不可逆抑制剂)以10、50和100mg的剂量在人中的口服治疗显著降低ast、alt、总蛋白的水平,并抑制两种酶肝细胞天冬氨酸氨基转移酶(ast)和丙氨酸氨基转移酶(alt)的细胞渗漏。
[0898]
在160名患有乳糜泻(ced)的成年患者中研究了用在实施例2所描述的硬明胶胶囊制剂中的式(i)的化合物进行的6周治疗的效力和安全性。在研究开始时处于临床和组织学缓解状态的患者接受每天3克谷蛋白摄入的挑战,并随机接受安慰剂或式(i)的化合物的3种剂量之一,即10mg、50mg或100mg。每天早上禁食至少6小时后,患者口服研究药物,随后在30分钟后,在早餐前吃一块含有3g谷蛋白的饼干。在为期6周的研究中,患者被要求继续他们的严格的无谷蛋白饮食。
[0899]
谷蛋白挑战造成在安慰剂组中从基线到第6周丙氨酸氨基转移酶(alt)的轻度但有统计学意义的升高,但令人惊讶的是,在实施例2描述的硬明胶胶囊制剂中的式(i)的化合物的任何组中都没有观察到这种升高。各药物组与安慰剂之间的alt差异具有统计学意义(对于所有对比,p《0.01),从而证明了式(i)的化合物对暴露于谷蛋白的乳糜泻患者的肝脏的保护作用。碱性磷酸酶(alp)水平也显示出类似的模式(p《0.05)。在安慰剂组中,所述值归一化至第10周的无谷蛋白饮食(gfd)(表1)。发现式(i)的化合物抑制肝损伤,所述肝损
伤是在活动性乳糜泻(ced)中谷蛋白驱动的肠外表现之一,反映为alt和alp的轻度升高,证实所述化合物发挥一般肝保护作用(参见图12)。
[0900]
式(i)的化合物在非酒精性脂肪性肝炎的小鼠模型中的施用证明了肝纤维化的剂量依赖性降低(实施例3)。令人惊讶的是,式(i)的化合物在stam小鼠中的施用还导致肝脏炎症的剂量依赖性和显著性减轻,这进一步证明了其肝保护作用。
[0901]
因此,本发明的一个实施方案涉及式(i)的化合物(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或式(i)的对映异构体、溶剂化物、水合物或药学上可接受的盐作为肝保护剂(即作为肝保护性药剂)的用途:
[0902][0903]
在一个实施方案中,本发明涉及用于保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤和/或预防或治疗肝障碍/疾病的式(i)的化合物、其对映异构体、溶剂化物、水合物或药学上可接受的盐。
[0904]
在一个实施方案中,本发明涉及用于保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤和/或预防或治疗肝障碍/疾病的式(i)的化合物、其对映异构体、溶剂化物、水合物或药学上可接受的盐,其中所述化合物降低至少一种肝酶的血清水平,优选地所述至少一种肝酶选自丙氨酸氨基转移酶(alt)、天冬氨酸氨基转移酶(ast)和碱性磷酸酶(alp)。
[0905]
在一个实施方案中,本发明涉及用于保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤和/或预防或治疗肝障碍/疾病的式(i)的化合物、其对映异构体、溶剂化物、水合物或药学上可接受的盐,其中所述肝障碍/疾病是肝纤维化、酒精性肝炎、非酒精性脂肪性肝炎(nash)、非酒精性脂肪肝疾病(nafld)、肝硬化、胆汁淤积性肝疾病诸如原发性硬化性胆管炎(psc)和原发性胆汁性胆管炎(pbc)、自身免疫性肝炎(aih)、酒精性脂肪性肝炎(ash)或肝炎症。
[0906]
在一个实施方案中,本发明涉及用于保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤和/或预防或治疗肝障碍/疾病的式(i)的化合物、其对映异构体、溶剂化物、水合物或药学上可接受的盐,其中所述肝毒性、所述肝损伤或所述肝障碍/疾病由至少一种肝毒物、乳糜泻或病毒感染造成,优选地所述至少一种肝毒物选自包含以下成员或由以下成员组成的集合:有毒的化学物质、外源性物质、抗癌药物、免疫抑制药物、镇痛药物、抗炎药物、抗结核药物、生物制品、辐射、重金属、真菌毒素、半乳糖胺和脂多糖;与特定遗传表型(hla dq2/dq8)和由转谷氨酰胺酶2(tg2)促进的病理学相关的乳糜泻;和/或甲型、乙型、丙型肝炎病毒的病毒感染。
[0907]
优选地,所述有毒的化学物质是醇类,外源性物质是四氯化碳、氯化烃、异氰酸盐、杀虫剂诸如杀昆虫剂、杀真菌剂、除草剂和去污剂诸如胆汁酸盐;抗癌药物是硫唑嘌呤、多
柔比星、顺铂;免疫抑制药物是环孢菌素、抗炎药物是对乙酰氨基酚和硫代乙酰胺;抗结核药物是异烟肼和利福平;生物制品是例如卡介苗疫苗,辐射优选是γ辐射,重金属是镉和砷;真菌毒素是黄曲霉毒素、半乳糖胺和脂多糖。
[0908]
优选地,本发明涉及用于保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤和/或预防或治疗肝障碍/疾病的式(i)的化合物、其对映异构体、溶剂化物、水合物或药学上可接受的盐,其中所述肝毒性、肝损伤或肝障碍/疾病是由乳糜泻造成,且乳糜泻与转谷氨酰胺酶2(tg2)相关。
[0909]
在一个实施方案中,本发明涉及用于如上所述用途的式(i)的化合物、其对映异构体、溶剂化物、水合物或药学上可接受的盐,其中口服施用所述化合物。
[0910]
用于用作肝保护剂的药物组合物
[0911]
本发明的另一个方面涉及用于用作肝保护剂的药物组合物,其包含
[0912]
式(i)的化合物(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯:
[0913][0914]
或其对映异构体、溶剂化物、水合物或药学上可接受的盐。
[0915]
优选地,所述药物组合物可用于保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤和/或预防或治疗肝障碍/疾病。
[0916]
优选地,所述肝毒性或所述肝损伤、所述肝障碍/疾病由至少一种肝毒物、乳糜泻或病毒感染造成。
[0917]
具体地,所述至少一种肝毒物选自包含以下成员或由以下成员组成的集合:有毒的化学物质、外源性物质、抗癌药物、免疫抑制药物、镇痛药物、抗炎药物、抗结核药物、生物制品、辐射、重金属、真菌毒素、半乳糖胺和脂多糖。
[0918]
在一个实施方案中,本发明涉及包含式(i)的化合物、其对映异构体、溶剂化物、水合物或药学上可接受的盐的药物组合物,其用于保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤和/或预防或治疗肝障碍/疾病,其中所述至少一种肝毒物选自包含以下成员或由以下成员组成的集合:有毒的化学物质、外源性物质、抗癌药物、免疫抑制药物、镇痛药物、抗炎药物、抗结核药物、生物制品、辐射、重金属、真菌毒素、半乳糖胺和脂多糖与特定遗传表型(hla dq2/dq8)和由转谷氨酰胺酶2(tg2)促进的病理学相关的乳糜泻;和/或甲型、乙型、丙型肝炎病毒的病毒感染。
[0919]
在一个实施方案中,本发明涉及所述包含式(i)的化合物、其对映异构体、溶剂化物、水合物或药学上可接受的盐的药物组合物,其用于保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤和/或预防或治疗肝障碍/疾病,其中所述化合物降低至少一种肝酶的血清水平,优选地所述至少一种肝酶选自丙氨酸氨基转移酶(alt)、天冬氨酸氨基转移酶
(ast)和碱性磷酸酶(alp)。
[0920]
在一个实施方案中,本发明涉及所述包含式(i)的化合物、其对映异构体、溶剂化物、水合物或药学上可接受的盐的药物组合物,其用于保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤和/或预防或治疗肝障碍/疾病,其中所述肝障碍/疾病是肝纤维化、酒精性肝炎、非酒精性脂肪性肝炎(nash)、非酒精性脂肪肝疾病(nafld)、肝硬化、胆汁淤积性肝疾病诸如原发性硬化性胆管炎(psc)和原发性胆汁性胆管炎(pbc)、自身免疫性肝炎(aih)、酒精性脂肪性肝炎(ash)或肝炎症。
[0921]
优选地,本发明也涉及所述包含式(i)的化合物、其对映异构体、溶剂化物、水合物或药学上可接受的盐的药物组合物,其与无谷蛋白饮食联合地用于保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤和/或预防或治疗肝障碍/疾病,其中所述肝毒性、肝损伤或肝障碍/疾病是由乳糜泻造成,且乳糜泻与转谷氨酰胺酶2(tg2)相关。
[0922]
在一个实施方案中,本发明涉及所述包含式(i)的化合物、其对映异构体、溶剂化物、水合物或药学上可接受的盐的药物组合物,其用于保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤和/或预防或治疗肝障碍/疾病,其中所述药物组合物进一步包含至少一种聚合物沉淀抑制剂。
[0923]
优选地所述“聚合物沉淀抑制剂”选自包含以下成员或由以下成员组成的集合:
[0924]
纤维素衍生物,包括、但不限于微晶纤维素(mcc)、醋酸邻苯二甲酸纤维素(cap)、醋酸对苯二甲酸纤维素、醋酸间苯二甲酸纤维素、醋酸丁酸纤维素(cab)、醋酸偏苯三酸纤维素(cat)、甲基纤维素(mc)、醋酸邻苯二甲酸甲基纤维素、乙基纤维素(ec)、羧甲基纤维素(cmc)、羧甲基纤维素钠、羧甲基乙基纤维素(cmec)、羟基甲基纤维素(hmc)、羟乙基纤维素(hec)、羟丙基纤维素(hpc或羟丙纤维素)、l-羟丙基纤维素、羟丙基甲基纤维素(hpmc或羟丙甲纤维素)、羧甲基羟乙基纤维素(cmhec)、羧甲基羟乙基纤维素钠(nacmhec)、邻苯二甲酸羟丙基甲基纤维素(hpmcp,邻苯二甲酸酯羟丙甲纤维素)、醋酸羟丙甲纤维素琥珀酸酯(hpmcas,醋酸羟丙甲基纤维素琥珀酸酯);
[0925]
淀粉衍生物,包括、但不限于羟乙基淀粉、羟丙基淀粉(hps)和预胶化淀粉;
[0926]
葡聚糖/糊精衍生物,包括、但不限于环葡聚糖(即,环异麦芽-七糖(ci-7)、环异麦芽-八糖(ci-8)、环异麦芽-九糖(ci-9))、羟丙基葡聚糖、麦芽糊精、α-/β-/γ-环糊精、2-羟乙基-β-环糊精、2-羟丙基-β-环糊精(hpβcd)、磺基丁醚-β-环糊精钠盐、甲基化-β-环糊精、2-羟丙基-γ-环糊精;
[0927]
聚醚衍生物,包括、但不限于聚乙二醇(peg)、聚环氧乙烷(peo)、聚醚多元醇、聚(丙二醇)双(2-氨基丙基醚)(ppgae)、聚(环氧乙烷)-聚(环氧丙烷)-聚(环氧乙烷)(peo-ppo-peo,泊洛沙姆)诸如泊洛沙姆188和泊洛沙姆407,
[0928]
聚乙烯基衍生物,包括、但不限于聚乙烯醇(pva)、聚醋酸乙烯邻苯二甲酸酯(pvap)、聚乙烯吡咯烷酮(pvp)、聚乙烯吡咯烷酮-共聚-聚乙酸乙烯酯(pvpva)、聚乙烯基己内酰胺-聚乙酸乙烯酯-聚乙二醇接枝共聚物
[0929]
聚丙烯酸衍生物,包括、但不限于聚(丙烯酸)(paa)、聚(丙烯酰胺/丙烯酸)(pac-ac)、聚甲基丙烯酸酯(pma)、聚甲基丙烯酸、聚(甲基丙烯酸/甲基丙烯酸甲酯)、聚(甲基丙烯酸/丙烯酸酯乙酯);
[0930]
聚胺衍生物,包括、但不限于聚乙烯亚胺(pei)、聚烯丙胺氯化氢、聚二烯丙基二甲
基氯化铵和聚(2-乙基-2-噁唑啉);
[0931]
聚磺酸衍生物,包括、但不限于聚苯乙烯磺酸(pssa);和
[0932]
至少两种上述聚合物沉淀抑制剂的组合。
[0933]
更优选地,所述“聚合物沉淀抑制剂”选自包含以下成员或由以下成员组成的集合:微晶纤维素(mcc)、醋酸邻苯二甲酸纤维素(cap)、醋酸对苯二甲酸纤维素、醋酸间苯二甲酸纤维素、醋酸丁酸纤维素(cab)、醋酸偏苯三酸纤维素(cat)、甲基纤维素(mc)、醋酸邻苯二甲酸甲基纤维素、乙基纤维素(ec)、羧甲基纤维素(cmc)、羧甲基纤维素钠、羧甲基乙基纤维素(cmec)、羟基甲基纤维素(hmc)、羟乙基纤维素(hec)、羟丙基纤维素(hpc或羟丙纤维素)、l-羟丙基纤维素、羟丙基甲基纤维素(hpmc或羟丙甲纤维素)、羧甲基羟乙基纤维素(cmhec)、羧甲基羟乙基纤维素钠(nacmhec)、邻苯二甲酸羟丙基甲基纤维素(hpmcp,邻苯二甲酸酯羟丙甲纤维素)、醋酸羟丙甲纤维素琥珀酸酯(hpmcas,醋酸羟丙甲基纤维素琥珀酸酯)、聚乙二醇(peg)、聚环氧乙烷(peo)、聚醚多元醇、聚(丙二醇)双(2-氨基丙基醚)(ppgae)、聚(环氧乙烷)-聚(环氧丙烷)-聚(环氧乙烷)(peo-ppo-peo,泊洛沙姆)诸如泊洛沙姆188和泊洛沙姆407、聚乙烯醇(pva)、聚醋酸乙烯邻苯二甲酸酯(pvap)、聚乙烯吡咯烷酮(pvp)、聚乙烯吡咯烷酮-共聚-聚乙酸乙烯酯(pvpva)、聚乙烯基己内酰胺-聚乙酸乙烯酯-聚乙二醇接枝共聚物聚(丙烯酸)(paa)、聚(丙烯酰胺/丙烯酸)(pac-ac)、聚甲基丙烯酸酯(pma)、聚甲基丙烯酸、聚(甲基丙烯酸/甲基丙烯酸甲酯)、聚(甲基丙烯酸/丙烯酸酯乙酯)和
[0934]
至少两种上述聚合物沉淀抑制剂的组合。
[0935]
优选地,所述至少一种聚合物沉淀抑制剂选自由以下成员组成的集合:l-羟丙基纤维素、羟丙基纤维素、l-羟丙基纤维素和羟丙基纤维素的组合、聚乙二醇、聚(环氧乙烷)-聚(环氧丙烷)-聚(环氧乙烷)、聚乙烯醇、聚乙烯吡咯烷酮、羧甲基纤维素、甲基纤维素、羟乙基纤维素、羟丙基甲基纤维素、乙基纤维素、聚乙烯基己内酰胺-聚乙酸乙烯酯-聚乙二醇接枝共聚物和羧甲基纤维素钠。
[0936]
因此,在一个实施方案中,本发明涉及所述包含式(i)的化合物、其对映异构体、溶剂化物、水合物或药学上可接受的盐的药物组合物,其用于保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤和/或预防或治疗肝障碍/疾病,其中所述药物组合物进一步包含至少一种聚合物沉淀抑制剂且所述至少一种聚合物沉淀抑制剂选自由以下成员组成的集合:l-羟丙基纤维素、羟丙基纤维素、l-羟丙基纤维素和羟丙基纤维素的组合、聚乙二醇、聚(环氧乙烷)-聚(环氧丙烷)-聚(环氧乙烷)、聚乙烯醇、聚乙烯吡咯烷酮、羧甲基纤维素、甲基纤维素、羟乙基纤维素、羟丙基甲基纤维素、乙基纤维素、聚乙烯基己内酰胺-聚乙酸乙烯酯-聚乙二醇接枝共聚物和羧甲基纤维素钠。
[0937]
另外,在人中的药代动力学研究的积极数据证实了化合物(i)的高生物利用度。必须与之前已经进行的动物研究相比来理解在该背景下的高生物利用度。
[0938]
stam-和uuo小鼠模型研究证实,通过施用含有根据式(i)的化合物的全身性制剂实现了对肝脏和肾脏的抗纤维化作用。因此,式(i)的药物在靶部位显示出高抗纤维化作用,并从而指示全身生物利用度。因此,式(i)的药物的施用在靶部位表现出高抗纤维化作用,并因此可以获得全身利用度(生物利用度),即药物在靶组织处被吸收。
[0939]
令人惊讶的是,式(i)的药物在stam小鼠中的施用不仅导致纤维化的减轻,而且导致肝脏炎症的剂量依赖性和显著性减轻,这进一步证明了肝保护作用。
[0940]
酸化剂的添加确保(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯在胃中的完全溶解,但在小肠中的ph从2增加到6,因此所述药物在它可以被小肠吸收之前可以沉淀。为了确保所述化合物在小肠中的完全溶解,根据本发明的制剂优选含有酸化剂和/或聚合物沉淀抑制剂。此外,在实施例9中可以证实,在人体中仅20mg的剂量就足以达到血浆中的有效药物浓度,并从而达到全身利用度。
[0941]
药代动力学研究表明,(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯在小肠中被吸收,并需要20-50mg的低剂量才能在人体中达到治疗有效的药物浓度(实施例7、图6)。此外,用20mg的人剂量已经可以实现抗纤维化作用(实施例9和图9)。
[0942]
此外,没有观察到脱靶效应。如前所述,这尤其令人惊讶,因为实际上tg2在几乎所有细胞类型和细胞区室中普遍表达,它存在于细胞表面上并分泌到细胞外基质中,并存在于各种器官中,且因此可以设想最可能发生脱靶效应。
[0943]
在一个实施方案中,本发明涉及所述用于保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤和/或预防或治疗肝障碍/疾病的药物组合物,其中所述药物组合物进一步包含至少一种酸化剂和/或至少一种粘合剂。
[0944]“粘合剂”是将粉末颗粒结合或“粘合”在一起并通过形成颗粒使它们粘合的物质,因此在制剂中充当“粘合剂”。粘合剂会增加在稀释剂或填充剂中已有的粘合强度。合适的粘合剂包括糖、蔗糖、多糖、黄原胶、瓜尔胶、角叉菜胶、从小麦、玉米、大米和马铃薯衍生出的淀粉、从小麦、玉米、大米和马铃薯衍生出的预凝(改性)淀粉、淀粉羟乙酸钠、天然树胶、金合欢胶、明胶、黄蓍胶、海藻的衍生物、海藻酸、海藻酸钠、海藻酸钙铵、纤维素、纤维素衍生物、羟丙基纤维素、l-羟丙基纤维素、低取代的羟丙基纤维素、甲基纤维素、羧甲基纤维素钠、羟丙基甲基纤维素、聚乙烯吡咯烷酮、聚维酮k25。
[0945]
在一个实施方案中,本发明涉及所述用于保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤和/或预防或治疗肝障碍/疾病的药物组合物,其中所述药物组合物进一步包含至少一种酸化剂且所述至少一种酸化剂选自由以下成员组成的集合:抗坏血酸、有机二羧酸诸如草酸、丙二酸、琥珀酸、戊二酸、酒石酸、富马酸、马来酸、苹果酸、己二酸或谷氨酸、和有机三羧酸诸如柠檬酸或柠檬酸氢钠。
[0946]
在一个实施方案中,本发明涉及所述包含式(i)的化合物、其对映异构体、溶剂化物、水合物或药学上可接受的盐的药物组合物,其用于保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤和/或预防或治疗肝障碍/疾病,其中所述药物组合物进一步包含至少一种粘合剂且所述至少一种粘合剂选自由以下成员组成的集合:糖、蔗糖、多糖、黄原胶、瓜尔胶、角叉菜胶、从小麦、玉米、大米和马铃薯衍生出的淀粉、从小麦、玉米、大米和马铃薯衍生出的预凝(改性)淀粉、淀粉羟乙酸钠、天然树胶、金合欢胶、明胶、黄蓍胶、海藻的衍生物、海藻酸、海藻酸钠、海藻酸钙铵、纤维素、纤维素衍生物、羟丙基纤维素、l-羟丙基纤维素、低取代的羟丙基纤维素、甲基纤维素、羧甲基纤维素钠、羟丙基甲基纤维素、聚乙烯吡咯烷酮、聚维酮k25。
[0947]
在一个优选实施方案中,本发明涉及所述包含式(i)的化合物、其对映异构体、溶剂化物、水合物或药学上可接受的盐的药物组合物,其用于保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤和/或预防或治疗肝障碍/疾病,其中所述药物组合物进一步包含至少一种聚合物沉淀抑制剂和至少一种酸化剂,
[0948]
所述至少一种聚合物沉淀抑制剂选自由以下成员组成的集合:l-羟丙基纤维素、羟丙基纤维素、l-羟丙基纤维素和羟丙基纤维素的组合、聚乙二醇、聚(环氧乙烷)-聚(环氧丙烷)-聚(环氧乙烷)、聚乙烯醇、聚乙烯吡咯烷酮、羧甲基纤维素、甲基纤维素、羟乙基纤维素、羟丙基甲基纤维素、乙基纤维素、聚乙烯基己内酰胺-聚乙酸乙烯酯-聚乙二醇接枝共聚物和羧甲基纤维素钠;和
[0949]
所述至少一种酸化剂选自由以下成员组成的集合:抗坏血酸、有机二羧酸诸如草酸、丙二酸、琥珀酸、戊二酸、酒石酸、富马酸、马来酸、苹果酸、己二酸或谷氨酸、和有机三羧酸诸如柠檬酸或柠檬酸氢钠。
[0950]
在一个优选实施方案中,本发明涉及所述包含式(i)的化合物、其对映异构体、溶剂化物、水合物或药学上可接受的盐的药物组合物,其用于保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤和/或预防或治疗肝障碍/疾病,其中所述药物组合物进一步包含至少一种聚合物沉淀抑制剂和至少一种粘合剂,
[0951]
所述至少一种聚合物沉淀抑制剂选自由以下成员组成的集合:l-羟丙基纤维素、羟丙基纤维素、l-羟丙基纤维素和羟丙基纤维素的组合、聚乙二醇、聚(环氧乙烷)-聚(环氧丙烷)-聚(环氧乙烷)、聚乙烯醇、聚乙烯吡咯烷酮、羧甲基纤维素、甲基纤维素、羟乙基纤维素、羟丙基甲基纤维素、乙基纤维素、聚乙烯基己内酰胺-聚乙酸乙烯酯-聚乙二醇接枝共聚物和羧甲基纤维素钠;和
[0952]
所述至少一种粘合剂选自由以下成员组成的集合:糖、蔗糖、多糖、黄原胶、瓜尔胶、角叉菜胶、从小麦、玉米、大米和马铃薯衍生出的淀粉、从小麦、玉米、大米和马铃薯衍生出的预凝(改性)淀粉、淀粉羟乙酸钠、天然树胶、金合欢胶、明胶、黄蓍胶、海藻的衍生物、海藻酸、海藻酸钠、海藻酸钙铵、纤维素、纤维素衍生物、羟丙基纤维素、l-羟丙基纤维素、低取代的羟丙基纤维素、甲基纤维素、羧甲基纤维素钠、羟丙基甲基纤维素、聚乙烯吡咯烷酮、聚维酮k25。
[0953]
在一个优选实施方案中,本发明涉及所述包含式(i)的化合物、其对映异构体、溶剂化物、水合物或药学上可接受的盐的药物组合物,其用于保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤和/或预防或治疗肝障碍/疾病,其中所述药物组合物进一步包含至少一种聚合物沉淀抑制剂、至少一种酸化剂和至少一种粘合剂,
[0954]
所述至少一种聚合物沉淀抑制剂选自由以下成员组成的集合:l-羟丙基纤维素、羟丙基纤维素、l-羟丙基纤维素和羟丙基纤维素的组合、聚乙二醇、聚(环氧乙烷)-聚(环氧丙烷)-聚(环氧乙烷)、聚乙烯醇、聚乙烯吡咯烷酮、羧甲基纤维素、甲基纤维素、羟乙基纤维素、羟丙基甲基纤维素、乙基纤维素、聚乙烯基己内酰胺-聚乙酸乙烯酯-聚乙二醇接枝共聚物和羧甲基纤维素钠;
[0955]
所述至少一种酸化剂选自由以下成员组成的集合:抗坏血酸、有机二羧酸诸如草酸、丙二酸、琥珀酸、戊二酸、酒石酸、富马酸、马来酸、苹果酸、己二酸或谷氨酸、和有机三羧
酸诸如柠檬酸或柠檬酸氢钠;和
[0956]
所述至少一种粘合剂选自由以下成员组成的集合:糖、蔗糖、多糖、黄原胶、瓜尔胶、角叉菜胶、从小麦、玉米、大米和马铃薯衍生出的淀粉、从小麦、玉米、大米和马铃薯衍生出的预凝(改性)淀粉、淀粉羟乙酸钠、天然树胶、金合欢胶、明胶、黄蓍胶、海藻的衍生物、海藻酸、海藻酸钠、海藻酸钙铵、纤维素、纤维素衍生物、羟丙基纤维素、l-羟丙基纤维素、低取代的羟丙基纤维素、甲基纤维素、羧甲基纤维素钠、羟丙基甲基纤维素、聚乙烯吡咯烷酮、聚维酮k25。
[0957]
优选地,本发明涉及上述的用于保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤和/或预防或治疗肝障碍/疾病的药物组合物中的任一种,其中所述药物组合物进一步包含稀释剂、崩解剂、润滑剂、助流剂和/或着色剂。
[0958]
合适的“稀释剂”是通常构成组合物或剂型的主要部分的物质。合适的稀释剂包括糖诸如乳糖、蔗糖、甘露醇和山梨醇,从小麦、玉米、大米和马铃薯衍生出的淀粉和纤维素诸如微晶纤维素。
[0959]
术语“崩解剂”表示添加到组合物中以支持分解(崩解)和释放药物的药学活性成分的物质。合适的崩解剂包括淀粉、“冷水溶性的”变性淀粉诸如羧甲基淀粉钠、天然的和合成的树胶诸如刺槐豆胶、卡拉牙胶、瓜尔胶、黄蓍胶和琼脂、纤维素衍生物诸如甲基纤维素和羧甲基纤维素钠、微晶纤维素和交联的微晶纤维素诸如交联羧甲基纤维素钠、海藻酸盐诸如海藻酸和海藻酸钠、粘土诸如皂粘土和泡腾混合物。
[0960]“润滑剂”表示添加到剂型中以通过减少摩擦或磨损使片剂颗粒等在压制后从模具释放的一类物质。合适的润滑剂包括金属硬脂酸盐诸如硬脂酸镁、硬脂酸钙或硬脂酸钾、硬脂酸、高熔点蜡、以及其它水溶性的润滑剂诸如氯化钠、苯甲酸钠、醋酸钠、油酸钠、聚乙二醇和d,l-亮氨酸。润滑剂通常在压缩前的最后一步添加,因为它们必须存在于颗粒表面。
[0961]“助流剂”是防止药物组合物的组分结块并改善颗粒的流动特征使得流动平滑和均匀的材料。合适的助流剂包括二氧化硅和滑石粉。
[0962]
因此,本发明的一个实施方案涉及用于保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤和/或预防或治疗肝障碍/疾病的药物组合物,其包含式(i)的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和至少一种赋形剂,或由它们组成,其中所述至少一种赋形剂是崩解剂。
[0963]
因此,本发明的一个实施方案涉及用于保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤和/或预防或治疗肝障碍/疾病的药物组合物,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和至少一种崩解剂或由它们组成。
[0964]
根据本发明的药物组合物可以包含酸化剂、聚合物沉淀抑制剂、粘合剂和/或崩解剂。
[0965]
根据本发明的一个实施方案涉及用于保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤和/或预防或治疗肝障碍/疾病的药物组合物,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨
2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和至少一种赋形剂,或由它们组成,其中所述至少一种赋形剂是稀释剂/填充剂/粘合剂。
[0973]
根据本发明的药物组合物可以包含酸化剂、聚合物沉淀抑制剂、粘合剂、崩解剂、润滑剂/助流剂和/或稀释剂/填充剂/粘合剂或由它们组成。
[0974]
本发明的一个实施方案涉及用于保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤和/或预防或治疗肝障碍/疾病的药物组合物,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐和至少一种赋形剂,或由它们组成,其中至少一种赋形剂选自包含以下成员或由以下成员组成的集合:酸化剂、聚合物沉淀抑制剂、粘合剂、崩解剂、润滑剂/助流剂和稀释剂/填充剂/粘合剂。
[0975]
本发明的一个实施方案涉及用于保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤和/或预防或治疗肝障碍/疾病的全身性制剂,其含有(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、至少一种酸化剂、至少一种聚合物沉淀抑制剂、至少一种粘合剂、至少一种崩解剂、至少一种润滑剂/助流剂和至少一种稀释剂/填充剂/粘合剂或由它们组成。
[0976]
以适合于口服应用的可施用形式提供优选药物组合物,诸如片剂诸如未包衣片剂、包衣片剂、泡腾片剂、可溶性片剂、咀嚼片剂、口服冻干粉剂、锭剂、软锭剂、压缩锭剂、舌下片剂、含服片剂、颗粒、泡腾颗粒和胶囊剂。更优选地,所述口服制剂是片剂或胶囊剂。未包衣和包衣片剂、以及硬或软胶囊剂是最优选的药物制剂。
[0977]
在某些实施方案中,本发明涉及所述用于保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤和/或预防或治疗肝障碍/疾病的药物组合物,其中所述药物组合物是口服制剂,优选地所述口服制剂是片剂、胶囊剂、粉剂或颗粒剂。
[0978]
用于根据本发明的用途的药物组合物也可以包含用于胶囊剂的其它成分,诸如胶囊剂的着色剂。在片剂中也可以存在着色剂作为其它成分。
[0979]
此外,用于包衣片剂的组分也被术语“其它成分”包括。
[0980]
胶囊剂的外壳可以包含着色剂。本文中使用的术语“着色剂”包括颜料诸如白色颜料。所述着色剂尤其可以是氧化铁、特别是氧化铁(iii)、氧化铁(ii、iii)或水合的氧化铁或二氧化钛。
[0981]“片剂”是指含有至少一种活性药物成分和合适的赋形剂的压缩固体剂型。通过压制通过本领域技术人员已知的湿法制粒、干法制粒或压实获得的混合物或颗粒,可以生产片剂。
[0982]
术语“胶囊”表示由甲基纤维素、聚乙烯醇或明胶或变性明胶或淀粉组成的特殊容器或壳,在其中可以包封活性剂。通常,硬壳胶囊由羟丙基甲基纤维素或由具有较高凝胶强度的猪骨和皮明胶的混合物制备。胶囊剂的壳可以含有少量的着色剂、遮光剂、软化剂和防腐剂。“软壳胶囊”含有明胶作为基本聚合物、较高量的一种或多种软化剂诸如甘油或山梨醇以及水。一般而言,软化剂的量是胶囊壳的20-30重量%,明胶的量是胶囊壳的40-45重量%,且水的量是胶囊壳的30-35重量%。在胶囊干燥后,水的量是胶囊壳的7-8重量%。
[0983]
胶囊壳可以包含明胶、羟丙基甲基纤维素(hmpc)、多糖诸如淀粉和角叉菜胶;和/或合成的聚合物诸如聚乙烯醇的共聚合物(compolymers)。此外,胶囊的壳可以包含着色剂。本文中使用的术语“着色剂”包括颜料诸如白色颜料。所述着色剂尤其可以是氧化铁、特别是氧化铁(iii)、氧化铁(ii、iii)或水合的氧化铁、二氧化钛、天然染料、偶氮(azo)和苍耳烷化合物。此外,胶囊壳可以包含防腐剂诸如对羟基苯甲酸酯或改善风味的物质诸如乙香草醛。另外,胶囊壳可以包含表面活性剂诸如月桂基硫酸钠。
[0984]
用于组合物的“粉末”表示含有活性组分和合适赋形剂的粉末混合物/掺合物,其可以在使用前悬浮在水或汁液中。球形颗粒也表示弹丸或珠子。
[0985]“颗粒”表示干燥和固体颗粒。每个颗粒代表粉末颗粒的附聚物。
[0986]
此外,为了进一步改善药物组合物的性能,可以调整特定psd(粒度分布)和/或psr(粒度范围)。
[0987]
因此,在根据本发明的药物组合物的用途中,所述药物组合物包含式(i)的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯:
[0988][0989]
或式(i)的溶剂化物、水合物或药学上可接受的盐,其中(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯颗粒具有从0.1至100μm的粒度范围。
[0990]
进一步更优选的是,(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐的粒度是在0.1μm至100μm的范围内,优选地在0.5μm至50μm的范围内,且更优选地在1.0μm至20μm的范围内。因此,(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐的粒度范围(psr)是从0.1μm至100μm、从0.5μm至50μm或从1.0μm至20μm。优选地,根据式(i)的药物的粒度≤10μm。
[0991]
根据本发明的另一个优选实施方案是用于保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤和/或预防或治疗肝障碍/疾病的药物组合物,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、己二酸和l-羟丙基纤维素或由它们组成,其中(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯颗粒具有从0.1μm至100μm的粒度范围。
[0992]
因此,根据本发明的一个实施方案涉及用于保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤和/或预防或治疗肝障碍/疾病的药物组合物,其包含式(i)的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯:
[0993][0994]
或式(i)的对映异构体、溶剂化物、水合物或药学上可接受的盐或由它们组成,其中(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯颗粒具有由d(0.95)≤25μm定义的粒度分布,其中(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐优选地被微粉化。
[0995]
此外,优选的是,(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐的粒度分布的特征在于从0.1至5μm的d(0.1)、从0.3至10μm的d(0.5)、从3至25μm的d(0.95),更优选从0.2至3μm的d(0.1)、从0.4至7.5μm的d(0.5)和从2至15μm的d(0.95),且最优选从0.3至3μm的d(0.1)、从0.5至5μm的d(0.5)和从1至10μm的d(0.95)
[0996]
通过激光衍射(malvern分析,样品分散在正己烷和脱水山梨糖醇单油酸酯中)测量粒度分布。因此,激光根据粒度被散射。从依赖于角度的散射光强度产生衍射图样,可以计算粒度。
[0997]
参数d(0.1)表示,当通过激光衍射(malvern分析,样品分散在正己烷和脱水山梨糖醇单油酸酯中)分析时,样品中颗粒的总体积的10%由具有小于指定值或值范围的直径的颗粒构成时的直径。因此,d(0.1)=0.1至5μm是指,限定样品中最小颗粒的10%的粒度范围的上限是在0.1μm至5μm之间。因此,总颗粒的10%具有不超过d(0.1)的粒度,在该情况下意味着,它们具有0.1μm至5μm的最大尺寸。
[0998]
相应地,参数d(0.5)表示,当通过激光衍射(malvern分析,样品分散在正己烷和脱水山梨糖醇单油酸酯中)分析时,样品中颗粒的总体积的50%由具有小于指定值或值范围的直径的颗粒构成时的直径。因此,d(0.5)=0.3至10μm是指,限定样品中最小颗粒的50%的粒度范围的上限是在0.3μm至10μm之间。因此,总颗粒的50%具有不超过d(0.5)的粒度,在该情况下意味着,它们具有0.3μm至10μm的最大尺寸。
[0999]
相应地,参数d(0.95)表示,当通过激光衍射(malvern分析,样品分散在正己烷和脱水山梨糖醇单油酸酯中)分析时,样品中颗粒的总体积的95%由具有小于指定值或值范围的直径的颗粒构成时的直径。因此,d(0.95)=3-25μm是指,限定样品中最小颗粒的95%
的粒度范围的上限是在3μm至25μm之间。因此,总颗粒的95%具有不超过d(0.95)的粒度,在该情况下意味着,它们具有3μm至25μm的最大尺寸。
[1000]
本发明的另一个实施方案涉及用于保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤和/或预防或治疗肝障碍/疾病的药物组合物,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、己二酸和l-羟丙基纤维素或由它们组成,其中(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯颗粒具有由d(0.95)≤25μm定义的粒度分布。
[1001]
本发明的一个优选实施方案涉及用于保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤和/或预防或治疗肝障碍/疾病的药物组合物,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐或由它们组成,其中(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯颗粒具有由从0.1至5μm的d(0.1)、从0.3至10μm的d(0.5)和从3至25μm的d(0.95)定义的粒度分布。
[1002]
根据本发明的一个更优选实施方案是用于保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤和/或预防或治疗肝障碍/疾病的药物组合物,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、己二酸和l-羟丙基纤维素或由它们组成,其中(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯颗粒具有由从0.1至5μm的d(0.1)、从0.3至10μm的d(0.5)和从3至25μm的d(0.95)定义的粒度分布。
[1003]
根据本发明的一个更优选实施方案是用于保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤和/或预防或治疗肝障碍/疾病的药物组合物,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、己二酸和l-羟丙基纤维素或由它们组成,其中(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯颗粒具有由从0.2至3μm的d(0.1)、从0.4至7.5μm的d(0.5)和从2至15μm的d(0.95)定义的粒度分布。
[1004]
根据本发明的一个甚至更优选的实施方案是用于保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤和/或预防或治疗肝障碍/疾病的药物组合物,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、己二酸、l-羟丙基纤维素、交联羧甲基纤维素钠和滑石粉或由它们组成,其中(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯颗粒具有由从0.1至5μm的d(0.1)、从
0.3至10μm的d(0.5)和从3至25μm的d(0.95)定义的粒度分布。
[1005]
根据本发明的一个特别优选的实施方案是用于保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤和/或预防或治疗肝障碍/疾病的药物组合物,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、己二酸、l-羟丙基纤维素、交联羧甲基纤维素钠、滑石粉、明胶和二氧化钛或由它们组成,其中(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯具有由从0.1至5μm的d(0.1)、从0.3至10μm的d(0.5)和从3至25μm的d(0.95)定义的粒度分布。
[1006]
本发明的另一个特别优选的实施方案涉及用于保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤和/或预防或治疗肝障碍/疾病的药物组合物,其包含(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐、己二酸、l-羟丙基纤维素、聚维酮k25、交联羧甲基纤维素钠、微晶纤维素和二氧化硅或由它们组成,其中(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯具有由从0.1至5μm的d(0.1)、从0.3至10μm的d(0.5)和从3至25μm的d(0.95)定义的粒度分布。
[1007]
因此,根据本发明的一个实施方案涉及一种药物组合物,其包含式(i)的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯:
[1008][1009]
或式(i)的对映异构体、溶剂化物、水合物或药学上可接受的盐或由它们组成,其中(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯颗粒具有从0.1至100μm的粒度范围和由d(0.95)≤25μm限定的粒度分布。
[1010]
所述药物组合物可以包含以下量的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或对映异构体、溶剂化物、水合物或药学上可接受的盐、溶剂化物或水合物:0.1重量%至99重量%,优选0.2重量%至90重量%,更优选0.3重量%至85重量%,甚至更优选0.4重量%至80重量%,甚至更优选0.5重量%至75重量%,甚至更优选0.6重量%至70重量%,甚至更优选0.7重量%至65重量%,甚至更优选0.8重量%至60重量%,甚至更优选0.9重量%至55重量%,甚至更优选1重量%至50重量%,甚至更优选1重量%至45重量%,甚至更优选1.25重量%至45重量%,甚至更优选1.5重量%至40重量%,甚至更优选1.75重
量%至35重量%,甚至更优选2重量%至34重量%,甚至更优选2.25重量%至33重量%,甚至更优选2.5重量%至32重量%,且最优选2.5重量%至31重量%,甚至更优选2.5重量%至30.5重量%,且甚至更优选2.6重量%至30.3重量%,甚至更优选3重量%至30重量%,甚至更优选3.5重量%至29重量%,甚至更优选4重量%至28重量%,甚至更优选4重量%至27重量%,甚至更优选4.5重量%至27重量%,且最优选5重量%至27重量%。“重量%”(重量百分比)表示在药物组合物中的重量百分比。
[1011]
所述药物组合物可以进一步包含在以下范围内的量的酸化剂:从0.1重量%至80重量%,优选从0.5重量%至77.5重量%,更优选从1重量%至75重量%,更优选从1.5重量%至72.5重量%,更优选从2重量%至70重量%,更优选从2.5重量%至62.5重量%,更优选从3重量%至57.5重量%,更优选从3.5重量%至55重量%,甚至更优选从4重量%至55重量%,甚至更优选从4.5重量%至55重量%,甚至更优选从5重量%至54重量%,甚至更优选从5.5重量%至53重量%,甚至更优选从6重量%至52重量%,甚至更优选从6.5重量%至51重量%,甚至更优选从7重量%至50重量%,甚至更优选从8重量%至49重量%,甚至更优选从8.5重量%至49重量%,且最优选从9重量%至49重量%。“重量%”(重量百分比)表示在药物组合物中的重量百分比。
[1012]
所述药物组合物可以进一步包含在以下范围内的量的聚合物沉淀抑制剂:从0.1重量%至40重量%,优选0.5重量%至39重量%,更优选1重量%至38重量%,更优选1.25重量%至38重量%,更优选1.5重量%至37重量%,更优选1.75重量%至36重量%,更优选2重量%至35重量%,更优选1.5重量%至34重量%,更优选1.6重量%至33重量%,更优选1.7重量%至32重量%,更优选1.8重量%至31重量%,更优选3.5重量%至30重量%,更优选4重量%至29重量%,更优选4.5重量%至28.5重量%,最优选5重量%至28.5重量%。
[1013]
所述药物组合物可以进一步包含在以下范围内的量的粘合剂:从0重量%至40重量%,优选从0重量%至35重量%,更优选从0重量%至30重量%,更优选从0重量%至25重量%,更优选从0重量%至20重量%,更优选从0重量%至15重量%,更优选从0重量%至12重量%,且最优选从0重量%至8.5重量%。
[1014]
所述药物组合物可以进一步包含在以下范围内的量的崩解剂:从0.1重量%至40重量%,优选从1重量%至35重量%,甚至更优选从2重量%至30重量%,甚至更优选从2.5重量%至29重量%,甚至更优选从3.0重量%至28重量%,甚至更优选从3.5重量%至27重量%,且最优选从3.5重量%至26.5重量%。
[1015]
所述药物组合物可以进一步包含在以下范围内的量的润滑剂/助流剂:从0.1重量%至10重量%,优选从0.25重量%至9.5重量%,更优选从0.5重量%至9重量%,更优选从0.75重量%至8.5重量%,更优选从1重量%至8重量%,更优选从1.25重量%至7.5重量%,更优选从1.5重量%至7重量%,且甚至更优选1.5重量%至6.5重量%。
[1016]
所述药物组合物可以进一步包含在以下范围内的量的稀释剂/填充剂/粘合剂:从0重量%至50%重量%,优选从1重量%至47.5%重量%,更优选从1.5重量%至45%重量%,更优选从2重量%至42.5%重量%,更优选从2.5至40重量%,更优选从3重量%至38%重量%,更优选3.5重量%至38重量%,更优选4重量%至38重量%,更优选至重量%,更优选4.5重量%至38重量%,且甚至更优选5重量%至38重量%
[1017]
所述药物组合物可以进一步包含相对于剂型在以下范围内的量的其它成分:从5
重量%至60重量%,优选从6重量%至57.5重量%,更优选7重量%至55重量%,甚至更优选从8重量%至52.5重量%,甚至更优选从9重量%至51重量%,且最优选10重量%至50重量%。
[1018]
在一个优选实施方案中,本发明涉及用于保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤和/或预防或治疗肝障碍/疾病的药物组合物,其中所述药物组合物包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯、3重量%至75重量%的酸化剂、2重量%至35重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂和1重量%至9重量%的润滑剂/助流剂。
[1019]
在一个优选实施方案中,本发明涉及用于保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤和/或预防或治疗肝障碍/疾病的药物组合物,其中所述药物组合物包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯、3重量%至75重量%的己二酸、2重量%至35重量%的l-羟丙基纤维素和/或羟丙基纤维素、0重量%至12重量%的聚维酮k25、2重量%至35重量%的交联羧甲基纤维素钠和1重量%至9重量%的滑石粉或二氧化硅。
[1020]
此外,在所述药物组合物中,所述酸化剂相对于(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐的质量的质量比的范围可以为从15至0.1质量/质量,优选从14.5至0.2质量/质量,更优选从14.0至0.3质量/质量,更优选从13.5至0.4质量/质量,更优选从13.0至0.5质量/质量,更优选从12.5至0.6质量/质量,更优选从12.0至0.7质量/质量,更优选从11.75至0.8质量/质量,更优选从11.5至0.9质量/质量,更优选从11.5至1.0质量/质量,更优选从11.5至1.1质量/质量,更优选从11.5至1.2质量/质量,更优选从11.5至1.3质量/质量,更优选从11.5至1.4质量/质量,更优选从11.5至1.5质量/质量,更优选从11.5至1.6质量/质量,更优选从11.5至1.7质量/质量,且最优选地优选从11.5至1.8质量/质量。
[1021]
此外,在所述药物组合物中,所述聚合物沉淀抑制剂相对于(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐的质量的质量比的范围可以为从0.05至10质量/质量,优选从0.06至9.5质量/质量,更优选从0.07至9.00质量/质量,更优选从0.08至8.50质量/质量,更优选从0.09至8.00质量/质量,更优选从0.1至7.5质量/质量,更优选从0.11至7.25质量/质量,更优选从0.12至7质量/质量,更优选从0.13至6.75质量/质量,更优选从0.14至6.5质量/质量,更优选从0.15至6.25质量/质量,甚至更优选从0.16至6质量/质量,甚至更优选从0.17至5.75质量/质量,甚至更优选从0.18至5.5质量/质量,甚至更优选从0.19至5.25质量/质量,且最优选从0.20至5质量/质量。
[1022]
此外,在所述药物组合物中,所述粘合剂相对于(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐的质量的质
量比的范围可以为从0-10质量/质量,优选从0.05至9.5质量/质量,更优选从0.06至9.00质量/质量,更优选从0.07至8.50质量/质量,更优选从0.08至8.00质量/质量,更优选从0.09至7.5质量/质量,更优选从0.1至7.25质量/质量,更优选从0.11至7.00质量/质量,更优选从0.12至6.75质量/质量,更优选从0.13至6.50质量/质量,更优选从0.14至6.25质量/质量,甚至更优选从0.15至6.00质量/质量,甚至更优选从0.16至5.75质量/质量,甚至更优选从0.17至5.50质量/质量,甚至更优选从0.18至5.25质量/质量,甚至更优选从0.19至5.5质量/质量,甚至更优选从0.20至5质量/质量,甚至更优选从0.20至4.5质量/质量,甚至更优选从0.20至4质量/质量,甚至更优选从0.20至3.5质量/质量,甚至更优选从0.20至3质量/质量,甚至更优选从0.20至2.5质量/质量,且甚至更优选从0.20至2质量/质量。
[1023]
此外,在所述药物组合物中,所述崩解剂相对于(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐的质量的质量比的范围可以为从0.05至12质量/质量,优选从0.06至11.5质量/质量,更优选从0.07至11质量/质量,更优选从0.08至10.5质量/质量,更优选从0.09至10质量/质量,更优选从0.1至9.5质量/质量,更优选从0.11至9质量/质量,更优选从0.12至8.5质量/质量,更优选从0.13至8质量/质量,更优选从0.14至7.5质量/质量,更优选从0.15至7质量/质量,甚至更优选从0.16至6.5质量/质量,甚至更优选从0.17至5.5质量/质量,甚至更优选从0.18至5质量/质量,甚至更优选从0.19至5质量/质量,且最优选0.2至5质量/质量。
[1024]
此外,在所述药物组合物中,所述润滑剂/助流剂相对于(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐的质量的质量比的范围可以为从0.05至2质量/质量,优选从0.06至1.8质量/质量,更优选从0.07至1.6质量/质量,0.08至1.4质量/质量,更优选从0.09至1.3质量/质量,且最优选从0.1至1.2质量/质量。
[1025]
此外,在所述药物组合物中,所述稀释剂/填充剂/粘合剂相对于(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐的质量的质量比的范围可以为从0质量/质量至20质量/质量,更优选0.01质量/质量至17.5质量/质量,更优选0.05质量/质量至15质量/质量,更优选0.1质量/质量至0.125质量/质量,更优选0.15质量/质量至10质量/质量,更优选0.175质量/质量至7.5质量/质量,更优选0.2质量/质量至6,更优选0.2质量/质量至5.5,更优选0.2质量/质量至5质量/质量。
[1026]
此外,在所述药物组合物中,其它成分相对于(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯或其对映异构体、溶剂化物、水合物或药学上可接受的盐的质量的质量比的范围可以为从0-30质量/质量,优选从0.2至27.5质量/质量,更优选从0.3至25质量/质量,更优选从0.35至22.5质量/质量,甚至更优选从0.4至21质量/质量,且最优选从0.45至20质量/质量。
[1027]
在一个优选实施方案中,本发明涉及所述用于保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤和/或预防或治疗肝障碍/疾病的药物组合物,其中所述药物组合物包含
1-15质量/质量的酸化剂、0.1至7质量/质量的聚合物沉淀抑制剂,其中相对于(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯的质量计算所述化合物的质量/质量(质量比)。
[1028]
本发明的另一个方面涉及有效量的式(i)的化合物(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯:
[1029][1030]
其对映异构体、溶剂化物、水合物或药学上可接受的盐用于制备作为肝保护剂的包含式(i)的化合物的药物组合物的用途。
[1031]
在一个实施方案中,本发明涉及有效量的化合物(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯、其对映异构体、溶剂化物、水合物或药学上可接受的盐或所述药物组合物在药物制备中的用途,所述药物用于保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤和/或预防或治疗肝障碍/疾病。
[1032]
优选地,所述肝毒性或所述肝障碍/疾病由至少一种肝毒物、乳糜泻或病毒感染造成。
[1033]
具体地,所述至少一种肝毒物选自包含以下成员或由以下成员组成的集合:有毒的化学物质、外源性物质、抗癌药物、免疫抑制药物、镇痛药物、抗炎药物、抗结核药物、生物制品、辐射、重金属、真菌毒素、半乳糖胺和脂多糖,与特定遗传表型(hla dq2/dq8)和由转谷氨酰胺酶2(tg2)促进的病理学相关的乳糜泻;和/或甲型、乙型、丙型肝炎病毒的病毒感染。
[1034]
在一个实施方案中,本发明涉及有效量的式(i)的化合物、其对映异构体、溶剂化物、水合物或药学上可接受的盐或所述药物组合物在药物制备中的用途,所述药物用于保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤和/或预防或治疗肝障碍/疾病,其中所述化合物降低至少一种肝酶的血清水平,优选地所述至少一种肝酶选自丙氨酸氨基转移酶(alt)、天冬氨酸氨基转移酶(ast)和碱性磷酸酶(alp)。
[1035]
在一个实施方案中,本发明涉及有效量的式(i)的化合物、其对映异构体、溶剂化物、水合物或药学上可接受的盐或包含式(i)的化合物的药物组合物在药物制备中的用途,所述药物用于保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤和/或预防或治疗肝障碍/疾病,其中所述肝障碍/疾病是肝纤维化、酒精性肝炎、非酒精性脂肪性肝炎(nash)、非酒精性脂肪肝疾病(nafld)、肝硬化、胆汁淤积性肝疾病诸如原发性硬化性胆管炎(psc)和原发性胆汁性胆管炎(pbc)、自身免疫性肝炎(aih)、酒精性脂肪性肝炎(ash)或肝炎症。
[1036]
在一个实施方案中,本发明涉及有效量的所述药物组合物在药物制备中的用途,
所述药物用于保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤和/或预防或治疗肝障碍/疾病,其中所述药物组合物进一步包含至少一种聚合物沉淀抑制剂。
[1037]
优选地,所述至少一种聚合物沉淀抑制剂选自由以下成员组成的集合:l-羟丙基纤维素、羟丙基纤维素、l-羟丙基纤维素和羟丙基纤维素的组合、聚乙二醇、聚(环氧乙烷)-聚(环氧丙烷)-聚(环氧乙烷)、聚乙烯醇、聚乙烯吡咯烷酮、羧甲基纤维素、甲基纤维素、羟乙基纤维素、羟丙基甲基纤维素、乙基纤维素、聚乙烯基己内酰胺-聚乙酸乙烯酯-聚乙二醇接枝共聚物和羧甲基纤维素钠。
[1038]
在一个实施方案中,本发明涉及有效量的所述药物组合物在药物制备中的用途,所述药物用于保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤、保护/修复肝损伤和/或预防或治疗肝障碍/疾病,其中所述药物组合物进一步包含至少一种酸化剂和/或至少一种粘合剂。
[1039]
优选地,所述至少一种酸化剂选自由以下成员组成的集合:抗坏血酸、有机二羧酸诸如草酸、丙二酸、琥珀酸、戊二酸、酒石酸、富马酸、马来酸、苹果酸、己二酸或谷氨酸、和有机三羧酸诸如柠檬酸或柠檬酸氢钠。
[1040]
优选地,所述至少一种粘合剂选自由以下成员组成的集合:糖、蔗糖、多糖、黄原胶、瓜尔胶、角叉菜胶、从小麦、玉米、大米和马铃薯衍生出的淀粉、从小麦、玉米、大米和马铃薯衍生出的预凝(改性)淀粉、淀粉羟乙酸钠、天然树胶、金合欢胶、明胶、黄蓍胶、海藻的衍生物、海藻酸、海藻酸钠、海藻酸钙铵、纤维素、纤维素衍生物、羟丙基纤维素、l-羟丙基纤维素、低取代的羟丙基纤维素、甲基纤维素、羧甲基纤维素钠、羟丙基甲基纤维素、聚乙烯吡咯烷酮、聚维酮k25。
[1041]
在一个实施方案中,本发明涉及有效量的所述药物组合物在药物制备中的用途,所述药物用于保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤和/或预防或治疗肝障碍/疾病,其中(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯颗粒具有由d(0.95)≤25μm定义的粒度分布。
[1042]
在某些实施方案中,本发明涉及用于所述用途的药物组合物,其中所述药物组合物是口服制剂,优选地所述口服制剂是片剂、胶囊剂、粉剂或颗粒剂。
[1043]
在一个优选实施方案中,本发明涉及有效量的所述药物组合物在药物制备中的用途,所述药物用于保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤和/或预防或治疗肝障碍/疾病,其中所述药物组合物包含1-15质量/质量的酸化剂、0.1至7质量/质量的聚合物沉淀抑制剂,其中相对于(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯的质量计算所述化合物的质量/质量(质量比)。
[1044]
在一个优选实施方案中,本发明涉及有效量的所述药物组合物在药物制备中的用途,所述药物用于保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤和/或预防或治疗肝障碍/疾病,其中所述药物组合物包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯、3重量%至75重量%的酸化剂、2重量%至35重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂和1重量%至9重
量%的润滑剂/助流剂。
[1045]
在一个优选实施方案中,本发明涉及有效量的所述药物组合物在药物制备中的用途,所述药物用于保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤和/或预防或治疗肝障碍/疾病,其中所述药物组合物包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯、3重量%至75重量%的己二酸、2重量%至35重量%的l-羟丙基纤维素和/或羟丙基纤维素、0重量%至12重量%的聚维酮k25、2重量%至35重量%的交联羧甲基纤维素钠和1重量%至9重量%的滑石粉或二氧化硅。
[1046]
本发明的另一个方面涉及一种保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤和/或预防或治疗肝障碍/疾病的方法,所述方法包含给受试者施用有效量的式(i)的化合物(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯:
[1047][1048]
其对映异构体、溶剂化物、水合物或药学上可接受的盐或包含式(i)的化合物的药物组合物作为肝保护剂。
[1049]
优选地,所述肝毒性或所述肝障碍/疾病由至少一种肝毒物、乳糜泻或病毒感染造成。
[1050]
本文中使用的术语“受试者”是哺乳动物,优选人。
[1051]
具体地,所述至少一种肝毒物选自包含以下成员或由以下成员组成的集合:有毒的化学物质、外源性物质、抗癌药物、免疫抑制药物、镇痛药物、抗炎药物、抗结核药物、生物制品、辐射、重金属、真菌毒素、半乳糖胺和脂多糖;与特定遗传表型(hla dq2/dq8)和由转谷氨酰胺酶2(tg2)促进的病理学相关的乳糜泻;和/或甲型、乙型、丙型肝炎病毒的病毒感染。
[1052]
在一个实施方案中,本发明涉及保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤和/或预防或治疗肝障碍/疾病的方法,所述方法包含给受试者施用有效量的式(i)的化合物、其对映异构体、溶剂化物、水合物或药学上可接受的盐或所述药物组合物,其中所述式(i)的化合物降低至少一种肝酶的血清水平,优选地所述至少一种肝酶选自丙氨酸氨基转移酶(alt)、天冬氨酸氨基转移酶(ast)和碱性磷酸酶(alp)。
[1053]
在一个实施方案中,本发明涉及保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤和/或预防或治疗肝障碍/疾病的方法,所述方法包含给受试者施用有效量的式(i)的化合物、其对映异构体、溶剂化物、水合物或药学上可接受的盐或所述包含式(i)的化合物的药物组合物,其中所述肝障碍/疾病是肝纤维化、酒精性肝炎、非酒精性脂肪性肝炎(nash)、非酒精性脂肪肝疾病(nafld)、肝硬化、胆汁淤积性肝疾病诸如原发性硬化性胆管
炎(psc)和原发性胆汁性胆管炎(pbc)、自身免疫性肝炎(aih)、酒精性脂肪性肝炎(ash)或肝炎症。
[1054]
在一个实施方案中,本发明涉及保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤和/或预防或治疗肝障碍/疾病的方法,所述方法包含给受试者施用有效量的所述包含式(i)的化合物的药物组合物,其中所述药物组合物进一步包含至少一种聚合物沉淀抑制剂。
[1055]
优选地,所述至少一种聚合物沉淀抑制剂选自由以下成员组成的集合:l-羟丙基纤维素、羟丙基纤维素、l-羟丙基纤维素和羟丙基纤维素的组合、聚乙二醇、聚(环氧乙烷)-聚(环氧丙烷)-聚(环氧乙烷)、聚乙烯醇、聚乙烯吡咯烷酮、羧甲基纤维素、甲基纤维素、羟乙基纤维素、羟丙基甲基纤维素、乙基纤维素、聚乙烯基己内酰胺-聚乙酸乙烯酯-聚乙二醇接枝共聚物和羧甲基纤维素钠。
[1056]
在一个实施方案中,本发明涉及保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤和/或预防或治疗肝障碍/疾病的方法,所述方法包含给受试者施用有效量的所述药物组合物,其中所述药物组合物进一步包含至少一种酸化剂和/或至少一种粘合剂。
[1057]
优选地,所述至少一种酸化剂选自由以下成员组成的集合:抗坏血酸、有机二羧酸诸如草酸、丙二酸、琥珀酸、戊二酸、酒石酸、富马酸、马来酸、苹果酸、己二酸或谷氨酸、和有机三羧酸诸如柠檬酸或柠檬酸氢钠。
[1058]
优选地,所述至少一种粘合剂选自由以下成员组成的集合:糖、蔗糖、多糖、黄原胶、瓜尔胶、角叉菜胶、从小麦、玉米、大米和马铃薯衍生出的淀粉、从小麦、玉米、大米和马铃薯衍生出的预凝(改性)淀粉、淀粉羟乙酸钠、天然树胶、金合欢胶、明胶、黄蓍胶、海藻的衍生物、海藻酸、海藻酸钠、海藻酸钙铵、纤维素、纤维素衍生物、羟丙基纤维素、l-羟丙基纤维素、低取代的羟丙基纤维素、甲基纤维素、羧甲基纤维素钠、羟丙基甲基纤维素、聚乙烯吡咯烷酮、聚维酮k25。
[1059]
在一个实施方案中,本发明涉及保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤和/或预防或治疗肝障碍/疾病的方法,所述方法包含给受试者施用有效量的所述药物组合物,其中(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯颗粒具有由d(0.95)≤25μm定义的粒度分布。
[1060]
在某些实施方案中,本发明涉及保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤和/或预防或治疗肝障碍/疾病的方法,所述方法包含给受试者施用有效量的所述药物组合物,其中所述药物组合物是口服制剂,优选地所述口服制剂是片剂、胶囊剂、粉剂或颗粒剂。
[1061]
在一个优选实施方案中,本发明涉及保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤和/或预防或治疗肝障碍/疾病的方法,所述方法包含给受试者施用有效量的所述药物组合物,其中所述药物组合物包含1-15质量/质量的酸化剂、0.1至7质量/质量的聚合物沉淀抑制剂,其中相对于(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯的质量计算所述化合物的质量/质量(质量比)。
[1062]
在一个优选实施方案中,本发明涉及保护肝脏免于肝毒性、改善肝功能、保护/修
复肝损伤和/或预防或治疗肝障碍/疾病的方法,所述方法包含给受试者施用有效量的药物组合物,其中所述药物组合物包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯、3重量%至75重量%的酸化剂、2重量%至35重量%的聚合物沉淀抑制剂、0重量%至12重量%的粘合剂、2重量%至35重量%的崩解剂和1重量%至9重量%的润滑剂/助流剂。
[1063]
在一个优选实施方案中,本发明涉及保护肝脏免于肝毒性、改善肝功能、保护/修复肝损伤和/或预防或治疗肝障碍/疾病的方法,所述方法包含给受试者施用有效量的药物组合物,其中所述药物组合物包含0.1重量%至45重量%的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯、3重量%至75重量%的己二酸、2重量%至35重量%的l-羟丙基纤维素和/或羟丙基纤维素、0重量%至12重量%的聚维酮k25、2重量%至35重量%的交联羧甲基纤维素钠和1重量%至9重量%的滑石粉或二氧化硅。
附图说明:
[1064]
图1显示了在uuo-模型中的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯(化合物1)。
[1065]
图2显示了在不同的剂量在肾组织中的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯(化合物1)和tg2的复合物的免疫组织化学证据。
[1066]
图3显示了在nash-模型中的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯(化合物1)。
[1067]
图4显示了(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯在c57bl/6-小鼠中的药代动力学。
[1068]
图5显示了剂量-活性关系。对于stam-和uuo-模型,描绘了依赖于剂量或依赖于暴露(血浆cmax或血浆-auc)的抗纤维化作用。
[1069]
图6显示了根据实施例7的多次定量施用后化合物的血浆曲线及其可推导出的人药代动力学数据。
[1070]
图7显示了人药代动力学数据与tg2抑制的体外数据的关联。
[1071]
图8显示了在制剂中或作为单纯化合物的不同剂量的式i的化合物在施用以后达到的最大血浆浓度(cmax)。为了汇编来自不同物种的数据,考虑到物种之间体表面积的差异,将剂量转换为人等效剂量(hed)。使用了在fda指南“估算治疗剂在成年健康志愿者中的初始临床试验中的最大安全起始剂量(estimating the maximum safe starting dose in initial clinical trials for therapeutics in adult healthy volunteers)”(发布日期2005年)中定义的被广泛接受的物种特异性转换因子。
[1072]
图9显示了依赖于cmax值以及auc值的在动物模型中的抗纤维化作用。此外,显示
了通过10、20和50mg剂量的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯在人中达到的cmax值。
[1073]
图10显示了依赖于auc值的在动物模型中的抗纤维化作用。此外,显示了通过10、20和50mg剂量的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯在人中达到的auc值。
[1074]
图11显示了(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯的饱和溶解度。
[1075]
图12显示了实施例14的试验设计示意图。
具体实施方案
[1076]
实施例1
[1077]
(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯(式(i)的化合物)的制备
[1078]
实施例1.1 6-氨基-庚-2-烯-二甲酸衍生物的制备
[1079]
(s)-2-(叔丁氧基羰基氨基)戊烷二酸1-叔丁基5-甲基酯
[1080][1081]
分子式:c15h27no6
[1082]
分子量:317.38
[1083]
将12.0g boc-glu-otbu(39.6mmol)溶解在200ml dmf中。在氩气氛下,加入7.09g碳酸铯(21.8mmol,0.55当量),并将得到的悬浮液在室温搅拌1小时。该时间以后,加入2.47ml碘代甲烷(39.6mmol)并在室温搅拌过夜。在真空中除去溶剂,并将得到的残余物溶解于400ml乙酸乙酯中。将未溶解的固体过滤并将滤液分别用75ml10%柠檬酸、10% nahco3溶液和盐水洗涤3次。将有机相经na2so4干燥以后,在真空中除去溶剂。得到作为黄色油的产物。产物可以不经进一步纯化地用在后续反应中。
[1084]
收率:13.4g,》100%
[1085]
esi-ms:340.2[m na]
[1086]
(s)-2-(双(叔丁氧基羰基)氨基)戊烷二酸1-叔丁基5-甲基酯
[1087][1088]
分子式:c20h35no8
[1089]
分子量:417.49
[1090]
将13.4g boc-glu(ome)-otbu(~39.6mmol)溶解在30ml乙腈中并用986mg dmap(7.91mmol,0.2当量)处理。在氮气氛下,加入17.6g二碳酸二叔丁酯(77.1mmol,2当量)在100ml乙腈中的溶液。搅拌过夜以后,在真空中除去溶剂并将得到的粗产物通过硅胶上的色谱法(柱:31*6.0cm,石油醚/乙酸乙酯9:1)纯化。
[1091]
柱色谱法:收集在250ml级分中,产物:级分6-13
[1092]
tlc对照:石油醚/乙酸乙酯8:2,rf=0.70
[1093]
收率:13.7g,32.8mmol,83%
[1094]
esi-ms:440.3[m na]
[1095]
(s)-2-(双(叔丁氧基羰基)氨基)-5-氧代戊酸叔丁酯
[1096][1097]
分子式:c19h33no7
[1098]
分子量:387.47
[1099]
将13.7g boc
2-glu(ome)-otbu(32.8mmol)溶解在200ml绝对乙醚中并在氩气氛下冷却至-78℃。在该温度,缓慢地滴入36.1ml(36.1mmol,1.1当量)的二异丁基氢化铝溶液(1m在己烷中)。加入以后,将溶液在-78℃搅拌另外15min,然后将反应混合物通过在相同温度加入50ml水进行淬灭。在剧烈搅拌下,将它温热至室温,并将混浊的溶液经硅藻土过滤。将滤液浓缩至干燥(in dryness)并将残余的水通过与甲苯一起共蒸馏而除去。得到浅色油,并将它不经进一步纯化地用在后续反应中。
[1100]
tlc对照:石油醚/乙酸乙酯8:2,rf=0.54
[1101]
收率:13.3g,》100%(纯度86.1%)
[1102]
500-mhz-1
h-nmr-cosy(dmso
d6
):δ[ppm]=9.65(s,1h,h-4),4.63(dd,1h,h-1,j
1/2a
=4.8hz,j
1/2b
=9.85hz),2.51-2.50(m,1h,h-3a),2.48-4.40(m,1h,h-3b),2.27-2.20(m,1h,h-2a),1.98-1.91(m,1h,h-2b),1.44(s,18h,6*ch3(boc)),1.92(s,9h,3*ch3(o-tbu)
[1103]
esi-ms:410.4[m na]
[1104]
(s,e)-6-(双(叔丁氧基羰基)氨基)庚-2-烯二酸7-叔丁基1-甲基酯
[1105][1106]
分子式:c22h37no8
[1107]
分子量:443.53
[1108]
将13.2g boc
2-glu(h)-otbu(~32.8mmol)提供在20ml干燥的苯中并在氩气氛下在室温加入11.2g的(甲氧基羰基亚甲基)-三苯基-正膦溶液(32.8mmol)。搅拌过夜以后,在真空中除去溶剂并将得到的油状残余物通过硅胶上的色谱法(柱:39*6.0cm,石油醚/乙酸乙酯9:1)纯化。
[1109]
柱色谱法:收集在250ml级分中,产物:级分2-12
[1110]
tlc对照:石油醚/乙酸乙酯8:2,rf=0.54
[1111]
收率:12.0g,27.1mmol,83%
[1112]
500-mhz-1
h-nmr-cosy(dmso
d6
):δ[ppm]=6.66(dt,1h,h-4,j
4/3
=6.8hz j
4/5
=15.9hz),5.64(d,1h,h-5,j
5/4
=15.9hz),4.45-4.2(m,1h,h-1),3.44(s,3h,ch
3-6),2.01-1.95(m,2-h,h-3a,h-3b),1.95-1.86(m,1h,h-2a),1.78-1.67(m,1h,h-2b),1.24(s,18h,6*ch3(boc)),esi-ms:466.3[m na]
[1113]
(s,e)-2-(叔丁氧基羰基氨基)-7-甲氧基-7-氧代庚-5-烯酸(1a1)
[1114][1115]
分子式:c13h21no6
[1116]
分子量:287.31
[1117]
将7.0g(s,e)-6-(双(叔丁氧基羰基)氨基)庚-2-烯二酸7-叔丁基1-甲基酯(15.8mmol)溶解在40ml二氯甲烷中并加入70ml三氟乙酸的溶液中。将它在室温搅拌4h。在真空中除去溶剂,并将绿色残余物在高真空下干燥。将得到的油不经纯化进一步使用。通过连续添加dipea,将ph值调至约7。
[1118]
将该油溶解于50ml的dmf中并用5.37ml dipea处理。加入4.08g的boc-osu
(18.9mmol,1.2当量),并在室温搅拌过夜。在真空中除去溶剂,并将残余物悬浮于130ml的5% khso4溶液中。将它用乙酸乙酯(1x 150ml,2x 100ml)萃取并将纠正过的有机相用盐水(75ml)洗涤。将有机相经na2so4干燥以后,在真空中除去溶剂。将残余物通过硅胶上的色谱法(柱:13*6.0cm,甲苯/乙酸乙酯65:35,0.5%乙酸)纯化。得到无色油。
[1119]
柱色谱法:收集在200ml级分中,产物:级分2-5,第一次运行500ml
[1120]
tlc对照:甲苯/乙酸乙酯1:1,0.5%乙酸,rf=0.35
[1121]
收率:4.04g,14.1mmol,89%(纯度88.6%);esi-ms:310.1[m na]
[1122]
实施例1.2吡啶酮衍生物的制备
[1123]
3-羟基吡啶-3-基-氨基甲酸苄酯
[1124][1125]
分子式:c13h12n2o3
[1126]
分子量:244.25
[1127]
将15g的2-羟基-烟酸(108mmol)悬浮于180ml干燥的二氧杂环己烷中。加入14.9ml三乙胺(108mmol)以后,悬浮液完全澄清。加入24ml二苯基磷酰基叠氮化物(dppa,108mmol),并将反应溶液在氩气氛下回流(130℃)。由此,观察到气体产生。16h以后,接连地加入另外16.3ml的tea和12.8ml苯甲醇(117mmol,1.1当量)并回流另外24h。
[1128]
在真空中除去溶剂,并将得到的棕色残余物溶解于300ml dcm和300ml盐水的混合物中。用1m hcl溶液,将ph值调至约1(约22ml),进行相分离并随后将水相用各200ml dcm萃取2次。将纠正过的有机相用10% nahco3溶液(3x150 ml)和盐水(1x 150ml)洗涤,经na2so4干燥,过滤并在真空中浓缩至干燥(in dryness)。将得到的棕色固体从300ml甲醇中重结晶。
[1129]
tlc对照:dcm/meoh 9:1,rf=0.70
[1130]
收率:16.2g,66.4mmol,62%(淡棕色,毡状固体)
[1131]
esi-ms:245.1[m h]
[1132]
2-(3-(苄氧基羰基氨基)-2-氧代吡啶-1(2h)-基)乙酸叔丁酯
[1133][1134]
分子式:c19h22n2o5
[1135]
分子量:358.39
[1136]
将16.2g 3-羟基吡啶-3-基-氨基甲酸苄酯(66.4mmol)悬浮于900ml绝对thf中并在氩气氛下冷却至0℃,并加入2.92g nah(60%在矿物油中,73.1mmol,1.1当量)。在气体产生结束后(约15min),向得到的溶液中加入13.7ml溴乙酸叔丁基酯(89.7mmol,1.35当量)。将它仍然在0℃搅拌15分钟并随后在室温搅拌过夜。将反应混合物过滤并将滤液浓缩至干燥(in dryness)。将残余物溶解于5ml乙酸乙酯中并用约50ml乙醚处理,并将得到的悬浮液
在冰箱中沉淀过夜。将晶体滤出,并用少量乙醚洗涤。
[1137]
将滤液浓缩并通过硅胶上的色谱法(床:20x 6cm,洗脱液:石油醚/乙酸乙酯=8/2)纯化。
[1138]
柱色谱法:收集在250ml级分中,产物:级分10-25
[1139]
tlc对照:石油醚/乙酸乙酯=7/3,rf=0.46
[1140]
收率:19.3g,54.0mmol,81%
[1141]
esi-ms:359.1[m h]
[1142]
2-(3-(苄氧基羰基氨基)-2-氧代吡啶-1(2h)-基)乙酸
[1143][1144]
分子式:c15h14n2o5
[1145]
分子量:302.28
[1146]
将4.00g 2-(3-(苄氧基羰基氨基)-2-氧代吡啶-1(2h)-基)乙酸叔丁酯(11.2mmol)溶解在50ml二氯甲烷中并用50ml三氟乙酸处理。将它在室温搅拌3h,然后在真空中除去挥发性组分。在高真空下干燥以后,得到棕色固体,并且它适合不经纯化用于进一步使用。
[1147]
收率:3.70g,》100%
[1148]
esi-ms:303.2[m h]
[1149]
1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基甲酸苄酯
[1150][1151]
分子式:c21h27n3o4
[1152]
分子量:385.46
[1153]
将3.70g 2-(3-(苄氧基羰基氨基)-2-氧代吡啶-1(2h)-基)乙酸(~11.2mmol)、3.58g tbtu(11.2mmol)、1.51g hobt(11.2mmol)的混合物溶解在60ml dmf中。通过加入5.70ml dipea(33.5mmol,3当量),将ph值调至约10。加入1.50ml 2-乙基-丁基胺(11.2mmol),并将混合物在室温搅拌过夜。在真空中除去溶剂,并将得到的残余物溶解于300ml dcm中,并随后用10%柠檬酸(3x75 ml)、饱和nahco3溶液(3x 75ml)和盐水(75ml)洗涤。将有机相经na2so4干燥,过滤并浓缩至干燥(in dryness)。得到淡棕色固体,并且它适合不经进一步纯化用于进一步加工。
[1154]
收率:5.22g,》100%
[1155]
esi-ms:386.3[m h]
[1156]
2-(3-氨基-2-氧代吡啶-1(2h)-基)-n-(2-乙基丁基)乙酰胺(2a)
[1157][1158]
分子式:c13h21n3o2
[1159]
分子量:251.32
[1160]
将5.22g 1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基甲酸苄酯(2.4,~11.2mmol)在氮气氛下溶解在60ml甲醇中。向该溶液中加入500mg pd/c(10%),并在氢气氛下在大气压下搅拌2.5h。将催化剂通过在硅胶上过滤进行分离,然后在真空中除去溶剂。得到深色油,并且它适合不经进一步纯化用于进一步加工。
[1161]
收率:3.62g,》100%
[1162]
esi-ms:252.2[m h]
[1163]
实施例1.3(s,e)-6-(叔丁氧基羰基氨基)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-7-氧代庚-2-烯酸甲酯的制备
[1164][1165]
分子式:c26h40n4o7;分子量:520.62
[1166]
提供3.36g 2-(3-氨基-2-氧代吡啶-1(2h)-基)-n-(2-乙基丁基)乙酰胺(2a,~10.4mmol)在20ml dmf中的溶液。向该溶液中,加入2.97g(s,e)-2-(叔丁氧基羰基氨基)-7-乙氧基-7-氧代庚-5-烯酸(1a1,10.4mmol)、3.93g hatu(10.4mmol)和3.52ml dipea(20.7mmol,2当量)在40ml dmf中的溶液。通过连续添加dipea,将ph值调至约7。将反应混合物在40℃搅拌2.5小时,以及在室温搅拌过夜,然后在真空中除去溶剂。将得到的棕色残余物溶解于250ml乙酸乙酯中,并随后用10%柠檬酸(3x75 ml)、饱和nahco3溶液(3x75 ml)和盐水(75ml)洗涤。将有机相经na2so4干燥并在真空中浓缩至干燥(in dryness)。将残余物通过硅胶上的色谱法(床:13x 6cm,洗脱液:甲苯/丙酮=7/3)纯化。
[1167]
柱色谱法:150ml第一次运行,在40ml级分中纠正,产物:级分6-15
[1168]
tlc对照:dcm/meoh=97/3,rf=0.40
[1169]
收率:3.34g,6.42mmol,62%
[1170]
esi-ms:543.4[m na]
[1171]
(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯(式(i)的化合物)
甲酰氨基)-7-氧代庚-2-烯酸甲酯和tg2的复合物的免疫组织化学定位。
[1184]
结果:
[1185]
用(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯的治疗导致肾脏纤维化区域的显著的、明显的、剂量依赖性减小。羟基脯氨酸含量不受影响。(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯在uuo-模型中的作用如图1所示。不同剂量的式(i)的化合物和tg2的复合物在肾组织中的免疫组织化学定位可以参见图2。
[1186]
结论:与对照相比肾组织学的显著改善表明,式(i)的化合物抑制了纤维化和纤维形成。在肾脏中的作用和潜在机制可能类似于在肝脏中的抗纤维化作用和机制。
[1187]
式(i)的化合物和tg2的复合物的免疫组织化学定位表明,(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯到达靶部位并抑制靶分子。
[1188]
实施例3
[1189]
在非酒精性脂肪性肝炎的stelic动物模型(stam-模型)中的研究
[1190]
在非酒精性脂肪性肝炎的stam-模型中研究了式(i)的化合物在肝脏中的抗纤维化作用。该模型基于借助于化学毒物(noxin)(链脲霉素)和含脂肪饮食的组合在c57bl/6-小鼠中诱导肝脏的慢性纤维化炎症。病理学类似于在人中描述的nash。
[1191]
在两周的时间段内用三种不同剂量的所述化合物直接处理8只stam-小鼠的组:100mg/kg体重、300mg/kg体重和1000mg/kg体重。以8小时的间隔以混悬液形式分两部分口服施用每日剂量。在对照组中,将stam-小鼠以相同的方式处理,但仅使用媒介物甲基纤维素。在处理结束后,测量血浆中的生化参数,并在解剖动物后进行肝脏的组织病理学研究,确定肝脏的脂肪含量以及确定炎症和纤维化标志物的表达。
[1192]
结果:用式(i)的化合物的治疗导致肝脏组织学的显著的、剂量依赖性的改善。详细言之,如在图3中所示的nafld活性评分(nas)在中和高剂量组中降低。nas的改善主要是由于肝细胞的炎症和气球样变(膨胀)的减轻。此外,可以观察到肝脏纤维化面积的明显的剂量依赖性减小,这在中和高剂量组中是显著的。与历史数据相比,高剂量组中纤维化的减小发生在作为阳性对照的替米沙坦的区域中。
[1193]
结论:式(i)的化合物的抗纤维化作用可能是由于肝脏中的tg2的抑制。结果,胶原纤丝的交联被阻止,并且与未处理的对照动物相比纤维化的形成减少。炎症和气球样变的减少可能继发于抗纤维化作用。(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯对肝脏中的脂肪含量没有影响。
[1194]
实施例4
[1195]
式(i)的化合物在c57bl/6-小鼠中的药代动力学
[1196]
该研究用于描述式(i)的化合物在c57bl/6-小鼠中的药代动力学。剂量类似于在stam-模型中(实施例3)或在uuo-模型中(实施例2)的剂量,以确保在这些模型中的全身暴露的估算,并将药代动力学数据与效力数据相关联。
[1197]
在7天的时间段内,用三种不同剂量的式(i)的化合物处理12只c57bl/6-小鼠的
组:100mg/kg体重、300mg/kg体重和1000mg/kg体重。以8小时的间隔以混悬液形式分两部分口服施用每日剂量。在处理的第7天,收集每只动物的三个不同血液样品。组中的时间点以这样的方式分布:24小时曲线被总共12个不同的时间点覆盖(每个时间点3只动物)。
[1198]
借助于先前验证过的hlpc-ms/ms方法,测定血浆中的式(i)的化合物。
[1199]
结论:式(i)的化合物的血浆曲线以及可推导出的药代动力学数据描绘在图4中。
[1200]
实施例5
[1201]
剂量-活性关系
[1202]
与未处理的对照动物相比组织中纤维化面积的减小可以被认为是式(i)的化合物在stam-模型中以及在uuo-模型中的抗纤维化作用的量度。对于stam-和uuo-模型,依赖于剂量或依赖于暴露的抗纤维化作用(血浆cmax或血浆-auc)描绘在图5中。
[1203]
结果:剂量-活性关系的研究结果描绘在图5中。
[1204]
结论:尽管肝脏和肾脏的组织结构不同,并且纤维化变化的发病机制在stam-模型中和在uuo-模型中存在根本不同,但是式(i)的化合物在两种模型中表现出相同的抗纤维化作用。明显的非线性剂量-活性关系可能是由于在此处应用的高剂量的口服施用以后吸收和全身暴露的饱和。如果考虑依赖于血浆中暴露的抗纤维化作用,则获得几乎线性的相关性。
[1205]
实施例6
[1206]
硬明胶胶囊剂的制备
[1207]
6.1硬明胶胶囊剂的制备a
[1208]
使用96%乙醇作为制粒液体,借助于湿法制粒进行酸性颗粒的制备。将式(i)的化合物、l-羟丙基纤维素和交联羧甲基纤维素钠以干燥形式过筛,并混合,此后通过加入乙醇,进行颗粒团聚和颗粒结构的形成。将颗粒块以湿形式过筛,在70℃干燥,并最后再次过筛。在干燥的混合器中,将过筛的己二酸以及滑石粉加入干燥的颗粒并混合。此后,将粉末混合物填充进硬明胶胶囊中。
[1209]
6.2硬明胶胶囊剂的制备b
[1210]
为了生产用于口服施用的固体制剂,将(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯(15.0%)与聚乙烯基醇(56.9%)混合。将混合物在热熔化挤出机中处理以得到挤出物。将挤出物冷却并研磨。在干燥的混合器中,将交聚维酮(7.5%)、l-羟丙基纤维素(7.2%)、富马酸(13.5%)加入研磨的挤出物中并混合。此后,将粉末混合物填充进硬明胶胶囊中。
[1211]
6.3硬明胶胶囊剂的制备c
[1212]
将羟丙基纤维素(2.3%)溶解在异丙醇(96%)中以产生制粒液体。混合(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯(38.8%)、纤维素(微晶;7.8%)、聚乙烯基己内酰胺-聚乙酸乙烯酯-聚乙二醇接枝共聚物(7.8%)、交联羧甲基纤维素钠(7.8%)和己二酸(34.9%)。将制粒液体加入粉末掺合物,由此形成颗粒块。将所述块以湿状态过筛,并然后干燥。干燥以后,将所述块再次过筛。在干燥的混合器中将二氧化硅(0.6%)加入干燥的颗粒。此后,将粉末混合物填充进胶囊中。
[1213]
实施例7
[1214]
式(i)的化合物在人中的药代动力学
[1215]
在健康的志愿者中研究了(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯(式(i)的化合物)的药代动力学。在7天的时间段内,将各18位受试者的组群分别用10、20、50和100mg式(i)的化合物的每日剂量处理。借助于先前验证过的hplc-ms/ms方法,进行血浆中所述化合物的测定。
[1216]
结果:在图6中描绘了在多次定量施用以后所述化合物的血浆曲线以及可推导出的人药代动力学数据。
[1217]
结论:用制剂达到的药物浓度在10-100mg剂量范围内按剂量比例增加,并且当归一化至体重时,明显高于在以混悬液形式施用药物的动物研究中的结果。
[1218]
将达到的药物浓度与在体外导致tg2酶活性抑制的浓度进行对比(图7)。由此,代表tg2的交联功能的、由tg2催化的丹磺酰基-尸胺(dansyl-cadaverine)向n,n二甲基酪蛋白中的掺入(dcc-测定)充当标记反应。根据这种相关性,已经在20mg的剂量达到tg2的半数最大抑制(ic
50
)。50mg新开发的制剂的剂量导致已经超过酶抑制的ic
90
的药物水平。在ic
90
的90%抑制可以视为最大药效动力学作用。
[1219]
实施例8
[1220]
制剂的药代动力学数据与单纯化合物的药代动力学数据的对比
[1221]
在施用实施例6所描述的硬明胶胶囊制剂以后,产生了在实施例7中描述的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯(式(i)的化合物)的人药代动力学数据。
[1222]
为了估算制剂的影响,将硬明胶制剂的药代动力学数据与口服施用未配制的单纯化合物以后产生的药代动力学数据进行对比。由于监管和伦理原因,仅在动物中产生单纯化合物的药代动力学数据,而不在人受试者中产生。
[1223]
单纯化合物的药代动力学数据来自于在猴、猪、兔、大鼠和小鼠中的几项研究。在所有研究中,将所述化合物在0.5%(w/v)甲基纤维素水溶液(ph 5
±
0.5)中悬浮以后口服施用。在药物施用后24h内的不同时间点采集血液样品,并借助于先前验证过的hplc-ms/ms方法进行量化。
[1224]
图8显示了在制剂中或作为单纯化合物的不同剂量的式i的化合物在施用以后达到的最大血浆浓度(cmax)。为了汇编来自不同物种的数据,考虑到物种之间体表面积的差异,将剂量转换为人等效剂量(hed)。使用了在fda指南“估算治疗剂在成年健康志愿者中的初始临床试验中的最大安全起始剂量(estimating the maximum safe starting dose in initial clinical trials for therapeutics in adult healthy volunteers)”(发布日期2005年)中定义的被广泛接受的物种特异性转换因子。
[1225]
图7中的对比证实,在宽剂量范围内,施用制剂后达到的cmax是施用单纯化合物后达到的cmax的10倍以上。尽管cmax的差异可以部分地归因于药代动力学的物种差异,但来自人和密切相关的猴的数据之间的巨大差异提示,该制剂在实现高全身暴露方面起主要作用。
[1226]
实施例9
[1227]
抗纤维化作用与人药代动力学的相关性
[1228]
(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯在动物模型中的抗纤维化作用提示所述化合物在人的纤维化肝或肾病的情况下的潜在用途。在动物实验中有效的剂量的(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯的全身暴露(cmax、auc)与在人中实现的全身暴露的对比允许估算潜在有效剂量范围。
[1229]
在动物模型中依赖于cmax值以及auc值的抗纤维化作用如图9和图10所示。此外,显示了通过10、20和50mg式(i)的化合物的剂量在人中达到的cmax或auc。
[1230]
结论:纤维化面积与cmax值(图9)或auc值(图10)之间的关系分别提示,在动物模型中显示的抗纤维化作用已经可以用20mg的人剂量实现。在人中,全身暴露进一步线性增加至100mg。来自全身暴露的抗纤维化作用的几乎线性依赖性提示,在较高的剂量,在人中可以实现比在动物模型中更强的抗纤维化作用。
[1231]
实施例10
[1232]
使用hplc/uv在从1至6.8的ph范围内测量式(i)的化合物的饱和溶解度。
[1233]
结果如图11所示。
[1234]
结果:显然,在ph=6.8(小肠)的饱和溶解度远低于在ph~1时。
[1235]
值得注意的是,在小鼠模型中的生物利用度是可测量的,尽管在ph=6.8的饱和溶解度远低于在ph~1时。
[1236]
实施例11:片剂形式的药物组合物的制备
[1237]
11.1片剂形式的药物组合物的制备a
[1238]
为了生产用于口服施用的固体制剂,将(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯(7.6%)与l-羟丙基甲基纤维素(18.3%)、交联羧甲基纤维素钠(1.5%)、聚维酮k25(8.4%)和纤维素(微晶;36.6%)混合。将粉末掺合物与乙醇(96%)一起造粒。湿法过筛以后,将颗粒干燥。将己二酸(13.7%)、交联羧甲基纤维素钠(12.2%)和二氧化硅(1.5%)加入颗粒以得到最终的掺合物,将其压制成片剂。
[1239]
然后可以给片剂包裹由以下组分组成的薄膜:乳糖一水合物、羟丙基甲基纤维素(e464;也被称作羟丙甲纤维素)、二氧化钛(e171)、三醋汀(e1518)、氧化铁黄(e172)和巴西棕榈蜡(e903)。
[1240]
11.2片剂形式的药物组合物的制备b
[1241]
为了生产用于口服施用的固体制剂,将(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯(22.0%)与l-羟丙基甲基纤维素(10.6%)、交联羧甲基纤维素钠(11.0%)和甘露醇(11.0%)混合。用羟丙基纤维素(1.3%)在乙醇(96%)中的溶液将粉末掺合物造粒。湿法过筛以后,将颗粒干燥。将戊二酸(39.7%)和滑石(4.4%)加入颗粒以得到最终的掺合物,将其压制成片剂。
[1242]
11.3片剂形式的药物组合物的制备c
[1243]
为了生产用于口服施用的固体制剂,将(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧
代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯(15.4%)与聚乙烯基醇(58.6%)混合。将混合物在热熔化挤出机中处理以得到挤出物。将产物冷却,研磨,并与交联羧甲基纤维素钠(6.2%)、纤维素(微晶;6.2%)、戊二酸(12.4%)、二氧化硅(0.6%)和滑石粉(0.6%)一起混合以得到最终的掺合物,将其压制成片剂。
[1244]
然后可以给片剂包裹由以下组分组成的薄膜:乳糖一水合物、羟丙基甲基纤维素(e464;也被称作羟丙甲纤维素)、二氧化钛(e171)、三醋汀(e1518)、氧化铁黄(e172)和巴西棕榈蜡(e903)。
[1245]
实施例12:用于胶囊剂的颗粒的制备
[1246]
12.1用于胶囊剂的颗粒的制备a
[1247]
将50mg l-羟丙基纤维素和25mg交联羧甲基纤维素钠加入10mg(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯中。将化合物以干燥状态过筛。加入50mg乙醇,由此形成颗粒块。将所述块以湿状态过筛,并然后干燥。干燥以后,将所述块再次过筛。在干燥的混合器中将115mg己二酸和12mg滑石粉加入干燥的颗粒。此后,将粉末混合物填充进胶囊中。
[1248]
12.2用于胶囊剂的颗粒的制备b
[1249]
将24mg l-羟丙基纤维素溶解在22ml乙醇中以产生制粒液体。混合10mg(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1、2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯、3mg l-羟丙基纤维素(低取代)、25mg交联羧甲基纤维素钠和25mg甘露醇。将制粒液体加入粉末掺合物,由此形成颗粒块。将所述块以湿状态过筛,并然后干燥。干燥以后,将所述块再次过筛。在干燥的混合器中将18mg己二酸和5mg滑石粉加入干燥的颗粒。此后,将粉末混合物填充进胶囊中。
[1250]
12.3用于胶囊剂的颗粒的制备c
[1251]
将羟丙基纤维素(1.3%)溶解在乙醇(96%)中以产生制粒液体。混合(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯(22.0%)、l-羟丙基纤维素(低取代;10.6%)、交联羧甲基纤维素钠(11.0%)和甘露醇(11.0%)。将制粒液体加入粉末掺合物,由此形成颗粒块。将所述块以湿状态过筛,并然后干燥。干燥以后,将所述块再次过筛。在干燥的混合器中将己二酸(39.7%)和滑石粉(4.4%)加入干燥的颗粒中。此后,将粉末混合物填充进胶囊中。
[1252]
实施例13:微粉化工艺
[1253]
将(s,e)-7-(1-(2-(2-乙基丁基氨基)-2-氧代乙基)-2-氧代-1,2-二氢-吡啶-3-基氨基)-6-(1-甲基-1h-咪唑-5-甲酰氨基)-7-氧代庚-2-烯酸甲酯微粉化,其中粒度分布优选地由从0.1至5μm的d(0.1)、从0.3至10μm的d(0.5)、从3至25μm的d(0.95)定义,且粒度范围是从0.1至100μm。
[1254]
实施例14:呈胶囊制剂形式的药物组合物的体内效力和安全性数据和肝保护作用
[1255]
在160名患有乳糜泻(ced)的成年患者中研究了用在实施例2所描述的硬明胶胶囊制剂中的式(i)的化合物进行的6周治疗的效力和安全性。在研究开始时处于临床和组织学
缓解状态的患者接受每天3克谷蛋白摄入的挑战,并随机接受安慰剂或式(i)的化合物的3种剂量之一,即10mg、50mg或100mg。每天早上禁食至少6小时后,患者口服研究药物,随后在30分钟后,在早餐前吃一块含有3g谷蛋白的饼干。在为期6周的研究中,患者被要求继续他们的严格的无谷蛋白饮食(参见图12)。
[1256]
谷蛋白挑战造成在安慰剂组中从基线到第6周丙氨酸氨基转移酶(alt)的轻度但有统计学意义的升高,但令人惊讶的是,在实施例2描述的硬明胶胶囊制剂中的式(i)的化合物的任何组中都没有观察到这种升高。各药物组与安慰剂之间的alt差异具有统计学意义(对于所有对比,p《0.01),从而提示式(i)的化合物对暴露于谷蛋白的乳糜泻患者的肝脏的保护作用。碱性磷酸酶(alp)水平也显示出类似的模式(p《0.05)。在安慰剂组中,所述值归一化至第10周的gfd(表1)。发现式(i)的化合物抑制肝损伤,所述肝损伤是在活动性乳糜泻(ced)中谷蛋白驱动的肠外表现之一,反映为alt和alp的轻度升高(参考文献3),证实所述化合物发挥一般肝保护作用。
[1257]
表1:从基线到第6周的平均(标准差)丙氨酸氨基转移酶(alt)、天冬氨酸氨基转移酶(ast)和碱性磷酸酶(alp)水平(安全人群,单位:u/l)
[1258][1259]
[1260]
成年女性/男性的正常范围:alt、ast(10-35/10-50u/l)、alp(35-104/40-129u/l)
[1261]
实施例14的参考文献:
[1262]
1.s,kaukinen k,collin p,等人.gluten-sensitive hypertransaminasemia in celiac disease:an infrequent and often subclinical finding.the american journal of gastroenterology2011;106:1689-96.
[1263]
2kahaly gj,frommer l,schuppan d.celiac disease and endocrine autoimmunity-the genetic link.autoimmun rev2018;17:1169-75.
[1264]
3.lebwohl b,sanders ds,green phr.coeliac disease.lancet2018;391:70-81.
[1265]
4ludvigsson jf,leffler da,bai jc,等人.the oslo definitions for coeliac disease and related terms.gut 2013;62:43-52.
[1266]
5.schuppan d,junker y,barisani d.celiac disease:from pathogenesis to novel therapies.gastroenterology 2009;137:1912-33.
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。