1.本发明涉及葡萄糖检测领域,具体涉及一种表面包覆纳米铜的泡沫铜及使用该表面包覆纳米铜的泡沫铜作为电极的无酶葡萄糖检测传感器。
背景技术:
2.葡萄糖是人体的重要组成成分,血中的葡萄糖称为血糖(glu),血糖必须保持一定的水平才能维持体内各器官和组织的需要,正常人血浆中葡萄糖含量为3.89-6.11mm,如果葡萄糖含量异常通常会引起生物体严重的疾病,如糖尿病、高血压等。因此快速准确地检测葡萄糖浓度在生命科学及临床医学领域有着十分重要的意义。检测葡萄糖浓度的方法有很多,如荧光检测、光学比色检测、射频测量和电化学检测等。由于具有高灵敏度、超高选择性和易于操作的优点,电化学法受到了广泛的关注。而电化学法的核心就在于传感器的性能。按生物传感器构建可分为有酶和无酶葡萄糖检测传感器,现阶段广泛应用的是有酶葡萄糖检测传感器。然而,有酶葡萄糖检测传感器受限于天然酶易变性、易受影响,导致稳定性差,且制作繁琐,制约了该传感器的发展。无酶葡萄糖检测传感器也就成为了目前研究热点,其利用电极催化或电子传递单元直接氧化葡萄糖,以实现其浓度检测。通常以电极材料划分为贵金属和非贵金属类传感器。虽然贵金属在葡萄糖电氧化中通常表现出较高的催化活性,但其成本高、储量有限制约了其广泛应用。近年来的研究主要集中在非贵金属在电化学无酶葡萄糖检测传感器中的应用。无酶葡萄糖检测传感器的各种非贵金属中,铜和铜基材料因其成本最低、易于合成、良好的电化学性能,是制备无酶葡萄糖检测传感器的一类很好的材料,特别是铜在传感界面上能够快速催化葡萄糖氧化。但是由于铜的传感器灵敏度不足,使用过程易发生氧化,稳定性不足等限制了其进一步的应用。因此,制备一种具有高灵敏度、高选择性和高稳定性的铜基无酶葡萄糖检测传感器仍然是一个挑战。
3.目前铜基无酶葡萄糖检测传感器主要通过改变工艺方法、引入其他金属等手段提高电极灵敏度和稳定性。
4.专利申请cn104698054a公开了一种纳米氧化铜修饰丝网印刷电极的非酶葡萄糖传感器,采用叉指电路,用印刷的方式印制电极,该电极表面积大,故产生活性面积大,从而可提高传感器的灵敏度和精确度,同时利用液相沉淀法制备了纳米氧化铜传感材料,制备得到了高灵敏度的葡萄糖电化学传感器。
5.专利申请cn106996953a公开了一种用于葡萄糖检测的纳米氢氧化铜电极及其制备方法,该法铜基材料表面原位制备纳米cu(oh)2电极,相比于普遍采用的粘涂法制备的电极,不仅导电效率高、稳定性强、过程简单,还可利用各种形貌的铜基及其它导电材料制备电极,便于规模化生产不同形式的电极。但是以上两种制备方法得到的传感器灵敏度和稳定性有限,在实际应用中难以广泛应用。
6.专利申请cn113125533a公开了一种用于葡萄糖检测的方法,以碳布导电为基底,利用电化学方法沉积纳米铜和纳米镍颗粒,制备cu-ni-碳布纳米合金修饰电极,在此基础
上为葡萄糖的测定提供一种新的分析方法。但是该方法仅提供了分析方法,未在葡萄糖检测传感器中使用,没有相关数据,且不可避免使用其他金属,增加了其使用成本。
7.贵金属无酶葡萄糖检测传感器价格高昂,而非贵金属无酶葡萄糖检测传感器中的铜具有价格低,效果好的优点。但是铜的不稳定性制约发展,目前铜基传感器存在灵敏度低、选择性差、稳定性差的缺点。研究者们不可避免的使用其他金属,增加成本。因此,需要开发一种具有高灵敏度、高选择性和高稳定性的铜基无酶葡萄糖检测传感器。
技术实现要素:
8.本发明的目的是为了解决现有技术的贵金属无酶葡萄糖检测传感器价格高昂、非贵金属无酶葡萄糖检测传感器灵敏度低、选择性差、稳定性差的问题,提供了一种表面包覆纳米铜的泡沫铜及使用该表面包覆纳米铜的泡沫铜作为电极的无酶葡萄糖检测传感器。本发明人发现,将泡沫铜材料表面氧化成纳米氧化亚铜,再通过甲酸盐辅助还原将表面转化为纳米铜。在纳米铜的表面得到更多的活性位点并且表面吸附的甲酸根离子在葡萄糖检测中具有极高的选择性、灵敏度和稳定性,由此获得了一种三维多孔、超稳定、超灵敏的葡萄糖检测传感器,大大降低了传统传感器制作成本,具有极高灵敏度,且对葡萄糖具有较高的选择性,对临床人血清和尿液中葡萄糖的检测具有良好的可靠性。
9.本发明的第一方面提供了一种表面包覆纳米铜的泡沫铜,其特征在于,包括泡沫铜基材、包覆在泡沫铜基材表面的纳米铜、以及纳米铜表面的钝化层,所述钝化层至少由铜离子、甲酸根离子和含氧离子构成。
10.在本发明的一种实施方式中,所述包覆在泡沫铜基材表面的纳米铜为纳米铜片或纳米铜球。
11.在本发明的一种实施方式中,所述纳米铜片尺寸为50-200nm,厚度为2-5nm。
12.在本发明的一种实施方式中,所述钝化层至少由碱式甲酸铜二聚体和氧离子构成,所述碱式甲酸铜二聚体至少由铜离子、甲酸根离子和含氧离子配位而成。
13.在本发明的一种实施方式中,所述含氧离子为氧离子和/或氢氧根离子。
14.本发明的第二方面提供了一种表面包覆纳米铜的泡沫铜的制备方法,包括以下步骤:
15.(1)将泡沫铜于含氧气氛或碱性溶液中进行表面氧化处理,得到表面氧化的泡沫铜;
16.(2)使所述表面氧化的泡沫铜与甲酸盐溶液在100-200℃下接触0.5-24小时。
17.在本发明的一种实施方式中,所述表面氧化处理在50-120℃温度下处理2-36小时。
18.在本发明的一种实施方式中,所述甲酸盐溶液的浓度为1-15m(即1-15mol/l)。
19.在本发明的一种实施方式中,向所述甲酸盐溶液中加入选自c8-c20长链胺和/或硫醇的保护剂。
20.在本发明的一种实施方式中,所述甲酸盐溶液中的溶剂为酰胺类溶剂。
21.本发明的第三方面提供了一种本发明的泡沫铜作为电极的用途。
22.本发明的第四方面提供了一种无酶葡萄糖检测传感器,其使用本发明的泡沫铜作为电极。
23.本发明的第五方面提供了一种葡萄糖浓度的检测方法,采用本发明的泡沫铜作为工作电极,采用三电极体系进行检测。
24.本技术具有以下有益效果:
25.1、成本低廉,工艺简单:以铜基材料作为无酶葡萄糖检测传感器电极,克服了有酶型葡萄糖检测传感器自身稳定性差、制作成本高的缺点,使用铜作为电极材料,更进一步降低了在无酶型传感器的成本。仅需通过化学修饰处理便能够解决铜基材料的稳定性问题,工艺步骤简单;
26.2、设计独特:以中空多孔、三维结构的泡沫铜作为导电衬底,拥有更大的比表面积,显著增加催化剂负载,有利于活性位点的暴露,促进葡萄糖的传质,显著提高电化学传感器的催化活性;
27.3、工艺创新:通过加热使铜材料表面氧化,再使用甲酸盐使其还原,在铜材料表面原位生成纳米铜,暴露更多活性位点的同时以甲酸根离子进行修饰,以其作为电极材料的葡萄糖检测传感器在选择性、灵敏度、稳定性上表现十分优异。
附图说明
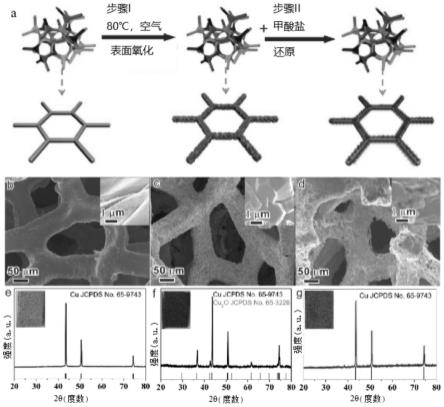
28.图1,(a)表面包覆纳米铜片的泡沫铜的设计与制备示意图;(b,e)泡沫铜、(c,f)表面包覆纳米氧化亚铜的泡沫铜、(d,g)表面包覆纳米铜片的泡沫铜的sem和xrd;
29.图2,从表面包覆纳米铜片的泡沫铜上剥离的纳米铜片的(a)xrd图、(b)tem图、(c)afm图、(d)afm对应高度图;
30.图3,(a)泡沫铜(cf)、表面包覆纳米氧化亚铜的泡沫铜(cu2o-cf)、表面包覆纳米铜片的泡沫铜(cunss-cf)在3mm葡萄糖(glu)的0.1m naoh溶液中的循环伏安曲线(cv)图,扫描速度为50mv/s;(b)泡沫铜、表面包覆纳米氧化亚铜的泡沫铜、表面包覆纳米铜片的泡沫铜在3mm葡萄糖、0.1m naoh中120次循环伏安后相对电流变化图,电压为0.5v;(c)表面包覆纳米铜片的泡沫铜在0.1m naoh中连续加入葡萄糖溶液的电流响应,电压为0.5v;(d)表面包覆纳米铜片的泡沫铜的葡萄糖浓度测定线性校准图;(e)表面包覆纳米铜片的泡沫铜对10nm浓度葡萄糖的电流响应;(f)表面包覆纳米铜片的泡沫铜在0.1m naoh中注射不同分析物时的电流反应图;
31.图4,由表面包覆纳米铜片的泡沫铜制备的葡萄糖检测传感器的临床样品分析(a)尿液、(b)血清的电流响应曲线;由表面包覆纳米铜片的泡沫铜制备的葡萄糖检测传感器的样品分析与医院用标准比色法样品分析(c)尿液、(d)血清;
32.图5,(a,c)表面包覆纳米氧化铜的泡沫铜和(b,d)表面包覆纳米铜球的泡沫铜的sem图;
33.图6,表面包覆纳米氧化铜的泡沫铜和表面包覆纳米铜球的泡沫铜的xrd图;
34.图7,表面包覆纳米铜球的泡沫铜(cunps-cf)在3mm葡萄糖的0.1m naoh溶液中120次伏安循环(电压为0.5v)后相对电流变化图。
具体实施方式
35.下面通过附图和实施例对本技术进一步详细说明。通过这些说明,本技术的特点和优点将变得更为清楚明确。
36.在这里专用的词“示例性”意为“用作例子、实施例或说明性”。这里作为“示例性”所说明的任何实施例不必解释为优于或好于其它实施例。尽管在附图中示出了实施例的各种方面,但是除非特别指出,不必按比例绘制附图。
37.此外,下面所描述的本技术不同实施方式中涉及的技术特征只要彼此之间未构成冲突就可以相互结合。
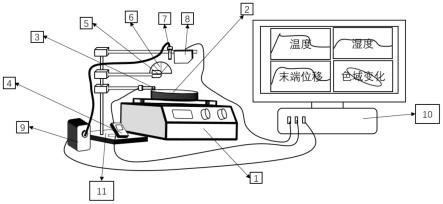
38.电化学传感器是将待测物的化学信号转化为电化学信号进行传感检测的一种传感器,它主要是由电化学工作站、三电极系统以及计算机三部分组成。三电极系统又包括工作电极、参比电极和对电极。工作电极与对电极(常用铂电极)组成一个极化回路,用于电流的测定;而工作电极与参比电极(常用氯化银电极)组成一个测量回路;参比电极提供一个已知电位,用于测定工作电极电位。电化学传感器具有携带方便、操作简单等优点而广泛应用。生物传感器是一种对生物物质敏感并将其浓度转换为电信号进行检测的仪器,是由固定化的生物敏感材料(包括酶、抗体、抗原、微生物、细胞、组织、核酸等生物活性物质)作识别元件、适当的理化换能器(如氧电极、光敏管、场效应管、压电晶体等等)及信号放大装置构成的分析工具或系统。最早使用氧作为酶电子传递的媒介,与电极之间形成电子通道,利用葡萄糖氧化酶在电极表面上形成酶膜,通过对生成产物过氧化氢的浓度或者氧气的消耗量进行测定。
39.在电化学测试葡萄糖浓度中,通常以线性扫描伏安法(lsv)在电极上施加一个特定的电压范围,随着外加电压的线性变化,记录电极上产生的电流,即可在很宽的电位范围内快速观察到氧化还原行为,以此来观察电极对葡萄糖电催化活性;循环伏安法(cv)是在电极上施加一个特定的电压范围,随着外加电压的线性变化,多次循环,记录电极上产生的电流,以此来观察电极在工作中的稳定性和寿命;安培响应法(i-t)是在外加恒电位的条件下,使参比电极和工作电极之间的电位保持恒定,测量对电极与工作电极之间的响应电流,通过测试已知浓度的检测物,得到对应的响应电流,确定检测物浓度与响应电流值的线性关系,从而实现未知浓度检测物的定量分析,也可用于衡量修饰电极的稳定性;通过加入可能的干扰生物分子(如抗坏血酸(aa)、多巴胺(da)、尿酸(ua),它们通常与人体血液中的葡萄糖共存)和葡萄糖类似物(如果糖、乳糖和麦芽糖),观察上述干扰物质是否在葡萄糖检测器中产生电流响应,以此判断选择性;通过检测临床尿液和血清样本中的葡萄糖浓度,进一步评估传感器的可靠性和重现性。
40.无酶葡萄糖检测传感器被称为第四代电化学葡萄糖检测传感器,在不需要酶的参与下,葡萄糖直接吸附在工作电极表面修饰材料上,并与材料发生电催化氧化,通过检测电信号而得到葡萄糖的浓度。相对于有酶葡萄糖检测传感器来说,无酶葡萄糖检测传感器不受环境中氧气的影响且不用考虑酶本身易受影响的问题,测试结果更加稳定,传感器的灵敏度也更高,制备过程中不用考虑酶的固定工艺,成本更低。关于发展无酶葡萄糖检测传感器,已有大量文献报道了一系列材料作为催化葡萄糖的人工酶。比如贵金属(au、pt、ag)、碳纳米材料(碳纳米管、石墨烯)以及过渡金属及其化合物(cu、co、ni)。贵金属因其优异的催化活性和生物相容性使得在该领域收到广泛关注,但是其高昂的价格和易被生物体质干扰的特点直接决定了制备的传感器应用受限,碳基材料拥有大的比表面积和生物活性,适用范围广,但是由于本身对葡萄糖没有活性,常与金属材料制备成复合材料使用。铜有高比表面积及对于葡萄糖有良好的电催化活性,原料易得,是制备无酶葡萄糖检测传感器的一种
很好的材料。
41.过渡金属(cu、co、ni)在碱性条件下,会被氧化成三价金属离子,此时金属离子的d轨道被空出,能够吸附物质于表面形成中间产物,利于催化反应的进行,使得电极表面可以迅速吸附有机物质,可以增强材料之间的协调作用。金属或金属化合物催化剂与葡萄糖发生反应原理如下:
[0042][0043][0044]
m(iii) 葡萄糖
→
m(ii) 葡糖酸内酯
[0045]
本发明的发明人发现,使用具有不同价态、不同形貌和不同基底的cu基材料作为工作电极,可以扩大暴露的活性位点,提高自身的电导率,以提高无酶型葡萄糖传感器的检测性能。通过设计不同的表面结构,更大的比表面积能够提供更多的活性位点,有利于与葡萄糖分子接触,从而获得非常低的检出限和超快响应。基于此,发明人完成了本发明。
[0046]
本发明的第一方面提供了一种表面包覆纳米铜的泡沫铜,其特征在于,包括泡沫铜基材、包覆在泡沫铜基材表面的纳米铜、以及纳米铜表面的钝化层,所述钝化层至少由铜离子、甲酸根离子和含氧离子构成。
[0047]
本发明的第二方面提供了一种表面包覆纳米铜的泡沫铜的制备方法,包括以下步骤:
[0048]
(1)将泡沫铜于含氧气氛或碱性溶液中进行表面氧化处理,得到表面氧化的泡沫铜;
[0049]
(2)使所述表面氧化的泡沫铜与甲酸盐溶液在100-200℃下接触0.5-24小时。
[0050]
泡沫铜是一种在铜基体中均匀分布,大量连通或不连通孔洞的新型多功能材料。泡沫铜的导电性和延展性好,且制备成本比泡沫镍低,导电性能更好,可将其用于制备电池负极(载体)材料、催化剂载体和电磁屏蔽材料。特别是泡沫铜用于电池作电极的基体材料,具有一些明显的优点,但由于铜的耐腐蚀性能不如镍好从而也就限制了它的一些应用。
[0051]
本发明巧妙地利用了铜易氧化的特点,人为使泡沫铜表面轻微氧化,再通过甲酸根将其还原成纳米铜,包覆在泡沫铜的表面,增加了比表面积,同时,原位生成的纳米铜修饰上甲酸根离子,形成了长程有序且致密的由甲酸铜二聚体和o
2-(或氢氧根)构成分子钝化层。这种独特的表面配位结构有效阻碍了o2在表面的吸附和活化,同时不影响cu的本征导电和导热性质。据信,该表面由碱式甲酸铜二聚体[cu(μ-hcoo)(oh)2]2单元和o
2-(或氢氧根)共同保护、钝化。实验和理论计算揭示了该表面配位钝化层的抗氧化防腐能力主要源于其能有效地阻止o2、cl-等氧化/腐蚀物种与内部金属铜的作用。表面甲酸根保障了铜基材及纳米铜本身的稳定性。更重要的是,这种甲酸根修饰的纳米铜表面为负电荷,在生物分子干扰下,具有很强的选择性。故而通过甲酸根修饰的超稳定泡沫铜在葡萄糖检测领域有着惊人的潜力。
[0052]
在本发明的一种示例性实施方式中,泡沫铜可以为各种可商购获得的泡沫铜产品,其规格没有特别的限制;所述包覆在泡沫铜基材表面的纳米铜为纳米铜片或纳米铜球。在本发明的一种优选的示例性实施方式中,所述纳米铜片尺寸为50-200nm,厚度为2-5nm。纳米铜片的尺寸是指纳米铜片的长度和/或宽度。
[0053]
在本发明的一种示例性实施方式中,如上所述,所述钝化层至少由碱式甲酸铜二
聚体和氧离子构成,所述碱式甲酸铜二聚体至少由铜离子、甲酸根离子和含氧离子配位而成。
[0054]
在本发明的一种示例性实施方式中,如图1(a)所示,显示了本发明的表面包覆纳米铜的泡沫铜的设计和制备示意图。首先使泡沫铜置于含氧气氛或碱性溶液中进行表面氧化处理,得到表面氧化的泡沫铜。例如,泡沫铜在80℃的空气中表面氧化为氧化亚铜,形成表面包覆氧化亚铜的泡沫铜。然后使用甲酸盐溶液还原上述表面包覆氧化亚铜的泡沫铜,即可获得表面包覆纳米铜的泡沫铜。
[0055]
在本发明的一种示例性实施方式中,泡沫铜的表面氧化处理可以在含氧气氛或碱性溶液中进行。通过使用不同的表面氧化处理环境,可以调控包覆的铜的形态。例如,在空气气氛中进行表面氧化处理,可以获得纳米铜片,而在氢氧化钠溶液中进行表面氧化处理,可以获得纳米铜球。所述表面氧化处理在50-120℃温度下处理2-36小时,优选在70-100℃温度下处理16-28小时。通过控制表面氧化处理的温度和时间,可以控制泡沫铜的表面的氧化层的厚度。表面氧化处理例如可以在烘箱或在碱溶液中进行。经过表面氧化处理后,泡沫铜的表面由红色变成棕色。
[0056]
在本发明中,在进行表面氧化处理前,优选对泡沫铜进行预处理,除去表面的氧化层,这样能够使得后续进行氧化处理时对氧化的程度进行调控。预处理例如可以通过采用盐酸清洗泡沫铜,然后再用超纯水和无水乙醇反复清洗。盐酸的浓度没有特别的限定,只要能够清洗除去泡沫铜表面的氧化层即可,例如可以为0.1m。
[0057]
在本发明的一种示例性的实施方式中,所述甲酸盐溶液的浓度为1-15m,优选为3-10m。在本发明的一种优选的实施方式中,甲酸盐可以选自甲酸锂、甲酸钠、甲酸镁、三甲酸铝、甲酸钾、甲酸铵、甲酸钙、甲酸锌、甲酸铁、甲酸铜、甲酸钡、甲酸铍、甲酸镍、甲酸钴、甲酸锰中的至少一种,优选为甲酸钠。
[0058]
在本发明的一种示例性的实施方式中,可以向甲酸盐溶液中加入选自c8-c20长链胺和/或硫醇的保护剂,所述c8-c20长链胺优选选自油胺、正辛胺、十二胺、正十三胺、十二烷基二甲基叔胺、十八烷基胺中的至少一种;所述硫醇优选选自甲硫醇、乙硫醇、乙二硫醇、十二硫醇、十六硫醇、1-丙硫醇、1,3-丙二硫醇、巯基吡啶及其衍生物、巯基乙醇、半胱氨酸、谷胱甘肽、巯基乙胺中的至少一种。保护剂用于进一步钝化甲酸根配位层中未能很好保护的台阶或缺陷位点,使铜表面的整体抗氧化性能提升。优选地,保护剂优选为十二胺、油胺。
[0059]
在本发明的一种示例性的实施方式中,所述甲酸盐溶液中的溶剂为酰胺类溶剂,优选选自甲酰胺、n,n-二甲基甲酰胺、n,n-乙甲基甲酰胺、n,n-二甲基乙酰胺、n,n-二乙基乙酰胺和n,n-二甲基丙酰胺中的至少一种。
[0060]
在本发明的一种示例性的实施方式中,甲酸盐溶液的浓度可以在较大范围内变动。为了使反应更有效进行,优选地,甲酸盐溶液的浓度为1-15m。
[0061]
本发明的第三方面提供了一种本发明的泡沫铜作为电极的用途。
[0062]
本发明的第四方面提供了一种无酶葡萄糖检测传感器,其使用本发明的泡沫铜作为电极。
[0063]
本发明的第五方面提供了一种葡萄糖浓度的检测方法,采用本发明的泡沫铜作为工作电极,采用三电极体系进行检测。三电极体系在上文中已经详细描述,在此不再赘述。
[0064]
由本发明方法得到的上述铜材料(尤其表面包覆纳米铜片的泡沫铜)制备的传感
器灵敏度高(8.667ma mm-1
cm-2
)、线性范围宽(0.01μm-0.08mm)、检出限低(10nm)、对葡萄糖的选择性高、抗干扰能力强、稳定性好,可以可靠地用于尿液和血清的临床血糖测定。
[0065]
下面通过实施例进一步说明本发明,但本发明并不限于此。
[0066]
实施例1
[0067]
(1)泡沫铜表面氧化预处理(即表面包覆纳米氧化亚铜的泡沫铜)
[0068]
使用0.1m盐酸清洗商用的泡沫铜(购自国药集团化学试剂有限公司),去除表面氧化层,再用超纯水和无水乙醇反复清洗。将清洗后的泡沫铜置于80℃烘箱中加热24小时,直至表面由红色变为棕色;
[0069]
(2)制备表面负载纳米铜片的泡沫铜(即表面包覆纳米铜片的泡沫铜)
[0070]
称取上述得到的表面预处理的泡沫铜500mg,置于含有200mg甲酸钙和10ml dmf(n,n-二甲基甲酰胺)溶液的耐高温高压容器中超声5分钟,加入2ml十二胺,然后在160℃保温16小时,自然冷却,用超纯水和无水乙醇多次洗涤,得到表面包覆纳米铜片的泡沫铜,真空干燥备用。
[0071]
对应于图1(a)所示的本发明的表面包覆纳米铜的泡沫铜的设计和制备示意图,图1(b)-(g)分别显示了本发明中泡沫铜、表面包覆纳米氧化亚铜的泡沫铜和表面包覆纳米铜片的泡沫铜的sem和xrd谱图。
[0072]
利用本实施例中使用和制备的中空多孔的泡沫铜(即作为原料的商用的泡沫铜)及表面包覆纳米铜片的泡沫铜作为电极,其中,表面包覆纳米铜片的泡沫铜的表面纳米铜片尺寸为50-200nm,厚度为2-5nm,如图2所示。
[0073]
(3)循环伏安检测
[0074]
利用本实施例中使用和制备的中空多孔的泡沫铜(即作为原料的商用的泡沫铜)、表面包覆纳米氧化亚铜的泡沫铜及表面包覆纳米铜片的泡沫铜(均为1
×
0.5cm2)作为工作电极,铂片电极为辅助电极,ag/agcl为参比电极,基于此三电极体系利用电化学工作站进行循环伏安测定,使用的溶液为含3mm葡萄糖的0.1m naoh溶液,扫描速度为50mv/s。结果如图3(a)所示,表面包覆纳米氧化亚铜的泡沫铜及表面包覆纳米铜片的泡沫铜电极均在约0.5v显示出了明显的葡萄糖氧化峰,并且表面包覆纳米铜片的泡沫铜电极的葡萄糖氧化峰明显更强,显示出了表面包覆纳米铜片的泡沫铜电极对葡萄糖氧化更优的催化性能和更高的检测灵敏度。
[0075]
(4)稳定性测试
[0076]
基于上述三电极体系利用电化学工作站进行循环伏安扫描,测定中空多孔的泡沫铜、表面包覆纳米氧化亚铜的泡沫铜及表面包覆纳米铜片的泡沫铜(均为1
×
0.5cm2)电极的电压-电流曲线。经过120次循环伏安后,计算0.5v的葡萄糖氧化的相对电流(与首次循环伏安的初始电流相比),以判断电极长期工作稳定性。如图3(b)所示,表面包覆纳米铜片的泡沫铜电极经120次伏安循环后,相对电流维持在初始电流的88.2%,显示了很高的稳定性。此外,商用的中空多孔的泡沫铜电极相对电流迅速下降至24.0%,表面包覆纳米氧化亚铜的泡沫铜电极相对电流下降至28.7%。
[0077]
下面以本实施例制备的表面包覆纳米铜片的泡沫铜(1
×
0.5cm2)作为工作电极,铂片电极为辅助电极,ag/agcl为参比电极,基于此三电极体系利用电化学工作站测定无酶葡萄糖检测传感器的性能。
[0078]
(5)葡萄糖浓度检测
[0079]
基于上述三电极体系利用电化学工作站进行恒电压检测,测定表面包覆纳米铜片的泡沫铜电极电催化氧化葡萄糖的电流-时间曲线。检测电压恒定为0.5v,在0.1m naoh溶液中逐次加入一定量的葡萄糖溶液并搅拌均匀,使得葡萄糖浓度分别为10nm、0.1μm、1μm、10μm、20μm、50μm、0.25mm、0.5mm、1.0mm。随着葡萄糖浓度的增加,电流也逐渐上升,如图3(c)所示。基于本实施例得到的电流-时间曲线对电流响应与葡萄糖浓度之间的关系进行线性拟合,如图3(d)所示,在0.01μm至0.08mm的浓度范围内,有明显的线性安培响应,葡萄糖浓度与响应电流之间的线性关系为i=0.0096c 0.007(i为电流密度,单位为ma/cm2;c为葡萄糖浓度,单位为μm),线性度r2为0.9982,灵敏度为8.667ma mm-1
cm-2
;如图3(e)所示,当葡萄糖的平衡浓度低至0.01μm,信噪比(s/n)大于3,依然可以触发明显的电流响应,检出限为0.01μm。
[0080]
(6)抗干扰能力测试
[0081]
基于上述三电极体系利用电化学工作站进行恒电压检测,测定血液中常见物质对表面包覆纳米铜片的泡沫铜电极电催化氧化葡萄糖的干扰性,在溶液中逐步加入葡萄糖(glu)、多巴胺(da)、抗坏血酸(aa)、尿酸(ua)、果糖(fru)、乳糖(lac)、麦芽糖(mal)、葡萄糖(glu),对电流响应进行检测。如图3(f)所示,上述干扰物质几乎没有电流响应,表明表面包覆纳米铜片的泡沫铜对血液中常见物质的抗干扰能力强。
[0082]
(7)临床样品分析
[0083]
采用本发明的表面包覆纳米铜片的泡沫铜电极作为无酶葡萄糖检测传感器,基于上述三电极体系利用电化学工作站,检测临床尿液和血清样本中的葡萄糖浓度,与医用标准比色法测量的葡萄糖浓度进行对比,判断该传感器在临川样品分析中的可靠性。基于上述三电极体系利用电化学工作站测定电流-时间曲线,检测电压恒定为0.5v,在0.1m naoh溶液中分别加入糖尿病患者尿液和健康人尿液100μl,重复检测3次。结果如图4(a)所示,与糖尿病患者尿液对比,健康人尿液几乎无反应。在0.1m naoh溶液中分别加入糖尿病患者血清和健康人血清,重复检测3次。结果如图4(b)所示,与糖尿病患者血清对比,健康人血清几乎无反应。如图4(c)和图4(d)所示,测试结果与医院用标准比色法测量的葡萄糖浓度相比,相对标准偏差小于5%。
[0084]
实施例2
[0085]
(1)商业泡沫铜表面氧化预处理
[0086]
使用0.1m盐酸清洗商用的泡沫铜(购自国药集团化学试剂有限公司),去除表面氧化层,再用超纯水和无水乙醇反复清洗。将清洗后的泡沫铜置于80℃的氢氧化钠溶液中24小时;
[0087]
(2)制备表面负载纳米铜球的泡沫铜(即表面包覆纳米铜球的泡沫铜)
[0088]
称取上述得到的表面预处理的泡沫铜500mg,置于含有200mg甲酸钙和10ml dmf溶液的耐高温高压容器中超声5分钟,加入2ml十二胺,然后在160℃保温16小时,自然冷却,用超纯水和无水乙醇多次洗涤,得到表面包覆纳米铜球的泡沫铜,真空干燥备用。
[0089]
如图5的sem和图6的xrd谱图所示,本实施例的泡沫铜经表面氧化预处理后形成表面包覆有纳米氧化铜颗粒的泡沫铜,而得到的表面包覆纳米铜球的泡沫铜由包覆在表面的纳米铜球和中空多孔的泡沫铜构成,其表面纳米铜球尺寸为50-200nm。
[0090]
下面以本实施例制备的表面包覆纳米铜球的泡沫铜(1
×
0.5cm2)为工作电极,铂片电极为辅助电极,ag/agcl为参比电极,基于此三电极体系利用电化学工作站测定无酶葡萄糖检测传感器的性能。
[0091]
(3)葡萄糖浓度检测
[0092]
基于上述三电极体系利用电化学工作站进行恒电压检测,测定表面包覆纳米铜球的泡沫铜电极电催化氧化葡萄糖的电流-时间曲线。检测电压恒定为0.54v,在0.1m naoh溶液中逐次加入一定量的葡萄糖溶液并搅拌均匀,随着葡萄糖浓度的增加,电流也逐渐上升。基于本实施例得到的电流-时间曲线对电流响应与葡萄糖浓度之间的关系进行线性拟合,在0.1μm至0.20mm的浓度范围内,有明显的线性安培响应,葡萄糖浓度与响应电流之间的线性关系为i=8.474c 0.00856(i为电流密度,单位为ma/cm2;c为葡萄糖浓度,单位μm),线性度r2为0.9988,灵敏度为6.196ma mm-1
cm-2
;当葡萄糖的平衡浓度低至0.1μm,信噪比(s/n)大于3,可以触发明显的电流响应,检出限为0.1μm。
[0093]
(4)稳定性测试
[0094]
基于上述三电极体系利用电化学工作站进行循环伏安扫描,测定表面包覆纳米铜球的泡沫铜(均为1
×
0.5cm2)电极测定电压-电流曲线。经过120次循环伏安后,计算其0.5v的葡萄糖氧化的相对电流,以判断电极长期工作稳定性。如图7所示,表面负载纳米铜球的泡沫铜电极经120次伏安循环后,相对电流维持在初始电流的78.8%,显示了很高的稳定性。
[0095]
(5)抗干扰能力测试
[0096]
基于上述三电极体系利用电化学工作站进行恒电压检测,测定血液中常见物质对表面包覆纳米铜球的泡沫铜电极电催化氧化葡萄糖的干扰性,在溶液中逐步加入葡萄糖、多巴胺、抗坏血酸、尿酸、果糖、乳糖、麦芽糖、葡萄糖,对电流响应进行检测,上述干扰物质几乎没有电流响应,表明表面包覆纳米铜球的泡沫铜对血液中常见物质的抗干扰能力强。
[0097]
对比例1
[0098]
(1)纳米铜片的制备:
[0099]
称取商用的纳米氧化铜片(购自国药集团化学试剂有限公司)500mg,置于含有200mg甲酸钙和10ml dmf溶液的耐高温高压容器中超声5分钟,加入2ml十二胺,然后在160℃保温16小时,自然冷却,用超纯水和无水乙醇多次洗涤,得到甲酸根修饰的纳米铜片,真空干燥备用。
[0100]
(2)制备表面负载纳米铜片的玻碳电极
[0101]
将本对比例制备的纳米铜片修饰于玻碳电极上,制成表面负载纳米铜片的玻碳电极,其表面修改的纳米铜片尺寸为50-200nm,厚度为2-5nm。
[0102]
下面以本对比例制备的表面负载纳米铜片的玻碳电极(1
×
0.5cm2)作为工作电极,铂片电极为辅助电极,ag/agcl为参比电极,基于此三电极体系利用电化学工作站测定相关数据。
[0103]
(3)葡萄糖浓度检测
[0104]
基于上述三电极体系利用电化学工作站测定电流-时间曲线。检测电压恒定为0.55v,随着葡萄糖浓度的增加,电流也逐渐上升,基于本对比例得到的电流-时间曲线对电流响应与葡萄糖浓度之间的关系进行线性拟合,在1.0mm至20.0mm的浓度范围内,有明显的
线性安培响应,葡萄糖浓度与响应电流之间的线性关系为i=0.0448c 0.0196(i为电流密度,单位为ma/cm2;c为葡萄糖浓度,单位为μm),线性度r2为0.9970,灵敏度为0.23ma mm-1
cm-2,
当葡萄糖的平衡浓度低至0.5μm,信噪比(s/n)大于3,可以触发明显的电流响应,检出限为0.5μm。这表明这种电极的灵敏度、检出限均明显劣于表面包覆纳米铜的泡沫铜电极。
[0105]
(4)稳定性测试
[0106]
基于上述三电极体系利用电化学工作站测定电压-电流曲线。经过120次循环伏安后,计算其葡萄糖氧化的相对电流,以判断电极长期工作稳定性,表面负载纳米铜片的玻碳电极经120次伏安循环后,相对电流维持在初始电流的76.3%,也低于表面包覆纳米铜的泡沫铜电极。
[0107]
(5)抗干扰能力测试
[0108]
基于上述三电极体系利用电化学工作站测定血液中常见物质的干扰性,在溶液中逐步加入葡萄糖、多巴胺、抗坏血酸、尿酸、果糖、乳糖、麦芽糖、葡萄糖对电流响应进行检测,上述干扰物质几乎没有电流响应。
[0109]
对比例2
[0110]
(1)以商用的泡沫铜(购自国药集团化学试剂有限公司,1
×
0.5cm2)为工作电极,铂片电极为辅助电极,ag/agcl为参比电极,基于此三电极体系利用电化学工作站测定相关数据。
[0111]
(2)葡萄糖浓度检测
[0112]
基于上述三电极体系利用电化学工作站测定电流-时间曲线。检测电压恒定为0.55v,在0.1m naoh溶液中逐次加入一定量的葡萄糖溶液并搅拌均匀,随着葡萄糖浓度的增加,电流也逐渐上升。基于本对比例得到的电流-时间曲线对电流响应与葡萄糖浓度之间的关系进行线性拟合,在1.0μm至0.5mm的浓度范围内,有明显的线性安培响应,葡萄糖浓度与响应电流之间的线性关系为i=5.8549c 0.00141(i为电流密度,单位为ma/cm2;c为葡萄糖浓度,单位为μm),线性度r2为0.9986,灵敏度为5.830ma mm-1
cm-2
;当葡萄糖的平衡浓度低至0.5μm,信噪比(s/n)大于3时,可以触发明显的电流响应,检出限0.5μm。这表明这种电极的灵敏度、检出限均明显劣于表面包覆纳米铜的泡沫铜电极。
[0113]
(3)稳定性测试
[0114]
基于上述三电极体系利用电化学工作站测定电压-电流曲线。经过120次循环伏安后,计算其葡萄糖氧化的相对电流,以判断电极长期工作稳定性,泡沫铜电极经120次伏安循环后,相对电流维持在初始电流的24.0%,明显低于表面包覆纳米铜的泡沫铜电极。
[0115]
(4)抗干扰能力测试
[0116]
基于上述三电极体系利用电化学工作站测定血液中常见物质的干扰性,在溶液中逐步加入葡萄糖、多巴胺、抗坏血酸、尿酸、果糖、乳糖、麦芽糖、葡萄糖对电流响应进行检测,上述干扰物质几乎没有电流响应。
[0117]
表1不同电极材料制作葡萄糖检测传感器数据
[0118][0119]
表1对比了不同材料作为葡萄糖检测传感器电极的检出限、灵敏度和稳定性。可以看出本实施例1经过甲酸根修饰表面包覆纳米铜片的泡沫铜作为电极材料在检出限和灵敏度上均优于表面包覆纳米铜球的泡沫铜,而表面包覆纳米铜球的泡沫铜又均优于无泡沫铜骨架的表面负载纳米铜片的玻碳电极、商用的泡沫铜。实施例1、实施例2、对比例1的纳米铜经过甲酸根修饰,作为电极材料在经过120次伏安循环后依旧稳定,而对比例2中的商用的泡沫铜在经过120次伏安循环后相对电流变化至24.0%,影响了工作使用。实施例1与对比例1对比可以发现,以大比表面积泡沫铜作为基材可以显著提高灵敏度。实施例1与实施例2对比可以发现,在泡沫铜表面包覆纳米铜片对比表面包覆纳米铜球有更好的表现。本实施例1能够通过临床样品(患者尿液、血清)分析测试,与目前医院标准比色法测量的葡萄糖含量偏差小于5%且具有可重复性,本实施例1所述电极材料更具有较高可靠性,能适用于临床分析的葡萄糖检测。
[0120]
以上结合了优选的实施方式对本技术进行了说明,不过这些实施方式仅是范例性的,仅起到说明性的作用。在此基础上,可以对本技术进行多种替换和改进,这些均落入本技术的保护范围内。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。