1.本发明涉及核酸疫苗领域,具体而言,涉及一种预防新型冠状病毒南非突变株病毒感染的疫苗。
背景技术:
2.疫苗的接种有利于全球范围内群体免疫的实现,是终结新型冠状病毒肺炎疫情的关键。然而,疫苗的紧急使用和广泛接种未能真正解除由新型冠状病毒持续引发的公共卫生危机。新型冠状病毒自身性质决定其突变性。在疫情持续的一年多里,新型冠状病毒平均每月发生1-2次变异,出现了传播性、致病性更强的毒株,其中南非突变株(b1.351)可能引起二次感染,正在降低各类疫苗的免疫效果。南非突变株含有k417n、e484k、n501y三个关键突变,其中刺突蛋白受体结合域rbd存在的e484k突变,可能是导致疫苗防护效力下降的关键。因此,新型冠状病毒肺炎疫苗需要及时更新,以抵御新型冠状病毒南非突变株病毒。
3.mrna疫苗的快速研发,简便制备等技术优势更适合新冠病毒及其突变株病毒的预防性疫苗的应急研制与开发。
4.研发我国具有自主知识产权的新冠南非突变株mrna疫苗,不仅对新冠病毒肺炎的防治具有重要意义,还能丰富我国的疫苗储备。mrna疫苗的成功研制很大程度上取决于mrna自身序列的优化,包括抗原编码区和抗原编码区以外的骨架部分。
5.有鉴于此,特提出本发明。
技术实现要素:
6.本发明的第一目的在于提供一种优化新型冠状病毒南非突变株mrna。
7.本发明的第二目的在于提供优化新型冠状病毒南非突变株mrna的应用。
8.本发明的第三目的在于提供与优化新型冠状病毒南非突变株mrna相关的生物材料。
9.本发明的第四目的在于提供一种预防新型冠状病毒南非突变株病毒感染的疫苗。
10.为了实现本发明的上述目的,特采用以下技术方案:
11.一种优化新型冠状病毒南非突变株mrna,转录所述优化新型冠状病毒南非突变株mrna的核苷酸如seq id no.1所示。
12.进一步地,所述优化新型冠状病毒南非突变株mrna的5’端连接有cap结构。
13.上述优化新型冠状病毒南非突变株mrna在制备预防新型冠状病毒南非突变株病毒感染的疫苗中的应用。
14.与上述优化新型冠状病毒南非突变株mrna相关的生物材料,包括如下(1)-(4)任一种:
15.(1)核酸分子,序列如seq id no.1所示;
16.(2)重组载体,含有(1)中核酸分子;
17.(3)工程菌,含有(1)中核酸分子或(2)中重组载体;
18.(4)细胞系,含有(1)中核酸分子或(2)中重组载体。
19.进一步地,重组载体为pcdna3.1( )。
20.进一步地,核酸分子位于pcdna3.1( )的nhei和xhoi位点之间。
21.进一步地,细胞系包括hek293t、hela、vero或huh 7。
22.一种预防新型冠状病毒南非突变株病毒感染的疫苗,所述疫苗的活性成分包括上述优化新型冠状病毒南非突变株mrna。
23.进一步地,还包括疫苗载体。
24.进一步地,疫苗载体包括脂质体、鱼精蛋白、多聚体或脂质多聚体。
25.与现有技术相比,本发明的有益效果为:
26.本发明提供的优化新型冠状病毒南非突变株mrna,由优化骨架代码和抗原编码区构成,转录其的核苷酸如seq id no.1所示。骨架部分可以有效实现mrna的体外转录,加强mrna的稳定性与蛋白表达效能;抗原编码区可以高效表达新型冠状病毒南非株病毒rbd(k417n,e484k,n501y)蛋白目的抗原。
27.本发明提供的预防新型冠状病毒南非突变株病毒感染的疫苗,小鼠经mrna疫苗制剂肌肉免疫两次后,检测到免疫血清中高效价抗原特异性结合抗体igg和新型冠状病毒南非突变株假病毒中和保护性抗体的产生;检测到免疫小鼠脾细胞在特异性刺激下产生了高效的th1型细胞免疫效应,充分证明预防新型冠状病毒南非突变株病毒感染的疫苗可同时诱导高效的体液和细胞免疫应答,具备良好的免疫保护原性,对新型冠状病毒南非突变病毒的预防有重要意义。
附图说明
28.为了更清楚地说明本发明具体实施方式或现有技术中的技术方案,下面将对具体实施方式或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图是本发明的一些实施方式,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
29.图1为本发明的优化新型冠状病毒南非突变株mrna的结构示意图;
30.图2为本发明的实施例1中的质量分析结果图;
31.图3为本发明的实施例1中的细胞转染蛋白表达检测结果图;
32.图4(1)为本发明的实施例2中的免疫小鼠体内体液免疫效力igg的评价;
33.图4(2)为本发明的实施例2中的免疫小鼠体内体液免疫效力中和抗体的评价;
34.图5(1)为本发明的实施例2中的免疫小鼠体内细胞免疫效应ifn-γ的评价;
35.图5(2)为本发明的实施例2中的免疫小鼠体内细胞免疫效应il-4的评价。
具体实施方式
36.下面将结合实施例对本发明的实施方案进行详细描述,但是本领域技术人员将会理解,下列实施例仅用于说明本发明,而不应视为限制本发明的范围。实施例中未注明具体条件者,按照常规条件或制造商建议的条件进行。
37.除非另有说明,本文中所用的专业与科学术语与本领域熟练人员所熟悉的意义相同。此外,任何与所记载内容相似或均等的方法或材料也可应用于本发明中。
38.本发明提供的优化新型冠状病毒南非突变株mrna,由优化骨架代码和抗原编码区构成,转录其的核苷酸如seq id no.1所示。骨架部分可以有效实现mrna的体外转录,加强mrna的稳定性与蛋白表达效能;抗原编码区可以高效表达新型冠状病毒南非株病毒rbd(k417n,e484k,n501y)蛋白目的抗原。
39.在优选地实施方式中,优化新型冠状病毒南非突变株mrna的5’端连接有cap结构。
40.本发明还提供优化新型冠状病毒南非突变株mrna在制备预防新型冠状病毒南非突变株病毒感染的疫苗中的应用。
41.本发明同时提供与优化新型冠状病毒南非突变株mrna相关的生物材料,包括核酸分子(seq id no.1)、重组载体、工程菌和细胞系。重组载体优选为pcdna3.1( ),具体地,核酸分子位于pcdna3.1( )的nhei和xhoi位点之间。细胞系可以为hek293t、hela、vero或huh 7。可以理解的是,本发明提供的生物材料可以直接作为研发模块应用于新冠南非突变株mrna的相关研究或产品制备中,简化研发工艺和降低成本。
42.本发明还提供一种预防新型冠状病毒南非突变株病毒感染的疫苗,活性成分为本发明的优化新型冠状病毒南非突变株mrna。
43.小鼠经mrna疫苗制剂肌肉免疫两次后,检测到免疫血清中高效价抗原特异性结合抗体igg和新型冠状病毒南非突变株假病毒中和保护性抗体的产生;检测到免疫小鼠脾细胞在特异性刺激下产生了高效的th1型细胞免疫效应,充分证明预防新型冠状病毒南非突变株病毒感染的疫苗可同时诱导高效的体液和细胞免疫应答,具备良好的免疫保护原性,对新型冠状病毒南非突变病毒的预防有重要意义。
44.在优选的实施方式中,疫苗还包括疫苗载体,优选为脂质体、鱼精蛋白、多聚体或脂质多聚体。
45.下面通过具体的实施例进一步说明本发明,但是,应当理解为,这些实施例仅仅是用于更详细地说明之用,而不应理解为用于以任何形式限制本发明。
46.实施例1、新型冠状病毒南非突变株(新冠南非突变株)mrna疫苗的序列设计、制备和体外多种细胞的抗原表达检测
47.一、新冠南非突变株mrna疫苗的序列设计
48.新冠南非突变株mrna疫苗(预防新型冠状病毒南非突变株病毒感染的疫苗)的序列设计采用优化的mrna骨架代码序列,加强mrna的稳定性与蛋白表达效能。新冠南非突变株mrna的cds由优化新冠南非突变株受体结合域rbd的的密码子构成,消除了部分核酸酶的酶切位点,提高了mrna的稳定性和蛋白表达量,,该密码子序列表达的氨基酸序列在新冠原毒株rbd的氨基酸序列出现k417n,e484k和n501y三个突变位点。
49.为实现mrna的体外转录,将新冠南非突变株mrna疫苗序列模板构建在载体pcdna3.1( )的多克隆位点区域nhei和xhoi位点之间得到重组质粒,利用载体序列上的t7启动子序列,在t7转录酶作用下启动体外转录。由此,设计优化得到新冠南非突变株mrna疫苗mrna-1083v2(优化新型冠状病毒南非突变株mrna),如图1所示;新冠南非突变株mrna疫苗mrna-1083v2的序列如序列表中序列1所示:
50.mrna-1083v2序列(seq id no.1):
51.自5’端第1至46为5
’‑
utr,第47至799为cds(编码新冠南非突变s蛋白的信号肽的1-14aa、ntd的306-318aa和rbd的319-541aa,其中存在k417n,e484k和n501y三个突变位
点),第800至925为3
’‑
utr,第926至1045为poly a尾。
52.二、新冠南非突变株mrna疫苗的体外合成
53.1.将设计的新冠南非突变株mrna疫苗序列进行dna模板合成,并通过测序验证。
54.2.将步骤1合成的dna模板进行扩增:将dna模板连接到载体pcdna3.1( )的nhei
‑‑
xhoi位点之间,得到重组质粒。将重组质粒转化感受态细胞dh5α,通过对宿主大肠杆菌的培养,得到大量扩增菌体。借助无内毒素质粒大提试剂盒(天根生物科技(北京)有限公司,dp117)提取扩增菌体中扩增的重组质粒。将扩增的重组质粒进行线性化:利用xbai和sapi对提取的重组质粒进行酶切线性化,经纯化得到可用于mrna体外合成的模板,并采用qubit
tm dsdna br assay kit(invitrogen,q32850)试剂盒进行定量。
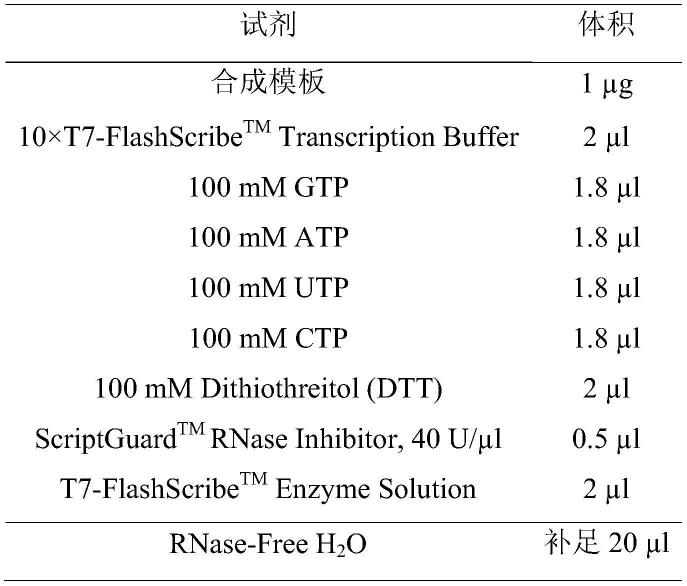
55.3.以步骤2扩增的dna为mrna的体外合成模板,配制表1所示的反应体系,37℃孵育1h进行体外转录,得到大量体外转录rna,并采用qubit
tm dsdna br assay kit(invitrogen,q32850)试剂盒进行定量。
56.表1.体外转录反应采用t7-flashscribe
tm transcription试剂盒(cellscript,c-asf3507)
[0057][0058]
4、将步骤3体外转录rna产物进行纯化:向转录反应体系中加入1μlrnase-free dnase i,37℃孵育15min,以去除体外转录产物体系中的dna模板,得到转录产物。再对得到的转录产物进行纯化,纯化方法如下:
[0059]
(1)向转录产物中加入rnase-free h2o补足体积200μl;
[0060]
(2)加入200μl混合液a(水饱和酚:氯仿:异戊醇,v:v:v,25:24:1),涡旋10s,4℃,13800
×
g离心5min,然后将管中上层水相移至新管中;
[0061]
(3)向新管中加入等体积混合液b(氯仿:异戊醇,v:v,24:1),涡旋10s,4℃,13800
×
g离心5min,然后将管中上层水相移至新管中;
[0062]
(4)向新管中加入等体积5m乙酸铵溶液,涡旋混匀后冰上放置15min后,4℃、13800
×
g离心15min,弃上清。
[0063]
(5)加入70%冰乙醇对rna进行清理后,弃去70%乙醇;加适量rnase-free水(solarbio,r1600)重悬,并采用qubit
tm rna br assay kit(invitrogen,q10211)试剂盒进行定量。
[0064]
5.对步骤4得到的rna转录纯化产物进行mrna加帽反应,具体步骤如下:
[0065]
(1)rna变性:取60μg转录纯化产物,65℃孵育15min进行变性处理,然后移至冰上。
[0066]
(2)mrna加帽反应:加入rna变性产物后,按照表2所示的配制反应体系,37℃孵育0.5h,得到mrna具有cap 1型结构的加帽产物。
[0067]
表2 mrna的cap 1加帽反应体系配制采用scriptcap
tm cap 1capping system试剂盒(cellscript,c-sccs1710)
[0068][0069][0070]
6.mrna加帽产物纯化:同步骤4。
[0071]
7.mrna的质量分析
[0072]
采用安捷伦2100生物分析仪和rna nano 6000assay kit(aglient,5067-1511)对合成mrna进行质量分析,具体步骤如下:
[0073]
(1)mrna变性:将mrna和mrna ladder,70℃变性2min,然后立即冰浴。
[0074]
(2)准备凝胶:按说明将rna gel matrix加入过滤管中,1500
×
g室温离心10min,4℃保存备用。
[0075]
(3)准备凝胶-染料混合物:rna染料避光平衡30min,然后涡旋数秒,瞬时离心后以65:1比例配制凝胶染料混合物,将混合物涡旋混匀,13000
×
g室温离心10min。
[0076]
(4)加载凝胶-染料混合物:使用rna nano芯片之前,调节芯片制备器夹子到最上方的位置。将rna芯片放入芯片槽,在注明黑色g的孔中加入9μl凝胶-染料混合物(不要有气泡);注射器活塞在1ml位置处时关闭注胶器,按压注射器,用夹子固定30s后再松开,5s后将活塞拉回1ml处的位置;打开注胶器,在其它注明白色g的孔中加入9μl凝胶-染料混合物。
[0077]
(5)加载marker:在所有样品孔与ladder孔中各加入6μl rna marker。
[0078]
(6)加载ladder与mrna:在标有梯子图样的孔中加入1μl ladder,将mrna加入到剩
余12个孔中(没有用到的孔可用rnase-free water代替),将芯片放到芯片涡旋振荡器上,2400r/min振荡1min,然后5min内将芯片放到agilent 2100仪中进行检测。
[0079]
结果如图2所示。结果显示,体外合成的新冠南非突变株mrna-1083v2条带与目标条带一致,浓度为2130ng/ul。
[0080]
三、mrna细胞转染蛋白表达检测
[0081]
1.接种细胞:将293t细胞、hela、vero和huh 7细胞(atcc)分别接种于12孔板中,每孔3
×
105个细胞,37℃,5%co2培养箱中至细胞达到80-90%融合度即可进行转染。
[0082]
2.配制转染复合物:采用-mrna transfection kit(mirus,mir2250):100μl opti-mem 1μg mrna 2μl mrna boost reagent 2μltransit-mrna reagent,混匀、室温静置2-5min形成转染复合物。
[0083]
3.转染细胞:将转染复合物滴加到细胞并上下左右晃动使转染复合物均匀分布,37℃,5%co2孵育18h后收取细胞,转染前后无需更换细胞培养液。
[0084]
4.提取细胞总蛋白:细胞用pbs清洗两次后,利用细胞裂解液ripa(金普莱,p06m11) 蛋白酶抑制剂100
×
(金普莱,p01c01),涡旋,以充分裂解细胞。冰浴30min后,4℃,离心13800
×
g,15min,取上清液。
[0085]
5.细胞总蛋白定量:利用bca蛋白定量试剂盒(金普莱,p06m16)对细胞裂解上清液中总蛋白进行定量。将细胞裂解上清液与bca工作液混匀,37℃,孵育45min,a
562nm
下检测吸光度,并计算细胞总蛋白浓度。
[0086]
6.western blotting(wb)检测目标蛋白表达:利用蛋白电泳预制胶bolt
tm 4 to 12%,bis-tris,1.0mm,mini protein gel(invitrogen,nw04120box)电泳(200v,22min)进行总蛋白(30μg)分离。将凝胶上的分离蛋白在梯度电压(20v,1min;23v,4min;25v,2min)作用下转移到iblot 2transfer stacks,pvdf(invitrogen,ib24001)膜上后,在含5%脱脂奶粉的1
×
tbst中室温摇育,20r/min,封闭1h。新冠病毒刺突蛋白受体结合区rbd兔多抗稀释液(1:2000),sars-cov-2(2019-ncov)spike rbd antibody,rabbit pab,antigen affinity purified(义翘神州,40592-t62),20r/min,室温摇育2h。用1
×
tbst清洗膜,60r/min,室温摇育10min,并重复3次,以彻底去除一抗残余。二抗采用辣根过氧化物酶(hrp)标记的山羊抗兔igg二抗稀释液(1:10000),goat anti-rabbit igg secondary antibody(hrp)(义翘神州,ssa004),20r/min,室温摇育1h。用1
×
tbst清洗膜,60r/min,室温摇育10min,并重复3次,以彻底去除二抗残余。利用ecl化学发光超敏显色试剂盒(翊圣生物,36208es60)与膜室温避光孵育3min,在化学发光仪中检测hrp标记的抗体结合抗原。通过曝光显现条带与蛋白marker,pageruler
tm prestained protein ladder(invitrogen,26617)条带比对,验证目标抗原蛋白的表达。利用膜再生液(索莱宝,sw3020)去除膜上抗体,再次对膜进行封闭后,孵育内参抗体,以检测蛋白上样量的一致性。一抗采用β-actin兔单抗稀释液(1:50000),actb rabbit mab(abclonal,ac038),二抗采用辣根过氧化物酶(hrp)标记的山羊抗兔igg二抗稀释液(1:10000),goat anti-rabbit igg secondary antibody(hrp)(义翘神州,ssa004)。
[0087]
结果如图3所示,结果显示:体外合成的新冠南非突变株mrna-1083v2分别转染hek293t、hela、vero和huh 7细胞后,wb均检测到高效表达的新冠南非突变株病毒rbd蛋白目的抗原。
[0088]
实施例2、新冠南非突变株mrna疫苗免疫小鼠后的免疫效力评价
[0089]
一、新冠南非突变株mrna疫苗的递送制剂制备
[0090]
采用上海斯微生物公司的脂质多聚物递送载体lpp制备了新冠南非突变株mrna-1083v2-lpps脂质多聚物疫苗制剂。该递送载体是一种以聚合物包载mrna为内核、磷脂包裹为外壳的双层结构。其双层纳米粒和传统的lnp相比具有更好的包载、保护mrna的效果,并能够随聚合物的降解逐步释放mrna分子。
[0091]
二、新冠南非突变株mrna疫苗的体内体液免疫效力评价
[0092]
将实验动物balb/c小鼠(雌,6-8周,16-18g,北京斯贝福)随机分为mrna-1083v2免疫组(免疫剂量为mrna-1083v2=10μg/只)和阴性对照组(pbs,ph=7.4)(每组6只,正常喂养),以肌肉注射方式免疫小鼠。免疫两次,每次免疫间隔14天。每次免疫后的第10天采用眼眶取血获得足够量的小鼠血清。通过elisa方法检测小鼠免疫血清抗原特异性结合抗体igg的产生,并利用新冠南非突变株假病毒评价免疫血清中和抗体效价,从而对新冠南非突变株mrna疫苗的体内免疫效力进行评价。
[0093]
1.elisa法检测免疫小鼠血清中新冠南非突变株rbd抗原特异性结合抗体情况,具体检测方法如下:
[0094]
(1)包被:南非突变株rbd蛋白(义翘神州,40591-v08h10)用碳酸盐缓冲液(50mm,ph 9.6,0.22μm滤膜过滤)稀释至2ng/μl。96孔板每孔中加入200μg rbd蛋白稀释液,密封、4℃过夜;
[0095]
(2)洗板:包被过夜后,倾倒96孔板去除蛋白包被液,每孔加入200μl洗涤液(含0.2%tween-20的1
×
tbs),手轻轻摇动30s后在纸上拍干,重复6次;
[0096]
(3)封闭:每孔加入200μl封闭液(含2%bsa的1
×
tbs),37℃温箱孵育2h;
[0097]
(4)洗板:倾倒96孔板去除封闭液,每孔加入200μl洗涤液(含0.2%tween-20的1
×
tbs),手轻轻摇动30s后在纸上拍干,重复6次;
[0098]
(5)孵育一抗:将免疫小鼠血清用抗体稀释液(含0.5%bsa的洗涤液)进行10倍梯度稀释得到10-1
至10-6
不同稀释度的血清,每孔加入100μl血清稀释液,37℃温箱孵育2h;
[0099]
(6)洗板:倾倒96孔板去除血清稀释液,每孔加入200μl洗涤液(含0.2%tween-20的1
×
tbs),手轻轻摇动30s后在纸上拍干,重复6次;
[0100]
(7)孵育二抗:将辣根过氧化物酶标记山羊抗小鼠igg(h l)(碧云天,a0216)用抗体稀释液(含0.5%bsa的洗涤液)进行250倍稀释得到二抗稀释液,每孔加入100μl二抗稀释液,37℃温箱孵育1h;
[0101]
(8)洗板:倾倒96孔板去除二抗稀释液,每孔加入200μl洗涤液(含0.2%tween-20的1
×
tbs),手轻轻摇动30s后在纸上拍干,重复6次;
[0102]
(9)显色:每孔加入100μl tmb底物(天根),室温、避光、孵育20min;
[0103]
(10)终止显色:每孔加入50μl 2m h2so4,在酶标仪上检测a
450
的od值;
[0104]
(11)血清结合抗体igg滴度判断:某一稀释血清od/阴性对照od≥2.1,下一稀释倍数od/阴性对照od<2.1,该稀释倍数为该血清样品对应的抗体滴度(如果阴性对照od<0.05则按0.05计算)。
[0105]
2.新冠南非突变株假病毒中和抗体nt
50
效价测定:
[0106]
利用新冠南非突变株假病毒,对新冠南非突变株mrna疫苗mrna-1083v2疫苗小鼠
免疫血清的抗体中和作用进行评价。评价使用的新冠南非突变株假病毒由中国食品药品检定研究院提供,评价方法学参照文献“基于假病毒的新冠病毒临床血清及相应生物制品中和活性抗体定量检测方法”,doi:10.1038/s41596-020-0394-5。具体检测方法如下:
[0107]
用dmem完全培养基对小鼠免疫血清从1/30进行连续3倍稀释,得到6个不同稀释度血清,与650tcid
50
假病毒37℃孵育。同时设有无假病毒的细胞对照组和无血清样品的假病毒对照组。孵育一小时后,各加入2
×
104个huh 7细胞,37℃,5%co2下进行细胞培养。因假病毒进入细胞会表达萤火虫荧光素酶,24小时后,与发光底物反应并进行发光检测。通过与假病毒对照组发光值比较,计算假病毒被抑制的百分比。通过计算公式可以计算出当假病毒50%被抑制时血清的稀释倍数,从而来计算半数抑制稀释度。用半数抑制稀释度来表示半数中和稀释度nt
50
,即血清抗体对假病毒中和活性的情况。
[0108]
结果如图4(1)显示:新冠南非突变株mrna疫苗mrna-1083v2免疫小鼠血清检测到高滴度抗原特异性结合抗体igg的产生,平均结合抗体igg滴度约为1:400000。
[0109]
结果如图4(2)显示:新冠南非突变株mrna疫苗mrna-1083v2免疫小鼠血清检测到高效价的新冠南非突变株假病毒中和抗体,平均nt
50
为约1:7533。
[0110]
综合图4(1)和(2)中结果,新冠南非突变株mrna疫苗mrna-1083v2诱导体液免疫,并产生高效价具有中和保护作用的抗体。
[0111]
三、新冠南非突变株mrna疫苗的体内细胞免疫效力评价
[0112]
利用酶联免疫斑点(elispot)技术对新冠南非突变株mrna疫苗的细胞免疫效力进行评价。初免后的第30天,对免疫小鼠和阴性对照组小鼠进行解剖得脾脏,并分离得脾细胞。小鼠脾细胞(1
×
106个)在新冠南非突变株rbd特异性肽库(5μg/ml/肽)刺激下,37℃,5%co2培养24小时后检测细胞因子ifn-γ和il-4的分泌情况。具体检测方法如下:
[0113]
(1)裂解细胞:倾倒孔内细胞及培养基,加入冰冷的去离子水,4℃放置10分钟实现低渗裂解细胞。
[0114]
(2)洗版:弃除孔内液体,加入1
×
washing buffer,停留一分钟后甩去孔内液体,操作重复6次。
[0115]
(3)检测抗体孵育:加入生物素标记的ifn-γ和il-4抗体,37℃孵育1小时。
[0116]
(4)洗板:重复步骤(2)。
[0117]
(5)酶联亲和素孵育:加入酶标亲和素,37℃孵育1小时。
[0118]
(6)洗板:重复步骤(2)。
[0119]
(7)显色:加入新鲜配制的aec显色液,室温避光静置5-30分钟,根据斑点生成情况选择终止显色时间。
[0120]
(8)终止显色:倾倒孔内液体,揭开板底座。用去离子水对孔正反面及底座洗涤3-5遍,终止显色。阴凉处自然晾干后合上底座。
[0121]
(9)elispot板斑点数计算:用全自动aid的vsr07 elispot读板仪对斑点计数,并记录斑点的各种参数。
[0122]
结果如图5(1)显示:新冠南非突变株mrna疫苗mrna-1083v2免疫小鼠脾细胞特异性刺激下分泌的th1型细胞免疫细胞因子ifn-γ与阴性对照组的相比显著增强。
[0123]
结果如图5(2)显示:新冠南非突变株mrna疫苗mrna-1083v2免疫小鼠脾细胞特异性刺激下分泌的th2型细胞免疫细胞因子il-4与阴性对照组的相比略显增强。
[0124]
综合图5(1)和(2)中结果,新冠南非突变株mrna疫苗mrna-1083v2诱导th1偏向型细胞免疫。
[0125]
尽管已用具体实施例来说明和描述了本发明,然而应意识到,在不背离本发明的精神和范围的情况下可以作出许多其它的更改和修改。因此,这意味着在所附权利要求中包括属于本发明范围内的所有这些变化和修改。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。