一种辅酶q10-硫辛酸型磷脂纳米复合胶束及其制备方法和应用
技术领域
1.本发明属于纳米复合材料技术领域,具体涉及一种辅酶q10-硫辛酸型磷脂纳米复合胶束及其制备方法和应用。
背景技术:
2.辅酶q10又名泛醌,也称为葵烯醌、泛醌醇、维生素q,其英文名为coenzyme q10或ubiquinone,分子式为c
59h90
o4。辅酶q10是人体自体物质,也广泛存在于动物心脏等器官中,可以从动物心脏中提取得到,也可以通过化学合成或生物合成得到。辅酶q10是人体中不可缺少的重要生理物质,其化学结构特点决定了它在人体中具有重要的生理功能,它是生命活动中重要的能量传递物质,是线粒体呼吸链限速反应的关键性物质,在细胞能量生成和增强生物活力方面发挥了重要作用。研究发现,在很多患者人群中,其辅酶q10生理水平下降明显,如在心衰病人(hf)人群中,病人心肌及血液中辅酶q10含量明显降低,从外源补充辅酶q10后能够明显改善病人症状。如在很多免疫力低下的人群中,其辅酶q10生理水平较低,从外源补充辅酶q10后能够明显改善病人症状。因此,人体从外源补充辅酶q10用于治疗各种辅酶q10生理水平低下已经成为一种公认的临床治疗方法。
3.α-硫辛酸为含硫八碳脂酸,其英文名为α-lipoic acid,分子式为c8h
14
o2s2。α-硫辛酸是一种存在于线粒体的酶,类似维他命,能消除加速老化与致病的自由基,其在6、8位上有二硫键相连(c6和c8上的氢原子被二硫键取代),是兼具脂溶性与水溶性的万能抗氧化剂,更是自由基捕手,是机体细胞利用糖类等能源物质产生能量所需的一种限制性必需营养物质,广泛用于治疗和预防心脏病、糖尿病等多种疾病。一般认为它能保存和再生其它抗氧化剂,如维生素c和e等,并能平衡血糖浓度,有效增强体内免疫系统,免受于自由基的破坏。硫辛酸还可以螯合某些金属离子(如铜、锰、锌等)形成稳定的螯合体。在动物模型中证明,它可以保护砷中毒并可以减轻铬中毒后的肝毒性,所以早期也被当做食物中毒和重金属中毒的解毒剂使用。然而,有关硫辛酸的应用依然存在一定的局限性,这主要与其特殊的物化性能有关,表现为在水中溶解度极其微弱,常温下溶解质量分数仅为0.08%,给后续产品的加工制备带来不便,同时硫辛酸在氧气和光照下极易分解,生物利用度低,稳定性差,并且具有一定的刺激性。
4.研究发现,硫辛酸可增加细胞内谷胱甘肽及辅酶q10的水平,将两者同时使用可取得更好的效果。但是目前没有关于两者联用的成熟研究和报道,辅酶q10的使用大多采用软胶囊和脂质体,硫辛酸的使用大多采用静脉注射和点滴的方式,国外有少数研究将硫辛酸用于治疗糖尿病的制剂,但是其载药量小,患者需要一天多次服用,且硫辛酸本身具有特殊气味,患者服药依从性差。cn105561329a公开了一种水溶性辅酶q10与α-硫辛酸复配的环糊精三元超分子包合物及制备方法,虽然该方法获得的包合物具有较大的水溶性和较高的生物利用度,但是该方法仅是使用环糊精对水溶性辅酶q10与α-硫辛酸进行简单包埋,这种包合物的稳定性不够好,辅酶q10及硫辛酸容易被氧化。cn114010522a公开了一种硫辛酸混合
胶束的制备方法,虽然采用该方法可以得到载药量较高的硫辛酸混合胶束,但是在制备过程中去除有机溶剂时需要水浴加热蒸馏,容易破坏硫辛酸使其失活。cn110742818a公开了一种辅酶q10脂质体的制备方法,该制备过程中需要使用三乙醇胺,其会对人体皮肤和黏膜产生强烈的刺激性。
技术实现要素:
5.本发明的目的是为了克服现有技术中辅酶q10-硫辛酸复合物无法同时兼具高稳定性且无有效物质损耗的问题,而提供一种高含量、高稳定性、人体安全性高、生物利用度高且制备过程基本无有效物质损耗的辅酶q10-硫辛酸型磷脂纳米复合胶束及其制备方法和应用。
6.具体地,本发明的第一方面提供了一种辅酶q10-硫辛酸型磷脂纳米复合胶束,其中,所述辅酶q10-硫辛酸型磷脂纳米复合胶束含有以下质量百分比含量的组分:辅酶q10 20%~50%、硫辛酸型磷脂10%~40%和透明质酸钠20%~50%,所述硫辛酸型磷脂为硫辛酸与溶血型磷脂的酯化反应产物。
7.在一种优选的实施方式中,所述硫辛酸型磷脂具有式(1)所示的结构:
[0008][0009]
式(1)中,r1为c
6-c
30
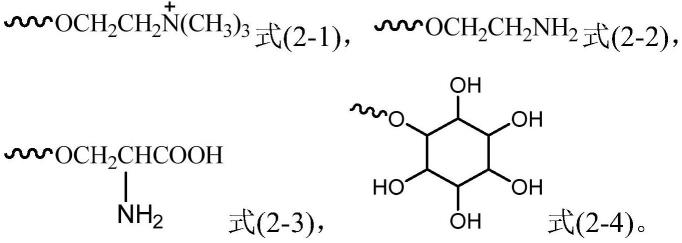
的烷基,r2具有式(2-1)、式(2-2)、式(2-3)、式(2-4)中任意一项所示的结构:
[0010][0011]
本发明的第二方面提供了上述辅酶q10-硫辛酸型磷脂纳米复合胶束的制备方法,该方法包括将辅酶q10以及硫辛酸型磷脂溶解于第一有机溶剂中得到底物溶液,再将所述底物溶液于第一超临界二氧化碳条件下进行反应后去除第一有机溶剂得到反应产物,之后将所得反应产物和含有透明质酸钠的磷酸盐缓冲液进行水化后冷冻干燥,得到辅酶q10-硫辛酸型磷脂纳米复合胶束。
[0012]
在一种优选的实施方式中,本发明提供的辅酶q10-硫辛酸型磷脂纳米复合胶束的制备方法还包括按照以下方法制备硫辛酸型磷脂:将硫辛酸、溶血型磷脂以及催化剂溶解于第二有机溶剂中得到反应液,再将所述反应液于第二超临界二氧化碳条件下进行酯化反
应,得到硫辛酸型磷脂。
[0013]
在一种优选的实施方式中,所述溶血型磷脂具有式(3)所示的结构:
[0014][0015]
式(3)中,r1为c
6-c
30
的烷基,r2具有式(4-1)、式(4-2)、式(4-3)、式(4-4)中任意一项所示的结构:
[0016][0017]
在一种优选的实施方式中,所述溶血型磷脂选自溶血型磷脂酰胆碱、溶血型磷脂酰乙醇胺、溶血型磷脂酰丝氨酸和溶血型磷脂酰肌醇中的至少一种。
[0018]
在一种优选的实施方式中,所述硫辛酸和溶血型磷脂的摩尔比为1:(1~2)。
[0019]
在一种优选的实施方式中,所述催化剂的用量为硫辛酸和溶血型磷脂总质量的3%~5%。
[0020]
在一种优选的实施方式中,所述第二有机溶剂的用量为硫辛酸和溶血型磷脂总质量的5~10倍。
[0021]
在一种优选的实施方式中,所述催化剂为磷脂酶a2。
[0022]
在一种优选的实施方式中,所述第二超临界二氧化碳条件包括反应温度为25~35℃,反应压强为40~65mpa,反应时间为2~12h。
[0023]
在一种优选的实施方式中,以质量百分比计,所述辅酶q10的用量为0.9%~2%,所述硫辛酸型磷脂的用量为0.5%~1.8%,所述第一有机溶剂的用量为1.0%~1.8%,所述含有透明质酸钠的磷酸盐缓冲液的用量为94.4%~97.6%。
[0024]
在一种优选的实施方式中,所述第一超临界二氧化碳条件包括反应温度为25~35℃,反应压强为40~65mpa,反应时间为2~15h。
[0025]
本发明的第三方面提供了由上述方法制备得到的辅酶q10-硫辛酸型磷脂纳米复合胶束。
[0026]
本发明的第四方面提供了所述辅酶q10-硫辛酸型磷脂纳米复合胶束在用于制备化妆品、保健品或药物中的应用。
[0027]
本发明的关键在于将硫辛酸经溶血型磷脂修饰得到硫辛酸型磷脂,该硫辛酸型磷脂与辅酶q10通过超临界流体技术制备得到的辅酶q10-硫辛酸型磷脂纳米复合胶束对光照、氧气以及高温均具有高稳定性。同时,硫辛酸经磷脂化后可以进一步加强辅酶q10-硫辛酸型磷脂纳米复合胶束与生物细胞的结合性能,从而有效提高其生物利用度。本发明通过超临界流体技术制备得到的辅酶q10-硫辛酸型磷脂纳米复合胶束无需经过蒸馏以除去有
机溶剂,避免了制备过程中有效物质(硫辛酸、辅酶q10)的损耗,制备得到的有效物质含量高、稳定性高且对人体安全性高,可以广泛应用于化妆品、保健品或药物中。
具体实施方式
[0028]
本发明的第一方面提供了一种辅酶q10-硫辛酸型磷脂纳米复合胶束,所述辅酶q10-硫辛酸型磷脂纳米复合胶束中含有辅酶q10、硫辛酸型磷脂和透明质酸钠。以质量百分比计,辅酶q10的含量可以为20%~50%,如20%、25%、30%、35%、40%、45%、50%以及它们之间的任意值;硫辛酸型磷脂的含量可以为10%~40%,如10%、15%、20%、25%、30%、35%、40%以及它们之间的任意值;透明质酸钠的含量可以为20%~50%,如20%、25%、30%、35%、40%、45%、50%以及它们之间的任意值。
[0029]
所述硫辛酸型磷脂为硫辛酸与溶血型磷脂的酯化反应产物,所述硫辛酸型磷脂优选具有式(1)所示的结构:
[0030][0031]
式(1)中,r1优选为c
6-c
30
的烷基,如己烷、庚烷、辛烷、壬烷、葵烷、十一烷基、十二烷基、十三烷基、十四烷基、十五烷基、十六烷基、十七烷基、十八烷基、十九烷基、二十烷基、二十一烷基、二十二烷基、二十三烷基、二十四烷基、二十五烷基、二十六烷基、二十七烷基、二十八烷基、二十九烷基、三十烷基等。
[0032]
式(1)中,r2具有式(2-1)、式(2-2)、式(2-3)或式(2-4)所示的结构:
[0033][0034]
本发明的关键在于将硫辛酸经磷脂修饰得到具有式(1)所示结构的硫辛酸型磷脂,该硫辛酸型磷脂与辅酶q10制备得到的辅酶q10-硫辛酸型磷脂纳米复合胶束对光照、氧气以及高温均具有高稳定性,且生物利用度高。
[0035]
本发明的第二方面提供了所述辅酶q10-硫辛酸型磷脂纳米复合胶束的制备方法,该方法包括将辅酶q10以及硫辛酸型磷脂溶解于第一有机溶剂中得到底物溶液,再将所述底物溶液于第一超临界二氧化碳条件下进行反应后去除第一有机溶剂得到反应产物,之后将所得反应产物和含有透明质酸钠的磷酸盐缓冲液进行水化后冷冻干燥,得到辅酶q10-硫辛酸型磷脂纳米复合胶束。
[0036]
本发明对硫辛酸型磷脂的来源没有特别的限定,可以商购得到,也可以按照现有的各种方法制备得到。在一种优选实施方式中,所述硫辛酸型磷脂按照以下方法制备得到:将硫辛酸、溶血型磷脂以及催化剂溶解于第二有机溶剂中得到反应液,再将所述反应液于第二超临界二氧化碳条件下进行酯化反应,得到硫辛酸型磷脂。
[0037]
所述溶血型磷脂为磷脂被磷脂酶a水解而成的化合物,其优选具有式(3)所示的结构:
[0038][0039]
式(3)中,r1优选为c
6-c
30
的烷基,如己烷、庚烷、辛烷、壬烷、葵烷、十一烷基、十二烷基、十三烷基、十四烷基、十五烷基、十六烷基、十七烷基、十八烷基、十九烷基、二十烷基、二十一烷基、二十二烷基、二十三烷基、二十四烷基、二十五烷基、二十六烷基、二十七烷基、二十八烷基、二十九烷基、三十烷基。
[0040]
式(3)中,r2具有式(4-1)、式(4-2)、式(4-3)或式(4-4)所示的结构:
[0041][0042]
在一种具体的实施方式中,所述溶血型磷脂选自溶血型磷脂酰胆碱、溶血型磷脂酰乙醇胺、溶血型磷脂酰丝氨酸和溶血型磷脂酰肌醇中的至少一种。
[0043]
所述溶血型磷脂酰胆碱的具体结构如式(3-1)所示:
[0044]
r1为c
6-c
30
的烷基。
[0045]
所述溶血型磷脂酰乙醇胺的具体结构如式(3-2)所示:
[0046]
r1为c
6-c
30
的烷基。
[0047]
所述溶血型磷脂酰丝氨酸的具体结构如式(3-3)所示:
[0048]
r1为c
6-c
30
的烷基。
[0049]
所述溶血型磷脂酰肌醇的具体结构式如式(3-4)所示:
[0050]
r1为c
6-c
30
的烷基。
[0051]
在上述硫辛酸型磷脂的制备过程中,硫辛酸与溶血型磷脂进行酯化反应的具体反应方程式如下所示:
[0052][0053]
本发明中,为了便于区分和描述,将辅酶q10以及硫辛酸型磷脂溶解于有机溶剂中所使用的有机溶剂称为“第一有机溶剂”,将制备硫辛酸型磷脂中所使用的有机溶剂称为“第二有机溶剂”。所述第一有机溶剂和第二有机溶剂可以相同,也可以不同,其具体实例包括但不限于:正己烷、乙醇、丙醇和正丁醇中的至少一种。同时,为了便于区分和描述,将制备辅酶q10-硫辛酸型磷脂纳米复合胶束中的超临界二氧化碳条件称为“第一超临界二氧化碳条件”,将制备硫辛酸型磷脂中的超临界二氧化碳条件称为“第二超临界二氧化碳条件”。所述第一超临界二氧化碳条件包括反应温度优选为25~35℃,例如25℃、26℃、27℃、28℃、29℃、30℃、31℃、32℃、33℃、34℃、35℃以及它们之间的任意值;反应压强优选为40~65mpa,例如40mpa、41mpa、42mpa、43mpa、44mpa、45mpa、46mpa、47mpa、48mpa、49mpa、50mpa、51mpa、52mpa、53mpa、54mpa、55mpa、56mpa、57mpa、58mpa、59mpa、60mpa、61mpa、62mpa、63mpa、64mpa、65mpa以及它们之间的任意值;反应时间优选为2~15h,例如2h、3h、4h、5h、6h、7h、8h、9h、10h、11h、12h、13h、14h、15h以及它们之间的任意值。所述第二超临界二氧化碳条件包括反应温度优选为25~35℃,例如25℃、26℃、27℃、28℃、29℃、30℃、31℃、32℃、33℃、34℃、35℃以及它们之间的任意值;反应压强优选为40~65mpa,例如40mpa、41mpa、42mpa、43mpa、44mpa、45mpa、46mpa、47mpa、48mpa、49mpa、50mpa、51mpa、52mpa、53mpa、54mpa、55mpa、56mpa、57mpa、58mpa、59mpa、60mpa、61mpa、62mpa、63mpa、64mpa、65mpa以及它们之间的任意值;反应时间优选为2~12h,例如2h、3h、4h、5h、6h、7h、8h、9h、10h、11h、12h以及它们之间的任意值。在本发明中,所述压强均指表压,即压力表的示数。
[0054]
本发明对制备硫辛酸型磷脂过程中所使用的硫辛酸、溶血型磷脂、催化剂以及第
二有机溶剂的用量没有特别的限定,优选地,所述硫辛酸和溶血型磷脂的摩尔比为1:(1~2),例如1:1、1:1.1、1:1.2、1:1.3、1:1.4、1:1.5、1:1.6、1:1.7、1:1.8、1:1.9、1:2以及它们之间的任意值。优选地,所述催化剂的用量为硫辛酸和溶血型磷脂总质量的3%~5%,例如3%、3.5%、4%、4.5%、5%以及它们之间的任意值。优选地,所述第二有机溶剂的用量为硫辛酸和溶血型磷脂总质量的5~10倍,例如5倍、6倍、7倍、8倍、9倍、10倍以及它们之间的任意值。当将硫辛酸、溶血型磷脂、催化剂以及第二有机溶剂的用量控制在上述优选范围内时,硫辛酸能够完全反应转化为硫辛酸型磷脂,得到的硫辛酸型磷脂产物具有高纯度。
[0055]
本发明对催化剂的种类没有特别的限定,可以为现有的各种能够使得硫辛酸与溶血型磷脂实现酯化反应的物质,考虑到原料的易得性,所述催化剂优选为磷脂酶a2。
[0056]
在上述硫辛酸型磷脂的制备过程中,由于硫辛酸与溶血型磷脂进行酯化反应所得硫辛酸型磷脂的分子量较大,当体系反应压强下降后其溶解度也随之下降,从而在反应釜底部析出,而其它未反应物质仍溶解于二氧化碳中,当反应结束时,从反应釜底部放出的物料即为硫辛酸型磷脂。
[0057]
本发明对制备辅酶q10-硫辛酸型磷脂纳米复合胶束中所使用的辅酶q10、硫辛酸型磷脂、第一有机溶剂以及含有透明质酸钠的磷酸盐缓冲液的用量没有特别的限定,以质量百分比计,优选地,所述辅酶q10的用量为0.9%~2%,例如0.9%、1%、1.1%、1.2%、1.3%、1.4%、1.5%、1.6%、1.7%、1.8%、1.9%、2.0%以及它们之间的任意值。优选地,所述硫辛酸型磷脂的用量为0.5%~1.8%,例如0.5%、0.6%、0.7%、0.8%、0.9%、1%、1.1%、1.2%、1.3%、1.4%、1.5%、1.6%、1.7%、1.8%以及它们之间的任意值。优选地,所述第一有机溶剂的用量为1.0%~1.8%,例如1.0%、1.1%、1.2%、1.3%、1.4%、1.5%、1.6%、1.7%、1.8%以及它们之间的任意值。优选地,所述含有透明质酸钠的磷酸盐缓冲液的用量为94.4%~97.6%,例如94.4%、94.5%、95%、95.5%、96%、96.5%、97%、97.5%、97.6%以及它们之间的任意值。
[0058]
本发明的第三方面提供了由上述方法制备得到的辅酶q10-硫辛酸型磷脂纳米复合胶束。本发明通过超临界流体技术制备得到的辅酶q10-硫辛酸型磷脂纳米复合胶束无需经过蒸馏以除去有机溶剂,避免了制备过程中有效物质(硫辛酸、辅酶q10)的损耗,制备得到的有效物质含量高、稳定性高且对人体安全性高。
[0059]
本发明的第四方面提供了所述辅酶q10-硫辛酸型磷脂纳米复合胶束在用于制备化妆品、保健品或药物中的应用。
[0060]
下面详细描述本发明的实施例,所述实施例的示例旨在用于解释本发明,而不能理解为对本发明的限制。实施例中未注明具体技术或条件者,按照本领域内的文献所描述的技术或条件或按照产品说明书进行。所用试剂或仪器未注明生产厂商者,均为可以通过市购获得的常规产品。
[0061]
以下各实施例和对比例中,溶血型磷脂酰胆碱购自上海阿拉丁生化科技股份有限公司,cas号为97281-36-2;溶血型磷脂酰乙醇胺购自上海阿拉丁生化科技股份有限公司,cas号为89576-29-4;溶血型磷脂酰肌醇购自上海甄准生物科技有限公司,cas号为796963-91-2;溶血型磷脂酰丝氨酸购自上海阿拉丁生化科技股份有限公司,cas号为383907-66-2。以下各实施例和对比例中,辅酶q10、硫辛酸型磷脂以及透明质酸钠的含量按照投料比计算得到。
[0062]
实施例1
[0063]
称取20g(0.097mol)硫辛酸和50g溶血型磷脂酰胆碱,加入350g正己烷溶解后再加入2.1g磷脂酶a2(默克公司,11306u/ml,分子量为14000,下同),混合搅拌均匀得到反应液;将所得反应液通入超临界二氧化碳反应釜中,通入二氧化碳,控制反应温度为25℃,逐渐加压至40mpa,反应4h后逐渐将反应釜泄压至15mpa,从反应器底部放出物料,即为硫辛酸型磷脂。
[0064]
称取1g辅酶q10和0.6g硫辛酸型磷脂溶解于1.2g正己烷中制得底物溶液,将底物溶液通入超临界二氧化碳反应釜中,通入二氧化碳,控制温度为25℃,逐渐加压至40mpa,反应2h后泄压除去正己烷溶剂,向反应釜中加入98.4g磷酸盐缓冲液(透明质酸钠含量为1%)进行水化1h,得到辅酶q10-硫辛酸型磷脂纳米复合胶束悬浮液,将该悬浮液进行冷冻干燥制备得到辅酶q10-硫辛酸型磷脂纳米复合胶束粉末,其中,辅酶q10的质量百分含量为38.7%、硫辛酸型磷脂的质量百分含量为23.2%、透明质酸钠的质量百分含量为38.1%。
[0065]
实施例2
[0066]
称取硫辛酸20g(0.097mol)和50g溶血型磷脂酰胆碱,加入400g正己烷溶解后再加入2.1g磷脂酶a2,混合搅拌均匀得到反应液;将所得反应液通入超临界二氧化碳反应釜中,通入二氧化碳,控制反应温度为25℃,逐渐加压至40mpa,反应4h后逐渐将反应釜泄压至15mpa,从反应器底部放出物料,即为硫辛酸型磷脂。
[0067]
称取1g辅酶q10和0.6g硫辛酸型磷脂溶解于1.2g正己烷中制得底物溶液,将底物溶液通入超临界二氧化碳反应釜中,通入二氧化碳,控制温度为25℃,逐渐加压至40mpa,反应2h后泄压除去正己烷溶剂,向反应釜中加入98.4g磷酸盐缓冲液(透明质酸钠含量为1%)进行水化1h,得到辅酶q10-硫辛酸型磷脂纳米复合胶束悬浮液,将该悬浮液进行冷冻干燥制备得到辅酶q10-硫辛酸型磷脂纳米复合胶束粉末,其中,辅酶q10的质量百分含量为38.7%、硫辛酸型磷脂的质量百分含量为23.2%、透明质酸钠的质量百分含量为38.1%。
[0068]
实施例3
[0069]
称取20g(0.097mol)硫辛酸和50g溶血型磷脂酰胆碱,加入400g正己烷溶解后再加入2.5g磷脂酶a2,混合搅拌均匀得到反应液;将所得反应液通入超临界二氧化碳反应釜中,通入二氧化碳,控制反应温度为25℃,逐渐加压至40mpa,反应4h后逐渐将反应釜泄压至15mpa,从反应器底部放出物料,即为硫辛酸型磷脂。
[0070]
称取1g辅酶q10和0.6g硫辛酸型磷脂溶解于1.2g正己烷中制得底物溶液,将底物溶液通入超临界二氧化碳反应釜中,通入二氧化碳,控制温度为25℃,逐渐加压至40mpa,反应2h后泄压除去正己烷溶剂,向反应釜中加入98.4g磷酸盐缓冲液(透明质酸钠含量为1%)进行水化1h,得到辅酶q10-硫辛酸型磷脂纳米复合胶束悬浮液,将该悬浮液进行冷冻干燥制备得到所述辅酶q10-硫辛酸型磷脂纳米复合胶束粉末,其中,辅酶q10的质量百分含量为38.7%、硫辛酸型磷脂的质量百分含量为23.2%、透明质酸钠的质量百分含量为38.1%。
[0071]
实施例4
[0072]
称取20g(0.097mol)硫辛酸和50g溶血型磷脂酰胆碱,加入450g正己烷溶解后再加入2.8g磷脂酶a2,混合搅拌均匀得到反应液;将所得反应液通入超临界二氧化碳反应釜中,通入二氧化碳,控制反应温度为25℃,逐渐加压至40mpa,反应4h后逐渐将反应釜泄压至15mpa,从反应器底部放出物料,即为硫辛酸型磷脂。
[0073]
称取1.2g辅酶q10和0.6g硫辛酸型磷脂溶解于1.2g正己烷中制得底物溶液,将底物溶液通入超临界二氧化碳反应釜中,通入二氧化碳,控制温度为25℃,逐渐加压至40mpa,反应2h后泄压除去正己烷溶剂,向反应釜中加入98.2g磷酸盐缓冲液(透明质酸钠含量为1%)进行水化1h,得到辅酶q10-硫辛酸型磷脂纳米复合胶束悬浮液,将该悬浮液进行冷冻干燥制备得到辅酶q10-硫辛酸型磷脂纳米复合胶束粉末,其中,辅酶q10的质量百分含量为43.1%、硫辛酸型磷脂的质量百分含量为21.6%、透明质酸钠的质量百分含量为35.3%。
[0074]
实施例5
[0075]
称取20g(0.097mol)硫辛酸和50g溶血型磷脂酰乙醇胺,加入450g正己烷溶解后再加入3g磷脂酶a2,混合搅拌均匀得到反应液;将所得反应液通入超临界二氧化碳反应釜中,通入二氧化碳,控制反应温度为25℃,逐渐加压至40mpa,反应5h后逐渐将反应釜泄压至15mpa,从反应器底部放出物料,即为硫辛酸型磷脂。
[0076]
称取1g辅酶q10和0.6g硫辛酸型磷脂溶解于1.2g正己烷中制得底物溶液,将底物溶液通入超临界二氧化碳反应釜中,通入二氧化碳,控制温度为25℃,逐渐加压至40mpa,反应2h后泄压除去正己烷溶剂,向反应釜中加入98.4g磷酸盐缓冲液(透明质酸钠含量为1%)进行水化1h,得到辅酶q10-硫辛酸型磷脂纳米复合胶束悬浮液,将该悬浮液进行冷冻干燥制备得到辅酶q10-硫辛酸型磷脂纳米复合胶束粉末,其中,辅酶q10的质量百分含量为38.7%、硫辛酸型磷脂的质量百分含量为23.2%、透明质酸钠的质量百分含量为38.1%。
[0077]
实施例6
[0078]
称取20g(0.097mol)硫辛酸和50g溶血型磷脂酰乙醇胺,加入450g正己烷溶解后再加入3.5g磷脂酶a2,混合搅拌均匀得到反应液;将所得反应液通入超临界二氧化碳反应釜中,通入二氧化碳,控制反应温度为30℃,逐渐加压至40mpa,反应5h后逐渐将反应釜泄压至15mpa,从反应器底部放出物料,即为硫辛酸型磷脂。
[0079]
称取1.2g辅酶q10和0.6g硫辛酸型磷脂溶解于1.2g正己烷中制成底物溶液,将底物溶液通入超临界二氧化碳反应釜中,通入二氧化碳,控制温度为30℃,逐渐加压至40mpa,反应2h后泄压除去正己烷溶剂,向反应釜中加入98.2g磷酸盐缓冲液(透明质酸钠含量为1%)进行水化1h,得到辅酶q10-硫辛酸型磷脂纳米复合胶束悬浮液,将该悬浮液进行冷冻干燥制备得到辅酶q10-硫辛酸型磷脂纳米复合胶束粉末,其中,辅酶q10的质量百分含量为43.1%、硫辛酸型磷脂的质量百分含量为21.6%、透明质酸钠的质量百分含量为35.3%。
[0080]
实施例7
[0081]
称取20g(0.097mol)硫辛酸和50g溶血型磷脂酰肌醇,加入600g正己烷溶解后再加入3.5g磷脂酶a2,混合搅拌均匀得到反应液;将所得反应液通入超临界二氧化碳反应釜中,通入二氧化碳,控制反应温度为30℃,逐渐加压至40mpa,反应4h后逐渐将反应釜泄压至15mpa,从反应器底部放出物料,即为硫辛酸型磷脂。
[0082]
称取1.5g辅酶q10和1g硫辛酸型磷脂溶解于1.5g正己烷中制得底物溶液,将底物溶液通入超临界二氧化碳反应釜中,通入二氧化碳,控制温度为25℃,逐渐加压至40mpa,反应2h后泄压除去正己烷溶剂,向反应釜中加入97.5g磷酸盐缓冲液(透明质酸钠含量为1%)进行水化1h,得到辅酶q10-硫辛酸型磷脂纳米复合胶束悬浮液,将该悬浮液进行冷冻干燥制备得到辅酶q10-硫辛酸型磷脂纳米复合胶束粉末,其中,辅酶q10的质量百分含量为43.2%、硫辛酸型磷脂的质量百分含量为28.8%、透明质酸钠的质量百分含量为28.0%。
[0083]
实施例8
[0084]
称取20g(0.097mol)硫辛酸和50g溶血型磷脂酰肌醇,加入700g正己烷溶解后再加入3.5g磷脂酶a2,混合搅拌均匀得到反应液;将所得反应液通入超临界二氧化碳反应釜中,通入二氧化碳,控制反应温度为30℃,逐渐加压至55mpa,反应4h后逐渐将反应釜泄压至15mpa,从反应器底部放出物料,即为硫辛酸型磷脂。
[0085]
称取2g辅酶q10和1.8g硫辛酸型磷脂溶解于1.8g正己烷中制得底物溶液,将底物溶液通入超临界二氧化碳反应釜中,通入二氧化碳,控制温度为35℃,逐渐加压至65mpa,反应3h后泄压除去正己烷溶剂,向反应釜中加入96.8g磷酸盐缓冲液(透明质酸钠含量为1%)进行水化1h,得到辅酶q10-硫辛酸型磷脂纳米复合胶束悬浮液,将该悬浮液进行冷冻干燥制备得到辅酶q10-硫辛酸型磷脂纳米复合胶束粉末,其中,辅酶q10的质量百分含量为41.9%、硫辛酸型磷脂的质量百分含量为37.8%、透明质酸钠的质量百分含量为20.3%。
[0086]
实施例9
[0087]
称取20g(0.097mol)硫辛酸和50g溶血型磷脂酰肌醇,加入700g正己烷溶解后再加入3.5g磷脂酶a2,混合搅拌均匀得到反应液;将所得反应液通入超临界二氧化碳反应釜中,通入二氧化碳,控制反应温度为30℃,逐渐加压至55mpa,反应6h后逐渐将反应釜泄压至15mpa,从反应器底部放出物料,即为硫辛酸型磷脂。
[0088]
称取2g辅酶q10和1.8g硫辛酸型磷脂溶解于1.8g正己烷中制得底物溶液,将底物溶液通入超临界二氧化碳反应釜中,通入二氧化碳,控制温度为35℃,逐渐加压至65mpa,反应3h后泄压除去正己烷溶剂,向反应釜中加入96.8g磷酸盐缓冲液(透明质酸钠含量为1%)进行水化1h,得到辅酶q10-硫辛酸型磷脂纳米复合胶束悬浮液,将该悬浮液进行冷冻干燥制备得到辅酶q10-硫辛酸型磷脂纳米复合胶束粉末,其中,辅酶q10的质量百分含量为41.9%、硫辛酸型磷脂的质量百分含量为37.8%、透明质酸钠的质量百分含量为20.3%。
[0089]
实施例10
[0090]
称取20g(0.097mol)硫辛酸和50g溶血型磷脂酰肌醇,加入700g正己烷溶解后再加入3.5g磷脂酶a2,混合搅拌均匀得到反应液;将所得反应液通入超临界二氧化碳反应釜中,通入二氧化碳,控制反应温度为30℃,逐渐加压至55mpa,反应10h后逐渐将反应釜泄压至15mpa,从反应器底部放出物料,即为硫辛酸型磷脂。
[0091]
称取2g辅酶q10和1.8g硫辛酸型磷脂溶解于1.8g正己烷中制得底物溶液,将底物溶液通入超临界二氧化碳反应釜中,通入二氧化碳,控制温度为35℃,逐渐加压至65mpa,反应3h后泄压除去正己烷溶剂,向反应釜中加入96.8g磷酸盐缓冲液(透明质酸钠含量为1%)进行水化1h,得到辅酶q10-硫辛酸型磷脂纳米复合胶束悬浮液,将该悬浮液进行冷冻干燥制备得到辅酶q10-硫辛酸型磷脂纳米复合胶束粉末,其中,辅酶q10的质量百分含量为41.9%、硫辛酸型磷脂的质量百分含量为37.8%、透明质酸钠的质量百分含量为20.3%。
[0092]
实施例11
[0093]
称取20g(0.097mol)硫辛酸和50g溶血型磷脂酰丝氨酸,加入700g正己烷溶解后再加入3.5g磷脂酶a2,混合搅拌均匀得到反应液;将所得反应液通入超临界二氧化碳反应釜中,通入二氧化碳,控制反应温度为30℃,逐渐加压至55mpa,反应11h后逐渐将反应釜泄压至15mpa,从反应器底部放出物料,即为硫辛酸型磷脂。
[0094]
称取2g辅酶q10和1.8g硫辛酸型磷脂溶解于1.8g正己烷中制得底物溶液,将底物
溶液通入超临界二氧化碳反应釜中,通入二氧化碳,控制温度为35℃,逐渐加压至65mpa,反应3h后泄压除去正己烷溶剂,向反应釜中加入96.8g磷酸盐缓冲液(透明质酸钠含量为1%)进行水化1h,得到辅酶q10-硫辛酸型磷脂纳米复合胶束悬浮液,将该悬浮液进行冷冻干燥制备得到辅酶q10-硫辛酸型磷脂纳米复合胶束粉末,其中,辅酶q10的质量百分含量为41.9%、硫辛酸型磷脂的质量百分含量为37.8%、透明质酸钠的质量百分含量为20.3%。
[0095]
实施例12
[0096]
称取20g(0.097mol)硫辛酸和50g溶血型磷脂酰丝氨酸,加入700g正己烷溶解后再加入3.5g磷脂酶a2,混合搅拌均匀得到反应液;将所得反应液通入超临界二氧化碳反应釜中,通入二氧化碳,控制反应温度为30℃,逐渐加压至55mpa,反应12h后逐渐将反应釜泄压至15mpa,从反应器底部放出物料,即为硫辛酸型磷脂。
[0097]
称取2g辅酶q10和1.8g硫辛酸型磷脂溶解于1.8g正己烷中制成底物溶液,将底物溶液通入超临界二氧化碳反应釜中,通入二氧化碳,控制温度为35℃,逐渐加压至65mpa,反应3h后泄压除去正己烷溶剂,向反应釜中加入96.8g磷酸盐缓冲液(透明质酸钠含量为1%)进行水化1h,得到辅酶q10-硫辛酸型磷脂纳米复合胶束悬浮液,将该悬浮液进行冷冻干燥制备得到辅酶q10-硫辛酸型磷脂纳米复合胶束粉末,其中,辅酶q10的质量百分含量为41.9%、硫辛酸型磷脂的质量百分含量为37.8%、透明质酸钠的质量百分含量为20.3%。
[0098]
实施例13
[0099]
称取20g(0.097mol)硫辛酸和50g溶血型磷脂酰丝氨酸,加入700g正己烷溶解后再加入3.5g磷脂酶a2,混合搅拌均匀得到反应液;将所得反应液通入超临界二氧化碳反应釜中,通入二氧化碳,控制反应温度为30℃,逐渐加压至55mpa,反应12h后逐渐将反应釜泄压至15mpa,从反应器底部放出物料,即为硫辛酸型磷脂。
[0100]
称取2g辅酶q10和1.8g硫辛酸型磷脂溶解于1.8g正己烷中制得底物溶液,将底物溶液通入超临界二氧化碳反应釜中,通入二氧化碳,控制温度为35℃,逐渐加压至65mpa,反应4h后泄压除去正己烷溶剂,向反应釜中加入96.8g磷酸盐缓冲液(透明质酸钠含量为1%)进行水化1h,得到辅酶q10-硫辛酸型磷脂纳米复合胶束悬浮液,将该悬浮液进行冷冻干燥制备得到辅酶q10-硫辛酸型磷脂纳米复合胶束粉末,其中,辅酶q10的质量百分含量为41.9%、硫辛酸型磷脂的质量百分含量为37.8%、透明质酸钠的质量百分含量为20.3%。
[0101]
实施例14
[0102]
称取20g(0.097mol)硫辛酸和50g溶血型磷脂酰乙醇胺,加入700g正己烷溶解后再加入3.5g磷脂酶a2,混合搅拌均匀得到反应液;将所得反应液通入超临界二氧化碳反应釜中,通入二氧化碳,控制反应温度为30℃,逐渐加压至55mpa,反应12h后逐渐将反应釜泄压至15mpa,从反应器底部放出物料,即为硫辛酸型磷脂。
[0103]
称取2g辅酶q10和1.8g硫辛酸型磷脂溶解于1.8g正己烷中制得底物溶液,将底物溶液通入超临界二氧化碳反应釜中,通入二氧化碳,控制温度为35℃,逐渐加压至65mpa,反应5h后泄压除去正己烷溶剂,向反应釜中加入96.8g磷酸盐缓冲液(透明质酸钠含量为1%)进行水化1h,得到辅酶q10-硫辛酸型磷脂纳米复合胶束悬浮液,将该悬浮液进行冷冻干燥制备得到辅酶q10-硫辛酸型磷脂纳米复合胶束粉末,其中,辅酶q10的质量百分含量为41.9%、硫辛酸型磷脂的质量百分含量为37.8%、透明质酸钠的质量百分含量为20.3%。
[0104]
对比例1
[0105]
按照实施例1的方法制备辅酶q10-硫辛酸纳米复合胶束粉末,与实施例1不同的是,未对硫辛酸进行酯化,其余步骤与实施例1相同。具体地,称取1g辅酶q10和0.6g硫辛酸溶解于1.2g正己烷中制得底物溶液,将底物溶液通入超临界二氧化碳反应釜中,通入二氧化碳,控制温度为25℃,逐渐加压至40mpa,反应2h后泄压除去正己烷溶剂,向反应釜中加入98.4g磷酸盐缓冲液(透明质酸钠含量为1%)进行水化1h,得到辅酶q10-硫辛酸纳米复合胶束悬浮液,将该悬浮液进行冷冻干燥制备得到辅酶q10-硫辛酸纳米复合胶束粉末,其中,辅酶q10的质量百分含量为38.7%、硫辛酸的质量百分含量为23.2%、透明质酸钠的质量百分含量为38.1%。
[0106]
对比例2
[0107]
称取1g辅酶q10和0.6g硫辛酸进行原料混合,得到辅酶q10-硫辛酸物理混合物。
[0108]
测试例
[0109]
1.粒度测试
[0110]
激光纳米粒度仪是通过大小不同的颗粒在各角度上散射光强的变化来反映出颗粒群的粒度大小和粒度分布规律。本发明采用马尔文激光粒度仪对实施例及对比例的胶束粒径大小进行测试,具体测试步骤为:分别称取实施例1~14制备得到的辅酶q10-硫辛酸型磷脂纳米复合胶束粉末、对比例1制备得到的辅酶q10-硫辛酸纳米复合胶束粉末以及对比例2制备得到的辅酶q10-硫辛酸物理混合物,分别加入生理盐水制得质量分数为3%的悬浮液,之后采用马尔文激光粒度仪测试其粒径大小。各样品的粒径大小如表1所示。
[0111]
表1各样品粒径大小
[0112]
粒径大小(μm)d10d50d90实施例10.0150.0810.201实施例20.0160.0900.214实施例30.0180.1020.225实施例40.0170.1030.221实施例50.0190.1050.227实施例60.0200.1110.236实施例70.0200.1120.230实施例80.0210.1170.240实施例90.0190.1140.225实施例100.0180.1120.220实施例110.0170.0980.195实施例120.0160.0950.196实施例130.0200.1010.203实施例140.0190.1030.205对比例10.2130.5370.902对比例2102209337
[0113]
从表1粒度测试结果可知,本发明中制备得到的辅酶q10-硫辛酸型磷脂纳米复合胶束悬浮液的粒度达到了纳米级别,并且各实施例之间的粒度分布也十分接近,说明采用本发明所提供的制备方法可以制得稳定的辅酶q10-硫辛酸型磷脂纳米复合胶束。然而,由
对比例1制备得到的辅酶q10-硫辛酸纳米复合胶束和由对比例2制备得到的辅酶q10-硫辛酸物理混合物不仅粒度大,而且粒度分布范围也大。
[0114]
2.药代动力学实验
[0115]
2.1样品制备
[0116]
测试例1:取实施例1制得的辅酶q10-硫辛酸型磷脂纳米复合胶束粉末并加入生理盐水进行搅拌,制备得到质量分数为3%的辅酶q10-硫辛酸型磷脂纳米复合胶束生理盐水悬浮液。
[0117]
测试例2:取实施例2制得的辅酶q10-硫辛酸型磷脂纳米复合胶束粉末并加入生理盐水进行搅拌,制备得到质量分数为3%的辅酶q10-硫辛酸型磷脂纳米复合胶束生理盐水悬浮液。
[0118]
测试例3:取实施例3制得的辅酶q10-硫辛酸型磷脂纳米复合胶束粉末并加入生理盐水进行搅拌,制备得到质量分数为3%的辅酶q10-硫辛酸型磷脂纳米复合胶束生理盐水悬浮液。
[0119]
对比测试例1:取对比例1制得的辅酶q10-硫辛酸纳米复合胶束粉末并加入生理盐水进行搅拌,制备得到质量分数为3%的辅酶q10-硫辛酸纳米复合胶束生理盐水悬浮液。
[0120]
对比测试例2:取对比例2制得的辅酶q10-硫辛酸物理混合物并加入生理盐水进行搅拌,制备得到质量分数为3%的辅酶q10-硫辛酸物理混合物生理盐水悬浮液。
[0121]
2.2实验条件
[0122]
为屏蔽环境,实验期间保持环境温度为23℃~24℃以及湿度为50%~56%,每日自由摄取去离子水和标准饲料。
[0123]
2.3实验动物与分组
[0124]
由长沙市开福区东创实验动物科技服务部(实验动物使用许可证号为syxk(湘)2010-0010)提供的spf级昆明种雄性小鼠,鼠龄3个月,体重18~22g。按照国际实验动物实验准则对动物进行操作,以减少实验动物在实验过程中的痛苦。采用完全随机设计将小鼠随机每10只分为一组,共5组,留待给药实验使用。
[0125]
2.4口服给药及药代动力学实验
[0126]
取上述禁食12h的小鼠随机10只分为一组,共5组。分别将上述制得的测试例1~3以及对比测试例1~2按50mg/kg给药剂量给予小鼠灌胃处理,给药5min、15min、30min、1h、2h、4h、6h、12h后分别从小鼠眼眶静脉取血0.5ml,置于肝素抗凝管中,于4℃、5000rpm条件下离心10min,将上层血浆分离处理后进行hplc测样。经hplc分析测定,根据血药浓度结果进行拟合分析,计算血药浓度数据。所得结果如表2和表3所示。
[0127]
表2小鼠经口服给药后各样品平均血药浓度随时间变化量(mean
±
sd,n=10)
[0128]
[0129][0130]
从表2实验结果可知,口服给药后,辅酶q10-硫辛酸型磷脂纳米复合胶束(测试例1~3)的峰值血药浓度明显高于对比测试例1~2,说明由本发明制备得到的辅酶q10-硫辛酸型磷脂纳米复合胶束有利于小鼠吸收并可以达到较高的血药浓度。
[0131]
表3小鼠经口服给药后各样品的药动力学参数
[0132]
参数测试例1测试例2测试例3对比测试例1对比测试例2auc(mg
·
l
·
h)86.3285.7985.9055.3240.12k(h)0.4210.4120.3980.5110.505t
max
(min)6060606060c
max
(mg/l)32.5933.1432.8325.3622.27
[0133]
从表3实验结果可知,测试例1、测试例2、测试例3的生物利用度(auc)分别是对比测试例1的1.56倍、1.55倍、1.55倍,测试例1、测试例2、测试例3的生物利用度分别是对比测试例2的2.15倍、2.14倍、2.14倍,说明由本发明制备得到的辅酶q10-硫辛酸型磷脂纳米复合胶束能够大大改善药物在小鼠体内的吸收过程,有效提高了药物的生物利用度。
[0134]
3.稳定性能测试
[0135]
分别取实施例1制得的中间产品辅酶q10-硫辛酸型磷脂纳米复合胶束悬浮液、实施例1胶束悬浮液冷冻干燥后的最终产品辅酶q10-硫辛酸型磷脂纳米复合胶束粉末、对比例1的辅酶q10-硫辛酸纳米复合胶束粉末以及对比例2辅酶q10-硫辛酸物理混合物(将上述化合物分别制备成质量分数为3%的生理盐水悬浮液)分别在5000lx光照强度照射、充氧灌装(25℃)以及恒温(50℃)下放置20天,分别于第0天、第5天、第10天、第15天和第20天取样,进行hplc测定辅酶q10、硫辛酸型磷脂或硫辛酸原料的标示量变化情况,以此考察光照、氧气、高温对于药物稳定性的影响,实验结果如表4~6所示。
[0136]
表4 5000lx光照下标示量变化表
[0137]
[0138]
表5充氧灌装(25℃)下标示量变化
[0139][0140]
表6恒温(50℃)下标示量变化
[0141][0142][0143]
从表4~6实验结果可知,由本发明制备得到的辅酶q10-硫辛酸型磷脂纳米复合胶束悬浮液或胶束粉末均可以大幅度提高辅酶q10和硫辛酸型磷脂对于光照、氧气、高温的稳定性,尤其对于硫辛酸,其在接枝溶血型磷脂后的稳定性显著提高。
[0144]
尽管上面已经示出和描述了本发明的实施例,可以理解的是,上述实施例是示例性的,不能理解为对本发明的限制,本领域的普通技术人员在不脱离本发明的原理和宗旨的情况下在本发明的范围内可以对上述实施例进行变化、修改、替换和变型。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。
