1.本发明属于图像处理技术领域,尤其涉及一种医学图像分割模型的构建方法、系统、设备和存储介质。
背景技术:
2.近年来,深度学习被广泛应用于自然图像的分类、分割、跟踪和识别等相关任务。得益于卷积神经网络良好的迁移学习能力,在医学图像领域之中的深度学习研究也越来越多。在医学图像领域中,需要将图像中不同器官或病灶区域划分出来。该任务通过自动或半自动对医学图像中的像素进行分类,进而将图像分割成不同的有意义的区域。
3.图像的分割精度会直接影响到医师对病灶部分的判断,因此本技术提供了一种分割精度高的医学图像分割模型的构建方法、系统、设备和存储介质。
技术实现要素:
4.本发明实施例的目的在于提供一种医学图像分割模型的构建方法、系统、设备和存储介质,旨在解决背景技术中确定的现有技术存在的技术问题。
5.本发明实施例是这样实现的,医学图像分割模型的构建方法,所述方法包括以下步骤:
6.获取用于进行模型训练的图像数据集;
7.根据所述图像数据集进行医学图像分割模型的训练;所述医学图像分割模型为混入有改进eca模块的图像语义分割网络,所述改进eca模块由eca模块和cbam注意力模块耦合而成,其中所述医学图像分割模型中,图像数据集经过改进eca模块处理后作为下一层下采样的输入,未经过改进eca模块处理的特征图做跳跃连接;
8.对所述医学图像分割模型进行观测以进行网格寻优以确定最优参数,直至所述医学图像分割模型达到最佳拟合后完成医学图像分割模型的构建。
9.本发明实施例的另一目的在于提供一种医学图像分割模型的构建系统,所述系统包括:
10.图像数据集获取模块,用于获取用于进行模型训练的图像数据集;
11.模型训练模块,用于根据所述图像数据集进行医学图像分割模型的训练;所述医学图像分割模型为混入有改进eca模块的图像语义分割网络,所述改进eca模块由eca模块和cbam注意力模块耦合而成,其中所述医学图像分割模型中,图像数据集经过改进eca模块处理后作为下一层下采样的输入,未经过改进eca模块处理的特征图做跳跃连接;
12.寻优再构建模块,用于对所述医学图像分割模型进行观测以进行网格寻优以确定最优参数,直至所述医学图像分割模型达到最佳拟合后完成医学图像分割模型的构建。
13.本发明实施例的另一目的在于提供一种计算机设备,包括存储器和处理器,所述存储器中存储有计算机程序,所述计算机程序被所述处理器执行时,使得所述处理器执行所述医学图像分割模型的构建方法的步骤。
14.本发明实施例的另一目的在于提供一种计算机可读存储介质,所述计算机可读存储介质上存储有计算机程序,所述计算机程序被处理器执行时,使得所述处理器执行所述医学图像分割模型的构建方法的步骤。
15.本发明实施例的有益效果是:由于图像经过每层下采样后得到的特征图与对应位置上的上采样的特征图进行特征拼接,即所述的跳跃连接,在进行上采样时能够获取到更多的高分辨率信息,进而更完善地恢复原始图像中的细节,通过底层特征与高层特征的融合,医学图像分割模型能够保留更多高层特征图蕴含的高分辨率信息,从而提高了图像分割精度。
附图说明
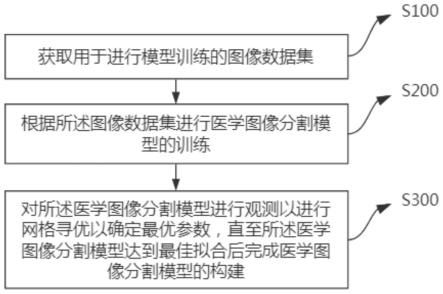
16.图1为本发明实施例提供的医学图像分割模型的构建方法的流程图;
17.图2为本发明实施例提供的医学图像分割模型的结构示意图;
18.图3为本发明实施例提供的获取用于进行模型训练的图像数据集的流程图;
19.图4为本发明实施例提供的对医学图像分割模型进行网格寻优的流程图;
20.图5为本发明实施例提供的医学图像分割模型的构建系统的结构框图;
21.图6为本发明实施例提供的图像数据集获取模块的结构框图;
22.图7为本发明实施例提供的寻优再构建模块的结构框图;
23.图8为一个实施例中计算机设备的内部结构框图;
24.图9为各模型算法针对海马体切片的分割结果图;
25.图10为各模型算法针对细胞图像的分割结果图;
26.图11为各模型算法针对眼部视网膜的分割结果图。
具体实施方式
27.为了使本发明的目的、技术方案及优点更加清楚明白,以下结合附图及实施例,对本发明进行进一步详细说明。应当理解,此处所描述的具体实施例仅仅用以解释本发明,并不用于限定本发明。
28.如图1所示,在一个实施例中,提出了一种医学图像分割模型的构建方法,所述方法包括以下步骤:
29.步骤s100,获取用于进行模型训练的图像数据集。
30.本发明实施例中,选择切片中选择包含有海马体的图片形成图像数据集,其图片应保证细节清晰、大小一致和质量优异,可将图像数据集分为训练集和测试集,其中训练集用于训练模型,而测试集则用于对模型精度等进行测试。作为优选的,所述训练集和测试集中的图片数量比例为9:1。有必要进行说明的是,本发明实施例中,针对医学图像分割模型的图像数据集,若后续医学图像分割模型用于对海马体图片进行分割识别的话,则其训练图像应为海马体相关图片。
31.步骤s200,根据所述图像数据集进行医学图像分割模型的训练;所述医学图像分割模型为混入有改进eca模块的图像语义分割网络,所述改进eca模块由eca模块和cbam注意力模块耦合而成,其中所述医学图像分割模型中,图像数据集经过改进eca模块处理后作为下一层下采样的输入,未经过改进eca模块处理的特征图做跳跃连接。
32.本发明实施例中,图像语义分割网络即unet网络模型,本发明实施例中正是基于unet网络模型的基础构建的,但是区别在于混入了改进eca模块。本发明实施例医学图像分割模型包括下采样和上采样部分,亦或是可以称为编码器-解码器结构。在实际应用时,待处理的图像会被输入到医学图像分割模型中,依次经过下采样和上采样过程,最后得到分割结果。
33.本发明实施例中,由于图像经过每层下采样后得到的特征图与对应位置上的上采样的特征图进行特征拼接,即所述的跳跃连接,同时特征图在经过改进eca模块后再作为下一层下采样的输入,改进eca模块在不降低维数的通道级全局平均池化之后,考虑每个通道及其k个邻居来捕获局部跨通道交互信息,通过一维卷积实现不降维的局部跨信道交互的同时结合空间注意力,更好地获取特征图上的位置信息。
34.关于本发明实施例中的改进eca模块,其是在eca模块的全局平均池化层后,将mlp模块(fc-》relu》fc-》sigmoid)转化为一维卷积的形式,而cbam模块中的通道注意力模块和senet基本一致,只是将单一的平均池化变为了同时采用最大池化和平均池化方法。本发明实施例对图像数据集在通道维度下做最大池化和平均池化,将池化后的两张特征图在通道维度相加,而后使用1x1卷积层,这避免了维度缩减,并可以有效捕获跨通道交互,同时在空间注意力模块采用最大池化和平均池化的堆叠。本技术技术方案的改进eca模块,结合了eca模块将全连接层改为一维卷积从而实现适当的跨通道交互的优点以及cbam模块在通道注意力后接入空间注意力以及采用最大池化和平均池化的相加或堆叠的优点。
35.步骤s300,对所述医学图像分割模型进行观测以进行网格寻优以确定最优参数,直至所述医学图像分割模型达到最佳拟合后完成医学图像分割模型的构建。
36.本发明实施例中,由于医学图像分割模型针对特定的数据集会有不同效果的偏差,所以要进行网格寻优,以使医学图像分割模型针对特定的数据集获取到最佳参数。
37.在一个实施例中,如图3所示,步骤s100具体可以包括以下步骤:
38.步骤s101,获取初始图像集。
39.步骤s102,对所述初始图像集进行预处理,所述预处理至少包括对初始图像集中图像的筛选、类型转换和尺寸修订。
40.本发明实施例中,针对与获得的初始图像集,需要选择其内图像细节清晰、大小一致、质量优异的图像,去除图像中含有模糊、伪影等不清晰图像,而且上述选择过程可以执行一至多次,本发明实施例在此不进行具体限定。
41.步骤s103,对经过预处理的初始图像集进行数据扩增,得到用于进行模型训练的图像数据集。
42.本发明实施例中,对经过预处理的初始图像集进行数据扩增,可以极大提升样本数量,来保证训练精度,而在实际应用时,数据扩增的方法可以为对图像进行旋转、移位等仿射变换,也可以使用镜像变换等。
43.作为优选的,本发明实施例提供了一种对经过预处理的初始图像集进行数据扩增的方法,具体为:通过弹性变换方法对所述经过预处理的初始图像集进行数据扩增。对初始图像集进行弹性变换的操作扩充样本以后,对于最后的识别效果有明显的提升。
44.在一个实施例中,如图2所示,所述医学图像分割模型包括下采样特征提取部和上采样特征提取部,其中所述下采样特征提取部由两个3
×
3的卷积层和一个2
×
2的池化层组
成;所述上采样特征提取部由通过双线性插值进行的上采样和特征拼接以及卷积层构成的。
45.为了进一步的说明该模型的相关参数,详细列举了网络模型的参数,将网络模型分成下采样特征提取部和上采样特征提取部,医学图像分割模型的参数如表1所示。
46.表1医学图像分割模型的参数表
[0047][0048]
在一个实施例中,如图4所示,步骤s300具体可以包括以下步骤:
[0049]
步骤s301,对医学图像分割模型的训练过程进行观测,逐步确定模型的参数范围。
[0050]
本发明实施例在实际应用时,利用pytorch框架(开源python机器学习库)完成医学图像分割模型的创建,利用tensorboard(符号数学系统的可视化工具)对整个模型训练的细节进行观测,进而逐步确定模型参数的范围。
[0051]
步骤s302,根据参数范围逐步确定所述医学图像分割模型的参数最优值。
[0052]
本发明实施例中,由于医学图像分割模型针对特定的数据集会有不同效果的偏差,所以要进行网格寻优,通过上述步骤,已经确定了医学图像分割模型参数的最优值所在的范围,在该范围中逐步确定模型参数的最优值,可以实现针对特定的网络模型以及数据集,确定最优的参数值,从而产生最优效果。
[0053]
步骤s303,根据所述参数最优值对所述医学图像分割模型进行再训练。
[0054]
步骤s304,判定所述医学图像分割模型是否达到最佳拟合,当所述医学图像分割模型达到最佳拟合时,完成医学图像分割模型的构建。
[0055]
本发明实施例中,对所述医学图像分割模型进行再训练时,再次通过tensorboard对模型的训练细节进行观测,来判定医学图像分割模型是否达到最佳拟合,当达到最佳拟合时,完成医学图像分割模型的构建,未达到最佳拟合时,则重新调整模型参数。
[0056]
如图5所示,在一个实施例中,提供了一种医学图像分割模型的构建系统,具体可以包括图像数据集获取模块100、模型训练模块200和寻优再构建模块300。其中:
[0057]
所述图像数据集获取模块100,用于获取用于进行模型训练的图像数据集;
[0058]
所述模型训练模块200,用于根据所述图像数据集进行医学图像分割模型的训练;所述医学图像分割模型为混入有改进eca模块的图像语义分割网络,所述改进eca模块由
eca模块和cbam注意力模块耦合而成,其中所述医学图像分割模型中,图像数据集经过改进eca模块处理后作为下一层下采样的输入,未经过改进eca模块处理的特征图做跳跃连接;
[0059]
所述寻优再构建模块300,用于对所述医学图像分割模型进行观测以进行网格寻优以确定最优参数,直至所述医学图像分割模型达到最佳拟合后完成医学图像分割模型的构建。
[0060]
本发明实施例中,由于图像经过每层下采样后得到的特征图与对应位置上的上采样的特征图进行特征拼接,即所述的跳跃连接,在进行上采样时能够获取到更多的高分辨率信息,进而更完善地恢复原始图像中的细节,通过底层特征与高层特征的融合,医学图像分割模型能够保留更多高层特征图蕴含的高分辨率信息,从而提高了图像分割精度。
[0061]
如图6所示,在一个实施例中,所述图像数据集获取模块100包括初始图像集获取单元101、预处理单元102和数据扩增单元103。其中,
[0062]
所述初始图像集获取单元101,用于获取初始图像集;
[0063]
所述预处理单元102,用于对所述初始图像集进行预处理,所述预处理至少包括对初始图像集中图像的筛选、类型转换和尺寸修订;
[0064]
所述数据扩增单元103,用于对经过预处理的初始图像集进行数据扩增,得到用于进行模型训练的图像数据集。
[0065]
本发明实施例中,针对与获得的初始图像集,需要选择其内图像细节清晰、大小一致、质量优异的图像,去除图像中含有模糊、伪影等不清晰图像,而且上述选择过程可以执行一至多次,本发明实施例在此不进行具体限定。对经过预处理的初始图像集进行数据扩增,可以极大提升样本数量,来保证训练精度,而在实际应用时,数据扩增的方法可以为对图像进行旋转、移位等仿射变换,也可以使用镜像变换等,本发明实施例中,通过弹性变换方法对所述经过预处理的初始图像集进行数据扩增。
[0066]
如图7所示,在一个实施例中,所述寻优再构建模块300包括观测单元301、最优值确定单元302、再训练单元303和拟合判定单元304。其中:
[0067]
所述观测单元301,用于对医学图像分割模型的训练过程进行观测,逐步确定模型的参数范围;
[0068]
所述最优值确定单元302,用于根据参数范围逐步确定所述医学图像分割模型的参数最优值;
[0069]
所述再训练单元303,用于根据所述参数最优值对所述医学图像分割模型进行再训练;
[0070]
所述拟合判定单元304,用于判定所述医学图像分割模型是否达到最佳拟合,当所述医学图像分割模型达到最佳拟合时,完成医学图像分割模型的构建。
[0071]
本发明实施例中,利用pytorch框架(开源python机器学习库)完成医学图像分割模型的创建,利用tensorboard(符号数学系统的可视化工具)对整个模型训练的细节进行观测,进而逐步确定模型参数的范围,在该范围中逐步确定模型参数的最优值,根据所述参数最优值对所述医学图像分割模型进行再训练,对所述医学图像分割模型进行再训练时,再次通过tensorboard对模型的训练细节进行观测,来判定医学图像分割模型是否达到最佳拟合,当达到最佳拟合时,完成医学图像分割模型的构建,未达到最佳拟合时,则重新调整模型参数。
[0072]
图8示出了一个实施例中计算机设备的内部结构图。如图8所示,该计算机设备包括通过系统总线连接的处理器、存储器、网络接口、输入装置和显示屏。其中,存储器包括非易失性存储介质和内存储器。该计算机设备的非易失性存储介质存储有操作系统,还可存储有计算机程序,该计算机程序被处理器执行时,可使得处理器实现医学图像分割模型的构建方法。该内存储器中也可储存有计算机程序,该计算机程序被处理器执行时,可使得处理器执行医学图像分割模型的构建方法。计算机设备的显示屏可以是液晶显示屏或者电子墨水显示屏,计算机设备的输入装置可以是显示屏上覆盖的触摸层,也可以是计算机设备外壳上设置的按键、轨迹球或触控板,还可以是外接的键盘、触控板或鼠标等。
[0073]
本领域技术人员可以理解,图8中示出的结构,仅仅是与本技术方案相关的部分结构的框图,并不构成对本技术方案所应用于其上的计算机设备的限定,具体的计算机设备可以包括比图中所示更多或更少的部件,或者组合某些部件,或者具有不同的部件布置。
[0074]
在一个实施例中,本技术提供的医学图像分割模型的构建系统可以实现为一种计算机程序的形式,计算机程序可在如图8所示的计算机设备上运行。计算机设备的存储器中可存储组成该医学图像分割模型的构建系统的各个程序模块,比如,图5所示的图像数据集获取模块100、模型训练模块200和寻优再构建模块300。各个程序模块构成的计算机程序使得处理器执行本说明书中描述的本技术各个实施例的医学图像分割模型的构建方法中的步骤。
[0075]
例如,图8所示的计算机设备可以通过如图5所示的医学图像分割模型的构建系统中的图像数据集获取模块100执行步骤s100。计算机设备可通过模型训练模块200执行步骤s200。计算机设备可通过寻优再构建模块300执行步骤s300。
[0076]
在一个实施例中,提出了一种计算机设备,所述计算机设备包括存储器、处理器及存储在所述存储器上并可在所述处理器上运行的计算机程序,所述处理器执行所述计算机程序时实现以下步骤:
[0077]
步骤s100,获取用于进行模型训练的图像数据集。
[0078]
步骤s200,根据所述图像数据集进行医学图像分割模型的训练;所述医学图像分割模型为混入有改进eca模块的图像语义分割网络,所述改进eca模块由eca模块和cbam注意力模块耦合而成,其中所述医学图像分割模型中,图像数据集经过改进eca模块处理后作为下一层下采样的输入,未经过改进eca模块处理的特征图做跳跃连接。
[0079]
步骤s300,对所述医学图像分割模型进行观测以进行网格寻优以确定最优参数,直至所述医学图像分割模型达到最佳拟合后完成医学图像分割模型的构建。
[0080]
在一个实施例中,提供一种计算机可读存储介质,计算机可读存储介质上存储有计算机程序,计算机程序被处理器执行时,使得处理器执行以下步骤:
[0081]
步骤s100,获取用于进行模型训练的图像数据集。
[0082]
步骤s200,根据所述图像数据集进行医学图像分割模型的训练;所述医学图像分割模型为混入有改进eca模块的图像语义分割网络,所述改进eca模块由eca模块和cbam注意力模块耦合而成,其中所述医学图像分割模型中,图像数据集经过改进eca模块处理后作为下一层下采样的输入,未经过改进eca模块处理的特征图做跳跃连接。
[0083]
步骤s300,对所述医学图像分割模型进行观测以进行网格寻优以确定最优参数,直至所述医学图像分割模型达到最佳拟合后完成医学图像分割模型的构建。
[0084]
为了评价本实施例中医学图像分割模型的效果,此处选取三个评价指标,分别为dice系数(相似系数)、miou(平均交叉比)和specificity(特异度)。
[0085]
首先,针对图像预测值(b)和真实值(a)之间的关系,可以将样本分为4类:
[0086]
真正值(tp):预测值为1,真实值为1;a∩b
[0087]
真负值(tn):预测值为0,真实值为0;(a∪b)
[0088]
假正值(fp):预测值为1,真实值为0;b-(a∩b)
[0089]
假负值(fn):预测值为0,真实值为1;a-(a∩b)
[0090]
相似系数(dice)可以衡量两个样本的重叠部分,指标范围从0~1,其中1代表完全重叠的状态,0代表完全不重叠的状态,即:
[0091][0092]
所述miou(平均交叉比)即计算预测区域和实际区域连个区域的交集和并集之比,即:
[0093][0094]
该比例也可以变形为tp(交集)比上tp、fp、fn之和(并集),即:
[0095][0096]
所述特异度的值是实际不是目标区域的像素点正确地判断为不是目标区域像素的比例,代表了能够正确判断不是目标区域像素点的能力,特异度的结果越接近1,说明分割效果越好,分割结果中包含非目标区域会导致特异性变低。特异度的计算公式为:
[0097][0098]
实验环境
[0099]
具体的,此处的实验环境如表2所示:
[0100]
表2网医学图像分割模型的详细参数
[0101][0102]
实验结果
[0103]
为了说明本发明实施例中医学图像分割模型的效果,采用了目前几种较为主流的方法作为对比算法。对比算法主要有基于unet网络的医学图像分割算法、基于unet 网络的医学图像分割算法、基于attention unet网络的医学图像分割算法、基于danet网络的医学图像分割算法、基于加入cbam模块的unet网络的医学图像分割算法、基于加入eca模块的unet网络的医学图像分割算法。为了直观展示实验结果,选取某病人的第75张切片展示,结果如图9所示。
[0104]
对比图9的实验结果,较为传统的unet和unet 算法分割出的区域与真值(groundtruth)差异较大,对于海马体的边缘处以及弯折的部位分割精度较差,无法很好的还原海马体原来的样子,而加入不同的这些注意力机制后,分割结果仍然并不能让人满意,从结果可以看出attention unet对于弯折处投入了更多的关注,但是对于尾部的细节并没有精确地分割出来,danet甚至比前者做得更差,这也导致它的指标低于了基线,而unet with cbam和unet with eca都更多的聚焦于整体的形状,导致它们在于弯折处和细节处有冗余,而本发明实施例提出的方法在其中是效果最好的,既能出色地分割出整体的轮廓,又能较好地还原海马体的细节之处。
[0105]
通过实验结果对比可以验证本发明实施例提出的方法相比于原始u-net网络具有更加良好的分割效果,达到了预期优化目标。从图9中可以看出,利用本发明实施例提出的方法进行分割得到的预测结果相比于数据集中由医生手工标注的结果,在整体形状和位置上都已十分接近,且相对于手工标注的边界更为圆滑,对于局部的图像信息也展现的较为
详细和清晰,线条相对逼真和准确,基本能够达到和医生手工标注同样的效果,能够对医疗诊断起到一定的辅助作用。
[0106]
从图像上能够直观的看出,由本发明实施例提出的方法生成的图像的结果较好。那么接下来将通过数值角度来比较几种算法的实验效果,从dice系数和iou两个评价指标来比较(为了便于观察结果,所有结果均精确到0.01%),分别如表2和表3所示:
[0107]
表2海马体分割结果的dice系数表
[0108][0109][0110]
表3海马体分割结果的iou表
[0111]
[0112]
再以上述方法对dsb2018细胞数据集进行分割处理,依然使用了本发明实施例方法以及目前几种较为主流的方法作为对比算法。对比算法主要有基于unet网络的医学图像分割算法、基于unet 网络的医学图像分割算法、基于attention unet网络的医学图像分割算法、基于加入cbam模块的unet网络的医学图像分割算法、基于加入eca模块的unet网络的医学图像分割算法。上述方法的分割结果如图10所示。
[0113]
从图10中可以看出,unet和unet 算法分割结果在暗部区域与真值(groundtruth)差异较大,attention unet、unet with cbam和unet with eca则在多个细胞有重合的区域分割误差较大,而本发明实施例方法在其中是效果最好的,既能出色地分割出光线不好的区域的细胞,又能较好地处理细胞抱团的情况。
[0114]
从图10中能够直观的看出,由本发明实施例方法生成的图像的结果较好。那么接下来从dice系数和iou两个评价指标来比较(为了便于观察结果,所有结果均精确到0.01%),结果分别如表4和表5所示。
[0115]
表4细胞数据集分割结果的dice系数表
[0116][0117]
表5细胞数据集分割结果的iou表
[0118][0119][0120]
再以在drive眼部视网膜数据集上的分割处理结果为例,依然使用了本发明实施例方法以及目前几种较为主流的方法作为对比算法,对比算法同上。为了直观展示实验结果,选取某位病人的图像展示,上述方法的分割结果如图11所示。
[0121]
从图11中,首先可以关注到左下角的区域unet和unet 算法分割结果均有断裂的情况,而对于加入了注意力机制的另外三种算法,断裂部分有所虽小,但仍然存在,在看中间多个分支交汇的区域,几个对比算法要么没有分割出,要么就是出现了误分割,而本发明实施例方法在其中是效果最好的,既能出色地分割出整体的轮廓,又能较好地还原分支的末端以及交汇之处。
[0122]
从图11中能够直观的看出,由本发明实施例方法生成的图像的结果较好。从dice系数和iou两个评价指标来比较(为了便于观察结果,所有结果均精确到0.01%),结果分别如表6和表7所示。
[0123]
表6眼部视网膜数据集分割结果的dice系数表
[0124] unetunet attntiongatedecacbam本技术方法172.00%70.25%72.96%71.67%66.87%77.11%267.10%64.67%67.99%69.12%62.60%74.71%372.68%72.73%73.45%74.02%69.71%78.70%473.31%74.64%72.47%72.99%73.71%79.70%572.78%74.23%73.37%73.27%70.24%77.86%均值71.57%71.30%72.05%72.22%68.63%77.62%方差2.54%4.09%2.30%1.93%4.15%1.89%
[0125]
表4眼部视网膜数据集分割结果的iou表
[0126] unetunet attntiongatedecacbam本技术方法
156.25%54.14%57.43%55.85%50.23%62.74%250.49%47.78%51.51%52.82%45.56%59.63%357.09%57.14%58.04%58.76%53.50%64.88%457.86%59.54%56.82%57.47%58.36%66.25%557.20%59.01%57.94%57.82%54.13%63.75%均值55.78%55.52%56.35%56.54%52.36%63.45%方差3.01%4.82%2.75%2.33%4.77%2.51%
[0127]
应该理解的是,虽然本发明各实施例的流程图中的各个步骤按照箭头的指示依次显示,但是这些步骤并不是必然按照箭头指示的顺序依次执行。除非本文中有明确的说明,这些步骤的执行并没有严格的顺序限制,这些步骤可以以其它的顺序执行。而且,各实施例中的至少一部分步骤可以包括多个子步骤或者多个阶段,这些子步骤或者阶段并不必然是在同一时刻执行完成,而是可以在不同的时刻执行,这些子步骤或者阶段的执行顺序也不必然是依次进行,而是可以与其它步骤或者其它步骤的子步骤或者阶段的至少一部分轮流或者交替地执行。
[0128]
本领域普通技术人员可以理解实现上述实施例方法中的全部或部分流程,是可以通过计算机程序来指令相关的硬件来完成,所述的程序可存储于一非易失性计算机可读取存储介质中,该程序在执行时,可包括如上述各方法的实施例的流程。其中,本技术所提供的各实施例中所使用的对存储器、存储、数据库或其它介质的任何引用,均可包括非易失性和/或易失性存储器。非易失性存储器可包括只读存储器(rom)、可编程rom(prom)、电可编程rom(eprom)、电可擦除可编程rom(eeprom)或闪存。易失性存储器可包括随机存取存储器(ram)或者外部高速缓冲存储器。作为说明而非局限,ram以多种形式可得,诸如静态ram(sram)、动态ram(dram)、同步dram(sdram)、双数据率sdram(ddrsdram)、增强型sdram(esdram)、同步链路(synchlink)dram(sldram)、存储器总线(rambus)直接ram(rdram)、直接存储器总线动态ram(drdram)、以及存储器总线动态ram(rdram)等。
[0129]
以上所述实施例的各技术特征可以进行任意的组合,为使描述简洁,未对上述实施例中的各个技术特征所有可能的组合都进行描述,然而,只要这些技术特征的组合不存在矛盾,都应当认为是本说明书记载的范围。
[0130]
以上所述实施例仅表达了本发明的几种实施方式,其描述较为具体和详细,但并不能因此而理解为对本发明专利范围的限制。应当指出的是,对于本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变形和改进,这些都属于本发明的保护范围。因此,本发明专利的保护范围应以所附权利要求为准。
[0131]
以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,均应包含在本发明的保护范围之内。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。
