1.本发明涉及一种具有养发育发功效的中草药活性物@囊泡复合物及其制备,属于化妆品技术领域。
背景技术:
2.头发是人体身体的组成部分之一,头发的变化与人体的生理病理变化有着密切的关系。现代人们生活节奏快、工作时间长、精神压力大,且作息不规律,脱发已经日渐成为越来越多当代人们的困扰,并且呈现年轻化的趋势。就中国来说,近年来脱发人群数量直线上升,每6人中就有1人脱发的情况。据统计,全世界人口脱发率达到了32.13%,且脱发患者数量逐年递增。那些有助于毛发生长、减少脱发和断发的育发类化妆产品的需求越来越旺盛,功效要求也越来越高。
3.头发出油、干燥、脱发并不只是头发出现了问题,追根溯源,其实是头皮和毛囊的问题。头皮和头发是土壤和草木的关系,好的土壤长出好的草木,同理,好的头皮才能有好的头发。所以,头皮护理才是解决脱发问题的关键。目前市面上治疗脱发的产品种类很多,其中西药以激素类居多,长期使用可能会对身体带来一定的副作用,且停药易复脱。2015年以来,随着国家政策对中医药支持力度的加深,中药类化妆品数量逐年增长。其实,中医治疗头发疾病历史悠久,多册医药古典都记载过养发良方,并流传至今。中草药提取物中含有类黄酮、鞣质、虫草酸、果酸、皂苷、氨基酸、微量元素等多种天然成分,具有扩张血管、消炎抗菌、抗氧化、调节免疫等功能,可有效治疗脱发,促进毛发生长。但是,由于中草药提取物中的活性成分种类繁多、复杂,物理化学性质等也大相径庭,故很难同时溶解于同一溶剂中,影响了活性物质的分散和吸收,阻碍了药效的发挥。
4.囊泡是由两亲分子聚集形成的具有核壳结构的闭合双分子层,能够包容多种物质,并按照物质的极性把它们增溶在不同部位。亲水性物质被包容在其亲水微区,也就是水核之中;疏水性物质则增溶于两亲分子的碳氢链夹层之中。故中草药提取物中的亲水性和疏水性活性成分皆可被囊泡同时增溶和负载,提高了难溶活性物质的溶解度和分散性,且囊泡双层膜结构带来的选择渗透性和缓释性能,可使活性物质在头皮上维持稳定、持久释放。活性物质在囊泡体系的加持下,在头皮表面、毛囊周围生成微生态环境,减少离子导入对毛囊的损伤,从根源上有效激发毛囊活力,从而获得药效的最佳利用,达到养发和育发的效果。
5.印度专利文件in1764mum2014a为了改善脂溶性差的药物的生物利用度或吸收,通过将草药活性成分与磷脂酰胆碱结合,增加了活性成分的溶解性。但磷脂酰胆碱所形成的脂质体渗透性差,对活性成分的释放不利。且该专利文件公开的中草药成分主要用于内服,无法确定中草药提取物用于外用时的溶解性和生物吸收度。
6.韩国专利文件kr1020090059445a公开了用于脱毛预防和毛发生长的护发组合物,更具体地涉及通过含有阳离子/阴离子表面活性剂混合囊泡促进头皮和头发吸附的脱毛预
50份、青皮5-15份、黄柏5-15份、黄精20-50份、制首乌20-50份、绞股蓝20-50份、侧柏叶20-50份、川芎5-15份、天麻5-15份、乌梅炭5-15份、地肤子5-15份、红车轴草20-50份、阿胶20-50份;
22.更优选为:何首乌10份、墨旱莲10份、沙参30份、白术30份、泽泻12份、赤芍30份、青皮12份、黄柏15份、黄精30份、制首乌30份、绞股蓝30份、侧柏叶30份、川芎12份、天麻12份、乌梅炭10份、地肤子10份、红车轴草25份、阿胶35份。
23.根据本发明,优选的,所述的囊泡前驱体,可选自下列之一或组合:单脂肪酸甘油酯、单烷基磷酸酯及其盐、2-羟基脂肪酸及其盐、烟酸及其衍生物、三嵌段共聚物。
24.根据本发明,优选的,所述的单脂肪酸甘油酯为直链单脂肪酸甘油酯;进一步优选为c
8-c
18
链长的直链单脂肪酸甘油酯;更优选为:辛酸甘油酯、癸酸甘油酯、月桂酸甘油酯、肉豆蔻酸甘油酯、十五烷酸甘油酯、棕榈酸甘油酯。
25.根据本发明,优选的,所述的单烷基磷酸酯及其盐为直链烷基磷酸酯及其盐;进一步优选为c
8-c
16
链长的直链单烷基磷酸酯或其盐;更优选为:辛基磷酸酯及其钠盐、钾盐、镁盐、锌盐,癸基磷酸酯及其钠盐、钾盐、镁盐、锌盐,月桂基磷酸酯及其钠盐、钾盐、镁盐、锌盐,肉豆蔻基磷酸酯及其钠盐、钾盐、镁盐、锌盐,棕榈基磷酸酯及其钠盐、钾盐、镁盐、锌盐。
26.根据本发明,优选的,所述的2-羟基脂肪酸及其盐为2-羟基直链脂肪酸及其盐;进一步优选为c
8-c
16
链长的2-羟基直链脂肪酸及其盐;更优选为:2-羟基辛酸及其钠盐、钾盐、镁盐、锌盐,2-羟基癸酸及其钠盐、钾盐、镁盐、锌盐,2-羟基月桂酸及其钠盐、钾盐、镁盐、锌盐,2-羟基肉豆蔻酸及其钠盐、钾盐、镁盐、锌盐,2-羟基棕榈酸及其钠盐、钾盐、镁盐、锌盐。
27.根据本发明,优选的,所述的烟酸及其衍生物为烟酸、烟酸苄酯、生育酚烟酸酯。
28.根据本发明,优选的,所述三嵌段共聚物化学组成通式为:peo
x-ppo
y-peo
x
,13≤x≤133,29≤y≤65;;更优选为:peo
77-ppo
29-peo
77
、peo
13-ppo
30-peo
13
、peo
24-ppo
35-peo
24
、peo
133-ppo
50-peo
133
、peo
19-ppo
30-peo
19
、peo
100-ppo
65-peo
100
、peo
26-ppo
40-peo
26
。
29.本发明的中草药活性物@囊泡复合物为均一稳定的体系,在常温下能稳定放置1年以上。
30.本发明所述的中草药活性物@囊泡复合物的制备方法,包括步骤如下:
31.向原料药物中加入混合溶剂提取,收集提取物,加入囊泡前驱体,混匀,醇沉,离心,过滤,浓缩,即得中草药活性物@囊泡复合物。
32.根据本发明,优选的,所述混合溶剂为乙醇-水混合液。根据本发明,优选的,所述的乙醇-水混合液的乙醇的体积百分比浓度为40%~80%,进一步优选55%~70%。
33.根据本发明,优选的,所述提取的次数为1~5次,每次所述提取的时间为1~5小时;所述提取的温度为55℃~80℃。
34.最优选的,提取的次数为4次,每次所述提取的时间为4小时,提取的温度为70℃。
35.根据本发明,所述的中草药活性物@囊泡复合物是在中草药活性物诱导下自发形成囊泡的同时制成。
36.根据本发明,所述的中草药活性物@囊泡复合物的应用,用于化妆品领域。
37.本发明的技术特点和有益效果如下:
38.现有的中草药活性成分,尤其是脂溶性活性成分,很难以分子状态增溶进入产品中作用于头皮与毛囊,无法发挥最佳药效,所以防脱育发效果大打折扣。且现有产品中的活
性成分绝大部分都是仅在使用瞬间对头皮发生高浓度作用,缺乏活性物的缓慢持续释放环境,无法使其维持在一定的动态有效浓度,故吸收效果较差。本发明针对现有技术的不足以及现有产品的缺陷,提供一种安全有效的具有防脱发和养发育发功效的中草药活性物@囊泡复合物及其制备方法。囊泡的核壳双层膜结构不仅可以同时增溶中草药提取物中的亲水性和疏水性活性成分,而且凭借其自身的选择渗透性和缓释性能,在头皮和毛囊周围形成了稳定的中草药活性物@囊泡微生态环境,从而获得药效的最佳利用,达到养发和育发的效果。
39.1、本发明提供了一类中草药活性物@囊泡复合物,活性物包覆于囊泡中,提高了难溶活性物质的溶解度和分散性。亲水性物质被包覆在其亲水微区,也就是水核之中;疏水性物质则增溶于囊泡的双层膜之间。
40.2、本发明的中草药活性物@囊泡微环境技术使活性物质能够稳定、持久释放,并且提高了活性成分提取物的稳定性,达到了更好的养发育发功效,在药物输送与控释和化妆品等领域有重要的应用前景。
41.3、本发明的中草药活性物@囊泡复合物的分散溶剂为乙醇-水混合液,较之纯水等溶剂,具有更优越的渗透性和杀菌能力。
42.4、本发明的中草药活性物@囊泡复合物制备方法简单,反应温和,适于大规模生产。
43.5、本发明的中草药活性物@囊泡复合物为均一稳定体系,中草药活性物的含量范围为30~100g/l,复合物粒径优可优选为纳米级(200~800nm),少量体系的复合体粒子粒径可达1~5μm,在常温下可稳定放置1年以上。
44.6、本发明中的中草药提取液的ph值为5~6,zete电位约﹣15
±
5.0mv,故选取非离子表面活性剂或阴离子表面活性剂为囊泡前驱体,避免了中草药提取的活性物质失活或者沉淀的发生。尤其是非离子表面活性剂类的囊泡前驱体,在水或者醇中皆有较好的溶解性能,由于不呈离子状态,故稳定性高,不易受酸、碱或者强电解质无机盐的影响。并且,它与其他类型表面活性剂的相容性好,可以复配使用。
45.7、本发明中的复合物采用酊溶剂(乙醇-水混合液),其中的短链醇是一种常用的囊泡破坏剂,故绝大多数相囊泡体系是无法在酊溶液中稳定存在的。而本发明中的囊泡复合物可在酊溶剂中自发形成,且稳定存在,具有更优越的透皮能力,这也是本发明剂型的一个优势。
附图说明
46.图1是实施例1中草药活性物@月桂酸甘油酯囊泡复合物的动态光散射粒径分布图和透射电子显微照片。
47.图2是实施例2中草药活性物@单十二烷基磷酸一钠囊泡复合物的动态光散射粒径分布图和光学显微照片。
48.图3是实施例3中草药活性物@烟酸(0.5g/l)囊泡复合物的动态光散射粒径分布图和透射电子显微照片。
49.图4是实施例4中草药活性物@烟酸(1g/l)囊泡复合物的动态光散射粒径分布图和透射电子显微照片。
50.图5是实施例5中草药活性物@2-羟基辛酸钠囊泡复合物的动态光散射粒径分布图和透射电子显微照片。
51.图6是实施例6中未包覆活性物的peo
77-ppo
29-peo
77
(5g/l)囊泡的动态光散射粒径分布图和透射电子显微照片。
52.图7是实施例6中草药活性物@peo
77-ppo
29-peo
77
(5g/l)囊泡复合物的动态光散射粒径分布图和透射电子显微照片。
53.图8是实施例7中草药活性物@peo
77-ppo
29-peo
77
(10g/l)囊泡复合物的动态光散射粒径分布图和透射电子显微照片。
54.图9是实施例8中草药活性物@peo
13-ppo
30-peo
13
囊泡复合物的动态光散射粒径分布图和和光学显微照片。
55.图10是试验例1中草药活性物@囊泡复合物的小鼠毛发生长实验表观照片。
56.图11是试验例1中草药活性物@囊泡复合物的小鼠背部毛囊光镜图。
57.图12是试验例1中草药活性物@囊泡复合物的小鼠背部炎症因子荧光染色图。
58.图13是对比例1未加入囊泡前驱体的中草药提取液的透射电子显微照片。
59.图14是对比例2改变添加顺序的月桂酸甘油酯与中草药提取液混合物的透射电子显微照片。
60.图15是对比例3中草药活性物与tween 80混合物的透射电子显微照片。
61.图16是对比例4中草药活性物与硬脂酸甘油酯混合物的透射电子显微照片。
62.图17是对比例5中草药活性物与peo
77-ppo
29-peo
77
(1g/l)混合物透射电子显微照片。
63.图18是对比例6中草药活性物与peo
13-ppo
30-peo
13
(25g/l)混合物的透射电子显微照片。
具体实施方式
64.以下结合具体实例来进一步说明本发明,但是,这实施例仅仅是用于更详细的具体说明之用,并不对本发明做任何形式的限制。除非特别说明,本发明采用的试剂、方法和设备为本技术领域常规试剂、方法和设备。
65.除非特别说明,以下示例所采用的试剂和材料均为市购。
66.实施例中使用的药材如下:
67.何首乌、墨旱莲、沙参、白术、泽泻、赤芍、青皮、黄柏、黄精、制首乌、绞股蓝、侧柏叶、川芎、天麻、乌梅炭、地肤子、红车轴草、阿胶。
68.活性成分的提取过程如下:
69.向原料药物中加入混合溶剂提取,收集提取物,加入囊泡前驱体,混匀,醇沉,离心,过滤,浓缩,即得中草药活性物@囊泡复合物。
70.实施例1:
71.(1)分别称取何首乌10g、墨旱莲10g、沙参30g、白术30g、泽泻12g、赤芍30g、青皮12g、黄柏15g、黄精30g、制首乌30g、绞股蓝30g、侧柏叶30g、川芎12g、天麻12g、乌梅炭10g、地肤子10g、红车轴草25g、阿胶35g混合后并粉碎至粉末状态。
72.(2)将操作(1)中药材粉末置于提取罐内,加入650ml三次水和800ml乙醇,浸泡30
分钟,醇沉,浓缩,提取,得到中草药提取物。其中提取的次数为4次,每次所述提取的时间为4小时,提取的温度为70℃。
73.(3)将操作(2)得到的中草药提取物中,加入0.3g月桂酸甘油酯,涡旋搅拌,离心,静置24小时,过滤,浓缩,即可得到中草药活性物@月桂酸甘油酯囊泡复合物。
74.本实施例得到的中草药活性物@月桂酸甘油酯囊泡复合物的动态光散射粒径分布图和透射电子显微照片如图1所示。由图1可知本实施例产品内有大量囊泡存在,囊泡粒径分布为700nm左右,并且负染色透射电子显微照片中还可观察到大量粒径为200nm左右的聚集体。
75.实施例2:
76.(1)分别称取何首乌10g、墨旱莲10g、沙参30g、白术30g、泽泻12g、赤芍30g、青皮12g、黄柏15g、黄精30g、制首乌30g、绞股蓝30g、侧柏叶30g、川芎12g、天麻12g、乌梅炭10g、地肤子10g、红车轴草25g、阿胶35g混合后并粉碎至粉末状态。
77.(2)将操作(1)中药材粉末置于提取罐内,加入650ml三次水和800ml乙醇,浸泡30分钟,醇沉,浓缩,提取,得到中草药提取物。其中提取的次数为4次,每次所述提取的时间为4小时,提取的温度为70℃。
78.(3)将操作(2)得到的中草药提取物中,加入1.5g单十二烷基磷酸一钠,涡旋搅拌,离心,静置24小时,过滤,浓缩,即可得到中草药活性物@单十二烷基磷酸一钠囊泡复合物。
79.本实施例得到的中草药活性物@单十二烷基磷酸一钠囊泡复合物的动态光散射粒径分布图和透射电子显微照片如图2所示。由图2可知本实施例产品内有大量纳米级囊泡和微米级囊泡共存,粒径分布分别为10~100nm和1~5μm之间。
80.实施例3:
81.(1)分别称取何首乌10g、墨旱莲10g、沙参30g、白术30g、泽泻12g、赤芍30g、青皮12g、黄柏15g、黄精30g、制首乌30g、绞股蓝30g、侧柏叶30g、川芎12g、天麻12g、乌梅炭10g、地肤子10g、红车轴草25g、阿胶35g混合后并粉碎至粉末状态。
82.(2)将操作(1)中药材粉末置于提取罐内,加入650ml三次水和800ml乙醇,浸泡30分钟,醇沉,浓缩,提取,得到中草药提取物。其中提取的次数为4次,每次所述提取的时间为4小时,提取的温度为70℃。
83.(3)将操作(2)得到的中草药提取物中,加入0.5g烟酸,涡旋搅拌,离心,静置24小时,过滤,浓缩,即可得到中草药活性物@烟酸(0.5g/l)囊泡复合物。
84.本实施例得到的中草药活性物@烟酸(0.5g/l)囊泡复合物的动态光散射粒径分布图和透射电子显微照片如图3所示。由图3可知本实施例产品内有大量粒径为200nm左右的囊泡存在,且分散均匀。
85.实施例4:
86.(1)分别称取何首乌10g、墨旱莲10g、沙参30g、白术30g、泽泻12g、赤芍30g、青皮12g、黄柏15g、黄精30g、制首乌30g、绞股蓝30g、侧柏叶30g、川芎12g、天麻12g、乌梅炭10g、地肤子10g、红车轴草25g、阿胶35g混合后并粉碎至粉末状态。
87.(2)将操作(1)中药材粉末置于提取罐内,加入650ml三次水和800ml乙醇,浸泡30分钟,醇沉,浓缩,提取,得到中草药提取物。其中提取的次数为4次,每次所述提取的时间为4小时,提取的温度为70℃。
88.(3)将操作(2)得到的中草药提取物中,加入1g烟酸,涡旋搅拌,离心,静置24小时,过滤,浓缩,即可得到中草药活性物@烟酸(1g/l)囊泡复合物。
89.本实施例得到的中草药活性物@烟酸(1g/l)囊泡复合物的动态光散射粒径分布图和透射电子显微照片如图4所示。由图4可知本实施例产品内有大量粒径为200~400nm左右的囊泡存在,且分散均匀。
90.实施例5:
91.(1)分别称取何首乌10g、墨旱莲10g、沙参30g、白术30g、泽泻12g、赤芍30g、青皮12g、黄柏15g、黄精30g、制首乌30g、绞股蓝30g、侧柏叶30g、川芎12g、天麻12g、乌梅炭10g、地肤子10g、红车轴草25g、阿胶35g混合后并粉碎至粉末状态。
92.(2)将操作(1)中药材粉末置于提取罐内,加入650ml三次水和800ml乙醇,浸泡30分钟,醇沉,浓缩,提取,得到中草药提取物。其中提取的次数为4次,每次所述提取的时间为4小时,提取的温度为70℃。
93.(3)将操作(2)得到的中草药提取物中,加入3.6g2-羟基辛酸钠,涡旋搅拌,离心,静置24小时,过滤,浓缩,即可得到中草药活性物@2-羟基辛酸钠囊泡复合物。
94.本实施例得到的中草药活性物@2-羟基辛酸钠囊泡复合物的动态光散射粒径分布图和透射电子显微照片如图5所示。由图5可知本实施例产品内有大量囊泡存在,囊泡粒径分布为600nm左右,并且负染色透射电子显微照片中还可观察到大量粒径为200nm左右的聚集体。
95.实施例6:
96.(1)分别称取何首乌10g、墨旱莲10g、沙参30g、白术30g、泽泻12g、赤芍30g、青皮12g、黄柏15g、黄精30g、制首乌30g、绞股蓝30g、侧柏叶30g、川芎12g、天麻12g、乌梅炭10g、地肤子10g、红车轴草25g、阿胶35g混合后并粉碎至粉末状态。
97.(2)将操作(1)中药材粉末置于提取罐内,加入650ml三次水和800ml乙醇,浸泡30分钟,醇沉,浓缩,提取,得到中草药提取物。其中提取的次数为4次,每次所述提取的时间为4小时,提取的温度为70℃。
98.(3)将操作(2)得到的中草药提取物中,加入5g peo
77-ppo
29-peo
77
,涡旋搅拌,离心,静置24小时,过滤,浓缩,即可得到中草药活性物@peo
77-ppo
29-peo
77
(5g/l)囊泡复合物。
99.未包覆中草药活性物的peo
77-ppo
29-peo
77
(5g/l)囊泡和本实施例得到的中草药活性物@peo
77-ppo
29-peo
77
(5g/l)囊泡复合物的动态光散射粒径分布图和透射电子显微照片分别如图6和图7所示。未包覆活性物前的囊泡分散均匀,粒径为200~400nm(图6);而包覆活性物后的中草药活性物@囊泡粒径显著增大,约为700-800nm,且膜壁增厚(图7)。
100.实施例7:
101.(1)分别称取何首乌10g、墨旱莲10g、沙参30g、白术30g、泽泻12g、赤芍30g、青皮12g、黄柏15g、黄精30g、制首乌30g、绞股蓝30g、侧柏叶30g、川芎12g、天麻12g、乌梅炭10g、地肤子10g、红车轴草25g、阿胶35g混合后并粉碎至粉末状态。
102.(2)将操作(1)中药材粉末置于提取罐内,加入650ml三次水和800ml乙醇,浸泡30分钟,醇沉,浓缩,提取,得到中草药提取物。其中提取的次数为4次,每次所述提取的时间为4小时,提取的温度为70℃。
103.(3)将操作(2)得到的中草药提取物中,加入10g peo
77-ppo
29-peo
77
,涡旋搅拌,离
心,静置24小时,过滤,浓缩,即可得到中草药活性物@peo
77-ppo
29-peo
77
(10g/l)囊泡复合物。
104.本实施例得到的中草药活性物@peo
77-ppo
29-peo
77
(10g/l)囊泡复合物的动态光散射粒径分布图和透射电子显微照片如图8所示。由图8可知本实施例产品内有大量囊泡存在,囊泡粒径为200nm左右,且分散均匀。
105.实施例8:
106.(1)分别称取何首乌10g、墨旱莲10g、沙参30g、白术30g、泽泻12g、赤芍30g、青皮12g、黄柏15g、黄精30g、制首乌30g、绞股蓝30g、侧柏叶30g、川芎12g、天麻12g、乌梅炭10g、地肤子10g、红车轴草25g、阿胶35g混合后并粉碎至粉末状态。
107.(2)将操作(1)中药材粉末置于提取罐内,加入650ml三次水和800ml乙醇,浸泡30分钟,醇沉,浓缩,提取,得到中草药提取物。其中提取的次数为4次,每次所述提取的时间为4小时,提取的温度为70℃。
108.(3)将操作(2)得到的中草药提取物中,加入5g peo
13-ppo
30-peo
13
,涡旋搅拌,离心,静置24小时,过滤,浓缩,即可得到中草药活性物@peo
13-ppo
30-peo
13
囊泡复合物。
109.本实施例得到的草药活性物@peo
13-ppo
30-peo
13
囊泡复合物的动态光散射粒径分布图和光学显微照片如图9所示。由图9可知本实施例产品内有大量囊泡微米级囊泡存在,粒径分布较宽,约为2~4μm左右。
110.实施例9:
111.(1)分别称取何首乌15g、墨旱莲5g、沙参20g、白术30g、泽泻12g、赤芍40g、青皮12g、黄柏15g、黄精30g、制首乌35g、绞股蓝25g、侧柏叶30g、川芎12g、天麻12g、乌梅炭10g、地肤子10g、红车轴草25g、阿胶35g混合后并粉碎至粉末状态。
112.(2)将操作(1)中药材粉末置于提取罐内,加入650ml三次水和800ml乙醇,浸泡30分钟,醇沉,浓缩,提取,得到中草药提取物。其中提取的次数为4次,每次所述提取的时间为4小时,提取的温度为70℃。
113.(3)将操作(2)得到的中草药提取物中,加入0.3g月桂酸甘油酯,涡旋搅拌,离心,静置24小时,过滤,浓缩,即可得到中草药活性物@月桂酸甘油酯囊泡复合物ⅱ。
114.实施例10:
115.(1)分别称取何首乌5g、墨旱莲5g、沙参35g、白术30g、泽泻12g、赤芍35g、青皮12g、黄柏10g、黄精40g、制首乌30g、绞股蓝30g、侧柏叶30g、川芎12g、天麻12g、乌梅炭5g、地肤子15g、红车轴草25g、阿胶35g混合后并粉碎至粉末状态。
116.(2)将操作(1)中药材粉末置于提取罐内,加入650ml三次水和800ml乙醇,浸泡30分钟,醇沉,浓缩,提取,得到中草药提取物。其中提取的次数为4次,每次所述提取的时间为4小时,提取的温度为70℃。
117.(3)将操作(2)得到的中草药提取物中,加入1.5g单十二烷基磷酸一钠,涡旋搅拌,离心,静置24小时,过滤,浓缩,即可得到中草药活性物@单十二烷基磷酸一钠囊泡复合物ⅱ。
118.实施例11:
119.(1)分别称取何首乌10g、墨旱莲20g、沙参30g、白术30g、泽泻12g、赤芍20g、青皮12g、黄柏15g、黄精20g、制首乌35g、绞股蓝30g、侧柏叶35g、川芎12g、天麻10g、乌梅炭15g、
地肤子12g、红车轴草20g、阿胶35g混合后并粉碎至粉末状态。
120.(2)将操作(1)中药材粉末置于提取罐内,加入650ml三次水和800ml乙醇,浸泡30分钟,醇沉,浓缩,提取,得到中草药提取物。其中提取的次数为4次,每次所述提取的时间为4小时,提取的温度为70℃。
121.(3)将操作(2)得到的中草药提取物中,加入10g peo
77-ppo
29-peo
77
,涡旋搅拌,离心,静置24小时,过滤,浓缩,即可得到中草药活性物@peo
77-ppo
29-peo
77
(10g/l)囊泡复合物ⅱ。
122.实施例12:
123.(1)分别称取何首乌10g、墨旱莲10g、沙参30g、白术30g、泽泻12g、赤芍30g、青皮12g、黄柏15g、黄精30g、制首乌30g、绞股蓝30g、侧柏叶30g、川芎12g、天麻12g、乌梅炭10g、地肤子10g、红车轴草25g、阿胶35g混合后并粉碎至粉末状态。
124.(2)将操作(1)中药材粉末置于提取罐内,加入650ml三次水和800ml乙醇,浸泡30分钟,醇沉,浓缩,提取,得到中草药提取物。其中提取的次数为4次,每次所述提取的时间为2小时,提取的温度为80℃。
125.(3)将操作(2)得到的中草药提取物中,加入0.3g月桂酸甘油酯,涡旋搅拌,离心,静置24小时,过滤,浓缩,即可得到中草药活性物@月桂酸甘油酯囊泡复合物ⅲ。
126.实施例13:
127.(1)分别称取何首乌10g、墨旱莲10g、沙参30g、白术30g、泽泻12g、赤芍30g、青皮12g、黄柏15g、黄精30g、制首乌30g、绞股蓝30g、侧柏叶30g、川芎12g、天麻12g、乌梅炭10g、地肤子10g、红车轴草25g、阿胶35g混合后并粉碎至粉末状态。
128.(2)将操作(1)中药材粉末置于提取罐内,加入650ml三次水和800ml乙醇,浸泡30分钟,醇沉,浓缩,提取,得到中草药提取物。其中提取的次数为4次,每次所述提取的时间为5小时,提取的温度为60℃。
129.(3)将操作(2)得到的中草药提取物中,加入0.3g月桂酸甘油酯,涡旋搅拌,离心,静置24小时,过滤,浓缩,即可得到中草药活性物@月桂酸甘油酯囊泡复合物ⅳ。
130.试验例1、中草药活性物@囊泡复合物的小鼠毛发生长实验
131.根据文献调研,本实验选择c57bl/6小鼠作为脱发模型建立对象。该小鼠毛发为黑色可表现出独特的毛发周期同步性。且该小鼠躯干皮肤的黑色素细胞只存在于毛囊中,而且仅在生长期时合成黑色素。在毛发的生长期,由于毛球部黑素细胞不断产生黑色素,并传递给毛囊角质形成细胞,使皮肤外观呈现黑色。退行期时,黑色素生成减少,皮肤呈灰黑色。在休止期由于毛球部微缩消失,毛囊停止生成黑色素,皮肤变为粉红色。休止期的毛发经拔除后局部可被诱导出高度同步的新毛发周期,组织学上同该鼠自然周期变化一致,故可从皮肤颜色的变化来推断毛发周期的改变。
132.动物造模:c57bl/6小鼠,雌性,7周龄,体重18-20g。使用动物剃毛器先进行简单剃毛后,再使用脱毛膏进行脱毛,脱毛面积为2
×
3cm2,皮肤为粉红色即为造模成功。
133.给药方法:将上述造模成功的小鼠随机分成6组,每组5只,按分组每天2次(早、晚)给予对应药物处理,涂抹时间相同,涂抹量每次0.4ml,连续给药21天。空白组给予55%酊溶剂涂抹处理,阳性对照组给予3%米诺地尔酊剂处理,药物治疗组给予本发明实施例配制样品。
134.其中:
135.给药组a给予中草药活性物提取液处理;
136.给药组b给予实施例2复合物处理;
137.给药组c给予实施例7复合物处理;
138.涂抹方式使用棉签蘸取均匀涂抹于脱毛区。
139.评价指标:给药后每天观察小鼠脱毛区肤色变化情况(每天固定时间),并于每7天拍摄一组照片,记录每只小鼠去毛区皮肤颜色由粉红色变成灰色的时间和由灰色至长满毛的时间,记录各组小鼠毛长平均值,并且记录小鼠体重变化平均值。
140.将连续给药21天的小鼠脱颈处死,使用动物剃毛器简单剃毛,用剪刀将背部皮肤修剪为2
×
2cm2的形状,用生理盐水冲去表面毛发,然后浸泡于4%多聚甲醛中24~36h,将剪裁好的皮肤组织切片及he染色后,在光学显微镜下观察组织切片横截面、纵截面毛囊个数及毛囊形态,各组小鼠取(
×
10)视野下毛囊个数,并用spss.26软件进行统计学分析处理,数据以进行表示,组间比较采用单向方差分析,p<0.05为具有统计意义。
141.将剪裁好的皮肤组织切片后,并选取炎症因子il-6和tnf-α进行标记并染色后,在荧光共聚焦显微镜下观察小鼠皮肤组织在视野(
×
200)下的炎症情况(阳性区域为绿色)。
142.中草药活性物@囊泡复合物的小鼠毛发生长实验结果如图10、表1和表2所示。给药组小鼠脱毛区的肤色变黑时间明显短于空白组;给药组的小鼠新生毛发长度在给药组均显著优于空白组;中草药活性物@囊泡复合物的小鼠毛发生长效果优于未添加囊泡前驱体的中草药提取物体系。综上,实施例2和实施例7均表现出了较好的促进小鼠毛模型毛发生长的特性。
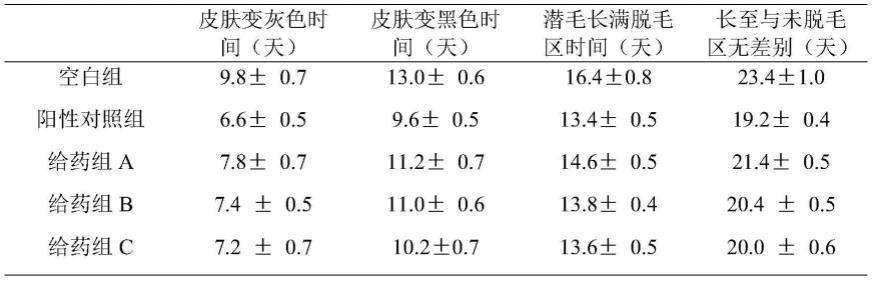
143.表1小鼠脱毛区肤色变化
[0144][0145]
表2用药21天后小鼠新生毛发长度平均值
[0146][0147]
表3用药21天后小鼠毛囊个数平均值
[0148][0149][0150]“**”表示与对照组之间有非常显著性差异,p<0.01
[0151]
中草药活性物@囊泡复合物的小鼠背部毛囊光镜实验结果如图11、表3所示。空白组毛囊数目较少,毛囊颜色变淡,下端退化,处于退行期,阳性对照组与给药组a、b、c毛囊数目较多,毛囊分布更为紧密,毛乳头较大,毛球内黑色素明显,毛囊仍处于生长期。且给药组b、c较给药组a毛囊数目略多,表现出了较好的促进小鼠毛模型毛发生长的特性。
[0152]
中草药活性物@囊泡复合物的小鼠背部炎症因子荧光染色实验结果如图12所示。各组小鼠炎症情况并没有明显差别,表明小鼠皮肤组织中的炎症因子分泌正常,给药组a、b、c在给药21天内均未表现出对小鼠生长的毒性效应。
[0153]
试验例2、中草药活性物@囊泡复合物的人体头发生长实验
[0154]
(1)对实施例1、2、4、5、7、8进行人体头发生长实验。
[0155]
(2)受试者共120人,男性60人,女性60人,年龄:26-60岁,符合受试者入选标准。将受试者随机分为6组,每组20人。
[0156]
(3)使用实施例1、2、4、5、7、8制备的中草药活性物@囊泡复合物来进行治疗。
[0157]
(4)取5ml中草药活性物@囊泡复合物涂抹于头皮部,每天2次,观察有无全身及局部不良反应,并详细记录结果,每周检测1次,观察4周,结果见表4。
[0158]
(5)疗效标准分为(a)显效:无明显脱发,有大量新毛发生成;(b)有效:脱发得到控制,有少量新毛发生成;(c)无效:治疗前后无明显变化;(d)有害:产生全身或局部有不良反应。
[0159]
(6)中草药活性物@囊泡复合物人体试用实验结果如表1所示。
[0160]
表4中草药活性物@囊泡复合物的人体试用实验结果
[0161][0162]
由表4可知,实施例1、2、4、5、7、8均表现出了较好的促进人体头发生长的特性。
[0163]
对比例1:
[0164]
(1)分别称取何首乌10g、墨旱莲10g、沙参30g、白术30g、泽泻12g、赤芍30g、青皮
12g、黄柏15g、黄精30g、制首乌30g、绞股蓝30g、侧柏叶30g、川芎12g、天麻12g、乌梅炭10g、地肤子10g、红车轴草25g、阿胶75g混合后并粉碎至粉末状态。
[0165]
(2)将操作(1)中药材粉末置于提取罐内,加入650ml三次水和800ml乙醇,浸泡30分钟,醇沉,浓缩,提取,得到中草药提取物。其中提取的次数为4次,每次所述提取的时间为4小时,提取的温度为70℃。
[0166]
(3)将操作(2)得到的中草药提取物涡旋搅拌,离心,静置24小时,过滤,浓缩,样品分层,底部有沉淀析出,常温下无法形成均一、稳定的溶液。
[0167]
对比例1中未加入囊泡前驱体,其中草药提取液的透射电子显微照片如图13所示。提取液中的活性物质分散性差,聚集严重。这说明囊泡前驱体对于中草药提取液中活性物质的分散性、均一性和稳定性起到了重要作用。
[0168]
对比例2:
[0169]
(1)分别称取何首乌10g、墨旱莲10g、沙参30g、白术30g、泽泻12g、赤芍30g、青皮12g、黄柏15g、黄精30g、制首乌30g、绞股蓝30g、侧柏叶30g、川芎12g、天麻12g、乌梅炭10g、地肤子10g、红车轴草25g、阿胶35g混合后并粉碎至粉末状态。
[0170]
(2)将操作(1)中药材粉末置于提取罐内,加入0.3g月桂酸甘油酯、650ml三次水和800ml乙醇,浸泡30分钟,醇沉,浓缩,提取,离心,静置24小时,过滤,浓缩,样品分层,有大量油滴析出,分散性差,常温下无法形成均一、稳定的中草药活性物@囊泡复合物。
[0171]
对比例2中改变了囊泡前驱体的添加顺序。月桂酸甘油酯与中草药提取液混合物的透射电子显微照片如图14所示,样品内提取物分散性差,聚集严重,说明囊泡前驱体的添加顺序会影响中草药提取物的溶解性以及分散性。
[0172]
对比例3:
[0173]
(1)分别称取何首乌10g、墨旱莲10g、沙参30g、白术30g、泽泻12g、赤芍30g、青皮12g、黄柏15g、黄精30g、制首乌30g、绞股蓝30g、侧柏叶30g、川芎12g、天麻12g、乌梅炭10g、地肤子10g、红车轴草25g、阿胶35g混合后并粉碎至粉末状态。
[0174]
(2)将操作(1)中药材粉末置于提取罐内,加入650ml三次水和800ml乙醇,浸泡30分钟,醇沉,浓缩,提取,得到中草药提取物。其中提取的次数为4次,每次所述提取的时间为4小时,提取的温度为70℃。
[0175]
(3)将操作(2)得到的中草药提取物中,加入5gtween 80,涡旋搅拌,离心,静置24小时,过滤,浓缩,样品中未发现球状囊泡结构,聚集严重,48小时后出现分层,常温下无法形成均一、稳定的中草药活性物@囊泡复合物。
[0176]
对比例3中的囊泡前驱体为tween 80,其与中草药活性物的混合物的透射电子显微照片如图15所示。tween 80在中草药提取物中无法形成囊泡结构,且提取物聚集严重,分散性较差,活性成分无法被包封和释放。
[0177]
对比例4:
[0178]
(1)分别称取何首乌10g、墨旱莲10g、沙参30g、白术30g、泽泻12g、赤芍30g、青皮12g、黄柏15g、黄精30g、制首乌30g、绞股蓝30g、侧柏叶30g、川芎12g、天麻12g、乌梅炭10g、地肤子10g、红车轴草25g、阿胶35g混合后并粉碎至粉末状态。
[0179]
(2)将操作(1)中药材粉末置于提取罐内,加入650ml三次水和800ml乙醇,浸泡30分钟,醇沉,浓缩,提取,得到中草药提取物。其中提取的次数为4次,每次所述提取的时间为
4小时,提取的温度为70℃。
[0180]
(3)将操作(2)得到的中草药提取物中,加入0.4g硬脂酸甘油酯,涡旋搅拌,离心,静置24小时,过滤,浓缩,样品分散性差,未发现囊泡结构,聚集严重,30分钟后出现分层,常温下无法形成均一、稳定的中草药活性物@囊泡复合物。
[0181]
对比例4中草药活性物与硬脂酸甘油酯混合物的透射电子显微照片如图16所示。混合样品中仅观测到油滴状物,说明硬脂酸甘油酯在中草药提取物中无法形成囊泡结构,体系溶解性以及分散性较差,活性成分无法被包封和释放。
[0182]
对比例5:
[0183]
(1)分别称取何首乌10g、墨旱莲10g、沙参30g、白术30g、泽泻12g、赤芍30g、青皮12g、黄柏15g、黄精30g、制首乌30g、绞股蓝30g、侧柏叶30g、川芎12g、天麻12g、乌梅炭10g、地肤子10g、红车轴草25g、阿胶35g混合后并粉碎至粉末状态。
[0184]
(2)将操作(1)中药材粉末置于提取罐内,加入650ml三次水和800ml乙醇,浸泡30分钟,醇沉,浓缩,提取,得到中草药提取物。其中提取的次数为4次,每次所述提取的时间为4小时,提取的温度为70℃。
[0185]
(3)将操作(2)得到的中草药提取物中,加入1g peo
77-ppo
29-peo
77
,涡旋搅拌,离心,静置24小时,过滤,浓缩,样品分散性差,未发现球状囊泡结构,24小时后出现分层,常温下无法形成均一、稳定的中草药活性物@囊泡复合物。
[0186]
对比例5中草药活性物与peo
77-ppo
29-peo
77
(1g/l)混合物透射电子显微照片如图17所示。囊泡前驱体peo
77-ppo
29-peo
77
在浓度过低时,在中草药提取物体系内无法形成囊泡,样品溶解性以及分散性较差,活性成分无法被包封和释放。
[0187]
对比例6:
[0188]
(1)分别称取何首乌10g、墨旱莲10g、沙参30g、白术30g、泽泻12g、赤芍30g、青皮12g、黄柏15g、黄精30g、制首乌30g、绞股蓝30g、侧柏叶30g、川芎12g、天麻12g、乌梅炭10g、地肤子10g、红车轴草25g、阿胶35g混合后并粉碎至粉末状态。
[0189]
(2)将操作(1)中药材粉末置于提取罐内,加入650ml三次水和800ml乙醇,浸泡30分钟,醇沉,浓缩,提取,得到中草药提取物。其中提取的次数为4次,每次所述提取的时间为4小时,提取的温度为70℃。
[0190]
(4)将操作(2)得到的中草药提取物中,加入25gpeo
13-ppo
30-peo
13
,涡旋搅拌,离心,静置24小时,过滤,浓缩,样品分散性差,未发现球状囊泡结构,常温下无法形成均一、稳定的中草药活性物@囊泡复合物。
[0191]
对比例6中草药活性物与peo
13-ppo
30-peo
13
(25g/l)混合物的透射电子显微照片如图18所示。当囊泡前驱体peo
13-ppo
30-peo
13
在浓度过高时,在该体系内无法形成囊泡,混合样品的溶解性以及分散性较差,聚结严重,活性成分无法被包封和释放。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。