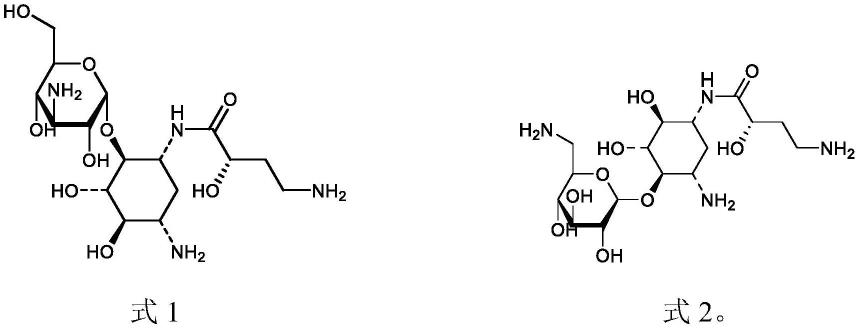
no:1-6所示序列之一至少70%、至少80%、至少90%、至少95%或100%相同的向导序列。
12.在又一方面,本公开涉及治疗、预防、抑制和/或减轻受试者中与rna病毒的感染、增殖和/或复制相关或由其引起的疾病的方法,其包括向需要其的受试者施用包含以下的分子系统:(a)rna引导性rna靶向效应蛋白和/或编码所述效应蛋白的多核酸,和(b)一种或更多种grna和/或编码一种或更多种grna的一种或更多种多核酸;其中所述一种或更多种grna中的每一种包含与seq id no:1-6所示序列之一至少70%、至少80%、至少90%、至少95%或100%相同的向导序列。
13.在另一方面,本公开涉及治疗、预防、抑制和/或减轻受试者中与rna病毒的感染、增殖和/或复制相关或由其引起的疾病的方法,其包括向需要其的受试者施用包含以下的分子系统:(a)rna引导性rna靶向效应蛋白和/或编码所述效应蛋白的多核酸,和(b)至少4个不同grna的集合和/或一种或更多种编码所述grna集合的多核酸;其中所述集合中至少4个grna包含与seq id no:1-6所示序列之一至少70%、至少80%、至少90%、至少95%或100%相同的向导序列。
14.在一方面,本公开涉及编码本文所公开的分子系统的多核苷酸。
15.在另一方面,本公开涉及编码一种或更多种grna的载体,其中由所述载体编码的一种或更多种grna包含与seq id no:1-6所示序列之一至少70%、至少80%、至少90%、至少95%或100%相同的向导序列。
16.在又一方面,本公开涉及编码本文所公开的分子系统的载体。
17.在一方面,本公开涉及包含本文所公开的多核苷酸和/或本文所公开的载体的组合物。
18.在又一方面,本公开涉及治疗、预防、抑制和/或减轻受试者中与肠病毒属(enterovirus genus)病毒的发病机制、感染、增殖和/或复制相关或由其引起的疾病的方法,其包括向需要其的受试者施用本文公开的多核苷酸和/或本文公开的载体和/或本文公开的组合物。
19.在一方面,本公开涉及向导rna分子(grna),其包括与seq id no:1-6所示序列之一至少70%、至少80%、至少90%、至少95%或100%相同的向导序列。
20.在另一方面,本公开涉及向导rna分子,其包含如seq no:1-6中任一个所示的向导序列。
21.附图简要说明
22.当结合非限制性实例和附图考虑详细描述时,参考该详细描述将更好地理解本发明,其中
23.图1显示了一副示意图,其显示用于aav包装crispr-casrx的质粒,即pzac2.1-cmv-casrx-3xha-polya-u6-grna质粒的设计和构建。在itr序列之间,有一个驱动casrx序列表达的cmv启动子,且在casrx序列的末端有一个3xha标签,接着是兔聚腺苷酸化序列。其后是驱动插入的向导序列转录的u6启动子,接着是另一个itr序列。利用bbsi限制性内切酶消化可以将向导序列克隆到该骨架上。全质粒序列和用于克隆质粒的引物如表1所示。
24.图2显示了验证实验的结果,其显示了casrx在aav-casrx转导的人细胞中的表达。为了验证包装的病毒能够转导哺乳动物细胞并表达casrx载货,以moi 100k对1x105人永生化角膜内皮细胞b4g12进行转导,并铺板于48孔板。进行1:200抗ha染色2小时,1:1500抗gfp
染色2小时。进行1:1000二抗染色2小时。对于亮场和488通道,拍摄曝光15毫秒时的图像,增益设置为6400;对于dapi通道,曝光设置为800us,增益设置为6400。结果表明,aavdj-egfp能够转导b4g12细胞,与无转导对照相比,检测到egfp的特异性信号(图2,分别为第1行和第2行)。结果也证实了casrx-3xha蛋白在aavdj-cmv-casrx转导的人b4g12细胞中的表达(图2,第三行),如无感染对照中的低背景信号所表明的(图2,第四行),一抗和二抗的信号都是特异性的。
25.图3显示了针对gfp基因序列设计的向导的位置比对。针对靶gfp基因序列在近5'端设计了两种rna向导,其逻辑是,由于蛋白质翻译从5’端开始,在较靠前的碱基上切割会更有效地终止翻译(图3)。使用这些向导进行gfp敲低,以验证casrx的rna切割活性。用于向导克隆的引物如表1所示。gfp向导1序列
–
(seq id no:7);gfp向导2序列
–
(seq id no:8)。
26.图4显示了针对ev71 3d蛋白基因序列设计的向导的位置比对。使用benchling-clustal omega比对和lasergene seqman pro 15(dnastar),基于对来自六种ev71毒株(h8-1、s41、sin002209、mz、nj2017iso2、shenzhen001-2006)的比对的高度保守区域(>85%相似性),设计了六种针对靶标ev71 3dpro基因序列的rna向导。针对毒株41的3dpro基因序列的向导序列和位置如上述图所示。用于克隆向导的引物如表1所示。比对如图10-12所示。ev71_3d向导1序列
–
(seq id no:1);ev71_3d向导2序列
–
(seq id no:2);ev71_3d向导3序列
–
(seq id no:3);ev71_3d向导4序列
–
(seq id no:4);ev71_3d向导5序列
–
(seq id no:5);ev71_3d向导6序列
–
(seq id no:6)。
27.图5显示了aav血清型的生物筛选以鉴定有效转导人横纹肌肉瘤(rd)细胞的aav的结果。人类骨骼肌被认为是支持ev71持续感染和复制的靶器官。使用人横纹肌肉瘤(rd)细胞系(atcc)进行了aav小组生物筛选实验,以确定最合适的可有效地转导人肌肉细胞以递送用于病毒rna靶向的crispr-cas工具的aav血清型。将10k细胞铺板到96孔板的每个孔中,用100k moi的每种aav血清型转导,并在转导后72小时定量gfp蛋白的表达。实验重复两次进行。结果表明,aav1、aav2和aavdj可以比测试的其他aav血清型更有效地转导人横纹肌肉瘤(rd)细胞,按照效率增加的顺序,分别为aav1、aavdj和aav2。
28.图6显示了验证在aav-casrx-gfp向导转导的人横纹肌肉瘤(rd)细胞中gfp表达敲低的结果。用moi 10k的aav2-gfp转导人肌肉永生细胞系rd以表达gfp。通过用moi 100k(左图)和moi 1000k(右图)的携带向导的aav2-casrx转导表达gfp的横纹肌肉瘤(rd)细胞来测试单独向导1、单独向导2和向导1 向导2的gfp敲低效率。结果表明,存在单种向导对gfp的敲低,但通过合并两种向导提高了敲低效率。使用prism 8软件,通过学生t检验(双尾)分析两组之间的比较。*p<0.05。
29.图7显示了在aav-casrx-ev71_3d向导转导的感染ev71的人横纹肌肉瘤(rd)细胞中ev71复制被抑制的结果。aav-crispr-casrx-ev71_3d向导抑制ev71病毒复制的能力的概念验证实验。在96孔板中,将10x103横纹肌肉瘤(rd)细胞接种在每个孔中,并用无向导的
aavdj-egfp或携带gfp向导2或ev71向导的aaavdj-casrx转导72小时,然后在moi为1的条件下进行ev71感染12小时,然后收获上清液进行病毒空斑测定。空斑测定计数的结果表明,单种向导在moi 100k时几乎没有抑制作用,但将这些向导(六种向导)合并在一起在aav moi为100k时可以对ev71复制产生高达3个对数级的病毒滴度降低的强烈抑制作用。使用无向导的对照或gfp向导也表明抑制作用是ev71向导特异性的。使用prism 8软件,通过学生t检验(双尾)分析两组(casrx-egfpg2和casrx-ev71_3d向导)之间的比较。*p<0.05。
30.图8显示了在用不同数量的casrx ev71 3dpro基因靶向向导转导的感染ev71的人横纹肌肉瘤(rd)细胞中ev71复制被抑制的结果。aav-crispr-casrx-ev71_3d向导抑制ev71病毒复制的能力的概念验证实验。在96孔板中,将10x103横纹肌肉瘤(rd)细胞接种在每个孔中,并用无向导的aav2-egfp或携带gfp向导2或ev71向导的aav2-casrx转导72小时,然后在moi为1的条件下进行ev71感染12小时,收获上清液用于病毒空斑测定。空斑测定计数的结果表明,全部六种单独向导在moi 1000k时具有高达1个对数病毒滴度降低的强烈抑制作用,但是逐渐将这些向导合并在一起可以对ev71复制产生渐增的抑制作用,对于6个向导的集,在1000k的aav2 moi下,病毒滴度降低高达4个对数级。在4种、5种和6种向导的集中,抑制效果的指数增加更强,这表明,临界(critical)数量的向导靶标或所述集中向导之间的协同作用对于获得更高的抑制效力是重要的。使用无向导的对照或gfp向导2也表明抑制作用是ev71向导特异性的。使用prism 8软件,通过学生t检验(双尾)分析两组(casrx-egfpg2和casrx-ev71_3d向导)之间的比较。*p<0.05。
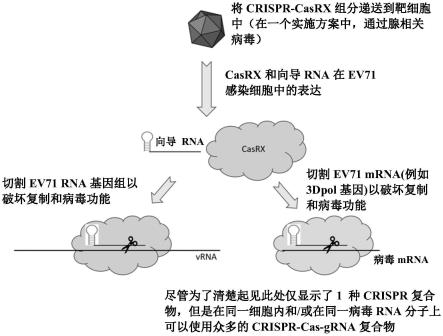
31.图9基于ev71 rna实例显示了本文所公开技术的示意图。第一步,将crispr-casrx组分递送到靶细胞中(在一个实施方案中,通过腺相关病毒),导致casrx和向导rna在感染ev71的细胞中表达。下一步,向导rna与casrx的组合导致诸如ev71 rna基因组的切割以破坏复制和病毒功能,以及导致诸如ev71 mrna(例如3dpol基因)的切割以破坏复制和病毒功能。请注意,尽管为了清楚起见此处仅显示了一种示例性crispr复合物,但是可以在同一细胞内和/或在同一病毒rna分子上使用众多的crispr-cas-grna复合物。
32.图10显示了毒株h8-1与其他肠病毒株的序列比对。图10所示的序列见表1。
33.图11显示了lc126150、cau05876和未命名共有序列的序列比对。图11所示的序列存在于表1中。
34.图12显示了埃可病毒(副肠孤病毒)株的共有序列与其他埃可病毒(副肠孤病毒)序列的序列比对。图12所示的序列存在于表1中。
35.定义
36.如本文所用,术语“生物筛选”指在不同aav血清型的较大文库中鉴定或选择表现最佳的aav血清型。
37.如本文所用,术语“rna引导性rna靶向效应蛋白”是指能够与向导rna或grna形成rna靶向复合物的蛋白,所述复合物能够与一种或更多种rna靶分子结合并实现其变化。rna靶标上实现的变化是指rna分子组分或结构的任何化学或物理变化,其可包括但不限于:破坏/切割多核苷酸,替换一个或更多个核苷酸碱基,和插入或删除一个或更多个核苷酸碱基。在一个实例中,rna引导性rna靶向效应蛋白是cas蛋白。在另一个实例中,cas蛋白是cas核酸酶。
38.术语“向导rna”或“grna”是指包含与靶rna序列充分互补的序列(向导序列)以与
靶rna序列杂交,并指导rna靶向复合物与靶rna序列的序列特异性结合的rna分子。在一些实施方案中,当使用合适的比对算法进行最佳比对时,向导序列(在向导rna内)和其对应的靶rna序列之间的互补程度为约60%或大于约60%、70%、80%、85%、90%、95%、97.5%、99%或100%。
39.如本文所用,术语“crispr-cas”是指基于成簇的规律间隔的回文重复序列(crispr)和例如crispr相关蛋白核酸酶的能力的基因组编辑技术,以诱导诸如双链(ds)dna在与整合到crispr-cas复合物/系统中的合成向导rna(sgrna)序列互补的特定位置断裂。这允许基因和/或其他基因组元件的删除、添加和/或修饰,例如但不限于转录元件、启动子、启动子增强子、转录增强子,限制性位点、突变、选择标记,例如抗生素选择盒等。这种核酸酶可以从例如化脓性链球菌(streptococcus pyogenes)中分离(在cas9的情况下)。
40.crispr(成簇的规律间隔的短回文重复序列)和crispr相关(cas)基因的功能对于选择的细菌和古细菌的适应性免疫至关重要,使这些生物体能够对入侵的遗传物质作出反应并消除。迄今为止,已经鉴定了三种类型的crispr机制,其中ⅱ型是研究最多的。此外,还开发了crispr的其他组合,例如crispr-cpf1。本文还考虑crispr技术的用途,其中所述cas蛋白或功能类似蛋白不是从化脓性链球菌(s.pyogenes)中分离的。cas蛋白的实例是但不限于cas核酸酶(例如cas9和cas13蛋白),或从化脓性链球菌(s.pyogenes)、金黄色葡萄球菌(staphylococcus aureus)或古细菌界的任一代表分离的具有相同功能的蛋白。cas9蛋白也可以被所谓的casx和casy蛋白取代。在另一个实例中,cpf1蛋白或具有相同功能的蛋白质的实例分离自但不限于氨基酸球菌属的种(acidaminococcus sp.)和毛螺菌科(lachnospiraceae)。在适应性免疫方面,crispr-cas介导的防御机制如下:将来自病毒或质粒的入侵dna切割成小片段,并在一系列短重复序列(约20个碱基对)中掺入crispr基因座。对基因座进行转录,然后转录物被处理以生成小rna(crrna
–
crispr rna;在体外环境中也称为合成的向导rna(sgrna)),基于序列互补其引导效应核酸内切酶靶向入侵的dna。在基因编辑方面,crispr-cas系统根据相同的原理工作,sgrna将效应核酸酶引导到dna的所需部分,在这些部分中进行切除。
41.本文所用的术语“载体”是指包含多核苷酸或与多核苷酸缔合的大分子或生物大分子缔合物,其可用于介导多核苷酸向细胞的递送。示例性载体包括例如质粒、病毒载体(病毒或其病毒基因组)、脂质体和其他基因递送媒介物。
42.如本文所用,术语“aav”是指腺相关病毒。术语aav可用于指病毒本身或其衍生物,例如但不限于病毒衣壳、病毒基因组、病毒颗粒、病毒片段及其组合。术语“aav”包括所有天然存在和重组形式的亚型及其变体,另有要求除外。天然存在形式的aav是指任何腺相关病毒或其衍生物,其包含由天然存在的病毒衣壳蛋白组成的病毒衣壳。天然存在的aav的非限制性实例包括aav 1型(aav-1)、aav 2型(aav-2)、aav 3型(aav-3)、aav 4型(aav-4)、aav 5型(aav-5)、aav 6型(aav2-6)、aav 7型(aav1-7)、aav 8型(aav6-8)、aav9、aav10、aav11、aav12、aav13、rh10、禽aav、牛aav、犬aav、马aav、灵长类aav、非灵长类aav和绵羊aav。“灵长类aav”是指感染灵长类动物的aav,“非灵长类aav”是指感染非灵长类哺乳动物的aav,“牛aav”是指感染牛哺乳动物的aav等。“重组aav”或“raav”包括在其病毒基因组中包含异源多核苷酸序列的任何aav。可用作载体的aav血清型和变体的其他实例包括但不限于aavdj、aav-php.s、aav-php.b、aav-php.eb和anc80。
43.如本文所用,术语“肠病毒71”(ev71),又称肠病毒a71(ev-a71),是指小核糖核酸病毒科(picornaviridae)肠病毒属的病毒,以在儿童中引起严重神经系统疾病和手足口病(hfmd)的流行而闻名。还据报道,肠病毒71很少引起脊髓灰质炎样综合征永久性瘫痪。
44.如本文所用,术语“柯萨奇病毒”是指属于无包膜、线性、正义单链rna病毒的小核糖核酸病毒科的少数相关肠病毒,以及其肠病毒属,其也包括脊髓灰质炎病毒和埃可病毒。肠病毒是最常见的人类病原体之一。通常,其成员通过粪-口途径传播。柯萨奇病毒与脊髓灰质炎病毒有许多共同特征。还已知柯萨奇病毒与埃可病毒和腮腺炎病毒一样,也是引起无菌性脑膜炎的主要病因。
45.如本文所用,术语“副肠孤病毒”,也称为“埃可病毒”,是指与人类肠病相关的多系群病毒。该名称源自“致肠细胞病变人孤儿病毒”。这些病毒最初与疾病无关,但许多后来被鉴定为致病因子。术语“埃可病毒”用于许多物种的学名。因此,术语“埃可病毒”已被术语“副肠孤病毒”取代,以表示属于小核糖核酸病毒科这一亚种的病毒,而以前被认为是埃可病毒的其他病毒已被重新分配到其他物种,但也属于小核糖核酸病毒科然而,现在所有的埃可病毒都被认为是不同物种的毒株,即使不是全部,其大部分属于小核糖核酸病毒科。值得注意的是,术语“埃可病毒”和“副肠孤病毒”在本文中可互换使用。副肠孤病毒的实例是但不限于副肠孤病毒a、副肠孤病毒b、副肠孤病毒c、副肠孤病毒d、副肠孤病毒e和副肠孤病毒f。
46.如本文所用,术语“手足口病”(hfmd)是指通常由柯萨奇病毒a16、肠病毒71或其他肠病毒引起的发热性疾病。感染导致手、足和口腔黏膜上的小疱疹。由柯萨奇病毒a6引起的非典型hfmd通常引起高热伴丘疹性病变,其进展为广泛分布于全身的水疱大疱性病变和大疱。引起hfmd的病毒属于小核糖核酸病毒科(picornaviridae family),柯萨奇病毒a16是hfmd最常见的病因。肠病毒71(ev-71)是第二常见的病因。许多其他柯萨奇病毒和肠病毒毒株也可能是病因。
47.如本文所用,术语“转导”或“转导的”是指载体介导的基因转移过程,其通常用于描述细菌和/或病毒介导的方法。
48.发明详细描述
49.肠病毒71、柯萨奇cav16和cav6以及副肠孤病毒属于小核糖核酸病毒科的病毒,根据定义,其由非包膜、正义、单链rna病毒组成。这些病毒因其在幼儿中表现为手足口病(hfmd)而被熟知,表现为口腔中可见的水泡或病变,且偶尔在手掌和脚底出现病变或水泡。在更严重的情况下,手足口病也会出现更严重的症状,例如但不限于瘫痪、无菌性脑膜炎和脑炎或甚至死亡。
50.目前尚无能够预防或治疗本文所公开疾病的商业性疫苗或治疗剂。公共卫生机构采取的唯一措施是保持良好的个人卫生和隔离感染者。
51.因此,本文公开了治疗、预防、抑制和/或减轻受试者中与肠病毒属病毒的发病机制、感染、增殖和/或复制相关或由其引起的疾病的方法。在另一个实例中,本文公开的方法包括向需要其的受试者施用本文公开的多核苷酸和/或本文公开的载体和/或本文公开的组合物。
52.crispr-cas自身呈现为抗病毒治疗剂开发的替代品。crispr代表成簇的规律间隔的短回文重复序列,且最早发现于细菌免疫系统。然而,直到2012年才发现crispr-cas系统
在真核生物中具有精确编辑dna的能力。在crispr出现之前,自用于治疗乳腺癌的抗her2人源化单克隆抗体赫赛汀的成功案例以来,研究工作主要集中在开发靶向中和表位的人源化单克隆抗体作为抗病毒剂。对化合物或小分子的候选名单进行传统药物筛选也是治疗剂开发的常用方法;然而,这些筛选方法通常对病毒复制具有抑制作用。尽管进行了药物筛选和单克隆抗体研究,但目前还没有正在进行的前瞻性临床试验,也没有任何用于hfmd治疗的商业化治疗剂。
53.crispr-cas的用途受到体内有效递送系统的限制,且目前fda批准的药物基于腺被认为对人类应用是安全的相关病毒(aav)递送,因为它不会引发急性炎症免疫反应。然而,腺相关病毒的最大载货量约为4.7千碱基对(kbp),这不足以递送大多数已知的cas酶,因为这些酶通常超过规定的限制所指出的限值,特别是在克隆到哺乳动物启动子序列中后。
54.因此,本文公开的分子系统可以包括由编码所述效应蛋白的多核酸或由其编码,和/或编码所述grna的一种或更多种多核酸被包含在一种或更多种载体中。如本文所用,术语“载体”指用于将编码信息转移到宿主细胞中的任何分子(例如但不限于核酸、质粒或病毒)。
55.如在本领域中使用的,病毒载体是用于将遗传物质递送到细胞中的工具。这个过程可以在活体(体内)或细胞培养(体外)中进行。具体来说,病毒已经进化出专门的分子机制,以有效地运输它们的基因组到它们感染的细胞内。通过载体递送基因或其他遗传物质被称为转导,被感染的细胞被称为被转导的。除了用于分子生物学研究外,病毒载体还用于基因治疗和疫苗开发。
56.因此,在一个实例中,载体是病毒载体。在另一个实例中,病毒载体是但不限于腺病毒载体、腺相关病毒(aav)载体、慢病毒载体或逆转录病毒载体。
57.以本公开申请中使用的载体为例,腺相关病毒(aav)是感染人类和一些其他灵长类物种的小病毒。目前尚不知道腺相关病毒会导致疾病,而且在感染时,已经证明仅会引起轻微免疫反应。腺相关病毒能够感染分裂细胞和非分裂细胞,并可将其基因组并入宿主细胞的基因组。此外,腺相关病毒大多保持游离状态(也就是说,它可以在宿主体内复制,而不会将其有效载荷并入到宿主染色体中);进行长时间稳定的表达。这些特征使腺相关病毒成为创建用于基因治疗的病毒载体的合适候选物。因此,在一个实例中,病毒载体是腺相关病毒(aav)载体。在另一个实例中,腺相关病毒(aav)载体是但不限于aav 1型(aav-1)、aav 2型(aav-2)、aav 3型(aav-3)、aav 4型(aav-4)、aav 5型(aav-5)、aav 6型(aav-6)、aav 7型(aav-7)、aav 8型(aav-8)、aav9、aav10、aav11、aav12、aav13、rh10、aavdj、aav-php.s、aav-php.b、aav-php.eb和anc80。在一个实例中,腺相关病毒(aav)载体是aav2或aavdj或aav1载体。
58.在一个实例中,公开了编码一种或更多种本文公开的grna的载体。在这样的实例中,由所述载体编码的一种或更多种grna包含与seq id no:1-6所示序列之一至少70%、至少80%、至少90%、至少95%或100%相同的向导序列。在另一个实例中,载体编码至少4种不同grna,其中所述grna的每一种包含seq id no:1-6所示的向导序列。在又一个实例中,载体编码至少6种不同grna,其中所述grna的每一种包含seq id no:1-6所示的向导序列。
59.本文进一步公开了编码本文公开的分子系统的多核苷酸,以及编码本文公开的分
子系统或组合物的所需组分的多核苷酸。
60.利用生物信息学挖掘cas酶,之前已发现casrx(最小的vi型crispr-cas酶)具有高的rna引导性rna靶向活性。在一个实例中,本文使用的crispr-cas模式属于cas家族vi-d型,其是rna引导性rna靶向的cas模式。这使得crispr-cas系统能够通过腺相关病毒(aav)递送系统被递送到体内的哺乳动物细胞中,这反过来允许rna靶向(外源)病毒rna基因组以进行切割。
61.因此,在一个实例中,rna引导性rna靶向效应蛋白是rna引导性rna靶向cas蛋白或其经修饰的变体。在另一个实例中,本文公开的方法或分子系统包含rna引导性rna靶向效应蛋白,其中rna引导性rna靶向效应蛋白是rna引导性rna靶向cas蛋白,或其经修饰的变体。
62.关于crispr-cas技术的安全性,已证明这些技术在诸如基因治疗和crispr-cas治疗中的使用是安全的。这也是crispr-cas技术与本领域已知的其他基因编辑方法相比具有更高特异性的结果。值得注意的是,本公开中使用的由iv型crispr-cas产生的任何rna编辑不是永久性的,且一旦外源dna降解或细胞分裂后将终止。crispr-cas治疗剂的高度特异性活性也将避免来自药物化合物或小分子使用的常见“副作用”问题,或如抗体疗法中所见的抗体依赖性增强(ade)或抗体依赖性细胞细胞毒性(adcc)问题。
63.值得注意的是,在本领域中,尚未发现能够精确靶向病原体基因组物质进行破坏的治疗药物。crispr-cas在抗病毒治疗剂中的应用显示其通过直接分解病毒本身来消除病毒复制的效果。由于直接靶向机制,这些治疗剂不依赖于免疫系统来帮助消除病毒,且因此可以同等效力地用于免疫受损患者或免疫力较弱的年轻和和年老患者。
64.本文公开的向导rna(grna)基于高度保守的区域,该区域在六种肠病毒71(ev71)株之间具有至少85%序列同一性的相似性(图4)。本文公开的向导rna能够靶向多种毒株。这种序列保守性进一步意味着,这些序列对病毒而言是功能上重要的。在不受理论约束的情况下,认为保守性较低的序列意味着病毒株能够在那些位点(保守性较低的位点)发生突变,从而逃避crispr靶向。因此,本文公开的(分子)系统、组合物和组合物的用途靶向流行致病株的保守区域。具体而言,在一个实例中,所选择的靶标是功能上重要的聚合酶3d基因。
65.因此,本文公开了基于能够靶向rna的crispr-cas系统的分子系统。这种分子系统包含,例如,(a)rna引导性rna靶向效应蛋白和(b)一种或更多种向导rna分子(grna)。本领域技术人员应理解,向导rna可以根据分子系统要影响的rna靶标进行定制和裁剪。
66.在一个实例中,本文所公开的分子系统用于治疗与rna病毒的感染、增殖和/或复制相关或由其引起的疾病。
67.本文还公开了具有确定序列的特异性向导rna(grna),其已被经验性地证实具有抗病毒活性。在一个实例中,向导株是如本文所公开的。
68.术语“序列同一性”是指两个多核苷酸或氨基酸序列在比较窗口上是相同的(即,在逐个核苷酸或逐个残基的基础上)。术语“序列同一性百分比”是通过在比较窗口上比较两个最佳比对的序列来计算的,确定在两个序列中相同的核酸碱基(例如,a、t、c、g、u或i)或残基出现的位置的数量,从而得到匹配位置的数量,将匹配位置的数量除以比较窗口中的位置总数(即窗口大小),并将结果乘以100得到序列同一性的百分比。如本文所用,术语“可观同一性(substantial identity)”表示多核苷酸或氨基酸序列的特征,其中所述多核苷酸或氨基酸包含在至少18个核苷酸(6个氨基酸)位置的比较窗口上,通常在至少24-48个核苷酸(8-16个氨基酸)位置的窗口上,与参考序列相比具有至少85%序列同一性、优选至少90%至95%序列同一性、更通常至少99%序列同一性的序列,其中序列同一性的百分比是通过将参考序列与可能包括缺失或添加的序列(在比较窗口内总计为参考序列的20%或更少)进行比较来计算。参考序列可以是更大序列的子集。
69.因此,本文还公开了向导rna分子(grna),其包含与本文所述的任何一个序列至少70%、至少71%、至少72%、至少73%、至少74%、至少75%、至少76%、至少77%、至少78%、至少79%、至少80%、至少81%、至少82%、至少83%、至少84%、至少85%、至少86%、至少87%、至少88%、至少89%、至少90%、至少91%、至少92%、至少93%、至少94%、至少95%、至少96%、至少97%、至少98%、至少99%或100%相同的向导序列。在一个实例中,向导rna分子的序列同一性与本文公开的seq id no 1-6相比较。本文还公开了向导rna分子,其包含如seq no:1-6中任一个所示的向导序列。
70.在另一个实例中,一种或更多种向导rna包含与seq id no:1-6所示序列之一至少70%、至少80%、至少90%、至少95%或100%相同的向导序列。在另一个实例中,向导rna如seq id no 1-6所述。
71.在本公开的范围内还公开了,可以通过使用多种向导rna分子的组合或集合来靶向多种rna,其中向导rna分子数量与用户希望靶向的rna靶数量相同。
72.在一个实例中,本文公开的分子系统包含至少4种不同向导rna分子(grna)的集合。该向导rna的集合能够靶向病毒rna上的相同或不同靶标,其中靶标由向导rna的序列定义。在一个实例中,所述集合中至少4种grna包含与seq id no:1-6所示序列之一至少70%、至少80%、至少90%至少95%或100%相同的向导序列。在另一个实例中,该集合包含至少4种本文所公开的grna,其中所述grna包含与seq id no:1-4所示序列之一至少70%、至少80%、至少90%至少95%或100%相同的向导序列。在另一个实例中,本文所公开集合包含至少6种不同的grna,其中所述集合中的6种grna包含与seq id no:1-6所示序列之一至少70%、至少80%、至少90%、至少95%或100%相同的向导序列。
73.本公开描述了靶向和消除外源rna(例如rna病毒)的技术和策略,其使用经编程以直接切割外源rna(例如rna病毒基因组)的vi型crispr-cas系统。
74.本文还公开了本文所述的(分子)系统、组合物和组合物中和病毒感染的用途。此外,本文所述(分子)系统、组合物和组合物的用途还可用于减少病毒复制,从而降低受试者中的病毒滴度。
75.应当理解,感染病毒的受试者可能不一定表现出已知该病毒引起的疾病的症状。这类受试者被称为病毒携带者,且通常无症状。在这种受试者中,本文所述(分子)系统、组合物和组合物的用途用于降低病毒滴度或抑制病毒复制,从而防止受试者出现疾病症状。
76.本文还公开了本文所述(分子)系统、组合物以及组合物用于治疗和/或预防手足口病(hfmd)的用途。本文还公开了所公开的组合物和分子系统减少受试者中病毒rna量的用途。这种病毒rna可以是但不限于引起手足口病(hfmd)的病毒。在一个实例中,引起手足口病(hfmd)的病毒是但不限于肠病毒71(如ev71)、柯萨奇病毒(如cav16和cav6)、副肠孤病毒(以前称为埃可病毒,包括但不限于副肠孤病毒a、副肠孤病毒b、副肠孤病毒c、副肠孤病
毒d、副肠孤病毒e和副肠孤病毒f)及其组合。
77.通过使用本文公开的crispr-cas系统切割病毒rna基因组使病毒基因组失活。在另一个实例中,cas蛋白或核酸酶是cas13或cas13d。在一个实例中,cas13d核酸酶是从黄瘤胃球菌(ruminococcus flavefaciens)中分离的(casrx)。在另一个实例中,cas13d是黄瘤胃球菌的cas13d直系同源物。vi型crispr-cas系统仅靶向rna病毒基因组,而没有针对宿主dna基因组的不良活性风险。
78.因此,基于本文的公开内容,在一个实例中,其中rna引导性rna靶向效应蛋白是rna引导性rna靶向cas蛋白或其经修饰的变体。在另一个实例中,cas蛋白是但不限于cas13a、cas13b、cas13c和cas13d蛋白。
79.应注意,在本公开的上下文中,所要求保护的系统以cas9作为核酸酶将不能发挥预期的功能,因为cas9是dna靶向模式。本文公开的应用需要rna靶向核酸酶以直接靶向和切割病毒基因组。相反,dna病毒(例如,比如,疱疹病毒、痘病毒)可以被cas9靶向,但无法被cas13靶向。因此,在一个实例中,cas核酸酶是靶向rna的一种。
80.本文还公开了一组针对肠病毒71(ev71)、柯萨奇病毒和副肠孤病毒(埃可病毒)病毒基因组的向导rna(grna)。已证明在所要求保护的系统中使用这些向导rna可消除靶病毒。这已通过与单独使用时不显示抗病毒活性的单种grna相比,感染细胞中病毒滴度的1000倍以上的降低被证实。图7显示了感染细胞中病毒滴度降低的示例性数据,显示了基于肠病毒71(ev71)实例的数据。
81.在一个实例中,本文所公开的分子系统包含cas蛋白,其中所述cas蛋白是casrx;并且集合包含6种不同的向导rna分子(grna),其中集合中所包含的每一种grna是seq id no:1-6所示的向导序列。
82.本公开还描述了既起预防作用,(也就是说,作为预防初次感染的化合物)又起治疗作用(意味着该组合物消除或减少现有感染)的组合物。
83.在一个实例中,公开了如本文公开的用于治疗的分子系统。在另一个实例中,公开了治疗、预防、抑制和/或减轻受试者中与rna病毒的感染、增殖和/或复制相关或由其引起的疾病的方法。本文还公开了本文公开的组合物用于在疗法中使用。
84.如本文所公开的,本文所公开的治疗方法可能包括向需要其的受试者施用包含以下的分子系统:(a)rna引导性rna靶向效应蛋白和/或编码所述效应蛋白的多核酸,和(b)一种或更多种grna和/或编码所述一种或更多种grna的一种或更多种多核酸;其中一种或更多种grna中的每一种包含与seq id no:1-6所示序列之一至少70%、至少80%、至少90%、至少95%或100%相同的向导序列。在另一个实例中,本文所公开的治疗方法可包括向需要其的受试者施用包含以下的分子系统:(a)rna引导性rna靶向效应蛋白和/或编码所述效应蛋白的多核酸,和(b)至少4种不同grna的集合和/或一种或更多种编码所述grna集合的多核酸;其中所述集合中至少4种grna包含与seq id no:1-6所示序列之一至少70%、至少80%、至少90%、至少95%或100%相同的向导序列。
85.本公开还包括以下任一项在制造用于治疗本文所公开疾病的药物中的用途,以下为本文公开的分子系统、载体、组合物或向导rna分子,或其组合。
86.在本说明书的上下文中,术语“治疗”指以任何方式纠正疾病状态或症状、预防疾病形成或以其他方式预防、阻碍、延缓或逆转疾病进展或其他不良症状的任何应用和所有
应用。
87.因此,本文还公开了包含本文公开的多核苷酸和/或本文公开的载体的组合物。本文公开的这种组合物在其范围内包括药学上可接受的组合物。因此,药物组合物适用于在本文公开的治疗方法中使用,也适用于在制造本文公开的药物中使用。
88.在一个实例中,本文公开的这一类组合物还包含rna引导性rna靶向效应蛋白。这种向导效应蛋白可以选自本文公开的rna靶向效应蛋白,例如但不限于cas13a、cas13b、cas13c和cas13d。
89.在本说明书的上下文中,术语“治疗有效量”和“诊断有效量”在其含义内包括本发明的化合物或组合物足以提供期望的治疗或诊断效果但无毒的量。所需的确切量将因受试者而异,取决于诸如被治疗的物种、受试者的年龄和一般状况、所治疗病症的严重程度、所施用的特定剂、施用模式等因素。因此,无法指定确切的“有效量”。然而,对于任何给定情况,适当的“有效量”可由本领域普通技术人员仅使用常规实验来确定。
90.本文公开的数据中显示,通过直接靶向病毒rna基因组进行切割来抑制病毒(例如,本文公开的病毒)复制。
91.本文公开了dna构建体,其包含:如本领域技术人员所理解的在哺乳动物细胞中驱动转基因表达的启动子;存在于启动子下游的编码rna引导性rna靶向蛋白的转基因,使得转基因在哺乳动物细胞内表达为其编码的转录物和蛋白质;所述转基因下游的终止转录的如本领域普通技术人员所理解的polya序列。在一个实例中,rna引导性rna靶向蛋白是vi型crispr cas。在另一个实例中,cas核酸酶是cas13。在又另一个实例中,cas核酸酶是来自黄瘤胃球菌的cas13d(casrx)。
92.本文还公开了在哺乳动物系统中驱动grna表达的第二种启动子(例如,但不限于,u6或h1启动子)。本文进一步公开了第二启动子下游的序列,其编码与表达的crispr-cas蛋白复合并将其引导至rna病毒基因组中特定rna序列的grna。在一个实例中,一种或更多种编码向导rna(grna)的序列导致一种或更多种向导rna(grna)在同一细胞内表达。这允许以一个表达构建体靶向病毒基因组内多个不相关的位点。在另一个实例中,向导rna(grna)是如表1所公开的。
93.在一个实例中,载体包含两个aav2反向末端重复序列(itr),其允许将表达的dna构建体包装到腺相关病毒(aav)颗粒中。当转导到哺乳动物细胞中时,包装的aav病毒允许cas蛋白和grna的表达。
94.本文还公开了确定grna效率的方法,以及选择针对病毒rna的grna的方法。在一个实例中,病毒rna是来自(但不限于)ev71、柯萨奇病毒和副肠孤病毒(埃可病毒)基因组的rna。在另一个实例中,本文公开的方法适用于抗病毒应用,例如但不限于治疗和预防手足口病(hfmd)。这是通过靶向例如但不限于肠病毒71的病毒基因组来实现的。在一个实例中,ev71基因组内的靶包括但不限于包括5’utr和3’utr的非编码序列和2apro、2bc、2b、2c、3ab、3a、3b(vpg)、3cdpro、3cpro、3dpol、vp1、vp2、vp3和vp4的编码序列。参考基因序列ev-a71的genbank登录号是af316321.2。
95.本公开描述了用于靶向和消除rna病毒的技术和组合物。本文公开的系统利用被编程为直接切割rna病毒基因组的vi型crispr-cas系统。其他类型的crispr-cas系统可以以类似的方式使用。此处的组合物和用途允许治疗和/或预防手足口病(hfmd);和/或通过
用本文公开的系统切割rna基因组减少受试者中的肠病毒71(ev71)、柯萨奇病毒(cav16和cav6)和副肠孤病毒(埃可病毒;副肠孤病毒a、副肠孤病毒b、副肠孤病毒c、副肠孤病毒d、副肠孤病毒e和副肠孤病毒f)、引起手足口病(hfmd)的病毒。在一个实例中,该系统包括crispr-cas13。在另一个实例中,cas13d来自黄瘤胃球菌(ruminococcus flavefaciens)(casrx)。vi型crispr-cas系统仅靶向rna病毒基因组,而没有针对宿主dna基因组的不良活性风险。
96.本文公开的技术可以通过改变向导序列应用于任何针对rna病毒的抗病毒治疗应用。
97.因此,在一个实例中,靶病毒是rna病毒。在一个实例中,rna病毒是小核糖核酸病毒科的病毒,小核糖核酸病毒科是包含感染脊椎动物(包括哺乳动物和鸟类)的相关无包膜rna病毒的病毒科。它们是代表具有30nm二十面体衣壳的小的正义单链rna病毒的大科的病毒。该科的病毒可导致一系列疾病,包括但不限于普通感冒、脊髓灰质炎、脑膜炎、肝炎和瘫痪。因此,在一个实例中,待治疗的疾病是,但不限于,脊髓灰质炎;轻度呼吸道疾病(普通感冒);手足口病(hfmd);急性出血性结膜炎;无菌性脑膜炎;心肌炎;严重的新生儿脓毒症样疾病;急性弛缓性麻痹;急性弛缓性脊髓炎;伯恩霍尔姆病;流行性胸膜炎;疱疹性咽峡炎;和慢性疲劳综合症。在一个实例中,要治疗的疾病是手足口病(hfmd)。
98.在另一个实例中,rna病毒是肠病毒属的病毒,肠病毒属是与几种人类和哺乳动物疾病相关的正义单链rna病毒属。肠病毒以其通过肠(intestine)的传播途径命名(肠的(enteric)指肠的(intestinal))。在另一个实例中,本文公开的分子系统、治疗方法、载体、向导rna分子和crispr-cas系统靶向至少一种病毒。病毒可以是但不限于肠病毒、柯萨奇病毒和副肠孤病毒。在另一个实例中,病毒可以是但不限于肠病毒71、柯萨奇病毒cav16、柯萨奇病毒cav6、副肠孤病毒a、副肠孤病毒b、副肠孤病毒c、副肠孤病毒d、副肠孤病毒e、副肠孤病毒f及其组合。
99.在本公开中还考虑使用所述技术作为筛选工具,以比较研究针对rna病毒序列的cas酶蛋白。
100.crispr-cas治疗剂提供了一类新型抗病毒治疗剂,其易于大规模制造以分销。本文显示的结果表明,通过使用crrna靶向例如ev71核酸,rna靶向rnase casrx将能够显著抑制病毒的复制。这是对aav包装的抗病毒crispr-cas工具的演示,如本文提供的数据所示,该工具基于ev71的实例显示了对rna病毒的有效作用。这种方法允许将治疗剂递送到体内系统中,例如哺乳动物或人体,以靶向整个身体的感染病毒的细胞中的病毒复制。在本文公开的向导分子的选择中,选择crrna向导以避免对人类基因组的任何可能的脱靶切除。
101.本文提供的数据还表明,这种抗病毒方法依赖于用于转导的aav治疗剂的moi,以及合并的crrna向导的动力学。这六种crrna向导的集已被鉴定为有效抑制ev71病毒复制的混合物。
102.本文说明性地描述的发明可以在没有本文未具体公开的任何一个要素或多个要素、一个限制或多个限制的情况下适当地实施。因此,例如,术语“包含/包括(comprising)”、“包括(including)”、“含有(containing)”等应扩展而不受限制地解读。此外,虽然本文中使用的术语和表达已用作描述性而非限制性的术语,并且在这些术语和表达的使用中并不意图排除所示和所描述特征的任何等价物或其部分,但是应当认识到,在
要求保护的本发明范围内,各种修改是可能的。因此,应当理解,尽管已经通过优选实施方案和可选特征具体公开了本发明,但是本领域技术人员可以对本文公开的其中所包含的发明进行修改和变化,并且这些修改和变化被认为在本发明的范围内。
103.如本技术中所使用的,单数形式“一种/个(a,an)”和“所述/该(the)”包括复数指代对象,上下文另有明确规定除外。例如,术语“遗传标记物”包括多个遗传标记物,包括其混合物和组合。
104.如本文使用的,术语“约”,在制剂成分浓度的背景中,通常是指规定值的
±
5%,更典型地是规定值的
±
4%,更典型地是规定值的
±
3%,更典型地是规定值的
±
2%,甚至更典型地是规定值的
±
1%,且甚至更典型地是规定值的
±
0.5%。
105.在整个公开中,某些实施方案可能以范围格式公开。应当理解,范围格式的描述仅仅是为了方便和简洁,而不应当被解释为对所公开范围的僵化限制。因此,应该认为对范围的描述已经具体公开了所有可能的子范围以及该范围内的各个数值。例如,应认为对范围例如从1至6的描述具有具体公开的子范围,例如从1至3、从1至4、从1至5、从2至4、从2至6、从3至6等,以及该范围内的单个数字,例如1、2、3、4、5和6。无论范围有多广,这都适用。
106.某些实施方案在本文中还可以被广泛和概括性地描述。属于概括公开的每个较窄的物种和亚属分组也形成本公开的一部分。这包括对本发明的概括性描述,伴随将任何主题从该属中移除的条件或负面限制,而不管所去除材料是否在本文中具体叙述。
107.本发明已经在本文中进行了广泛和概括性的描述。属于一般公开的每个较窄的物种和亚属组也构成本发明的一部分。这包括对本发明的一概括性描述,伴随将任何主题从该属中移除的条件或负面限制,而不管所去除材料是否在本文中具体叙述。
108.其他实施方案在以下权利要求和非限制性实例范围内。另外,在根据马库什组描述本发明的特征或方面的情况下,本领域技术人员将认识到,本发明也因此以马库什组的任何单个成员或成员的亚组来描述。
109.实验部分
110.casrx构建体的设计与合成。casrx序列获自addgene(pxr001:ef1a-casrx-2a-egfp,质粒编号109049)。在哺乳动物cmv启动子驱动下,casrx被克隆为带有ha标签和兔polya尾(casrx-ha-polya)。紧挨表达盒的下游,克隆了由人u6启动子驱动的grna骨架,且该序列获自addgene(pxr003:casrx grna克隆骨架,质粒编号109053)。
111.细胞系和病毒。人横纹肌肉瘤(rd)细胞购自美国标准菌种保藏中心(atcc)。人b4g12细胞购自creative bioarray。使细胞分别在atcc和creative bioarray推荐的培养基中生长。aav是内部生成的。简言之,通过三重转染293aav细胞系(cell biolabs aav-100)来包装aav,将该细胞系铺板在hyperflask
‘
m’(corning)中的生长培养基中,所述生长培养基由dmem glutamax 丙酮酸 10%fbs(thermo fisher)组成、补充有1xmem非必需氨基酸(gibco)。转染时的汇合度为70-90%。转染前,将培养基更换为新鲜预热的生长培养基。对于每个hyperflask
‘
m’,将200μg phelper(cell biolabs)、100μg prepcap(编码血清型dj或2的衣壳蛋白)和100μg pzac-casi-gfp或pzac-cmv-casrx混合在5ml dmem中,并以pei:dna质量比为5:1加入2mg pei“max”(polysciences)(40kda,1mg/ml于水中,ph 7.1)。将混合物孵育15分钟,然后逐滴转移到细胞培养基中。转染后第二天,将培养基更换为dmem glutamax 丙酮酸 2%fbs。转染48至72小时后,通过刮除或用1
×
pbs(ph7.2) 5mm edta裂
解来收获细胞,并在1500g下沉淀12分钟。将细胞沉淀重悬在1-5ml的裂解缓冲液(tris hcl ph 7.5,2mm mgcl,150mm nacl)中,并在干冰乙醇浴和37℃水浴之间冻融3次。以4000g持续5分钟去除细胞碎片,并收集上清液。将收集的上清液用50u/ml核酸酶(sigma-aldrich)和1u/ml rnase混合物(invitrogen)在37℃下处理30分钟,以去除未包装的核酸。孵育后,将裂解物加到29.9ml optiseal聚丙烯管(beckman-coulter)中由15%、25%、40%、60%optiprep各6ml组成的不连续的密度梯度顶部。将试管在70ti型转子上以54000rpm于18℃超离心1.5小时。提取40%级分,并使用amicon ultra-15(100kda mwco)(millipore)用补充有35mm nacl的1
×
pbs(ph 7.2)透析。纯化的aav载体储备液的滴度使用itr序列特异性引物和探针采用实时qpcr测定,并相对于atcc参考标准物质8(atcc)参考。使用的肠病毒株为ev-a71株5865/sin/000009。
112.免疫荧光测定。将10,000个人永生化角膜内皮细胞b4g12铺板于48孔板中的玻璃载玻片上,并用moi 100k的aavdj-casrx或aavdj-gfp转导。转导后3天,将细胞固定并用甲醇透化10分钟,用含5%bsa的1x pbs封闭细胞1小时。随后在室温下以1:200稀释的抗ha(abcam)一抗孵育2小时,或在室温下以1:1500的抗gfp(abcam)孵育2小时。在室温下以1:1000(thermo fisher)进行二抗染色2小时。然后用1x pbs洗涤载玻片3次,并使用prolong封片剂(thermo)封片。使用olympus显微镜拍摄图像,对于明场和488通道,曝光设置为15毫秒,增益设置为6400;对于dapi通道,曝光设置为800us,增益设置为6400。
113.用于aav血清型选择的生物筛选测定。将永生化人横纹肌肉瘤(rd)细胞以每孔10,000个细胞的密度接种在含有10%fbs的200μl dmem的48孔板中。将细胞在37℃培养过夜并使其粘附于孔中。使用一组aav(1、2、6、7、8、9、rh10、dj和anc80)以100k的moi转导细胞,重复三次。转导后72小时,收获细胞并使用gfp定量试剂盒(biovision)在多孔酶标仪(tecan)上定量总gfp蛋白。
114.aavdj-casrx转导的细胞中的rna基因干扰活性。将永生化人横纹肌肉瘤(rd)细胞以每孔10,000个细胞的密度接种在含有10%fbs的200μl dmem的48孔板中。以10k moi的aav2-gfp转导细胞以表达gfp。单独向导1、单独向导2和向导1 向导2的gfp敲低效率通过用moi 100k和moi 1000k的携带相应向导的aav2-casrx转导表达gfp的横纹肌肉瘤(rd)细胞来测试。在转导后72小时,收获细胞并使用gfp定量试剂盒(biovision)在多孔酶标仪(tecan)上定量总gfp蛋白。
115.使用ev71的体外抗病毒空斑测定。为了筛选抗ev71活性,将横纹肌肉瘤(rd)细胞以每孔104个细胞的密度接种于96孔板中,并在培养箱中孵育过夜。将待转导的携带不同向导的aav2-casrx以单独或合并的形式以moi为1k、10k、100k和1000k稀释在100μl体积中。转导后72小时,用moi为1的ev-a71病毒感染细胞。用1x pbs洗涤平板两次,并用含2%fbs的dmem孵育12小时。在感染后12小时收获每个孔的上清液,并用于随后的病毒空斑测定。对于病毒空斑测定,将横纹肌肉瘤(rd)细胞接种到24孔板中,并与10至106倍连续稀释的上清液样本在100μl体积中孵育。用pbs洗涤平板两次,并向每个孔中加入覆盖培养基,并以15分钟摇动间隔培养1小时,然后将其置于培养箱中培养4天。培养4天后,移除覆盖培养基并加入结晶紫染色,以使空斑可视化以便计数。
116.表1:序列表
117.除非另有说明,所有序列都以5
’‑3’
提供。
118.119.120.121.122.123.124.125.126.127.[0128][0129]
环状
[0130]
序列注释:
[0131]
特性:位置/限定符
[0132]
引物:互补序列(121..144)/
[0133]
标签=“2225”/说明=“序列:(seq id no:38)
[0134]
重复_区域:364..493/标签=“itr”[0135]
引物:534..557/标签=“ek18011”/说明:=“序列:”(seq id no:39)
[0136]
引物:534..593/标签=“ek18001”/说明:=“序列:”(seq id no:40)
[0137]
增强子:555..934/标签=“cmv增强子"
[0138]
cds:555..934/标签=“翻译555-934”[0139]
引物:622..645/标签=“1075”/说明=“序列:(seq id no:41)
[0140]
引物:722..741/标签=“1324”/说明=“序列:”(seq id no:42)
[0141]
引物:811..830/标签=“2394”/说明=“序列:”(seq id no:43)
[0142]
启动子:936..1134/标签=“cmv启动子”[0143]
引物:互补序列(1052..1077)/标签=“ek18015”/说明:=“序列:”(seq id no:44)
[0144]
引物:互补序列(1111..1134)/标签=“gg001”/说明=“序列:”(seq id no:45)
[0145]
引物:互补序列(1111..1134)/标签=“sv036”/说明:=“序列:”(seq id no:46)
[0146]
misc_feature:1135..1140/标签=“kozak”[0147]
misc_feature:1141..4017/标签=“casrx”[0148]
cds:1141..4017/标签=“翻译1141-4017”[0149]
引物:4018..4044/标签=“gg004”/说明=“序列:
[0168]
misc_feature:4920..5060/标签=“itr”[0169]
引物:互补序列(5206..5225)/标签=“2452”/说明=“序列:”(seq id no:61)
[0170]
引物:5824..5849/标签=“1625”/说明=“序列:”(seq id no:62)
[0171]
引物:互补序列(7226..7246)/标签=“2372”/说明=“序列:”(seq id no:63)
[0172]
全序列:
[0173]
[0174]
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。