一种具有x射线介导的光动力治疗效果的纳米复合材料及其制备方法和应用
技术领域
1.本发明涉及闪烁晶体制备技术领域,特别涉及一种具有x射线介导的光动力治疗效果的纳米复合材料及其制备方法和应用。
背景技术:
2.肿瘤放射治疗是利用放射线治疗肿瘤的一种方法。放疗是一种局部治疗方法,所用放射线包括放射性同位素产生的α、β、γ射线和各类x射线治疗机或加速器产生的x射线、电子线、质子束及其他粒子束等。大约70%的癌症患者在治疗癌症的过程中需要用放射治疗,约有40%的癌症可以用放疗根治,是治疗恶性肿瘤的主要手段之一。
3.放疗是癌症治疗的重要手段。然而,单纯的放疗并不能实现理想的治疗效果,因此我们需要设计新的方案以增强放疗的治疗效果。
4.光动力治疗是一种新型的癌症治疗手段。然而光在组织中的穿透能力差,限制了其在深部组织中的应用。因此,通过设计新途径以规避光的组织穿透性不足的缺点是实现光动力治疗在深层肿瘤组织应用的亟待解决的问题。
技术实现要素:
5.本发明的目的在于提供一种具有x射线介导的光动力治疗效果的纳米复合材料及其制备方法和应用。通过在lu3al5o
12
:mn/ca纳米闪烁体表面负载光敏剂ce6,并修饰peg及包覆sio2,增加了纳米闪烁体复合材料的水溶性及生物相容性,以实现放疗增敏及x射线介导的光动力治疗效果。
6.为实现上述目的,本发明提供了如下技术方案:本发明技术方案之一:提供一种具有x射线介导的光动力治疗效果的纳米复合材料的制备方法,包括以下步骤:(1)lu3al5o
12
:mn/ca纳米闪烁体的合成:将含有lu
3
、al
3
、mn
2
和ca
2
的前体盐溶液滴加到nh4hco3溶液中进行反应,反应完成后所得沉淀干燥、煅烧,煅烧产物与聚乙二醇加入至水中进行反应,得到lu3al5o
12
:mn/ca纳米闪烁体;(2)lu3al5o
12
:mn/ca-ce6纳米复合材料的合成:将所述lu3al5o
12
:mn/ca纳米闪烁体与二氢卟吩e6、n-羟基丁二酰亚胺(nhs)、n-(3-二甲基氨基丙基)-n
′‑
乙基碳二亚胺盐酸盐(edc)混合于溶剂中,避光反应,离心,沉淀干燥,得到lu3al5o
12
:mn/ca-ce6纳米复合材料;(3)lu3al5o
12
:mn/ca-ce6@sio2纳米复合材料的合成:将所述lu3al5o
12
:mn/ca-ce6纳米复合材料分散于溶剂中,滴加十六烷基三甲基铵水溶液进行反应,反应完成后除去溶剂;沉淀和硅酸四乙酯加入至氢氧化钠的乙醇水溶液中,加热反应,离心并洗涤沉淀,得到lu3al5o
12
:mn/ca-ce6@sio2纳米复合材料。
7.本发明加入的mn
2
可作为激活剂产生红光发射,ca
2
则作为电荷补偿剂增强mn
2
的红光发射。mn
4
离子具有 3d
3 的电子构型,在进行掺杂时通过取代合适基质中具有八面体配位环境的 ge
4
, al
3
, si
4
等离子而稳定存在,本实验中lu3al5o
12
中的 al
3
所具有的八面体配位环境十分适合 mn
4
,并且 mn
4
和 al
3
具有相似离子半径可被 mn
4
替换,从而展现红光发射和可见光以及近紫外光的吸收。 mn
4
优良的光谱特征为它独特的电子结构提供了宽带激发和窄带发射。由于mn
4
离子的高价态使其具有强晶体场环境,导致其与自旋和宇称禁戒的 2eg
→4a2跃迁过程对应着的发射光谱在670nm左右的红光发射峰。由于mn
4
不等价取代al
3
使得荧光颗粒因不满足电中性原理而影响了mn
4
的跃迁发光,导致其荧光性能极具下降。ca
2
引入上述体系取代al
3
可以有效的中和mn
4
不等价取代产生的电荷和缺陷,从而显著改善其荧光发射。
8.本发明中nhs和edc的加入可调节溶液中的电荷属性和材料表面基团,使得ce6容易在材料表面固定。ce6中的羧基-cooh和荧光颗粒表面的聚乙二醇中的-oh均可与nhs和edc表面的胍基(nh2)
2-c=nh(一个碳连2个氨基,双键再连一个亚胺基,碱性与koh相当)中氨基反应,发生的是酸碱中和反应,即羟基去h
,氨基得h
。机理是羧基中羰基的氧诱导作用吸电子,使羧基中—oh氧电负性减弱,对h
的束缚能力,从而使得ce6在荧光纳米颗粒表面固定更牢。
9.优选地,步骤(1)中所述lu
3
、al
3
、mn
2
和ca
2
的摩尔比为3:4.998:0.001:0.001;所述nh4hco3溶液的浓度为2m;所述干燥的温度为80℃;所述煅烧的温度为1000℃,时间为4h;所述聚乙二醇为peg600,煅烧产物与peg600的质量与体积比为10mg:4ml。
10.优选地,步骤(1)中所述含有lu
3
、al
3
、mn
2
和ca
2
的前体盐溶液与所述nh4hco3溶液的反应时间为30min;所述煅烧产物与所述聚乙二醇的反应时间为12h。
11.优选地,步骤(2)中所述lu3al5o
12
:mn/ca纳米闪烁体、二氢卟吩e6、n-羟基丁二酰亚胺和n-(3-二甲基氨基丙基)-n
′‑
乙基碳二亚胺盐酸盐的质量比为100:1:5:3;所述避光反应的时间为24h。
12.优选地,步骤(3)中所述lu3al5o
12
:mn/ca-ce6纳米复合材料与所述硅酸四乙酯的质量与体积比为100mg:300μl。
13.优选地,步骤(3)中所述氢氧化钠的乙醇水溶液由水、乙醇、2m的氢氧化钠溶液按比体积比40:6:0.3混合得到。
14.优选地,步骤(3)中所述十六烷基三甲基铵水溶液的浓度为10mg/ml,滴加速度为5ml/min。
15.优选地,步骤(3)还包含对所述lu3al5o
12
:mn/ca-ce6@sio2纳米复合材料的除杂步骤,具体为将所述lu3al5o
12
:mn/ca-ce6@sio2纳米复合材料与nh4no3分散于乙醇中,50℃反应2h,然后用水洗涤,干燥,完成除杂步骤。
16.本发明技术方案之二:提供一种根据上述具有x射线介导的光动力治疗效果的纳米复合材料的制备方法制得的具有x射线介导的光动力治疗效果的纳米复合材料。
17.本发明技术方案之二:提供一种上述具有x射线介导的光动力治疗效果的纳米复合材料在制备放疗药物中的应用。
18.优选地,所述放疗药物为x射线介导的辅助治疗药物。
19.本发明的有益技术效果如下:
本发明通过在lu3al5o
12
:mn/ca纳米闪烁体表面负载光敏剂ce6,并修饰peg及包覆sio2,增加了纳米闪烁体复合材料的水溶性及生物相容性,以实现放疗增敏及x射线介导的光动力治疗效果。实验证明,所制得具有x射线介导的光动力治疗效果的纳米复合材料可在x射线激发下诱导肿瘤细胞产生更多的活性氧,造成更多的dna损伤及细胞凋亡,并且其在小鼠模型中的肿瘤抑制率达到87%(单纯x射线组肿瘤抑制率为35%),体现出良好的治疗效果。
附图说明
20.图1为实施例1中原料ce6及中间产物lamc和终产物lamccs的表征图;其中a为lamcc与ce6单体的紫外-可见光吸收光谱图,b为lamc与lamcc的傅里叶变换红外光谱图,c为lamc与lamcc的x射线衍射图谱,d为lamc、lamcc及lamccs粒径及zeta电位检测图,e为lamc、lamccs的x-光致发光谱及ce6的紫外-可见光吸收光谱。
21.图2为实施例1中终产物lamccs的表征图;其中a为lamccs的透射电镜及高分辨透射电镜显微图像,b为lamccs的能量色散谱,c为lamccs的元素定位图像。
22.图3为实施例1中lamc、lamccs的x射线介导的光动力效果图;其中a为lamc、lamccs在不同条件下产生单线态氧(1o2)激发的检测指标信号强度,b为hela细胞在不同刺激条件下产生的活性氧水平。
23.图4为实施例1中lamc、lamccs的体外肿瘤杀伤效果;其中a为hela细胞在不同条件刺激下的细胞平板克隆实验,b为hela细胞在不同条件刺激下的dna损伤水平(蓝色为细胞核,绿色为dna双链损伤),c为hela细胞在不同条件刺激下凋亡水平。
24.图5为实施例1中lamc、lamccs的体内肿瘤杀伤效果;其中a为不同处理组小鼠肿瘤图像,b为不同处理组小鼠肿瘤体积生长曲线,c为不同处理组小鼠体重变化曲线。
具体实施方式
25.现详细说明本发明的多种示例性实施方式,该详细说明不应认为是对本发明的限制,而应理解为是对本发明的某些方面、特性和实施方案的更详细的描述。应理解本发明中所述的术语仅仅是为描述特别的实施方式,并非用于限制本发明。
26.另外,对于本发明中的数值范围,应理解为还具体公开了该范围的上限和下限之间的每个中间值。在任何陈述值或陈述范围内的中间值,以及任何其他陈述值或在所述范围内的中间值之间的每个较小的范围也包括在本发明内。这些较小范围的上限和下限可独立地包括或排除在范围内。
27.除非另有说明,否则本文使用的所有技术和科学术语具有本发明所述领域的常规技术人员通常理解的相同含义。虽然本发明仅描述了优选的方法和材料,但是在本发明的实施或测试中也可以使用与本文所述相似或等同的任何方法和材料。
28.关于本文中所使用的“包含”、“包括”、“具有”、“含有”等等,均为开放性的用语,即意指包含但不限于。
29.实施例1具有x射线介导的光动力治疗效果的纳米复合材料的制备:(1)lu3al5o
12
:mn/ca纳米闪烁体(lamc)的合成:
将0.1m的lu2o3分散到200ml的去离子水中,加入10ml浓硝酸并升温到90oc溶解,而后稀释于终浓度0.5m。将 lu(no3)3、al(no3)3、mncl2和ca(no3)2按化学式:lu3(al
0.9996
mn
0.0002
ca
0.0002
)5o
12
配比混合于去离子水中,磁力搅拌30分钟,得到前体盐溶液。然后,于室温下将前体盐溶液缓慢滴于150ml浓度为2m的nh4hco3溶液中,并让反应持续30分钟。通过去离子水和乙醇的清洗离心去除杂质,并将得到的沉淀于80℃的环境下干燥,并在1000℃下煅烧4小时,为增加煅烧产物水溶性,将煅烧产物(10mg)与peg 600(4ml)混合于10ml去离子水中反应12小时。混合溶液10000转离心5分钟,并用水清洗离心3次以去除多余的peg 600,得到的lamc,将得到的lamc于4℃保存备用。
30.(2)lu3al5o
12
:mn/ca-ce6纳米复合材料(lamcc)的合成:将步骤(1)所得lamc(100mg)、二氢卟吩e6(ce6,1mg)、n-羟基丁二酰亚胺(nhs,5mg)、n-(3-二甲基氨基丙基)-n
′‑
乙基碳二亚胺盐酸盐(edc,3mg)混合于100ml乙醇中,避光反应24h。将分散溶液8000转离心5分钟,并用乙醇及水清洗三次。然后,将反应物冻干24h,获得lamcc。
31.(3)lu3al5o
12
:mn/ca-ce6@sio2纳米复合材料(lamccs),即具有x射线介导的光动力治疗效果的纳米复合材料的合成:为进一步增强纳米材料的生物相容性,通过硅酸四乙酯(teos)水解的方法得到lamccs纳米复合材料。lamcc(100mg)分散于20ml乙醇中,十六烷基三甲基铵(ctab)于40℃温水中(浓度为10mg/ml)溶解并以5ml/min的速率滴加于lamcc乙醇分散溶液中。将溶液加热至80℃蒸发多余的乙醇并离心得到反应物。去离子水(40ml)、乙醇(6ml)、naoh溶液(300μl,2m)混合后置于三口烧瓶中,加热至80℃后,将lamcc反应物与teos(300μl)逐滴滴加于烧瓶中,反应10分钟。冷却后,离心并用乙醇反复清洗得到lamccs。最后,将nh4no3(0.8 g)与lamccs分散于50ml乙醇中,50℃反应2小时以去除未反应的ctab。反应结束后,lamccs用水清洗3次并冻干供后续使用。
32.图1为实施例1中原料ce6及中间产物和终产物lamccs的表征图;其中a为lamcc与ce6单体的紫外-可见光吸收光谱图,b为lamc与lamcc的傅里叶变换红外光谱图,c为lamc与lamcc的x射线衍射图谱,d为lamc、lamcc及lamccs粒径及zeta电位检测图,e为lamc、lamccs的x-光致发光谱及ce6的紫外-可见光吸收光谱。
33.图1中a为将lamcc和ce6分散于乙醇中,通过u-4100分光光度计(hitachi, japan)检测lamcc和ce6的紫外-可见光吸收光谱;结果显示,ce6吸收峰在670纳米附近,lamcc在670纳米附近有一吸收峰,证明ce6被负载于lamcc。
34.从图1中b为通过nicolet 670 ftir光谱仪(thomas nicolet,usa)记录4000-500 cm-1
频谱范围的傅里叶变换红外光谱;从中可以看出,3488 cm-1
、2358 cm-1
和1641 cm-1
处有吸收峰,是由于结合水的水分子的对称伸缩振动及弯曲振动产生的,吸附水通过h-o相互结合,使得其惯性矩和分子簇相对较大。同时,n-h与o-h吸收峰的位置不对称重合。2358 cm-1
、1394 cm-1 和1096 cm-1
处有吸收峰,是由于ce6的羰基的伸缩振动及弯曲振动导致的。这些证明ce6被负载到了lamc上。
35.图1中c为以cu
‑−
kα作为靶材,利用x射线衍射仪对物质的晶体结构进行研究,其测试的 2 θ 角的范围为10-80度,结果显示lamc和lamccs的结晶度与lu3al5o
12
一致,体现了本发明通过静电和化学吸附的方式成功合成了lamccs复合纳米材料。
36.图1中d显示,lamccs的粒径约为125纳米;由于mn
4
/ca
2
对lu3al5o
12
矩阵中lu
3
的不等效替换,lamc显示出 36.8 mv的电位,这使ce6 (-21.2 mv)更容装载到lamc上,包覆sio2后,lamccs的电位为-18.6 mv。
37.图1中e为在室温下使用装备有φ60-mm积分球(isf-513, jasco, tokyo, japan)及150-w氙灯作为激发光源的荧光光谱仪(fp-6500, jasco co., japan)检测lamc、lamccs的x-光致发光谱图,及使用u-4100分光光度计(hitachi, japan)检测ce6的紫外-可见光吸收光谱图。在6gy的x射线激发下,lamc在670、686、705纳米波段有发射峰。686纳米处的发射峰的产生基于mn
4 (2e-4
a2)红光辐射跃迁,670、705处的发射峰的产生基于mn
4 的声子及电子跃迁的相互作用。ce6在660纳米处有吸收峰,ce6的吸收光谱与lamc的光致光谱在红光处有较大面积的重合,证明了使用lamc激发ce6的合理性。
38.图2为实施例1中终产物lamccs的表征图;其中a为lamccs的透射电镜及高分辨透射电镜显微图像,b为lamccs的能量色散谱,c为lamccs的元素定位图像。
39.从图2中a可以看出,透射电镜显示了lamcc的软团聚体(soft agglomeration)形态,高分辨透射电镜显示材料的晶面间距(interplanar spacing)为0.484纳米,与lu3al5o
12
的晶格面(lattice plane)一致。
40.通过观察图2中b和c的能量色散谱及元素分布,显示mn/ca成功掺杂到lu3al5o
12
中,并且成功在lamcc表面包覆sio2外壳。
41.图3为实施例1中lamc、lamccs的x射线介导的光动力效果图;其中a为lamc、lamccs在不同条件下产生单线态氧激发的检测指标信号强度,b为hela细胞在不同刺激条件下产生的活性氧水平。
42.图3中a为单线态氧通过特异性指示剂单线态氧荧光探针 (singlet oxygen sensor green reagent,sosg)检测反应体系接受10gy x射线(x-ray)照射的条件下产生的单线态氧的量。反应体系中的纳米颗粒、sosg的浓度分别为100 μg/ml、100 μm。设置6个组(control,lamc,lamccs,x-ray,lamc x-ray,lamccs x-ray)。经过照射后,将反应体系置于低速摇床上30℃避光孵育12小时,之后12000转离心2分钟,通过荧光分光光度计检测激发波长为488纳米时溶液的荧光强度;结果显示lamccs较lamc组的荧光强度更高,具有更高的单线态氧转化效率。
43.图3中b为将hela细胞接种于24孔板中(8
×
104个/孔),设置6个组:(1)对照组、(2)lamc、(3)lamccs、(4)x-ray、(5)lamc x-ray、(6)lamccs x-ray;接种细胞24小时后,每孔加入500μl培养基,纳米颗粒的浓度为100
µ
g/ml;接受x射线照射组的照射剂量为5gy。照射2小时后,每孔加入含有10
ꢀµ
m的 dcfh-da探针的无血清培养基,37℃孵育2小时,pbs清洗3次,荧光显微镜拍摄488纳米激发光下的荧光图像。结果显示lamccs可以显著增加x射线照射下细胞产生的活性氧。
44.图4为实施例1中lamc、lamccs的体外肿瘤杀伤效果;其中a为hela细胞在不同条件刺激下的细胞平板克隆实验,b为hela细胞在不同条件刺激下的dna损伤水平(蓝色为细胞核,绿色为dna双链损伤),c为hela细胞在不同条件刺激下凋亡水平。
45.图4中a为将hela细胞接种于6孔板中(1000个/孔)孵育24小时,设置6个组:(1)对照组、(2)lamc、(3)lamccs、(4)x-ray、(5)lamc x-ray、(6)lamccs x-ray,每孔加入1ml培养基,纳米颗粒浓度为100
µ
g/ml,孵育12小时,接受x射线照射组的照射剂量为2gy。更换新鲜
培养基孵育7天后,4%多聚甲醛固定并用结晶紫染色,统计细胞群落数;结果显示lamccs可显著降低x射线照射后细胞的增殖能力。
46.图4中b为将hela细胞接种于24孔板中(5
×
104个/孔)孵育24小时,设置6个组:(1)对照组、(2)lamc、(3)lamccs、(4)x-ray、(5)lamc x-ray、(6)lamccs x-ray,每孔加入500
µ
l培养基,纳米颗粒浓度为100
µ
g/ml,孵育12小时,接受x射线照射组的照射剂量为5gy。更换新鲜培养基孵育12小时后,4%多聚甲醛固定,0.2%的triton-x 100透膜,bsa溶液封闭,抗γ-h2ax抗体室温孵育1小时,pbs清洗后荧光二抗孵育1小时,pbs清洗后使用dapi染核,荧光显微镜观察;结果显示,lamccs可显著增加x射线照射后细胞dna双链损伤水平。
47.图4中c为将hela细胞接种于6孔板中(1
×
105个/孔)孵育24小时,设置6个组:(1)对照组、(2)lamc、(3)lamccs、(4)x-ray、(5)lamc x-ray、(6)lamccs x-ray,每孔加入1ml培养基,纳米颗粒浓度为100
µ
g/ml,孵育12小时,接受x射线照射组的照射剂量为5gy。更换新鲜培养基孵育48小时后,收集细胞并用annexin v-fitc/pi凋亡检测试剂盒染色,流式细胞仪检测。结果显示lamccs可显著增加x射线照射后的细胞凋亡。
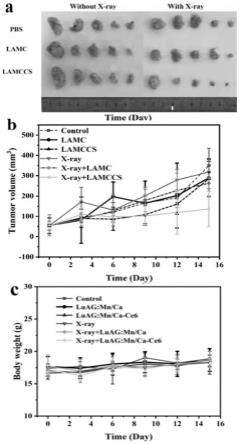
48.图5为实施例1中lamc、lamccs的体内肿瘤杀伤效果;其中a为不同处理组小鼠肿瘤图像,b为不同处理组小鼠肿瘤体积生长曲线,c为不同处理组小鼠体重变化曲线。
49.构建宫颈癌裸鼠模型,将1
×
107hala细胞接种于6周龄balb/c雌性裸鼠右侧腹股沟,1周后将裸鼠随机分为6组:(1)对照组、(2)lamc、(3)lamccs、(4)x-ray、(5)lamc x-ray、(6)lamccs x-ray,瘤内注射25μl pbs或纳米颗粒溶液(纳米颗粒浓度为2 mg/ml),接受x射线照射组分别于注射后第1、4、7天给予肿瘤局部x射线照射5gy,第15天处死小鼠,取肿瘤组织;不同处理组小鼠肿瘤图像见图5中a;小鼠分组并注射药物后每3天测量一次肿瘤大小,并计算肿瘤体积(计算公式:体积=1/2
×
长
×
宽2),绘制肿瘤体积增长曲线,见图5中b,结果显示lamccs可显著抑制x射线放疗后肿瘤生长;小鼠分组并注射药物后每3天测量一次小鼠体重,绘制小鼠体重变化曲线,见图5中c,结果显示小鼠体重未发生明显变化且不同处理组间无明显差异,表面本发明制备的lamccs生物相容性好。
50.以上所述的实施例仅是对本发明的优选方式进行描述,并非对本发明的范围进行限定,在不脱离本发明设计精神的前提下,本领域普通技术人员对本发明的技术方案做出的各种变形和改进,均应落入本发明权利要求书确定的保护范围内。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。