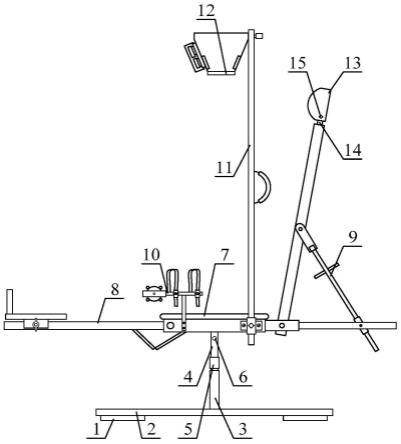
1.本发明涉及受试者的神经系统病症的治疗。具体地,本发明涉及受试者的脊髓损伤的治疗。本发明涉及与神经系统病症相关的病变的治疗。
背景技术:
2.脊髓是包含神经组织的长管状结构,其主要功能是传递神经信号或信息,使身体和大脑能够进行交流。它还负责协调反射。脊髓被包裹在脊柱内。脊神经位于椎骨之间的空间中,并且神经根在每个椎骨的任一侧离开脊髓。脊髓被分成段,并且主要的身体功能对应于特定的段。在人的脊髓中有31个脊髓神经段。
3.脊髓损伤(sci)是导致脊髓功能改变的脊髓损坏。这些改变可能是暂时的,也可能是永久的。损伤可以发生在脊髓的任何段,可以是完全的也可以是不完全的。运动和感官功能的丧失取决于损伤的部位和损坏的程度。
4.外伤造成的脊椎错位或断裂可能导致脊髓挫伤或横断。这种原发性机械损伤会对脊髓造成初始伤害,扰乱血液供应,并对细胞和神经元造成损坏。继发性反应随之而来,并导致脊髓中央物质的破坏。髓鞘的丧失导致信号转导的丧失。神经胶质细胞迁移至脊髓损伤的部位,试图修复所造成的损坏。然后在损伤部位周围形成神经胶质疤痕,阻止再生。神经胶质疤痕由细胞和生物化学两部分组成。在脊髓损伤后,发生星形胶质细胞增生和小胶质细胞活化。它们分泌过多的分子,包括硫酸软骨素蛋白聚糖。
5.有两百万或更多的脊髓挫伤病例。有600万或更多的中风病例。有70万或更多的脑瘫病例。有一百万或更多的帕金森氏症病例。有40万或更多的多发性硬化症病例。
6.目前用于脊髓损伤的静脉治疗方法包括在损伤后8小时内注射名为甲基强的松龙的类固醇,但这已被证明疗效有限或没有疗效。
7.神经可塑性是中枢神经系统(cns)通过突触连接和回路的重组来适应外部环境变化的过程。这对脊髓损伤后成功的功能恢复至关重要。神经束膜网(pnn)是遍布cns的致密细胞外基质结构(kwok等,2011),其形成与发育可塑性的终止有关(carulli等,2010;pizzorusso等,2002)。pnn包裹神经元的表面,突触所在的位置有孔(图7)。这意味着这些神经元不太可能拥有用于功能恢复的突触。这限制了突触的形成,从而限制了神经可塑性。
8.硫酸软骨素蛋白聚糖(cspg)是抑制神经突生长并因此抑制再生和可塑性的多糖家族(kwok等,2011;silver和miller,2004)。已发现cspg存在于pnn中,并在脊髓损伤后的神经胶质疤痕中上调。
9.在长达18个月的急性和慢性损伤模型中,已经证明通过注射软骨素酶abc(chabc)去除pnn和神经胶质疤痕中的cspg打开了可塑性和再生的窗口,以促进sci后的恢复(bradbury等,2002;wang等,2011;warren等,2018)。chabc已被证明有利于恢复以及其它治疗,包括康复(garcia-alias等,2011)。然而,这种方法在将其转化为人类应用时存在显著障碍(例如,由于酶的稳定性有限,因此需要重复注射,注射是侵入性的,由于长时间暴露于细菌蛋白质而可能产生免疫反应)。
10.4-甲基伞形酮是常用于胆汁疗法的化合物。它在欧洲以羟甲香豆素的名称出售。这种药物在这个领域已经使用了很多年,并且具有很好的安全性。nakamura等人于1995年首次在体外使用该化合物来抑制皮肤成纤维细胞中的ha合成(nakamura等,1995)。
11.fontaine等人对4-甲基伞形酮进行了毒理学和致畸性研究(fontaine等,1968)。他们报告了对几个物种的急性毒性、慢性毒性、局部耐受性和实验性致畸作用的研究结果。在慢性毒性研究中,发现大鼠口服的最大耐受剂量等于6000mg/kg。在慢性研究中,给大鼠服用200mg/kg/天和40mg/kg/天,持续三个月。未报告死亡率,大鼠的食欲行为和外观未受影响。作者的结论是,总之,在这些条件下,大鼠耐受的总剂量可以固定为至少200mg/kg/天,这是人类预期日剂量的10倍。作者还报道了该药物在当地得到了很好的支持。该产品似乎没有致畸作用,即使在非常高的剂量下,对三个物种进行研究:大鼠、小鼠和兔子。特别地,发现该药物即使在1200mg/kg/天的剂量下也能被怀孕大鼠很好地支持。对幼鼠的发育也没有影响。
12.本发明用于解决现有技术的问题,并提供用于治疗神经系统病症的药物。特别地,本发明提供了用于治疗脊髓损伤的药物。
13.成人中枢神经系统轴突不保留再生能力。损伤后,细胞外基质在加强再生失败中起着不同的作用。硫酸软骨素蛋白聚糖是细胞外基质分子家族,其在脊髓损伤后的神经胶质疤痕中被上调,并抑制神经突生长从而抑制再生。此外,硫酸软骨素蛋白聚糖也存在于称为pnn的特殊结构中,pnn限制了潜在功能恢复的可塑性。脊髓的免疫组织化学显示,运动神经元周围的pnn下调,这是由羟甲香豆素抑制透明质酸合成所致。此外,我们还观察到硫酸软骨素蛋白聚糖的染色强度在脊髓中急剧降低。
技术实现要素:
14.本发明的一方面提供了用于治疗神经系统病症的4-甲基伞形酮(本文称为“本发明的pnn抑制剂(pnni)”)、其衍生物或盐。
15.在实施方案中,神经系统病症与病变的形成有关。在一个实施方案中,病变是神经胶质疤痕。在一个实施方案中,病变是由毒性蛋白聚集物累积产生的斑块。一个实例是淀粉样疤痕。
16.在另一实施方案中,神经系统病症可以选自包括由创伤、损伤、感染、变性、结构缺陷、肿瘤和血流中断引起的病症的组。
17.病症可以选自包括中风、短暂性脑缺血发作、脊髓病、出血、脑膜炎、脑炎、贝尔麻痹、脑或脊髓肿瘤、帕金森病、亨廷顿舞蹈病和阿尔茨海默病的组。其可能是脑瘫。
18.在实施方案中,神经系统病症可以是对神经系统的损伤。优选地,病症是脊髓损伤。
19.本发明的一方面提供了用于治疗与神经系统病症相关的病变的4-甲基伞形酮、其衍生物或盐,即本发明的pnn抑制剂(pnni)。此病症可以是本文公开的病症。
20.本发明的一方面提供了治疗受试者的神经系统病症的方法,该方法包括向所述受试者施用4-甲基伞形酮(本文称为“本发明的pnn抑制剂(pnni)”)、其衍生物或盐。此病症可以是本文公开的病症。
21.在另一方面,本发明提供了治疗受试者的与神经系统病症相关的病变的方法。该
方法包括向所述受试者施用4-甲基伞形酮(本文称为“本发明的pnn抑制剂(pnni)”)、其衍生物或盐。此病症可以是本文公开的病症。
22.定义
23.本文提及的所有出版物、专利、专利申请和其它参考文献出于所有目的通过引用整体并入本文,如同每个单独的出版物、专利或专利申请被具体和单独地指出通过引用并入本文,并且其内容被全部引用。
24.在本文中使用时,除非特别指出,否则除了术语在本领域中可能享有的任何更广义(或更狭义)的含义之外,以下术语旨在具有以下含义:
25.除非上下文另有要求,本文使用的单数应理解为包括复数,反之亦然。与实体相关使用的术语“一(a)”或“一(an)”应被理解为指代一个或多个该实体。因此,术语“一(a)”或“一(an)”、“一个或多个”和“至少一个”在本文中可互换使用。
26.如本文所用,术语“包括(comprise)”或其变体,例如“包括(comprises)”或“包括(comprising)”,应被理解为表示包括任何所述的整体(例如特征、元件、特性、性质、方法/工艺步骤或限制)或整体组(例如特征、元件、特性、性质、方法/工艺步骤或限制),但不排除任何其它整体或整体组。因此,如本文所用,术语“包括”是包含性的或开放式的,并且不排除额外的、未列举的整体或方法/工艺步骤。
27.本文使用的术语“神经系统”或“人神经系统”是指协调动作并在身体各部分之间传递信号或信息的身体部分。神经系统包括中枢神经系统或cns(大脑和脊髓)和外周神经系统或pns。
28.本文所用术语“神经系统病症”可以是影响神经系统正常功能的任何疾病、障碍或病症。病症可能是损伤或损坏。病症可选自但不限于由创伤、损伤、感染、退化、结构缺陷、肿瘤、血流中断和自身免疫障碍引起的病症。病症可选自但不限于中风、短暂性脑缺血发作、脊髓病、出血、脑膜炎、脑炎、贝尔麻痹、脑或脊髓肿瘤、帕金森病、多发性硬化、肌营养侧索硬化(als)、亨廷顿舞蹈病和阿尔茨海默病。
29.本文所用术语“脊髓损伤”是指导致其功能改变的脊髓或其部分的任何损伤或损坏。它可以在脊髓的任何部位或段,损坏可以在任何水平。可能有一个或多个损伤部位。损伤包括涉及外周神经的圆锥下方的损伤。为避免疑问,该术语包括:脊髓开放性、闭合性和穿透性损伤。这包括完全和不完全病变、部分和完全横断、中央脊髓综合征、布朗塞卡尔综合征、马尾综合征以及任何程度或类型的脊髓病和神经根病。
30.如本文所用,术语“病症”用于定义任何损害生理功能并与特定症状相关的异常病症。该术语被广泛用于包括其中生理功能受损的任何疾病、障碍、病痛、异常、病理、生病、病症或综合征,而不考虑病因学的性质(或者实际上是否建立了疾病的病因学基础)。因此,它包括由感染、创伤、损伤、手术、放射性消融、中毒或营养缺乏引起的病症。
31.如本文所用,术语“治疗(treatment)”或“治疗(treating)”是指治愈、改善或减轻病症或疾病的症状或消除其病因(或减轻其影响)的干预(例如向受试者施用药剂)。在这种情况下,术语治疗也可以包括促进恢复。在这种情况下,该术语与术语“(therapy)疗法”同义使用。此外,术语“治疗(treatment)”或“治疗(treating)”是指在被治疗人群中预防或延迟疾病的发作或进展或降低(或根除)其发病率的干预(例如向受试者施用药剂)。术语“治疗”与术语“预防”同义使用。
32.如本文所用,药剂的“有效量”或“治疗有效量”定义为可施用于受试者而没有过度毒性、刺激、过敏反应或其它问题或并发症,与合理的效益/风险比相当,但足以提供所需效果的量,例如通过受试者病症的永久或暂时改善而表现出的治疗或预防。取决于个体的年龄和一般病症、给药方式和其它因素,该量将因个体而异。因此,虽然不可能确定精确的有效量,但是本领域技术人员能够使用常规实验和背景常识在任何个别情况下确定合适的“有效”量。在这种情况下,治疗结果包括症状的根除或减轻、疼痛或不适的减轻、存活时间的延长、活动能力的提高以及其它临床改善的标志。治疗结果不一定是完全治愈。
33.在上文定义的治疗和有效量的上下文中,术语受试者(在上下文允许的情况下,应理解为包括“个体”、“动物”、“患者”或“哺乳动物”)定义了需要治疗的任何受试者,尤其是哺乳动物受试者。在优选的实施方案中,受试者是人。在实施方案中,受试者是成年人。在实施方案中,受试者是儿科大龄受试者,即21岁或更小。受试者可以是任何性别。
34.如本文所用,术语“组合物”应该理解为是指人工制造的事物,不包括天然存在的组合物。组合物可以配制成单位剂量形式,即含有单位剂量或单位剂量的倍数或亚单位的不连续部分的形式。
35.如本文所用,术语“药物组合物”涉及与一种或多种药学上可接受的载体、稀释剂或赋形剂混合的本发明的pnni或本发明的组合物。尽管本发明的pnni可以单独施用,但它通常与药物载体、赋形剂或稀释剂混合施用,特别是用于人类治疗。药物组合物可用于人类医学的人类或兽医学的动物。用于本文描述的各种不同形式的药物组合物的这种合适的赋形剂的例子可以在由a wade和pj weller编辑的第8版的药物赋形剂手册(handbook of pharmaceutical excipients)中找到。特别地,美国药学综述“生物药物发现中的机遇和挑战(opportunities and challenges in biologic drug discovery)”(hooven,2017),在david osborne和antonio aman、taylor&francis编辑的局部给药制剂中描述了用于局部给药的制剂,其全部内容通过引用并入本文。
36.用于治疗用途的可接受的载体或稀释剂在药物领域是众所周知的,并且描述于例如雷明顿制药科学(remington’s pharmaceutical sciences),mack出版公司(a.r.gennaro编辑1985)。合适载体的实例包括乳糖、淀粉、葡萄糖、甲基纤维素、硬脂酸镁、甘露醇、山梨醇等。合适的稀释剂的实例包括乙醇、甘油和水。药物载体、赋形剂或稀释剂的选择可以根据预期的施用途径和标准药物实践来选择。除了载体、赋形剂或稀释剂之外,药物组合物可以包含任何合适的粘合剂、润滑剂、悬浮剂、包衣剂、增溶剂。合适的粘合剂的例子包括淀粉、明胶、天然糖例如葡萄糖、无水乳糖、自由流动乳糖、β-乳糖、玉米甜味剂、天然和合成树胶例如阿拉伯胶、黄蓍胶或海藻酸钠、羧甲基纤维素和聚乙二醇。合适的润滑剂的实例包括油酸钠、硬脂酸钠、硬脂酸镁、苯甲酸钠、乙酸钠、氯化钠等。药物组合物中可以含有防腐剂、稳定剂、染料甚至调味剂。防腐剂的实例包括苯甲酸钠、山梨酸和对羟基苯甲酸的酯。也可以使用抗氧化剂和悬浮剂。
37.在具体的实施方案中,术语“药学上可接受的”是指由联邦或州政府的管理机构批准的,或在美国药典或其它公认的药典中列出的,用于动物,更具体是用于人。
38.如本文所用,术语“衍生物”是指衍生自4-甲基伞形酮的已经被修饰的化合物,例如通过化学反应,但保留了去除pnn的能力,即治疗本文所述的神经系统病症。确定pnn去除的方法可以如本文所述。与4-甲基伞形酮相比,该衍生物可以具有但不限于一个或多个烷
基、芳基、酰基、羟基、羟甲基、甲氧基、甲基和/或磺酰基取代基。该术语可与功能衍生物互换使用。4-甲基伞形酮衍生物在本领域中是众所周知的。可以在us2019269647或us2018201640中找到实例,所有这些文献都通过引用并入本文。所有这些衍生物都在本公开的范围内。
39.衍生物或药学上可接受的盐可用于本公开的治疗方法。本发明的pnn抑制剂或化合物可以是盐的形式,但是药物化学领域的技术人员将会理解,盐的选择并不重要,并且可以通过众所周知的方法制备其它药学上可接受的盐。本发明的pnn抑制剂或化合物可以是代谢物或前药的形式。
40.如本文所用,术语“病变”是指由于损伤或疾病导致的器官或其部分的异常改变。它可能包括疤痕或斑块。
41.术语“持续释放”以与化合物或活性物质的传递系统相关的常规意义使用,其在一段时间内提供该化合物或活性物质的逐渐释放,并且优选地,尽管不是必须的,在一段时间内具有相对恒定的化合物释放水平。
42.羟甲香豆素是透明质酸合成抑制剂。它是(4-甲基伞形酮)(andreichenko等,2019)。我们的数据显示,为期10天的非侵入性口服施用下调了脊髓中的硫酸软骨素和透明质酸。这使得羟甲香豆素成为减少脊髓损伤后抑制性硫酸软骨素蛋白多糖的主要候选药物。
43.pnn参与限制可塑性是生理事件。即使在正常生理条件下pnn被去除,也可以观察到可塑性的激活。慢性期脊髓损伤表现出与正常生理学中pnn相似的特征,并且同样是有益的反应。
[0044]“烷基”是指具有指定碳原子数的直链或支链烷基(例如c
1-c4烷基),或该范围内的任何数目的直链或支链烷基(甲基、乙基、丙基、异丙基、丁基、异丁基、叔丁基等)。烷基可以是c
1-c
18
、c
1-c
12
或c
1-c6。
[0045]“芳基”:通过去除氢原子从芳烃衍生的任何单价有机自由基。例如,简单的芳基基团是苯基(化学式为c6h5),它是由苯衍生而来的基团。
[0046]“酰基”:由键合至r基团的羰基组成的一组原子。酰基基团是分子式为rco-的官能团,其中r是以单键键合至碳原子上的烷基基团。通常地,酰基基团连接至更大的分子上,使得碳和氧原子通过双键连接。当从含氧酸中除去一个或多个羟基时,就形成了酰基基团。尽管酰基基团几乎只在有机化学中讨论过,但它们也可以衍生自无机化合物,例如膦酸和磺酸。酯、酮、醛和酰胺都含有酰基。具体实例包括乙酰氯(ch3cocl)和苯甲酰氯(c6h5cocl)。
附图说明
[0047]
参考附图,从下面仅以实施例的方式给出的实施方案的描述中,将更清楚地理解本发明,其中:
[0048]
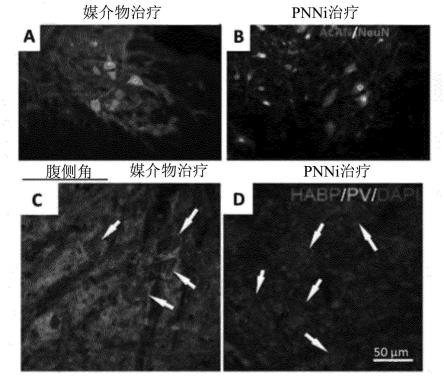
图1示出了(a-b)在用本发明的pnni治疗后观察到的pnn和细胞外基质中,特别是在腹侧角中,聚集蛋白聚糖(acan)染色(pnn标记)的缺乏;(c-d)pnni治疗诱导小清蛋白(pv)阳性神经元周围和细胞外基质中透明质酸结合蛋白(habp)的减弱。
[0049]
图2示出了basso、beattie和bresnahan(bbb)后肢运动开阔场地测试装置(hindlimb locomotor open field test apparatus)(basso等,1995)。(a)平坦开阔的场
地装置,直径约1m。(b)每周将大鼠置于开阔场地装置中4分钟,以评估后肢运动能力。
[0050]
图3示出了用于机械感官评估的装置;von frey分析。将动物放入具有金属丝网底部(b)的用于足底刺激的完整基座组件(a),并适应约20分钟。将对数增加的厚度(c)的von frey毛发推过金属丝团底部,并垂直压在左或右后肢的足底表面上,使用dixon上下法确定50%缩回阈值。
[0051]
图4示出了图2至图5所示实施例的研究时间轴。
[0052]
图5示出了:(a)大鼠的挫伤力分析。在所有实验组中,所有大鼠都受到相似的挫伤强度;(b)basso、beattie和brenahan(bbb)得分。结果表明,在中度t9挫伤后,pnni治疗的大鼠(每日治疗)有更好的功能恢复。当媒介物治疗的大鼠在损伤后5周达到~10分时,4-mu治疗组达到~15分;(c)von frey毛发测试结果。使用von frey毛发测试,来自不同治疗组的大鼠在触觉敏感性上没有显示出任何差异。所有组n=11。
[0053]
图6示出了本发明的pnni的日剂量计算。
[0054]
图7示出了神经束膜网(pnn)(a)神经元表面的pnn(绿色)的示意图;(b)发现突触小泡(红色)聚集在pnn(绿色)的孔中(de winter等,2016;vo等,2013)。
[0055]
图8是脊髓中α运动神经元上pnn存在的代表性图像(galtrey等,2008;irvine和kwok,2018)。聚集蛋白聚糖(acan)阳性pnn包围大多数α运动神经元(mn)neun,chat共定位表示mn。(a)被neun、acan-阳性pnn及其共定位(acan /neun )包围的腹侧运动池中的mn百分比。共聚焦图像显示脊髓中acan-阳性的pnn(b)分别包围neun阳性的mn(c)和chat-阳性的mn(d)。误差
±
sd;n=3。统计学单因素anova;显著性水平:*p《0.05。比例尺,100μm。
[0056]
图9(a-s):体外pnni去除pnn的功效分析(a-i)。尽管未治疗的pnn
hek细胞显示了wfa阳性pnn的清晰信号,(b),向pnn
hek细胞施用两天的pnni治疗(0.5mm或1.0mm),去除了86.4
±
4.47%(f
3,66
=73.60,所有治疗时间点vs未治疗p《0.0001)的wfa-阳性染色。在治疗后三天内,染色强度部分恢复至基线凝集素结合的43.6
±
14.6%(图c-i,治疗后3天和5天vs治疗期,p《0.0001)。给药10天后终止的动物组织学显示,与未治疗的动物相比,施用pnni的两种方法都足以降低整个cns的wfa-阳性结合(j-o)。脊髓背角中的定量表明,口服施用pnni 10天,诱导wfa-阳性部分的部分去除,达到基线ecm水平的71.0
±
7.20%(t(3)=5.15,p=0.0142;图9p)。短期pnni足以诱导接受治疗的完整大鼠感官功能的改变,但不能诱导运动功能的改变(q-s)。
[0057]
图10(a-s):神经束膜网抑制剂(pnni)诱导完整大鼠的感官运动图(m1)的重组。使用皮质内微刺激(icms),hl和fl皮质活动代表图被用于研究长期使用预期可塑性增强剂pnni治疗后的完整/假手术动物的m1的功能组织。在胸椎中段椎板切除术(假手术)11周后或年龄受控的完整大鼠中,在立体定位坐标下,在距前囟门(b)(a)头侧/尾侧5mm的右半球开颅术中进行icms。将单个icms图组合起来,以给出每组的代表性热图,热图说明每个立体定位坐标的动物百分比,其中后肢(hl;b-d)或前肢(fl;k-m)活动能够被诱发。为lister hooded大鼠生成基线hl和fl皮质图(b,k;b-d,k-m的虚线轮廓)来比较假手术组(c,l)和长期pnni施用组(d,m)的功能可塑性。hl分析(f-g)的测量值如e)所示。h)经pnni治疗后,hl代表的平均区域(mm2)减少。pnni治疗降低了引起hl的完整hl中心的百分比(f),但未降低完整hl中心中每组总计的引起hl区域的百分比(g)。对(i)短刺激间期(20-40ms)和(j)长刺激间期(150-250ms)的场电位进行成对脉冲刺激,未发现组间(i-j)观察到的短期或长期成对
脉冲比率发生变化。fl分析(p-s)的测量值如o)所示。pnni治疗后,在与fl或hl运动无关的区域诱发了fl活动(见基线hl图右侧;白色虚线轮廓k-m)。虽然引起fl的总表面积没有显著变化(n),但假手术动物的pnni治疗减少了在完整fl中心引起fl的区域(p),但没有引起完整hl区域中引起fl活动的相应增加(r)。假手术或pnni治疗并没有改变fl完整中心(q)或hl完整中心(s)的总fl百分比。对于所有icms组,完整组n=4,假手术组n=4,假手术/pnni组n=5。对于成对脉冲组,完整组n=32,假手术组n=15,假手术/pnni组n=19。统计学,单因素anova;显著性水平:*p《0.05**p《0.01***p《0.001。
[0058]
图11(a-n):在神经束膜网抑制剂(pnni)和脊髓损伤(sci)结合后,前肢(fl)转移至感官运动皮质(m1)的后肢(hl)区域。pnni和/或损伤独立地增强脊髓损伤大鼠的皮质可塑性。损伤后11周,在立体定位坐标下,在距前囟(b)(a)头侧/尾侧5mm的右半球开颅术中进行皮质内微刺激(icms)。每组的代表性热图示出了每个立体定位坐标下能够诱发hl(b-c)或fl(d-e)活动的动物的百分比。将lister hooded大鼠基线hl和fl皮质图(b-e中的虚线轮廓)与胸椎中段sci组(b,d)和/或长期pnni施用组(c,e)进行比较,以评估结构可塑性。sci后,不能诱发hl活动(b-c)。fl分析(k-n)的测量值如j)中所示。pnni和/或sci后,在先前诱发hl活动的区域诱发了fl活动(见右侧白色虚线轮廓d-e)。虽然引起fl的总表面积没有显著变化(f),完整fl中心的fl百分比也没有显著变化(k-l),但与假手术对照组相比,与损伤后用pnni治疗的完整hl中心相关的fl区域增加(p=0.197,m;p《0.05,n)。g:每组的平均场电位振幅vs.刺激强度的曲线图。通过放置在皮质层v/vi中的双极电极的电刺激,在皮质层ii/iii中诱发突触反应。在皮质切片上进行记录,坐标如下:ml:2-3mm,ap 1.40-1.8mm,尾侧至前囟。损伤和pnni治疗的组合提高了突触传递(g)。短(20-40ms)和长(150-250ms)刺激间隙的场电位的成对脉冲刺激显示,在组(i)之间没有观察到长期成对脉冲比率(ppr)的改变。然而,观察到单独损伤的短期ppr较低(p=0.052;h)。统计学,单因素anova;对于各组,假手术组n=4,媒介物组n=3,pnni组n=3。g:数据以平均值
±
sem表示,n代表皮质切片。统计学:双向重复测量方差分析(anova)。h-i:统计学,单因素anova;对于各组。
[0059]
图12(a-e):在持续康复的同时限制pnni的施用可以进一步恢复后肢(hl)的运动。当在实验结束(8周pnni治疗)前2-3周终止pnni治疗以允许pnn重建时,在继续进行康复训练的动物中观察到进一步的hl改善(a)。条形图显示了在pnni施用结束时,在损伤后9周(wpi)、10wpi和12wpi,能够实现前肢-后肢(fl-hl)协调的动物的百分比(b)。堆叠条形图显示了,在9和12wpi,(c)hl和(d)前肢(fl)踩在水平阶梯上的分类,在经典阶梯评分系统中,踩中:得分为3-6,错误(slip):1-2,未踩中:0(metz和whishaw,2009)。e)在9和12wpi,进行的von frey分析确定的足底后爪的左-右(l-r)平均50%缩回阈值没有显示痛觉过敏。pnni治疗终止后,pnn的巩固不会诱导感官改变。(对于各组,8周pnni和8周pnni t的n分别为10和9。统计学,a,c-e:双向混合因子anova;显著性水平:*p《0.05**p《0.01和***p《0.001。a、c、d:误差线为
±
sem。)
[0060]
图13(a-k):8周的pnni伴随持续康复部分恢复了fl区域的皮质重组为完整的组织。将单个icms图组合起来,给出每组的代表性热图,热图显示每个立体定位坐标的动物百分比,其中后肢(hl;b-c)活动不能够被诱发,但前肢(fl;d-e)活动能够被诱发。虚线轮廓表示hl(b-c)和fl(d-e)的完整基线面积,用于比较8周pnni施用组(b,d)和8周pnni伴随持续跑步机训练组(c,e)的功能可塑性。f)仅通过受限的pnni治疗伴随持续的训练,fl表现的平
均面积(mm2)减少至正常/完整水平。i)中示出了用于分析的测量值(g-h,j-k)。脊髓损伤后,在先前诱发hl活动的区域诱发fl活动(基线hl图显示为白色虚线轮廓d-e)。g)fl活动大部分能够在完整的fl区域内引起,在8周pnni t(p=0.243)时有轻微的减少趋势。h)在8周的pnni治疗后,在完整的fl区域引起的总计fl区域的比例下降,只有持续训练时有这种趋势(p=0.112)。j)损伤后,8周pnni治疗可在hl区域诱发fl活动。然而,只有在持续训练的情况下,才观察到部分fl从hl区域收缩(p=0.514)。k)与未损伤的对照组相比,在完整的hl区域引起的fl区域的比例似乎增加(p=0.114,8周pnni;和p=0.177周pnni t)。
[0061]
图14:jd009和jd013减弱pnn形成。使用免疫细胞化学分析pnni、jd009和jd013在减少pnn形成中的功效。使用n-乙酰半乳糖胺结合凝集素wfa标记pnn,来测量染色强度。与未治疗的细胞相比,1mm和2mm的pnni不足以引起细胞中pnn形态和表达的实质性改变。相反,jd009和jd013治疗在0.5mm和1mm浓度下改变了细胞中pnn的表达。
[0062]
图15:长期pnni治疗优先减少腹侧角(vh)中由关键pnn成分标记的神经束膜网(pnn)的表达。将在损伤后12周获得的大鼠脊髓切片(t4-6)染色,并在vh中分析强度。pnni部分减少了pnn的数量,如聚集蛋白聚糖(acan;m)和紫藤凝集素(wfa;n)所标记的pnn,特别是在损伤后。共聚焦图像显示在有损伤的vh中整体acan(a-f)和wfa(g-l)的表达(a-c,g-i)。pnni-治疗的假手术(d,j)动物显示pnn总体表达的改变。然而,单独用pnni治疗(e,k)或用pnni和训练联合治疗(f,l)的损伤动物,显示出vh中wfa表达的减少。比例尺,100μm。对于所有图形,误差线
±
sd;每个治疗组n=3。统计学,单因素anova;显著性水平:*p《0.05**p《0.01***p《0.001。
具体实施方式
[0063]
发明人惊奇地发现,4-甲基伞形酮(本文称为“本发明的pnn抑制剂(pnni)”)可用于治疗神经系统病症。
[0064]
4-甲基伞形酮是小分子,具有以下化学结构:
[0065][0066]
4-甲基伞形酮的衍生物可用于本发明的用途和治疗方法中。4-甲基伞形酮的衍生物可以是4-甲基伞形酮的修饰形式。
[0067]
在实施方案中,4-甲基伞形酮的衍生物是以下结构的化合物:
[0068]
红色数字表示碳位置
[0069]
其中可以加入一个或多个烷基、芳基、酰基、二甲氨基、羟基、羟甲基、甲氧基、甲基、吗啉代和磺酰基取代基。取代可以发生在任何位置。
[0070]
取代可以在c4位置。取代可以是烷基、芳基、酰基、二甲氨基、羟基、羟甲基、甲氧基、甲基、吗啉代和磺酰基取代基中的一个或多个。在一个实施方案中,nr1r2可以在c4加成至甲基基团(ch3)上,其中r1和/或r2可以各自独立地是h、烷基、芳基、酰基、磺酰基。优选地,r1和r2是烷基。烷基可以是c1至c
18
,例如c1至c6。
[0071]
这种衍生物具有如下结构:
[0072][0073]
在一个实施方案中,or1可以在c4加成至甲基基团(ch3)上,其中r1可以是烷基、芳基、酰基。优选地,r1是羟乙基。
[0074]
这种衍生物具有如下结构:
[0075][0076]
取代可以在c3位置。取代可以是烷基、芳基、酰基、二甲氨基、羟基、羟甲基、甲氧基、甲基、吗啉代和磺酰基取代基中的一个或多个。
[0077]
取代可以在c5位置。取代可以是烷基、芳基、酰基、二甲氨基、羟基、羟甲基、甲氧基、甲基、吗啉代和磺酰基取代基中的一个或多个。
[0078]
取代可以在c6位置。取代可以是烷基、芳基、酰基、二甲氨基、羟基、羟甲基、甲氧基、甲基、吗啉代和磺酰基取代基中的一个或多个。
[0079]
取代可以在c8位置。取代可以是烷基、芳基、酰基、二甲氨基、羟基、羟甲基、甲氧基、甲基、吗啉代和磺酰基取代基中的一个或多个。
[0080]
在一个实施方案中,取代可以在c1位置。取代可以是烷基、芳基、酰基、二甲氨基、羟基、羟甲基、甲氧基、甲基、吗啉代和磺酰基取代基中的一个或多个。优选地,衍生物是下式的化合物
[0081][0082]
其中位置1的o被nr1取代。r1可以是芳基、酰基。优选地,r1是烷基。
[0083]
值得注意的是,在本发明的实施方案中,衍生物是具有以下结构的分子或化合物。
[0084]
jd01-009:
[0085][0086]
iupac命名:4-[(二甲氨基)甲基-7-羟基-2h-1-苯并吡喃-2-酮
[0087]
jd01-013:
[0088][0089]
iupac命名:7-羟基-4-[(吗啉-4-基)甲基]-2h-1-苯并吡喃-2-酮
[0090]
在实施方案中,pnni是羟甲香豆素(c
10
h8o3)。
[0091]
应当理解,4-甲基伞形酮或其衍生物的药学上可接受的盐、代谢物或前药可用于本发明的用途和治疗方法中。本文公开的与本发明的pnni相关的特征、用途和方法也适用于4-甲基伞形酮的衍生物、盐、代谢物和前药。
[0092]
本发明的另一方面提供了4-甲基伞形酮衍生物或其盐,以及包含所述衍生物的组合物。该衍生物是本文公开的衍生物。
[0093]
神经束膜网(pnn)是遍布中枢神经系统的致密细胞外基质结构。pnn包裹神经元的表面。特别地,在脊髓中发现了被pnn包裹的神经元群。pnn包围脊髓中的大多数(~97%)α运动神经元(mn)。pnn为聚集蛋白聚糖(acan)/cspg-阳性。例如,在脊髓损伤后,pnn在病变部位降解,但在远离损伤的部位保持完整。尽管pnn在病变部位降解,但抑制性cspg在疏松的细胞外基质中上调。
[0094]
发明人惊奇地发现,4-甲基伞形酮,即本发明的pnni,下调透明质酸和cpsg,因此去除中枢神经系统中的pnn。pnn的去除打开了可塑性的窗口,并促进了受试者的再生。
[0095]
如所附实施例中所示,本发明的pnni诱导透明质酸的减弱,这通过围绕小清蛋白(pv)阳性神经元的透明质酸结合蛋白(habp)强度的降低来指示。
[0096]
发明人还发现,本发明的pnni还具有抑制中枢神经系统中cspg合成的功能。减少cspg促进可塑性。
[0097]
在这方面,本发明的pnni可用于通过促进可塑性和再生来治疗神经系统病症。这一行动有助于恢复。
[0098]
神经系统的病症可以是受试者的中枢或外周神经系统的病症。神经系统的病症可以是与至少一种病变的形成相关的任何病症。病变是与cspg相关的病变。与未患有该病症的受试者相比,cspg可以上调。病变可能是神经胶质疤痕。
[0099]
病变可以是斑块。病变可以在脊髓内或脊髓附近。病变可能在大脑中。
[0100]
神经系统病症可以选自包括创伤、损伤、感染、变性、结构缺陷、肿瘤、血流中断和自身免疫疾病的组。病症可以选自但不限于中风、短暂性脑缺血发作、出血、脑膜炎、脑炎、贝尔麻痹、脑或脊髓肿瘤、帕金森病、多发性硬化、肌营养侧索硬化(als)、亨廷顿舞蹈病、阿
尔茨海默病和脑瘫。
[0101]
神经系统病症可以是脊髓损伤。损伤可以在脊髓的任何段。应当理解,脊髓损伤可以是任何类型的脊髓损伤,并且都包括在本文中。
[0102]
当用于治疗脊髓损伤的上下文中,本发明的pnni及其衍生物破坏pnn形成,并从pnn和形成的神经胶质疤痕中去除ha和cspg。这打开了可塑性和再生的窗口,以促进脊髓损伤后的恢复。
[0103]
本发明的pnni可以在脊髓损伤后的任何时间施用。它可以在损伤后立即施用、在损伤后1小时内施用、在损伤后2-12小时内施用,或在损伤后前7天内的任何时间施用。当脊髓损伤是慢性脊髓损伤时,可以在损伤后的任何时间施用。受试者可以接受如上所述的本发明的pnni的初始施用,然后任选进行长期施用。它可以是连续的每日治疗或阶段性治疗。施用可以持续任意数月或数年,通常为约1个月至约36个月,或6个月至12或24个月。可以理解的是,施用的方式和时间将取决于损伤引起的程度。
[0104]
本发明的pnni可以与康复组合施用给受试者。康复可以发生在施用本发明的pnni之前、施用期间,即同时、或施用之后,或其任意组合。本发明的pnni可以是本发明的组合物。适宜的康复方法是本领域已知的,并且都在本文考虑的范围内。考虑用于本发明的实施例包括在garc
í
a-al
í
as等和wang等(garcia-alias等,2009;王等,2011)公开的那些。
[0105]
本发明的pnni可以与电刺激组合施用。电刺激可以发生在施用本发明的pnni之前、施用期间,即同时、或施用之后,或其任意组合。本发明的pnni可以是本发明的组合物。适宜的电刺激方法是本领域已知的,并且都在本文考虑的范围内。实施例包括us62/800,817或us16/781,696中的那些。
[0106]
本发明的pnni可以与其它治疗方法组合施用给受试者,以最大化功能恢复。其它治疗可以是对脊髓损伤的治疗。这种治疗是本领域已知的。治疗可以是isp肽或修饰的isp肽。
[0107]
本发明的pnni可以是药物组合物。在这方面,本发明提供了包含治疗有效量的4-甲基伞形酮或其衍生物的药物组合物。该药物组合物用于本文公开的治疗中。
[0108]
本发明还提供了用于治疗神经系统病变的本发明的pnni。病变可以是受试者中枢或外周神经系统中的任何病变或疤痕。
[0109]
在一个实施方案中,病变是脊髓损伤后形成的神经胶质疤痕。在这方面,应当理解,本发明提供了用于治疗脊髓损伤的pnni。该治疗可以促进脊髓损伤后的恢复。病变可能是神经胶质疤痕。病变可以是蛋白质聚集斑块。其它实施例包括淀粉样病变、tau聚集体和路易体中的一种或多种。
[0110]
对病变的治疗可以是完全或部分去除。治疗可以是破坏病变。治疗可以使相关区域恢复正常功能。
[0111]
本发明的pnni或本发明的组合物的导入或施用方法包括但不限于皮内、肌内、腹膜内、静脉内、皮下、鼻内、硬膜外、鼻内、脑内、经直肠和口服途径。它可以是舌下滴剂。本发明的pnni或本发明的组合物可以通过任何方便的途径施用,例如通过输注或弹丸注射,通过上皮或粘膜皮肤衬里(例如口腔粘膜、直肠和肠粘膜等)吸收。施用可以是全身施用或局部施用。此外,可能需要通过任何适宜的途径(包括脑室内和鞘内注射)将本发明的制剂或组合物引入中枢神经系统;脑室注射可以通过例如连接在储液器上的脑室导管来实现。本
发明的pnni或组合物可以配制成缓释或持续释放。
[0112]
本发明的pnni或组合物可以按照常规程序配制。本发明的pnni可以配制成适于其施用的制剂。通常,本发明的pnni或本发明的组合物可以配制成口服给药。本发明的pnni或本发明的组合物可以被配制用于注射。在脊髓损伤的上下文中,注射可以直接进入脊髓。注射可以直接进入胶质疤痕。
[0113]
本发明的pnni或本发明的组合物可以配制成从医疗装置中释放。医疗装置可以是可植入装置,例如贴片或支架。
[0114]
本发明的pnni和包含本发明的pnni的组合物可以以多种适宜的形式制备/配制和/或施用。这种形式包括,但不限于,例如,液体、半固体和固体剂型,例如液体溶液(例如,可注射和不溶性溶液)、分散体或悬浮液、乳液、微乳液、片剂、丸剂、粉末、脂质体、树枝状聚合物和其它纳米颗粒、微粒和栓剂。应当理解的是,形式可以取决于预期的施用方式。
[0115]
在脊髓损伤的上下文中,由于受试者的病症,本发明的pnni或组合物可以作为初始剂量静脉内施用。随后的剂量可以口服和/或静脉注射。施用方法取决于患者的病症、损伤的程度和/或部位。
[0116]
应当理解,本发明的pnni的剂量取决于待治疗的病症和病症的严重程度以及受试者。这将取决于多种因素,包括所用化合物的活性、代谢稳定性和该化合物的作用时间长短、年龄、体重、总体健康状况、性别、饮食、施用方式和时间、排泄率、药物组合、特定病症的严重程度以及接受治疗的个体。当然,可能存在需要更高或更低剂量范围的个别情况,这也在本发明的范围内。例如,该组合物可以以5至60mg/kg体重/天的剂量施用,例如10-50mg/kg体重,优选17-42mg/kg体重/天。在一个实施方案中,向受试者施用1000至3000mg/天,优选1000至2000mg/天,优选地,向受试者施用1200至1300mg/天。数量和频率最适合该目的。根据每个受试者的需要,应用或施用的频率可以变化很大,应用或施用的推荐范围为每月一次至每天十次,优选每周一次至每天四次,更优选每周三次至每天三次,甚至更优选每天一次或两次。根据受试者的需要,治疗的时间长短可以有很大的不同。在优选实施方案中,提供了的重复使用。
[0117]
剂量可以是适宜儿科使用的剂量。
[0118]
在实施方案中,pnni被配制成口服施用的片剂形式。该片剂可包含大于400mg的本发明的pnni,优选含量为500mg至600mg。每片为一剂,剂量频率可以是每天两次,或每天三次。
[0119]
在实施方案中,受试者可以每天接受2至3次剂量,例如片剂,持续数月,例如2至6个月,或3至4个月,并且任选地可以有一段时间不施用药物,例如2至6个月,或3至4个月。然后可以重复这种方案。剂量可以如本文所述。
[0120]
实施例
[0121]
实施例1
[0122]
在急性挫伤性脊髓损伤动物模型的脊髓中,口服施用pnni增强了脊髓损伤的功能恢复
[0123]
方法
[0124]
从查尔斯河实验室(charles river laboratories)(坎特伯雷,英国)获得成年雌性lister-hooded大鼠(200-250g)。将大鼠成对圈养在中央生物医学服务中心(利兹大学,
英国),环境温度控制在(20
±
1℃),光照/黑暗周期为12h(07:00光照)。所有程序和实验均符合1986年英国动物(科学程序)法案。
[0125]
图4概述了这项研究的时间轴。
[0126]
椎板切除术和挫伤(cx)损伤
[0127]
使用异氟烷作为麻醉剂(o2中掺杂5%用于诱导,o2中掺杂1-2%用于手术期间),将动物剃毛并灭菌。暴露脊椎段t7-13,并在t8进行背部椎板切除术。稳定脊椎段t7和t8,同时使用无限水平冲击器(精确系统和仪器(precision systems and instrumentation),llc,费尔法克斯站,va)在t9段提供200kdyn cx(中度损伤)。缝合肌肉,用自动夹子闭合皮肤。在手术后,立即进行皮下注射镇痛剂(vetagesic buprenorphine;0.015mg/kg;汉瑞祥公司动物健康部(henry schein animal health),敦夫里斯,英国)和抗生素(拜有利恩诺沙星;2.5mg/kg;汉瑞祥公司动物健康部,敦夫里斯,英国),并在手术后持续注射三天。
[0128]
治疗
[0129]
在外科手术cx损伤后,根据治疗模式对动物进行分组,以测试小分子pnn抑制剂(pnni),即4-甲基伞形酮,对促进sci后增强恢复的功效。
[0130]
由于康复作为sci治疗的重要性,pnni和康复训练组合组被包括在内,以寻找相容性问题。
[0131]
药理学施用
[0132]
从损伤当天开始药物治疗(pnni;2g/kg,来自0.2g/ml的储备溶液)。此剂量高于pnni治疗非cns相关疾病的许可剂量,并且是通过初步体外实验确定的。与填喂法相反,口服施用通过注射器给药实现,每天两次以完成每日剂量。
[0133]
由于pnni是口服化合物,因此可以控制施用时间长短。首先,从损伤/手术日至终止治疗日长期施用该药物。
[0134]
康复
[0135]
训练包括分布式练习四足间歇踏车训练,以提供特定任务的康复。第一次训练在损伤后天数(dpi)7开始,进行如下所述的运动行为测试。每天的训练包括10分钟的跑步机训练,然后休息10分钟,最后10分钟的跑步机训练。大鼠每周接受五次最大速度训练,每次在跑步机上10分钟内保持连续踏步。
[0136]
运动评估
[0137]
在整个研究过程中,对后肢(hl)功能的行为和功能评估进行了评估。
[0138]
basso、beattie和bresnahan(bbb)hl运动开阔场地测试
[0139]
使用bbb hl运动量表在急性sci范例的不同时间点评估hl运动能力。使用开阔运动场地(定制的有机玻璃o形圈:直径80cm,高30cm)进行bbb测试,将动物放置在该场地持续4分钟(图2)。每个bbb试验由两个个体同时评估。为了客观,将所得分数汇总并平均。bbb测试使用0-21的分级标准评估hl运动功能。根据动物的bbb评分,将动物分为三大类:早期阶段(0-7分)表现出很少或没有肢体运动;中期阶段(8-13分)伴随着不协调步伐的发作;和晚期阶段(14-21分)表现为fl和hl协调和稳定(basso等,1995)。损伤后,在1dpi进行bbb以确认损伤,然后从7dpi开始每周进行一次。如果动物也接受了康复训练,则事先进行bbb。
[0140]
von frey分析
[0141]
使用von frey方法评估hl感官功能的改变,以寻找痛觉过敏和神经病理性疼痛。
在测试开始之前,一次让四只动物适应具有金属丝网底的有机玻璃笼子(图3)大约15至20分钟,直至一般运动和梳理活动停止。von frey细丝(20个的touch test
tm
感官评估套件;#39337500;徕卡生物系统公司,米尔顿凯因斯,英国,图3c)通过网底笼压在hl脚垫的更敏感的足底弓上,其中肢体的缩回被认为是积极的结果。退缩也被认为是积极的反应,而行走是模糊的反应,需要在适当的延迟后重新测试。所有动物的左后爪和右后爪连续进行,以在刺激之间提供足够的间隔。如chaplin等(1994)(chaplan等,1994)描述的,进行感官测试程序和分析,使用dixon上下法(dixon,1980)确定每个hl的50%缩回阈值。
[0142]
组织学
[0143]
组织制备
[0144]
给动物服用过量的戊巴比妥钠(pentoject;henry schein;200mg/kg;腹膜内注射)来深度麻醉而不停止心脏功能。然后,使用磷酸钠缓冲液(pb;0.12m磷酸二氢钠;0.1m naoh;ph 7.4),然后是4%多聚甲醛(pfa;在pb中;ph 7.4)用于组织固定,进行穿心灌注。解剖出脑和脊髓,后固定于pfa(4%;4℃)过夜,并在30%蔗糖溶液(30%v/w蔗糖的pb溶液;4℃)中冷冻保护直至组织饱和。切除左大脑半球和适宜的脊髓段,并在最佳温度培养基中冷冻(oct;徕卡fsc 22冻节媒介(leica fsc 22 frozen section media);徕卡生物系统公司(leica biosystems)),然后在-80℃下储存直至切片。使用低温恒温器(徕卡cm1850;徕卡生物系统公司)将组织切片,分成用于自由漂浮切片的40μm横切面,并收集至含有生理缓冲液(pbs;0.13m氯化钠、0.7m磷酸氢二钠、0.003m磷酸二氢钠;ph 7.4)的48孔板中,以在转移至30%蔗糖溶液(用于在4℃储存)之前除去oct。
[0145]
免疫组织化学技术
[0146]
在室温(rt)下,将切片在tris缓冲盐水(tbs;0.1m tris碱,0.15m nacl;ph 7.4)洗涤三次,每次5min,以除去蔗糖残余物。然后将组织在0.3%tbst(1x tbs溶液和0.3%v/vtriton x-100)和3%正常驴血清(nds;v/v)中封闭2小时。然后将切片转移至含有一抗的封闭缓冲液(0.3%tbst中的3%nds;ph 7.4)中于4℃共孵育。
[0147]
在一抗或凝集素孵育后,用tbs洗涤切片三次(10min;rt)。为了可视化每个一抗染色,然后将组织与针对一抗的种类的荧光缀合的二抗(1:500;2h;rt)在黑暗中共孵育。然后将组织在tbs中洗涤三次(10min;rt)同时避光。在tris非盐水(tns;0.5m tris,ph 7.6)中进行最后一次洗涤,以减少风干前的沉淀。将组织固定在superfrost plus载玻片上,风干并用固定介质fluorsave
tm
试剂(emd millipore)盖片。
[0148]
一抗为:cspg成分,包括acan、bcan和ncan。
[0149]
凝集素类:生物素化紫藤凝集素(bio-wfa)、生物素化透明质酸结合蛋白(bhabp)。
[0150]
神经元总数和被pnn包围的神经元数量由两位独立的研究人员进行量化,他们对该研究不知晓。结果用单因素anova进行统计显著性分析。
[0151]
pnni的机制和药代动力学的确定
[0152]
目的(1)pnni如何穿过血脑屏障(bbb)的机制
[0153]
背景:我们的初步结果清楚地表明,口服施用pnni导致中枢神经系统(cns)中pnn的减少。然而,pnni如何诱导这种效应的机制仍不清楚。pnni会穿过bbb并在原位耗尽pnni吗?或者pnni会系统地耗尽底物库,因此较少的底物会穿过bbb进行pnn合成?
[0154]
方法:成年大鼠连续10天口服施用pnni。将在第0、5和10天收集大鼠的血液、尿液
和脑脊液,用于分析样本中存在的pnni浓度。使用荧光光谱测定法来测量pnni的存在。
[0155]
动物数量:8只大鼠
[0156]
目的(2)重建pnni的药代动力学
[0157]
背景:以前发表的药代动力学数据表明,小鼠和大鼠口服施用的致死剂量分别为7.5和6.2g/kg动物体重。然而,在我们对小鼠进行的初步实验中,我们连续6个月对小鼠施用了6.8-12.8g/kg的剂量,但小鼠并未表现出任何致死性,也未观察到不良症状。这促使我们质疑之前的药代动力学是否建立正确。本文中,我们旨在重建pnni在成年大鼠和小鼠中的药代动力学。
[0158]
方法:全面的药代动力学研究将不可避免地涵盖导致动物致死的剂量。因此,在英国,不可能根据任何单独的项目许可证进行此项工作。我们将使用charles river公司(一家合法的动物供应商)的服务来进行这些实验。
[0159]
相关信息可以在这个网址找到:
[0160]
https://www.criver.com/products-services/safety-assessment/dmpk/pharmacokinetics-toxicokinetics?region=3696
[0161]
结果与结论
[0162]
每周使用basso、beattie和bresnahan(bbb)评估运动功能。然后使用霍乱毒素b和生物素化葡聚糖对神经束进行逆向和顺向追踪。
[0163]
bbb和von frey测试的结果
[0164]
如图5(a)所示,在所有实验组中,所有大鼠都受到了相似的挫伤强度。(中)basso、beattie和brenahan(bbb)评分表明,在中度t9挫伤损伤后,pnni治疗的大鼠(每日治疗)具有更好的功能恢复。在损伤后5周,媒介物治疗的大鼠达到~10分,而4-mu治疗组达到~15分。(右)使用von frey毛发测试,来自不同治疗组的大鼠在触觉敏感性上没有显示出任何差异。所有组n=11。
[0165]
这些结果表明,使用pnni的口服治疗增强了功能恢复。
[0166]
免疫化学结果
[0167]
如图15所示,长期pnni治疗减少了腹侧角(vh)中由关键pnn成分标记的pnn的表达。将在损伤后12周获得的大鼠脊髓切片(t4-6)染色,并在vh中分析强度。pnni部分减少pnn的数量,如聚集蛋白聚糖(acan)和紫藤凝集素(wfa)标记的pnn,特别是在损伤后。
[0168]
实施例2
[0169]
pnni对大鼠体内pnn的清除
[0170]
结果与结论
[0171]
如图1所示,完整大鼠口服施用pnni 10天后,pnn减少。图1a和b显示缺乏acan染色(cspg;pnn标记),特别是在pnni治疗后观察到的腹侧角中。图c和d显示pnni治疗诱导小清蛋白(pv)阳性神经元周围的透明质酸结合蛋白(habp)的减弱。
[0172]
这表明pnni在去除脊髓中的cspg方面也是有效的。
[0173]
实施例3
[0174]
在此实施例中,本发明人引入了非侵入性化合物pnn抑制剂(pnni),以可逆地去除pnn并增强可塑性,从而通过破坏pnn形成来去除pnn,以增强急性脊髓损伤后的恢复。
[0175]
pnn包围脊髓中的大多数(~97%)α运动神经元(mn)
[0176]
大多数pnn的研究是在脑样本中进行的,发明人试图确定脊髓中被pnn包裹的神经元群体。图8是脊髓中α运动神经元上pnn存在的代表性图像(galtrey等,2008;irvine和kwok,2018)。
[0177]
pnni在体外和体内动态去除pnn
[0178]
以前开发的人胚胎肾293t(hek)细胞模型,被工程化以表达必需的ecm成分(透明质酸合酶3(has-3)和hapln-1),是诱导细胞周pnn样结构(pnn
hek细胞)形成所必需的(kwok等,2010),这些细胞模型被用于研究pnni在体外去除pnn的功效(图9a-i)。尽管未治疗的pnn
hek细胞显示了wfa阳性pnn的清晰信号(图9b),但对pnn
hek细胞施用两天的pnni治疗(0.5mm或1.0mm),去除了86.4
±
4.47%(f
3,66
=73.60,所有治疗时间点vs.未治疗时间点,p《0.0001)的wfa阳性染色。在治疗后三天内,染色强度部分恢复至基线凝集素结合的43.6
±
14.6%(治疗后3天和5天vs.治疗期间,p《0.0001,图9c-i)。这些结果表明,pnni介导的pnn去除是动态和可逆的。
[0179]
口服施用pnni去除脊髓中的pnn
[0180]
因此,体内研究了pnni治疗,通过口服或腹膜内(i.p.)注射短期施用(10天),每天两次。给药10天后终止的动物组织学显示,与未治疗的动物相比,施用pnni的两种方法都足以降低整个cns的wfa阳性结合(图1j-o)。有趣的是,与皮质相比,pnni在下调凝集素在脊髓中的结合方面似乎更有效(图9j-o)。重要的是,这表明pnni或其代谢产物可以穿过血脑屏障影响cns中的ecm。脊髓背角中的定量可以表明,口服施用pnni 10天诱导了wfa阳性部分的部分去除,达到基线ecm水平的71.0
±
7.20%(t(3)=5.15,p=0.0142;图9p)。短期口服pnni也下调ha结合蛋白染色至64.0
±
5.84%(habp;t(3)=7.69,p=0.00456),而对于hapln-1,为背角基线水平的68.3
±
8.09%(t(3)=5.01,p=0.0153)。由于口服pnni治疗是非侵入性的,并且在体内对神经ecm产生了足够的作用,以下用lister hooded大鼠进行的pnni剂量实验使用了这种施用方法。
[0181]
用pnni的急性短期治疗部分去除pnn没有显示出副作用
[0182]
首先,发明人质疑在整个cns中去除pnn是否会影响正常的感官和运动功能。为了对此进行研究,成年雌性lister hooded大鼠(n=11)被给予10天的口服pnni治疗并接受常规行为测试。这些结果表明,短期pnni足以在接受治疗的完整大鼠中诱导感官功能的变化,但不能诱导运动功能的变化(图9q-s)。与相同大鼠的治疗前基线(7.9
±
2.73g)相比,显示短期pnni施用将缩回阈值降低至5.5
±
2.03g,代表敏感性增加约30%(t(10)=2.76;p=0.02图9q)。开阔场地运动试验发现短期pnni治疗无显著差异,所有动物在basso、beattie,bresnahan后肢(hl)量表中均达到最高分21分(basso等,1995)(n.s;p=1;数据未显示)。当使用更熟练的行走任务来评估运动时,hl运动活动在pnni治疗和未治疗的动物之间也表现出一致性(图9r),在水平阶梯上,正确迈步(绿色)的时间约为92.7
±
0.82%(n.s.,t(16)=0.259,p=0.799),错误(黄色)和未迈步(红色)分别占所有步中的5.43
±
0.70%(n.s.,t(16)=-0.978,p=0.343)和1.92
±
0.41%(n.s.,t(16)=1.15,p=0.268)。类似地,前肢(fl)的表现不受短期pnni的影响(图9s),未迈步为1.13
±
0.24%(n.s.,t(16)=-1.64,p=0.121),错误4.35
±
0.54%(n.s.,t(16)=1.97,p=0.0667)和正确迈步94.4
±
0.56%(n.s.,t(16)=-1.34,p=0.197)。不考虑治疗,hl和fl功能表现一样好,具有低百分比的迈步误差。总之,在正常成年大鼠中急性去除pnn,轻微增加了受试肢体的敏感性,这与相同治
疗模式下背角中的pnn成分的下调一致,但不影响运动功能。没有观察到其它行为差异。
[0183]
感官运动皮层(m1)包含运动活动的高度组织化的地形学表现,其在对感官运动学习或神经元损伤的反应中受到结构和功能可塑性的影响。
[0184]
使用皮质内微刺激(icms),通过与完整的基线hl和fl代表或“中心”进行比较,hl和fl皮质运动代表图被用于研究长期使用预期可塑性增强剂pnni治疗后的完整/假手术动物的m1的功能组织(见虚线;图10)。虽然pnni治疗减少了能够诱发hl活动的总面积(假手术/pnni组vs.完整组,f
2,12
=10.7,p=0.00764,假手术/pnni组vs.假手术组,p=0.00914),这是由于一些完整的hl中心不再能够诱发hl活动(假手术组vs.假手术/pnni组,f
2,12
=18.6,p=0.00411,完整组vs.假手术/pnni组,p《0.001;图10a-h)。成对脉冲协议(gigout等,2013;luhmann等,1995)被用作平行研究皮质内gaba能抑制的可能变化的指标,使用体外感官运动皮质切片,其中短和长刺激间期的成对脉冲比率(ppr)允许我们分别研究gabaa和gabab受体介导的抑制。健康的对照切片表现出明显的成对脉冲抑制(ppr:~0.5),然而,这没有被假手术或pnni治疗改变(n.s.,f
2,65
=1.52,p=0.227,图10i;f
2,65
=2.35,p=0.0960,图10j)。这表明,观察到的pnni诱导的hl面积减少是由于结构重组,而不是皮质抑制的改变
‑‑
神经可塑性的证据。
[0185]
像在hl代表中观察到的那样,pnni诱导了假手术动物中fl代表的功能重组(图10k-s)。尽管诱发fl活动的总表面积没有变化(n.s.,f2,12=0.249,p=0.784;图2n),这些的发生率在完整的fl中心降低(f2,12=5.61,p=0.0226;图2p)但似乎没有侵占hl区域(n.s.,f2,12=0.900,p=0.437,图2r;f2,12=2.38,p=0.142,图10s)。经pnni治疗后,诱发hl或fl活动所需的皮质刺激阈值没有显著变化。由于短期pnni施用增加了触觉敏感性,而长期pnni治疗诱导了结构重组,我们可以得出结论,如上所述,pnni对pnn的部分去除足以产生有利于在多个cns水平上促进功能可塑性的环境。由于这些可塑性变化已在经治疗的完整动物中观察到,这可能导致适应性不良的连接。
[0186]
pnni和/或损伤独立增强脊髓损伤大鼠的皮质可塑性
[0187]
在胸中段sci后,icms不能诱发hl活动(图11b-c),尽管有开阔场地hl行走的证据,但在完整的fl和hl区域都可以诱发fl活动(图11d-e)。损伤和/或治疗未导致诱发fl活动所需的最小或平均皮质刺激阈值发生变化(补充表1)。损伤和/或长期pnni治疗诱发fl活动的表面积没有总的变化(n.s.,f
2,9
=0.403,p=0.683,图5f),与完整fl中心相关的面积也没有变化(n.s.,f
2,9
=0.891,p=0.452,图5k;f
2,9
=0.0685,p=0.934,图5l)。然而,损伤和长期pnni治疗的组合导致与以前诱发hl活动的区域相关的更大百分比的fl活动(从4.27
±
1.56%至23.9
±
8.01%),这表明与假手术对照组相比,该组代表性的fl区域整体转移而不是扩展至完整的hl中心(假手术组vs.sci/pnni组,f
2,9
=2.58,p=0.197,图5m;假手术组vs.sci/pnni组,f
2,9
=5.23,p=0.0432,图11n)。
[0188]
针对体外皮质切片的局部兴奋性的平行实验使用了场电位振幅的单个输入-输出曲线(图11g),该曲线通过波尔兹曼方程拟合,产生psp
max
、i
50
和斜率因子。重要的是,这表明sci和pnni治疗的组合给出了与所有其它实验组显著不同的结果(greenhouse-geisser f
1.49,13.4
=1.61,所有组vs.sci/pnni组,p《0.001,图11g),表明pnni和损伤一起产生了皮质内突触传递增加的环境,特别是在更高的刺激强度下,这可能有助于在该组中观察到的m1的重组。成对脉冲协议还表明单独损伤,而不是sci/pnni的组合,在短而不是长的刺激间隔
影响成对脉冲反应,其中ppr从0.42
±
0.26增加至0.63
±
0.24(假手术组vs.sci/赋形剂组,f
2,57
=3.09,p=0.052,图5h-i),这意味着sci诱导gaba
a-受体介导的传递减少。总之,尽管损伤和pnni都能够独立诱导m1中cspg含量的类似降低,但只有长期pnni施用才能充分增强可塑性,以促进皮质运动图的重组,这表明额外的机制,例如观察到的局部皮质内兴奋性的增加,可能是这些功能变化的基础。
[0189]
在持续康复的同时限制pnni治疗可以使运动功能恢复
[0190]
为了提高可塑性以实现有效的功能恢复,我们施用pnni8周,同时进行11周的康复。在持续康复的同时限制pnni施用允许进一步的后肢(hl)运动,但不允许感官恢复(图12)。当在实验(8周pnni治疗)结束前2-3周终止pnni治疗以允许pnn重建时,在继续进行康复训练的动物中观察到进一步的hl改善(a)。条形图显示了,在pnni施用结束时,损伤后周数(wpi)9和12wpi时,能够实现前肢-后肢(fl-hl)协调的动物的百分比(b)。持续进一步康复训练(8周pnni t)的动物显示,从9wpi至12wpi,动物能够进行fl-hl协调的百分比增加(a和b)。堆叠条形图显示了,在9和12wpi,(c)hl和(d)前肢(fl)踩在水平阶梯上的分类,在经典阶梯评分系统中,踩中:得分为3-6,错误:1-2,未踩中:0(metz和whishaw,2009)。当限制pnni治疗且仅施用持续康复治疗时,hl在阶梯上的表现改善。虽然总误差减少(黑色),但受限的pnni治疗和康复训练特别减少了未踩中的hl步数(红色)。受限的pnni治疗伴随持续的训练也提高了fl的表现。e)在9和12wpi,进行的von frey分析确定的足底后爪的左-右(l-r)平均50%缩回阈值没有显示痛觉过敏。pnni治疗终止后,pnn的巩固不会诱导感官改变。(对于各组,8周pnni和8周pnni t,n分别为10和9。统计学,a,c-e:双向混合因子anova;显著性水平:*p《0.05**p《0.01和***p《0.001。a、c、d:误差线为
±
sem。)
[0191]
8周的pnni伴随持续康复部分恢复了fl区域的皮质重组为完整的组织。
[0192]
大约在胸中部中度挫伤损伤后15周,在立体定位坐标下,在右侧半球(a)于前囟上下5mm处(在每个尺度上标记为b)的开颅手术中进行皮质内微刺激(icms)(图13)。将单个icms图组合起来,给出每组的代表性热图,热图显示每个立体定位坐标的动物百分比,其中后肢(hl;b-c)活动不能够被诱发,但前肢(fl;d-e)活动能够被诱发。虚线轮廓表示hl(b-c)和fl(d-e)的完整基线面积,用于比较8周pnni施用组(b,d)和8周pnni伴随持续跑步机训练组(c,e)的功能可塑性。f)仅通过受限的pnni治疗伴随持续训练,fl表现的平均面积(mm2)减少至正常/完整水平。i)中示出了用于分析的测量值(g-h,j-k)。脊髓损伤后,在先前诱发hl活动的区域诱发fl活动(基线hl图显示为白色虚线轮廓d-e)。g)fl活动大部分能够在完整的fl区域内引起,在8周pnni t时有轻微的减少趋势(p=0.243)。h)经8周pnni治疗后,在完整fl区引起的总fl区的比例下降,只有持续训练有这种趋势(p=0.112)。j)损伤后,8周pnni治疗可在hl区诱发fl活动。然而,只有在持续训练的情况下,才观察到部分fl从hl区域收缩(p=0.514)。k)与未损伤的对照相比,在完整的hl区域中引起的fl区域的比例似乎增加(p=0.114,8周pnni;和p=0.177周pnni t)。
[0193]
这表明,受限的pnni结合持续康复限制了适应性不良的可塑性,并巩固了从康复至功能恢复的新建立的联系。
[0194]
pnn类似物的初步结果
[0195]
jd009和jd013可以在比pnni更低的浓度下减弱pnn的形成
[0196]
鉴于pnni在水溶液中几乎不溶(nagy等,2015年),开发了溶解度增加的pnni衍生
物(jd009和jd013)。发明人假设,由于在设计pnni类似物时,活性所需的羟基官能团没有改变,因此它们应该保留有效还原pnn的能力。
[0197]
为了比较pnni、jd009和jd013在减少pnn形成中的功效,使用n-乙酰半乳糖胺结合凝集素wfa标记pnn,进行了免疫细胞化学。将pnn-hek293细胞在体外暴露于0.5mm和1mm的化合物3天。dmso媒介物对照也包括在内,使用量不超过总体积的0.1%。在匹配的目标区域(roi)中对每个细胞的wfa荧光强度进行定量,并将总wfa荧光强度标准化为细胞数。下图显示,与未治疗的细胞相比,0.5和1mm剂量的pnni不足以引起细胞中pnn形态和表达的实质性变化。相反,jd009和jd013治疗在0.5mm和1mm浓度下改变了细胞中pnn的表达。
[0198]
参考文献
[0199]
24 moshayedi p,ng g,kwok jcf,yeo gsh,bryant ce,fawcett jw,franze k,guck j(2014)the relationship between glial cell mechanosensitivity and foreign body reactions in the central nervous system.biomaterials 35,3919-25.(106 citations)
[0200]
2013
[0201]
23
§ dick g,tan ct,alves jn,ehlert eme,miller gm,hsieh-wilson lc,sugahara k,oosterhof a,van kuppevelt th,verhaagen j,fawcett jw and kwok jcf(2013)semaphorin 3a binds to the perineuronal nets via chondroitin sulfate type e motifs in rodent brains.j biol chem 288(38),27384-395.(72 citations)
[0202]
22^ vo t*,carulli d*,ehlert eme*,kwok jcf*,dick g,mecollari v,moloney eb,neufeld g,de winter f,fawcett jw,verhaagen j(2013)the chemorepulsive axon guidance protein semaphorin 3a is a constituent of perineuronal nets in the adult rodent brain.mol cell neurosci 56c,186-200.(67 citations)
[0203]
21 vorobyov v,kwok jc,fawcett jw,sengpiel f.(2013)effects of digesting chondroitin sulfate proteoglycans on plasticity in cat primary visual cortex.j neurosci 33,234-43.(40citations)
[0204]
2012
[0205]
20^ kwok jc,yuen ly,lau,wk,zhang fx,fawcett jw,chan ys,shum dky(2012)chondroitin sulfates in the developing rat hindbrain confine commissural projections of vestibular nuclear neurons.neural dev.7,6-13.
[0206]
19^ kwok jc,warren p,fawcett jw(2012)chondroitin sulfate:a key molecule in the brain matrix.int j biochem cell biol.44,582-6.(83citations)
[0207]
18 tan cl,andrews mr,kwok jc,heintz tgp,gumy lf, r,fawcett jw(2012)kindlin-1 enhances axon growth on inhibitory chondroitin sulfate proteoglycans and promotes sensory axon regeneration.j neurosci 32,7325-35.(43citations)
[0208]
2011
[0209]
17^ kwok jc,tan cl,wang d,heller j,fawcett jw(2011)chondroitin sulfates in axon regeneration and plasticity.trends in glycosci and glycotech 133,201-11.
intrinsic rcgcncrativc ability of cns axons.elife 6,e26956.
[0238]
39
§ yang s,alves j n,hilton s,saksida lm,bussey tm,matthews rt,kitagawa h,spillantini mg,kwok jcf*,fawcett jw*(2017)antibody recognizing 4-sulphated chondroitin sulphate proteoglycans restores memory in tauopathy-induced neurodegeneration.neurobiolaging 59,197-209.
[0239]
38 kempf a,fritz r,boda e,kwok jcf,kaelin am,schmandke a,ristic z,tews b,fawcett jw,buffo a,pertz o,schwab me.(2017)control of cell shape,neurite outgrowth and migration by a novel nogo-a/hspg interaction.dev cell s1534-5807,30674-3.
[0240]
37
§
^ foscarin s,fawcett jw,kwok jcf(2017)brain ageing changes proteoglycan sulphation,rendering perineuronal nets more inhibitory.aging-us 9(6),1607-1622.
[0241]
36
§
^ djerbal l,lortat-jacob h*,kwok jcf*(2017)chondroitin sulfates and their binding molecules in the central nervous system.glycoconj j 34(3):363-376.
[0242]
2016
[0243]
35 sorg ba,berretta s,blacktop jm,fawcett jw,kitagawa h,kwok jcf,miquel m(2016)casting a wide net:role of perineuronal nets in neural plasticity.j neurosci 36,11459-11468.(51 citations)
[0244]
34
§ vecino e,kwok jcf(2016)the extracellular matrix in the nervous system:the good and the bad aspects.intech 2016,95-114.
[0245]
33 carulli d,kwok jcf,pizzorusso t(2016)perineuronal nets and cns plasticity and repair.neural plasticity 2016,4327082.
[0246]
32 de winter f,kwok jcf,fawcett jw,vo tt,carulli d and verhaagen j(2016)the chemorepulsive protein semaphorin 3a and perineuronal net-mediated plasticity.neural plasticity 2016,3679545.
[0247]
2015
[0248]
31 heller jp,kwok jcf,vecino e,martin kr and fawcett jw(2015)a method for the isolation and culture of adult rat retinal pigment epithelial(rpe)cells to study retinal diseases.front cell neurosci 9,449.
[0249]
30 smith pd,coulson-thomas vj,foscarin s,kwok jcf and fawcett jw(2015)“gag-ing with the neuron”:the role of glycosaminoglycan patterning in the central nervous system.exp neurol.274(pt b),100-14.
[0250]
29 tan cl,kwok jcf,heller jpd,zhao r,eva r,fawcett jw(2015)full length talin stimulates integrin activation and axon regeneration.mole cell neuro68,1-8.
[0251]
28
§ rowlands d,sugahara k,kwok jcf(2015)glycosaminoglycans and glycomimetics in the central nervous system.molecules20,3527-48.
[0252]
2014
proteoglycans,hyaluronan,link proteins and tenascin-r in the rat spinal cord.eur j neurosci.27:1373-1390.
[0266]
garcia-alias,g.,s.barkhuysen,m.buckle,and j.w.fawcett.2009.chondroitinase abc treatment opens a window of opportunity for task-specific rehabilitation.nat neurosci.12:1145-1151.
[0267]
garcia-alias,g.,h.a.petrosyan,l.schnell,p.j.horner,w.j.bowers,l.m.mendell,j.w.fawcett,and v.l.arvanian.2011.chondroitinase abc combined with neurotrophin nt-3 secretion and nr2d expression promotes axonal plasticity and functional recovery in rats with lateral hemisection of the spinal cord.j neurosci.31:17788-17799.
[0268]
gigout,s.,j.louvel,d.rinaldi,b.martin,and r.pumain.2013.thalamocortical relationships and network synchronization in a new genetic model“in mirror”for absence epilepsy.brain research.1525:39-52.
[0269]
hooven,m.d.2017.opportunities and challenges in biologic drug delivery.american pharmaceutical review.
[0270]
irvine,s.,and j.kwok.2018.perineuronal nets in spinal motoneurones:chondroitin sulphate proteoglycan around alpha motoneurones.international journal of molecular sciences.19:1172.
[0271]
kwok,j.c.,g.dick,d.wang,and j.w.fawcett.2011.extracellular matrix and perineuronal nets in cns repair.dev neurobiol.71:1073-1089.
[0272]
kwok,j.c.f.,d.carulli,and j.w.fawcett.2010.in vitro modeling of perineuronal nets:hyaluronan synthase and link protein are necessary for their formation and integrity.journal of neurochemistry.114:1447-1459.
[0273]
luhmann,h.j.,t.mittmann,g.van luijtelaar,and u.heinemann.1995.impairment of intracortical gabaergic inhibition in a rat model of absence epilepsy.epilepsy research.22:43-51.
[0274]
metz,g.a.,and i.q.whishaw.2009.the ladder rung walking task:a scoring system and its practical application.j vis exp:1204.
[0275]
nagy,n.,h.f.kuipers,a.r.frymoyer,h.d.ishak,j.b.bollyky,t.n.wight,and p.l.bollyky.2015.4-methylumbelliferone treatment and hyaluronan inhibition as a therapeutic strategy in inflammation,autoimmunity,and cancer.frontiers in immunology.6.
[0276]
nakamura,t.,k.takagaki,s.shibata,k.tanaka,t.higuchi,and m.endo.1995.hyaluronic-acid-deficient extracellular matrix induced by addition of 4-methylumbelliferone to the medium of cultured human skin fibroblasts.biochemical and biophysical research communications.208:470-475.
[0277]
pizzorusso,t.,p.medini,n.berardi,s.chierzi,j.w.fawcett,and l.maffei.2002.reactivation of ocular dominance plasticity in the adult visual cortex.science.298:1248-1251.
[0278]
silver,j.,and j.h.miller.2004.regeneration beyond the glial scar.nat rev neurosci.5:146-156.
[0279]
vo,t.,d.carulli,e.m.e.ehlert,j.c.f.kwok,g.dick,v.mecollari,e.b.moloney,g.neufeld,f.de winter,j.w.fawcett,and j.verhaagen.2013.the chemorepulsive axon guidance protein semaphorin3a is a constituent of perineuronal nets in the adult rodent brain.molecular and cellular neuroscience.56:186-200.
[0280]
wang,d.,r.m.ichiyama,r.zhao,m.r.andrews,and j.w.fawcett.2011.chondroitinase combined with rehabilitation promotes recovery of forelimb function in rats with chronic spinal cord injury.j neurosci.31:9332-9344.
[0281]
warren,p.m.,s.c.steiger,t.e.dick,p.m.macfarlane,w.j.alilain,and j.silver.2018.rapid and robust restoration of breathing long after spinal cord injury.nature communications.9:4843.
[0282]
usptor参考文献
[0283]
9415218;9101769;9393409;9409023;7326649;8805542;9409011;62/800,817;62/828,853
[0284]
mg fehlings et al traumatic spinal cord injury nat.rev.dis.primers 3.17018(2017)
[0285]
ros lynch neurological report 21
st august 2018 jsuggitt ms otr/l clt
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。