具有集成的基于流动的测定的流体传输装置及其使用方法
1.相关申请的交叉引用
2.本技术要求2019年12月11日提交的名称为“fluid transfer devices with integrated flow-based assay and methods of using the same”的美国临时专利申请序列第62/946,680号的优先权和权益,其公开内容通过引用以其整体并入本文。
技术背景
3.本文所述的实施方案总体上涉及体液样品的获取和即时诊断测试(point of care diagnostic testing),并且更具体地涉及具有集成的基于流动的测定系统的体液传输装置,例如允许初始即时诊断测试的侧向流测定(lateral flow assay)。
4.保健从业者使用肠胃外获得的体液对患者进行各种类型的微生物诊断测试以及其它广泛的诊断测试。在一些情况下,一些严重患者疾患的有效治疗可能是时间依赖性的,治疗延迟可能导致发病率和/或死亡率的风险增加。例如,败血症是通常由细菌感染(或不太常见的真菌或病毒感染)引起的严重的患者疾病。败血症是对原本可以是普通感染的感染的不寻常的全身反应,可能代表了免疫系统对损伤的反应模式。高度炎症反应之后通常是免疫抑制阶段,在此期间存在多器官功能障碍并且患者易受医院感染。败血症患者通常出现不适、发热、寒战和白细胞增多,这可提示医生评价此类患者血流中细菌的存在——通常通过细菌培养测试。
5.随着细菌培养测试和/或其它先进诊断技术的发展和改进,可以提供给临床医生的信息的速度、准确性(灵敏度和特异度)和价值不断提高。此类诊断技术的实例可包括例如微生物检测、分子诊断、基因测序(例如,脱氧核糖核酸(dna)、核糖核酸(rna)、下一代测序(ngs)等)、生物标志物鉴定等。一些已知的培养方法和/或其它诊断技术可能容易受到污染,这可能会产生不准确的、扭曲的、掺入杂质的、假阳性的、假阴性的和/或否则不代表患者的实际状况(或体内状况)的结果。反过来,这些结果可导致错误的、不准确的、混乱的、不确定的、低置信度的和/或否则不希望的临床决策。在一些情况下,污染可能由生物物质的存在引起,所述生物物质包括在预期样品源外部的细胞和/或其它外部污染物,其被无意地包括在被分析的体液样品中。一些已知的装置和/或系统可用于降低用于测试的体液样品的污染和/或掺假的可能性,这可以降低不准确或错误的诊断测试结果的可能性并导致更好的患者结果。例如,一些已知的装置可被设计成传输和隔离初始体积的体液,所述体液更可能含有污染物。
6.虽然此类诊断技术能够提供来自清洁或无掺杂体液测试的高度灵敏度和/或特异度信息,但测试通常需要6小时至约5天或更长时间才能产生结果。此外,已知的诊断技术通常使用需要训练有素的人员和/或通常使用专门定制的培养方案来鉴定各种细菌物种的系统来进行。因此,此类培养方法和/或诊断技术不适用于治疗某些快速进展的疾病可能需要的快速诊断和/或高效筛查。例如,败血症可迅速进展为多器官功能障碍和/或死亡,这可促使医生在收到诊断测试结果之前开出治疗处方(例如,抗生素)。
7.因此,存在对体液的快速测试(例如使用侧向流动测定的即时诊断测试或其它快
速诊断技术)的需要。另外,存在对将快速测试(例如,侧向流动测定)集成到装置(其可用于从患者获取额外的体液样品,例如,配置成获取具有减少的污染的体液样品的装置)中的需要。
技术实现要素:
8.本文所述的实施方案和方法涉及具有允许初始即时诊断测试的集成的基于流动的测定(例如,侧向流动测定)的体液传输装置。在一些实施方案中,系统包括基于流动的测定装置和流体传输装置。流体传输装置具有被配置成与体液源流体连通地放置的入口和被配置成与样品储器流体连通地放置的出口。流体传输装置包括隔离室和与隔离室选择性连通的端口。隔离室被配置成与入口流体连通地放置以在流体传输装置处于第一状态时接收第一体积的体液。出口被配置成与入口流体连通地放置以在流体传输装置处于第二状态时接收第二体积的体液。基于流动的测定装置被配置成耦接到端口以在流体传输装置处于第三状态时接收第一体积的体液的一部分。基于流动的测定装置被配置成提供与第一体积体液的一部分中存在目标分析物相关的指示。
附图说明
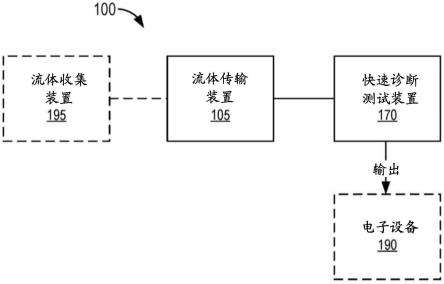
9.图1是根据实施方案的流体传输和测定系统的示意图。
10.图2是根据实施方案的侧向流动测定装置的示意图。
11.图3是根据实施方案的流体传输和测定系统的示意图。
12.图4是根据实施方案的流体传输和测定系统的示意图。
13.图5a和图5b分别是根据实施方案的处于第一状态和第二状态中的流体传输和测定系统的示意图。
14.图6a至图6d是分别根据实施方案的处于第一状态、第二状态、第三状态和第四状态中的流体传输和测定系统的至少一部分的示意图。
15.图7a至图7d是分别根据实施方案的处于第一状态、第二状态、第三状态和第四状态中的流体传输和测定系统的至少一部分的示意图。
16.图8是根据实施方案的流体传输和测定装置(或系统)的透视图。
17.图9a至图9d是分别以第一、第二、第三和第四状态示出的图12的流体传输和测定装置(或系统)的剖视图。
18.图10是根据实施方案的流体传输和测定装置(或系统)的透视图。
19.图11是图10的流体传输和测定装置(或系统)的侧视图,所述装置的壳体是部分透明的,以示出该装置的内部特征。
20.图12a和图12b是处于第一状态的图11的流体传输和测定装置(或系统)的侧视图。
21.图12c是处于第二状态的图11的流体传输和测定装置(或系统)的侧视图。
22.图12d是处于第三状态的图11的流体传输和测定装置(或系统)的侧面透视图。
23.图13至图16是根据实施方案的流体传输和测定装置(或系统)的各种视图。
24.图17至图20是根据不同实施方案的流体传输和测定装置(或系统)的各种视图。
具体实施方案
25.本文所述的任何流体传输装置可被配置成接收、获取和/或传输体液的流动、推注、体积等。另外,本文所述的任何流体传输装置可包括用于对通过流体传输装置获取的至少一部分体液进行一种或多种快速诊断测试的集成装置。在一些实施方案中,流体传输装置可以是注射器、传输适配器和/或被配置成接收体液流的任何其它装置。在一些实施方案中,流体传输装置可以是流体转向和/或隔离装置,其被配置成接收初始体积的体液并将其与例如在培养测试等中使用的后续取样体积隔离。在此类实施方案中,用于快速诊断测试的集成装置可以被配置成接收至少一部分初始体液体积或至少一部分后续取样体积。用于快速诊断测试的集成装置可以是例如侧向流动测定和/或任何其它合适的诊断测试装置。用于快速诊断测试的集成装置可用于测试体液的量,并至少提供定性结果,该定性结果又可在用于视觉检查的装置上输出或由该装置输出。在其它情况下,测试装置可以将与结果相关联的数据传输到电子设备(例如,经由有线或无线网络),所述电子设备然后可对数据执行任何合适的分析,并且可以例如在设备的显示器上以图形方式表示至少一些数据(例如,定性或定量测试结果)。
26.在一些实施方案中,快速诊断测试装置可被包括或集成到流体传输装置(例如,样品收集装置)中,并用于提供获取的体液的初始测试结果。最初的测试结果可用获取的体液的附加测试诸如培养测试来补充。例如,集成快速诊断测试装置(在本文中也称为“快速测试装置”或“初始测试装置”)可以提供相对快速地测试体液中微生物(例如,革兰阳性菌、革兰阴性细菌、真菌或病毒)或其它类型的生物物质(例如,特定类型的细胞、生物标志物、蛋白质、抗原、酶、血液组分等)的存在的方法,所述微生物或其它类型的生物物质的存在可为临床医生制定有关治疗策略的决策提供信息。在一些实施方案中,初始测试装置可以测试能够导致和/或以其它方式导致败血症的细菌和/或其它感染,从而允许临床医生提供快速治疗,诸如广谱抗生素。此外,本文所述的流体传输装置可获取额外的取样体积,其可用于更灵敏的测试(诸如培养测试)或其它技术,诸如分子聚合酶链式反应(pcr)、磁共振和其它磁分析平台、自动化显微镜检查、空间克隆分离、流式细胞术、全血(“不含培养物”)样本分析(例如,ngs)和相关技术、形态动力学细胞分析和/或其它用于表征患者样本和/或用于检测、鉴定、分型、分类和/或表征特定生物体、抗生素敏感性等的普通、先进或发展中的技术。
27.在一些实施方案中,系统包括基于流动的测定装置和流体传输装置。流体传输装置具有被配置成与体液源流体连通地放置的入口和被配置成与样品储器流体连通地放置的出口。流体传输装置包括隔离室和与隔离室选择性连通的端口。隔离室被配置成与入口流体连通地放置以在流体传输装置处于第一状态时接收第一体积的体液。出口被配置成与入口流体连通地放置以在流体传输装置处于第二状态时接收第二体积的体液。基于流动的测定装置被配置成耦接到端口以在流体传输装置处于第三状态时接收第一体积的体液的一部分。基于流动的测定装置被配置成提供与第一体积体液的一部分中存在目标分析物相关的指示。
28.在一些实施方案中,系统包括流体传输装置,所述流体传输装置具有被配置成接收来自体液源的体液流的入口、被配置成与样品储器流体连通地放置的出口、被配置成接收第一体积的体液的隔离室和至少暂时与隔离室流体连通的端口。流体传输装置被配置成在第一状态与第二状态之间转换,在第一状态下,隔离室与入口流体连通以接收第一体积
的体液,在第二状态下,出口与入口流体连通以接收第二体积的体液。当隔离室接收第一体积的体液时,隔离室的端口允许气流流过隔离室。基于流动的测定装置被配置成在第二状态下耦接到流体传输装置。当耦接到流体传输装置时,基于流动的测定装置的一部分与端口接合,以允许第一体积的体液的一部分从隔离室传输到基于流动的测定装置。该基于流动的测定装置被配置成提供与该部分初始体积的体液中目标分析物的存在相关的指示。
29.在一些实施方案中,方法包括将流体传输装置的入口设置成与体液源流体连通,从入口接收第一体积的体液并将使其进入流体传输装置的隔离室,其中在接收期间,流体传输装置的流动控制器允许气体流过流动控制器,但不允许体液流通过流动控制器,以使隔离室通气。在所述第一体积的体液被接收在所述隔离室中之后,将所述流体传输装置从所述第一状态转换到第二状态。响应于流体传输装置处于第二状态:在流体传输装置的入口与出口之间建立流体连通,以允许第二体积的体液流到与出口流体连通的样品储器。将第一体积体液的一部分从隔离室输送到基于流动的测定装置的取样元件,其至少暂时与隔离室流体耦接;以及将缓冲溶液输送到基于流动的测定装置的取样元件。
30.在一些实施方案中,系统包括流体传输装置和侧向流动测定装置。流体传输装置包括被配置成与体液源流体连通地放置的入口、被配置成与样品储器流体连通地放置的出口和被配置成接收初始体积的体液的隔离室。流体传输装置被配置成在(1)第一状态、(2)第二状态和(3)第三状态之间转换,在第一状态下,隔离室与入口流体连通以接收初始体积的体液,在第二状态下,出口与入口流体连通以接收后续的体液流,在第三状态下,侧向流动测定装置耦接到与隔离室流体连通的端口。侧向流动测定装置被配置成接收一部分初始体积的体液,并确定所述初始体积的体液中的目标分析物的存在。
31.如本说明书和/或本文所包括的任何权利要求中所使用的,除非上下文中另有明确规定,否则单数形式“一个/种(a)”、“一个/种(an)”和“该(the)”包括复数指示物。因此,例如,术语“一个(a)构件”旨在表示单个构件或构件的组合,“一种(a)材料”旨在表示一种或多种材料,等等。
32.如本文中所用,“体液”可包括直接或间接从患者体内获得的任何流体。例如,“体液”包括但不限于血液、脑脊液、尿、胆汁、淋巴液、唾液、滑液、浆液、胸膜液、羊水、粘液、痰、玻璃状液(vitreous)、空气等,或其任意组合。
33.如本文中所用,词语“近端”和“远端”分别指更靠近和远离将装置放置成与患者接触的用户的方向。因此,例如,首先接触患者身体的装置的末端将是装置的远端,而装置的相对端(例如,由用户操作的装置的末端)将是装置的近端。
34.如本文中所用,术语“约”、“大致”和/或“基本上”在与一个或多个所述值和/或一个或多个几何结构或一种或多种关系结合使用时,旨在传达如此定义的值或特性名义上是所述值或所述特性。在一些情况下,术语“约”、“大致”和/或“基本上”通常可以表示和/或通常可以预期在期望公差(例如,所述值或特性的
±
10%)内的所述的值或特性。例如,约为0.01的值可以包括0.009和0.011,约为0.5的值可以包括0.45和0.55,约为10的值可以包括9至11,约为100的值可以包括90至110。类似地,当表面名义上平行时,第一表面可被描述为基本上平行于第二表面。虽然所述的值、结构和/或关系可能是期望的,但是应该理解,由于例如制造公差或其它实际考虑(诸如,通过装置、导管、管腔等的一部分施加的压力或力),可能会出现一些变化。因此,术语“约”、“大致”和/或“基本上”在本文中可用于说明此类公
差和/或考虑。
35.如本文中所用,术语“第一”、“初始”和/或“取样前”在用于描述体液体积时,可互换使用,以描述在获取“样品”体积前被收集、转向、隔离、测试等的体液的量、分数或体积。“第一”、“初始”和/或“取样前”体积可以是预定的、确定的、所需的和/或给定的体液的量。例如,诸如血液等的体液的预定和/或所需的取样前体积可以是一滴血、几滴血、约0.1毫升(ml)、约0.2ml、约0.3ml、约0.4ml、约0.5ml、约0.6ml、约0.7ml、约0.8ml、约0.9ml、约1.0ml、约2.0ml、约3.0ml、约4.0ml、约5.0ml、约6.0ml、约7.0ml、约8.0ml、约9.0ml、约10.0ml、约20.0ml、约50.0ml的体积和/或其间的任何体积或体积分数。在其它情况下,取样前体积可以大于50ml或小于0.1ml。作为具体实例,预定和/或所需的取样前体积可介于约0.1ml至约5.0ml之间。作为另一个实例,取样前体积可以是例如任何数量的管腔的体积或组合体积(例如,针的管腔和/或组合管腔,其形成从体液源到初始收集室、部分、储器等的流动路径的至少一部分)。作为又一个实例,取样前体积可以是,例如,足以进行初始测试或取样前测试(例如,使用侧向流动测定和/或任何其它快速测试装置的快速诊断测试)的体液体积。
36.如本文中所用,术语“第二”、“后续”和/或“取样”在用于描述体液体积时,可互换使用,以描述在收集第一、初始和/或取样前体积的体液后收集的体液的量、分数或体积。“第二”、“后续”和/或“取样”体积可以是在收集、转向、隔离和/或测试取样前体积的体液后收集的体液的随机体积或预定体积或所需体积。在一些情况下,体液的所需取样体积可以是约10ml至约60ml。在其它情况下,体液的所需取样体积可以小于10ml或大于60ml。在其它情况下,所需取样体积可以至少部分地基于要对取样体积执行的一个或多个测试、测定、分析和/或处理。
37.在一些实施方案中,第二、后续和/或取样体积的体液可用于一个或多个样品或诊断测试,例如培养测试等。在一些情况下,在收集、隔离、分离和/或测试“取样前”体积的体液之后收集“取样”体积的体液可导致取样体积含有污染物诸如皮肤上驻留的微生物等的可能性较低。因此,体液的取样体积可适用于原本易于由于污染而导致不准确的结果的灵敏测试。
38.本文所述的实施方案和/或其部分可由一种或多种生物相容性材料形成或构造。在一些实施方案中,可基于组成材料的一种或多种性质(例如刚度、韧度、硬度、生物活性等)来选择生物相容性材料。合适的生物相容性材料的实例包括金属、玻璃、陶瓷或聚合物。合适金属的实例包括医药级不锈钢、金、钛、镍、铁、铂、锡、铬、铜和/或其合金。聚合物材料可以是可生物降解的或不可生物降解的。合适的生物可降解聚合物的实例包括聚丙交酯、聚乙交酯、聚丙交酯-共-乙交酯(plga)、聚酸酐、聚原酸酯、聚醚酯、聚己内酯、聚酯酰胺、聚(丁酸)、聚(戊酸)、聚氨酯和/或其掺混物和共聚物。不可生物降解的聚合物的实例包括尼龙、聚酯、聚碳酸酯、聚丙烯酸酯、聚硅氧烷(硅酮)、乙烯-乙酸乙烯酯和其它酰基取代的醋酸纤维素的聚合物、不可降解的聚氨酯、聚苯乙烯、聚氯乙烯、聚氟乙烯、聚(乙烯基咪唑)、氯磺化聚烯烃、聚环氧乙烷和/或其掺混物和共聚物。
39.现在参考附图,图1是根据实施方案的流体传输和测定系统100的示意图。虽然下面可能描述了各种组件、元件、特性和/或功能,但是应当理解,它们仅通过示例而非限制的方式呈现。本领域技术人员将理解,如本文所述,可以在不改变流体传输和测定系统100执行获取体液样品和提供快速诊断测试方法的功能的能力的情况下,对流体传输和测定系统
100的形式和/或特性进行改变。
40.流体传输和测定系统100(本文中也称为“系统”)可以至少包括流体传输装置105和快速诊断测试装置170。在一些实施方案中,系统100可以任选地包括至少一个电子设备190和/或至少一个流体收集装置195。
41.流体传输装置105(本文中也称为“传输装置”)可具有任何合适的形状、尺寸和/或配置,如本文参考具体实施方案所描述的。在一些实施方案中,传输装置105可被配置成从患者抽取体液(例如,血液)并将其转移到传输装置105中。另外,传输装置105可被配置成将至少一些抽取的体液转移到一个或多个其它装置、储器、容器、小瓶、机器、测试、测定等,例如快速诊断测试装置170和/或一个或多个任选的流体收集装置195。
42.在一些实施方案中,传输装置105可被配置成将一定量或体积的体液传输、引导和/或转向到(或通过)传输装置105的一个或多个部分中,并且随后将这些量或体积传输到与传输装置105耦接或集成的一个或多个装置中,传输到一个或多个样品储器、容器、瓶子等中。例如,传输装置105可被配置成将第一分数、量或体积的体液传输到或通过传输装置105的第一或隔离部分,并随后将第二分数、量或体积(例如,后续量)的体液传输到传输装置105的第二或取样部分。在一些实施方案中,传输装置105和/或传输装置105的隔离部分可被配置成将第一量的体液(例如,在传输装置105的隔离部分内)与后续量的体液隔离,如本文参考具体实施方案进一步详细描述的。在一些实施方案中,传输装置105可以被配置成将至少一些第一量的体液(例如,包含在传输装置105的隔离部分中)传输到快速诊断测试装置170,并将至少一些第二量的体液传输到一个或多个任选的流体收集装置195。
43.快速诊断测试装置170(本文也称为“快速测试装置”或简称为“测试装置”)可具有任何合适的形状、尺寸和/或配置,如本文参考具体实施方案所描述的。在一些实施方案中,快速测试装置170可以可移除地耦接到传输装置105或其任何合适的部分(例如,入口部分、出口部分、隔离部分、取样部分和/或任何其它合适的部分)。在其它实施方案中,快速测试装置170可被集成到传输装置105中。例如,可以整体地或单一地形成传输装置105和快速测试装置170和/或以其它方式集成。在其它实施方案中,传输装置105可以包括和/或可以形成端口、适配器和/或接收部分,快速测试装置170可以耦接到所述端口、适配器和/或接收部分,或者快速测试装置170可以插入所述端口、适配器和/或接收部分,以在它们之间建立流体连通。在一些此类实施方案中,将快速测试装置170耦接到传输装置105可用于将一个或多个流动控制器、阀、隔膜、端口、密封件等从关闭或密封状态转换成打开状态,以允许传输装置105与测试装置170之间流体连通。
44.在一些实施方案中,快速测试装置170可被配置成从传输装置105接收第一量的体液,并使用第一量的体液来执行一个或多个测试、测定和/或诊断程序。例如,快速测试装置170可以是色谱侧向流动免疫测定(chromatographic lateral flow immunoassay),其可以测试任何合适的分析物、生物标志物、蛋白质、分子、颗粒等。色谱侧向流动免疫测定(本文称为“侧向流动测定”或“lfa”)通常是基于硝酸纤维素的装置,其被配置成检测样品(例如,生物样品和/或体液样品,诸如血液、尿液等)中目标分析物的存在。一般而言,lfa包括一系列毛细管床,诸如多孔纸片、微结构化或烧结的聚合物等,它们可被设置在基底上的期望位置和/或布置中,以引导样品(例如,第一数量的体液中的至少一些)沿着lfa的一部分流动。
45.lfa可用于广泛的应用,其中期望具有相对快速、易于使用且低成本的方法用于快速抗原检测。lfa通常在几乎没有或没有样品或试剂制备的情况下进行,这可以在短至数分钟内(或者如果需要更灵敏的测试结果,则可能需要更长时间)获得可用的测试结果。此外,在一些实施方案中,lfa可被配置成测试人体响应于体内条件(例如,诸如败血症等感染)而产生的分析物和/或生物标志物,这又意味着这种lfa对污染物(例如,皮肤上驻留的微生物等)具有相对低的敏感度,所述污染物可被包含在通过传输装置105从患者抽取的第一数量的体液中。
46.通常,根据目标分析物上结合位点的尺寸和/或数量,使用两种类型的lfa。具体来说,竞争性lfa通常在测试较小的分析物时使用,而夹心lfa通常在测试较大的分析物时使用。就上下文而言,家庭妊娠试验是公知的夹心侧向流动测定。在一些情况下,可能需要使用夹心lfa来测试与例如体液(诸如血液)样品中的败血症和/或其它感染状况相关的抗原、分析物和/或生物标志物。虽然本文所述的实施方案包括和/或实现了夹心lfa,但是应该理解,实施方案不限于此。例如,本文所述的任何实施方案可以使用和/或执行竞争性lfa和/或任何其它合适的快速诊断测试装置。
47.图2中示出了用于上下文的夹心lfa 170a的示意性实例。夹心lfa 170a(本文中称为“lfa”)包括基底171,其上有取样元件172、缀合元件(conjugate element)173、捕获元件174、控制元件175和吸液芯176。基底171可以具有任何合适的形状、尺寸和/或配置。例如,基底171可以是矩形背衬卡(backing card)或条带,其具有恒定宽度和预定长度,能够提供足够的表面积以容纳lfa 170a的各种组件。基底171可由半刚性聚合物制成,所述聚合物被设计成提供均匀性和平坦特性。基底171可包含一种或多种压敏粘合剂,其被配置成有助于附着lfa 170a的各种组件,如本文进一步描述的。
48.如所显示的,取样元件172通常被设置在基底的一端,并被配置成接收取样体积。取样元件172可以是垫,其提供表面以接收用于分析的血液和/或其它生物流体的样品,并有助于以平滑、连续和均匀的方式将样品输送到侧流测试条带的其它组件。取样元件172可具有任何合适的形状、尺寸和/或配置。将缀合元件173在下游方向上邻近取样元件172设置。缀合元件173包含被配置成包括所需生物活性颗粒的干燥基质(例如,盐-糖基质)。包含在基质中的生物活性颗粒包括已被固定在缀合元件173之上或之中的特异性抗体和/或亲和试剂(例如,dna适体、蛋白质结合剂等)。可以基于lfa 170a被配置来检测的目标分子(例如,抗原或分析物)来选择抗体和/或亲和试剂。另外,将抗体和/或亲和试剂直接或间接缀合于被配置成允许检测的分子。例如,抗体可用有色颗粒(例如,具有蓝色的胶乳、具有红色的胶体金和/或任何其它合适的颗粒)、荧光颗粒、磁性颗粒、用于随后信号产生的酶等来标记。因此,标记的抗体可与所需的抗原或分析物结合,从而产生标记的目标分析物177,其可以在lfa 170a的其它部分中检测或通过lfa 170a的其它元件检测。
49.捕获元件174被设置在缀合元件173附近和/或下游,并且包含已被固定在捕获元件174之中或之上的颗粒或分子。颗粒或分子可被配置成与标记的分析物177结合,从而将标记的分析物177捕获或固定在捕获元件174之中或之上。随着捕获和/或固定的标记分析物177的浓度增加(例如,捕获元件174内的分子数量增加),检测分子(例如,有色标记物)的光密度也增加。以这种方式,lfa 170a被配置成呈现离散的比色信号线、区域或条,以指示取样体积中目标分析物的存在(例如,阳性测试结果)。
50.控制元件175被设置在捕获元件174附近和/或下游。控制元件175包含已被固定在控制元件175之中或之上的颗粒或分子。与捕获元件174相反,包含在控制元件175中的颗粒或分子可被配置成结合到多种不同颗粒,例如标记的分析物177、未结合到抗原的标记的生物活性颗粒等。因此,控制元件175可被配置成结合和/或以其它方式固定原本未被固定在捕获元件174之中或之上的标记颗粒。因此,控制元件175可以呈现有色部分或条带,其可用于显示反应发生和/或测试已经进行。例如,如果取样体积中不存在目标分析物,则可能希望确认测定被正确执行,并且阴性结果(捕获元件174上不存在有色条带或捕获元件174未呈现有色条带)指示取样体积的状况,而不是lfa 170a的故障。吸液芯176被设置在控制元件175的附近和/或下游,并被配置成吸收或芯吸未被固定在捕获元件174和/或控制元件175之中或之上的样品的部分。
51.测定
52.lfa 170a可用于测试任何合适的目标分析物、生物标志物、分子、颗粒等在取样体积(例如,血液样品或任何其它合适的体液样品)中的存在。例如,本文所述的任何实施方案可以包括和/或实现lfa(例如,lfa 170a)和/或任何其它合适的基于流动的快速诊断系统,所述快速诊断系统被配置成测试特定分析物或生物标志物的存在,所述特定分析物或生物标志物可提供用于诊断患者状况例如败血症的信息。
53.例如,血液乳酸(lactate)可以是用于败血症的临床诊断和管理的生物标志物。在一些情况下,许多其它生物标志物可以作为乳酸的替代物或补充物来指导临床决策。合适的生物标志物的非穷尽列表可以包括促炎细胞因子和/或趋化因子,其与败血症的过度炎症期(hyper-inflammatory phase)相关;c-反应蛋白和/或降钙素原(pct),其是响应感染和炎症而合成的;与嗜中性粒细胞和/或单核细胞活化相关的生物标志物;抗炎细胞因子,其与败血症的免疫抑制期相关;和/或单核细胞和/或淋巴细胞的细胞表面标志物的改变。在一些情况下,多重lfa中的促炎和抗炎生物标志物的组合可以用于,例如,鉴定在实质性器官功能障碍之前正在发展严重败血症的患者。在一些情况下,可以合成一种或多种适体,以靶向特定的促炎生物标志物、抗炎生物标志物和/或任何其它合适的生物标志物,诸如本文所述的那些中的任一种。
54.乳酸
55.在一些实施方案中,本文所述的任何实施方案可用于检测乳酸生物标志物、pct生物标志物和/或本文所述的与败血症相关和/或以其它方式用于鉴定败血症的任何其它合适的生物标志物。例如,在一些实施方案中,快速测试装置170可被配置成使用例如便携式血气分析仪来测试体液(例如,血液)样品中的血液乳酸水平。在其它实施方案中,快速测试装置170可以是被配置成测试血液(例如,全血、血清等)乳酸生物标志物(例如,抗原)的lfa(例如,lfa 170a)。例如,使用血清乳酸水平诊断败血症的有效性如下表1所示,该表给出了根据需要血管加压药(vasopressor)(例如,导致血管收缩的药剂)的败血症患者的血清乳酸水平的急性住院死亡率的研究结果。
56.表1:
[0057][0058]
乳酸(lactic acid)是葡萄糖在组织中厌氧分解的终产物,其可以分解成乳酸(lactate),羟基一元羧酸阴离子,其是由羧基的去质子化产生的乳酸的共轭碱。当组织的能量需求不能通过充分的需氧呼吸来满足时,体内乳酸的形成就发生了。乳酸可以在血液中转运到肝脏,在肝脏中通过cori循环转化回葡萄糖。然而,如果肝脏和肾脏不能充分清除乳酸,积累的乳酸浓度会导致乳酸酸中毒。临床上,酸中毒的原因可以分类为a型紊乱和b型紊乱,a型紊乱中存在组织氧合减少,诸如败血症,b型紊乱由某些药物和/或毒素引起,伴随全身性疾病等。医学证据表明,乳酸水平持续升高的患者发病率和死亡率增加。体内过量的乳酸还会导致出血、呼吸衰竭、创伤、癫痫发作、局部缺血、肾脏问题、肝脏疾病、组织缺氧、休克、失血、贫血等。因此,乳酸监测对于诊断和评估缺氧情况下(即,其中体内乳酸水平升高超过可接受值的情况)出现的健康问题至关重要。据报道,健康无应激个体血液中乳酸的浓度在0.1至1.0毫摩尔(mm)的范围内。相比之下,重症患者,诸如出现严重败血症或脓毒性休克的患者,可表现出高于4mm的浓度。
[0059]
乳酸可作为两种光学异构体(l-乳酸和其镜像,d-乳酸)之一存在。用于检测和定量乳酸的分析方法包括高效液相色谱(hplc)、荧光测定法、比色试验、化学发光和磁共振光谱学。尽管这些方法可以提供准确的结果,但是它们存在一些缺点,诸如耗时的样品制备、使用昂贵的仪器以及需要训练有素的人员。因此,使用这些分析方法来检测和定量生物流体中的乳酸更适合于集中式实验室,并且它们作为即时诊断工具的实施可能受到限制。
[0060]
包括血液和/或血浆在内的生物流体中乳酸水平的检测也可以使用酶来实现。这些酶可被固定在固体表面或支持物(例如,生物传感器)上,以通过稳定过渡反应态(transition reaction state)或降低特定乳酸化学反应的活化能来提供催化乳酸化学反应的反应位点,产生一种或多种可被监测以将其演变与乳酸浓度相关联的种类。例如,可使用诸如l-乳酸氧化酶(lod)和l-乳酸脱氢酶(ldh)等酶来检测l-乳酸。lod是球状黄素蛋白,其可从诸如片球菌属(pediococcus)、气球菌属(aerococcus)、草绿色链球菌属(viridans)和分枝杆菌属(mycobacterium)等多种细菌源获得。lod的来源可以影响酶可以显示足够催化活性的ph范围,表现出介于4与9之间的典型范围。作为黄素单核苷酸(fmn)家族的一员,lod利用fmn作为辅因子来在其反应中催化羟基酸的氧化,所述反应涉及乙醇酸氧化酶、l-乳酸、单加氧酶、黄素细胞色素b2、长链α-羟基酸氧化酶和l-扁桃酸脱氢酶。lod可被固定在固体支持物上,并暴露于诸如血液和血浆等生物流体中,用于检测l-乳酸的存在。lod可以在溶解氧存在的情况下催化l-乳酸氧化成丙酮酸(pa),产生还原的lod和作为副产物的过氧化氢(h2o2)。乳酸氧化产生的过氧化氢可以通过二次化学和/或电化学反应来精确定量。例如,在lod酶存在的情况下乳酸氧化过程中产生的过氧化氢可被电化学还原或氧化,从而产生可被电极监测的电信号。然后,还原的lod酶可在电极上在第二反应步骤中被再氧化,如下面的反应方案中所示:
[0061][0062]
h2o2→
o2 2h
2e-[0063]
与lod类似,ldh酶可用于检测和定量各种生物流体中l-乳酸的存在。ldh是四级蛋白质,其可存在于动物、植物和原核生物。ldh存在于整个组织中,并在组织损伤时释放。ldh酶包括五种不同的同工酶形式,以微小的结构差异来区分。根据来源,已知lhd酶在5-8的相对较窄的ph范围内是稳定的,更具体地说,在约7.2-7.4的ph范围内是稳定的。ldh还可以通过其辅因子烟酰胺腺嘌呤二核苷酸(nad)催化l-乳酸到丙酮酸盐(pa)的反应,烟酰胺腺嘌呤二核苷酸可以以氧化(nad
)和还原(nadh)形式存在。在反应过程中,lhd将l-乳酸转化为丙酮酸盐(pa),并将nad
转化为nadh。然后,用ldh酶检测乳酸可通过次级反应实现,如上文参考用lod酶检测l-乳酸所描述的。例如,nadh可以在用电极产生的外加电势的影响下被电化学氧化,产生的电流与l-乳酸浓度成比例,如下面的反应式所示:
[0064][0065][0066]
如上所述,使用酶通过乳酸酶促氧化来检测生物流体中的乳酸依赖于乳酸向一种或多种副产物诸如nadh和过氧化氢(h2o2)的转化,所述副产物可以通过次级反应来精确定量。次级反应通常涉及在电极表面进行的电化学转化(例如,用于乳酸感测的电化学技术),该转化产生与样品中存在的乳酸的量成比例的瞬时电流。或者,如本文进一步描述的,乳酸的酶促反应的副产物可以通过光转移过程(例如,用于乳酸感测的电致化学发光和荧光技术)来定量。
[0067]
依靠电化学技术检测乳酸的生物传感器(即电化学生物传感器)使用固定在支撑基底上的酶,所述支撑基底位于电极表面附近或邻近电极表面。电化学生物传感器的性能特征可以根据酶的来源、包括ph和温度在内的环境条件、用于将酶固定到生物传感器上的方法、用于固定酶的基质或支持物的化学性质和/或电子转移机制而变化很大。酶可以根据不同的方法进行固定,它们的反应性取决于它们与支持物的相互作用、酶的性质以及吸附的种类、介质(mediator)和添加剂的存在。常见的酶固定化技术包括物理吸附、截留在透析膜或聚合物膜后面、通过交联剂共价偶联和掺入碳复合材料基质的本体内。
[0068]
与酶的固定化相关的挑战包括再现性、稳定性,以及由于抑制剂和/或污垢种类的演化和/或积累而导致的失活。例如,通过物理吸附固定在包含au电极的生物传感器上的lod酶在仅仅1个月的储存后可表现出50%的稳定性损失,而使用聚乙烯醇(pva)的聚合物基质固定在介孔二氧化硅中的lod酶在9个月后可表现出其初始活性的98%。因此,使用lod酶检测乳酸的传感器的开发需要确定合适的固定技术、合适的基质支持物以及使用和/或储存环境条件,使得酶的活性或保存期限可以长时间保持。
[0069]
乳酸检测的电化学生物传感器通常包括含有两个或三个电极感测平台的装置。乳酸的精确测量通常包括使用参比电极(通常由ag/agcl2制成),该参比电极保持在工作电极附近,以保持稳定和已知的电位。工作电极充当换能器,而反电极由于工作电极处的电势变化而建立了通过电流的路径。测量乳酸检测过程中产生的电信号的常用方法包括循环伏安法、电流分析法和电位测定法。电化学生物传感器可以提供高灵敏度、宽线性范围和快速响
应。然而,由于复杂的实验设置、由于污垢剂导致的系统钝化以及由于竞争性反应导致的信号减弱和干扰,它们的使用存在局限性。例如,在l-乳酸通过lod酶的酶促氧化过程中产生的过氧化氢(h2o2)的电化学定量需要高氧化电位,这导致由其它可电氧化的种类引起的干扰。
[0070]
被配置成测试血液(例如全血、血清等)的乳酸生物标志物(例如,抗原)的侧向流动测定(lfa)提供了替代工具来促进和/或帮助败血症的诊断。如上参考图2所示,可以在包括一个或多个装配在塑料背衬叠层或基底171上的组件的条带上进行lfa。被配置用于量化血液和/或其它生物流体中的乳酸的lfa的组件可以至少包括取样元件172和缀合元件173。
[0071]
取样元件172可以是垫,如上所述,该垫提供表面以接收血液和/或其它生物流体的样品用于分析,并有助于以平滑、连续和均匀的方式将样品输送到侧流测试条的其它组件。取样元件172可具有任何合适的形状和/或尺寸。在一些实施方案中,取样元件172的形状可以是矩形条,其被配置成吸附和接收一定体积的血液和/或其它生物流体的样品。在其它实施方案中,取样元件172的形状可以是矩形条带,其中其一端包括尺寸大于条带宽度的区域,以便于吸取一定体积的血液和/或其它生物流体的样品。例如,取样元件172可以是矩形条带,其包括连接到条带一端的圆形区域。取样元件172的圆形区域可以提供更大的表面积,用于通过微量移液管接收血液和/或其它生物流体的样品。备选地,在一些实施方案中,取样元件172可包括大直径圆形区域,该圆形区域具有在径向方向上源自圆形区域的中心的各种矩形条带。每个矩形条带可以便于将血液和/或其它生物流体样品的一部分输送到侧流测试条的其它组件,用于同时检测多种生物标志物(即,多路复用),和/或用于重复测定用于验证目的。
[0072]
取样元件172可被设置在塑料背衬叠层的表面上,以向lfa提供机械支撑。在一些实施方案中,取样元件172可以包括涂覆在样品垫的一个表面上的粘合剂,以有助于附着到塑料背衬叠层。取样元件172的形状和尺寸可以预先确定,使得取样元件可被设置在塑料背衬叠层上。可以选择取样元件172的厚度,以便于取样元件172粘附到塑料背衬叠层上,同时保持垫的机械结构。此外,可以选择取样元件172的厚度,以容纳大量的血液和/或其它生物流体,防止垫上的样品过饱和,并引导至塑料背衬叠层。例如,在一些实施方案中,取样元件172的厚度可以在0.18mm与0.34mm之间。
[0073]
取样元件172可由纤维素、硝酸纤维、玻璃纤维和/或任何其它合适的材料制成。在一些实施方案中,取样元件172可由被配置成促进约3至5mm/min的线性流速的纤维素膜和/或层析纸制成。取样元件172还可包括一种或多种化学试剂,所述化学试剂被配置成在将样品输送到其它下游部件之前对样品进行预处理。在一些实施方案中,取样元件172的表面可以用缓冲水溶液浸渍,所述缓冲水溶液提供具有受控ph的环境。在一些实施方案中,取样元件172的表面可以用缓冲溶液浸渍,所述缓冲溶液包括但不限于磷酸盐缓冲盐水(pbs)、2-乙磺酸(mes)、三(羟基甲基)氨基甲烷(tris)、哌嗪-n,n
′‑
双(pipes)、3-吗啉代丙烷-1-磺酸(mops)、2-[4-(2-羟基乙基)哌嗪-1-基]乙磺酸(hepes)、[三(羟基甲基)甲基氨基]丙磺酸(taps)、n-环己基-2-氨基乙磺酸(ches)和/或n-环己基-3-氨基丙磺酸(caps)。
[0074]
在一些实施方案中,取样元件172可以包括一个或多个部件,所述部件被配置成捕获和分离血液和/或其它生物流体中存在的可对lfa测定造成干扰的种类。例如,在一些实施方案中,取样元件172可包括一个或多个被配置成分离血液和/或其它生物流体样品中存
在的红细胞的区域。在一些情况下,被配置成分离血细胞的一个或多个区域可以是一个或多个分离垫,其可被设置在取样元件172上。在其它实施方案中,血液分离区域可以是位于取样元件172附近的垫。在一些情况下,血液分离垫可以包括一个或多个层,诸如聚酯基质和复合基质,其被设计成具有不同孔隙度和孔径分布的不对称形态,这有利于在较大的孔中捕获血液的细胞组分(即,红细胞、白细胞和血小板),同时允许血浆通过较小尺寸的孔向下游流动。
[0075]
用于检测和定量来自血液和/或其它生物流体样品的乳酸的lfa的缀合元件173可以是位于邻近取样元件172下游的垫。缀合元件173可包含干燥的基质(例如,盐-糖基质),其包括可以与乳酸反应并产生可以通过比色法检测的种类的生物活性种类,如本文进一步描述的。缀合元件173可被配置成容纳一种或多种生物活性种类,其可在与沉积在上游取样元件172上的移动液体样品接触时被释放。如上文参考取样元件172所述,缀合元件173可以是具有任何合适形状和/或尺寸的垫。在一些实施方案中,缀合元件173的形状可以是具有与取样元件172基本类似的尺寸和/或形状的条带。在一些实施方案中,缀合元件173和取样元件172可由单个垫制成,并且可被设置在其相对端,并且任选地附着到塑料背衬叠层的表面,以向lfa提供机械支撑。在又一另外的实施方案中,缀合元件173和取样元件171可由包括矩形条带的单个垫制成,在所述条带中,条带的第一端包括尺寸大于条带宽度的区域,以提供容纳用于乳酸氧化和比色检测的生物活性种类的区域,与条带的第一端相对的第二端尺寸大于条带宽度,以提供容纳一定体积的血液和/或其它生物流体样品的区域。或者,在一些实施方案中,缀合元件173可以包括多个矩形条带,所述矩形条带在径向方向上耦接到大直径圆形区域,其中大直径圆形区域被配置成容纳取样元件171。在这种配置中,每个缀合元件173可以有助于检测血液和/或其它生物流体的样品的一部分中存在的多个生物标志物(即,多路复用),和/或用于重复测定用于验证目的。
[0076]
缀合元件173可以包括干燥的基质,所述基质被配置成包括用于检测和定量血液和/或其它生物流体样品中的乳酸的所需生物活性种类。例如,在该实施方案中,缀合元件173的基质可以包括检测酶和定量酶。检测酶可被配置成对乳酸的催化氧化表现出高活性和高选择性,产生一种或多种副产物,可以通过次级化学反应来监测该副产物,以定量样品中存在的乳酸的浓度。例如,在一些实施方案中,缀合元件173的基质可包括检测酶,诸如l-乳酸氧化酶(lod)。在其它实施方案中,缀合元件173的基质可包括其它合适的检测酶,诸如l-乳酸脱氢酶(ldh)。一种或多种检测酶可被松散地沉积在缀合元件173垫的表面上,使得它们可以溶解在从取样元件172流出的一定体积的血液和/或其它生物流体样品中。
[0077]
定量酶可被配置成对乳酸的酶促氧化过程中产生的一种或多种种类的化学计量转换表现出高活性和高选择性,产生可被定量的信号。在一些实施方案中,干燥的基质可包括一种或多种含血红素的酶,诸如过氧化氢酶和/或过氧化物酶,其可以催化与氢过氧化物(诸如乳酸氧化过程中产生的过氧化氢(h2o2))的氧化还原反应。含血红素的酶可以是例如辣根过氧化物酶,其可催化过氧化氢(h2o2)和3,3
′‑
二氨基联苯胺(dab)的氧化还原反应,产生可以通过比色法检测和定量的深棕色不溶性产物。
[0078]
虽然lfa 170a在上文中被描述为还包括捕获元件174、控制元件175和吸液芯176,但是在该实施方案中,可以在例如缀合元件173上或缀合元件173处进行乳酸的检测。因此,lfa不需要包括单独的捕获元件、控制元件和/或吸液芯。
[0079]
例如,在一些实施方案中,lfa可以耦接到光学装置诸如cmos或ccd照相机,所述光学装置被配置成收集由过氧化氢氧化产生的3,3
′‑
二氨基联苯胺(dab)深棕色沉淀的图像,以测定样品中最初存在的乳酸的浓度。例如,在一些实施方案中,lfa的缀合元件173可以通过诸如专用光学检测器或智能手机的外围设备的照相机成像,并且图像的强度可以通过图像软件分析,以便估计dab沉淀物的浓度、过氧化氢的浓度,并因此估计样品中最初存在的乳酸的浓度。在一些实施方案中,样品中存在的乳酸的浓度可以通过以下过程确定:(1)记录dab棕色沉淀的图像,(2)借助图像处理软件计算灰度模式值,以及(3)将灰度模式值与具有已知乳酸含量的样品中存在的乳酸的浓度相关联。图像可以采用的灰度模式值的范围是0到255,接近0的值对应于较暗的图像,接近255的值对应于较亮的图像。
[0080]
被配置成检测血液和/或其它生物流体中的乳酸的侧向流动测定(lfa)可以克服对于乳酸检测方法所观察到的某些缺点,所述乳酸检测方法依赖于电化学反应来定量乳酸氧化时产生的过氧化氢(h2o2)的量。如上所述,过氧化氢(h2o2)与3,3
′‑
二氨基联苯胺(dab)的酶促反应产生棕色沉淀,该沉淀不溶于血液和/或生物流体样品,并且可以通过光学方法诸如比色法进行定量。此外,过氧化氢和dab的反应在类似于乳酸氧化所需的ph和温度条件下进行。因此,在lfa的干燥基质中使用添加剂可以保护检测酶和定量酶不被分解,有利于储存长达9个月的时期,如本文进一步描述的。相反地,检测和定量乳酸的电化学方法通常需要使用高氧化电位来将过氧化氢转化为电信号。这些电位可经常引发血液和/或生物流体样品中存在的其它可电氧化的种类的干扰反应,其导致不准确的结果。另外,将酶固定到固体表面会带来几个挑战,包括(1)需要复杂和/或耗时的制造和表征方法,以及储存期间酶的稳定性降低。
[0081]
在一些实施方案中,在一种或多种化学试剂和/或稳定添加剂存在的情况下,检测酶和定量酶可以包含在干燥的基质中,所述化学试剂和/或稳定添加剂被配置成在储存期间以及在血液和/或其它生物流体样品中的乳酸氧化期间保持酶的活性和稳定性。例如,干燥的基质可包括弱酸或碱(例如,缓冲剂),其可以溶解在血液和/或其它生物流体样品中,并且可以在样品中离解以在它们的酸种类与它们的缀合物之间建立平衡,将样品的ph值保持在酶表现出高催化活性的值的范围内。在一些实施方案中,干燥的基质可以包括一种或多种缓冲剂,诸如磷酸盐缓冲盐水(pbs)、2-乙磺酸(mes)、三(羟基甲基)氨基甲烷(tris)、哌嗪-n,n
′‑
双(pipes)、3-吗啉代丙烷-1-磺酸(mops)、2-[4-(2-羟基乙基)哌嗪-1-基]乙磺酸(hepes)、[三(羟基甲基)甲基氨基]丙磺酸(taps)、n-环己基-2-氨基乙磺酸(ches)和/或n-环己基-3-氨基丙磺酸(caps)。
[0082]
在一些实施方案中,干燥的基质可以包括多糖,诸如壳聚糖,一种无毒的生物相容性生物聚合物,其可以提供抗微生物活性和抗氧化活性,以长时间保持酶的化学完整性。在一些实施方案中,壳聚糖稳定剂可以伴随有一种或多种试剂,所述试剂被配置成增加壳聚糖在血液和/或其它生物流体样品中的溶解度。例如,在一些实施方案中,干燥的基质可以包括壳聚糖和诸如甲酸、乙酸和/或丙酸等弱有机酸,适于增加壳聚糖在一定体积的血液和/或生物流体中的溶解度。在一些实施方案中,干燥的基质可以包含包括壳聚糖、乙酸和/或缓冲剂在内的添加剂的组合,其被吸附在缀合物173的表面上并且被配置成溶解在从取样元件170输送的一定体积的血液和/或生物流体中。
[0083]
如上所述和被配置成测试血液和/或其它生物流体中的乳酸的侧向流动测定
(lfa)可以检测存在于各种样品中的乳酸,所述样品包括缓冲溶液、血清、血浆和/或全血。更具体地说,在一些实施方案中,lfa可以表现出2-6(mm)的可检测乳酸的动态范围,以及在缓冲液和/或血清样品中等于或高于0.5mm乳酸的灵敏度。在一些实施方案中,lfa可在缓冲液/血清中表现出2mm和4m的截断乳酸浓度。使用被配制用于乳酸检测的lfa获得乳酸结果所需的总时间可约为10分钟。当在37℃下进行加速降解研究时,配置用于乳酸检测的lfa可以随着时间的推移保持相对稳定,其中降解主要发生在测试的第一周。更具体地说,配置用于乳酸检测的lfa可以在37℃下保持稳定长达4周,显示信号响应变化较小,支持lfa检测将在很长一段时间内保持可行的观点。
[0084]
降钙素原
[0085]
在一些实施方案中,快速测试装置170可以是被配置成测试pct生物标志物的lfa(例如,lfa 170a)。例如,在败血症的诊断中使用血液中的血清pct生物标志物浓度的有效性在下面示于表2中,该表给出了根据血清pct测量对败血症、严重败血症和脓毒性休克的诊断的研究结果。
[0086]
表2:
[0087][0088]
降钙素原(pct)是116个氨基酸的肽,具有大约14.5kda的分子量mw,并且属于降钙素肽家族。pct分子由以下三部分组成:氨基末端(57个氨基酸)、未成熟降钙素(33个氨基酸)和称为抗钙素(katacalcin)的降钙素羧基末端肽1(ccp-1)(21个氨基酸)。pct是降钙素的前体激素,其在健康个体中检测不到,因为在无全身性炎症的情况下,该肽不会被释放到血液中。然而,在由细菌感染引起的败血症的情况下,pct合成在组织中被诱导,因此在血液中变得可检测。细菌毒素诸如内毒素和细胞因子(例如,白细胞介素(il)-1β、白细胞介素-6和肿瘤坏死因子(tnf)-α)可触发pct的产生。pct水平可在细菌感染的2小时至6小时之间迅速升高,并在6小时至24小时内达到峰值。除了细菌感染之外,一些真菌和寄生虫感染也与血流中pct的释放相关。引发体内高水平pct的其它条件包括最近的大手术、严重创伤、严重烧伤、长期心源性休克和慢性肾脏疾病。
[0089]
一些甲状腺外组织缺乏将pct切割成其成熟形式降钙素的能力,使得pct在血液中积聚。因此,pct可用作细菌性炎症与病毒性炎症之间具有相对较高区分度的生物标志物,其可用于患有败血症的患者。此外,pct水平可以与细菌感染的严重性相关和/或指示细菌感染的严重性。在败血症病例中,细菌感染的迅速诊断降低了不必要或不适当使用抗生素的风险,这种不必要或不适当使用抗生素会增加患者的对抗生素的耐药性或毒副作用。
[0090]
诊断由血流感染引起的败血症的常规方法包括培养血液、尿液、脑脊液、支气管液标本。这些测试方法通常需要24小时至48小时才能产生结果,并且时间通常能够有助于鉴定病原体,提供关于微生物类型及其对抗生素的易感性的信息。然而,临床症状可以在缺乏
阳性培养的情况下表现出来,导致基于假阴性结果的医学治疗。pct的半衰期(25小时至30小时)加上其对细菌感染的特异性以及其在健康个体中基本上不存在,使得pct成为细菌感染的合适生物标志物。
[0091]
pct可以通过基于夹心elisa原理的免疫测定来定量。在这些免疫测定中,抗体-降钙素原-抗体复合物形成,并通过一种或多种包括化学发光、酶促、荧光和比浊免疫测定在内的仪器技术定量。例如,pct的化学发光测定采用两步夹心法。在该方法中,在试剂缓冲液存在的情况下,将与碱性磷酸酶缀合的抗pct单克隆抗体加入患者样品中。孵育后,将包被有单克隆抗pct抗体的顺磁性颗粒加入到测试中。pct与顺磁性颗粒结合,而溶液中的抗pct抗体与pct分子的不同抗原位点反应。通过磁体将颗粒与非缀合的材料分离。向测试中加入化学发光底物,用光度计测量反应产生的光,其中光子的产生与样品中pct的浓度成比例。
[0092]
或者,pct可以使用基于时间分辨扩大的穴状发射技术(time resolved amplified cryptate emission technology)(trace)的定量均相测定(brahms,hennigsdorf,germany)来测量。该测试包括将氮激光337nm光束对准含有pct和识别pct肽的不同表位的2种荧光标记抗体的样品。暴露于激光激发会触发供体与受体分子之间的非辐射能量转移;供体分子在620nm发射长寿命荧光信号,受体分子在665nm发射短寿命信号。当供体和受体分子通过与pct结合而靠近时,产生的信号在665nm处被放大,并持续数微秒,长至足以在生物样品中常见的背景荧光衰减后被检测到。
[0093]
被配置成测试血液(例如全血、血清等)pct生物标志物(例如,抗原)的侧向流动测定(lfa)为败血症的诊断提供了替代工具。如上参考图2所述,可以在包括装配在基底171上方的一个或多个组件的条带上方进行lfa。被配置用于检测和定量血液和/或其它生物流体中的pct的lfa的组件可包括取样元件172、缀合元件173、捕获元件174、控制元件175和吸液芯176。
[0094]
如上所述,基底171可以是被配置成向lfa的组件提供机械支撑的背衬叠层或背衬卡。如上所述,基底171可具有任何合适的形状、尺寸和/或配置。例如,基底171可以是恒定宽度和预定长度的矩形背衬卡或条带,能够提供足够的表面积来容纳lfa的各种组件。基底171可由半刚性聚合物制成,所述聚合物被设计成提供均匀性和平坦特性。基底171可包括一种或多种压敏粘合剂,其被配置成有助于附着lfa的各种部件,如本文中进一步描述的。
[0095]
取样元件172可以是垫,其提供表面以接收用于分析的血液和/或其它生物流体的样品,并有助于以平滑、连续和均匀的方式将样品输送到侧流测试条的其它部件。取样元件172可具有任何合适的形状和/或尺寸。在一些实施方案中,取样元件172的形状可以是矩形条,其被配置成吸附和接收一定体积的血液和/或其它生物流体的样品。取样元件172可被设置在基底171的表面上,以向lfa提供机械支撑。在一些实施方案中,取样元件172可以包括涂覆在样品垫的一个表面上的粘合剂,以有助于附着到塑料背衬叠层。取样元件172的形状和尺寸可以预先确定,使得取样元件可被设置在塑料背衬叠层上。可以选择取样元件172的厚度,以便于取样元件172粘附到塑料背衬叠层上,同时保持垫的机械结构。此外,可以选择取样元件172的厚度,以容纳大量的血液和/或其它生物流体,防止垫上的样品过饱和,并引导至塑料背衬叠层。取样元件172可由纤维素、硝酸纤维、玻璃纤维和/或任何其它合适的材料制成。
[0096]
用于检测和定量来自血液和/或其它生物流体样品中的pct的lfa的缀合元件173
可以是位于取样元件172下游附近的垫,如图2所示。缀合元件173可具有任何合适的形状和/或尺寸。在一些实施方案中,取样元件172的形状可具有与取样构件171的宽度相似的宽度的矩形条带,其被设置在基底171的表面上,以向lfa提供机械支撑。缀合元件173可包含包括生物活性颗粒和添加剂的干燥基质(例如,盐-糖基质)。包含在基质中的生物活性颗粒包括已被固定在缀合元件173之上或之中的特异性抗体和/或亲和试剂(例如,dna适体、蛋白质结合剂等)。例如,在一些实施方案中,取样元件172的表面可以用缓冲水溶液浸渍,该缓冲水溶液提供具有受控ph的环境。在一些实施方案中,取样元件172的表面可以用缓冲溶液浸渍,该缓冲溶液包括但不限于硼酸盐缓冲溶液、磷酸盐缓冲盐水(pbs)、2-乙磺酸(mes)、三(羟基甲基)氨基甲烷(tris)、哌嗪-n,n
′‑
双(pipes)、3-吗啉代丙烷-1-磺酸(mops)、2-[4-(2-羟基乙基)哌嗪-1-基]乙磺酸(hepes)、[三(羟基甲基)甲氨基]丙磺酸(taps)、n-环己基-2-氨基乙磺酸(ches)和/或n-环己基-3-氨基丙磺酸(caps)。
[0097]
取样元件172的干燥基质可包括一种或多种用作润湿剂的表面活性剂,用于溶解样品中存在的极性种类。例如,在一些实施方案中,缀合元件173的干燥基质可包括非离子型表面活性剂,诸如缩水甘油、tergitol、乙氧基化和烷氧基化脂肪酸、乙氧基化胺、烷基和壬基苯酚乙氧基化物、乙氧基化脱水山梨醇酯、蓖麻油乙氧基化物等。干燥的基质可包含一种或多种被配置成通过抑制广谱微生物来促进延长lfa的保存期的生物杀灭剂。生物杀灭剂可以以低浓度配制在缀合元件173的干燥基质中,以最小化和/或避免潜在的健康危害、毒理学问题和处置问题。例如,在一些实施方案中,干燥基质可包括5-氯-2-甲基-4-异噻唑啉-3-酮(cmit)、2-甲基-4-异噻唑啉-3-酮(mit)、专有的二醇(proprietary glycol)、改性的烷基羧酸盐和/或其它商购可得的防腐剂制剂,诸如proclin 300
tm
。在一些实施方案中,干燥基质可包括一种或多种去垢剂或任何可用于蛋白质增溶的两亲分子,诸如tween20、triton x、辛基硫代葡糖苷等。
[0098]
缀合元件173的干燥基质可包括一种或多种抗体和/或亲和试剂,其缀合于被配置成允许检测的分子。在一些实施方案中,干燥基质可以包括一种或多种能够结合pct并表现出高稳定性的检测抗体。例如,在一些实施方案中,检测抗体可包括降钙素原人抗体,包括单克隆抗pct抗体14a2cc、单克隆抗ct抗体796、pp3等。
[0099]
检测抗体可被固定到一种或多种有色颗粒(例如,蓝色胶乳、红色胶体金和/或任何其它合适的颗粒)、荧光颗粒、磁性颗粒或任何其它可用于捕获和定量血液和/或其它生物流体样品中的pct的合适颗粒上。在一些实施方案中,检测抗体可被固定到金纳米颗粒上。金纳米颗粒和/或金纳米壳可以用抗体功能化,所述抗体对pct分子的某些区域表现出特异性结合活性(例如,生物缀合)。在生物缀合过程中,金纳米颗粒的表面可以使用物理方法用检测抗体进行官能化,所述物理方法依赖于检测抗体与金纳米颗粒表面之间的物理相互作用,诸如离子相互作用、疏水相互作用和/或配位结合(dative binding)。物理相互作用是通过抗体自发吸附到金纳米颗粒表面上而发生的。在离子相互作用的情况下,检测抗体中的带正电荷的基团被吸引到金纳米颗粒的带负电荷的表面。疏水相互作用发生在检测抗体的疏水部分与金属表面之间。
[0100]
通过物理方法用检测抗体将金纳米颗粒官能化的优点包括容易制造、简单、低成本、快速制造,以及使用最少的可引起有害毒理效应的化学品和/或添加剂。然而,物理方法的某些不利方面可包括在官能化金纳米颗粒的制备中使用大量检测抗体、检测抗体的随机
取向以及检测抗体相对容易地被具有类似特征的其它分子替换。由于金纳米颗粒上结合形式的低特异性,这些不利方面常会导致高测定可变性和低pct捕获能力。例如,抗体与金纳米颗粒表面的缀合可以通过非特异性结合位点进行,所述非特异性结合位点可以封闭适合于pct捕获的抗体的区域。例如,在一些情况下,通过重链中存在的恒定结构域与纳米颗粒表面之间的相互作用,抗体可被物理地吸附在金纳米颗粒的表面上。在这种配置中,抗体的抗原结合位点可部分地可用于与pct相互作用。在其它情况下,抗体可以通过pct抗原结合位点之间的相互作用物理吸附在金纳米颗粒的表面上,这排除了抗原结合位点与pct的相互作用。
[0101]
或者,在一些实施方案中,抗体可以通过涉及共价键的化学方法,诸如通过硫醇衍生物、双功能接头和/或衔接分子的化学吸附缀合于金纳米颗粒。通过金原子与硫原子之间的化学反应在颗粒表面产生强键,可以实现具有硫醇衍生基团的金纳米颗粒的直接官能化。例如,硫醇官能化的抗体可以直接附着至金纳米颗粒上。然而,这种方法存在挑战,诸如使用可能损害纳米颗粒稳定性的反应条件,并且可能需要苛刻的条件。
[0102]
本文所述的实施方案、实施方案和/或方法可以例如通过包括使用可使用双官能接头连接至金纳米颗粒表面的其它基团来克服这些限制,所述双官能接头在金纳米颗粒表面提供特定官能化。例如,用硫醇基团官能化的羧化聚乙二醇(peg)分子(peg-sh)可用于官能化金纳米颗粒的表面。官能化至金纳米颗粒上的peg分子也可包括端羧基基团(carboxyl terminated group)。这些端羧基基团可以用包括水溶性碳二亚胺(edc)和n-羟基-琥珀酰亚胺(nhs)化合物在内的偶联化学来修饰,以产生与抗体分子中的伯胺基团结合的反应性官能团。水溶性碳二亚胺与含peg的金纳米颗粒中的羧基部分反应,产生中间活性基团,该中间活性基团将与n-羟基-琥珀酰亚胺化合物反应,形成反应性酯基团。当与抗体直接接触时,抗体中的伯胺基团与金纳米颗粒表面中形成的酯基团反应。这种反应被设计成产生酰胺键以将抗体附接至金纳米颗粒,而不在它们之间添加间隔分子。
[0103]
用于检测和定量来自血液和/或其它生物流体样品中的pct的lfa的捕获元件174可以是被设置在缀合元件173附近和/或下游的垫,包含已被固定在捕获元件174之中或之上的颗粒或分子。如上文参考图2所述,当在一定体积的血液和/或其它生物流体样品中向下游流动时,颗粒或分子可被配置成与检测抗体结合,其缀合于上文参考缀合元件173所述的有色颗粒。在一些实施方案中,捕获元件174可包含固定和/或化学结合至捕获元件174表面的捕获抗体。捕获抗体可被配置成与检测抗体相互作用,以捕获结合到检测抗体的pct,产生检测抗体及其缀合的有色颗粒的局部积累。在一些实施方案中,捕获抗体可被吸附在捕获元件174的表面上。
[0104]
如上文参考检测抗体所述,捕获抗体可包括包括单克隆抗pct抗体14a2cc、单克隆抗ct抗体796、pp3等在内的降钙素原人抗体。固定的捕获抗体可被配置成结合pct分子,所述pct分子已经预先结合至缀合元件173中的检测抗体(及其缀合的有色颗粒)。结果,捕获元件174暴露于先前流过缀合元件173的含有pct的血液和/或其它生物流体的样品,可导致与捕获抗体缔合的有色颗粒的积累,所述抗体结合样品中存在的pct分子。捕获元件174上的这种有色颗粒的积聚可以通过一种或多种光学方法来记录和定量,以确定样品中pct的浓度。例如,在一些实施方案中,积聚在捕获元件174上的有色颗粒可通过标准侧向流动读取器诸如商购可得的leelu读取器(lumos diagnostics)来确定,其被配置成检测有色颗
粒,提供合适的光学灵敏度和足以覆盖宽浓度范围的动态范围。
[0105]
lfa可以包括控制元件175,以捕获原本未被捕获元件174捕获的检测抗体。在其它实施方案中,lfa不需要包括控制元件。被配置用于检测和定量来自血液和/或其它生物流体样品的pct的lfa的吸液芯176可以是设置在捕获元件174(或控制元件175,如果包括的话)附近和/或下游的垫。如参考图2所述,吸液芯176可被配置成吸收或芯吸未被固定在捕获元件174(和/或控制元件175,如果包括的话)之中或之上的样品的部分。
[0106]
上述被配置成测试血液和/或其它生物流体中的pct的侧向流动测定(lfa)可以检测存在于包括缓冲溶液、血清、血浆和/或全血在内的各种样品中的pct。更具体地说,在一些实施方案中,lfa在缓冲液和血清中可以表现出0.2ng/ml-2ng/ml的可检测pct的动态范围,以及等于或高于0.1ng/ml的灵敏度。在一些实施方案中,lfa在缓冲液/血清中可表现出0.2ng/ml和0.5ng/ml的截止pct浓度。使用被配置用于pct检测的lfa获得结果所需的总时间可约为10分钟。被配置用于pct检测的lfa在于37℃进行的加速稳定性测试期间可以保持相对稳定,而无明显的缀合物释放和通过侧向流动条的流动。
[0107]
虽然上文描述了血清乳酸和/或血清pct浓度的测试,但是应当理解,测试血液(例如,全血或血液的其它合适部分)将产生相似或基本相同的结果。虽然上文描述了乳酸生物标志物和pct生物标志物,但是应当理解,它们仅仅是通过示例而非限制的方式呈现的。在一些实施方案中,快速测试装置(例如,lfa 170a)可被配置成测试与败血症和/或任何其它传染性或疾病状况相关联和/或以其它方式指示所述疾病或疾病状况的任何合适的生物标志物。此外,应该理解的是,快速测试装置170和/或lfa 170a(和/或任何其它合适的基于流动的测定)可以与本文参照具体实施方案所述的任何流体传输装置结合使用。
[0108]
适体
[0109]
在一些实施方案中,快速测试装置170可以是lfa(例如,lfa170a),其被配置成使用适体来测试与败血症和/或任何其它感染状况相关联的任何合适的生物标志物。适体是单链dna或rna分子,可以以高亲和力和特异性与相应的靶标选择性结合。这些单链分子由可变区组成,该可变区在中端包含20-40个碱基,两侧有两个恒定区,包含结合位点。由于分子间杂交,适体可以折叠成二级结构和三维形状。适体-靶标结合的平衡解离常数在1皮摩尔(pm)至1纳摩尔(nm)范围内。适体与抗体对靶分子具有相似的亲和力,并且可以针对所需靶标(诸如毒性小分子、非免疫原性靶标或不与抗体结合的单个分子)而产生。此外,适体可以被热或化学品可逆地变性,这对于抗体是不可能的。
[0110]
适体在靶标识别和各种应用方面类似于抗体。然而,适体的使用可呈现出优于使用抗体的有利方面,包括例如经由体外方法的制造(所述体外方法,与从细菌、细胞培养物和/或动物细胞(包括人细胞)中获得抗体所需的复杂实验相反,依赖于容易控制和高度可再现的化学反应)、结合抗体不识别的靶标(诸如离子、小分子、复杂的多活性位点分子、蛋白质、细菌细胞、病毒和/或癌细胞)的能力、通过聚合酶链式反应(pcr)在短时间内大量扩增的能力、引入功能性部分(例如,荧光团、猝灭剂和纳米材料)的修饰的容易性、在苛刻条件下的稳定性以及由于其非免疫原性特征而在体内应用中的使用安全性。在一些情况下,适体可以改善转运特性,允许细胞特异性靶向和改善的组织穿透。
[0111]
适体可以针对通过指数富集(selex)方法系统性进化配体而获得的特定靶标进行定制。该方法包括三个主要步骤:文库的生成、选择和扩增。在第一步骤中,通过组合化学合
成技术设计并合成随机文库,以产生包含可变区的寡核苷酸,所述可变区具有20-40个碱基,每个末端的侧翼是上游和下游引物结合位点。产生的文库可包含1012-1015个ssdna或rna序列。在第二步骤中,在结合缓冲液存在的情况下,将靶分子与文库一起孵育数分钟。适体将与靶标结合并形成适体-靶标复合物,非特异性序列将保留在结合缓冲液中。可以收集适体-靶标复合物并用洗涤缓冲液洗涤数次。然后可以通过用洗脱缓冲液处理,将适体与适体-靶标复合物分离。选择步骤可包括反选择程序,其中靶标被类似物取代,与类似物结合的核酸序列被排除。在第三步骤中,在dna的情况下,通过pcr扩增第二步骤中洗脱的序列,对于rna,通过逆转录酶(rt)-pcr进行扩增,以产生用于第二轮selex方法的子文库。该方法可以重复数轮,直至产生对靶标具有高特异性的适体。
[0112]
当与靶标结合的序列的亲和力饱和时,它们被送去克隆和测序,随后以高灵敏度和特异度鉴定与靶标结合的适体序列。可以使用几种技术来改善未结合的序列与适体-靶标复合物的分离。例如,在一些情况下,适体的选择可以包括基于硝酸纤维素膜过滤的selex、亲和色谱和基于磁珠的selex、毛细管电泳和/或基于微流控的selex。基于硝酸纤维素膜过滤的selex使用硝酸纤维素膜来保留适体-靶标的复合物,并基于尺寸来去除未结合的寡核苷酸序列。膜表面上的微米尺寸的多个孔允许dna或rna寡核苷酸通过并且将蛋白质捕获在膜上。然后通过pcr或rt-pcr扩增该材料,用于下一轮制造。亲和色谱和基于磁珠的selex使用填充在柱上的琼脂糖珠粒作为固定相。磁珠也用于通过特定标签与其配体(在珠上)之间的物理相互作用或化学反应来固定靶标。毛细管电泳和基于微流体的selex用于提高分离速度、分辨率和容量,同时最大限度地减少样品稀释。在该方法中,由于在电场中的电泳迁移率的差异,未结合的核苷酸与适体-靶标复合物分离。适体可以通过靶标、配体或靶标-配体复合物的混合物的迁移速度获得。与其它方法相比,基于毛细管电泳的selex可用于在数轮中选择适体。基于微流体的selex技术是自动化和小型化的平台,其使得能够在芯片上进行适体选择。为了自动执行选择方法,该系统包括若干个模块,带有微型泵、微型阀、储液歧管、废物室和pcr室。包括原子力显微镜、高通量测序、氧化石墨烯、紫外线交联、流式细胞术和表面等离子共振(spr)在内的其它方法可以与selex方法结合使用。这些方法用于丰富选择手段以及提高适体选择的效率。
[0113]
适体的应用包括体内治疗剂、分子生物传感器、靶标捕获、药物递送、新药开发、危险检测、环境监测、临床诊断、生物标志物发现和食品检查。适体用作识别元件用于分析工具,包括电化学和荧光生物传感器、比色测定、表面等离子体共振测定和扩增技术。
[0114]
检测
[0115]
在一些情况下,快速测试装置170(例如,lfa 170a和/或任何其它合适的快速测试装置)可被配置成呈现可由人(例如,医生、护士、技术人员等)通过目视检查检测和/或评估的测试结果。例如,医生、护士、技术人员等可以目视检查lfa 170a的捕获元件174,以确定沿着捕获元件174是否存在条带。另外,可以目视检查lfa 170a的控制元件175,以验证测试的性能。在一些此类情况下,由人进行的目视检查可以相对简单地实施,并且可以不使用额外的设备来提供定性结果(例如,阳性或阴性测试结果)。
[0116]
在其它情况下,lfa 170a可被配置成输出测试结果,所述测试结果进而可以被一个或多个电子设备(例如,图1所示的电子设备190)接收、检查、分析、解释等。例如,在一些情况下,便携式条读取器可用于读取、扫描和/或评估沿着捕获元件174和/或控制元件175
的一个或多个条带。条带读取器可包括照相机、扫描仪、读取器等,其可使用互补金属氧化物半导体(cmos)器件、电荷耦接器件(ccd)和/或任何其它合适的检测器件或照相机来检测一个或多个条带。在一些实施方案中,条带读取器可被配置成定义测试结果(条)的数据或数字表示,其可以是定性的、半定量的和/或定量的。例如,捕获元件强度可以与分析物的浓度成比例,从而允许分析物的定量。在一些情况下,条带读取器可被配置成读取、扫描和/或识别一个或多个条带的存在以及所述一个或多个条带的强度,从而提供定性和定量数据。在一些实施方案中,电子设备190可被集成到快速测试装置170中/上,或者其可以是其中可插入快速测试装置170和/或一个或多个盒(例如,快速测试装置170的一个或多个部分)用于读取和分析的独立设备。
[0117]
在一些实施方案中,条带读取器可被配置成提供定性和/或定量数据作为电子设备190的输入,电子设备190可以分析、处理和/或以其它方式使用数据来产生一个或多个定性和/或定量测试结果。电子设备190可以是任何合适的基于硬件的计算设备,其被配置成接收、处理、定义和/或存储数据,例如一个或多个诊断测试结果、测量结果数据所依据的测试标准、预定和/或预先定义的治疗计划、患者概况、疾病概况等。另外,电子设备190可被配置成经由有线或无线连接或网络发送和/或接收数据。在一些实施方案中,电子设备190可以是例如移动电子设备(例如,智能手机、平板电脑、膝上型电脑和/或任何其它移动或可穿戴设备)、个人计算机(pc)、工作站、服务器设备或服务器设备的分布式网络、虚拟服务器或机器、虚拟专用服务器等(其作为实例(instance)或客户机在物理服务器或服务器组上执行和/或运行)和/或任何其它合适的设备。在一些实施方案中,电子设备190可被配置成提供由快速测试装置170产生的测试结果的图形和/或数字表示。另外,在一些实施方案中,基于与测试结果相关联和/或代表测试结果的数据,电子设备190可被配置成确定并以图形或数字方式呈现一个或多个诊断、一个或多个治疗计划、一个或多个模拟和/或与体液样品、患者和/或患者的医学治疗相关联的任何其它合适的数据。
[0118]
如上所述,在一些实施方案中,传输装置105可被配置成将第一量的体液传输至快速测试装置170,并将至少一些第二量的体液传输至一个或多个任选的流体收集装置195。例如,传输装置105的第二部分或取样部分可以包括出口或端口和/或可以与出口或端口流体连通,这可允许第二量的体液被转移出传输装置105的第二部分或取样部分。在一些情况下,一个或多个任选的流体收集装置195可以物理地和/或流体地耦接到传输装置105(例如,通过出口或端口)以接收至少一些第二量的体液。
[0119]
在一些实施方案中,任选的一个或多个流体收集装置195可以是用于至少暂时容纳体液的任何一个或多个合适的装置。例如,流体收集装置195可包括但不限于任何合适的器皿、容器、储器、瓶子、适配器、皿、小瓶、注射器、装置、诊断和/或测试机器等。在一些实施方案中,流体收集装置可以与已知的样品容器基本类似或相同,所述容器是例如(由becton dickinson and company(bd)制造)、bact/sn或bact/fa(由biomerieux,inc.制造)和/或任何合适的储器、小瓶、微量管、微升小瓶、纳升小瓶、容器、微容器、纳米容器等。在一些实施方案中,流体收集装置可以与2007年12月13日提交的题为“systems and methods for parenterally procuring bodily-fluid samples with reduced contamination”的美国专利第8,197,420号(
“‘
420专利”)中描述的任何样品储器基本类似或相同,该专利的公开内容通过引用以其整体并入
本文。
[0120]
在一些实施方案中,在接收取样体积的体液之前,流体收集装置195可以没有内容物。例如,在一些实施方案中,流体收集装置195或储器可以限定和/或可被配置成限定或产生真空、抽吸和/或负压条件,例如基于真空的收集管(例如,)、注射器等。在一些实施方案中,流体收集装置195可以物理地和/或流体地耦接到传输装置105(例如,出口或端口),使得流体收集装置195内的负压条件便于从患者抽取体液,并使其进入或通过传输装置105的一个或多个部分,如本文参考具体实施方案进一步详细描述的。
[0121]
在一些实施方案中,流体收集装置195可包括任何合适的添加剂、培养基、物质、酶、油、流体等。例如,流体收集装置195可以是样品或培养瓶,包括例如需氧或厌氧培养基。样品瓶或培养瓶可被配置成接收体液样品,然后可以测试(例如,在通过体外诊断(ivd)测试和/或任何其它合适的测试进行孵育之后)所述体液样品的革兰阳性菌、革兰阴性菌、酵母、真菌和/或任何其它生物体的存在。在一些情况下,如果培养基的这种测试产生阳性结果,则可以随后使用基于核酸的系统(例如,一种或多种基于pcr的系统、一种或多种杂交探针、一种或多种核酸扩增测试(naat)等)来测试培养基以鉴定特定的生物体。在一些实施方案中,除了培养基之外或者代替培养基,样品储器可以包括例如任何合适的添加剂等。此类添加剂可以包括例如肝素、柠檬酸盐、乙二胺四乙酸(edta)、草酸盐、聚乙醇磺酸钠(sps)等。在一些实施方案中,流体收集装置195可以包括任何合适的添加剂或培养基,并且可被抽成真空和/或以其它方式除去空气。
[0122]
虽然“培养基”在上文中被描述为被配置成与体液中的有机体(例如,微生物,诸如细菌)反应的物质,而“添加剂”在上文中被描述为被配置成与体液的部分(例如,血液、血液、滑液等的组成细胞)反应的物质,应该理解的是,样品储器可以包含任何合适的物质、液体、固体、粉末、冻干化合物、气体等。此外,当提及样品储器内的“添加剂”时,应该理解的是,添加剂可以是培养基,诸如包含在培养瓶中的需氧培养基和/或厌氧培养基,包含在培养瓶和/或任何其它合适的储器(例如上述那些)中的添加剂和/或任何其它合适的物质或物质的组合。也就是说,本文所述的实施方案可以与包含任何合适的物质或物质的组合的任何合适的流体储器等一起使用。
[0123]
在一些实施方案中,包含在传输装置105的第二部分或取样部分中和/或包含在任选的一个或多个流体收集装置195中的第二量的体液可作为生物样品用于一个或多个测试、测定和/或诊断程序。在一些情况下,将第一量的体液与第二量的体液隔离可以隔离第一量的体液中和/或传输装置105的隔离部分中的污染物等。隔离又可以使第二量的体液基本上不含污染物。因此,第二部分或第二量的体液可用于一种或多种测试,诸如血液培养测试等,所述测试对污染物可能相对敏感(例如,由于污染物的存在可产生掺杂的结果)。以这种方式,系统100可被配置成获取第一量的体液和第二量的体液,所述第一量的体液可用于对污染具有相对低的敏感度的测试,第二量的体液可用于对污染具有相对高的敏感度的测试。在一些情况下,对第一量的体液的测试可提供相对快速的初始结果,该结果可为一种或多种治疗选择提供信息,而对第二量的体液的测试可提供更详细的测试结果,所述结果通常需要更长的时间来形成。因此,对于对时间敏感的疾病状况(例如,败血症),测试第一量的体液的初始结果能够允许医生或内科医生在对第二量的体液进行更详细的测试的同时提供快速的初始治疗。
specimen container”的美国专利第10,123,783号(
“‘
783专利”)和/或2020年3月6日提交的标题为“universal transfer adapters and methods of using the same”的美国临时专利申请第62/986,244号(
“‘
244申请”)中描述的那些,和/或可以耦接到流体传输装置,诸如2015年6月2日提交的标题为“sterile bodily-fluid collection device and methods”的美国专利第10,772,548号(
“‘
548专利”)中所描述的那些,每个专利的公开内容通过引用以其整体并入本文。在此类实施方案中,流体传输适配器可以耦接到流体收集装置295的一部分和/或可以接收流体收集装置295的一部分,并且可以在出口213与流体收集装置295之间建立流体连通。在其它实施方案中,出口213可以通过居间结构(图3中未示出)诸如无菌管道等可操作地耦接到流体收集装置295。
[0130]
在一些实施方案中,出口213的布置可以使得出口213在耦接到流体收集装置295之前被物理地和/或流体地密封。在一些实施方案中,出口213可以响应于被耦接到流体收集装置295和/或响应于出口213和/或壳体210内的环境与流体收集装置295内的环境之间的负压差而从密封配置转换为未密封的配置。
[0131]
流体收集装置295可以是用于至少暂时容纳体液的任何合适的装置,例如上文参考流体收集装置195详细描述的任何装置(例如,抽成真空的容器、样品储器、注射器、培养瓶等)。在一些实施方案中,流体收集装置295可以是样品储器,其包括真空密封件,所述真空密封件保持样品储器内的负压条件(真空条件),这又可以有助于经由真空或吸力从患者抽取体液,通过传输装置205,并进入样品储器。如本文所进一步详细描述的,在流体收集装置295是抽成真空的容器等的实施方案中,用户可以将流体收集装置295耦接到出口213,以启动来自患者的体液流并使其进入装置205,使得体液流的第一部分或初始部分被传输至例如快速诊断测试装置270中和/或被快速诊断测试装置270隔离,并且使得体液流的第二部分或后续部分绕过快速诊断测试装置270和/或以其它方式转离快速诊断测试装置270并到流体收集装置295中(例如,经由出口213)中。
[0132]
装置205的致动器250至少部分地设置在壳体210内,并且被配置成控制、引导和/或以其它方式促进流体选择性地流过壳体210的至少一部分和/或一个或多个流体流动路径215的至少一部分。致动器250可具有任何合适的形状、尺寸和/或配置。在一些实施方案中,致动器250可以是被配置成在两个或更多个状态(例如,至少第一状态和第二状态)之间转换的构件或装置。例如,致动器250可以是阀、柱塞、密封件、薄膜、气囊、挡板、板、杆、开关和/或等等。致动器250可以以任何合适的方式被致动和/或在任何数量的状态(例如,至少第一状态和第二状态)之间转换。例如,转换致动器250可以包括激活、按压、移动、平移、旋转、切换、滑动、打开、关闭和/或以其它方式重新配置致动器250。
[0133]
在一些实施方案中,致动器250可被配置成响应于用户的手动致动(例如,在按钮、滑块、柱塞、开关、阀、旋转构件、导管等上手动施加力)而在至少第一与第二状态之间转换。在其它实施方案中,致动器250可被配置成响应于压力差(或无压力差)、势能或动能的变化、组成或配置的变化(例如,致动器的一部分可以至少部分溶解或转换)和/或等等,在至少第一状态与第二状态之间自动转换。在其它实施方案中,致动器250可以基于预定时间、接收的体液体积、体液流的体积流速、体液流的流速等被机械致动或转换和/或电致动或转换(例如,通过马达、弹簧释放机构和/或等等)。虽然提供了致动器和/或致动器可以转换的方式的实例,但是应当理解,它们仅仅是作为实例而非限制给出的。
[0134]
在图3所示的实施方案中,致动器250可被配置成当处于第一状态时选择性地建立入口212与快速诊断测试装置270之间的流体连通,并且当处于第二状态时选择性地建立入口212与出口213之间的流体连通。当处于第一状态时,致动器250可被配置成允许体液从入口212,通过流体流动路径215的至少一部分,到达或进入快速诊断测试装置270。在一些实施方案中,致动器250可被配置成隔离、分开、分离和/或以其它方式防止出口213与入口212、流体流动路径215的至少一部分和/或快速诊断测试装置270之间的流体连通。当处于第二状态时,如本文进一步详细描述的,致动器250可被配置成允许后续体积的体液(例如,初始体积的体液之后的一定体积的体液)从入口212通过流体流动路径215的至少一部分传输到出口213(和/或与出口213流体耦接的流体收集装置295)。此外,当处于第二状态时,如本文进一步详细描述的,致动器250可被配置成隔离、分开、分离和/或以其它方式防止快速诊断测试装置270与入口212、出口213和/或流体流动路径215的至少一部分之间的流体连通。
[0135]
快速诊断测试装置270(本文中也称为“快速测试装置”或简称为“测试装置”)可具有任何合适的形状、尺寸和/或配置。在一些实施方案中,快速测试装置270可以可移除地耦接到传输装置205或其任何合适的部分(例如,入口部分、出口部分、隔离部分、取样部分和/或任何其它合适的部分)。在其它实施方案中,快速测试装置270可被集成到传输装置205中。例如,可以整体地或单一地形成传输装置205和快速测试装置270和/或以其它方式集成传输装置105和快速测试装置170。在其它实施方案中,传输装置205可以包括和/或可以形成端口、适配器和/或接收部分,快速测试装置270可以耦接到所述端口、适配器和/或接收部分,或者快速测试装置270可以插入所述端口、适配器和/或接收部分,以在它们之间建立流体连通。在一些此类实施方案中,将快速测试装置270耦接到传输装置205可用于将一个或多个流动控制器、阀、隔膜、端口、密封件等从关闭或密封状态转换成打开状态,以允许传输装置205与测试装置270之间流体连通。
[0136]
在一些实施方案中,快速测试装置270可被配置成从传输装置205接收第一量的体液,并使用第一量的体液来执行一个或多个测试、测定和/或诊断程序。快速测试装置270可以是任何合适的测试装置。例如,如上文参考图2所示的lfa 170a所详细描述的,快速测试装置270可以是lfa等。在一些实施方案中,测试装置270可以是lfa,其被配置成测试特定分析物或生物标志物的存在,所述特定分析物或生物标志物可以提供用于诊断患者疾患例如败血症和/或任何其它疾病状态的信息。例如,lfa可被配置成测试乳酸和/或pct生物标志物,所述乳酸和/或pct生物标志物可以是败血症的指标。在其它实施方案中,测试装置可以是lfa,其被配置成测试上文参考图2所示的lfa 170a所描述的任何目标分析物和/或生物标志物。
[0137]
在一些情况下,快速测试装置270可被配置成在传输装置205和/或致动器250处于第一状态时输出与测试从传输装置205传输的体液体积相关联的测试结果。测试结果(如图3通过标有“输出”的箭头所指示的)可由人通过视觉检查来检测和/或评估,和/或可由一个或多个电子设备(例如,电子设备290)来检测和/或评估。在一些情况下,快速测试装置270输出的测试结果可以是定性的、半定量的和/或定量的。因此,快速测试装置270可以在结构上和/或功能上与上文详细描述的快速测试装置170类似或相同,因此在本文中不再详细描述。
[0138]
如上所述,系统200可用于从患者获取一个或多个体积的体液,其可用于一个或多个测试、测定和/或诊断程序。例如,在一些情况下,用户诸如医生、内科医生、护士、抽血技师、技术人员等可以操纵装置205以在入口212与体液源(例如,患者的静脉、来自脊髓腔的脑脊液(csf)、尿液收集物和/或等等)之间建立流体连通。作为具体的实例,在一些情况下,入口212可以耦接到针等和/或可以包括针等,所述针等可被操作以刺穿患者的皮肤并将针的至少一部分插入患者的静脉,从而将入口212置于与体液源(例如,静脉、iv导管、picc等)流体连通。
[0139]
在一些情况下,当入口212被放置成与体液源(例如,患者的一部分)流体连通时,致动器250可处于第一状态,使得流体流动路径215的至少一部分在入口212与快速测试装置270(和/或快速测试装置270所耦接的装置205的一部分)之间建立流体连通。这样,传输装置205可被配置成将初始体积的体液从体液源(例如,患者)传输到快速测试装置270。在一些实施方案中,初始体积的体液可以响应于与患者的脉管系统相关联的正压和/或响应于2018年6月11日提交的标题为“fluid control devices and methods of using the same”的美国专利公布第2018/0353117号(
“‘
117公布”)中描述的任何流体传输方法,而被动地(例如,不存在用户干预和/或一个或多个部件的转换)流向快速测试装置270,所述公布的公开内容通过引用以其整体并入本文。
[0140]
在其它实施方案中,传输装置205和/或其一部分可被配置成在流体流动路径215的至少一部分内产生负压差(例如,部分真空、吸力和/或等等),所述负压差可以启动和/或维持初始体积的体液从体液源向快速测试装置270的流动。例如,在一些情况下,致动器250可在使用前以第三状态(例如,储存状态)储存,并且可从储存状态转换成第一状态,以启动初始体积的体液的流动。在此类情况下,致动器250的转换可以产生负压,所述负压可以将体液从入口212抽吸到快速测试装置270。在一些此类实施方案中,可以以与以下美国专利或美国专利公布中描述的任何方式类似和/或基本上相同的方式转换致动器250以产生负压差:2012年10月22日提交的标题为“fluid diversion mechanism for bodily-fluid sampling”的美国专利第8,535,241号(
“‘
241专利”);2013年5月29日提交的标题为“fluid diversion mechanism for bodily-fluid sampling”的美国专利第9,060,724号(
“‘
724专利”);2013年12月2日提交的标题为“syringe-based fluid diversion mechanism for bodily-fluid sampling”的美国专利第9,155,495号(
“‘
495专利”);2016年6月23日提交的标题为“devices and methods for syringe based fluid transfer for bodily-fluid sampling”的美国专利公布第2016/0361006号(
“‘
006公布”);和/或2019年2月8日提交的标题为“devices and methods for bodily fluid collection and distribution”的美国专利公布第2020/0253524号(
“‘
524公布”),所述专利或专利公布的每一个的公开内容通过引用以其整体并入本文。在其它实施方案中,如本文参考其它实施方案进一步详细描述的,初始体积的体液可以响应于由流体收集装置295产生的负压差而流向快速测试装置270。
[0141]
体液的初始体积可以是任何合适的体液体积,诸如上述的任何体积或量。例如,在一些情况下,传输装置205可以保持在第一状态或配置,直至预定和/或所需体积(例如,初始体积)的体液被传输到快速测试装置270。在一些实施方案中,初始体积可以与足以使快速测试装置270执行一个或多个测试或测定的所需体积相关联和/或至少部分基于所述所需体积。在其它实施方案中,体液的初始体积可以与等于或大于与体液源与快速测试装置
270之间限定的流体流动路径相关的体积的体液的量或体积相关联,和/或至少部分基于所述量或体积。在其它实施方案中,传输装置205可被配置成将体液流(例如,初始体积)传输到快速测试装置270中,直至快速测试装置270与入口212或体液源之间的压差达到基本均等和/或以其它方式降低到所需阈值以下。
[0142]
在一些实施方案中,当初始体积被传输到例如取样元件等(例如,取样元件171)中时,快速测试装置270可以启动初始体积的体液的测试和/或测定或者对初始体积的体液测试和/或测定。在一些情况下,快速测试装置270可被配置成提供一种或多种可以与初始体积混合或组合的溶液、缓冲液、混合物、添加剂和/或等等。以这种方式,初始体积的体液(无论是单独的还是与另外的组分混合的)可以流过快速测试装置270(例如,如上参考图2所述的lfa),这进而可以对初始体积执行一个或多个测试或测定。例如,在一些情况下,如上文所详细描述的,快速测试装置270可以是lfa,其被配置成测试乳酸和/或pct的存在。此外,如上文所详细描述的,一旦测试或测定完成,快速测试装置270可被配置成输出测试结果,所述测试结果可由人和/或一个或多个电子设备检测和/或评估。
[0143]
在初始体积的体液被传输和/或转换到快速测试装置270中之后,传输装置205可从第一状态或配置转换成到第二状态或配置。例如,在一些实施方案中,当初始体积的体液被传输到快速测试装置270中时,致动器250可以从其第一状态转换成其第一状态,这又将传输装置205置于其第二状态。在一些实施方案中,传输装置205的布置可以使得传输装置205在快速测试装置270中收集初始体积之前不能转换成第二状态。
[0144]
在一些实施方案中,传输装置205、致动器250和/或快速测试装置270的布置可以使得响应于接收到初始体积,进入快速测试装置270的体液流基本停止或减慢。在一些情况下,使用者可以目视检查一部分的装置205和/或壳体210,以确定初始体积的体液被设置在快速测试装置270中和/或进入快速测试装置270的体液流已经减慢或基本停止。在一些实施方案中,用户可以对致动器250施加力和/或可以以其它方式致动致动器250,以将致动器250从其第一状态转换成其第一状态。在其它实施方案中,致动器250可以自动转换(例如,无需用户干预)。此外,在一些实施方案中,当快速测试装置270对初始体积的体液进行一个或多个测试或一个或多个测定时,装置205和/或致动器250可以从第一状态转换成第二状态。换句话说,快速测试装置270可以对初始体积的体液进行测定,同时装置205用于传输一个或多个后续体积的体液(例如,在一个或多个并行过程等中)。
[0145]
在一些实施方案中,致动器250从其第一状态至其第二状态的转换(例如,将传输装置205置于其第二状态或配置)可将初始量的体液隔离、分离、分开和/或保留在快速测试装置270中。换句话说,致动器250可以将快速测试装置270与入口212、出口213和流体流动路径215的一个或多个部分隔离和/或分离。如本文中进一步详细描述的,在一些情况下,污染物,例如在静脉穿刺事件中脱落的皮肤上残留的微生物等、其它外部污染源、用于收集样本的导管和picc管的定植和/或等等,可能被夹带和/或包含在初始体积的体液中。因此,这些污染物被隔离在初始体积中。此外,如上文所详细描述的,快速测试装置270的布置可以使得由快速测试装置270执行的测试和/或测定不容易受到此类污染,这意味着由快速测试装置270输出的测试结果的准确性不受此类污染影响。
[0146]
除了将快速测试装置270与入口212、出口213和流体流动路径215的至少一部分隔离之外,将致动器250置于其第二状态还经由流体流动路径215的至少一部分在入口212与
出口213之间建立流体连通。例如,在一些实施方案中,将致动器250从其第一状态转换成其第二状态可以例如打开或关闭端口或阀,移动一个或多个密封件,移动或移除一个或多个障碍物,限定流动路径的一个或多个部分和/或等等。
[0147]
在一些实施方案中,在致动器250从第一状态转换成第二状态之前和/或同时,流体收集装置295可以流体地耦接到出口213。如上所述,流体收集装置295可以是任何合适的储器、容器和/或被配置成接收一定体积的体液的装置。例如,流体收集装置295可以是限定负压的抽成真空的储器或容器,和/或可以是可被操作以产生负压的注射器。在一些情况下,将出口213耦接到流体收集装置295选择性地将流体流动路径215的至少一部分暴露于流体收集装置295内的负压和/或吸力。因此,响应于负压和/或吸力,一个或多个后续体积的体液可从入口212流动,通过流体流动路径215的至少一部分,通过出口213,并进入流体收集装置295。如上所述,在收集或获取一个或多个后续体积的体液之前隔离初始体积的体液(例如,在快速测试装置270中)减少和/或基本上消除了所述一个或多个后续体积中的一定量的污染物。因此,后续量的体液可用于一个或多个测试,例如血液培养测试和/或等等,所述些测试可能对污染物相对敏感(例如,可以由于污染物的存在而产生掺杂的结果)。以这种方式,系统200可被配置成获取初始体积的体液和一个或多个后续体积的体液,初始体积的体液可用于对污染具有相对较低的敏感度的测试,后续体积的体液可用于对污染具有相对较高的敏感度的测试。在一些情况下,初始量的体液的测试(例如,通过快速测试装置270)可以提供相对快速的初始结果,其可以提示一种或多种治疗选择,而一个或多个后续量的体液的测试可以提供更详细的测试结果,该测试结果通常需要更长的时间来形成。
[0148]
图4是根据实施方案的流体传输和测定系统300的示意图。流体传输和测定系统300(本文中也称为“系统”)可以至少包括流体传输装置305和快速诊断测试装置370。在一些实施方案中,系统300可包括至少一个流体收集装置395,其可以物理地和/或流体地耦接到流体传输装置305。流体传输装置305、快速诊断测试装置370和/或流体收集装置395的部分和/或方面,可以分别与上文参考图3所详细描述的流体传输装置105和/或205、快速诊断测试装置170(和/或lfa170a)和/或270和/或流体收集装置195和/或295类似于和/或基本上相同。3所示。因此,本文不再进一步详细描述这些部分和/或方面。
[0149]
流体传输装置305(本文中也称为“传输装置”)可具有任何合适的形状、尺寸和/或配置。在一些实施方案中,传输装置305可被配置成从患者抽取体液(例如,血液)并使其进入和/或通过传输装置305。此外,传输装置305可被配置成将至少一些抽取的体液传输至一个或多个其它装置、储器、容器、小瓶、机器、测试、测定等,诸如快速诊断测试装置370和/或一个或多个流体收集装置395。
[0150]
传输装置305包括壳体310、流动控制器340和致动器350。装置305的壳体310可具有任何合适的形状、尺寸和/或配置。例如,在一些实施方案中,壳体310可以与上文参考图3所述的壳体210类似和/或基本相同。具体地,壳体310具有和/或形成入口312和出口313,并在它们之间限定至少一个流体流动路径315。入口312可以是任何合适的入口或端口,并且可以被配置成在壳体310与体液源(例如,患者)之间建立流体连通。出口313可以是任何合适的出口或端口,并且可被配置成在壳体310与流体收集装置395之间建立流体连通。此外,流体收集装置395可以与流体收集装置295类似或基本相同,因此在本文中不再详细描述。如本文所进一步详细描述的,由壳体310限定的一个或多个流体流动路径315在入口312与
and methods of using the same”的美国专利公布第2019/0076074号(
“‘
074公布”);2019年5月30日提交的标题为“fluid control devices and methods of using the same”的美国专利公布第2019/0365303号(
“‘
303公开”);和/或2019年3月11日提交的标题为“fluid control devices and methods of using the same”的美国专利公布第2020/0289039号(
“‘
039公开”),每个公布的公开内容通过引用以其整体并入本文。
[0156]
在一些实施方案中,传输装置305可被配置成至少部分地基于传输装置305的两个或更多个部分之间的压力差选择性地将一定量的体液传输到隔离室330或出口313。例如,压力差可由出口313与流体收集装置395的流体耦接产生,所述流体收集装置395可以限定负压和/或可被配置成产生负压(例如,抽成真空的储器、注射器、加压罐和/或产生真空或压力差的其它源或势能)。在其它实施方案中,压力差可以由体积和/或温度的变化产生。在其它实施方案中,压力差可由传输装置305、壳体310、致动器350至少一部分和/或流体流动路径315的被抽成真空和/或充注的部分(例如,隔离室330和/或任何其它合适的部分)产生。在一些实施方案中,压力差可以自动建立或者通过直接或间接干预(例如,由用户)建立。
[0157]
在一些实施方案中,流动控制器340可被配置成便于空气(或其它流体)位移通过传输装置305的一个或多个部分,这在一些情况下可以允许或导致横跨壳体310的一个或多个部分上的压力差和/或压力均等。此外,由压力差产生的流体(例如,气体和/或液体)的流动可以通过流动控制器340来选择性控制。例如,流动控制器340可被配置成在一个或多个操作状态或条件之间转换,以控制流体流量。在一些实施方案中,流动控制器340可以是由吸收性或半渗透性材料形成的构件或装置,其被配置成选择性地允许流体流过。例如,如在
‘
117公布和/或
‘
380申请中所详细描述的,这种吸收材料可以从第一状态转换成第二状态,在第一状态下,所述材料允许气体(例如空气)流过,但是阻止液体(例如,体液)流过,在第二状态下,所述材料基本上阻止气体和液体流过(例如,流动控制器340可以是可选择性渗透的血液屏障)。
[0158]
在一些实施方案中,流动控制器340可被配置成响应于施加在流动控制器340的至少一部分上的负压差和/或吸力而从第一状态转换成第二状态。例如,流动控制器340可包括一个或多个阀、膜、膈膜和/或等等。例如,在使用装置305之前,流动控制器340可以处于第一状态(例如,储存或非使用状态),并且响应于出口313流体耦接到流体收集装置395(例如,限定或被配置成限定负压和/或吸力的收集装置),流动控制器340可以转换成第二状态。在一些实施方案中,如
‘
380申请和/或
‘
477申请中所详细描述的,流动控制器340可以是被配置成响应于施加在气囊表面上的负压差和/或吸力而从第一状态转换或“翻转”成第二状态的气囊。
[0159]
在一些实施方案中,流动控制器340的尺寸、形状、布置和/或构成材料可被配置和/或以其它方式选择,使得流动控制器340以预定方式和/或以预定或所需速率从第一状态转换成第二状态。在一些情况下,控制流动控制器340从第一状态转换成第二状态的速率又可以控制和/或调节体液流入隔离室330的速率和/或隔离室330中产生的吸力的大小,所述吸力可用于将初始体积的体液吸入隔离室330。尽管图4未显示,在一些实施方案中,壳体310和/或流动控制器340可以包括任何合适的构件、特征、开口等,被配置成调节施加在流动控制器340上或通过其的吸力,这又可以调节流动控制器340从第一状态转换成第二状态
的速率。在一些情况下,控制流动控制器340转换的速率和/或隔离室330内产生的压力差和/或吸力的大小可以减少例如血液样品的溶血和/或静脉塌陷的可能性(例如,当从脆弱患者获取体液样品时,这尤其重要)。在一些情况下,调节流动控制器340的转换和/或在隔离室330中产生的压力差可以至少部分地控制传输到隔离室330中的体液的量或体积(即,可以控制初始量的体液的体积)。
[0160]
在一些实施方案中,流动控制器340可包括装置、构件和/或特征的任何合适的组合。应该理解的是,包括在本文所述实施方案中的流动控制器是通过示例而非限制的方式呈现的。因此,尽管在本文中描述了特定的流动控制器,但是应该理解,可以通过任何合适的方式来控制通过传输装置305的流体流动。
[0161]
装置305的致动器350至少部分地设置在壳体310内,并且被配置成控制、引导和/或以其它方式促进流体选择性地流过壳体310的至少一部分和/或一个或多个流体流动路径315的至少一部分。致动器350可具有任何合适的形状、尺寸和/或配置。在一些实施方案中,致动器350可以是被配置成以任何合适的方式在任何数量的状态之间转换的构件或装置。另外,致动器350可以以任何合适的方式(例如,用户致动、自动致动、机械致动、电子致动、化学致动和/或等等)致动。例如,致动器350可以与上文参考致动器250所描述的任何类似和/或基本相同。
[0162]
在图4所示的实施方案中,致动器350可被配置成当处于第一状态时选择性地建立入口312与隔离室330之间的流体连通,而当处于第二状态时选择性地建立入口312与出口313之间的流体连通。当处于第一状态时,致动器350可被配置成允许体液从入口312流出,通过流体流动路径315的至少一部分,到达或进入隔离室330。在一些实施方案中,致动器350可被配置成隔离、分开、分离和/或以其它方式防止出口313与入口312、流体流动路径315的至少一部分和/或隔离室330之间的流体连通。当处于第二状态时,如本文进一步详细描述的,致动器350可被配置成允许后续体积的体液(例如,初始体积的体液之后的一定体积的体液)从入口312通过流体流动路径315的至少一部分传输到出口313(和/或与出口313流体耦接的流体收集装置395)。另外,当处于第二状态时,致动器350可被配置成隔离、分开、分离和/或以其它方式防止隔离室330与入口312、出口313和/或流体流动路径315的至少一部分之间的流体连通。在图4所示的实施方案中,如本文进一步详细描述的,传输装置305使得致动器350和流动控制器340共同控制通过该装置的流体(例如,气体和/或液体)的流动。
[0163]
快速诊断测试装置370(本文中也称为“快速测试装置”或简称为“测试装置”)可具有任何合适的形状、尺寸和/或配置。在一些实施方案中,快速测试装置370可以可移除地耦接到传输装置305或其任何合适的部分。例如,在图4所示的实施方案中,快速测试装置370可以至少流体耦接到传输装置305的隔离室。在其它实施方案中,快速测试装置370可被集成到传输装置305中,使得快速测试装置370与隔离室330流体连通。例如,可以整体地或单一地形成传输装置305和快速测试装置370和/或以其它方式集成传输装置305和快速测试装置370。在其它实施方案中,壳体310可包括和/或可以形成端口、适配器和/或接收部分,快速测试装置370可以耦接到所述端口、适配器和/或接收部分,或者快速测试装置370可被插入所述端口、适配器和/或接收部分,以在快速测试装置370与隔离室330之间建立流体连通。
[0164]
在一些此类实施方案中,将快速测试装置370耦接到传输装置305可用于将一个或多个流动控制器、阀、隔膜、端口、密封件等从关闭或密封状态转换成打开状态,以允许传输装置305与测试装置370之间流体连通。尽管图4未显示,但在一些实施方案中,传输装置305可包括可被操纵以在隔离室330与快速测试装置370之间建立流体连通的第二致动器等。在其它实施方案中,致动器350可被转换以在隔离室330与快速测试装置370之间建立流体连通。
[0165]
在一些实施方案中,快速测试装置370可被配置成从传输装置305接收第一量的体液,并使用第一量的体液来执行一个或多个测试、测定和/或诊断程序。快速测试装置370可以是任何合适的测试装置。例如,如上文参考图2所示的lfa 170a所详细描述的,快速测试装置370可以是lfa等。在一些实施方案中,测试装置370和/或其方面或部分可以与上文详细描述的快速测试装置170和/或270基本类似。因此,快速测试装置370和/或其方面或部分在本文中不再详细描述。
[0166]
如上所述,系统300可用于从患者获取一个或多个体积的体液,其可用于一个或多个测试、测定和/或诊断程序。例如,在一些情况下,如上所述,用户诸如医生、内科医生、护士、抽血技师、技术人员等可操纵装置305以在入口312与体液源(例如,患者的静脉、来自脊髓腔的脑脊液(csf)、尿液收集物和/或等等)之间建立流体连通。在一些情况下,当入口312被放置成与体液源(例如,患者的一部分)流体连通时,致动器350可处于第一状态,使得流体流动路径315的至少一部分在入口312与隔离室330之间建立流体连通。
[0167]
这样,传输装置305可被配置成将初始体积的体液从体液源(例如,患者)传输到快速测试装置370。更具体地说,在图4所示的实施方案中,一旦入口312被放置成与体液源(例如,患者的一部分)流体连通,出口313就可以与流体收集装置395流体耦接。如上所述,在一些实施方案中,流体收集装置395可以是被配置成接收一定量的体液的任何合适的储器、容器和/或装置。例如,流体收集装置395可以是限定负压的抽成真空的储器或容器,和/或可以是可被操作以产生负压的注射器。在一些情况下,将出口313耦接到流体收集装置395选择性地将流体流动路径315的至少一部分暴露于流体收集装置395内的负压和/或吸力。在一些实施方案中,致动器350可处于第一状态,使得出口313与入口312隔离。另外,当致动器350处于第一状态时,出口313可以与流动控制器340流体连通(例如,经由流体流动路径315的一部分)。当流体收集装置395耦接到出口313时,流动控制器340可以类似地处于其第一状态。
[0168]
在流动控制器340是可选择性渗透的构件或膜的实施方案中,流动控制器340和致动器350的布置可以使得空气或气体流被允许通过出口313与隔离室330之间的流动控制器340。在此类实施方案中,如
‘
117公布和/或
‘
380申请中所详细描述的,这种布置导致由流体收集装置395产生的负压差或吸力的至少一部分被传输到隔离室330和/或通过隔离室330,这又可用于从体液源抽取初始体积的体液通过入口312和流体流动路径315的至少一部分,并进入隔离室330。
[0169]
或者,在流动控制器340是膈膜、挡板、阀、套管等的实施方案中,流动控制器340和致动器350的布置可使得流动控制器340的一部分和/或表面与出口313流体连通(例如,经由流体流动路径315的一部分)。这样,负压和/或吸力可施加在流动控制器340的一部分和/或表面上,进而可用于将流动控制器340从其第一状态转换成其第二状态,在第一状态下,
隔离室330具有第一容积,在第二状态下,隔离室330具有大于第一容积的第二容积。隔离室330可以使得容积的增加导致隔离室330内的压力降低,从而产生可用于将体液吸入隔离室330的负压差。因此,在此类实施方案中,如在
‘
380申请和/或
‘
477申请中所详细描述的,响应于流动控制器340的转换,初始体积的体液可被吸入隔离室330(例如,由于流动控制器340从第一状态转换成第二状态,隔离室330的体积增加)。
[0170]
体液的初始体积可以是任何合适的体液体积,诸如上述的任何体积或量。例如,在一些情况下,传输装置305可保持在第一状态或配置,直至预定和/或所需体积(例如,初始体积)的体液被传输到隔离室330。在一些实施方案中,初始体积可与隔离室330或其部分的体积相关联和/或至少部分基于该体积(例如,足以填充隔离室330或隔离室330的所需部分的体积)。在一些实施方案中,初始体积可以与足以使快速测试装置370执行一个或多个测试或测定的所需体积相关联和/或至少部分基于该体积。在其它实施方案中,体液的初始体积可与等于或大于与体液源和隔离室330之间限定的流体流动路径相关的体积的体液的量或体积相关联和/或至少部分基于该量或体积。在其它实施方案中,传输装置305可被配置成将体液流(例如,初始体积)传输到隔离室330中,直至隔离室330与入口312或体液源之间的压力差达到基本均等和/或以其它方式降低至所需阈值以下。
[0171]
在一些实施方案中,传输装置305可被配置成将体液流(例如,初始体积)传输到隔离室330中,直至流动控制器340转换成其第二配置。换句话说,在一些实施方案中,将初始体积的体液传输到隔离室330中可用于将流动控制器340置于其第二状态或配置。例如,在流动控制器340是可选择性渗透的构件的实施方案中,将初始体积的体液传输到隔离室330中可以使得初始体积的至少一部分润湿和/或浸透流动控制器340,这又将流动控制器340置于其第二状态,如在
‘
117申请和/或
‘
380申请中所详细描述的。在流动控制器340是膈膜和/或等等的实施方案中,如在
‘
380申请和/或
‘
477申请中详细描述的,初始体积向隔离室330的传输可与流动控制器340被置于其第二状态和/或配置(例如,响应于由流体收集装置395产生的负压)基本一致。此外,在图4所示的实施方案中,流动控制器340的布置使得当处于其第二状态和/或配置时,流动控制器340使隔离室330与出口313隔离和/或使隔离室330与出口313流体地分离,使得由流体收集装置395产生的负压和/或吸力不再作用于或通过隔离室330。
[0172]
在一些实施方案中,当流动控制器340处于其第二状态时并且在致动器从其第一状态转换成其第二状态之前,至少一部分初始体积的体液可被从隔离室330传输到快速测试装置370中。在一些实施方案中,致动器350被配置成将隔离室330与入口313、出口315和流体流动路径315的至少一部分隔离。在此类实施方案中,在致动器350从其第一状态转换成其第二状态之前,在转换过程中,和/或在致动器350从其第一状态转换成其第二状态之后,可以从隔离室330传输部分初始体积的体液。在一些实施方案中,初始体积的一部分的传输可以是自动的。在其它实施方案中,初始体积的一部分的传输可以响应于一个或多个用户输入和/或等等。
[0173]
在一些实施方案中,如上文参考快速测试装置270所详细描述的,将初始体积的体液的一部分传输到快速测试装置370中可以启动对初始体积的体液的该部分的测试和/或测定。此外,快速测试装置370可被配置成执行任何合适的测试和/或测定。例如,如上文所详细描述的,快速测试装置370可以是被配置成测试乳酸和/或pct的存在的lfa。此外,如上
面所详细描述的,一旦测试或测定完成,快速测试装置370可被配置成输出测试结果,所述测试结果可由人和/或一个或多个电子设备检测和/或评估。
[0174]
在一些实施方案中,致动器350从其第一状态到其第二状态的转换(例如,将传输装置305置于其第二状态或配置)可将初始体积的体液隔离、分离、分开和/或保留在隔离室330和/或快速测试装置370中。换句话说,致动器350可将隔离室330与入口312、出口313和流体流动路径315的一个或多个部分隔离和/或分离。在一些情况下,将初始体积的体液隔离在隔离室330中也可以隔离初始体积中的污染物。此外,如上面详细描述的,快速测试装置370的布置可以使得由快速测试装置370执行的测试和/或测定不容易受到此类污染,这意味着由快速测试装置370输出的测试结果的准确性不受此类污染影响。
[0175]
除了将隔离室330与入口312、出口313和流体流动路径315的至少一部分隔离之外,将致动器350置于其第二状态(并且使流动控制器340处于其第二状态)还经由流体流动路径315的至少一部分在入口312与出口313之间建立流体连通。例如,在一些实施方案中,将致动器350从其第一状态转换成其第二状态可以例如打开或关闭端口或阀,移动一个或多个密封件,移动或移除一个或多个障碍物,限定流动路径的一个或多个部分和/或等等。因此,响应于由流体收集装置395产生的负压和/或吸力,一个或多个后续体积的体液可从入口312流动,通过流体流动路径315的至少一部分,通过出口313,并进入流体收集装置395。如上所述,在收集或获取一个或多个后续体积的体液之前隔离初始体积的体液(例如,在快速测试装置370中)减少和/或基本上消除了所述一个或多个后续体积中的一定量的污染物。因此,系统300可被配置成获取初始体积的体液和一个或多个后续体积的体液,所述初始体积的体液可用于对污染具有相对低的敏感度的快速测试,一个或多个后续体积的体液可用于对污染具有相对高的敏感度的测试,如上面参考系统100和/或200所描述的。
[0176]
图5a和图5b是根据实施方案的流体传输和测定系统400的示意图,并且分别以第一状态和第二状态示出。流体传输和测定系统400(本文中也称为“系统”)可以至少包括流体传输装置405和快速诊断测试装置470。流体传输装置405和/或快速诊断测试装置470的部分和/或方面可以分别与上面详细描述的流体传输装置105、205和/或305和/或快速诊断测试装置170(和/或lfa 170a)、270和/或370类似和/或基本上相同。因此,本文不再进一步详细描述这些部分和/或方面。
[0177]
流体传输装置405(本文中也称为“传输装置”)可具有任何合适的形状、尺寸和/或配置。在一些实施方案中,传输装置405可被配置成从患者抽取体液(例如,血液)并使其进入和/或通过传输装置405。另外,传输装置405可被配置成将至少一些抽取的体液传输到一个或多个其它装置、储器、容器、小瓶、机器、测试、测定等,诸如快速诊断测试装置470和/或一个或多个流体收集装置(未在图5a和图5b中显示)。
[0178]
传输装置405至少包括壳体410和致动器450。装置405的壳体410可具有任何合适的形状、尺寸和/或配置。例如,在一些实施方案中,壳体410可以与上述壳体210和/或310类似和/或基本相同。具体而言,壳体410具有和/或形成入口412和出口413,并且可以在它们之间限定至少一个流体流动路径(未在图5a和图5b中显示)。入口412可以是任何合适的入口或端口,并且可以被配置成在壳体410与体液源(例如,患者)之间建立流体连通。出口413可以是任何合适的出口或端口,并且可被配置成在壳体410与流体收集装置之间建立流体连通(未在图5a和图5b显示),诸如上面详细描述的那些中的任一个。如本文所进一步详细
描述的,一条或多条由壳体410限定的流体流动路径在入口412与出口413之间延伸,并且可以选择性地在它们之间建立流体连通。
[0179]
如上面参考壳体310所描述的,图5a和图5b所示的壳体410包括隔离室430、形成隔离室430和/或耦接到隔离室430,所述隔离室430被配置成被选择性地放置成与流体流动路径和/或至少入口412流体连通。另外,隔离室430包括快速诊断测试装置470、耦接到快速诊断测试装置470和/或以其它方式配置成与快速诊断测试装置470流体连通地放置。隔离室430可具有任何合适的形状、尺寸和/或配置。例如,在一些实施方案中,隔离室430可具有约0.1ml至约5.0ml之间的体积和/或流体容量。在一些实施方案中,隔离室430可具有根据被配置成传输到隔离室430中和/或被配置成由快速诊断测试装置470测试的体液的量(例如,体液的初始或第一量)测量的体积。在一些实施方案中,隔离室430和/或其至少一部分可至少在形式和/或功能上与上文参照图4描述的隔离室330基本类似。因此,本文不再进一步详细描述隔离室430的部分和/或方面。
[0180]
在图5a和图5b所示的实施方案中,隔离室430的至少一部分可以包括吸收剂和/或亲水材料431。另外,隔离室430包括取样部分435和排气口424。吸收材料431可被设置在隔离室430的一部分内。例如,隔离室431的一个或多个内表面可以衬有吸收材料431和/或由吸收材料431形成。如图5a和图5b所示,隔离室430的布置可以使得隔离室430的取样部分435在吸收材料431的下游(例如,相对于隔离室430的一部分暂时流体耦接到入口412。以这种方式,吸收材料431可被配置成接收和/或吸收传输到隔离室430中的初始体积的体液的第一部分(portion)或部份(part)。在一些实施方案中,吸收材料431可在吸收预定量或体积的体液后变得饱和,使得传输到隔离室430中的任何额外量或体积的体液可流入取样部分435。如本文所进一步详细描述的,隔离室430的取样部分435可被放置成与快速诊断测试装置470流体连通,以将置于取样部分435中的一部分初始体积的体液传输到快速诊断测试装置470中。
[0181]
排气口424耦接到壳体410和/或隔离室430,并与隔离室430的内部容积流体连通。排气口424可被配置成当初始体积的体液被传输到隔离室430中时,将空气或气体排出隔离室430和/或以其它方式使空气或气体流出隔离室430。在一些实施方案中,将空气或气体排出隔离室430(例如,经由排气口424)可以降低原本可限制和/或阻碍体液流入隔离室430的隔离室430内的压力量。在一些实施方案中,通过排气口424排出空气或气体可以允许产生负压差,所述负压差可以促进初始体积的体液传输到隔离室430中。尽管吸收材料431和排气口424在图5a和图5b中显示为是分开的部件,但在其它实施方案中,吸收材料431可形成一个或多个排气口,所述排气口被配置成给隔离室430排气以及被配置成吸收初始体积的第一部分或部份。例如,吸收材料431可以形成隔离室430的一个或多个壁或壁的一个或多个部分。
[0182]
装置405的致动器450可具有任何合适的形状、尺寸和/或配置。在一些实施方案中,致动器450和/或其方面或部分可以与上文所详细描述的致动器150、250和/或350类似和/或基本相同。在一些实施方案中,致动器450可以至少部分地设置在壳体410内和/或部分地由壳体410形成。如上所述,致动器450可被配置成控制、引导和/或以其它方式促进流体选择性地流过壳体410的至少一部分和/或一个或多个流体流动路径的至少一部分。在一些实施方案中,致动器450可以是被配置成以任何合适的方式(例如,用户致动、自动致动、
机械致动、电子致动、化学致动和/或等等)在任何数量的状态(例如,两个、三个、四个或更多个)之间转换的构件或装置。
[0183]
更具体地,在图5a和图5b所示的实施方案中,致动器450可被配置成在第一状态与第二状态之间转换,在第一状态下,入口412与隔离室430流体连通(图5a),在第二状态下,入口412与出口413流体连通(图5b)。在一些实施方案中,致动器450在处于第一状态时,可被配置成隔离、分开、分离和/或以其它方式防止出口413与入口412之间和/或出口413与隔离室430之间的流体连通。相反地,在第二状态下,致动器450可被配置成允许后续体积的体液(例如,初始体积的体液之后的体积的体液)从入口412通过一个或多个流体流动路径(未在图5a和图5b中显示)传输到出口413(和/或与出口413流体耦接的流体收集装置)。另外,当处于第二状态时,致动器450可被配置成隔离、分开、分离和/或以其它方式防止隔离室430与入口412、隔离室430与出口413和/或隔离室430与在入口412与出口413之间延伸的流体流动路径的至少一部分之间的流体连通。这样,致动器450可以在结构上和/或功能上类似于上文详细描述的致动器150、250和/或350。
[0184]
快速诊断测试装置470(本文中也称为“快速测试装置”或简称为“测试装置”)可具有任何合适的形状、尺寸和/或配置。在一些实施方案中,快速测试装置470可以可移除地耦接到传输装置405或其任何合适的部分。例如,在图5a和图5b所示的实施方案中,快速测试装置470可被配置成接合或耦接到壳体410和/或隔离室4350,使得快速测试装置470被放置成与隔离室430的取样部分435流体连通。在一些实施方案中,壳体410可以包括和/或可以形成端口、适配器和/或接收部分,快速测试装置470可耦接到所述端口、适配器和/或接收部分,或者快速测试装置470可被插入所述端口、适配器和/或接收部分,以在快速测试装置470与隔离室430的取样部分435之间建立流体连通。此外,在图5a和图5b所示的实施方案中,将致动器450从其第一状态转换为其第二状态可以在隔离室430与快速测试装置470之间建立流体连通(例如,通过一个或多个流动控制器、阀、膈膜、端口、密封件、对齐的流动路径和/或用于建立流体连通的其它合适的构件或装置)。在一些实施方案中,将致动器450从其第一状态转换为其第二状态可以在隔离室430与快速测试装置470之间建立流体连通。
[0185]
在一些实施方案中,快速测试装置470可被配置成从隔离室430的取样部分435接收第一量的体液,并使用第一量的体液进行一种或多种测试、测定和/或诊断程序。快速测试装置470可以是任何合适的测试装置。例如,如上面参考图2所示的lfa 170a所详细描述的,快速测试装置470可以是lfa等。在一些实施方案中,测试装置470和/或其方面或部分可以与上文所详细描述的快速测试装置170、270和/或370基本上类似。因此,快速测试装置470和/或其方面或部分在本文中不再详细描述。
[0186]
系统400可用于从患者获取一个或多个体积的体液,其可用于一个或多个测试、测定和/或诊断程序。如上所述,例如,入口412可被放置成与体液源流体连通。在一些情况下,如图5a所示的,当入口412被放置成与体液源(例如,患者的一部分)流体连通时,致动器450可处于第一状态,从而在入口412与隔离室430之间建立流体连通,并将出口413与入口412隔离。这样,传输装置405可被配置成将初始体积的体液从体液源(例如,患者)传输到快速测试装置470。在一些实施方案中,初始体积的体液可以响应于隔离室430与入口412和/或体液源之间的压力差,流向隔离室430和/或流入隔离室430。在一些实施方案中,排气口424可被配置成允许空气或气体流出隔离室430,这可有助于初始体积的体液流入隔离室430。
在一些实施方案中,排气口424可被配置成以类似于例如
‘
117公布中描述的排气口和/或等等的方式给隔离室430排气。
[0187]
体液的初始体积可以是任何合适的体液体积,诸如上述的任何体积或量。更具体地说,在图5a和图5b所示的实施方案中,体液的初始体积足以浸透和/或润湿(或基本上浸透和/或润湿)置于隔离室430中的吸收材料431,以及足以填充(或基本上填充)隔离室430的取样部分435。在一些实施方案中,隔离室430的填充可以是连续的,因为初始体积的体液流首先被吸收材料431吸收,直至吸收材料431被浸透,然后初始体积的体液的剩余部分可以流入和/或填充隔离室430的取样部分435。在一些实施方案中,连续填充隔离室430可以使得初始体积的体液的一部分(例如,第一部分)可以包含污染物(例如,与静脉穿刺事件相关的和/或由静脉穿刺事件产生的,流体耦接一种或多种成分,等等),而初始体积的体液的一部分(例如,第二部分)可以包含减少量的污染物和/或可以基本上不含污染物。在一些情况下,一旦初始体积的体液被传输到隔离室430中,体液的流动就可以停止并且/或者基本上可使压力差均等,这可以减缓或停止体液的流动。
[0188]
在一些实施方案中,在将初始体积的体液传输到隔离室430中后,致动器450可从其第一状态(图5a)转换成其第二状态(图5b)。例如,在一些实施方案中,致动器450可以相对于入口412和出口413被移动、滑动、切换、旋转和/或以其它方式转换。在一些实施方案中,转换和/或移动致动器450可包括转换和/或移动壳体410的至少一部分。在其它实施方案中,致动器450可以相对于壳体410被移动(例如,壳体410无需被转换和/或移动)。
[0189]
如图5b所示,将致动器450从第一状态转换成第二状态可以在隔离室430的取样部分435与快速测试装置470之间建立流体连通,并且可将隔离室430与入口412、出口413和/或它们之间的流体流动路径的一个或多个部分隔离。在一些实施方案中,致动器450的布置可以使得将致动器450置于第二状态导致和/或增加包括吸收材料431的隔离室430的一部分与包括、形成和/或限定取样部分435的隔离室430的一部分之间的气隙。气隙能够有助于体液从取样部分435传输到快速测试装置470(例如,通过允许所需相对压力或压力差)。另外,在污染物包含在被吸收材料431吸收的初始体积的部分中的情况下,这种布置可以确保只有置于隔离室430的取样部分435中的初始体积的一部分被传输到快速测试装置470中。
[0190]
当致动器450从其第一状态转换成其第二状态时,至少一部分初始体积的体液可从隔离室430的取样部分435传输到快速测试装置470中。在一些实施方案中,初始体积的一部分的传输可以是自动的。在其它实施方案中,初始体积的一部分的传输可以响应于一个或多个用户输入和/或等等。在一些实施方案中,将致动器450置于第二状态可以将快速测试装置470流体耦接到隔离室430的取样部分435,从而允许流体在它们之间传输。
[0191]
在一些实施方案中,如上文参考快速测试装置270所详细描述的,将初始体积的体液的一部分传输到快速测试装置470中可以启动对初始体积的体液的该部分的测试和/或测定。在一些情况下,如图5b所示,系统400、传输装置405和/或快速测试装置470可被配置成提供缓冲液481(或任何其它合适的溶液),其可以与初始体积的体液的一部分混合。快速测试装置470可被配置成执行任何合适的测试和/或测定。例如,如上文所详细描述的,快速测试装置470可以是被配置成测试乳酸和/或pct的存在的lfa。此外,一旦测试或测定完成,快速测试装置470就可被配置成输出测试结果,所述测试结果可由人和/或一个或多个电子设备检测和/或评估,如上文参考快速测试装置170、270和/或370所详细描述的。
[0192]
将致动器450从其第一状态转换成其第二状态可以将初始体积的液体隔离、分离、分开和/或保留在隔离室430和/或快速测试装置470中。换句话说,致动器450可将隔离室430与入口412、出口413和流体流动路径的一个或多个部分隔离和/或分离。在一些情况下,将初始体积的体液隔离在隔离室430中也可以隔离初始体积中的污染物(例如,被吸收材料431吸收的初始体积的至少一部分)。此外,如上面所详细描述的,快速测试装置470的布置可以使得由快速测试装置470执行的测试和/或测定不容易受到此类污染,这意味着由快速测试装置470输出的测试结果的准确性不受此类污染影响。在其它情况下,吸收性材料431接收和/或吸收体液的初始体积的第一部分或部份可以允许快速测试装置470进行一种或多种可能至少部分地对污染物敏感的测试。
[0193]
另外,将致动器450转换成其第二状态经由设置在入口412与出口413之间的流体流动路径的至少一部分在入口412与出口413之间建立流体连通。例如,将致动器450从其第一状态转换成其第二状态可以打开或关闭端口或阀,移动一个或多个密封件,移动或移除一个或多个障碍物,限定流动路径的一个或多个部分,和/或等等。在一些实施方案中,在致动器被置于其第二状态之前或之后,出口413可被置于与流体收集装置流体连通。如上文所详细描述的,流体收集装置可以限定负压和/或吸力和/或可被配置成产生负压和/或吸力,所述负压和/或吸力可用于将体液吸入流体收集装置。因此,响应于负压和/或吸力,一个或多个后续体积的体液可从入口412,通过任何合适的流体流动路径或其部分,通过出口413,流入流体收集装置。如上所述,在收集或获取一个或多个后续体积的体液之前,将初始体积的体液隔离在隔离室430中减少和/或基本上消除了一个或多个后续体积中的污染物的量。因此,如上文参考系统100、200和/或300所描述的,系统400可被配置成获取初始体积的体液和一个或多个后续体积的体液,初始体积的体液可用于一个或多个快速测试过程,后续体积的体液可用于对污染具有相对高的灵敏度的测试(例如,血液培养测试)。
[0194]
图6a至图6d是根据实施方案的至少一部分的流体传输和测定系统500的示意图。流体传输和测定系统500(本文中也称为“系统”)可以至少包括流体传输装置505和快速诊断测试装置570。流体传输装置505和/或快速诊断测试装置570的部分和/或方面可以分别与于上文所详细描述的流体传输装置105、205、305和/或405和/或快速诊断测试装置170(和/或lfa 170a)、270、370和/或470类似和/或基本上相同。因此,本文不再进一步详细描述这些部分和/或方面。
[0195]
流体传输装置505(本文中也称为“传输装置”)可具有任何合适的形状、尺寸和/或配置。在一些实施方案中,传输装置505可被配置成从患者抽取体液(例如,血液)并使其进入和/或通过传输装置505。另外,传输装置505可被配置成将至少一些抽取的体液传输到一个或多个其它装置、储器、容器、小瓶、机器、测试、测定等,诸如快速诊断测试装置570和/或一个或多个流体收集装置(未在图6a-图6d中显示)。传输装置505和/或其方面或部分可与上文所详细描述的传输装置105、205、305和/或405中的任一个基本类似。因此,在本文中不再详细描述传输装置505。
[0196]
快速诊断测试装置570(本文中也称为“快速测试装置”或简称为“测试装置”)可以是任何合适的测试装置。在一些实施方案中,测试装置570和/或其方面或部分可与上文详细描述的快速测试装置170(和/或lfa 170a)、270、370和/或470基本上类似。因此,快速测试装置570和/或其方面或部分在本文中不再详细描述。
170a)、270、370、470和/或570类似和/或基本相同。因此,本文不再进一步详细描述这些部分和/或方面。
[0202]
流体传输装置605(本文中也称为“传输装置”)可具有任何合适的形状、尺寸和/或配置。在一些实施方案中,传输装置605可被配置成从患者抽取体液(例如,血液)并使其进入和/或通过传输装置605。另外,传输装置605可被配置成将至少一些抽取的体液传输到一个或多个其它装置、储器、容器、小瓶、机器、测试、测定等,诸如快速诊断测试装置670和/或一个或多个流体收集装置(未在图7a-图7d中显示).
[0203]
传输装置605至少包括壳体610和致动器650。装置605的壳体610可具有任何合适的形状、尺寸和/或配置。例如,在一些实施方案中,壳体610可以与上述壳体210、310和/或410类似和/或基本相同。具体地,壳体610具有和/或形成入口612和出口613,并且可以在它们之间限定流体流动路径615。入口612可以是任何合适的入口或端口,并且可以被配置成在壳体610与体液源(例如,患者)之间建立流体连通。出口613可以是任何合适的出口或端口,并且可被配置成在壳体610与流体收集装置之间建立流体连通(未在图7a-图7d中显示),例如上文所详细描述的那些中的任一个。如本文所进一步详细描述的,由壳体610限定的流体流动路径615在入口612与出口613之间延伸,并且可以选择性地在它们之间建立流体连通。
[0204]
如上文参考壳体410所述,图7a-图7d所示的壳体610包括、形成和/或耦接到隔离室630,所述隔离室630被配置成选择性地放置成与流体流动路径和/或至少入口612流体连通。另外,隔离室630包括、形成和/或限定取样部分635和端口625。隔离室630可具有任何合适的形状、尺寸和/或配置。例如,在一些实施方案中,隔离室630和/或其至少一部分可以至少在形式和/或功能上与上文所详细描述的隔离室330和/或430基本类似。因此,本文不再进一步详细描述隔离室630的部分和/或方面。
[0205]
端口625耦接到壳体610和/或隔离室630,并与隔离室630的内部容积流体连通。更具体地说,如图7a-图7d所示,端口625包含在壳体610中和/或耦接到壳体610,并与隔离室630的取样部分635流体连通。在一些实施方案中,如上文参考排气口424所详细描述的,端口625和/或其至少一部分可被配置成在初始体积的体液被传输到隔离室630中时将空气或气体排出隔离室630和/或以其它方式使空气或气体流出隔离室630。隔离室630的取样部分635可被放置成与快速诊断测试装置670流体连通,以将置于取样部分635中的一部分初始体积的体液传输到快速诊断测试装置670中。在图7a-图7d所示的实施方案中,如上文参考图6a和图6b中所示的端口525所描述的,快速诊断测试装置670可被放置成通过端口625和/或任何其它合适的端口与取样部分635流体连通。
[0206]
装置605的致动器650可具有任何合适的形状、尺寸和/或配置。在一些实施方案中,致动器650和/或其方面或部分可以与上文所详细描述的致动器150、250、350和/或450类似和/或基本相同。在一些实施方案中,致动器650可以至少部分地设置在壳体610内和/或部分地由壳体610形成。如上所述,致动器650可被配置成控制、引导和/或以其它方式促进流体选择性地流过壳体610的至少一部分和/或一个或多个流体流动路径的至少一部分。致动器650可以是被配置成以任何合适的方式(例如,用户致动、自动致动、机械致动、电子致动、化学致动等)在任何数量的状态(例如,两个、三个、四个或更多个)之间转换的任何一个或多个合适的构件或一个或多个装置。
[0207]
更具体地,在图7a-图7d所示的实施方案中,致动器650包括第一构件651和第二构件660。致动器650的第一构件651可具有任何合适的形状、尺寸和/或配置。第一构件651可以是具有至少一个密封件652(例如,设置在第一构件651的端部)的柱塞等。在一些实施方案中,第一构件651的端部可以例如分离和/或至少部分限定隔离室630的取样部分635。例如,隔离室630的取样部分635可被设置在第一构件651的端部的一侧,而隔离室630的其余部分被设置在第一构件651的端部的相对侧。此外,密封件652的布置可以使得密封件652接合和/或接触壳体610的内表面,以在其间形成和/或限定基本上不透流体的密封。第一构件651还包括一个或多个阀、端口、开口、通道、选择性渗透构件等(本文中称为“阀653”),其被配置成在隔离室635的取样部分635与隔离室630的其余部分之间建立选择性流体连通,如本文所进一步详细描述的。
[0208]
致动器650的第二构件660可具有任何合适的形状、尺寸和/或配置。例如,在图7a-图7d所示的实施方案中,第二构件660可被设置在第一构件651的至少一部分周围和/或之上。第二构件660包括一组密封件661。更具体地,第二构件660可以包括一组三个密封件。如图所示,第二构件660可具有第一端部和与第一端部相对的第二端部。第二构件660的第一端部包括外部密封件661,其被配置成接合和/或接触壳体610的内表面,以在其间限定基本上不透流体的密封。另外,第二构件660的第一端部包括内部密封件661,其被配置成接合和/或接触第一构件651的一部分,以在其间限定基本上不透流体的密封。第二构件660的第二端部包括外部密封件661,其被配置成接合和/或接触壳体的内表面,以在其间限定基本上不透流体的密封。
[0209]
如图7a-图7d所示,致动器的第一构件651和第二构件660的布置使得隔离室630的一部分(例如,除取样部分635之外的部分)被设置和/或限定在例如第一构件651的端部与第二构件660的第一端部之间。另外,第二构件660被配置成至少部分地限定第二构件660的第一端部与第二端部之间的流体流动路径615。因此,第二构件660的第一端部和密封件661(包括在第一端部中)将隔离室630与流体流动路径615隔离和/或流体分离。
[0210]
致动器650被配置成在至少第一状态、第二状态和第三状态之间转换。如图7a-图7d所示,无论致动器650的状态如何,第一构件651的端部和包括在其中的密封件652被设置在入口612的第一侧和出口613的第一侧上并且保留在其上。类似地,无论致动器650的状态如何,第二构件660的第二端部和包括在其中的密封件661都被设置在入口612的第二侧(与第一侧相对)和出口613的第二侧(与第一侧相对)上并保留在其上。然而,第二构件660的第一端部和设置在其中的密封件661被配置成:(i)当致动器650处于第一状态和第二状态时(图7a和图7b),设置在入口612的第二侧和出口613的第一侧上,和(ii)当致动器650处于第三状态时(图7c和7d),设置在入口612的第一侧和出口613的第一侧上。因此,如本文所进一步详细描述的,致动器650的布置使得转换致动器650可以经由流体流动路径615选择性地引导和/或转换(i)入口612与隔离室630之间以及(ii)入口612与出口613之间的流体流。
[0211]
快速诊断测试装置670(本文中也称为“快速测试装置”或简称为“测试装置”)可以是任何合适的测试装置。例如,如上面参考图2所示的lfa 170a所详细描述的,快速测试装置670可以是lfa等。在一些实施方案中,测试装置670和/或其方面或部分可与上文所详细描述的快速测试装置170、270、370和/或470基本上类似。因此,快速测试装置670和/或其方面或部分在本文中不再详细描述。
[0212]
如图7d所示,快速测试装置670可被配置成经由端口625接合或耦接到壳体610。在一些实施方案中,例如,端口625可以是阀、耦接器和/或任何合适的可重新配置的构件或装置,其被配置成(i)从隔离室630中排出空气或气体,如上文参考排气口424所述的,以及(ii)接收快速测试装置670的一部分,以将快速测试装置670放置成与隔离室630的取样部分635流体连通。例如,快速测试装置670可包括耦接构件678,当快速测试装置670与其耦接时,所述耦接构件678可与隔离室630的取样部分635建立流体连通。在一些实施方案中,耦接构件678可以是例如能够穿刺和/或以其它方式前进通过端口625的穿刺构件、针、管、毛细管等。在一些实施方案中,耦接构件678可与上文参照图6a-图6d所描述的耦接构件578基本上类似。在一些实施方案中,端口625可以是自愈合的,一旦从端口625移除测试装置670的耦接部分678,则端口625就可以密封。如图7d所示,测试装置670的耦接部分678可以耦接到测试装置670的基底671(例如,直接耦接到基底671和/或经由诸如附接机构579等附接机构耦接)。以这种方式,耦接部分678可以将一定体积的体液从隔离室630的取样部分635传输到测试装置670中。作为响应,测试设备670可以使用该体积的体液来执行一个或多个测试、测定和/或诊断程序。
[0213]
系统600可用于从患者获取一个或多个体积的体液,其可用于一个或多个测试、测定和/或诊断程序。如上所述,例如,入口612可被放置成与体液源流体连通。如图7a所示,当入口612被放置成与体液源(例如,患者的一部分)流体连通时,致动器650可处于第一状态,从而在入口612与隔离室630之间建立流体连通,并将出口613与入口612隔离。此外,当致动器650处于第一状态时,第一构件651的端部可以靠近或邻近入口612的第一侧,并且第二构件660的第一端部可以靠近或邻近入口612的第二侧。以这种方式,限定在第一构件651与第二构件660之间的隔离室630的部分可以具有第一容积。
[0214]
在一些情况下,一旦入口612被放置成与体液源流体连通,致动器650就可从其第一状态转换成其第二状态。例如,如图7b所示,第一构件651可相对于入口612和第二构件660转移或移动,这又增加了设置在第一构件651与第二构件660之间的隔离室630的部分的容积。另外,第一构件651的转移和/或移动可减少隔离室630的取样部分635的容积,且端口625的布置可使得取样部分635中含有的空气或气体可被允许逸出和/或流出取样部分635。第一构件651的端部可被配置成限制和/或基本上防止空气从隔离室630的取样部分635流入隔离室630的其余部分,使得隔离室630的其余部分内的容积增加导致负压差,所述负压差有效地通过入口612从体液源抽取初始体积的体液,并使其进入隔离室630,如图7b所示。
[0215]
体液的初始体积可以是任何合适的体液体积,诸如上述的任何体积或量。在一些实施方案中,一旦初始体积的体液被传输到隔离室630中,体液的流动可以停止并且/或者可使压力差基本上均等,这可以减缓或停止体液的流动。在此类实施方案中,致动器650然后可以从其第二状态转换成其第三状态。在其它实施方案中,致动器650通过三个状态的转换可以是基本上连续的转换。在这种实施方案中,初始体积的体液可以是当致动器650从其第一状态转换成其第二状态时传输到隔离室630中的体液量,并且继续使致动器650从其第二状态转换成其第三状态可用于停止流入隔离室630中。
[0216]
当初始体积的体液被包含在隔离器630中时,致动器650可从其第二状态转换成其第三状态。如图7c所示,将致动器650转换成第三状态可以包括相对于入口612和致动器650的第一构件651转移和/或移动第二构件660。第二构件660的转移和/或移动将第二构件的
第一端部从入口612的第二侧转移和/或移动到入口612的第一侧,从而将隔离室630与入口612隔离和/或流体分离。此外,第二构件660相对于第一构件651的转移和/或移动可减小设置在其间的隔离室630的部分的容积。在一些实施方案中,如图7c所示,隔离室630的该部分的容积减小导致压力的增加,这可用于将阀653从关闭状态转换成打开状态,从而允许至少一些初始体积的体液传输到隔离室630的取样部分635中。
[0217]
如图7d所示,快速测试装置670可耦接到壳体610和/或以其它方式放置成与隔离室630的取样部分635流体连通(例如,通过耦接构件678)。因此,至少一部分体液可以从隔离室630的取样部分635传输并进入快速测试装置670中。在一些实施方案中,初始体积的一部分的传输可以是自动的。在其它实施方案中,初始体积的一部分的传输可以响应于一个或多个用户输入等(例如,经由致动器650和/或图7a-图7d中未显未的任何其它合适的致动机构)。在一些实施方案中,如上文参考快速测试装置270所详细描述的,将初始体积的体液的一部分传输到快速测试装置670中可以启动对初始体积的体液的该部分的测试和/或测定。尽管图7a-图7d中未所示,但在一些情况下,系统600、传输装置605和/或快速测试装置670可被配置成提供缓冲液(或任何其它合适的溶液),所述缓冲液可以与该部分初始体积的体液混合。快速测试装置670可被配置成执行任何合适的测试和/或测定。例如,如上文所详细描述的,快速测试装置670可以是被配置成测试乳酸和/或pct的存在的lfa。此外,如上文参考快速测试装置170、270、370和/或470所详细描述的,一旦测试或测定完成,则快速测试装置670就可被配置成输出测试结果,所述测试结果可以被人和/或一个或多个电子设备检测和/或评估。
[0218]
如上所述,将致动器650从其第二状态转换成其第三状态可以将初始体积的体液隔离、分离、分开和/或保留在隔离室630和/或快速测试装置670中,这又可以隔离初始体积中的污染物。此外,如上面所详细描述的,快速测试装置670的布置可以使得由快速测试装置670执行的测试和/或测定不容易受到此类污染,这意味着由快速测试装置670输出的测试结果的准确性不受此类污染影响。
[0219]
如图7c和图7d所示,将致动器650从其第二状态转换成其第三状态经由设置在致动器650的第二构件660的第一端部与第二端部之间的流体流动路径615在入口612与出口613之间建立了流体连通。更具体地,当致动器650处于其第三状态时,第二构件660的第一端部被设置在入口612的第一侧上,第二构件660的第二端部设置在出口613的第二侧上。换句话说,入口612和出口613都设置在第二构件660的第一端部与第二端部之间。因此,当致动器650处于第三状态时,流体流动路径615可以在入口612与出口613之间建立流体连通。
[0220]
在一些实施方案中,在致动器650被放置在其第三状态之前或之后,出口613可被放置成与流体收集装置流体连通(未在图7a-7d中示出)。如上文所详细描述的,流体收集装置可以限定负压和/或吸力和/或可被配置成产生负压和/或吸力,所述负压和/或吸力可用于将体液吸入流体收集装置。因此,响应于负压和/或吸力,一个或多个后续体积的体液可从入口612流动,通过流体流动路径615,通过出口613,并进入流体收集装置。如上所述,在收集或获取一个或多个后续体积的体液之前,将初始体积的体液隔离在隔离室630中减少和/或基本上消除了一个或多个后续体积中的污染物的量。因此,系统600可被配置成获取初始体积的体液和一个或多个后续体积的体液,初始体积的体液可用于对污染具有相对低的敏感度的快速测试,后续体积的体液可用于对污染具有相对高的敏感度的测试,如上文
参考系统100、200、300和/或400所描述的。
[0221]
图8和图9a-9d示出了根据实施方案的流体传输和测定系统700。流体传输和测定系统700(本文中也称为“系统”)可以至少包括流体传输装置705和快速诊断测试装置770。流体传输装置705和/或快速诊断测试装置770的部分和/或方面可以分别与上文详细描述的的流体传输装置105、205、305、405、505和/或605,和/或快速诊断测试装置170(和/或lfa 170a)、270、370、470、570和/或670类似和/或基本上相同。因此,本文不再进一步详细描述这些部分和/或方面。
[0222]
流体传输装置705(本文中也称为“传输装置”)可具有任何合适的形状、尺寸和/或配置。在一些实施方案中,传输装置705可被配置成从患者抽取体液(例如,血液)并使其进入和/或通过传输装置705。另外,传输装置705可被配置成将至少一些抽取的体液传输到一个或多个其它装置、储器、容器、小瓶、机器、测试、测定等,诸如快速诊断测试装置770和/或一个或多个流体收集装置(未在图8和图9a-9d中显示)。
[0223]
传输装置705至少包括壳体710和致动器750。装置705的壳体710可具有任何合适的形状、尺寸和/或配置。例如,在一些实施方案中,壳体710可与至少上述壳体610类似和/或基本相同。具体地,壳体710具有和/或形成入口712和出口713,并且可以在它们之间限定流体流动路径715。入口712可以是任何合适的入口或端口,并且可以被配置成在壳体710与体液源(例如,患者)之间建立流体连通。出口713可以是任何合适的出口或端口,并且可被配置成在壳体710与流体收集装置之间建立流体连通(未在图8-9d中显示),诸如上文所详细描述的那些中的任一个。如本文所进一步详细描述的,至少部分由壳体710限定的流体流动路径715在入口712与出口713之间延伸,并且可以选择性地在其之间建立流体连通。
[0224]
如上所述,至少参考壳体610、壳体710(图8-9d所示)包括、形成和/或耦接到隔离室730,所述隔离室730被配置成选择性地放置成与流体流动路径和/或至少入口712流体连通。此外,壳体限定了开口721和/或端口,所述开口和/或端口被配置成接收快速诊断测试装置770的一部分,如本文所进一步详细描述的。隔离室730可具有任何合适的形状、尺寸和/或配置。例如,在一些实施方案中,隔离室730和/或其至少一部分可以至少在形式和/或功能上与上文所详细描述的隔离室330、430和/或630基本上类似。因此,本文不再进一步详细描述隔离室730的部分和/或方面。
[0225]
装置705的致动器750可具有任何合适的形状、尺寸和/或配置。在一些实施方案中,致动器750和/或其方面或部分可以与上文所详细描述的致动器150、250、350、450和/或650类似和/或基本相同。在一些实施方案中,致动器750可以至少部分地设置在壳体710内和/或部分地由壳体710形成。如上所述,致动器750可被配置成控制、引导和/或以其它方式促进流体选择性地流过壳体710的至少一部分和/或一个或多个流体流动路径的至少一部分。致动器750可以是被配置成以任何合适的方式(例如,用户致动、自动致动、机械致动、电子致动、化学致动等)在任何数量的状态(例如,两个、三个、四个或更多个)之间转换的任何一个或多个合适的构件或一个或多个装置。
[0226]
更具体地说,如图9a-9d所示,致动器750包括第一构件751、第二构件760和第三构件765。致动器750的第一构件751可具有任何合适的形状、尺寸和/或配置。例如,第一构件751可以至少在形式和/或功能上与上文所详细描述的致动器650的第一构件651类似。第一构件751包括设置在第一构件751的第一端部的至少一个密封件752。密封件752的布置可以
使得密封件752接合和/或接触壳体710的内表面,以在其间形成和/或限定基本上不透流体的密封。
[0227]
第一构件751的第一端部还包括与取样通道735流体连通的端口725。在一些实施方案中,例如,端口725可以是阀、耦接器和/或任何合适的可重新配置的构件或装置,其被配置成(i)将空气或气体排出取样通道735和/或允许空气或气体流出取样通道735,和(ii)接收快速测试装置770的一部分,以将快速测试装置770置于与取样通道735流体连通,如上文参考端口625所描述的。取样通道735被设置在第一构件751中和/或由第一构件751限定。例如,在一些实施方案中,第一构件751可具有限定取样通道735的中空细长部分。此外,第一构件751的这一部分可以限定和/或可具有开口、端口、阀、可选择性渗透的构件等,其被配置成将取样通道735放置成与隔离室730选择性流体连通。在一些实施方案中,虽然取样通道735被包括在致动器750的第一构件751中和/或由致动器750的第一构件751限定,但是取样通道735可以至少在形式和/或功能上与上文参照图7a-7d所描述的隔离室630的取样部分635类似。
[0228]
如图9a-9d所示,第一构件751还包括接合构件755,其被设置在第一构件751的与第一端部相对的第二端部处或其上。接合构件755可以是任何合适的形状、尺寸和/或配置。例如,在一些实施方案中,接合构件755可以是突起、袢扣(tab)、按钮、旋钮和/或任何其它合适的接合构件。如本文所进一步详细描述的,接合构件755被配置成选择性地接合致动器750的第三构件765的一部分,以引导和/或至少部分地控制第一构件751、第二构件760和/或第三构件765之间的相对运动。
[0229]
致动器750的第二构件760可具有任何合适的形状、尺寸和/或配置。如图9a-9d所示,第二构件760可被设置在第一构件751的至少一部分周围和/或之上。第二构件760包括一组密封件761。如所显示的,第二构件760可包括具有内部密封件761和外部密封件761的第一端部,以及与第一端部相对的具有外部密封件761的第二端部。以这种方式,第二构件760可以与致动器650的第二构件660类似和/或基本相同。因此,第二构件760和/或其方面或部分在本文中不再详细描述。
[0230]
第三构件765可具有任何合适的形状、尺寸和/或配置。在一些实施方案中,第三构件765可包括在壳体710的一部分和/或传输装置705的外部分中和/或可形成壳体710的一部分和/或传输装置705的外部分。例如,如图9a-9d所示,壳体710、第一构件751和第二构件760的至少一部分可被设置在第三构件765的一部分内。更具体地,第三构件765可以是具有开口端和基本封闭端的基本中空的圆柱体等。基本封闭的端部包括棘爪、凹部、开口和/或接合结构(本文中称为“接合结构766”)和/或限定棘爪、凹部、开口和/或接合结构。接合结构766可以与第一构件751的接合构件755接触和/或以其它方式选择性地接合第一构件751的接合构件755。例如,如本文所进一步详细描述的,接合构件755可以被配置成接合和/或接触接合结构766,这又可以导致当致动器750在两个或更多个状态或配置之间转换时,第一构件751和第三构件765一起和/或同时移动。此外,如本文所进一步详细描述的,致动器750的一部分转换可导致接合构件755脱离接合结构766和/或相对于接合结构766移动,这又可导致第一构件751相对于第三构件765移动(或者反之亦然)。
[0231]
如图9a-9d所示,致动器的第一构件751和第二构件760的布置使得隔离室730设置和/或限定在例如第一构件751的第一端部与第二构件760的第一端部之间。另外,第二构件
760被配置成至少部分地限定第二构件760的第一端部与第二端部之间的流体流动路径715。因此,第二构件760的第一端部和密封件761(包括在第一端部中)将隔离室730与流体流动路径715隔离和/或流体分离。
[0232]
致动器750被配置成在至少第一状态、第二状态、第三状态和第四状态之间转换。如图9a-图9d所示,无论致动器750的状态如何,第一构件751的第一端部和包括在其中的密封件752设置在入口712的第一侧和出口713的第一侧上并保留在其上。类似地,无论致动器750的状态如何,第二构件760的第二端部和包括在其中的密封件761都被设置在入口712的第二侧(与第一侧相对)和出口713的第二侧(与第一侧相对)上并保留在其上。然而,第二构件760的第一端部和设置在其中的密封件761被配置成:(i)当致动器750处于第一状态(图9a)、第二状态(图9b)和第三状态(图9c)时,设置在入口712的第二侧和出口713的第一侧,和(ii)当致动器750处于第四状态(图9d)时设置在入口712的第一侧和出口713的第一侧。因此,如本文所进一步详细描述的,致动器750的布置使得转换致动器750可以经由流体流动路径715选择性地引导和/或转换(i)入口712与隔离室730之间以及(ii)入口712与出口713之间的流体流。
[0233]
快速诊断测试装置770(本文中也称为“快速测试装置”或简称为“测试装置”)可以是任何合适的测试装置。例如,如上面参考图2所示的lfa 170a所详细描述的,快速测试装置770可以是lfa等。在一些实施方案中,测试装置770和/或其方面或部分可以基本上类似于上面详细描述的快速测试装置170、270、370、470、570和/或670。因此,快速测试装置770和/或其方面或部分在本文中不再详细描述。
[0234]
如图9d所示,快速测试装置770包括耦接构件778,其耦接到测试装置770的基底771和/或至少与测试装置770的基底771流体连通(例如,直接耦接到基底771和/或经由诸如附接机构579等附接机构耦接)。当快速测试装置770与传输装置705连接时,连接构件778可以至少部分地插入通过壳体710的开口721,以建立与取样通道735的流体连通。例如,耦接构件778可以是穿刺构件、针、管、毛细管和/或能够穿刺和/或以其它方式前进通过端口725的类似物。在一些实施方案中,基底771和耦接构件778可以基本上类似于上面详细描述的基底571和/或671以及耦接构件578和/或678。因此,基底771和耦接构件778(和/或其方面或部分)在此不再详细描述。
[0235]
系统700可用于从患者获取一个或多个体积的体液,其可用于一个或多个测试、测定和/或诊断程序。如上所述,例如,入口712可被放置成与体液源流体连通。当入口712与体液源(例如患者的一部分)流体连通时,致动器750可处于第一状态,从而在入口712和隔离室730之间建立流体连通,并将出口713与入口712隔离,如图9a所示。此外,当致动器750处于第一状态时,第一构件751的第一端部可以靠近或邻近入口712的第一侧,第二构件760的第一端部可以靠近或邻近入口712的第二侧。以这种方式,限定在第一构件751和第二构件760之间的隔离室730可以具有第一容积。
[0236]
在一些情况下,一旦入口712被放置成与体液源流体连通,致动器750就可从其第一状态转换成其第二状态。例如,如图9b所示,使用者可在第三构件765上施加力,该力可操作以相对于壳体710移动第三构件765。如上所述,第一构件751的接合构件755和第三构件765的接合结构766的布置使得第三构件765相对于壳体710的运动导致第一构件751的类似运动。第一构件751的移动也是相对于第二构件760的(例如,第二构件760还没有移动),这
又增加了设置在第一构件751和第二构件760之间的隔离室730的容积。此外,第一构件751的转换和/或移动可减少第一构件751的与隔离室730相对的一侧上的壳体710内的体积,并且开口721可使得包含在其中的空气或气体可被允许逸出和/或流出取样通道735。因此,致动器750从其第一状态(图9a)转换成其第二状态(图9b)可导致在隔离室中产生负压差,可操作地从体液源抽取初始体积的体液,通过入口712,并进入隔离室730,如上文参考隔离室630所详细描述的。此外,体液的初始体积可以是任何合适的体液体积,例如上述任何体积或量。
[0237]
当初始体积的体液包含在隔离室730中时,致动器750可以从其第二状态(图9b)转换到其第三状态(图9c)。如上文参考传输装置605所述,致动器750从第二状态到第三状态的转换可响应于安置在隔离室730中的初始体液量、响应于一个或多个压差的均衡、响应于致动器750从第一状态转换到第四状态的连续过程中的给定点等。在一些情况下,转换可以是自动的或者响应于施加的力。
[0238]
如图9c所示,将致动器750转换到第三状态可以包括将第一构件751和第三构件765相对于壳体710和第二构件760转换和/或移动额外的量。更具体地,当处于第三状态时,第一构件751可以相对于第二构件760放置在一个位置,使得开口、端口、阀等(这里称为“开口754”)被放置成与隔离室730和/或入口712流体连通,如图9c所示。以这种方式,一定体积的体液可以被转移到由第一构件751限定的取样通道735中。如上所述,在一些实施方案中,端口725可以被配置成给取样通道735排气,以促进体液流入取样通道735。
[0239]
随着取样通道735中包含一定体积的体液,致动器750可以从其第三状态(图9c)转换到它的第四状态(图9d)。更具体地,在一些实施方案中,第三构件765和第二构件760可以相对于壳体710移动,而第一构件751相对于壳体710保持在基本固定的位置。换句话说,第三构件765和第二构件760一起并且相对于第一构件751移动。
[0240]
如图9d所示,当致动器750转换到第四状态时,接合构件755脱离接合表面766和/或相对于接合表面766移动。在一些实施方案中,接合构件755和/或接合表面766可以被定尺寸和/或配置成保持接触和/或接合,直到施加了足以克服保持接合的力(例如,摩擦力、足以使接合构件755和/或接合表面766弹性和/或塑性变形的力、和/或任何其它合适的力)的期望的和/或预定的力。换句话说,当力满足标准和/或大于力的阈值量时,第三构件765可以相对于第一构件751移动。
[0241]
当致动器750转换到第四状态时,致动器750的第二构件760与第三构件765一起并且在相同的方向上移动。如图9d所示,第二构件760的转移和/或移动将第二构件760的第一端部从入口712的第二侧转移和/或移动到入口712的第一侧,从而隔离和/或流体隔离隔离室730与入口712。此外,第二构件760相对于第一构件751的转移和/或移动可以将第一构件751的开口754放置在第二构件760的第一端部中或第一端部上包括的内部密封件561的相对侧,这在一些情况下可以允许取样通道735排气,如本文进一步详细描述的。
[0242]
如图9d所示,快速测试装置770可以耦接到壳体710和/或可以至少部分地插入和/或穿过壳体710的开口721,以允许耦接构件778建立与取样通道735的流体连通(例如,通过端口725)。因此,至少一部分体液可以从取样通道735转移到快速测试装置770中,如上文参考快速测试装置470、570和/或670详细描述的。在一些实施方案中,将一定体积的体液从取样通道735转移到快速测试装置770中可以启动对该部分初始体积的体液的测试和/或测
定,如上文参考快速测试装置270详细描述的。此外,在一些情况下,经由开口754使取样通道735排气可以允许取样通道735内的期望压差,这可以促进体液从取样通道735转移到快速测试装置770中。快速测试装置770可以被配置成执行任何合适的测试和/或测定(例如,测试乳酸和/或pct的存在),例如上面详细描述的那些中的任何一种。此外,一旦测试或测定完成,快速测试装置770可以被配置成输出测试结果,该测试结果可以由人和/或一个或多个电子设备检测和/或评估,如上面参考快速测试装置170、270、370、470、570和/或670详细描述的。
[0243]
如上所述,将致动器750从其第三状态转换到其第四状态可以将初始体积的体液隔离、分离、分开和/或保留在隔离室730和/或快速测试装置770中,这又可以隔离初始体积的污染物。此外,如上文所详细描述的,快速测试装置770的布置可以使得由快速测试装置770执行的测试和/或测定不容易受到此类污染,这意味着由快速测试装置770输出的测试结果的准确性不受此类污染影响。
[0244]
如图9d所示,将致动器750从其第三状态转换到其第四状态经由设置在致动器750的第二构件760的第一端部和第二端部之间的流体流动路径715在入口712和出口713之间建立了流体连通。当致动器750处于其第四状态时,第二构件760的第一端部设置在入口712的第一侧上,并且第二构件760的第二端部设置在出口713的第二侧上,如上文参照致动器650详细描述的。
[0245]
在一些实施方案中,在致动器750被置于其第四状态之前或之后,出口713可被放置成与流体收集装置流体连通(图8-9d中未显示)。如上文所详细描述的,流体收集装置可以限定负压和/或吸力和/或可被配置成产生负压和/或吸力,所述负压和/或吸力可用于将体液吸入流体收集装置。因此,响应于负压和/或吸力,一个或多个后续体积的体液可从入口712流动,通过流体流动路径715,通过出口713,并进入流体收集装置。如上所述,在收集或获取一个或多个后续体积的体液之前,将初始体积的体液隔离在隔离室730中减少和/或基本上消除了一个或多个后续体积中的污染物的量。因此,系统700可被配置成获取初始体积的体液和后续体积的体液,初始体积的体液可用于对污染具有相对低敏感度的快速测试,后续体积的体液可用于对污染具有相对高敏感度的测试,如上文参考系统100、200、300、400和/或600所述。
[0246]
图10、图11和图12a-12d示出了根据实施方案的流体传输和测定系统800。流体传输和测定系统800(本文中也称为“系统”)可以至少包括流体传输装置805和快速诊断测试装置870。流体传输装置805和/或快速诊断测试装置870的部分和/或方面可以分别与上文详细描述的流体传输装置105、205、305、405、505、605和/或705和/或快速诊断测试装置170(和/或lfa 170a)、270、370、470、570、670和/或770类似和/或基本相同。因此,本文不再进一步详细描述这些部分和/或方面。
[0247]
流体传输装置805(本文中也称为“传输装置”)可具有任何合适的形状、尺寸和/或配置。在一些实施方案中,传输装置805可被配置成从患者抽取体液(例如,血液)并使其进入和/或通过传输装置805。另外,传输装置805可被配置成将至少一些抽取的体液传输到一个或多个其它装置、储器、容器、小瓶、机器、测试、测定等,诸如快速诊断测试装置870和/或一个或多个流体收集装置(未在图10、图11和图12a-12d中显示)。
[0248]
传输装置805至少包括壳体810和致动器850。装置805的壳体810可具有任何合适
的形状、尺寸和/或配置。例如,在一些实施方案中,壳体810可以与上述壳体210、310、410、510、610和/或710中的任何一个类似和/或基本相同。具体地,壳体810具有和/或形成入口812和出口813。壳体810可以形成和/或限定致动器腔室814、流体流动路径815和隔离室830。入口812可以是任何合适的入口或端口,并且可以被配置成在壳体810与体液源(例如,患者)之间建立流体连通。如图11所示,入口812与致动器腔室814流体连通,致动器腔室814又与流体流动路径815和隔离室830流体连通。出口813可以是任何合适的出口或端口,并且可被配置成在壳体810与流体收集装置之间建立流体连通(未在图10-图12d中显示),诸如上文所详细描述的那些中的任一个。出口813与流体流动路径815流体连通。此外,出口813被配置成经由流动控制器840与隔离室830选择性流体连通,如本文中进一步详细描述。
[0249]
隔离室830可被配置成从入口812接收体液流和/或体液量,并隔离(例如,隔离、分开、容纳、保留、隔离等)隔离室830内的体液流和/或体液体积的至少一部分,如本文进一步详细描述的。隔离室830可具有任何合适的形状、尺寸和/或配置。例如,在一些实施方案中,隔离室830和/或其至少一部分可以至少在形式和/或功能上基本类似于上文详细描述的隔离室330、430、630和/或730。因此,本文不再进一步详细描述隔离室830的部分和/或方面。
[0250]
流动控制器840至少部分地设置在壳体810内,并配置成控制、引导和/或以其它方式促进流体选择性地通过壳体810的至少一部分、流体流动路径815的至少一部分和/或隔离室830的至少一部分。流动控制器840可以被配置成便于流体通过壳体810的一个或多个部分的移动,在一些情况下,这可以允许或导致壳体810的一个或多个部分上的压力差和/或压力均衡。在本文中,流体流例如可以是诸如水、油、润湿液、体液和/或任何其它合适的液体的液体,和/或可以是诸如空气、氧气、二氧化碳、氦气、氮气、环氧乙烷和/或任何其它合适的气体的气体。
[0251]
流动控制器840可具有任何合适的形状、尺寸和/或配置。在一些实施方案中,流动控制器840可以与上面参照图4详细描述的流动控制器340类似和/或基本上相同。例如,流动控制器840可以被配置成响应于压差、吸力、与体液的接触和/或体液的流动等从第一状态转换到第二状态。更具体地说,在图如图10-图12d所示的实施方案中,流动控制器840可以是由吸收性或半渗透性材料形成的构件或装置,该构件或装置被配置成当处于第一状态时可渗透气体或空气流而不可渗透液体(例如血液或其它体液)流,并且被配置成当处于第二状态时不可渗透气体和液体。因此,流动控制器840和/或其方面或部分在本文中不再详细描述。
[0252]
装置805的致动器850可具有任何合适的形状、尺寸和/或配置。例如,致动器850可以是被配置成以任何合适的方式(例如,用户致动、自动致动、机械致动、电子致动、化学致动等)在任何数量的状态(例如,两个、三个、四个或更多个)之间转换的任何合适的一个或多个构件或一个或多个装置。在一些实施方案中,致动器850和/或其方面或部分可以与上文所详细描述的致动器150、250、350、450、650和/或750类似和/或基本相同。如图11所示,致动器850形成和/或包括杆,所述杆至少部分可移动地设置在壳体810的致动器室814的一部分中。另外,致动器850包括沿着致动器850(或杆)的长度设置在预定位置的一组密封件852,其可以允许致动器850控制、引导和/或以其它方式促进流体选择性地流过壳体810的至少一部分。如本文所进一步详细描述的,致动器850包括一组四个密封件852,其沿着致动器850(或杆)的长度设置在期望的位置,以选择性地控制流体从入口812流入隔离室830、快
速诊断测试装置870和/或流体流动路径815中的至少一者。此外,当致动器850在两种或更多种状态之间转换时,密封件852的布置还可以允许致动器850隔离隔离室830、快速诊断测试装置870和/或流体流动路径815。
[0253]
虽然包括在前面实施方案中的快速测试装置已被示出和/或描述为耦接到壳体810,但是在图10-图12d所示的实施方案中,快速测试装置870被设置在壳体810内和/或集成到壳体810中。快速诊断测试装置870(本文中也称为“快速测试装置”或简称为“测试装置”)可以是任何合适的测试装置。例如,快速测试装置870和/或其方面或部分可以与上文所详细描述的快速测试装置170、270、370、470、570、670和/或770基本上类似。在一些实施方案中,如上文参照图2所示的lfa 170a所详细描述的,快速测试装置870可以是lfa等。
[0254]
例如,如图11所示,快速测试装置870至少包括设置在基底871端部上的取样元件872、设置在取样元件872下游的基底871上的缀合元件873、设置在缀合元件873下游的基底871上的捕获元件874和设置在捕获元件874下游的基底871上的控制元件875。快速测试装置870可被设置在壳体810内,使得可以通过观察开口819等从壳体810的外部观察捕获元件874和控制元件875。此外,壳体810和/或快速测试装置870包括和/或耦接到包含一定体积的缓冲溶液881的缓冲致动器880。在一些实施方案中,缓冲致动器880可以是泡罩包装、易碎或可刺穿的容器、包括一个或多个可重新配置的部分(例如,一个或多个阀或流动控制器)的储器等。如本文所进一步详细描述的,缓冲致动器880可被致动以向快速测试装置870的取样元件872提供缓冲溶液881,该缓冲溶液881又可与传输到取样元件872的体液体积混合。
[0255]
系统800可用于从患者获取一个或多个体积的体液,其可用于一个或多个测试、测定和/或诊断程序。如上所述,例如,入口812可被放置成与体液源流体连通。当入口812被放置成与体液源(例如,患者的一部分)流体连通时,致动器850可处于第一状态,从而在入口812与隔离室830之间建立流体连通,如图11所示的。更具体地,当致动器850处于第一状态时,入口812和隔离室830可以与致动器850的两个密封件852之间限定的致动器室814的一部分流体连通。例如,设置在致动器850的端部处或附近的第一密封件852(例如,端部密封件)可设置在致动器室814内快速测试装置870与隔离室830之间的位置,并且邻近(或最接近)第一或端部密封件852的第二密封件852可设置在致动器室814内入口812与流体流动路径815之间。以这种方式,当致动器850处于第一状态时,入口812与隔离室830流体连通,如图11所示。
[0256]
在图10-图12d所示的实施方案中,一旦入口812被放置成与体液源(例如,患者的一部分)流体连通,出口813就可以流体耦合到流体收集装置,诸如本文所述的那些中的任一个。例如,流体收集装置可以是被配置成接收一定体积的体液的任何合适的储器、容器和/或装置。在一些实施方案中,流体收集装置可以是限定负压的真空储器或容器,和/或可以是可被操纵以产生负压的注射器。这样,将流体收集装置耦接到出口813选择性地将流体流动路径815的至少一部分暴露于流体收集装置内的负压和/或吸力。
[0257]
致动器850被配置成当流体收集装置与出口813流体耦合时处于第一状态。如图12a所示,流体流动路径815与致动器室814的一部分流体连通,所述部分被限定在设置在入口812与流体流动路径815之间的密封件852(例如,从底部数第二个)与设置在流体流动路径815的相对侧上的相邻密封件852(例如,从底部数第三个)之间。以这种方式,流体流动路
径815将出口813放置成与致动器腔室814的一部分流体连通,所述致动器腔室814的部分被设置在流体流动路径815的任一侧的密封件852隔离和/或流体分离。如上所述,出口813和/或流体流动路径815也与流动控制器840流体连通,当流体收集装置耦接到出口813时,流动控制器840可以处于其第一状态。
[0258]
流动控制器840(例如,可选择性渗透的构件)的布置可以使得空气或气体流被允许通过出口813(和/或流体流动路径815)与隔离室830之间的流动控制器840,而液体流(例如,体液)不被允许通过流动控制器840。结果,由流体收集装置产生的负压差或吸力的至少一部分可被转移到隔离室830中和/或通过隔离室830,这又可以用于从体液源抽吸初始体积的体液、通过入口812、限定在两个相应的密封件852之间的致动器室814的一部分,并且进入隔离室830中,如以上参照转移装置305详细描述的。
[0259]
体液的初始体积可以是任何合适的体液体积,诸如上述的任何体积或量。例如,在一些情况下,致动器850和/或传输装置805可保持在第一状态或配置,直至预定和/或所需体积(例如,初始体积)的体液被传输到隔离室830。在一些实施方案中,初始体积可与隔离室830或其部分的体积相关联和/或至少部分基于该体积(例如,足以填充隔离室830或隔离室830的所需部分的体积)。在一些实施方案中,传送装置805可被配置成将体液流(例如,初始体积)传送到隔离室830中,直至流动控制器840转变成其第二配置。换句话说,在一些实施方案中,将初始体积的体液传送到隔离室830中可用于将流动控制器840置于其第二状态或配置。例如,将初始体积的体液转移到隔离室830中可以使得初始体积的至少一部分润湿和/或浸透流动控制器840,这进而将流动控制器840置于其第二状态,如上文参照流动控制器340所详细描述的。如图12a和图12b所示,体液的初始体积可足以基本填充隔离室830,使得初始体积的至少一部分被设置在两个密封件852(例如,两个最低密封件852)之间的致动器室814内。
[0260]
当流动控制器840转换成其第二状态和/或配置时,流动控制器840将隔离室830与出口813隔离和/或流体分离。这样,由流体收集装置产生的负压和/或吸力不再作用于隔离室830或通过隔离室830。在一些情况下,这可以允许隔离室830与入口812之间的压差基本上相等和/或降低到所需阈值以下。在一些情况下,压力均等可以使得体液停止流入隔离室830。
[0261]
在初始体积的体液包含在隔离室830中之后,致动器850可以从其第一状态(图11和图12a)转换成其第二状态(图12b和图12c),由此将传输装置805从其第一状态转换成其第二状态。如上文参考传输装置605所述,致动器850从第一状态到第二状态的转换可响应于被置于隔离室830中的初始体液量、响应于一个或多个压差的均等等。在一些情况下,转换可以是自动的或者响应于施加的力(例如,如图12b中箭头所示)。
[0262]
如图12b所示,当处于第二状态或配置时,致动器850可被设置在致动器室814内,使得密封件852相对于快速测试装置870、隔离室830、入口812和流体流动路径815处于所需位置。例如,隔离室830与致动器室814的一部分流体连通,所述部分设置在密封件852(其位于快速测试装置870与隔离室830之间)与密封件852(其位于隔离室830与入口812之间)之间。这样,当流动控制器840处于其第二状态且致动器850转换成其第二状态时,隔离室830与传输装置805的其它部分隔离和/或流体分离(参见例如图12b-图12d)。换句话说,致动器850(和流动控制器840)可将隔离室830与入口812、出口813、流体流动路径815和快速测试
装置870隔离和/或分离。在一些情况下,将初始体积的体液隔离在隔离室830中也可以隔离初始体积中的污染物。
[0263]
如图12c所示,当处于第二状态或配置时,致动器850还经由流体流动路径815和致动器室814的一部分在入口812与出口813之间建立流体连通。例如,在一些实施方案中,入口812和流体流动路径815各自与致动器室814的设置在相应的一对密封件852(例如,顶部一对密封件852)之间的部分流体连通。因此,响应于由流体收集装置产生的负压和/或吸力,一个或多个后续体积的体液可从入口812流动,通过致动器腔室814的一部分和流体流动路径815,通过出口813,并进入流体收集装置(未显示)。如上所述,在收集或获取一个或多个后续体积的体液之前,将初始体积的体液隔离在隔离室830中减少和/或基本上消除了一个或多个后续体积中的污染物的量。
[0264]
如图12c所示,当致动器850处于第二状态或配置时,快速测试装置870与致动器腔室814的设置在相应的一对密封件852(例如,端部对)之间的部分流体连通,这可以允许设置在该对密封件852之间的致动器腔室814内的一部分初始体积的体液传送到快速测试装置870的取样元件872内或之上。如图12d所示,通过操纵和/或接合缓冲致动器880以将缓冲致动器880从其第一状态转换成其第二状态,可将传输装置805从其第二状态转换成第三状态,以将其中包含的缓冲溶液881的至少一部分传输到取样元件872中或其上。例如,缓冲致动器880可以包括易碎部分,所述易碎部分可以响应于用户施加在缓冲致动器880上的力而破裂和/或刺穿。如图12d所示,快速测试装置870和/或壳体810可包括穿刺构件882等,其可被配置成破裂、刺穿和/或以其它方式打开缓冲溶液。在此类实施方案中,穿刺构件882可以限定能够与取样元件872流体连通的管腔。因此,施加在缓冲致动器880上的力可用于将至少一部分缓冲溶液881转移到取样元件872中和/或取样元件872上。此外,随着大量体液也被传输到取样元件872,体液和缓冲溶液881可以开始混合。
[0265]
在一些实施方案中,体液与缓冲溶液881在取样元件872之中或之上的的混合可以启动体液的测试和/或测定或对体液的测试和/或测定,如上文参考快速测试装置270所详细描述的。此外,快速测试装置870可被配置成执行任何合适的测试和/或测定。在一些实施方案中,缓冲溶液881可以至少部分基于正在进行的测试。例如,在一些情况下,如上面详细描述的,快速测试装置870可被配置成测试乳酸和/或pct的存在。此外,一旦测试或测定完成,快速测试装置870就可被配置成输出可被检测和/或评估的测试结果。例如,在一些情况下,人可以通过由壳体810限定的观察开口819观察捕获元件874和/或控制元件875。在其它实施方案中,电子设备可以经由观察开口819执行捕获元件874和/或控制元件875的一次或多次扫描。在其它实施方案中,一个或多个电子设备可以集成和/或设置在壳体810中,并且捕获元件874和/或控制元件875不需要由人观察。
[0266]
如上文所详细描述的,在一些实施方案中,快速测试装置870的布置可以使得由快速测试装置870执行的测试和/或测定不容易受到这种污染,这意味着由快速测试装置870输出的测试结果的准确性不受初始体积的体液体积中可能包含的污染的影响,如上文所详细描述的。因此,系统800可被配置成获取初始体积的体液和一个或多个后续体积的体液,所述初始体积的体液可用于对污染具有相对低的敏感度的快速测试,所述后续体积的体液可用于对污染具有相对高的敏感度的测试,如上文参考系统100、200、300、400、600和/或700所描述的。
[0267]
图13至图16示出了根据实施方案的至少一部分的流体传送和测定系统900。流体传送和测定系统900(本文中也称为“系统”)可以至少包括流体传送装置905和快速诊断测试装置970。系统900的部分和/或方面可以与上面详细描述的系统(或装置)100、200、300、400、500、600、700和/或800相似和/或基本相同。因此,本文不再进一步详细描述这些部分和/或方面。
[0268]
流体传送装置905(本文中也称为“传送装置”)可具有任何合适的形状、尺寸和/或构型。在一些实施方案中,传送装置905可被配置成从患者抽取体液(例如,血液)并将其送入和/或通过传送装置905。另外,传送装置905可被配置成将至少一些抽取的体液传送到一个或多个其它装置、储器、容器、小瓶、机器、测试、测定等,诸如快速诊断测试装置970和/或一个或多个流体收集装置(未在图13-16中显示)。在一些实施方案中,传输装置905和/或其方面或部分可与于上文所详细描述的传输装置105、205、305、405、505、605、705和/或805中的任一种基本上类似。
[0269]
例如,传输装置905至少包括壳体910和致动器950。壳体910具有和/或形成入口912和出口913。入口912可以是任何合适的入口或端口,并且可以被配置成在壳体910与体液源(例如,患者)之间建立流体连通。出口913可以是任何合适的出口或端口,并且可被配置成在壳体910与流体收集装置之间建立流体连通(未在图13-图16中显示),诸如上文所详细描述的那些中的任一个。另外,壳体910包括和/或限定端口925,其可被配置成在壳体910的至少一部分和/或设置在其中的一个或多个储器或室与例如快速诊断测试装置970之间建立流体连通。在一些实施方案中,端口925可以至少在形式和/或功能上与上文参考图6a-图6d所描述的端口525基本上类似。以这种方式,壳体910和/或其部分或方面可以与上述壳体210、310、410、510、610、710和/或810中的任何一个类似和/或基本相同,因此在本文中不再详细描述。
[0270]
致动器950至少部分设置在壳体910内。装置905的致动器950可具有任何合适的形状、尺寸和/或配置。例如,致动器950可以是被配置成在两种或更多种状态之间转换以控制、引导和/或以其它方式促进流体通过壳体910的至少一部分的选择性流动的构件或装置。此外,可以以任何合适的方式使致动器950致动和/或使其在任何数量的状态之间转换。在图13-图16所示的实施方案中,致动器950可以在至少第一状态与第二状态之间转换。当处于第一状态时,致动器950可被配置成允许初始体积的体液从入口912进入壳体910的初始或第一部分,诸如上文参考隔离室330、430、630、730和/或830所详细描述的隔离室等。在一些实施方案中,当处于第一状态时,致动器950可被配置成隔离、分离、分开和/或以其它方式防止出口913与入口912之间,和/或出口913与壳体910的初始或第一部分之间的流体连通。当处于第二状态时,致动器950可被配置成允许后续体积的体液(例如,初始体积的体液之后的一定体积的体液)从入口912通过壳体910的至少一部分(例如,第二部分)传输到出口913(和/或流体耦接到出口913的流体收集装置)。此外,当处于第二状态时,致动器950可被配置成隔离、分离、分开和/或以其它方式防止壳体910的初始或第一部分与入口912、出口913和/或壳体910的一个或多个其它部分之间的流体连通。以这种方式,致动器950和/或其部分或方面可以与上文详细描述的致动器250、350、450、650、750和/或850中的任一种基本上类似,因此在本文中不再详细描述。
[0271]
快速诊断测试装置970(本文中也称为“快速测试装置”或简称为“测试装置”)可以
是任何合适的测试装置。例如,测试装置970和/或其方面或部分可以与上文详细描述的快速测试装置170、270、370、470、570、670、770和/或870基本上类似。在一些实施方案中,快速测试装置970可以是lfa等,如上文参考图2所示的lfa 170a所详细描述的。例如,快速测试装置970至少包括置于基底971端部的取样元件972、置于取样元件972下游的基底971上的缀合元件973、置于缀合元件973下游的基底971上的捕获元件974和置于捕获元件974下游的基底971上的控制元件975。
[0272]
快速测试装置970还包括壳体983和测试装置致动器986,所述壳体983被配置成包含和/或容纳快速测试装置970的至少一部分,所述测试装置致动器986被配置成选择性地建立快速测试装置970与壳体910之间的流体连通。在一些实施方案中,快速测试装置970可被配置成基本上模块化的装置,其可以耦至到和/或附接到任何合适的流体传输装置、管道、储器、机构、传输适配器等。在一些实施方案中,测试装置970的模块化布置可以允许传输装置905和测试装置970独立制造和/或运输,并且在使用点耦接和/或组装。在一些实施方案中,测试设备970的模块化布置可以允许测试装置970的各种形式与传输装置905兼容,其中测试装置970的每个形式被配置成执行不同的测试或测定。换句话说,测试装置970的模块化布置可以允许测试装置970的不同形式测试不同的生物标志物,同时保持基本相同的形状因子和/或兼容性。
[0273]
如图14-图16所示,壳体983可具有任何合适的形状、尺寸和/或配置。在一些实施方案中,测试装置970的壳体983可被配置成耦接到传输装置905的壳体910的一部分。壳体983包括、容纳和/或限定排气口985,排气口985被配置成允许空气或气体流出壳体983。如上文参考传输装置所详细描述的,在一些实施方案中,对测试装置970的壳体983进行排气可以促进流体流过测试装置970(例如,沿着基底971)。另外,壳体983包括和/或限定了观察开口984。如图14和图15所示,测试装置970可设置在壳体983内,使得至少捕获元件974和/或控制元件975通过观察开口984可见和/或可检测。
[0274]
测试装置致动器986可移动地耦接到测试装置970的壳体983,并且被配置成在第一状态与第二状态之间转换,以在传输装置905与测试装置905之间建立流体连通。例如,在一些实施方案中,测试装置致动器986可以是弹簧加载按钮等,其可以包括穿刺构件987。测试装置970和/或测试装置970的壳体983可以包括膈膜988和/或可以形成膈膜988。另外,测试装置致动器986可以与膈膜988对齐。在一些实施方案中,测试装置致动器986可被配置成使得当测试装置致动器986处于第一状态时,穿刺构件987被设置在膈膜988的第一侧上并且在测定装置970的壳体983内(参见例如,图15),以及当测试装置致动器986处于第二状态时,穿刺构件987延长通过膈膜988并且在测试装置970的壳体983外部(未在图13-图16中显示)。
[0275]
测试装置970和/或其壳体983被配置成耦接到传输装置905的壳体910,使得测试装置致动器986与壳体910中包括的和/或由壳体910形成的端口925基本对齐。这样,当测试装置致动器986转换成其第二状态时,穿刺构件987可以延伸通过测试装置970的隔膜988并通过传输装置905的端口925,以在其间建立流体连通。以这种方式,穿刺构件987可以接收设置在传输装置905中的初始体液体积的至少一部分(例如,通过毛细作用、压力差和/或任何其它流体传输形式)。如图15所示,穿刺构件987与基底971的一部分,例如取样元件972流体连通。因此,体液流可以从传输装置905的一部分(例如,壳体的一部分、隔离室等)传输到
取样元件972。
[0276]
尽管图13-图16中未显示,但在一些实施方案中,测试装置970可被配置成将缓冲溶液等连同体液体积一起输送到取样元件972(例如,如上文参考测试装置870所描述的)。在此类实施方案中,缓冲溶液可以与体液体积混合,并且混合物可以沿着基底971流动用于测试,如上文所详细描述的。在一些实施方案中,快速测试装置970可被配置成测试乳酸和/或pct的存在,乳酸和/或pct的存在可以指示诸如败血症等患者状况。此外,一旦测试或测定完成,快速测试装置970就可被配置成输出可被检测和/或评估的测试结果。例如,在一些情况下,人可以通过由测试装置970的壳体983限定的观察开口984观察捕获元件974和/或控制元件975。在其它实施方案中,电子设备可以经由观察开口984执行捕获元件974和/或控制元件975的一次或多次扫描。在其它实施方案中,一个或多个电子设备可以集成和/或设置在壳体910中,并且捕获元件974和/或控制元件975不需要由人观察。
[0277]
除了将一定体积的体液输送到快速测试装置970之外,在一些情况下,传输装置905还可被配置成将一个或多个后续体积的体液传输到耦接到出口913的任何合适的装置、储器、测试装置等。因此,系统900可被配置成获取可用于快速测试(例如,对污染具有相对较低的敏感性的测试)的初始体积的体液和可用于后续测试(例如,对污染具有相对较高的敏感性的测试)的一个或多个后续体积的体液,如上文参考系统100、200、300、400、600、700和/或800所描述的。
[0278]
图17-图20示出了根据不同实施方案的流体传输和测定系统和/或装置的各种实例。例如,图17示出了流体传输和测定系统1000(本文中也称为“系统”)。系统1000可以在形式和/或功能上与上文参考图13-图16描述的系统900基本上类似。虽然传输装置905的端口925在图14显示为被设置在壳体910的端部处或其附近,但在图17所示的实施方案中,包括在系统1000中的传输装置可包括和/或形成在其入口附近或邻近处设置的端口。以这种方式,通过耦接到系统1000的传送装置的快速测试装置的体液流可以相对于通过例如上文参考图13-图17所描述的快速测试装置970的体液流处于基本相反的方向。
[0279]
图18示出了流体传输和测定系统1100(本文中也称为“系统”)。在该实施方案中,系统1100包括“在线”快速诊断测试装置。例如,在一些实施方案中,系统1100可包括在线快速诊断测试装置,该装置被包括在系统1100的入口管道、出口管道和/或任何其它合适的部分中和/或耦接到所述管道和/或部分。在一些实施方案中,包括在系统中的在线快速测试装置可以接收体液流,并且可进行如上文所详细描述的测试或测定。此外,在一些情况下,在线快速测试装置可包括一个或多个流通或旁路机构等(例如,自动或手动致动机构),所述机构可以在其接收初始体积的体液后允许体液流过在线快速测试装置。因此,在线快速测试装置可对初始体积的体液进行一个或多个测试或测定,同时后续体积的体液继续流过系统1100。
[0280]
图19示出了流体传输和测定系统1200(本文中也称为“系统”)。在该实施方案中,系统1200包括被配置为注射器的流体传输装置。在一些实施方案中,注射器可以是例如被配置成抽取一定体积的体液的标准注射器。在其它实施方案中,注射器可以是例如被配置成在抽取“取样体积”的体液之前抽取和隔离初始体积的体液的注射器。例如,这种注射器可与上文通过引用并入的’495专利和/或’006公布中描述的那些的任一种类似和/或基本上相同。如图19所示,系统1200可包括快速诊断测试装置,所述装置可以耦接到注射器的任
何合适的部分,以被放置成与其内部容积流体连通。在注射器被配置成抽取和隔离初始体积的体液的实施方案中,快速测试装置可以耦接到注射器,使得在注射器的隔离部分与快速测试装置之间建立流体连通。以这种方式,系统1200可以至少与上文详细描述的系统300、400、600、700和/或800类似。
[0281]
图20示出了流体传送和测定系统1300(本文中也称为“系统”)。在该实施方案中,系统1300包括流体耦接到例如注射器的流体传输装置。如上文至少参考系统200、300和800所描述的,系统1300可包括流体传输装置,所述流体传输装置被配置成将初始体积的体液抽取到隔离室中,并被配置成响应于例如由流体收集装置等产生的负压差而抽取后续体积的体液。虽然一些实施方案在本文中被描述为耦接到抽成真空的容器(例如,等),但是图20所示的实施方案被配置成耦接到可被操作以产生负压差的注射器。此外,图20所示的流体传输装置被配置成耦接到快速测试装置,诸如本文中描述的任何快速测试装置。以这种方式,系统1300可以至少在形式和/或功能上与本文所详细描述的任何系统类似。
[0282]
虽然上文已经描述了各种实施方案,但是应该理解,它们仅仅是通过实例的方式呈现的,而不是限制性的。例如,虽然一些实施方案在本文中被描述为用于为一个或多个测定、测试等获取体液,但是应当理解,实施方案不限于这种用途。本文所述的任何实施方案和/或方法可用于将体液流传输至与其流体连通的任何合适的装置。因此,尽管本文描述了具体实例,但是装置、方法和/或概念并不旨在限于此类具体实例。
[0283]
虽然已经具体示出和描述了实施方案,但是应当理解,可以进行形式和细节上的各种改变。在示意图和/或实施方案指示以特定取向或位置布置的特定组件的情况下,可以修改组件的布置。尽管各种实施方案已经被描述为具有特定的特征、概念和/或组件的组合,但是具有来自本文描述的任何实施方案的任何特征、概念和/或组件的任何组合或子组合的其它实施方案是可能的。
[0284]
各种组件的具体配置也可以变化。例如,各种部件的尺寸和具体形状可以不同于所示的实施方案,同时仍然提供本文所述的功能。在一些实施方案中,改变这些组件的尺寸和/或形状可以减小装置的整体尺寸和/或可以增加装置的工效学,而不改变装置的功能。在一些实施方案中,各种部件的尺寸和/或形状可以根据期望或预期的用途来具体选择。例如,在一些实施方案中,被配置成与看似健康的成年患者一起使用或在看似健康的成年患者身上使用的装置可以被配置成获取第一量的体液,而被配置成与例如重病患者和/或儿科患者一起使用或在例如重病患者和/或儿科患者身上使用的装置可以被配置成获取小于第一量的第二量的体液。因此,应该理解的是,除非上下文中另有明确说明,否则实施方案和/或其部件的尺寸、形状和/或布置可以适用于给定的用途。
[0285]
本文描述的实施方案和/或其部分可以包括由一个或多个部件、特征、结构等形成的组件。当提到此类组件时,应该理解,所述组件可以由具有任意数量的区段、区域、部分和/或特征的单个部件形成,或者可以由多个部件或特征形成。例如,当提到诸如壁或室的结构时,所述结构可被认为是具有多个部分的单个结构,或者被认为是耦接以形成该结构的多个不同的子结构等。因此,整体构建的结构可以包括例如一组子结构。这样一组子结构可以包括彼此连续或不连续的多个部分。一组子结构也可以由单独生产并随后连接在一起(例如,通过焊接、粘合剂或任何合适的方法)的多个项目或部件制成。
[0286]
本文描述的任何实施方案可以与任何合适的诊断测试装置或机器、快速诊断测试装置、测定装置(例如,侧向流动测定装置)等结合使用。本文所述的任何实施方案可包括任何合适的流体传输装置、流体收集装置和/或流体储存装置和/或可与其结合使用,所述流体储存装置是例如样品储器、器皿、容器、瓶子、适配器、皿、小瓶、注射器和/或装置(包括例如其微米和/或纳米构型)。此外,本文描述的任何实施方案可以包含任何合适的流体传输装置、转移适配器和/或其组件(诸如在
‘
420专利、
‘
783专利、
‘
244申请、
‘
510公布、
‘
117公布、
‘
241专利、
‘
724专利、
‘
495专利、
‘
006公布、
‘
999申请、
‘
074公布、
‘
380申请和/或
‘
477申请(它们的公开内容通过引用以其整体并入本文)中描述的任何装置和/或组件),可以包括所述流体传输装置、转移适配器和/或其组件和/或可以与所述流体传输装置、转移适配器和/或其组件结合使用。
[0287]
虽然上述一些实施方案包括物理地和/或机械地隔离流体传输装置的一个或多个部分的流动控制器和/或致动器,但是在其它实施方案中,流体传输装置不需要物理地和/或机械地隔离流体传输装置的一个或多个部分。例如,在一些实施方案中,致动器(诸如本文所述的任一种致动器)可从第一状态转换成第二状态,在第一状态下,初始体积的体液可从入口流到隔离室或隔离部分,在第二状态下,(1)隔离室或隔离部分被物理和/或机械隔离,以及(2)入口与流体传输装置的出口流体连通。然而,在其它实施方案中,流体传输装置的致动器和/或任何其它合适的部分可从第一状态转换成第二状态,在第一状态下,初始体积的体液可从入口流到隔离室或隔离部分,在第二状态下,入口被放置成与出口流体连通,而不是物理地和/或机械地隔离(或分离)隔离室或隔离部分。当这种传输装置处于第二状态时,该传输装置的一个或多个特征和/或几何形状可导致体液优先从入口流向出口,并且初始体积的体液可以保留在隔离室或隔离部分中,而不会被物理地和/或机械地隔离或分离。
[0288]
尽管未显示,本文所述的任何装置可包括与隔离室流体连通的开口、端口、耦合器、膈膜、luer-lok、垫圈、阀、螺纹连接器、标准流体接口等(为简单起见称为“端口”)。在一些此类实施方案中,端口可被配置成耦接和/或接受任何合适的装置、储器、压力源、测试装置等。例如,在一些实施方案中,端口可被配置成耦接到本文描述的任何快速诊断测试装置。在一些实施方案中,端口可以耦接到负压源,诸如抽成真空的容器、泵、注射器等,以将一部分或全部体积的体液收集在隔离室、通道、储器等中,并且可以将该体液体积(例如,取样前体积)用于其它临床和/或体外诊断测试目的。在一些实施方案中,隔离室可被配置成添加有集成到该室中的快速诊断测试组件(例如,本文所述的任何快速诊断测试装置),从而允许初始体积的体液的至少一部分用于该测试。在其它些实施方案中,隔离室和/或耦接到隔离室或形成隔离室的一部分的快速测试装置可被设计、定制尺寸和配置成可移除并与测试设备兼容,和/或可专门用于通常对疑似病症患者进行的其它类型的体液测试(例如,本文所述的快速诊断测试装置被配置成测试败血症等)。在一些实施方案中,端口(等)可与任何合适的压力源或输注装置耦接,所述压力源或输注装置被配置成将隔离在隔离室中的初始体积的体液的至少一部分输注回患者和/或体液源(例如,在儿科患者、重病患者、低血容量患者等的情况下)。
[0289]
虽然本文描述的一些实施方案包括快速诊断测试装置(所述快速诊断测试装置耦接到或插入到流体传输装置的一部分中,以接收用于测试的一定体积的体液),但是在其它
实施方案中,快速诊断测试装置可被集成到传送装置的一个或多个部分中。例如,本文描述的任何实施方案可以包括集成的传输和测定装置,诸如上文参考系统800所描述的一个或多个装置。尽管快速测试装置870被显示为设置或容纳在壳体810内,但是在其它实施方案中,快速测试装置可以形成流体传输装置的外部和/或可以至少暂时耦接到流体传输装置的外部。
[0290]
尽管未显示,但在一些实施方案中,流体传输装置可以包括一个或多个管腔、通道、流动路径等,被配置成选择性地允许体液的“旁路(bypass)”流动,其中初始量或体积的体液可以从入口流过管腔、通道、流动路径等,以绕过隔离室(或快速测试装置),并进入收集装置。在一些实施方案中,流体传输装置可包括致动器,所述致动器具有例如至少三种状态-第一状态,其中体液可从入口流入隔离室(或快速测试装置);第二状态,其中在初始体积被隔离在隔离室中之后,体液可从入口流入出口;第三状态,其中体液可从入口通过旁路流动路径流入出口。在其它实施方案中,如上文参考具体实施方案所详细描述的,传输装置可包括被配置成在第一与第二状态之间转换装置的第一致动器,并且可以包括被配置成将装置转换成旁路配置等的第二致动器。在其它实施方案中,传输装置可包括被配置成选择性地将流体传输装置置于旁路配置或状态的任何合适的装置、特征、组件、机构、致动器、控制器等。
[0291]
虽然一些方法在本文中被描述为包括以特定顺序叙述的步骤,但是在其它实施方案中,在本文中描述的任何方法或过程中的某些事件和/或过程的顺序可以被修改,并且这种修改符合本发明的变型。另外,当可能时,某些事件和/或过程可以在并行过程中同时执行,以及如上所述顺序执行。在进行后续步骤之前,某些步骤可被部分完成或者可被省略。
[0292]
例如,虽然一些装置在本文中被描述为在离散操作等中从第一状态转换成第二状态,但是应当理解,本文中描述的装置可以被配置成自动和/或被动地从第一状态转换成第二状态,并且这种转换可以在一段时间内发生。换句话说,在一些情况下,从第一状态到第二状态的转换可以是相对渐进的。例如,在一些情况下,当初始体积的体液的最后部分被传输到装置(例如,其初始或隔离部分)中时,该装置可以开始从第一状态转换成第二状态。在一些情况下,可以选择性地控制从第一状态转换成第二状态时的变化率,以实现与转换相关联的一个或多个所需特性。此外,在一些此类情况下,初始体积的最后部分的流入可以限制和/或基本上防止已经布置在初始或隔离部分中的体液从中逸出。因此,虽然从第一状态到第二状态的转换可以在给定的时间内发生,但是装置的初始部分或隔离部分仍然可以隔离设置在其中的初始体积的体液。
[0293]
本文所述的一些实施方案和/或方法包括一种或多种电子装置,其被配置成执行本文所述的流体传输和/或快速诊断测试系统和方法中包括的和/或与之相关联的一个或多个过程。本文所述的一种或多种电子设备(例如,电子设备190)可以是被配置成接收、处理、定义和/或存储数据的任何合适的基于硬件的计算设备,所述数据是例如一个或多个诊断测试结果、测量结果数据所依据的测试标准、预定和/或预定义的治疗计划、患者概况、疾病概况等。在一些情况下,一种或多种电子设备可以接收与诊断测试、测定等(例如,快速测试装置170)相关联的数据,并且可被配置成分析、处理和/或以其它方式使用数据来产生与测试相关联的一个或多个定性和/或定量测试结果。在一些情况下,这种测试可以是对例如败血症和/或任何其它疾病状况的测试。
[0294]
下面提供了电子设备和/或其组件的实例。虽然描述了某些设备和/或组件,但是应当理解,它们仅仅是作为实例而非限制来呈现的。可以使用具有能够执行本文描述的过程、程序和/或方法的任何其它合适的组件的任何其它合适的电子设备。
[0295]
本文描述的一种或多种电子设备可以是例如移动电子设备(例如,智能手机、平板电脑、膝上型电脑和/或任何其它移动或可穿戴设备)、pc、工作站、服务器设备或服务器设备的分布式网络、虚拟服务器或机器、虚拟专用服务器和/或作为物理服务器或服务器组上的实例或客户机执行和/或运行的类似设备,和/或任何其它合适的设备。在一些实施方案中,一种或多种电子设备可以被配置成提供由本文描述的任何快速测试装置产生的测试结果的图形和/或数字表示。此外,在一些实施方案中,基于与测试结果相关联和/或代表测试结果的数据,一种或多种电子设备可被配置成确定并以图形或数字方式呈现一个或多个诊断、一个或多个治疗计划、一个或多个模拟和/或与体液样品、患者和/或患者的医学治疗相关联的任何其它合适的数据。
[0296]
一种或多种电子设备的组件可以包含在单个壳体或机器内,或者可以分布在多个物理机器、虚拟机和/或其任意组合内和/或之间。在一些实施方案中,一种或多种电子设备可以在云计算环境中存储、运行、执行和/或以其它方式实现。在一些实施方案中,一种或多种电子设备可以包括客户端或移动设备(例如,智能手机、平板电脑、可穿戴设备等)和服务器或一个或多个主机设备和/或可由所述设备共同形成,它们可以经由一个或多个网络进行通信。此外,一种或多种电子设备和/或其任何组件可被包括、容纳和/或集成在本文所述的任何流体传输装置和/或快速诊断测试装置或其任意合适的组合中。
[0297]
本文描述的实施方案中包括的一种或多种电子设备可以至少包括存储器、处理器和通信接口。存储器、处理器和通信接口可被连接和/或电耦合(例如,经由系统总线等),使得电信号和/或电子信号可以在存储器、处理器和通信接口之间发送。一种或多种电子设备还可包括数据库和/或一种或多种用户接口或输入/输出(i/o)设备和/或可以以其它方式可操作地耦合到所述数据库和/或用户接口或输入/输出设备,如本文所进一步详细描述的。
[0298]
在一些实施方案中,存储器可以是例如随机存取存储器(ram)、存储缓冲器、硬盘驱动器、只读存储器(rom)、可擦除可编程只读存储器(eprom)、电可擦除可编程只读存储器(eeprom)、闪存等或其合适的组合。在一些实施方案中,存储器可以物理地容纳和/或包含在一种或多种电子设备中或者可由一种或多种电子设备容纳和/或包含,或者可以可操作地耦接到一种或多种电子设备和/或至少其处理器。在此类实施方案中,存储器可以例如被包括在和/或分布在一种或多种设备中,所述设备是例如服务器设备、基于云的计算设备、网络计算设备等。存储器可被配置成存储例如一个或多个软件模块和/或代码,其可包括可使处理器执行一个或多个过程、功能等(例如,与存储、分析和/或呈现与本文所述的流体传输和/或快速诊断测试系统和方法相关联的数据相关联的过程、功能等)的指令。
[0299]
存储器和/或其至少一部分可以包括一个或多个数据存储结构(例如一个或多个数据库等)和/或可以与一个或多个所述数据存储结构通信。数据库可以是任何合适的一个或多个数据存储结构,例如表格、储存库、关系数据库、面向对象的数据库、对象关系数据库、结构化查询语言(sql)数据库、可扩展标记语言(xml)数据库等。在一些实施方案中,数据库可被设置在壳体、机架和/或至少包括存储器、处理器和/或通信接口的其它物理结构
中。在其它实施方案中,一种或多种电子设备可以包括任何数量的数据库和/或可以可操作地耦合到任何数量的数据库。在一些实施方案中,数据库可被配置成存储与本文所述的流体传送和/或快速诊断测试系统和方法相关联的数据。
[0300]
在一些实施方案中,处理器可以是基于硬件的集成电路(ic)和/或被配置成运行或执行存储在例如存储器中的一组指令和/或代码的任何其它合适的处理设备。例如,处理器可以是通用处理器、中央处理单元(cpu)、加速处理单元(apu)、专用集成电路(asic)、网络处理器、前端处理器、现场可编程门阵列(fpga)、可编程逻辑阵列(pla)等。处理器可以经由任何合适的互连、系统总线、电路等与存储器(以及电子设备的任何其它组件)通信。处理器可包括任意数量的引擎、处理单元、内核等,所述引擎、处理单元、内核等被配置成执行与本文所述的流体传输和/或快速诊断测试系统和方法相关联的代码、指令、模块、过程和/或功能。
[0301]
在一些实施方案中,通信接口可以是与处理器和存储器和/或存储在存储器中并由处理器执行的任何合适的软件通信的任何合适的基于硬件的装置。在一些实施方案中,通信接口可被配置成与网络和/或与网络通信的任何合适的设备通信。通信接口可以包括一种或多种有线和/或无线接口,例如网络接口卡(nic)、通用串行总线(usb)卡和/或任何其它合适的通信和/或外围卡或设备。例如,在一些实施方案中,nic可包括例如一个或多个以太网接口、光载波(oc)接口、异步传输模式(atm)接口、一个或多个无线电(例如,无线电、无线电、近场通信(nfc)无线电等)等。在一些实施方案中,通信接口可被配置成向包括在本文描述的流体传输和/或测定装置和/或系统中的任何合适的部分或设备、一种或多种外围组件(例如,读取器、扫描仪、照相机、分析器、检测器、i/o设备等)、用户或客户端设备(例如,智能手机、平板电脑、可穿戴电子设备、pc等)等发送数据和/或从其接收数据(例如,经由一个或多个网络)。
[0302]
在一些实施方案中,网络可以是任何类型的网络,例如局域网(lan)、无线局域网(wlan)、诸如虚拟局域网(vlan)等的虚拟网络、广域网(wan)、城域网(man)、微波接入全球互通网络(wimax)、电话网络(诸如公共交换电话网(pstn)和/或公共陆地移动网(plmn))、内联网、因特网、基于光纤(或光纤)的网络、蜂窝网络和/或任何其它合适的网络。此外,可将网络和/或其一个或多个部分实现为有线和/或无线网络。例如,网络可以包括一个或多个任何类型的网络,例如有线或无线lan和因特网。在一些实现中,网络可以是连接的和/或以其它方式置于通信中(经由有线或无线连接(例如,usb连接、以太网连接、wifi网络、蓝牙网络、nfc网络等))的的装置的任何合适组合。
[0303]
在一些实施方案中,用户界面可以是显示器或屏幕,例如阴极射线管(crt)监视器、液晶显示器(lcd)监视器、发光二极管(led)监视器等。在一些情况下,显示器可以是触敏显示器等(例如,智能手机、平板电脑、可穿戴设备、pc等的触敏显示器)。在一些情况下,显示器可为软件应用(例如,移动应用、pc应用、互联网web浏览器等)提供用户界面,其可以允许用户操作一种或多种电子设备。在一些实施方案中,用户界面可以包括任何合适类型的人机界面设备、人-计算机界面设备、批处理界面、图形用户界面(gui)等。在一些实施方案中,用户界面可以是任何其它合适的用户界面和/或一种或多种输入/输出(i/o)设备,例如全息显示器、诸如隐形眼镜显示器、光学头戴式显示器、虚拟现实显示器、增强现实显示器等可穿戴设备、鼠标、键盘等或其组合。因此,本文描述的一种或多种电子设备可以接收、
处理、定义和/或存储数据,例如一个或多个诊断测试结果、测量结果数据所依据的测试标准、预定和/或预定义的治疗计划、患者概况、疾病概况等。此外,一种或多种电子设备可以呈现(例如,在其显示器上)与本文所述的任何快速诊断测试方法(例如,用于败血症和/或任何其它疾病状况的快速诊断测试)相关联的一个或多个定性和/或定量测试结果。
[0304]
本文描述的一些实施方案涉及具有非暂时性计算机可读介质(例如,存储器或一个或多个存储器)的计算机存储产品,该介质具有用于执行各种计算机实现的操作的指令或计算机代码。计算机可读介质(或处理器可读介质)在其本身不包括瞬时传播信号(例如,在诸如空间或电缆等传输介质上携带信息的传播电磁波)的意义上是非暂时性的。介质和计算机代码(也可称为代码)可以是针对一个或多个特定目的而设计和构建的。非暂时性计算机可读介质的实例包括但不限于磁存储介质,诸如硬盘、软盘和磁带;光学存储介质,诸如压缩盘/数字视频盘(cd/dvd)、压缩盘只读存储器(cd-rom)和全息设备;磁光存储介质,诸如光盘;载波信号处理模块;以及专门被配置成存储和执行程序代码的硬件设备,诸如asic、rom设备、ram设备和/或可编程逻辑设备(pld)。本文描述的其它实施方案涉及计算机程序产品,其可以包括例如本文讨论的指令和/或计算机代码。
[0305]
本文描述的一些实施方案和/或方法可以由软件(在硬件上执行)、硬件或其组合来执行。硬件模块可以包括例如通用处理器、cpu、fpga、asic等。(在硬件上执行的)软件模块可以用各种软件语言(例如,计算机代码)来表达,所述软件语言包括c、c 、java
tm
、ruby、visual basic
tm
、python
tm
和/或其它面向对象的、过程化的或其它编程语言和开发工具。计算机代码的实例包括但不限于微代码或微指令、机器指令(诸如由编译器产生的指令)、用于产生网络服务的代码以及包含由计算机使用解释器执行的高级指令的文件。例如,实施方案可以使用命令式编程语言(例如,c、fortran等)、函数式编程语言(haskell、erlang等)、逻辑编程语言(例如,prolog)、面向对象的编程语言(例如,java、c 等)或其它合适的编程语言和/或开发工具和/或其组合(例如,python
tm
)来实现。计算机代码的其它实例包括但不限于控制信号、加密代码和压缩代码。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。