3-(5-甲氧基-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮衍生物及其用途
1.优先权要求
2.本技术要求于2019年12月18日提交的美国临时申请号62/950,048的优先权权益,其披露内容通过引用以其全文并入本文。
技术领域
3.本披露涉及3-(5-甲氧基-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮化合物和药物组合物以及它们在降低宽间隔的锌指基序(wiz)蛋白表达水平、和/或诱导胎儿血红蛋白(hbf)蛋白表达水平、和在治疗遗传性血液病(血红蛋白病,例如β-血红蛋白病),例如镰状细胞病和β-地中海贫血中的用途。
背景技术:
4.镰状细胞病(scd)是一组严重的遗传性血液病,其导致红细胞扭曲成镰刀状。这些细胞可引起血流堵塞,从而导致剧烈疼痛、器官损伤和过早死亡。β地中海贫血是一组遗传性血液病,其由引起贫血的β球蛋白的合成减少或缺乏而导致。
5.已知胎儿血红蛋白(hbf)诱导可改善scd和β-地中海贫血患者的症状,并在临床上得到了遗传学(球蛋白控制基因座和bcl11a中的单核苷酸多态性)和药理学(羟基脲)验证(vinjamur,d.s.等人(2018),the british journal of haematology[英国血液病学杂志],180(5),630-643)。羟基脲是针对scd的当前护理标准,并且被认为经由诱导hbf提供益处,但具有遗传毒性,引起剂量限制性嗜中性粒细胞减少症,并且应答率低于40%。临床和临床前靶向的其他机制包括抑制hdac1/2(shearstone等人,2016,plos one[公共科学图书馆],11(4),e0153767)、lsd1(rivers等人,2018,experimental hematology[实验血液学],67,60-64)、dnmt1、pde9a(mcarthur等人,2019,haematologica[血液学].doi:10.3324/haematol.2018.213462)、hri激酶(grevet等人,2018,science[科学],361(6399),285-290)和g9a/glp(krivega等人,2015,blood[血液],126(5),665-672;renneville等人,2015,blood[血液],126(16),1930-1939)。另外,免疫调节剂泊马度胺和来那度胺在人原代红系细胞中离体(moutouh-de parseval,l.a.等人(2008),the journal of clinical investigation[临床调查杂志],118(1),248-258)和体内(meiler,s.e.等人(2011),blood[血液],118(4),1109-1112)诱导hbf。wiz被广泛表达,并在将g9a/glp组蛋白甲基转移酶靶向基因组基因座以调节染色质结构和转录中发挥作用(bian,chen等人(2015),elife 2015;4:e05606。
技术实现要素:
[0006]
本披露内容涉及有效降低wiz蛋白表达水平和/或诱导胎儿血红蛋白(hbf)表达的治疗剂。在一个实施例中,该治疗剂是小分子,sirna、shrna、aso、mirna、amo。本披露进一步涉及3-(5-甲氧基-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮化合物(其有效降低wiz蛋白表达
水平和/或诱导胎儿血红蛋白(hbf)表达)、其药学上可接受的盐、其组合物、以及其在用于以上详述的病症和目的的疗法中的用途。
[0007]
本披露提供了具有式(i’)的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,
[0008][0009]
其中:
[0010]
y选自o、ch2、cf2、和chf;
[0011]
z是从0至2的整数;
[0012]rx1
和r
x2
各自独立地选自氢和c
1-c6烷基;
[0013]ry1
和r
y2
各自独立地选自氢和c
1-c6烷基;
[0014]rz1
和r
z2
都是氢
[0015]
或
[0016]rz1
和r
z2
中的1个以及r
y1
和r
y2
中的1个一起形成c
1-c2亚烷基桥接基团,并且r
z1
和r
z2
以及r
y1
和r
y2
中的另一个都是氢;
[0017]
r1选自氢和c
1-c6烷基;
[0018]
r2选自氢、-c(=o)-r3、c
3-c8环烷基、c
1-c6卤代烷基、和c
1-c
10
烷基,其中所述烷基被独立地选自以下的0-1个取代基取代:c
6-c
10
芳基,包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基,包含独立地选自n、o和s的1-2个杂原子的4元至11元杂环基,c
3-c8环烷基和-o-(r
2a
),
[0019]
其中所述芳基、杂芳基、杂环基和环烷基各自独立地被0-5个r4取代;
[0020]r2a
是c
1-c6烷基,其中所述烷基被独立地选自c
6-c
10
芳基的0-1个取代基取代;
[0021]
r3选自-ch=cr
3ar3b
,c
6-c
10
芳基,包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基,包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基,c
3-c8环烷基,和c
1-c6烷基,其中所述烷基被0-3个r
3c
取代,并且
[0022]
其中所述芳基、杂芳基、杂环基和环烷基各自独立地被0-5个r4取代;
[0023]r3a
和r
3b
连同它们所附接的碳原子一起形成c
3-c8环烷基环;
[0024]
每个r
3c
在每次出现时独立地选自-c(=o)-r
3d
,nr
3er3f
,c
1-c6烷氧基,-o-r
3d
,羟基,-o-c
6-c
10
芳基,c
1-c6芳基c
6-c
10
烷基-o-,-o-(包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基),c
6-c
10
芳基,包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基,包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基,和c
3-c8环烷基,
[0025]
其中所述-o-芳基、芳基烷基-o-、和-o-杂芳基各自独立地被0-3个r
4a
取代,并且
[0026]
其中所述芳基、杂芳基、杂环基和环烷基各自独立地被0-5个r4取代;
[0027]r3d
是包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基;
[0028]r3e
和r
3f
各自独立地选自氢和c
1-c6烷基;
[0029]
每个r4在每次出现时独立地选自c
6-c
10
芳基,-o-c
6-c
10
芳基,c
1-c6芳基c
6-c
10
烷基-o-,-o-(包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基),包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基,包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基,c
1-c
10
烷基,c
1-c6烷氧基,c
1-c6卤代烷基,-so2r
4c
,卤素,羟基,-cn,-o-包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基,氧代,c
1-c6卤代烷氧基,-c(=o)-o-(r5),-c(=o)-(r5),-c(=o)-nr
6ar6b
,nr
6ar6b
,-nh-c(=o)-o-(c
1-c6烷基),和c
3-c8环烷基,其中所述芳基、-o-芳基、芳基烷基-o-、-o-杂芳基、杂芳基和杂环基各自独立地被0-3个r
4a
取代,
[0030]
其中所述烷基和烷氧基各自独立地被0-1个r
4b
取代,并且
[0031]
其中所述环烷基被各自独立地选自以下的0-3个取代基取代:-cn、c
1-c6烷基、c
1-c6烷氧基、羟基和c
1-c6卤代烷基;
[0032]r4a
在每次出现时独立地选自-cn,c
1-c6烷氧基,c
1-c6卤代烷基,卤素,羟基,-c(=o)-o-(r5),包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基,二(c
1-c6烷基)氨基c
1-c6烷基,c
1-c6烷基,包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基,和c
3-c6环烷基,其中所述烷基被0-1个r
4b
取代,并且其中所述杂芳基被0-3个r
4a-1
取代;
[0033]r4a-1
在每次出现时独立地选自c
1-c6烷基、二(c
1-c6烷基)氨基c
1-c6烷基、-cn、c
1-c6烷氧基、和c
1-c6卤代烷基;
[0034]r4b
在每次出现时独立地选自-cn,卤素,-c(=o)nr
6ar6b
,nr
6ar6b
,包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基,-c(=o)-oh,c
1-c6烷氧基,包含独立地选自n、o和s的1个或2个杂原子的4元至6元杂环基,c
3-c8环烷基,c
2-c4炔基,和c
6-c
10
芳基,其中所述芳基被各自独立地选自以下的0-1个取代基取代:-cn、c
1-c6卤代烷基、和c
1-c6烷基;
[0035]r4c
选自c
6-c
10
芳基、羟基、nh2、和卤素;
[0036]
r5选自c
1-c6烷基、c
6-c
10
芳基、和c
6-c
10
芳基c
1-c6烷基;
[0037]r6a
和r
6b
各自独立地选自氢和c
1-c6烷基;
[0038]
或r
6a
和r
6b
连同它们所附接的氮原子一起形成包含选自n、o和s的0-1个另外的杂原子的5元或6元杂环基,其中所述杂环基被0-2个r
6c
取代;
[0039]r6c
在每次出现时独立地选自c
6-c
10
芳基c
1-c6烷基、-c(=o)-o-(c
1-c6烷基)、-c(=o)-(c
1-c6烷基)、氧代和c
1-c6烷基,其中所述烷基被独立地选自以下的0-1个取代基取代:-cn和包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基。
[0040]
在一个实施例中,z是1;并且r
z1
和r
z2
中的1个以及r
y1
和r
y2
中的1个一起形成c
1-c2亚烷基桥接基团,并且r
z1
和r
z2
以及r
y1
和r
y2
中的另一个都是氢。
[0041]
在一个实施例中,z是1;并且r
z1
和r
z2
中的1个以及r
y1
和r
y2
中的1个一起形成c1亚烷基桥接基团,并且r
z1
和r
z2
以及r
y1
和r
y2
中的另一个都是氢。
[0042]
在一个实施例中,z是1;并且r
z1
和r
z2
中的1个以及r
y1
和r
y2
中的1个一起形成c2亚烷基桥接基团,并且r
z1
和r
z2
以及r
y1
和r
y2
中的另一个都是氢。
[0043]
在第一方面,本披露提供了具有式(i)的化合物或其药学上可接受的盐、水合物、
溶剂化物、前药、立体异构体、或互变异构体,
[0044][0045]
其中:
[0046]
y选自o、ch2、和cf2;
[0047]
z是从0至2的整数;
[0048]rx1
和r
x2
各自独立地选自氢和c
1-c6烷基;
[0049]ry1
和r
y2
各自独立地选自氢和c
1-c6烷基;
[0050]
r1选自氢和c
1-c6烷基;
[0051]
r2选自氢、-c(=o)-r3、c
3-c8环烷基、c
1-c6卤代烷基、和c
1-c
10
烷基,其中所述烷基被独立地选自以下的0-1个取代基取代:c
6-c
10
芳基,包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基,包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基,和c
3-c8环烷基,
[0052]
其中所述芳基、杂芳基、杂环基和环烷基各自独立地被0-5个r4取代;
[0053]
r3选自-ch=cr
3ar3b
,c
6-c
10
芳基,包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基,包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基,c
3-c8环烷基,和c
1-c6烷基,其中所述烷基被0-3个r
3c
取代,并且
[0054]
其中所述芳基、杂芳基、杂环基和环烷基各自独立地被0-5个r4取代;
[0055]r3a
和r
3b
连同它们所附接的碳原子一起形成c
3-c8环烷基环;
[0056]
每个r
3c
在每次出现时独立地选自-c(=o)-r
3d
,nr
3er3f
,c
1-c6烷氧基,-o-r
3d
,羟基,-o-c
6-c
10
芳基,c
1-c6芳基c
6-c
10
烷基-o-,-o-(包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基),c
6-c
10
芳基,包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基,包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基,和c
3-c8环烷基,
[0057]
其中所述-o-芳基、芳基烷基-o-、和-o-杂芳基各自独立地被0-3个r
4a
取代,并且
[0058]
其中所述芳基、杂芳基、杂环基和环烷基各自独立地被0-5个r4取代;
[0059]r3d
是包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基;
[0060]r3e
和r
3f
各自独立地选自氢和c
1-c6烷基;
[0061]
每个r4在每次出现时独立地选自c
6-c
10
芳基,-o-c
6-c
10
芳基,c
1-c6芳基c
6-c
10
烷基-o-,-o-(包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基),包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基,包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基,c
1-c
10
烷基,c
1-c6烷氧基,c
1-c6卤代烷基,-so2r
4c
,卤素,羟基,-cn,-o-包含独立地
选自n、o和s的1-2个杂原子的4元至6元杂环基,氧代,c
1-c6卤代烷氧基,-c(=o)-o-(r5),-c(=o)-(r5),-c(=o)-nr
6ar6b
,nr
6ar6b
,-nh-c(=o)-o-(c
1-c6烷基),和c
3-c8环烷基,其中所述芳基、-o-芳基、芳基烷基-o-、-o-杂芳基、杂芳基和杂环基各自独立地被0-3个r
4a
取代,
[0062]
其中所述烷基和烷氧基各自独立地被0-1个r
4b
取代,并且
[0063]
其中所述环烷基被各自独立地选自以下的0-3个取代基取代:-cn、c
1-c6烷基、c
1-c6烷氧基、和羟基;
[0064]r4a
在每次出现时独立地选自-cn,c
1-c6烷氧基,c
1-c6卤代烷基,卤素,羟基,-c(=o)-o-(r5),包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基,二(c
1-c6烷基)氨基c
1-c6烷基,和c
1-c6烷基,其中所述烷基被0-1个r
4b
取代,并且其中所述杂芳基被0-3个r
4a-1
取代;
[0065]r4a-1
在每次出现时独立地选自c
1-c6烷基、二(c
1-c6烷基)氨基c
1-c6烷基、-cn、c
1-c6烷氧基、和c
1-c6卤代烷基;
[0066]r4b
在每次出现时独立地选自-cn,-c(=o)nr
6ar6b
,nr
6ar6b
,包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基,-c(=o)-oh,c
1-c6烷氧基,包含独立地选自n、o和s的1个或2个杂原子的4元至6元杂环基,c
3-c8环烷基,c
2-c4炔基,和c
6-c
10
芳基,其中所述芳基被各自独立地选自以下的0-1个取代基取代:-cn、c
1-c6卤代烷基、和c
1-c6烷基;
[0067]r4c
选自c
6-c
10
芳基、羟基、nh2、和卤素;
[0068]
r5选自c
1-c6烷基、c
6-c
10
芳基、和c
6-c
10
芳基c
1-c6烷基;
[0069]r6a
和r
6b
各自独立地选自氢和c
1-c6烷基;
[0070]
或r
6a
和r
6b
连同它们所附接的氮原子一起形成包含选自n、o和s的0-1个另外的杂原子的5元或6元杂环基,其中所述杂环基被0-2个r
6c
取代;
[0071]r6c
在每次出现时独立地选自c
6-c
10
芳基c
1-c6烷基、-c(=o)-o-(c
1-c6烷基)、-c(=o)-(c
1-c6烷基)、氧代和c
1-c6烷基,其中所述烷基被独立地选自以下的0-1个取代基取代:-cn和包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基。
[0072]
在第二方面,本披露提供了药物组合物,所述药物组合物包含治疗有效量的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,以及药学上可接受的载体或赋形剂。
[0073]
在第三方面,本披露提供了具有式(i’)、(i)、(i-i)、(i-i-a)、(i-i-b)、(i-i-c)、(i-i-d)、(i-i-e)、(i-i-f)、(i-ii)、(i-ii-a)、(i-ii-b)、(i-ii-c)、(i-ii-d)、(i-ii-e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、(ia-xiii)、(ia-xiv)、(ie)、(if)、(ig)、(ih)、(ih-i)、或(ih-ii)的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,用作药物。
[0074]
在第四方面,本披露提供了治疗或预防有需要的受试者中的疾病或障碍的方法,所述方法包括向受试者施用治疗有效量的具有式(i’)、(i)、(i-i)、(i-i-a)、(i-i-b)、(i-i-c)、(i-i-d)、(i-i-e)、(i-i-f)、(i-ii)、(i-ii-a)、(i-ii-b)、(i-ii-c)、(i-ii-d)、(i-ii-e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、(ia-xiii)、(ia-xiv)、(ie)、(if)、(ig)、(ih)、(ih-i)、或(ih-ii)的化合物或其药学上可接受的盐、水合物、溶剂
d)、(i-ii-e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、(ia-xiii)、(ia-xiv)、(ie)、(if)、(ig)、(ih)、(ih-i)、或(ih-ii)的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体。
[0081]
在第十一方面,本披露提供了增加有需要的受试者的胎儿血红蛋白表达的方法,所述方法包括向受试者施用治疗有效量的具有式(i’)、(i)、(i-i)、(i-i-a)、(i-i-b)、(i-i-c)、(i-i-d)、(i-i-e)、(i-i-f)、(i-ii)、(i-ii-a)、(i-ii-b)、(i-ii-c)、(i-ii-d)、(i-ii-e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、(ia-xiii)、(ia-xiv)、(ie)、(if)、(ig)、(ih)、(ih-i)、或(ih-ii)的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体。
[0082]
在第十二方面,本披露提供了治疗有需要的受试者的血红蛋白病,例如β-血红蛋白病的方法,所述方法包括向受试者施用治疗有效量的具有式(i’)、(i)、(i-i)、(i-i-a)、(i-i-b)、(i-i-c)、(i-i-d)、(i-i-e)、(i-i-f)、(i-ii)、(i-ii-a)、(i-ii-b)、(i-ii-c)、(i-ii-d)、(i-ii-e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、(ia-xiii)、(ia-xiv)、(ie)、(if)、(ig)、(ih)、(ih-i)、或(ih-ii)的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体。
[0083]
在第十三方面,本披露提供了治疗有需要的受试者中的镰状细胞病的方法,所述方法包括向受试者施用治疗有效量的具有式(i’)、(i)、(i-i)、(i-i-a)、(i-i-b)、(i-i-c)、(i-i-d)、(i-i-e)、(i-i-f)、(i-ii)、(i-ii-a)、(i-ii-b)、(i-ii-c)、(i-ii-d)、(i-ii-e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、(ia-xiii)、(ia-xiv)、(ie)、(if)、(ig)、(ih)、(ih-i)、或(ih-ii)的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体。
[0084]
在第十四方面,本披露提供了治疗有需要的受试者的β-地中海贫血的方法,所述方法包括向受试者施用治疗有效量的具有式(i’)、(i)、(i-i)、(i-i-a)、(i-i-b)、(i-i-c)、(i-i-d)、(i-i-e)、(i-i-f)、(i-ii)、(i-ii-a)、(i-ii-b)、(i-ii-c)、(i-ii-d)、(i-ii-e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、(ia-xiii)、(ia-xiv)、(ie)、(if)、(ig)、(ih)、(ih-i)、或(ih-ii)的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体。
[0085]
在第十五方面,本披露提供了具有式(i’)、(i)、(i-i)、(i-i-a)、(i-i-b)、(i-i-c)、(i-i-d)、(i-i-e)、(i-i-f)、(i-ii)、(i-ii-a)、(i-ii-b)、(i-ii-c)、(i-ii-d)、(i-ii-e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、(ia-xiii)、(ia-xiv)、(ie)、(if)、(ig)、(ih)、(ih-i)、或(ih-ii)的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,用于治疗疾病或障碍。
[0086]
在第十六方面,本披露提供了具有(i’)、(i)、(i-i)、(i-i-a)、(i-i-b)、(i-i-c)、
(i-i-d)、(i-i-e)、(i-i-f)、(i-ii)、(i-ii-a)、(i-ii-b)、(i-ii-c)、(i-ii-d)、(i-ii-e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、(ia-xiii)、(ia-xiv)、(ie)、(if)、(ig)、(ih)、(ih-i)、或(ih-ii)的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,用于治疗选自镰状细胞病和β-地中海贫血的疾病或障碍。
[0087]
在第十七方面,本披露提供了具有式(i’)、(i)、(i-i)、(i-i-a)、(i-i-b)、(i-i-c)、(i-i-d)、(i-i-e)、(i-i-f)、(i-ii)、(i-ii-a)、(i-ii-b)、(i-ii-c)、(i-ii-d)、(i-ii-e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、(ia-xiii)、(ia-xiv)、(ie)、(if)、(ig)、(ih)、(ih-i)、或(ih-ii)的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,用于治疗或预防受wiz蛋白水平降低影响的疾病或障碍。
[0088]
在第十八方面,本披露提供了具有式(i’)、(i)、(i-i)、(i-i-a)、(i-i-b)、(i-i-c)、(i-i-d)、(i-i-e)、(i-i-f)、(i-ii)、(i-ii-a)、(i-ii-b)、(i-ii-c)、(i-ii-d)、(i-ii-e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、(ia-xiii)、(ia-xiv)、(ie)、(if)、(ig)、(ih)、(ih-i)、或(ih-ii)的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,用于降低wiz蛋白水平。
[0089]
在第十九方面,本披露提供了具有式(i’)、(i)、(i-i)、(i-i-a)、(i-i-b)、(i-i-c)、(i-i-d)、(i-i-e)、(i-i-f)、(i-ii)、(i-ii-a)、(i-ii-b)、(i-ii-c)、(i-ii-d)、(i-ii-e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、(ia-xiii)、(ia-xiv)、(ie)、(if)、(ig)、(ih)、(ih-i)、或(ih-ii)的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,用于治疗或预防受wiz蛋白表达的抑制影响的疾病或障碍。
[0090]
在第二十方面,本披露提供了具有式(i’)、(i)、(i-i)、(i-i-a)、(i-i-b)、(i-i-c)、(i-i-d)、(i-i-e)、(i-i-f)、(i-ii)、(i-ii-a)、(i-ii-b)、(i-ii-c)、(i-ii-d)、(i-ii-e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、(ia-xiii)、(ia-xiv)、(ie)、(if)、(ig)、(ih)、(ih-i)、或(ih-ii)的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,用于治疗或预防受wiz蛋白降解影响的疾病或障碍。
[0091]
在第二十一方面,本披露提供了具有式(i’)、(i)、(i-i)、(i-i-a)、(i-i-b)、(i-i-c)、(i-i-d)、(i-i-e)、(i-i-f)、(i-ii)、(i-ii-a)、(i-ii-b)、(i-ii-c)、(i-ii-d)、(i-ii-e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、(ia-xiii)、(ia-xiv)、(ie)、(if)、(ig)、(ih)、(ih-i)、或(ih-ii)的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,用于抑制、降低、或消除wiz蛋白的活性或wiz蛋白
e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、(ia-xiii)、(ia-xiv)、(ie)、(if)、(ig)、(ih)、(ih-i)、或(ih-ii)的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,用于治疗受胎儿血红蛋白表达增加的影响的疾病或障碍。
[0099]
在第二十九方面,本披露提供了具有式(i’)、(i)、(i-i)、(i-i-a)、(i-i-b)、(i-i-c)、(i-i-d)、(i-i-e)、(i-i-f)、(i-ii)、(i-ii-a)、(i-ii-b)、(i-ii-c)、(i-ii-d)、(i-ii-e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、(ia-xiii)、(ia-xiv)、(ie)、(if)、(ig)、(ih)、(ih-i)、或(ih-ii)的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,用于治疗受wiz蛋白的活性或wiz蛋白表达的抑制、降低、或消除影响的疾病或障碍。
[0100]
在第三十方面,本披露提供了具有式(i’)、(i)、(i-i)、(i-i-a)、(i-i-b)、(i-i-c)、(i-i-d)、(i-i-e)、(i-i-f)、(i-ii)、(i-ii-a)、(i-ii-b)、(i-ii-c)、(i-ii-d)、(i-ii-e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、(ia-xiii)、(ia-xiv)、(ie)、(if)、(ig)、(ih)、(ih-i)、或(ih-ii)的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,用于治疗受胎儿血红蛋白的诱导或促进影响的疾病或障碍。
[0101]
在第三十一方面,本披露提供了具有式(i’)、(i)、(i-i)、(i-i-a)、(i-i-b)、(i-i-c)、(i-i-d)、(i-i-e)、(i-i-f)、(i-ii)、(i-ii-a)、(i-ii-b)、(i-ii-c)、(i-ii-d)、(i-ii-e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、(ia-xiii)、(ia-xiv)、(ie)、(if)、(ig)、(ih)、(ih-i)、或(ih-ii)的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,用于治疗受胎儿血红蛋白产生或表达的重新激活影响的疾病或障碍。
[0102]
本文以及在权利要求中描述了本披露的各个方面。
[0103]
除非另外定义,否则本文所用的所有技术术语和科学术语均具有与本披露内容所属领域的普通技术人员通常所理解的相同的含义。在本说明书和权利要求书中,单数形式还包括复数,除非上下文另外明确地指示。虽然类似或等同于本文所述的那些的方法和材料可以用于本公开的实践或测试,但以下描述了合适的方法和材料。本文所提到的所有出版物、专利申请、专利和其他参考文献均通过引用以其整体并入,用于所有目的。本文引用的参考文献不被视为要求保护的披露的现有技术。在冲突的情况下,则以包括定义在内的本说明书为准。此外,这些材料、方法和实例仅仅是说明性的,而并不旨在进行限制。
[0104]
根据以下的具体实施方式和权利要求书,本文所披露的化合物、组合物和方法的其他特征和优点将显而易见。
附图说明
[0105]
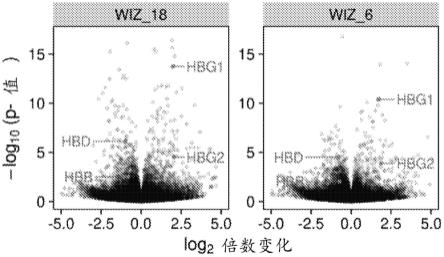
图1a描绘了来自wiz ko细胞的差异表达基因与加扰grna对照相比的火山图。每个
点代表一个基因。hbg1/2基因与靶向wiz ko的wiz_6和wiz_18grna差异性地上调。
[0106]
图1b描绘了条形图,其显示了由于shrna介导的wiz在人动员的外周血cd34 源性红系细胞中的缺失而导致的hbf 细胞的频率。
[0107]
图1c描绘了条形图,其显示了由于crispr/cas9介导的wiz在人动员的外周血cd34 源性红系细胞中的缺失而导致的hbf 细胞的频率。
具体实施方式
[0108]
本文披露的化合物能有效降低wiz蛋白表达水平、或诱导胎儿血红蛋白(hbf)表达。不希望受任何理论的束缚,据信所披露的化合物可以通过诱导胎儿血红蛋白hbf表达来治疗血液病,例如遗传性血液病,如镰状细胞病和β-地中海贫血。
[0109]
定义
[0110]
除非另有说明,术语“本披露的化合物(compounds of the present disclosure、compounds of the disclosure、或compound of the disclosure)”是指具有式(i’)、(i)、(i-i)、(i-i-a)、(i-i-b)、(i-i-c)、(i-i-d)、(i-i-e)、(i-i-f)、(i-ii)、(i-ii-a)、(i-ii-b)、(i-ii-c)、(i-ii-d)、(i-ii-e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、(ia-xiii)、(ia-xiv)、(ie)、(if)、(ig)、(ih)、(ih-i)和(ih-ii)的化合物、示例性化合物、其盐(特别是其药学上可接受的盐)、水合物、溶剂化物、前药以及所有立体异构体(包括非对映异构体和对映异构体)、旋转异构体、互变异构体和同位素标记的化合物(包括氘取代物)、以及固有形成的部分。
[0111]
在下文定义的基团(group、radical)或部分中,通常在基团之前指出碳原子数目,例如c
1-c
10
烷基意指具有1至10个碳原子的烷基基团。一般而言,对于包含两种或两种以上亚基团的基团,最后提及的基团为基团附接点,例如“烷基芳基”意指具有式烷基-芳基-的单价基团,而“芳基烷基”意指具有式芳基-烷基-的单价基团。因此,术语c
6-c
10
芳基c
1-c6烷基意指具有式c
6-c
10
芳基c
1-c6烷基-的单价基团,使得所述基团经由c
1-c6烷基部分附接到基础分子。
[0112]
在r
3c
或r4是芳基烷基-o-的实施例中,这意指具有式芳基-烷基-o-或-o-烷基-芳基的单价o基团。
[0113]
此外,使用表示单价基团的术语而其中二价基团是合适的,则应理解为表示相应的二价基团,反之亦然。除非另有说明,否则假定术语对照的常规定义和常规的稳定原子的原子价,并在全部式和基团中体现。冠词“一个/种(a/an)”是指一个/种或多于一个/种(例如,至少一个/种)该冠词的语法宾语。通过举例,“一个要素”意指一个要素或多于一个要素。
[0114]
除非另有指示,否则术语“和/或”意指“和”或者“或”。
[0115]
术语“经取代的”是指指定的基团或部分携带一个或多个合适的取代基,其中这些取代基可以在一个或多个位置处与所述指定的基团或部分连接。例如,被环烷基取代的芳基可指示所述环烷基通过键或通过与芳基稠合并共享两个或更多个共同原子而与所述芳基的一个原子连接。
[0116]
在与任何r基团(例如r4)连接的键不与任何指定原子(例如,如下所示的杂芳基基
团
[0117]
)连接的实施例中,这意指r4基团可以经由环上的任何原子键合。
[0118]
如本文所用,术语“c
1-c
10
烷基”是指仅由碳和氢原子组成的直链或支链烃链基团,所述基团不含有不饱和度、具有从一至十个碳原子、并且通过单键附接到分子的其余部分。术语“c
1-c3烷基”、“c
1-c4烷基”、“c
1-c6烷基”、“c
1-c8烷基”应相应地进行解释。c
1-c
10
烷基的实例包括但不限于甲基、乙基、正丙基、1-甲基乙基(异丙基)、正丁基、1-甲基丙基(仲丁基)、2-甲基丙基(异丁基)、1,1-二甲基乙基(叔丁基)、正戊基、正己基、正庚基、4-庚基、正辛基、2-异丙基-3-甲基丁基、正壬基和正癸基。
[0119]
如本文所用,术语“c
1-c6烷氧基”是指具有式-ora的基团,其中ra是如上一般定义的c
1-c6烷基基团。c
1-c6烷氧基的实例包括但不限于甲氧基、乙氧基、丙氧基、异丙氧基、丁氧基、异丁氧基、叔丁氧基、仲丁氧基、戊氧基和己氧基。
[0120]“炔基”意指含有2-12个碳原子的直链或支链不饱和烃。“炔基”基团在链中含有至少一个三键。术语“c
2-c4炔基”应相应地进行解释。炔基基团的实例包括乙炔基、炔丙基、正丁炔基、异丁炔基、戊炔基、或己炔基。炔基基团可以是未经取代的或经取代的。
[0121]“c
2-c4炔基”的优选实例包括但不限于乙炔基、丙-1-炔基、丙-2-炔基和丁-2-炔基。
[0122]
如本文所用,术语“c
1-c6卤代烷基”是指被如本文所定义的一个或多个卤代基团取代的以上所定义的c
1-c6烷基基团。c
1-c6卤代烷基的实例包括但不限于三氟甲基、二氟甲基、氟甲基、三氯甲基、1,1-二氟乙基、2,2-二氟乙基、2,2,2-三氟乙基、2-氟丙基、3,3-二氟丙基和1-氟甲基-2-氟乙基、1,3-二溴丙-2-基、3-溴-2-氟丙基和1,4,4-三氟丁-2-基。
[0123]
如本文所用,术语“c
1-c6卤代烷氧基”意指被一个或多个卤代基团取代的如本文所定义的c
1-c6烷氧基基团。c
1-c6卤代烷氧基基团的实例包括但不限于三氟甲氧基、二氟甲氧基、氟甲氧基、三氯甲氧基、1,1-二氟乙氧基、2,2-二氟乙氧基、2,2,2-三氟乙氧基、1-氟甲基-2-氟乙氧基、五氟乙氧基、2-氟丙氧基、3,3-二氟丙氧基和3-二溴丙氧基。优选地,c
1-c6卤代烷氧基的一个或多个卤代基团是氟。优选地,c
1-c6卤代烷氧基选自三氟甲氧基、二氟甲氧基、氟甲氧基、1,1-二氟乙氧基、2,2-二氟乙氧基、2,2,2-三氟乙氧基、1-氟甲基-2-氟乙氧基、和五氟乙氧基。
[0124]
术语“卤素”或“卤代”意指氟、氯、溴、或碘。
[0125]
如本文所用,术语“环烷基”意指含有3-18个碳原子的单环或多环饱和或部分不饱和碳环,其中在环碳之间没有共用的离域π电子(芳香性)。术语“c
3-c8环烷基”和“c
3-c6环烷基”应相应地进行解释。术语多环涵盖桥接(例如降莰烷(norbomane))、稠合(例如十氢化萘)和螺环环烷基。优选地,环烷基,例如c
3-c8环烷基是3至8个碳原子的单环或桥接烃基团。
[0126]
环烷基基团的实例包括但不限于环丙烯基、环丙基、环丁基、环丁烯基、环戊基、环己基、环庚烷基、环辛烷基、降莰烷基(norboranyl)、降莰烯基(norborenyl)、双环[2.2.2]辛烷基、双环[2.2.2]辛烯基、双环[1.1.1]戊烷基及其衍生物。
[0127]c3-c8环烷基的优选实例包括但不限于环丙基、环丁基、环戊基、环己基、双环
噻二唑基、1,2,4-噻二唑基、1,2,5-噻二唑基、1,3,4-噻二唑基)、四唑基、吡喃基、吡啶基、哒嗪基、嘧啶基、吡嗪基、1,2,3-三嗪基、1,2,4-三嗪基、1,3,5-三嗪基、噻二嗪基、氮杂基、吖癸因基(azecinyl)等。
[0136]
杂芳基还旨在包括含有选自氧、氮和硫(o、n和s)的一个或多个杂原子的双环杂环芳族环。代表性实例是吲哚基、异吲哚基、苯并呋喃基、苯并噻吩基、吲唑基、苯并吡喃基、苯并咪唑基、苯并噻唑基、苯并异噻唑基、苯并噁唑基、苯并异噁唑基、苯并噁嗪基、苯并三唑基、萘啶基、酞嗪基、蝶啶基、嘌呤基、喹唑啉基、噌啉基、喹啉基、异喹啉基、喹唑啉基、噁唑并吡啶基、异噁唑并吡啶基、吡咯并吡啶基、呋喃并吡啶基、噻吩并吡啶基、咪唑并吡啶基、咪唑并嘧啶基、吡唑并吡啶基、吡唑并嘧啶基、吡唑并三嗪基、三唑并吡啶基、三唑并嘧啶基、咪唑并噻唑基、三唑并吡啶基、三唑并嘧啶基等。
[0137]
杂芳基还旨在包括含有选自氧、氮和硫(o、n和s)的一个或多个杂原子的多环杂环芳族环。代表性实例是咔唑基、吩噁嗪基、吩嗪基、吖啶基、吩噻嗪基、咔啉基、菲咯啉基等。
[0138]
杂芳基还旨在包括含有选自氧、氮和硫(o、n和s)的一个或多个杂原子的部分饱和单环、双环或多环杂环基。代表性实例是咪唑啉基、二氢吲哚基、二氢苯并呋喃基、二氢苯并噻吩基、二氢苯并吡喃基、二氢吡啶并噁嗪基、二氢苯并二噁英基(例如2,3-二氢苯并[b][1,4]二噁英基)、苯并间二氧杂环戊烯基(例如苯并[d][1,3]间二氧杂环戊烯)、二氢苯并噁嗪基(例如3,4-二氢-2h-苯并[b][1,4]噁嗪)、四氢吲唑基、四氢苯并咪唑基、四氢咪唑并[4,5-c]吡啶基、四氢喹啉基、四氢异喹啉基、四氢喹喔啉基等。
[0139]
杂芳基环结构可以被一个或多个取代基取代。这些取代基本身可以是任选地经取代的。杂芳基环可以经由碳原子或杂原子键合。
[0140]
术语“5-10元杂芳基”应相应地进行解释。
[0141]
5-10元杂芳基的实例包括但不限于吲哚基、咪唑并吡啶基、异喹啉基、苯并噁唑酮基、吡啶基、嘧啶基、吡啶酮基、苯并三唑基、哒嗪基、吡唑并三嗪基、吲唑基、苯并咪唑基、喹啉基、三唑基(例如1,2,4-三唑基)、吡唑基、噻唑基、噁唑基、异噁唑基、吡咯基、噁二唑基(例如1,2,3-噁二唑基、1,2,4-噁二唑基、1,2,5-噁二唑基、1,3,4-噁二唑基)、咪唑基、吡咯并吡啶基、四氢吲唑基、喹喔啉基、噻二唑基(例如1,2,3-噻二唑基、1,2,4-噻二唑基、1,2,5-噻二唑基、1,3,4-噻二唑基)、吡嗪基、噁唑并吡啶基、吡唑并嘧啶基、苯并噁唑基、二氢吲哚基、异噁唑并吡啶基、二氢吡啶并噁嗪基、四唑基、二氢苯并二噁英基(例如2,3-二氢苯并[b][1,4]二噁英基)、苯并间二氧杂环戊烯基(例如苯并[d][1,3]间二氧杂环戊烯)和二氢苯并噁嗪基(例如3,4-二氢-2h-苯并[b][1,4]噁嗪)。
[0142]
如本文所用,术语“c
6-c
10
芳基c
1-c6烷基”是指具有式-r
a-c
6-c
10
芳基的单价基团,其中ra是如上一般定义的c
1-c6烷基基团。c
6-c
10
芳基c
1-c6烷基的实例包括但不限于c1烷基-c6h5(苄基)、c1烷基-c
10
h7、-ch(ch3)-c6h5、-c(ch3)
2-c6h5和-(ch2)
2-6-c6h5。
[0143]
如本文所用,术语“氧代”是指基团=o。
[0144]
如本文所用,术语“二(c
1-c6烷基)氨基c
1-c6烷基”是指具有式-r
a1-n(r
a2
)-r
a2
的基团,其中r
a1
是如上所定义的c
1-c6烷基基团并且每个r
a2
是如上所定义的可以相同或不同的c
1-c6烷基。氮原子可以与任一烷基基团中的任何碳原子键合。实例包括但不限于(c1烷基-nr
6ar6b
)、(c1烷基-ch
2-nr
6ar6b
)、(-(ch2)
3-nr
6ar6b
)、(-(ch2)
4-nr
6ar6b
)、(-(ch2)
5-nr
6ar6b
)和(-(ch2)
6-nr
6ar6b
),其中r
6a
和r
6b
如本文所定义。
[0145]
如本文所用,术语“二(c
1-c6烷基)氨基”是指具有式-n(r
a1
)-r
a1
的氨基基团,其中每个r
a1
是如上所定义的可以相同或不同的c
1-c6烷基基团。
[0146]“氰基”或
“‑
cn”意指具有通过三键连接氮原子和碳原子的取代基,例如c≡n。
[0147]
如本文所用,术语“c
1-c2亚烷基”是指仅由碳和氢原子组成的直链或支链烃链二价基团,所述基团中不存在不饱和,具有一个至两个碳原子。术语“c
1-c2亚烷基”应相应地进行解释。
[0148]
关于r
z1
和r
z2
中的1个以及r
y1
和r
y2
中的1个形成桥接基团的实施例,这被理解为在含有n的杂环烷基的两个不相邻碳原子处形成的环,这两个不相邻碳原子连接以形成c
1-c2亚烷基接头,例如c1或c2亚烷基基团。包含在具有式(i’)的化合物内的桥接基团的实例包括但不限于
[0149]
如本文所用,术语“任选地经取代”包括未经取代或经取代。
[0150]
如本文所用,表示与分子的其他部分的附接点。
[0151]
如本文所用,具有式(x)的化合物或通用方案1至4任一项中的任何中间体及其子式中的术语氮保护基团(pg)是指应保护有关的官能团免于不希望的二次反应(例如酰化、醚化、酯化、氧化、溶剂分解和类似反应)的基团。可以在脱保护条件下将其除去。取决于所使用的保护基团,技术人员通过参考已知方法将知道如何去除保护基团以获得游离胺nh2基团。这些方法包括参考有机化学教科书和文献方法,例如j.f.w.mcomie,“protective groups in organic chemistry[有机化学中的保护基团]”,plenum press[plenum出版社],伦敦和纽约1973;t.w.greene和p.g.m.wuts,“greene's protective groups in organic synthesis[格林有机合成中的保护基团]”,第四版,wiley[威利出版社],纽约2007;在“the peptides[肽]”;第3卷(编辑:e.gross和j.meienhofer),academic press[学术出版社],伦敦和纽约1981;p.j.kocienski,“protecting groups[保护基团]”,第三版,georg thieme verlag[格奥尔格蒂梅出版社],斯图加特和纽约2005;以及在“methoden der organischen chemie”(methods of organic chemistry)[有机化学方法],houben weyl,第4版,第15卷/i,georg thieme verlag[格奥尔格蒂梅出版社],斯图加特1974。
[0152]
优选的氮保护基团通常包括:c
1-c6烷基(例如叔丁基),优选地c
1-c4烷基,更优选地c
1-c2烷基,最优选地c1烷基,其被以下各项单取代、二取代或三取代:三烷基甲硅烷基-c
1-c7烷氧基(例如三甲基甲硅烷基乙氧基)、芳基(优选地苯基)或杂环基团(例如苄基、枯基、二苯甲基、吡咯烷基、三苯甲基、吡咯烷基甲基、1-甲基-1,1-二甲基苄基、(苯基)甲基苯),其中所述芳基环或杂环基团未被取代或被一个或多个(例如两个或三个)例如选自由以下组成的组的残基取代:c
1-c7烷基、羟基、c
1-c7烷氧基(例如对甲氧基苄基(pmb))、c
2-c
8-烷酰基-氧基、卤素、硝基、氰基、和cf3、芳基-c
1-c
2-烷氧基羰基(优选地苯基-c
1-c
2-烷氧基羰基(例如苄氧基羰基(cbz)、苄氧基甲基(bom)、新戊酰氧基甲基(pom))、c
1-c
10-烯氧基羰基、c
1-c6烷基羰基(例如乙酰基或新戊酰基)、c
6-c
10-芳基羰基;c
1-c
6-烷氧基羰基(例如叔
丁氧基羰基(boc)、甲基羰基、三氯乙氧基羰基(troc)、新戊酰基(piv)、烯丙氧基羰基),c
6-c
10-芳基c
1-c
6-烷氧基羰基(例如9-芴基甲基氧基羰基(fmoc)),烯丙基或肉桂基,磺酰基或次磺酰基,琥珀酰亚胺基基团,甲硅烷基基团(例如三芳基甲硅烷基、三烷基甲硅烷基、三乙基甲硅烷基(tes)、三甲基甲硅烷基乙氧基甲基(sem)、三甲基甲硅烷基(tms)、三异丙基甲硅烷基或叔丁基二甲基甲硅烷基)。
[0153]
根据本披露,优选的保护基团(pg)可以选自包括以下的组:叔丁基氧基羰基(boc)、苄氧基羰基(cbz)、对甲氧基苄基(pmb)、甲基氧基羰基、三甲基甲硅烷基乙氧基甲基(sem)和苄基。保护基团(pg)优选地是叔丁基氧基羰基(boc)。
[0154]
在一些实施例中,本披露的化合物对其他蛋白质具有选择性。
[0155]
如本文所用,与降低wiz蛋白表达水平和/或诱导胎儿血红蛋白(hbf)表达的方法有关的术语“治疗剂”是指导致wiz基因或wiz蛋白的表达可检测地降低或wiz蛋白的活性水平降低(与不存在这种物质情况下的水平相比)的物质。在一些实施例中,该物质是小分子化合物,其可靶向wiz以进行降解(例如,通过e3泛素途径,又称为“wiz降解剂”,例如,如本文所述的化合物)。在一些实施例中,该物质是抗wiz shrna。在一些实施例中,该物质是抗wiz sirna。在一些实施例中,该物质是抗wiz aso。在一些实施例中,该物质是抗wiz amo(抗mirna寡核苷酸)。在一些实施例中,该物质是抗wiz反义核酸。在一些实施例中,该物质是本文所述的组合物或细胞或细胞群(其包含本文所述的grna分子)。
[0156]
如本文所用,术语“小分子”是指分子量《900道尔顿的药剂。根据本披露的小分子可以靶向wiz蛋白以进行降解,例如,通过e3泛素途径和/或诱导胎儿血红蛋白(hbf)表达。在一个实施例中,小分子是指如本文所披露的化合物,例如,具有式(i’)的化合物。
[0157]
如本文所用,“sirna”是指形成双链rna的核酸,当该sirna在与基因或靶基因相同的细胞中存在(例如表达)时,该双链rna能够降低或抑制该基因或靶基因的表达。sirna典型地长度为约5至约100个核苷酸,更典型地长度为约10至约50个核苷酸,更典型地长度为约15至约30个核苷酸,最典型地长度为约20-30个碱基核苷酸、或约20-25或约24-29个核苷酸,例如长度为20、21、22、23、24、25、26、27、28、29或30个核苷酸。sirna分子和产生这些分子的方法描述于例如,bass,2001,nature[自然],411,428-429;elbashir等人,2001,nature[自然],411,494-498;wo 00/44895;wo 01/36646;wo 99/32619;wo 00/01846;wo 01/29058;wo 99/07409;以及wo 00/44914。转录dsrna或sirna的dna分子(例如,作为发夹双链体)还提供rnai。转录dsrna的dna分子披露于美国专利号6,573,099和美国专利申请公开号2002/0160393和2003/0027783,以及tuschl和borkhardt,molecular interventions[分子介入],2:158(2002)。
[0158]
如本文所用,反义寡核苷酸(aso)是与所选序列互补的dna或rna单链。在反义rna的情况下,它们通过与某些信使rna链结合(这一过程称为杂交)来阻止这些信使rna链的蛋白质翻译。反义寡核苷酸可用于靶向特异性的互补(编码或非编码)rna。如果发生结合,这种杂合体可以被酶rna酶h降解。
[0159]
如本文所用,“调节剂”或“降解剂”意指例如本披露的化合物,该化合物有效调节、降低、或减少特异性蛋白(例如wiz)的水平或降解特异性蛋白(例如wiz)。可以通过将用本披露的化合物处理后剩余的特异性蛋白(例如wiz)的量与用本披露的化合物处理前测量的存在的特异性蛋白(例如wiz)的初始量或水平进行比较来测量降解的特异性蛋白(例如
wiz)的量。
[0160]
如本文所用,“选择性调节剂”、“选择性降解剂”、或“选择性化合物”意指例如本披露的化合物,其有效调节、降低、或减少特异性蛋白(例如wiz)的水平或降解特异性蛋白(例如wiz)至比任何其他蛋白更大的程度。例如,可以通过将化合物调节、降低、或减少特异性蛋白(例如wiz)的水平或降解特异性蛋白的能力与该化合物调节、降低、或减少其他蛋白水平或降解其他蛋白的能力进行比较,来鉴定“选择性调节剂”、“选择性降解剂”、或“选择性化合物”。在一些实施例中,可以通过测量化合物的ec
50
或ic
50
鉴定选择性。降解可以通过介导e3连接酶(例如包含蛋白质cereblon的e3-连接酶复合物)来实现。
[0161]
在一个实施例中,降解的特异性蛋白是wiz蛋白。在一个实施例中,与初始水平相比,至少约30%的wiz被降解。在一个实施例中,与初始水平相比,至少约40%的wiz被降解。在一个实施例中,与初始水平相比,至少约50%的wiz被降解。在一个实施例中,与初始水平相比,至少约60%的wiz被降解。在一个实施例中,与初始水平相比,至少约70%的wiz被降解。在一个实施例中,与初始水平相比,至少约75%的wiz被降解。在一个实施例中,与初始水平相比,至少约80%的wiz被降解。在一个实施例中,与初始水平相比,至少约85%的wiz被降解。在一个实施例中,与初始水平相比,至少约90%的wiz被降解。在一个实施例中,与初始水平相比,至少约95%的wiz被降解。在一个实施例中,与初始水平相比,超过95%的wiz被降解。在一个实施例中,与初始水平相比,至少约99%的wiz被降解。
[0162]
在一个实施例中,与初始水平相比,从约30%至约99%的量的wiz被降解。在一个实施例中,与初始水平相比,从约40%至约99%的量的wiz被降解。在一个实施例中,与初始水平相比,从约50%至约99%的量的wiz被降解。在一个实施例中,与初始水平相比,从约60%至约99%的量的wiz被降解。在一个实施例中,与初始水平相比,从约70%至约99%的量的wiz被降解。在一个实施例中,与初始水平相比,从约80%至约99%的量的wiz被降解。在一个实施例中,与初始水平相比,从约90%至约99%的量的wiz被降解。在一个实施例中,与初始水平相比,从约95%至约99%的量的wiz被降解。在一个实施例中,与初始水平相比,从约90%至约95%的量的wiz被降解。
[0163]
如本文所用,术语“诱导胎儿血红蛋白”、“胎儿血红蛋白诱导”、或“增加胎儿血红蛋白表达”是指增加受试者血液中hbf的百分比。在一个实施例中,受试者血液中总hbf的量增加。在一个实施例中,受试者血液中总血红蛋白的量增加。在一个实施例中,与不存在本文披露的化合物的任一情况相比,hbf的量增加了至少约10%、或至少约20%、或至少约30%、或至少约40%、或至少约50%、或至少约60%、或至少约70%、或至少约80%、或至少约90%、或至少约100%、或超过100%,例如至少约2倍、或至少约3倍、或至少约4倍、或至少约5倍、或至少约6倍、或至少约7倍、或至少约8倍、或至少约9倍、或至少约10倍、或超过10倍。
[0164]
在一个实施例中,与不存在本文披露的化合物的任一情况相比,血液(例如受试者血液)中总血红蛋白增加了至少约10%、或至少约20%、或至少约30%、或至少约40%、或至少约50%、或至少约60%、或至少约70%、或至少约80%、或至少约90%、或至少约100%、或超过100%,例如至少约2倍、或至少约3倍、或至少约4倍、或至少约5倍、或至少约6倍、或至少约7倍、或至少约8倍、或至少约9倍、或至少约10倍、或超过10倍。
[0165]
本披露的化合物的术语“治疗有效量”是指将引起受试者的生物学或医学响应(例
如,酶或蛋白活性的降低或抑制,或改善症状、缓解病症、减慢或延迟疾病进展或预防疾病等)的本披露的化合物的量。在一个实施例中,术语“治疗有效量”是指本披露的化合物的如下量:当施用于受试者时有效地(1)至少部分缓解、预防或改善以下病症或障碍或疾病:(i)由wiz介导,或(ii)与wiz活性相关,或者(iii)通过wiz的活性(正常或异常表征);(2)降低或抑制wiz的活性;或(3)减少或抑制wiz的表达。在另一个实施例中,术语“治疗有效量”是指本披露的化合物的以下量,当施用至细胞、或组织、或非细胞生物材料、或介质时,所述量有效地至少部分地降低或抑制wiz的活性;或至少部分地减少或抑制wiz的表达。
[0166]“hbf依赖性疾病或障碍”意指任何直接地或间接地受hbf蛋白水平的调节影响的疾病或障碍。
[0167]
如本文所用,术语“受试者”是指灵长类动物(例如,人(男性或女性))、狗、兔、豚鼠、猪、大鼠和小鼠。在某些实施例中,受试者是灵长类动物。在又其他实施例中,受试者是人。
[0168]
如本文所用,术语“抑制(inhibit、inhibition或inhibiting)”是指减少或抑制给定的病症、症状或障碍、或疾病,或在生物活性或过程的基线活性方面的显著降低。
[0169]
如本文所用,术语任何疾病或障碍的“治疗(treat、treating或treatment)”是指减轻或改善疾病或障碍(即,减慢或阻止疾病或其至少一种临床症状的发展);或者减轻或改善与所述疾病或障碍相关联的至少一种物理参数或生物标志物,包括针对患者可能无法辨别的那些物理参数或生物标志物。
[0170]
如本文所用,术语任何疾病或障碍的“预防(prevent、preventing或prevention)”是指疾病或障碍的预防性治疗;或延迟疾病或障碍的发作或进展。
[0171]
如本文所用,如果受试者将在生物学上、在医学上或在生活质量上从治疗中获益,则这样的受试者是“需要”这种治疗的。
[0172]
如本文所用,术语“一个/种(a、an)”、“所述(the)”以及在本披露的上下文中(特别是在权利要求的上下文中)使用的类似术语应被解释为涵盖单数和复数两者,除非本文另外指示或与上下文明显相矛盾。
[0173]
本文描述了本披露的多个列举的实施例。应认识到,每个实施例中指定的特征可以与其他指定特征组合以提供本披露的另外实施例。
[0174]
列举的实施例
[0175]
实施例1.一种具有式(i’)的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,
[0176][0177]
其中:
[0178]
y选自o、ch2、cf2、和chf;
[0179]
z是从0至2的整数;
[0180]rx1
和r
x2
各自独立地选自氢和c
1-c6烷基;
[0181]ry1
和r
y2
各自独立地选自氢和c
1-c6烷基;
[0182]rz1
和r
z2
都是氢
[0183]
或
[0184]rz1
和r
z2
中的1个以及r
y1
和r
y2
中的1个一起形成c
1-c2亚烷基桥接基团,并且r
z1
和r
z2
以及r
y1
和r
y2
中的另一个都是氢;
[0185]
r1选自氢和c
1-c6烷基;
[0186]
r2选自氢、-c(=o)-r3、c
3-c8环烷基、c
1-c6卤代烷基、和c
1-c
10
烷基,其中所述烷基被独立地选自以下的0-1个取代基取代:c
6-c
10
芳基,包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基,包含独立地选自n、o和s的1-2个杂原子的4元至11元杂环基,c
3-c8环烷基和-o-(r
2a
),
[0187]
其中所述芳基、杂芳基、杂环基和环烷基各自独立地被0-5个r4取代;
[0188]r2a
是c
1-c6烷基,其中所述烷基被独立地选自c
6-c
10
芳基的0-1个取代基取代;
[0189]
r3选自-ch=cr
3ar3b
,c
6-c
10
芳基,包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基,包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基,c
3-c8环烷基,和c
1-c6烷基,其中所述烷基被0-3个r
3c
取代,并且
[0190]
其中所述芳基、杂芳基、杂环基和环烷基各自独立地被0-5个r4取代;
[0191]r3a
和r
3b
连同它们所附接的碳原子一起形成c
3-c8环烷基环;
[0192]
每个r
3c
在每次出现时独立地选自-c(=o)-r
3d
,nr
3er3f
,c
1-c6烷氧基,-o-r
3d
,羟基,-o-c
6-c
10
芳基,c
1-c6芳基c
6-c
10
烷基-o-,-o-(包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基),c
6-c
10
芳基,包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基,包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基,和c
3-c8环烷基,
[0193]
其中所述-o-芳基、芳基烷基-o-、和-o-杂芳基各自独立地被0-3个r
4a
取代,并且
[0194]
其中所述芳基、杂芳基、杂环基和环烷基各自独立地被0-5个r4取代;
[0195]r3d
是包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基;
[0196]r3e
和r
3f
各自独立地选自氢和c
1-c6烷基;
[0197]
每个r4在每次出现时独立地选自c
6-c
10
芳基,-o-c
6-c
10
芳基,c
1-c6芳基c
6-c
10
烷基-o-,-o-(包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基),包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基,包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基,c
1-c
10
烷基,c
1-c6烷氧基,c
1-c6卤代烷基,-so2r
4c
,卤素,羟基,-cn,-o-包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基,氧代,c
1-c6卤代烷氧基,-c(=o)-o-(r5),-c(=o)-(r5),-c(=o)-nr
6ar6b
,nr
6ar6b
,-nh-c(=o)-o-(c
1-c6烷基),和c
3-c8环烷基,其中所述芳基、-o-芳基、芳基烷基-o-、-o-杂芳基、杂芳基和杂环基各自独立地被0-3个r
4a
取代,
[0198]
其中所述烷基和烷氧基各自独立地被0-1个r
4b
取代,并且
[0199]
其中所述环烷基被各自独立地选自以下的0-3个取代基取代:-cn、c
1-c6烷基、c
1-c6烷氧基、羟基和c
1-c6卤代烷基;
[0200]r4a
在每次出现时独立地选自-cn,c
1-c6烷氧基,c
1-c6卤代烷基,卤素,羟基,-c(=o)-o-(r5),包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基,二(c
1-c6烷基)氨基c
1-c6烷基,c
1-c6烷基,包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基,和c
3-c6环烷基,其中所述烷基被0-1个r
4b
取代,并且其中所述杂芳基被0-3个r
4a-1
取代;
[0201]r4a-1
在每次出现时独立地选自c
1-c6烷基、二(c
1-c6烷基)氨基c
1-c6烷基、-cn、c
1-c6烷氧基、和c
1-c6卤代烷基;
[0202]r4b
在每次出现时独立地选自-cn,卤素,-c(=o)nr
6ar6b
,nr
6ar6b
,包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基,-c(=o)-oh,c
1-c6烷氧基,包含独立地选自n、o和s的1个或2个杂原子的4元至6元杂环基,c
3-c8环烷基,c
2-c4炔基,和c
6-c
10
芳基,其中所述芳基被各自独立地选自以下的0-1个取代基取代:-cn、c
1-c6卤代烷基、和c
1-c6烷基;
[0203]r4c
选自c
6-c
10
芳基、羟基、nh2、和卤素;
[0204]
r5选自c
1-c6烷基、c
6-c
10
芳基、和c
6-c
10
芳基c
1-c6烷基;
[0205]r6a
和r
6b
各自独立地选自氢和c
1-c6烷基;
[0206]
或r
6a
和r
6b
连同它们所附接的氮原子一起形成包含选自n、o和s的0-1个另外的杂原子的5元或6元杂环基,其中所述杂环基被0-2个r
6c
取代;
[0207]r6c
在每次出现时独立地选自c
6-c
10
芳基c
1-c6烷基、-c(=o)-o-(c
1-c6烷基)、-c(=o)-(c
1-c6烷基)、氧代和c
1-c6烷基,其中所述烷基被独立地选自以下的0-1个取代基取代:-cn和包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基。
[0208]
实施例2.根据权利要求1所述的具有式(i’)的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其中:z是1;并且r
z1
和r
z2
中的1个以及r
y1
和r
y2
中的1个一起形成c
1-c2亚烷基桥接基团,并且r
z1
和r
z2
以及r
y1
和r
y2
中的另一个都是氢。
[0209]
实施例3.根据权利要求1或2所述的具有式(i’)的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其中:z是1;并且r
z1
和r
z2
中的1个以及r
y1
和r
y2
中的1个一起形成c1亚烷基桥接基团,并且r
z1
和r
z2
以及r
y1
和r
y2
中的另一个都是氢。
[0210]
实施例4.根据实施例1所述的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其具有式(i)
[0211][0212]
其中:
[0213]
y选自o、ch2、和cf2;
[0214]
z是从0至2的整数;
[0215]rx1
和r
x2
各自独立地选自氢和c
1-c6烷基;
[0216]ry1
和r
y2
各自独立地选自氢和c
1-c6烷基;
[0217]
r1选自氢和c
1-c6烷基;
[0218]
r2选自氢、-c(=o)-r3、c
3-c8环烷基、c
1-c6卤代烷基、和c
1-c
10
烷基,其中所述烷基被独立地选自以下的0-1个取代基取代:c
6-c
10
芳基,包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基,包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基,和c
3-c8环烷基,
[0219]
其中所述芳基、杂芳基、杂环基和环烷基各自独立地被0-5个r4取代;
[0220]
r3选自-ch=cr
3ar3b
,c
6-c
10
芳基,包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基,包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基,c
3-c8环烷基,和c
1-c6烷基,其中所述烷基被0-3个r
3c
取代,并且
[0221]
其中所述芳基、杂芳基、杂环基和环烷基各自独立地被0-5个r4取代;
[0222]r3a
和r
3b
连同它们所附接的碳原子一起形成c
3-c8环烷基环;
[0223]
每个r
3c
在每次出现时独立地选自-c(=o)-r
3d
,nr
3er3f
,c
1-c6烷氧基,-o-r
3d
,羟基,-o-c
6-c
10
芳基,c
1-c6芳基c
6-c
10
烷基-o-,-o-(包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基),c
6-c
10
芳基,包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基,包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基,和c
3-c8环烷基,
[0224]
其中所述-o-芳基、芳基烷基-o-、和-o-杂芳基各自独立地被0-3个r
4a
取代,并且
[0225]
其中所述芳基、杂芳基、杂环基和环烷基各自独立地被0-5个r4取代;
[0226]r3d
是包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基;
[0227]r3e
和r
3f
各自独立地选自氢和c
1-c6烷基;
[0228]
每个r4在每次出现时独立地选自c
6-c
10
芳基,-o-c
6-c
10
芳基,c
1-c6芳基c
6-c
10
烷基-o-,-o-(包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基),包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基,包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基,c
1-c
10
烷基,c
1-c6烷氧基,c
1-c6卤代烷基,-so2r
4c
,卤素,羟基,-cn,-o-包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基,氧代,c
1-c6卤代烷氧基,-c(=o)-o-(r5),-c
(=o)-(r5),-c(=o)-nr
6ar6b
,nr
6ar6b
,-nh-c(=o)-o-(c
1-c6烷基),和c
3-c8环烷基,其中所述芳基、-o-芳基、芳基烷基-o-、-o-杂芳基、杂芳基和杂环基各自独立地被0-3个r
4a
取代,
[0229]
其中所述烷基和烷氧基各自独立地被0-1个r
4b
取代,并且
[0230]
其中所述环烷基被各自独立地选自以下的0-3个取代基取代:-cn、c
1-c6烷基、c
1-c6烷氧基、和羟基;
[0231]r4a
在每次出现时独立地选自-cn,c
1-c6烷氧基,c
1-c6卤代烷基,卤素,羟基,-c(=o)-o-(r5),包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基,二(c
1-c6烷基)氨基c
1-c6烷基,和c
1-c6烷基,其中所述烷基被0-1个r
4b
取代,并且其中所述杂芳基被0-3个r
4a-1
取代;
[0232]r4a-1
在每次出现时独立地选自c
1-c6烷基、二(c
1-c6烷基)氨基c
1-c6烷基、-cn、c
1-c6烷氧基、和c
1-c6卤代烷基;
[0233]r4b
在每次出现时独立地选自-cn,-c(=o)nr
6ar6b
,nr
6ar6b
,包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基,-c(=o)-oh,c
1-c6烷氧基,包含独立地选自n、o和s的1个或2个杂原子的4元至6元杂环基,c
3-c8环烷基,c
2-c4炔基,和c
6-c
10
芳基,其中所述芳基被各自独立地选自以下的0-1个取代基取代:-cn、c
1-c6卤代烷基、和c
1-c6烷基;
[0234]r4c
选自c
6-c
10
芳基、羟基、nh2、和卤素;
[0235]
r5选自c
1-c6烷基、c
6-c
10
芳基、和c
6-c
10
芳基c
1-c6烷基;
[0236]r6a
和r
6b
各自独立地选自氢和c
1-c6烷基;
[0237]
或r
6a
和r
6b
连同它们所附接的氮原子一起形成包含选自n、o和s的0-1个另外的杂原子的5元或6元杂环基,其中所述杂环基被0-2个r
6c
取代;
[0238]r6c
在每次出现时独立地选自c
6-c
10
芳基c
1-c6烷基、-c(=o)-o-(c
1-c6烷基)、-c(=o)-(c
1-c6烷基)、氧代和c
1-c6烷基,其中所述烷基被独立地选自以下的0-1个取代基取代:-cn和包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基。
[0239]
实施例5.根据实施例1或4所述的化合物或其药学上可接受的盐,其具有式(i-i)
[0240][0241]
其中r
x1
、r
x2
、r
y1
、r
y2
、r1、r2和z是根据前述实施例中任一项定义的。
[0242]
实施例6.根据实施例1、4或5所述的化合物或其药学上可接受的盐,其具有式(i-i-a)或(i-i-b)
[0243][0244]
其中r
x1
、r
x2
、r
y1
、r
y2
、r1、r2和z是根据前述实施例中任一项定义的。
[0245]
实施例7.根据实施例1、4至6所述的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其具有式(i-i-c)或(i-i-d)
[0246][0247]
其中r
x1
、r
x2
、r
y1
、r
y2
、r1、r2和z是根据前述实施例中任一项定义的。
[0248]
实施例8.根据实施例1、4至6所述的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其具有式(i-i-e)或(i-i-f)
[0249][0250]
其中r
x1
、r
x2
、r
y1
、r
y2
、r1、r2和z是根据前述实施例中任一项定义的。
[0251]
实施例9.根据实施例1或4所述的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其具有式(i-ii)
[0252][0253]
(i-ii),其中r
x1
、r
x2
、r
y1
、r
y2
、r1、r2和z是根据前述实施例中任一项定义的。
[0254]
实施例10.根据实施例1、4、9所述的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其具有式(i-ii-a)或(i-ii-b)
[0255][0256]
其中r
x1
、r
x2
、r
y1
、r
y2
、r1、r2和z是根据前述实施例中任一项定义的。
[0257]
实施例11.根据实施例1、4、9、10所述的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其具有式(i-ii-c)或(i-ii-d)
[0258][0259]
其中r
x1
、r
x2
、r
y1
、r
y2
、r1、r2和z是根据前述实施例中任一项定义的。
[0260]
实施例12.根据实施例1、4、9、10所述的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其具有式(i-ii-e)或(i-ii-f)
[0261][0262]
其中r
x1
、r
x2
、r
y1
、r
y2
、r1、r2和z是根据前述实施例中任一项定义的。
[0263]
实施例13.根据前述实施例中任一项所述的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,
[0264]
其中:
[0265]
y选自o、ch2、和cf2;
[0266]
z是从0至2的整数;
[0267]rx1
和r
x2
各自独立地选自氢和c
1-c6烷基;
[0268]ry1
和r
y2
各自独立地选自氢和c
1-c6烷基;
[0269]
r1选自氢和c
1-c6烷基;
[0270]
r2选自氢、-c(=o)-r3、c
3-c8环烷基、和c
1-c
10
烷基,其中所述烷基被独立地选自以下的0-1个取代基取代:c
6-c
10
芳基,包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基,包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基,和c
3-c8环烷基,
[0271]
并且其中所述芳基、杂芳基、杂环基和环烷基各自独立地被0-5个r4取代;
[0272]
r3选自c
6-c
10
芳基,包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基,包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基,c
3-c8环烷基,和c
1-c6烷基,其中所述烷基被0-3个r
3c
取代,并且
[0273]
其中所述芳基、杂芳基、杂环基和环烷基各自独立地被0-5个r4取代;
[0274]r3c
在每次出现时独立地选自nr
3er3f
,c
1-c6烷氧基,-o-r
3d
,羟基,-o-c
6-c
10
芳基,c
1-c6芳基c
6-c
10
烷基-o-,-o-(包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基),c
6-c
10
芳基,包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基,包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基,和c
3-c8环烷基,
[0275]
其中所述-o-芳基、芳基烷基-o-、和-o-杂芳基各自独立地被0-3个r
4a
取代,并且
[0276]
其中所述芳基、杂芳基、杂环基和环烷基各自独立地被0-5个r4取代;
[0277]r3d
是包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基;
[0278]r3e
和r
3f
各自独立地选自氢和c
1-c6烷基;
[0279]
r4在每次出现时独立地选自c
6-c
10
芳基,-o-c
6-c
10
芳基,c
1-c6芳基c
6-c
10
烷基-o-,-o-(包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基),包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基,包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基,c
1-c
10
烷基,c
1-c6烷氧基,c
1-c6卤代烷基,-so2r
4c
,卤素,羟基,-cn,-o-包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基,氧代,c
1-c6卤代烷氧基,-c(=o)-o-(r5),-c(=
o)-(r5),-c(=o)-nr
6ar6b
,nr
6ar6b
,-nh-c(=o)-o-(c
1-c6烷基),和c
3-c8环烷基,其中所述芳基、-o-芳基、芳基烷基-o-、-o-杂芳基、杂芳基和杂环基各自独立地被0-3个r
4a
取代,
[0280]
其中所述烷基和烷氧基各自独立地被0-1个r
4b
取代,并且
[0281]
其中所述环烷基被各自独立地选自以下的0-2个取代基取代:-cn、c
1-c6烷基、和c
1-c6烷氧基;
[0282]r4a
在每次出现时独立地选自-cn,c
1-c6烷氧基,c
1-c6卤代烷基,卤素,羟基,-c(=o)-o-(r5),包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基,二(c
1-c6烷基)氨基c
1-c6烷基,和c
1-c6烷基,其中所述烷基被0-1个r
4b
取代,并且其中所述杂芳基被0-3个r
4a-1
取代;
[0283]r4a-1
在每次出现时独立地选自c
1-c6烷基、二(c
1-c6烷基)氨基c
1-c6烷基、-cn、c
1-c6烷氧基、和c
1-c6卤代烷基;
[0284]r4b
在每次出现时独立地选自-cn,-c(=o)nr
6ar6b
,nr
6ar6b
,包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基,-c(=o)-oh,c
1-c6烷氧基,包含独立地选自n、o和s的1个或2个杂原子的4元至6元杂环基,c
3-c8环烷基,c
2-c4炔基,和c
6-c
10
芳基,其中所述芳基被各自独立地选自以下的0-1个取代基取代:-cn、c
1-c6卤代烷基、和c
1-c6烷基;
[0285]r4c
选自c
6-c
10
芳基、羟基、nh2、和卤素;
[0286]
r5选自c
1-c6烷基、c
6-c
10
芳基、和c
6-c
10
芳基c
1-c6烷基;
[0287]r6a
和r
6b
各自独立地选自氢和c
1-c6烷基;
[0288]
或r
6a
和r
6b
连同它们所附接的氮原子一起形成包含选自n、o和s的0-1个另外的杂原子的5元或6元杂环基,其中所述杂环基被0-2个r
6c
取代;
[0289]r6c
在每次出现时独立地选自c
6-c
10
芳基c
1-c6烷基、-c(=o)-o-(c
1-c6烷基)、-c(=o)-(c
1-c6烷基)、氧代和c
1-c6烷基,其中所述烷基被独立地选自以下的0-1个取代基取代:-cn和包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基。
[0290]
实施例14.根据前述实施例中任一项所述的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,
[0291]
其中:
[0292]
y选自o和ch2;
[0293]
z是从0至2的整数;
[0294]rx1
和r
x2
各自独立地选自氢和c
1-c6烷基;
[0295]ry1
和r
y2
各自独立地选自氢和c
1-c6烷基;
[0296]
r1选自氢和c
1-c6烷基;
[0297]
r2选自氢、-c(=o)-r3、c
3-c8环烷基、和c
1-c
10
烷基,其中所述烷基被独立地选自以下的0-1个取代基取代:c
6-c
10
芳基,包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基,包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基,和c
3-c8环烷基,
[0298]
并且其中所述芳基、杂芳基、杂环基和环烷基各自独立地被0-5个r4取代;
[0299]
r3选自c
6-c
10
芳基,包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基,包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基,c
3-c8环烷基,和c
1-c6烷基,其中所述烷基被0-3个r
3c
取代,并且
[0300]
其中所述芳基、杂芳基、杂环基和环烷基各自独立地被0-5个r4取代;
[0301]r3c
在每次出现时独立地选自二(c
1-c6烷基)氨基,c
1-c6烷氧基,-o-c
6-c
10
芳基,c
1-c6芳基c
6-c
10
烷基-o-,-o-(包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基),c
6-c
10
芳基,包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基,包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基,和c
3-c8环烷基,
[0302]
其中所述-o-芳基、芳基烷基-o-、和-o-杂芳基各自独立地被0-3个r
4a
取代,并且
[0303]
其中所述芳基、杂芳基、杂环基和环烷基各自独立地被0-5个r4取代;
[0304]
r4在每次出现时独立地选自c
6-c
10
芳基,-o-c
6-c
10
芳基,c
1-c6芳基c
6-c
10
烷基-o-,-o-(包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基),包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基,包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基,c
1-c
10
烷基,c
1-c6烷氧基,c
1-c6卤代烷基,-so2r
4c
,卤素,羟基,-cn,-o-包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基,氧代,c
1-c6卤代烷氧基,-c(=o)-o-(r5),-c(=o)-(r5),-c(=o)-nr
6ar6b
,nr
6ar6b
,-nh-c(=o)-o-(c
1-c6烷基),和c
3-c8环烷基,其中所述芳基、-o-芳基、芳基烷基-o-、-o-杂芳基、杂芳基和杂环基各自独立地被0-3个r
4a
取代,
[0305]
其中所述烷基和烷氧基各自独立地被0-1个r
4b
取代,并且
[0306]
其中所述环烷基被各自独立地选自以下的0-2个取代基取代:-cn、c
1-c6烷基、甲氧基、和乙氧基;
[0307]r4a
在每次出现时独立地选自-cn,c
1-c6烷氧基,c
1-c6卤代烷基,卤素,羟基,-c(=o)-o-(r5),包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基,二(c
1-c6烷基)氨基c
1-c6烷基,和c
1-c6烷基,其中所述烷基被0-1个r
4b
取代,并且其中所述杂芳基被0-3个r
4a-1
取代;
[0308]r4a-1
在每次出现时独立地选自c
1-c6烷基、二(c
1-c6烷基)氨基c
1-c6烷基、-cn、c
1-c6烷氧基、和c
1-c6卤代烷基;
[0309]r4b
在每次出现时独立地选自-cn,-c(=o)nr
6ar6b
,nr
6ar6b
,包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基,-c(=o)-oh,c
1-c6烷氧基,包含独立地选自n、o和s的1个或2个杂原子的4元至6元杂环基,c
3-c8环烷基,c
2-c4炔基,和c
6-c
10
芳基,其中所述芳基被各自独立地选自以下的0-1个取代基取代:-cn、c
1-c6卤代烷基、和c
1-c6烷基;
[0310]r4c
选自c
6-c
10
芳基、羟基、nh2、和卤素;
[0311]
r5选自c
1-c6烷基、c
6-c
10
芳基、和c
6-c
10
芳基c
1-c6烷基;
[0312]r6a
和r
6b
各自独立地选自氢和c
1-c6烷基;
[0313]
或r
6a
和r
6b
连同它们所附接的氮原子一起形成包含选自n、o和s的0-1个另外的杂原子的5元或6元杂环基,其中所述杂环基被0-2个r
6c
取代;
[0314]r6c
在每次出现时独立地选自c
6-c
10
芳基c
1-c6烷基、-c(=o)-o-(c
1-c6烷基)、-c(=o)-(c
1-c6烷基)、氧代和c
1-c6烷基,其中所述烷基被独立地选自以下的0-1个取代基取代:-cn和包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基。
[0315]
实施例15.根据前述实施例中任一项所述的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,
[0316]
其中:
[0317]
y选自o和ch2;
[0318]
z是从0至2的整数;
[0319]rx1
和r
x2
各自独立地选自氢和c
1-c6烷基;
[0320]ry1
和r
y2
各自独立地选自氢和c
1-c6烷基;
[0321]
其中当r
x1
和r
x2
都是c
1-c6烷基时,则r
y1
和r
y2
都是氢,并且其中当r
x1
和r
x2
都是氢时,则r
y1
和r
y2
都是c
1-c6烷基;
[0322]
r1选自氢和c
1-c6烷基;
[0323]
r2选自氢、-c(=o)-r3、c
3-c8环烷基、和c
1-c6烷基,其中所述烷基被独立地选自以下的0-1个取代基取代:c
6-c
10
芳基,包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基,包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基,和c
3-c8环烷基,
[0324]
并且其中所述芳基、杂芳基、杂环基和环烷基各自独立地被0-5个r4取代;
[0325]
r3选自c
6-c
10
芳基,包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基,和c
3-c8环烷基,和c
1-c3烷基,其中所述烷基被0-2个r
3c
取代,并且
[0326]
其中所述芳基、杂芳基和环烷基各自独立地被0-5个r4取代;
[0327]r3c
在每次出现时独立地选自c
6-c
10
芳基,包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基,和c
3-c8环烷基,
[0328]
其中所述芳基、杂芳基和环烷基各自独立地被0-5个r4取代;
[0329]
r4在每次出现时独立地选自c
6-c
10
芳基,-o-c
6-c
10
芳基,c
1-c6芳基c
6-c
10
烷基-o-,-o-(包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基),包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基,包含独立地选自n和o的1-2个杂原子的4元至6元杂环基,c
1-c
10
烷基,c
1-c6烷氧基,c
1-c6卤代烷基,-so2r
4c
,卤素,羟基,-cn,氧代,c
1-c6卤代烷氧基,-c(=o)-o-(r5),-c(=o)-nr
6ar6b
,nr
6ar6b
,-nh-c(=o)-o-(c
1-c6烷基),和c
3-c8环烷基,其中所述芳基、-o-芳基、芳基烷基-o-、-o-杂芳基、杂芳基和杂环基各自独立地被0-3个r
4a
取代,
[0330]
其中所述烷基和烷氧基各自独立地被0-1个r
4b
取代,并且
[0331]
其中所述环烷基被独立地选自-cn的0-1个取代基取代;
[0332]r4a
在每次出现时独立地选自-cn,c
1-c6烷氧基,c
1-c6卤代烷基,卤素,羟基,-c(=o)-o-(r5),包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基,二(c
1-c6烷基)氨基c
1-c6烷基,和c
1-c6烷基,其中所述烷基被0-1个r
4b
取代,并且其中所述杂芳基被0-3个r
4a-1
取代;
[0333]r4a-1
在每次出现时独立地选自c
1-c6烷基、二(c
1-c6烷基)氨基c
1-c6烷基、-cn、c
1-c6烷氧基、和c
1-c6卤代烷基;
[0334]r4b
在每次出现时独立地选自-cn,-c(=o)nr
6ar6b
,包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基,-c(=o)-oh,包含独立地选自n、o和s的1个或2个杂原子的4元至6元杂环基,c
3-c8环烷基,c
2-c4炔基,和c
6-c
10
芳基,其中所述芳基被各自独立地选自以下的0-1个取代基取代:-cn、c
1-c6卤代烷基、和c
1-c6烷基;
[0335]r4c
选自c
6-c
10
芳基、nh2、和卤素;
[0336]
r5选自c
1-c6烷基、和c
6-c
10
芳基c
1-c6烷基;
[0337]r6a
和r
6b
各自独立地选自氢和c
1-c6烷基;
[0338]
或r
6a
和r
6b
连同它们所附接的氮原子一起形成包含选自n和o的0-1个另外的杂原子的5元或6元杂环基,其中所述杂环基被0-2个r
6c
取代;
[0339]r6c
在每次出现时独立地选自c
6-c
10
芳基c
1-c6烷基、-c(=o)-o-(c
1-c6烷基)、-c(=
o)-(c
1-c6烷基)、氧代和c
1-c6烷基,其中所述烷基被独立地选自以下的0-1个取代基取代:包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基。
[0340]
实施例16.根据前述实施例中任一项所述的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,
[0341]
其中:
[0342]
y选自o和ch2;
[0343]
z是从0至2的整数;
[0344]rx1
和r
x2
各自独立地选自氢和c
1-c6烷基;
[0345]ry1
和r
y2
各自独立地选自氢和c
1-c6烷基;
[0346]
其中当r
x1
和r
x2
都是c
1-c6烷基时,则r
y1
和r
y2
都是氢,并且其中当r
x1
和r
x2
都是氢时,则r
y1
和r
y2
都是c
1-c6烷基;
[0347]
r1选自氢和c
1-c6烷基;
[0348]
r2选自c
3-c8环烷基,c
1-c6烷基,-(ch2)
1-2-c
6-c
10
芳基,-(ch2)
1-2-包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基,-(ch2)
1-2-包含独立地选自n和o的1-2个杂原子的4元至6元杂环基,和-(ch2)
1-2-c
3-c8环烷基,
[0349]
并且其中所述芳基、杂芳基、杂环基和环烷基各自独立地被0-4个r4取代;
[0350]
r4在每次出现时独立地选自c
6-c
10
芳基,-o-c
6-c
10
芳基,-o-(包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基),包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基,包含独立地选自n和o的1-2个杂原子的4元至6元杂环基,c
1-c
10
烷基,c
1-c6烷氧基,c
1-c6卤代烷基,-so2r
4c
,卤素,羟基,-cn,氧代,c
1-c6卤代烷氧基,-c(=o)-o-(r5),-c(=o)-nr
6ar6b
,nr
6ar6b
,-nh-c(=o)-o-(c
1-c6烷基),和c
3-c8环烷基,其中所述芳基、-o-芳基、-o-杂芳基、杂芳基和杂环基各自独立地被0-3个r
4a
取代,
[0351]
其中所述烷基和烷氧基各自独立地被0-1个r
4b
取代,并且
[0352]
其中所述环烷基被独立地选自-cn的0-1个取代基取代;
[0353]r4a
在每次出现时独立地选自-cn,c
1-c6烷氧基,c
1-c6卤代烷基,卤素,-c(=o)-o-(r5),包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基,和c
1-c6烷基,其中所述烷基被0-1个r
4b
取代,并且其中所述杂芳基被0-2个r
4a-1
取代;
[0354]r4a-1
在每次出现时独立地选自c
1-c6烷基、和二(c
1-c6烷基)氨基c
1-c6烷基;
[0355]r4b
在每次出现时独立地选自-c(=o)nr
6ar6b
,包含独立地选自n和o的1-4个杂原子的5元至10元杂芳基,-c(=o)-oh,包含独立地选自n、o和s的1个或2个杂原子的4元至6元杂环基,和c
6-c
10
芳基,其中所述芳基被各自独立地选自以下的0-1个取代基取代:-cn和c
1-c6卤代烷基;
[0356]r4c
选自c
6-c
10
芳基、和nh2;
[0357]
r5选自c
1-c6烷基、和c
6-c
10
芳基c
1-c6烷基;
[0358]r6a
和r
6b
各自独立地选自氢和c
1-c6烷基;
[0359]
或r
6a
和r
6b
连同它们所附接的氮原子一起形成包含选自n和o的0-1个另外的杂原子的5元或6元杂环基,其中所述杂环基被0-1个r
6c
取代;
[0360]r6c
在每次出现时独立地选自c
6-c
10
芳基c
1-c6烷基、-c(=o)-o-(c
1-c6烷基)、氧代、和c
1-c6烷基,其中所述烷基被独立地选自以下的0-1个取代基取代:包含独立地选自n、o和s
的1-2个杂原子的4元至6元杂环基。
[0361]
实施例17.根据前述实施例中任一项所述的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,
[0362]
其中:
[0363]
y选自o和ch2;
[0364]
z是从0至2的整数;
[0365]rx1
和r
x2
各自独立地选自氢和c
1-c6烷基;
[0366]ry1
和r
y2
各自独立地选自氢和c
1-c6烷基;
[0367]
其中当r
x1
和r
x2
都是c
1-c6烷基时,则r
y1
和r
y2
都是氢,并且其中当r
x1
和r
x2
都是氢时,则r
y1
和r
y2
都是c
1-c6烷基;
[0368]
r1选自氢和c
1-c6烷基;
[0369]
r2选自c
1-c6烷基,-(ch2)-苯基,-(ch2)-包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基,-(ch2)-包含独立地选自n和o的1个杂原子的6元杂环基,和-(ch2)-c
3-c8环烷基,
[0370]
并且其中所述苯基、杂芳基、杂环基和环烷基各自独立地被0-3个r4取代;
[0371]
r4在每次出现时独立地选自苯基,-o-苯基,-o-(包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基),包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基,包含独立地选自n和o的1-2个杂原子的6元杂环基,c
1-c
10
烷基,c
1-c6烷氧基,c
1-c6氟烷基,-so2r
4c
,卤素,羟基,-cn,氧代,c
1-c6氟烷氧基,-c(=o)-o-(r5),-c(=o)-nr
6ar6b
,nr
6ar6b
,-nh-c(=o)-o-(c
1-c6烷基),和c
3-c8环烷基,其中所述苯基、-o-苯基、-o-杂芳基、杂芳基和杂环基各自独立地被0-3个r
4a
取代,
[0372]
其中所述烷基和烷氧基各自独立地被0-1个r
4b
取代,并且
[0373]
其中所述环烷基被独立地选自-cn的0-1个取代基取代;
[0374]r4a
在每次出现时独立地选自c
1-c6氟烷基,氟,-c(=o)-o-(r5),包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基,和c
1-c6烷基,其中所述烷基被0-1个r
4b
取代,并且其中所述杂芳基被0-2个r
4a-1
取代;
[0375]r4a-1
在每次出现时独立地选自c
1-c6烷基、和二(c
1-c6烷基)氨基c
1-c6烷基;
[0376]r4b
在每次出现时独立地选自-c(=o)nr
6ar6b
,包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基,-c(=o)-oh,包含独立地选自n和o的1个或2个杂原子的4元至6元杂环基,和苯基,其中所述苯基被各自独立地选自-cn的0-1个取代基取代;
[0377]r4c
选自苯基和nh2;
[0378]
r5选自c
1-c6烷基和苄基;
[0379]r6a
和r
6b
各自独立地选自氢和c
1-c6烷基;
[0380]
或r
6a
和r
6b
连同它们所附接的氮原子一起形成包含选自n和o的0-1个另外的杂原子的5元或6元杂环基,其中所述杂环基被0-1个r
6c
取代;
[0381]r6c
在每次出现时独立地选自苄基、-c(=o)-o-(c
1-c6烷基)、氧代、和c
1-c6烷基,其中所述烷基被独立地选自以下的0-1个取代基取代:包含1个o杂原子的4元杂环基。
[0382]
实施例18.根据前述实施例中任一项所述的化合物或者其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其中r3选自苯基,包含独立地选自n、o和
s的1-4个杂原子的5元至10元杂芳基,包含独立地选自n和o的1-2个杂原子的4元至6元杂环基,c
3-c6环烷基,和c
1-c6烷基,其中所述烷基被0-3个r
3c
取代,并且
[0383]
其中所述苯基、杂芳基、杂环基和环烷基各自独立地被0-4个r4取代。
[0384]
实施例19.根据前述实施例中任一项所述的化合物或者其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其中r3选自苯基,包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基,包含独立地选自n和o的1-2个杂原子的4元至6元杂环基,c
3-c6环烷基,和c
1-c6烷基,其中所述烷基被0-1个r
3c
取代,
[0385]
其中所述苯基、杂芳基、杂环基和环烷基各自独立地被0-4个r4取代,并且
[0386]
其中r
3c
在每次出现时独立地选自苯基,包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基,包含独立地选自n和o的1-2个杂原子的4元至6元杂环基,和c
3-c6环烷基。
[0387]
实施例20.根据前述实施例中任一项所述的化合物或者其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其中r3选自苯基,包含独立地选自n、o和s的1-4个杂原子的5-10元杂芳基,包含独立地选自n、o和s的1-2个杂原子的4元、5元或6元杂环基,c
3-c8环烷基,-(ch2)
1-2-苯基,-(ch2)
1-2-包含独立地选自n、o和s的1-4个杂原子的5-10元杂芳基,-(ch2)
1-2-包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基,和-(ch2)
1-2-c
3-c8环烷基。
[0388]
实施例21.根据前述实施例中任一项所述的化合物或者其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其中每个r4在每次出现时独立地选自c
6-c
10
芳基,-o-c
6-c
10
芳基,c
1-c6芳基c
6-c
10
烷基-o-,-o-(包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基),包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基,包含独立地选自n和o的1-2个杂原子的4元至6元杂环基,c
1-c
10
烷基,c
1-c6烷氧基,c
1-c6卤代烷基,-so2r
4c
,卤素,羟基,-cn,-o-包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基,氧代,c
1-c6卤代烷氧基,-c(=o)-o-(r5),-c(=o)-(r5),-c(=o)-nr
6ar6b
,nr
6ar6b
,-nh-c(=o)-o-(c
1-c6烷基),和c
3-c8环烷基,其中所述芳基、杂芳基、和杂环基各自独立地被0-2个r
4a
取代,其中所述-o-芳基、芳基烷基-o-、和-o-杂芳基各自独立地被0-3个r
4a
取代,
[0389]
其中所述烷基和烷氧基各自独立地被0-1个r
4b
取代,并且
[0390]
其中所述环烷基被各自独立地选自以下的0-2个取代基取代:-cn、c
1-c6烷基、甲氧基和乙氧基。
[0391]
实施例22.根据前述实施例中任一项所述的化合物或者其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其中每个r4在每次出现时独立地选自苯基,-o-苯基,苄基-o-,-o-(包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基),包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基,包含独立地选自n和o的1-2个杂原子的4元至6元杂环基,c
1-c8烷基,c
1-c6烷氧基,c
1-c6卤代烷基,-so2r
4c
,卤素,羟基,-cn,-o-包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基,氧代,c
1-c6卤代烷氧基,-c(=o)-o-(r5),-c(=o)-nr
6ar6b
,nr
6ar6b
,-nh-c(=o)-o-(c
1-c6烷基),和c
3-c8环烷基,
[0392]
其中所述烷基和烷氧基各自独立地被0-1个r
4b
取代,
[0393]
其中所述环烷基被各自独立地选自以下的0-2个取代基取代:-cn、c
1-c6烷基、甲氧基和乙氧基,
[0394]
其中所述苯基和杂芳基各自独立地被独立地选自以下的0-2个取代基取代:-cn、c1-c6烷基、c
1-c6烷氧基、c
1-c6卤代烷基和氢,
[0395]
其中所述杂环基独立地被各自独立地选自以下的0-2个取代基取代:-c(=o)-o-(r5)和c
1-c6烷基,其中所述烷基独立地被独立地选自以下的0-1个取代基取代:c
6-c
10
芳基和包含独立地选自n和o的1-2个杂原子的4元至6元杂环基,
[0396]
并且其中所述-o-苯基、苄基-o-、和-o-杂芳基各自独立地被各自独立地选自以下的0-3个取代基取代:羟基、-c(=o)-o-(r5)、卤素、c
1-c6烷基,其中所述烷基独立地被独立地选自以下的0-1个取代基取代:-c(=o)-nr
6ar6b
、和nr
6ar6b
、
[0397]
和包含独立地选自n、o和s的1-4个杂原子的5-10元杂芳基,其中杂芳基被各自独立地选自以下的0-2个取代基取代:c
1-c6烷基和二(c
1-c6烷基)氨基c
1-c6烷基。
[0398]
实施例23.根据前述实施例中任一项所述的化合物或者其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其中r2是未经取代的c
1-c6烷基,或被包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基取代的c
1-c
10
烷基(例如c
1-c6烷基,例如c1烷基),或-c(=o)-r3,
[0399]
其中r3是包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基,或被包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基取代的c
1-c6烷基,
[0400]
其中所述杂芳基在每次出现时独立地选自吲哚基、咪唑并吡啶基、异喹啉基、苯并噁唑酮基、吡啶基、嘧啶基、吡啶酮基、苯并三唑基、哒嗪基、吡唑并三嗪基、吲唑基、苯并咪唑基、喹啉基、三唑基、吡唑基、噻唑基、噁唑基、异噁唑基、吡咯基、噁二唑基、咪唑基、吡咯并吡啶基、四氢吲唑基、喹喔啉基、噻二唑基、吡嗪基、噁唑并吡啶基、吡唑并嘧啶基、苯并噁唑基、二氢吲哚基、异噁唑并吡啶基、二氢吡啶并噁嗪基和四唑基,
[0401]
并且其中所述杂芳基在每次出现时独立地被0-4个r4取代,其中r4如根据前述实施例中任一项所定义。
[0402]
实施例24.根据前述实施例中任一项所述的化合物或者其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其中r2是未经取代的c
1-c6烷基,或被包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基取代的c
1-c
10
烷基(例如c
1-c6烷基,例如c1烷基),或-c(=o)-r3,
[0403]
其中r3是包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基,或被包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基取代的c
1-c6烷基,
[0404]
其中所述杂芳基在每次出现时独立地选自:
[0405][0406][0407]
并且其中所述杂芳基在每次出现时独立地被0-4个r4取代,其中r4如根据前述实施例中任一项所定义。
[0408]
实施例25.根据前述实施例中任一项所述的化合物或者其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其中r2是未经取代的c
1-c6烷基,或被包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基取代的c
1-c
10
烷基(例如c
1-c6烷基,例如c1烷基),或-c(=o)-r3,
[0409]
其中r3是包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基,或被包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基取代的c
1-c6烷基,
[0410]
其中所述杂芳基在每次出现时独立地选自:
[0411][0412]
并且其中所述杂芳基在每次出现时独立地被0-3个r4取代,其中r4如根据前述实施例中任一项所定义。
[0413]
实施例26.根据前述实施例中任一项所述的化合物或者其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其中r2是未经取代的c
1-c6烷基,或被包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基取代的c
1-c
10
烷基(例如c
1-c6烷基,例如c1烷基),或-c(=o)-r3,
[0414]
其中r3是包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基,或被包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基取代的c
1-c6烷基,
[0415]
其中所述杂芳基在每次出现时独立地选自:
[0416]
[0417][0417]
其中r4如根据前述实施例中任一项所定义。
[0418]
实施例27.根据前述实施例中任一项所述的化合物或者其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其中r2是未经取代的c
1-c6烷基,或被包
含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基取代的c
1-c
10
烷基(例如c
1-c6烷基,例如c1烷基),或-c(=o)-r3,
[0419]
其中r3是包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基,或被包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基取代的c
1-c6烷基,
[0420]
其中所述杂芳基在每次出现时独立地选自:
[0421][0421][0421]
其中r4如根据前述实施例中任一项所定义。
[0422]
实施例28.根据前述实施例中任一项所述的化合物或者其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其中r2是未经取代的c
1-c6烷基,或被包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基取代的c
1-c
10
烷基(例如c
1-c6烷基,例如c1烷基),或-c(=o)-r3,
[0423]
其中r3是包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基,或被包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基取代的c
1-c6烷基,
[0424]
其中所述杂芳基在每次出现时独立地选自:
[0425][0425][0425]
其中r4如根据前述实施例中任一项所定义。
[0426]
实施例29.根据前述实施例中任一项所述的化合物或者其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其中r2是未经取代的c
1-c6烷基,或被包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基取代的c
1-c
10
烷基(例如c
1-c6烷基,例如c1烷基),或-c(=o)-r3,
[0427]
其中r3是包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基,或被包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基取代的c
1-c6烷基,
[0428]
其中所述杂环基在每次出现时独立地选自哌啶基、哌嗪基、吗啉基、四氢呋喃、二氢异噁唑基、四氢吡喃、吡咯烷基和2-氧杂螺[3.3]庚烷基,
[0429]
并且其中所述杂环基在每次出现时独立地被0-4个r4取代,其中r4如根据前述实施例中任一项所定义。
[0430]
实施例30.根据前述实施例中任一项所述的化合物或者其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其中r2是未经取代的c
1-c6烷基,或被包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基取代的c
1-c
10
烷基(例如c
1-c6烷基,例如c1烷基),或-c(=o)-r3,
[0431]
其中r3是包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基,或被包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基取代的c
1-c6烷基,
[0432]
其中所述杂环基在每次出现时独立地选自:
[0433][0434]
并且其中所述杂环基在每次出现时独立地被0-3个r4取代,其中r4如根据前述实施例中任一项所定义。
[0435]
实施例31.根据前述实施例中任一项所述的化合物或者其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其中r2是未经取代的c
1-c6烷基,或被包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基取代的c
1-c
10
烷基(例如c
1-c6烷基,例如c1烷基),或-c(=o)-r3,
[0436]
其中r3是包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基,或被包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基取代的c
1-c6烷基,
[0437]
其中所述杂环基在每次出现时独立地选自
[0438][0439]
其中r4如根据前述实施例中任一项所定义。
[0440]
实施例32.根据前述实施例中任一项所述的化合物或者其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其中r2是未经取代的c
1-c6烷基,或被包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基取代的c
1-c
10
烷基(例如c
1-c6烷基,
例如c1烷基),或-c(=o)-r3,
[0441]
其中r3是包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基,或被包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基取代的c
1-c6烷基,
[0442]
其中所述杂环基在每次出现时独立地选自:
[0443][0444]
其中r4如根据前述实施例中任一项所定义。
[0445]
实施例33.根据前述实施例中任一项所述的化合物或者其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其中每个r4在每次出现时独立地选自苯基,-o-苯基,苄基-o-,-o-(包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基),包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基,包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基,c
1-c8烷基,c
1-c6烷氧基,c
1-c6卤代烷基,-so2r
4c
,卤素,羟基,-cn,-o-包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基,氧代,c
1-c6卤代烷氧基,-c(=o)-o-(r5),-c(=o)-nr
6ar6b
,nr
6ar6b
,-nh-c(=o)-o-(c
1-c6烷基),和c
3-c6环烷基,其中所述苯基、-o-苯基、苄基-o-、-o-杂芳基、杂芳基和杂环基各自独立地被0-3个r
4a
取代,
[0446]
其中所述烷基和烷氧基各自独立地被0-1个r
4b
取代,并且
[0447]
其中所述环烷基被各自独立地选自以下的0-3个取代基取代:-cn、c
1-c6烷基、c
1-c6烷氧基、和羟基。
[0448]
实施例34.根据前述实施例中任一项所述的化合物或者其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其中每个r4在每次出现时独立地选自苯基,-o-苯基,苄基-o-,-o-(包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基),包含独立地选自n和o的1-4个杂原子的5元至10元杂芳基,包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基,c
1-c8烷基,c
1-c6烷氧基,c
1-c6卤代烷基,-so2r
4c
,卤素,羟基,-cn,-o-包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基,氧代,c
1-c6卤代烷氧基,-c(=o)-o-(r5),-c(=o)-(r5),-c(=o)-nr
6ar6b
,nr
6ar6b
,-nh-c(=o)-o-(c
1-c6烷基),和c
3-c6环烷基,其中所述苯基、-o-苯基、苄基-o-、-o-杂芳基、杂芳基和杂环基各自独立地被0-3个r
4a
取代,
[0449]
其中所述烷基和烷氧基各自独立地被0-1个r
4b
取代,并且
[0450]
其中所述环烷基被各自独立地选自以下的0-3个取代基取代:-cn、c
1-c8烷基、c
1-c6烷氧基、和羟基。
[0451]
实施例35.根据前述实施例中任一项所述的化合物或者其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其中r2是未经取代的c
1-c6烷基、或被c
6-c
10
芳基取代的c
1-c
10
烷基(例如c
1-c6烷基,例如c1烷基)、或-c(=o)-r3,
[0452]
其中r3是c
6-c
10
芳基、或被c
6-c
10
芳基取代的c
1-c6烷基,
[0453]
其中所述芳基在每次出现时独立地被0-3个r4取代,
[0454]
其中每个r4在每次出现时独立地选自苯基,-o-苯基,苄基-o-,-o-(包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基),包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基,包含独立地选自n和o的1-2个杂原子的4元至6元杂环基,c
1-c8烷基,c
1-c6烷氧基,c
1-c6卤代烷基,-so2r
4c
,卤素,羟基,-cn,-o-包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基,c
1-c6卤代烷氧基,-c(=o)-o-(r5),-c(=o)-nr
6ar6b
,nr
6ar6b
,-nh-c(=o)-o-(c
1-c6烷基),和c
3-c6环烷基,其中所述苯基、-o-苯基、苄基-o-、-o-杂芳基、杂芳基和杂环基各自独立地被0-3个r
4a
取代,
[0455]
其中所述烷基和烷氧基各自独立地被0-1个r
4b
取代,并且
[0456]
其中所述环烷基被独立地选自-cn的0-1个取代基取代。
[0457]
实施例36.根据前述实施例中任一项所述的化合物或者其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其中r2是未经取代的c
1-c6烷基、或被c
6-c
10
芳基取代的c
1-c
10
烷基(例如c
1-c6烷基,例如c1烷基)、或-c(=o)-r3,
[0458]
其中r3是c
6-c
10
芳基、或被c
6-c
10
芳基取代的c
1-c6烷基,
[0459]
其中所述芳基在每次出现时独立地被0-3个r4取代,
[0460]
其中每个r4在每次出现时独立地选自-o-苯基,苄基-o-,-o-(包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基),包含独立地选自n、o和s的1-4个杂原子的5元至6元杂芳基,包含独立地选自n和o的1个杂原子的4元至6元杂环基,c
1-c8烷基,c
1-c6烷氧基,c
1-c6卤代烷基,-so2r
4c
,卤素,羟基,-cn,-o-包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基,c
1-c6卤代烷氧基,-c(=o)-nr
6ar6b
,和nr
6ar6b
,
[0461]
其中所述烷基和烷氧基各自独立地被0-1个r
4b
取代,
[0462]
其中所述-o-苯基、苄基-o-、和-o-杂芳基各自独立地被各自独立地选自以下的0-2个取代基取代:羟基、-c(=o)-o-(r5)、卤素、和c
1-c6烷基,
[0463]
其中所述杂环基独立地被独立地选自以下的0-1个取代基取代:c
1-c6烷基,并且
[0464]
其中所述杂芳基独立地被独立地选自以下的0-1个取代基取代:-cn、c
1-c6烷基、c
1-c6烷氧基、和c
1-c6卤代烷基。
[0465]
实施例37.根据前述实施例中任一项所述的化合物或者其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其中r2是未经取代的c
1-c6烷基、或被c
6-c
10
芳基取代的c
1-c
10
烷基(例如c
1-c6烷基,例如c1烷基)、或-c(=o)-r3,
[0466]
其中r3是c
6-c
10
芳基、或被c
6-c
10
芳基取代的c
1-c6烷基,
[0467]
其中所述芳基在每次出现时独立地被0-3个r4取代,
[0468]
其中每个r4在每次出现时独立地选自噁二唑基,吡唑基,四唑基,包含1个o杂原子的4元杂环基,c
1-c8烷基,c
1-c6烷氧基,c
1-c6卤代烷基,氟,氯,碘,羟基,-cn,-o-包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基,-c(=o)-nr
6ar6b
,和nr
6ar6b
,
[0469]
其中所述烷基独立地被独立地选自以下的0-1个取代基取代:包含独立地选自n、o和s的1-4个杂原子的5-6元杂芳基,c
1-c6烷氧基,和苯基,
[0470]
其中所述烷氧基独立地被独立地选自以下的0-1个取代基取代:-c(=o)-n(ch2)
4-5
和吗啉基,其中与所述吗啉基的附接点是经由n原子,
[0471]
其中所述杂环基独立地被独立地选自以下的0-1个取代基取代:c
1-c6烷基,并且
[0472]
其中所述噁二唑基、吡唑基、和四唑基各自独立地被独立地选自以下的0-1个取代基取代:-cn、c
1-c6烷基、c
1-c6烷氧基、和c
1-c6卤代烷基。
[0473]
实施例38.根据前述实施例中任一项所述的化合物或者其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其中r2选自c
1-c6烷基、烷基、
[0474]
其中
[0475]
代表任选的c=c双键,当其存在时,a是o;
[0476]
a选自n-r
4d
、o和ch2;
[0477]
r4选自c
1-c6烷基、c
1-c6烷氧基、c
1-c6卤代烷基、氟、氯、碘、羟基和-cn;
[0478]r4d
选自氢、-c(=o)-o-(c
1-c6烷基)、包含选自n和o的1个杂原子的4元至6元杂环基、c
3-c6环烷基、c
1-c6卤代烷基和c
1-c6烷基,其中所述烷基被选自以下的0-1个取代基取代:c
3-c6环烷基、包含选自n和o的1-2个杂原子的4元至6元杂环基;
[0479]
sub选自c
1-c6烷基、卤素和c
1-c6卤代烷基。
[0480]
实施例39.根据前述权利要求中任一项所述的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其中r2选自c
1-c6烷基、烷基、
[0481]
其中
[0482]
a选自n-r
4d
、o和ch2;
[0483]
r4是c
1-c6烷基;
[0484]r4d
选自氢、-c(=o)-o-(c
1-c6烷基)、包含选自n和o的1个杂原子的4元至6元杂环基、c
3-c6环烷基、c
1-c6卤代烷基和c
1-c6烷基,其中所述烷基被选自以下的0-1个取代基取代:c
3-c6环烷基、包含1个o杂原子的4元至6元杂环基;
[0485]
sub是c
1-c6卤代烷基,例如cf3。
[0486]
实施例40.根据前述实施例中任一项所述的化合物或者其药学上可接受的盐、水
合物、溶剂化物、前药、立体异构体、或互变异构体,其中r2是未经取代的c
1-c6烷基,或被c
3-c8环烷基取代的c
1-c
10
烷基(例如c
1-c6烷基,例如c1烷基),或-c(=o)-r3,
[0487]
其中r3是c
3-c8环烷基、或被c
3-c8环烷基取代的c
1-c6烷基,
[0488]
其中所述环烷基在每次出现时独立地选自环丙基、环丁基、环戊基、环己基、环庚基、和桥接c
5-c8环烷基,
[0489]
并且其中所述环烷基在每次出现时独立地被0-3个r4取代,其中r4如根据前述实施例中任一项所定义。
[0490]
实施例41.根据前述实施例中任一项所述的化合物或者其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其中r2是未经取代的c
1-c6烷基,或被c
3-c8环烷基取代的c
1-c
10
烷基(例如c
1-c6烷基,例如c1烷基),或-c(=o)-r3,
[0491]
其中r3是c
3-c8环烷基、或被c
3-c8环烷基取代的c
1-c6烷基,
[0492]
其中所述环烷基在每次出现时独立地选自环丙基、环丁基、环戊基、环己基、双环[1.1.1]戊基、双环[2.1.1]己基、双环[2.1.1]庚基、双环[2.2.2]辛基和双环[1.1.1]戊烷基,
[0493]
并且其中所述环烷基在每次出现时独立地被0-3个r4取代,其中r4如根据前述实施例中任一项所定义。
[0494]
实施例42.根据前述实施例中任一项所述的化合物或者其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其中r2是未经取代的c
1-c6烷基,或被c
3-c8环烷基取代的c
1-c
10
烷基(例如c
1-c6烷基,例如c1烷基),或-c(=o)-r3,
[0495]
其中r3是c
3-c8环烷基、或被c
3-c8环烷基取代的c
1-c6烷基,
[0496]
其中所述环烷基在每次出现时独立地选自环丙基、环丁基、环戊基、环己基和
[0497]
并且其中所述环烷基在每次出现时独立地被0-3个r4取代,其中r4如根据前述实施例中任一项所定义。
[0498]
实施例43.根据前述实施例中任一项所述的化合物或者其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其中r2是未经取代的c
1-c6烷基,或被c
3-c8环烷基取代的c
1-c
10
烷基(例如c
1-c6烷基,例如c1烷基),或-c(=o)-r3,
[0499]
其中r3是c
3-c8环烷基、或被c
3-c8环烷基取代的c
1-c6烷基,
[0500]
其中所述环烷基在每次出现时独立地选自环丁基、环戊基、环己基和其中所述环烷基在0-2次出现时被r4取代,其中r4如根据前述实施例中任一项所定义。
[0501]
实施例44.根据前述实施例中任一项所述的化合物或者其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其中r2是未经取代的c
1-c6烷基,或被选自以下的一个c
3-c8环烷基取代的c
1-c6烷基(例如c1烷基):
[0502]
其中r4如根据前述实施例中任一项所定义。
[0503]
实施例45.根据前述实施例中任一项所述的化合物或者其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其中r2是未经取代的c
1-c6烷基,或被选自以下的一个c
3-c8环烷基取代的c
1-c6烷基(例如c1烷基):烷基):其中r4如根据前述实施例中任一项所定义。
[0504]
实施例46.根据前述实施例中任一项所述的化合物或者其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其中每个r4在每次出现时独立地选自c
1-c6烷氧基、-nh-c(=o)-o-(c
1-c6烷基)、-c(=o)-o-(c
1-c6烷基)、卤素、和-cn。
[0505]
实施例47.根据前述实施例中任一项所述的化合物或者其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其中每个r4在每次出现时独立地选自c
1-c6烷氧基、-nh-c(=o)-o-(c
1-c6烷基)、-c(=o)-o-(c
1-c3烷基)、氟、和-cn。
[0506]
实施例48.根据实施例1、4至47中任一项所述的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其具有式(ia)
[0507][0508]
其中r
y1
、r
y2
、r1和r2根据前述实施例中任一项所定义。
[0509]
实施例49.根据实施例1、4至47中任一项所述的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其具有式(ib)
[0510][0511]
其中r
x1
、r
x2
、r1和r2根据前述实施例中任一项所定义。
[0512]
实施例50.根据实施例1、4至47中任一项所述的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其具有式(ic)
[0513][0514]
其中r1和r2根据前述实施例中任一项所定义。
[0515]
实施例51.根据实施例1、4至47中任一项所述的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其具有式(id)
[0516][0517]
其中r1和r2根据前述实施例中任一项所定义。
[0518]
实施例52.根据实施例1、4至48中任一项所述的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其具有式(ia-i)
[0519][0520]
其中r
y1
、r
y2
、r1和r2如前述实施例中任一项所定义。
[0521]
实施例53.根据实施例1、4至48中任一项所述的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其具有式(ia-ii)
[0522][0523]
其中r
y1
、r
y2
、r1和r2如前述实施例中任一项所定义。
[0524]
实施例54.根据实施例1、4至48、53中任一项所述的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其具有式(ia-iii)
[0525][0526]
其中r
y1
、r
y2
、r1和r2如前述实施例中任一项所定义。
[0527]
实施例55.根据实施例1、4至48、53中任一项所述的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其具有式(ia-iv)
[0528][0529]
其中r
y1
、r
y2
、r1和r2如前述实施例中任一项所定义。
[0530]
实施例56.根据实施例1、4至48、52中任一项所述的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其具有式(ia-v)或(ia-vi)
[0531][0532]
其中r
y1
、r
y2
、r1和r2如前述实施例中任一项所定义。
[0533]
实施例57.根据实施例1、4至48、52、56中任一项所述的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其具有式(ia-vii)或(ia-viii)
[0534][0535]
其中r
y1
、r
y2
、r1和r2如前述实施例中任一项所定义。
[0536]
实施例58.根据实施例1、4至48、52、56中任一项所述的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其具有式(ia-ix)或(ia-x)
[0537][0538]
其中r
y1
、r
y2
、r1和r2如前述实施例中任一项所定义。
[0539]
实施例59.根据实施例1、4至48、53至55中任一项所述的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其具有式(ia-xi)或(ia-xii)
[0540][0541]
其中r
y1
、r
y2
、r1和r2如前述实施例中任一项所定义。
[0542]
实施例60.根据实施例1、4至48、53至55中任一项所述的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其具有式(ia-xiii)或(ia-xiv)
[0543][0544]
其中r
y1
、r
y2
、r1和r2如前述实施例中任一项所定义。
[0545]
实施例61.根据实施例1、4至48中任一项所述的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其具有式(ie)
[0546][0547]
其中r
y1
、r
y2
、r1和r2如前述实施例中任一项所定义。
[0548]
实施例62.根据实施例1、4至48中任一项所述的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其具有式(if)
[0549][0550]
其中r
y1
、r
y2
、r1和r2如前述实施例中任一项所定义。
[0551]
实施例63.根据前述实施例中任一项所述的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其中:
[0552]ry1
和r
y2
各自独立地选自氢和c
1-c6烷基;
[0553]
r1选自氢和c
1-c6烷基;
[0554]
r2选自氢,c
1-c6烷基,-c(=o)-ch
2-(ch2)
0-1-r
3c
,c
3-c8环烷基,-(ch2)
1-2-苯基,-(ch2)
1-2-包含独立地选自n、o和s的1-4个杂原子的5-10元杂芳基,-(ch2)
1-2-包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基,和-(ch2)
1-2-c
3-c8环烷基,并且其中所述苯基、杂芳基、杂环基和环烷基各自独立地被0-5个r4取代。
[0555]
实施例64.根据前述实施例中任一项所述的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其中:
[0556]ry1
和r
y2
各自独立地选自氢和甲基;
[0557]
r1选自氢和c
1-c6烷基;
[0558]
r2选自c
1-c6烷基,c
3-c8环烷基,-(ch2)
1-2-苯基,-(ch2)
1-2-包含独立地选自n、o和s的1-4个杂原子的5-10元杂芳基,-(ch2)
1-2-包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基,和-(ch2)
1-2-c
3-c8环烷基,并且其中所述苯基、杂芳基、杂环基、和环烷基各自独立地被0-5个r4取代。
[0559]
实施例65.根据前述实施例中任一项所述的化合物或者其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其中r
y1
和r
y2
是相同的并且选自氢和c
1-c6烷基。
[0560]
实施例66.根据前述实施例中任一项所述的化合物或者其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其中r
x1
和r
x2
是相同的并且选自氢和c
1-c6烷基。
[0561]
实施例67.根据前述实施例中任一项所述的化合物或者其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其中r1选自氢和c
1-c4烷基。
[0562]
实施例68.根据前述实施例中任一项所述的化合物或者其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其中r1是氢。
[0563]
实施例69.根据前述实施例中任一项所述的化合物或者其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其中r1是甲基。
[0564]
实施例70.根据前述实施例中任一项所述的化合物或者其药学上可接受的盐、水
合物、溶剂化物、前药、立体异构体、或互变异构体,其中r2选自氢,c
1-c6烷基,-c(=o)-r3,c
3-c8环烷基,-(ch2)
1-2-苯基,-(ch2)
1-2-包含独立地选自n、o和s的1-4个杂原子的5-10元杂芳基,-(ch2)
1-2-包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基,和-(ch2)
1-2-c
3-c8环烷基,其中所述苯基、杂芳基和杂环基各自独立地被0-4个r4取代,并且其中所述环烷基独立地被0-3个r4取代。
[0565]
实施例71.根据前述实施例中任一项所述的化合物或者其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其中r2选自c
1-c6烷基和-(ch2)-苯基,其中所述苯基在0-4次出现时被r4取代。
[0566]
实施例72.根据前述实施例中任一项所述的化合物或者其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其中r2是c
1-c6烷基。
[0567]
实施例73.根据前述实施例中任一项所述的化合物或者其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其中r2是-(ch2)-苯基,其中所述苯基在0-3次出现时被r4取代。
[0568]
实施例74.根据实施例1、4至48中任一项所述的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其具有式(ig)
[0569][0570]
其中r1和r2如前述实施例中任一项所定义,
[0571]
例如r1选自氢和c
1-c6烷基,并且r2选自c
1-c6烷基,例如未经取代的c
1-c6烷基、烷基、
[0572]
其中
[0573]
代表任选的c=c双键,当其存在时,a是o;
[0574]
a选自n-r
4d
、o和ch2;
[0575]
r4选自c
1-c6烷基、c
1-c6烷氧基、c
1-c6卤代烷基、氟、氯、碘、羟基和-cn;
[0576]r4d
选自氢、-c(=o)-o-(c
1-c6烷基)、包含选自n和o的1个杂原子的4元至6元杂环
基、c
3-c6环烷基、c
1-c6卤代烷基和c
1-c6烷基,其中所述烷基被选自以下的0-1个取代基取代:c
3-c6环烷基、包含选自n和o的1-2个杂原子的4元至6元杂环基;
[0577]
sub选自c
1-c6烷基、卤素和c
1-c6卤代烷基。
[0578]
实施例75.根据实施例1、4至48、63至74中任一项所述的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其具有式(ih)
[0579][0580]
其中r2如前述实施例中任一项所定义,
[0581]
例如r2选自c
1-c6烷基,例如未经取代的c
1-c6烷基、烷基、
[0582]
其中
[0583]
a选自n-r
4d
、o和ch2;
[0584]
r4选自c
1-c6烷基、c
1-c6烷氧基、c
1-c6卤代烷基、氟、氯、碘、羟基和-cn;
[0585]r4d
选自氢、-c(=o)-o-(c
1-c6烷基)、包含选自n和o的1个杂原子的4元至6元杂环基、c
3-c6环烷基、c
1-c6卤代烷基和c
1-c6烷基,其中所述烷基被选自以下的0-1个取代基取代:c
3-c6环烷基、包含选自n和o的1-2个杂原子的4元至6元杂环基;
[0586]
sub选自c
1-c6烷基、卤素和c
1-c6卤代烷基。
[0587]
实施例76.根据实施例1、4至48、63至75中任一项所述的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其具有式(ih-i)
[0588][0589]
其中r2根据前述实施例中任一项所定义,例如r2根据实施例75所定义。
[0590]
实施例77.根据实施例1、4至48、63至75中任一项所述的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其具有式(ih-ii)
[0591][0592]
其中r2根据前述实施例中任一项所定义,例如r2根据实施例75所定义。
[0593]
实施例78.根据前述权利要求中任一项所述的化合物,其中所述分子的戊二酰亚胺部分是
[0594]
实施例79.根据前述权利要求中任一项所述的化合物,其中所述分子的戊二酰亚胺部分是
[0595]
实施例80.一种化合物、或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其选自:
[0596]
3-(5-(((r)-1-((1-环己基-1h-吡唑-4-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0597]
3-(5-(((r)-1-((1-甲基-5-苯基-1h-吡唑-3-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0598]
甲基4-(4-(((2r)-2-(((2-(2,6-二氧代哌啶-3-基)-1-氧代异吲哚啉-5-基)氧
基)甲基)哌啶-1-基)甲基)苯氧基)苯甲酸酯;
[0599]
3-(5-(((r)-1-((1-苄基-1h-吡唑-4-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0600]
3-(1-氧代-5-(((r)-1-(3-(吡咯烷-1-基)苄基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮;
[0601]
3-(5-(((r)-1-(3-((1h-吡唑-1-基)甲基)苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0602]
3-(1-氧代-5-(((r)-1-((3-(间甲苯基)-1h-吡唑-4-基)甲基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮;
[0603]
3-(5-(((r)-1-(4-(2h-1,2,3-三唑-2-基)苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0604]
3-(1-氧代-5-(((r)-1-((6-(吡咯烷-1-基)吡啶-3-基)甲基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮;
[0605]
3-(5-(((r)-1-(3-甲氧基-4-甲基苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0606]
3-(5-(((r)-1-(4-(2-甲基-1h-咪唑-1-基)苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0607]
3-(5-(((r)-1-(4-((1h-咪唑-1-基)甲基)苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0608]
3-(5-(((r)-1-((1-异丁基-1h-吡唑-4-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0609]
3-(5-(((2s)-1-((1-(环己-3-烯-1-基甲基)哌啶-4-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0610]
3-(5-(((r)-1-((6-(二乙基氨基)吡啶-3-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0611]
3-(5-(((s)-1-(2-氯-6-氟苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0612]
3-(5-(((r)-1-((5-(苄氧基)-6-甲氧基-1h-吲唑-3-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0613]
3-(5-(((r)-1-((1-苄基哌啶-4-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0614]
3-(5-(((r)-1-(4-吗啉代苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0615]
3-(5-((r)-1-((r)-1-乙基哌啶-2-基)乙氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0616]
叔丁基4-(4-(((2r)-2-(((2-(2,6-二氧代哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)哌啶-1-基)甲基)苯基)哌嗪-1-甲酸酯;
[0617]
3-(5-(((r)-1-(3-((1h-咪唑-1-基)甲基)苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
二酮;
[0639]
乙基3-(((2r)-2-(((2-(2,6-二氧代哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)哌啶-1-基)甲基)-1h-吲唑-4-甲酸酯;
[0640]
3-(5-(((s)-1-((2-乙基-4-甲基-1h-咪唑-5-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0641]
甲基4-(4-(((2s)-2-(((2-(2,6-二氧代哌啶-3-基)-1-氧代-2,3,3a,7a-四氢-1h-异吲哚-5-基)氧基)甲基)哌啶-1-基)甲基)苯氧基)苯甲酸酯;
[0642]
3-(5-(((r)-1-((5-甲基异噁唑-3-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0643]
3-(5-(((r)-1-((1h-吡咯并[2,3-b]吡啶-4-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0644]
3-(5-(((r)-1-((2-吗啉代吡啶-4-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0645]
3-(5-(((r)-1-((1-甲基-1h-苯并[d][1,2,3]三唑-5-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0646]
3-(5-(((s)-1-((1-甲基-1h-吲哚-4-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0647]
4-(((2r)-2-(((2-(2,6-二氧代哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)哌啶-1-基)甲基)苯磺酰胺;
[0648]
3-(5-(((s)-1-(3-((1h-吡唑-1-基)甲基)苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0649]
3-(5-(((s)-1-((6-(二乙基氨基)吡啶-3-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0650]
3-(5-(((s)-1-(3-甲氧基-4-甲基苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0651]
3-(5-(((s)-1-((1-异丁基-1h-吡唑-4-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0652]
3-(5-(((s)-1-((1-苄基-1h-吡唑-4-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0653]
3-(5-(((s)-1-(3-氯-4-羟基苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0654]
3-(1-氧代-5-(((s)-1-((1-(苯基磺酰基)-1h-吡咯-2-基)甲基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮;
[0655]
3-(5-(((s)-1-(2-(4-甲基哌嗪-1-基)苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0656]
3-(5-(((r)-1-((1h-吡唑-4-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0657]
3-(1-氧代-5-(((s)-1-((6-(吡咯烷-1-基)吡啶-3-基)甲基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮;
[0658]
3-(5-(((r)-1-((1-异丙基哌啶-4-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0659]
3-(1-氧代-5-(((r)-1-((1-(吡嗪-2-基)-1h-吡唑-4-基)甲基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮;
[0660]
3-(5-(((s)-1-(3-异丙基-1-甲基-1h-吡唑-5-羰基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0661]
3-(5-(((r)-1-异丙基哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0662]
3-(5-(((s)-1-((5-氯-3-(4-(2-((二甲基氨基)甲基)-1-甲基-1h-咪唑-5-基)苯氧基)吡啶-2-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0663]
3-(5-(((r)-1-((5-氯-3-(4-(2-((二甲基氨基)甲基)-1-甲基-1h-咪唑-5-基)苯氧基)吡啶-2-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0664]
3-(5-(((s)-1-(5-(4-溴苯基)异噁唑-3-羰基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0665]
3-(5-(((r)-1-(3-(5-甲基-1,2,4-噁二唑-3-基)苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0666]
3-(5-(((s)-1-(2-甲氧基苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0667]
3-(5-(((r)-1-((2-(二甲基氨基)嘧啶-5-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0668]
3-(5-(((s)-1-(3,5-二乙基异噁唑-4-羰基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0669]
3-(5-(((s)-1-(4-(2h-1,2,3-三唑-2-基)苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0670]
3-(5-(((s)-1-(3',5-二甲基-[3,5'-二异噁唑]-4'-羰基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0671]
苄基4-(((2r)-2-(((2-(2,6-二氧代哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)哌啶-1-基)甲基)哌啶-1-甲酸酯;
[0672]
3-(5-(((r)-1-(咪唑并[1,2-a]吡啶-8-基甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0673]
3-(5-(((s)-1-((2-吗啉代吡啶-4-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0674]
3-(5-(((s)-1-(3,4-二甲氧基苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0675]
3-(5-(((s)-1-(4-(4-甲基哌嗪-1-基)苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0676]
3-(5-(((s)-1-((1-异丙基哌啶-4-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0677]
3-(5-(((s)-1-(3,5-二氟-4-甲氧基苯甲酰基)哌啶-2-基)甲氧基)-1-氧代异吲
哚啉-2-基)哌啶-2,6-二酮;
[0678]
甲基(1r,3s)-3-(((2r)-2-(((2-(2,6-二氧代哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)哌啶-1-基)甲基)环戊烷-1-甲酸酯;
[0679]
3-(5-(((r)-1-(((1r,4r)-4-甲氧基环己基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0680]
3-(5-(((r)-1-((2-(甲基氨基)吡啶-3-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0681]
3-(5-(((s)-1-(4-(3-甲基-1,2,4-噁二唑-5-基)苯甲酰基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0682]
3-(5-(((s)-1-(2,5-二甲基-1-(5-甲基异噁唑-3-基)-1h-吡咯-3-羰基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0683]
3-(5-(((s)-1-((1h-吡唑-4-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0684]
3-(5-(((s)-1-(3-(苄氧基)-4-甲氧基苯甲酰基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0685]
3-(1-氧代-5-(((r)-1-(2-(2-氧代-2-(哌啶-1-基)乙氧基)苄基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮;
[0686]
3-(5-(((r)-1-(((1s,4s)-4-甲氧基环己基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0687]
3-(5-(((r)-1-((4-甲基-1h-咪唑-5-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0688]
3-(5-(((r)-1-((1h-咪唑-4-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0689]
3-(1-氧代-5-(((s)-1-(2-(哌啶-1-基)噻唑-5-羰基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮;
[0690]
3-(5-(((s)-1-(4-(2-甲基-1h-咪唑-1-基)苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0691]
3-(1-氧代-5-(((s)-1-(4-戊基苯甲酰基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮;
[0692]
3-(5-(((r)-1-((2-甲基咪唑并[1,2-a]吡啶-3-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0693]
3-(5-(((r)-1-((3,3-二氟环丁基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0694]
3-(5-(((s)-1-(4-甲基-3,4-二氢-2h-吡啶并[3,2-b][1,4]噁嗪-7-羰基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0695]
3-(5-(((s)-4-乙基-6,6-二甲基吗啉-3-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0696]
4-(((2r)-2-(((2-(2,6-二氧代哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)哌啶-1-基)甲基)-3-甲氧基苯甲腈;
[0697]
2-(((2r)-2-(((2-(2,6-二氧代哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)哌啶-1-基)甲基)咪唑并[1,2-a]吡啶-7-甲腈;
[0698]
3-(5-(((r)-1-((2-乙基-4-甲基-1h-咪唑-5-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0699]
3-(5-(((r)-1-(环己基甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0700]
3-(5-(((r)-1-((2-甲基-1h-咪唑-5-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0701]
3-(1-氧代-5-(((r)-1-((2-氧代-1,2-二氢吡啶-3-基)甲基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮;
[0702]
3-(1-氧代-5-(((s)-1-(4-(吡咯烷-1-羰基)苄基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮;
[0703]
3-((3-(((2r)-2-(((2-(2,6-二氧代哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)哌啶-1-基)甲基)-2-氧代吡啶-1(2h)-基)甲基)苯甲腈;
[0704]
2-(4-(((2r)-2-(((2-(2,6-二氧代哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)哌啶-1-基)甲基)-1h-咪唑-1-基)乙酸;
[0705]
3-(5-(((r)-1-(4-(5-甲基-1,3,4-噁二唑-2-基)苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0706]
3-(5-(((s)-1-(5-(4-氟苯基)吡啶甲酰基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0707]
3-(5-(((s)-1-((1-甲基-1h-咪唑-5-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0708]
2-(((2r)-2-(((2-(2,6-二氧代哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)哌啶-1-基)甲基)苯甲腈;
[0709]
3-(5-(((s)-1-(5-丁基-4-甲氧基嘧啶-2-羰基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0710]
2-(((2s)-2-(((2-(2,6-二氧代哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)哌啶-1-基)甲基)苯甲腈;
[0711]
乙基4-(((2r)-2-(((2-(2,6-二氧代哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)哌啶-1-基)甲基)-1h-吡唑-3-甲酸酯;
[0712]
4-(((2s)-2-(((2-(2,6-二氧代哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)哌啶-1-基)甲基)苯磺酰胺;
[0713]
3-(1-氧代-5-(((s)-1-(4-(2-氧代吡咯烷-1-基)苄基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮;
[0714]
3-(5-(((s)-1-(4-(3-甲基氧杂环丁烷-3-基)苯甲酰基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0715]
3-(5-(((s)-1-(3,5-二甲基-1-苯基-1h-吡唑-4-羰基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0716]
3-(5-(((s)-1-((6-吗啉代吡啶-2-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚
啉-2-基)哌啶-2,6-二酮;
[0717]
3-(1-氧代-5-(((s)-1-((5-(吡啶-3-基氧基)-1h-吲唑-3-基)甲基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮;
[0718]
3-(5-(((s)-1-(3-(5-甲基-1,2,4-噁二唑-3-基)苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0719]
3-(5-(((s)-1-(2,3-二羟基苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0720]
3-(5-(((r)-1-((1-甲基-1h-咪唑-5-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0721]
3-(1-氧代-5-(((s)-1-(4-(戊-3-炔-1-基氧基)苯甲酰基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮;
[0722]
3-(5-(((s)-1-((1h-咪唑-4-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0723]
3-(5-(((s)-1-(4-吗啉代苯甲酰基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0724]
3-(5-(((s)-1-((5-(苄氧基)-6-甲氧基-1h-吲唑-3-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0725]
苄基4-(((2s)-2-(((2-(2,6-二氧代哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)哌啶-1-基)甲基)哌啶-1-甲酸酯;
[0726]
3-(5-(((s)-1-(4-氯-3-碘苯甲酰基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0727]
3-(5-(((s)-1-(3-氟-4-甲氧基苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0728]
3-(5-(((s)-1-(4-甲基-3-苯基-1h-吡唑-5-羰基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0729]
3-(1-氧代-5-(((r)-1-((四氢-2h-吡喃-4-基)甲基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮;
[0730]
3-(5-(((s)-1-((6-甲氧基吡啶-3-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0731]
3-(5-(((s)-1-(2-(2-吗啉代乙氧基)苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0732]
甲基(1r,3s)-3-(((2s)-2-(((2-(2,6-二氧代哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)哌啶-1-基)甲基)环戊烷-1-甲酸酯;
[0733]
3-(5-(((r)-1-((1h-咪唑-2-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0734]
3-(1-氧代-5-(((s)-1-(1-苯基-1h-1,2,4-三唑-3-羰基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮;
[0735]
3-(5-(((s)-1-(5-新戊基异噁唑-3-羰基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0736]
3-(5-(1-((s)-1-乙基吡咯烷-2-基)乙氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0737]
3-(5-((r)-1-((s)-1-乙基吡咯烷-2-基)乙氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0738]
3-(5-(((s)-1-((2-(二甲基氨基)嘧啶-5-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0739]
3-(5-(((s)-1-((1-甲基-1h-苯并[d][1,2,3]三唑-5-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0740]
3-(5-(((s)-1-(4-(5-甲基-1,3,4-噁二唑-2-基)苯甲酰基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0741]
3-(5-(((r)-1-异丁基哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0742]
3-(1-氧代-5-(((r)-1-(嘧啶-5-基甲基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮;
[0743]
3-(5-(((s)-1-((2-羟基吡啶-4-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0744]
3-(5-(((s)-1-((2-氨基嘧啶-5-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0745]
3-(5-(((s)-1-(3-(4-甲氧基苯基)-1h-吡唑-5-羰基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0746]
2-氯-5-(((2s)-2-(((2-(2,6-二氧代哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)哌啶-1-基)甲基)苯磺酰胺;
[0747]
3-(5-(((s)-1-(噁唑-4-基甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0748]
3-(1-氧代-5-(((s)-1-(2-(2-氧代-2-(哌啶-1-基)乙氧基)苄基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮;
[0749]
3-(1-氧代-5-(((s)-1-(5-丙基异噁唑-3-羰基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮;
[0750]
甲基4-(((2r)-2-(((2-(2,6-二氧代哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)哌啶-1-基)甲基)-1-(3-(三氟甲基)苯基)-1h-吡唑-3-甲酸酯;
[0751]
3-(5-(((r)-1-(2-((1h-1,2,4-三唑-1-基)甲基)苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0752]
3-(5-(((r)-1-((1-甲基-1h-苯并[d]咪唑-2-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0753]
2-(((2s)-2-(((2-(2,6-二氧代哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)哌啶-1-基)甲基)咪唑并[1,2-a]吡啶-7-甲腈;
[0754]
叔丁基(1-(((2r)-2-(((2-(2,6-二氧代哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)哌啶-1-基)甲基)环戊基)氨基甲酸酯;
[0755]
3-(((2s)-2-(((2-(2,6-二氧代哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)
哌啶-1-基)甲基)苯甲腈;
[0756]
3-(5-(((s)-1-(1-甲基-5-苯基-1h-吡唑-3-羰基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0757]
3-(5-(((s)-1-(5-异丙基异噁唑-3-羰基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0758]
3-(1-氧代-5-(((s)-1-((2-氧代-1,2-二氢吡啶-3-基)甲基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮;
[0759]
3-(5-((1-乙基-3,3-二甲基哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0760]
3-(5-(((s)-1-乙基-3,3-二甲基哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0761]
4-(((2s)-2-(((2-(2,6-二氧代哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)哌啶-1-基)甲基)-3-甲氧基苯甲腈;
[0762]
3-(5-(((s)-1-(2-乙基噻唑-5-羰基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0763]
3-(5-(((s)-1-((2-(甲基氨基)吡啶-3-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0764]
3-(5-(((r)-1-(2-羟基-5-(5-(三氟甲基)-1h-四唑-1-基)苄基)哌啶-2-基)甲氧基)-1-氧代-1,3,3a,4,7,7a-六氢-2h-异吲哚-2-基)哌啶-2,6-二酮;
[0765]
3-(5-(((s)-1-(7-甲氧基-1h-吲哚-3-羰基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0766]
3-(5-(((s)-1-(3-异丙基异噁唑-5-羰基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0767]
3-(5-(((r)-1-((3,5-二甲基异噁唑-4-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0768]
3-(5-(((s)-1-((1-甲基-1h-苯并[d]咪唑-2-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0769]
3-(5-(1-((s)-1-乙基吡咯烷-2-基)乙氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0770]
3-(5-((s)-1-((s)-1-乙基吡咯烷-2-基)乙氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0771]
3-(5-((4-乙基-6,6-二甲基吗啉-3-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0772]
3-(5-(((r)-4-乙基-6,6-二甲基吗啉-3-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0773]
3-(5-(((r)-1-((4-甲基四氢-2h-吡喃-4-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0774]
3-(5-(((s)-4-乙基吗啉-3-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0775]
3-(1-氧代-5-(((s)-1-(嘧啶-5-基甲基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌
啶-2,6-二酮;
[0776]
3-(5-(((s)-1-((5-甲基异噁唑-3-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0777]
4-(((2s)-2-(((2-(2,6-二氧代哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)哌啶-1-基)甲基)吡啶甲腈;
[0778]
3-(1-氧代-5-(((s)-1-(喹喔啉-6-羰基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮;
[0779]
3-(5-(((s)-1-(3-(二氟甲氧基)苯甲酰基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0780]
3-(5-(((s)-1-(3-(1-甲基-1h-吡唑-3-基)苯甲酰基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0781]
3-(5-(((s)-1-(2-吗啉代噻唑-4-羰基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0782]
3-(5-(((s)-1-(3-氟双环[1.1.1]戊烷-1-羰基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0783]
3-(5-((1-乙基-3,3-二甲基哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0784]
3-(5-(((r)-1-乙基-3,3-二甲基哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0785]
3-(5-(((r)-1-((6-氟吡啶-3-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0786]
3-(5-(((r)-1-(4,4-二氟环己基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0787]
3-(5-(((r)-1-(4-(4-乙基哌嗪-1-基)苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0788]
3-(1-氧代-5-(((r)-1-(4-(三氟甲氧基)苄基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮;
[0789]
3-(5-((s)-1-((r)-1-乙基哌啶-2-基)乙氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0790]
3-(5-((s)-1-((s)-1-乙基哌啶-2-基)乙氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0791]
3-(5-(((r)-1-异丁酰基哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0792]
3-(5-(((r)-1-(2,4-二氟苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0793]
3-(((2r)-2-(((2-(2,6-二氧代哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)哌啶-1-基)甲基)双环[1.1.1]戊烷-1-甲腈;
[0794]
3-(5-(((r)-1-(4-(4-(氧杂环丁烷-3-基甲基)哌嗪-1-基)苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0795]
3-(5-(((r)-1-(3,4-二氟苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0796]
3-(5-((r)-1-((s)-1-乙基哌啶-2-基)乙氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0797]
3-(5-(((r)-1-(4-(4-异丁基哌嗪-1-基)苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0798]
3-(5-(((r)-1-苯甲酰基哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0799]
3-(5-((1-乙基氮杂环庚烷-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0800]
3-(5-(((r)-1-(噁唑-5-羰基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0801]
3-(5-(((r)-1-(((1r,3r)-3-甲氧基环丁基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0802]
3-(5-(((r)-1-((3-氟双环[1.1.1]戊烷-1-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0803]
3-(5-(((r)-1-(2-吗啉代苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0804]
3-(5-(((r)-1-(4-(4-(环丙基甲基)哌嗪-1-基)苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0805]
3-(5-(((r)-1-((2-氧杂螺[3.3]庚烷-6-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0806]
叔丁基4-(2-(((2r)-2-(((2-(2,6-二氧代哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)哌啶-1-基)甲基)苯基)哌嗪-1-甲酸酯;
[0807]
3-(1-氧代-5-(((r)-1-(2-(哌嗪-1-基)苄基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮;
[0808]
3-(5-(((r)-1-(2-(4-异丁基哌嗪-1-基)苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0809]
3-(1-氧代-5-(((r)-1-(2-(4-((四氢-2h-吡喃-4-基)甲基)哌嗪-1-基)苄基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮;
[0810]
3-(1-氧代-5-(((r)-1-(4-(4-(四氢-2h-吡喃-4-基)哌嗪-1-基)苄基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮;
[0811]
叔丁基7-(((2r)-2-(((2-(2,6-二氧代哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)哌啶-1-基)甲基)吲哚啉-1-甲酸酯;
[0812]
3-(5-(((r)-1-(吲哚啉-7-基甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0813]
3-(5-(((r)-1-((1-乙基吲哚啉-7-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0814]
3-(5-(((r)-1-(4-氟苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,
6-二酮;
[0815]
3-(5-(((r)-1-(2-氯-4-氟苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0816]
3-(5-(((r)-1-((5-氟吡啶-2-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0817]
3-(5-(((r)-1-(((1s,3s)-3-甲氧基环丁基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0818]
3-(1-氧代-5-(((r)-1-(2-(哌啶-1-基)苄基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮;
[0819]
叔丁基4-(2-(((2r)-2-(((2-(2,6-二氧代哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)哌啶-1-基)甲基)苯基)哌啶-1-甲酸酯;
[0820]
3-(5-(((r)-1-(2-(1-乙基哌啶-4-基)苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0821]
叔丁基4-(4-(((2r)-2-(((2-(2,6-二氧代哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)哌啶-1-基)甲基)苯基)哌啶-1-甲酸酯;
[0822]
3-(5-(((r)-1-(4-(1-乙基哌啶-4-基)苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0823]
3-(5-(((r)-1-(2,4-二甲氧基苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0824]
3-(5-(((r)-1-(2-甲氧基苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0825]
3-(5-(((r)-1-((2,3-二氢苯并[b][1,4]二噁英-5-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0826]
3-(5-(((r)-1-(苯并[d][1,3]间二氧杂环戊烯-5-基甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0827]
3-(5-(((r)-1-(((1r,3r)-3-羟基环丁基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0828]
3-(5-(((r)-1-(((1s,3s)-3-羟基环丁基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0829]
3-(5-(((r)-1-(3-氟-4-甲氧基苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0830]
3-(5-(((r)-1-(3-氟-2-羟基苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0831]
3-(1-氧代-5-(((r)-1-(3,4,5-三氟苄基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮;
[0832]
(5-(((r)-1-((2,4-二甲基噻唑-5-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0833]
3-(5-(((r)-1-((2,4-二甲基噻唑-5-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0834]
3-(1-氧代-5-(((r)-1-(吡啶-4-基甲基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮;
[0835]
3-(5-(((r)-1-(2,6-二氟苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0836]
3-(5-(((r)-1-(4-羟基苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0837]
3-(5-(((r)-1-((2-氟吡啶-3-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0838]
3-(1-氧代-5-(((r)-1-(喹啉-3-基甲基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮;
[0839]
3-(5-(((r)-1-((4-甲基噻唑-2-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0840]
3-(1-氧代-5-(((r)-1-(喹啉-2-基甲基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮;
[0841]
叔丁基4-(4-(((2r)-2-(((2-(2,6-二氧代哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)哌啶-1-基)甲基)-2-乙基苯基)哌啶-1-甲酸酯;
[0842]
3-(5-(((r)-1-(3-乙基-4-(哌啶-4-基)苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0843]
3-(5-(((r)-1-(3-乙基-4-(1-乙基哌啶-4-基)苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0844]
3-(5-(((r)-1-(4-(叔丁基)苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0845]
3-(1-氧代-5-(((r)-1-(4-(哌啶-1-基)苄基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮;
[0846]
3-(5-(((r)-1-((3-甲氧基双环[1.1.1]戊烷-1-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0847]
叔丁基4-(2-(((2r)-2-(((2-(2,6-二氧代哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)哌啶-1-基)甲基)-4-氟苯基)哌嗪-1-甲酸酯;
[0848]
3-(5-(((r)-1-(5-氟-2-(哌嗪-1-基)苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0849]
3-(5-(((r)-1-(2-(4-乙基哌嗪-1-基)-5-氟苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0850]
3-(1-氧代-5-(((r)-1-(4-(1-(三氟甲基)环丙基)苄基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮;
[0851]
3-(5-(((r)-1-((3,4-二氢-2h-苯并[b][1,4]噁嗪-5-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0852]
3-(5-(((r)-1-((4-乙基-3,4-二氢-2h-苯并[b][1,4]噁嗪-5-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0853]
3-(1-氧代-5-(((r)-1-((3-氧代-3,4-二氢-2h-苯并[b][1,4]噁嗪-5-基)甲基)
哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮;
[0854]
3-(5-(((r)-1-(2-(苄氧基)乙基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0855]
3-(5-(((r)-1-((2,2-二氟苯并[d][1,3]间二氧杂环戊烯-5-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0856]
3-(5-(((r)-1-((6-吗啉代吡啶-3-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0857]
3-(5-(((r)-1-(4-(3,6-二氢-2h-吡喃-4-基)苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0858]
叔丁基4-(5-(((2r)-2-(((2-(2,6-二氧代哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)哌啶-1-基)甲基)吡啶-2-基)哌嗪-1-甲酸酯;
[0859]
3-(5-(((r)-1-((6-(4-乙基哌嗪-1-基)吡啶-3-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0860]
4-(((2r)-2-(((2-(2,6-二氧代哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)哌啶-1-基)甲基)-2-甲氧基苯甲腈;
[0861]
3-(5-(((r)-1-((1h-苯并[d]咪唑-5-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0862]
5-(((2r)-2-(((2-(2,6-二氧代哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)哌啶-1-基)甲基)-2-甲氧基苯甲腈;
[0863]
3-(1-氧代-5-(((r)-1-(4-(1-((四氢-2h-吡喃-4-基)甲基)哌啶-4-基)苄基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮;
[0864]
3-(5-(((r)-1-(4-(1-(2-氟乙基)哌啶-4-基)苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0865]
3-(5-(((r)-1-(苯并[d]噁唑-5-基甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0866]
3-(5-(((r)-1-(氧杂环丁烷-3-基甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0867]
3-(5-(((r)-1-(4-(1-(氧杂环丁烷-3-基甲基)哌啶-4-基)苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0868]
3-(1-氧代-5-(((r)-1-(((r)-四氢呋喃-3-基)甲基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮;
[0869]
3-(1-氧代-5-(((r)-1-(((s)-四氢呋喃-3-基)甲基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮;
[0870]
3-(5-(((r)-1-(环丙基甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0871]
3-(5-((1s)-1-(1-(((1r,4s)-4-甲氧基环己基)甲基)哌啶-2-基)乙氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0872]
3-(5-((1r)-1-(1-(((1r,4r)-4-甲氧基环己基)甲基)哌啶-2-基)乙氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0873]
3-(5-(((1r,3s,4s)-2-乙基-2-氮杂双环[2.2.1]庚烷-3-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0874]
3-(5-(((r)-1-(4-(4-异丙基哌嗪-1-基)苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0875]
3-(5-(((r)-1-(4-(4-(叔丁基)哌嗪-1-基)苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0876]
3-(5-(((r)-1-(4-(4-环丙基哌嗪-1-基)苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0877]
3-(5-((1-乙基-4-氟哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0878]
3-(5-((4,4-二氟哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0879]
(s)-3-(5-(((s)-1-乙基-4,4-二氟哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0880]
(r)-3-(5-(((s)-1-乙基-4,4-二氟哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0881]
(r)-3-(5-(((r)-1-乙基-4,4-二氟哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0882]
(s)-3-(5-(((r)-1-乙基-4,4-二氟哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0883]
(r)-3-(5-(((1s,3s,4r)-2-乙基-2-氮杂双环[2.2.1]庚烷-3-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0884]
(s)-3-(5-(((1s,3s,4r)-2-乙基-2-氮杂双环[2.2.1]庚烷-3-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮;
[0885]
(r)-3-(5-(((1r,3r,4s)-2-乙基-2-氮杂双环[2.2.1]庚烷-3-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮,以及
[0886]
(s)-3-(5-(((1r,3r,4s)-2-乙基-2-氮杂双环[2.2.1]庚烷-3-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮。
[0887]
实施例81.一种化合物、或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其选自:
[0888]
3-(5-((r)-1-((r)-1-乙基哌啶-2-基)乙氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮-3-d;
[0889]
3-(5-((r)-1-((r)-1-乙基哌啶-2-基)乙氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮-3,4,4,5,5-d5;
[0890]
3-(5-(((r)-1-(2-(4-甲基哌嗪-1-基)苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮-3-d;
[0891]
3-(5-(((r)-1-(2-(4-甲基哌嗪-1-基)苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮-3,4,4,5,5-d5;
[0892]
3-(5-(((r)-1-(4-(4-甲基哌嗪-1-基)苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮-3-d;
[0893]
3-(5-(((r)-1-(4-(4-甲基哌嗪-1-基)苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮-3,4,4,5,5-d5;
[0894]
3-(5-(((r)-1-乙基哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮-3-d;
[0895]
3-(5-(((r)-1-乙基哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮-3,4,4,5,5-d5;
[0896]
3-(5-(((r)-1-(4-(4-(氧杂环丁烷-3-基甲基)哌嗪-1-基)苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮-3-d;
[0897]
3-(5-(((r)-1-(4-(4-(氧杂环丁烷-3-基甲基)哌嗪-1-基)苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮-3,4,4,5,5-d5;
[0898]
3-(5-(((r)-1-(((1r,3r)-3-甲氧基环丁基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮-3-d;和
[0899]
3-(5-(((r)-1-(((1r,3r)-3-甲氧基环丁基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮-3,4,4,5,5-d5。
[0900]
实施例82.根据前述实施例中任一项所述的化合物或者其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,其中所述药学上可接受的盐是酸加成盐。
[0901]
实施例83.一种药物组合物,所述药物组合物包含治疗有效量的根据实施例1至82中任一项所述的化合物、或其药学上可接受的盐、以及药学上可接受的载体或赋形剂。
[0902]
实施例84.一种治疗或预防有需要的受试者的疾病或障碍的方法,所述方法包括向所述受试者施用治疗有效量的根据权利要求1至82中任一项所述的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体。
[0903]
实施例85.一种降解有需要的受试者的wiz蛋白的方法,所述方法包括向所述受试者施用治疗有效量的根据实施例1至82中任一项所述的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体。
[0904]
实施例86.一种抑制有需要的受试者中的wiz蛋白表达的方法,所述方法包括向受试者施用治疗有效量的根据实施例1至82中任一项所述的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体。
[0905]
实施例87.一种抑制、降低、或消除wiz蛋白的活性或wiz蛋白表达的方法,所述方法包括向所述受试者施用根据实施例1至82中任一项所述的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体。
[0906]
实施例88.一种诱导或促进有需要的受试者的胎儿血红蛋白的方法,所述方法包括向所述受试者施用治疗有效量的根据实施例1至82中任一项所述的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体。
[0907]
实施例89.一种重新激活有需要的受试者中的胎儿血红蛋白产生或表达的方法,所述方法包括向受试者施用治疗有效量的根据实施例1至82中任一项所述的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体。
[0908]
实施例90.一种增加有需要的受试者的胎儿血红蛋白表达的方法,所述方法包括向所述受试者施用治疗有效量的根据实施例1至82中任一项所述的化合物或其药学上可接
受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体。
[0909]
实施例91.一种治疗有需要的受试者中的血红蛋白病,例如β-血红蛋白病的方法,所述方法包括向受试者施用治疗有效量的如实施例1至82中任一项所述的化合物或者其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体。
[0910]
实施例92.一种治疗有需要的受试者的镰状细胞病的方法,所述方法包括向所述受试者施用治疗有效量的根据实施例1至82中任一项所述的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体。
[0911]
实施例93.一种治疗有需要的受试者的β-地中海贫血的方法,所述方法包括向所述受试者施用治疗有效量的根据实施例1至82中任一项所述的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体。
[0912]
实施例94.一种治疗受wiz蛋白水平的调节影响的疾病或障碍的方法,所述方法包括向有需要的患者施用根据实施例1至82中任一项所述的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体。
[0913]
实施例95.一种治疗或预防有需要的受试者的受wiz蛋白水平降低影响的障碍的方法,所述方法包括向所述受试者施用治疗有效量的根据实施例1至82中任一项所述的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体。
[0914]
实施例96.一种用于降低受试者的wiz蛋白水平的方法,所述方法包括以下步骤:向有需要的受试者施用治疗有效量的根据实施例1至82中任一项所述的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体。
[0915]
实施例97.根据实施例1至82中任一项所述的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,用作药物。
[0916]
实施例98.根据实施例1至82中任一项所述的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,用于治疗选自镰状细胞病和β-地中海贫血的疾病或障碍。
[0917]
实施例99.根据实施例1至82中任一项所述的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,用于治疗或预防有需要的受试者中的疾病或障碍。
[0918]
实施例100.根据实施例1至82中任一项所述的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,用于在治疗或预防有需要的受试者的受wiz蛋白水平降低影响的障碍中使用。
[0919]
实施例101.根据实施例1至82中任一项所述的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,用于在抑制有需要的受试者的wiz蛋白表达中使用。
[0920]
实施例102.根据实施例1至82中任一项所述的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,用于在降解有需要的受试者的wiz蛋白中使用。
[0921]
实施例103.根据实施例1至82中任一项所述的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,用于在抑制、降低、或消除有需要的受试者的wiz蛋白活性或wiz蛋白表达中使用。
[0922]
实施例104.根据实施例1至82中任一项所述的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,用于在诱导或促进有需要的受试者的胎儿血红蛋白中使用。
[0923]
实施例105.根据实施例1至82中任一项所述的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,用于在重新激活有需要的受试者的胎儿血红蛋白产生或表达中使用。
[0924]
实施例106.根据实施例1至82中任一项所述的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,用于在增加有需要的受试者的胎儿血红蛋白表达中使用。
[0925]
实施例107.根据实施例1至82中任一项所述的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,用于治疗有需要的受试者的血红蛋白病。
[0926]
实施例108.根据实施例1至82中任一项所述的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,用于在治疗有需要的受试者的镰状细胞病中使用。
[0927]
实施例109.根据实施例1至82中任一项所述的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,用于在治疗有需要的受试者的β-地中海贫血中使用。
[0928]
实施例110.根据实施例1至82中任一项所述的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体在制造用于治疗疾病或障碍的药物中的用途,所述疾病或障碍受wiz蛋白水平降低、wiz蛋白表达抑制或wiz蛋白降解影响。
[0929]
实施例111.根据实施例1至82中任一项所述的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体在制造用于治疗受诱导或促进胎儿血红蛋白影响的疾病或障碍的药物中的用途。
[0930]
实施例112.根据实施例1至82中任一项所述的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体在制造用于治疗受重新激活胎儿血红蛋白产生或表达影响的疾病或障碍的药物中的用途。
[0931]
实施例113.根据实施例1至82中任一项所述的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体在制造用于治疗受增加胎儿血红蛋白表达影响的疾病或障碍的药物中的用途。
[0932]
实施例114.根据实施例110至113中任一项所述的化合物的用途,其中所述疾病或障碍选自镰状细胞病和β-地中海贫血。
[0933]
实施例115.根据实施例1至82中任一项所述的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体在制造用于治疗疾病或障碍的药物中的用途,所述疾病或障碍受wiz蛋白水平降低、wiz蛋白表达抑制或wiz蛋白降解影响。
[0934]
实施例116.根据实施例1至82中任一项所述的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体在制造用于治疗受诱导胎儿血红蛋白影响的疾病或障碍的药物中的用途。
[0935]
实施例117.根据实施例1至82中任一项所述的化合物或其药学上可接受的盐、水
合物、溶剂化物、前药、立体异构体、或互变异构体在制造用于治疗受重新激活胎儿血红蛋白产生或表达影响的疾病或障碍的药物中的用途。
[0936]
实施例118.根据实施例1至82中任一项所述的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体在制造用于治疗受增加胎儿血红蛋白表达影响的疾病或障碍的药物中的用途。
[0937]
实施例119.如实施例115至118中任一项所述的化合物的用途,其中所述疾病或障碍选自镰状细胞病和β-地中海贫血。
[0938]
实施例120.根据实施例1至82中任一项所述的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体在治疗疾病或障碍中的用途,所述疾病或障碍受wiz蛋白水平降低、wiz蛋白表达抑制或wiz蛋白降解影响。
[0939]
实施例121.根据实施例1至82中任一项所述的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体在治疗疾病或障碍中的用途,所述疾病或障碍受诱导胎儿血红蛋白、重新激活胎儿血红蛋白产生或表达、或增加胎儿血红蛋白表达影响。
[0940]
实施例122.根据实施例120或121所述的用途,其中所述疾病或障碍选自镰状细胞病和β-地中海贫血。
[0941]
实施例123.一种药物组合,其包含根据实施例1至82中任一项所述的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,以及一种或多种另外的治疗剂。
[0942]
根据起始材料和程序的选择,所述化合物可以呈可能的异构体形式或作为其混合物(例如作为纯的光学异构体或作为异构体混合物,如外消旋体和非对映异构体混合物)存在,这取决于不对称中心的数目。本披露旨在包括所有此类可能的异构体,包括外消旋混合物、对映异构体富集的混合物、非对映异构体混合物和光学纯的形式。光学活性(r)-和(s)-异构体可以使用手性合成子或手性试剂来制备,或使用常规技术拆分。如果化合物含有二取代或三取代的环烷基,则该一个或多个环烷基取代基可以具有顺式或反式构型。本披露包括经取代的环烷基基团的顺式构型和反式构型以及其混合物。所有互变异构形式也包括在内。特别地,当含有作为环原子的n的杂芳基环是2-吡啶酮时,例如则包括其中羰基被描述为羟基(例如2-羟基吡啶)的互变异构体。
[0943]
药学上可接受的盐
[0944]
如本文所用,术语“盐(salt或salts)”是指本披露的化合物的酸加成盐或碱加成盐。“盐”特别地包括“药学上可接受的盐”。术语“药学上可接受的盐”是指保留本披露化合物的生物有效性和特性,并且典型地不是生物学上或其他方面不希望的盐。由于氨基和/或羧基或与其类似的基团的存在,本披露的化合物能够形成酸盐和/或碱盐。
[0945]
可以用无机酸和有机酸形成药学上可接受的酸加成盐。可以衍生出盐的无机酸包括,例如盐酸、氢溴酸、硫酸、硝酸、磷酸等。可以衍生出盐的有机酸包括,例如乙酸、丙酸、乙醇酸、草酸、马来酸、丙二酸、琥珀酸、富马酸、酒石酸、柠檬酸、苯甲酸、扁桃酸、甲磺酸、乙磺酸、甲苯磺酸、磺基水杨酸、甲酸、三氟乙酸等。
[0946]
可以用无机碱和有机碱形成药学上可接受的碱加成盐。可以衍生出盐的无机碱包括例如铵盐和来自元素周期表第i至xii列的金属。在某些实施例中,盐衍生自钠、钾、铵、
钙、镁、铁、银、锌和铜;特别合适的盐包括铵盐、钾盐、钠盐、钙盐和镁盐。
[0947]
可以衍生出盐的有机碱包括例如伯胺、仲胺和叔胺;取代的胺(包括天然存在的取代的胺);环胺;碱性离子交换树脂等。某些有机胺包括异丙胺、苄星、胆碱盐、二乙醇胺、二乙胺、赖氨酸、葡甲胺、哌嗪和氨丁三醇。
[0948]
在另一个方面,本披露提供了呈以下形式的化合物:乙酸盐、抗坏血酸盐、己二酸盐、天冬氨酸盐、苯甲酸盐、苯磺酸盐、溴化物/氢溴酸盐、碳酸氢盐/碳酸盐、硫酸氢盐/硫酸盐、樟脑磺酸盐、癸酸盐、氯化物/盐酸盐、氯脲鎓酸盐(chlortheophyllonate)、柠檬酸盐、乙二磺酸盐、富马酸盐、葡庚糖酸盐、葡糖酸盐、葡萄糖醛酸盐、谷氨酸盐、戊二酸盐、乙醇酸盐、马尿酸盐、氢碘酸盐/碘化物、羟乙基磺酸盐、乳酸盐、乳糖醛酸盐、十二烷基硫酸盐、苹果酸盐、马来酸盐、丙二酸盐、扁桃酸盐、甲磺酸盐、甲基硫酸盐、粘酸盐、萘甲酸盐、萘磺酸盐、烟酸盐、硝酸盐、十八烷酸盐、油酸盐、草酸盐、棕榈酸盐、双羟萘酸盐、磷酸盐/磷酸氢盐/磷酸二氢盐、聚半乳糖醛酸盐、丙酸盐、癸二酸盐、硬脂酸盐、琥珀酸盐、磺基水杨酸盐、硫酸盐、酒石酸盐、甲苯磺酸盐、三苯乙酸盐(trifenatate)、三氟乙酸盐或昔萘酸盐形式。
[0949]
在另一个方面,本披露提供了呈以下形式的化合物:钠、钾、铵、钙、镁、铁、银、锌、铜、异丙胺、苄星、胆碱、二乙醇胺、二乙胺、赖氨酸、葡甲胺、哌嗪或氨丁三醇盐形式。
[0950]
优选地,具有式(i’)、(i)、(i-i)、(i-i-a)、(i-i-b)、(i-i-c)、(i-i-d)、(i-i-e)、(i-i-f)、(i-ii)、(i-ii-a)、(i-ii-b)、(i-ii-c)、(i-ii-d)、(i-ii-e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、(ia-xiii)、(ia-xiv)、(ie)、(if)、(ig)、(ih)、(ih-i)和(ih-ii)的化合物的药学上可接受的盐是酸加成盐。
[0951]
同位素标记的化合物
[0952]
本文给出的任何式也旨在表示化合物的未标记形式以及同位素标记形式。同位素标记的化合物具有由本文给出的式描绘的结构,除了一个或多个原子被具有所选择的原子质量或质量数的原子替代。可以掺入本披露化合物的同位素的实例包括氢、碳、氮、氧、硫、氟、氯和碘的同位素,例如,分别是2h、3h、
11
c、
13
c、
14
c、
18
o、
15
n、
18
f、
17
o、
18
o、
35
s、
36
cl、
123
i、
124
i、
125
i。本披露包括如本文所定义的各种同位素标记的化合物,例如其中掺入放射性同位素(例如3h和
14
c)的那些化合物,或其中掺入非放射性同位素(例如2h和
13
c)的那些化合物。此类同位素标记的化合物可用于代谢研究(用
14
c)、反应动力学研究(例如用2h或3h)、检测或成像技术(例如正电子发射断层扫描(pet)或单光子发射计算机断层扫描(spect),包括药物或底物组织分布测定),或用于患者的放射治疗。特别地,
18
f化合物对于pet或spect研究可能是特别理想的。同位素标记的具有式(i’)、(i)、(i-i)、(i-i-a)、(i-i-b)、(i-i-c)、(i-i-d)、(i-i-e)、(i-i-f)、(i-ii)、(i-ii-a)、(i-ii-b)、(i-ii-c)、(i-ii-d)、(i-ii-e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、(ia-xiii)、(ia-xiv)、(ie)、(if)、(ig)、(ih)、(ih-i)和(ih-ii)的化合物通常可以通过本领域技术人员已知的常规技术或通过与所附实例和通用方案(例如通用方案5a和5b)所述的那些类似的方法,使用适当的同位素标记的试剂代替未标记的先前使用的试剂来制备。
[0953]
在本披露的任一方面的一个实施例中,具有式(i’)或式(i)的化合物中的氢以其正常同位素丰度存在。在另一个实施例中,氢以同位素氘(d)的形式被富集,并且在本发明
的特定实施例中,位于具有式(i’)或式(i)的化合物的戊二酰亚胺部分的一个或多个氢以d的形式被富集,例如
[0954]
此外,用较重的同位素、特别是氘(即,2h或d)进行的取代可以提供来源于更大的代谢稳定性(例如,体内半衰期增加或剂量需求减少或治疗指数改善)的某些治疗优点。应理解,在此上下文中的氘被认为是具有式(i’)、(i)、(i-i)、(i-i-a)、(i-i-b)、(i-i-c)、(i-i-d)、(i-i-e)、(i-i-f)、(i-ii)、(i-ii-a)、(i-ii-b)、(i-ii-c)、(i-ii-d)、(i-ii-e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、(ia-xiii)、(ia-xiv)、(ie)、(if)、(ig)、(ih)、(ih-i)和(ih-ii)的化合物的取代基。这种较重的同位素(特别是氘)的浓度可以由同位素富集因子来定义。如本文所用的术语“同位素富集因子”是指同位素丰度与指定同位素的天然丰度之间的比率。如果本披露化合物中的取代基指示氘,这种化合物具有针对每个指定的氘原子的同位素富集因子为至少3500(在每个指定的氘原子处52.5%氘掺入)、至少4000(60%氘掺入)、至少4500(67.5%氘掺入)、至少5000(75%氘掺入)、至少5500(82.5%氘掺入)、至少6000(90%氘掺入)、至少6333.3(95%氘掺入)、至少6466.7(97%氘掺入)、至少6600(99%氘掺入)、或至少6633.3(99.5%氘掺入)。
[0955]
根据本披露的药学上可接受的溶剂化物包括其中结晶溶剂可以被同位素取代的那些,例如,d2o/d
6-丙酮、d
6-dmso。
[0956]
本披露的化合物,即含有能够充当氢键供体和/或受体的基团的具有式(i’)、(i)、(i-i)、(i-i-a)、(i-i-b)、(i-i-c)、(i-i-d)、(i-i-e)、(i-i-f)、(i-ii)、(i-ii-a)、(i-ii-b)、(i-ii-c)、(i-ii-d)、(i-ii-e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、(ia-xiii)、(ia-xiv)、(ie)、(if)、(ig)、(ih)、(ih-i)和(ih-ii)的化合物,能够与合适的共晶形成物形成共晶。这些共晶可以通过已知的共晶形成方法由具有式(i’)、(i)、(i-i)、(i-i-a)、(i-i-b)、(i-i-c)、(i-i-d)、(i-i-e)、(i-i-f)、(i-ii)、(i-ii-a)、(i-ii-b)、(i-ii-c)、(i-ii-d)、(i-ii-e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、(ia-xiii)、(ia-xiv)、(ie)、(if)、(ig)、(ih)、(ih-i)和(ih-ii)的化合物制备。此类方法包括研磨、加热、共升华、共熔具有(i’)、(i)、(i-i)、(i-i-a)、(i-i-b)、(i-i-c)、(i-i-d)、(i-i-e)、(i-i-f)、(i-ii)、(i-ii-a)、(i-ii-b)、(i-ii-c)、(i-ii-d)、(i-ii-e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、(ia-xiii)、(ia-xiv)、(ie)、(if)、(ig)、(ih)、(ih-i)和(ih-ii)的化合物或使其与共晶形成物在结晶条件下在溶液中接触,并分离由此形成的共晶。合适的共晶形成物包括wo 2004/078163中描述的那些。
[0957]
在本文描述的所有方法能够以任何合适顺序进行,除非本文另外指明或另外与上下文明显相矛盾。本文提供的任何和所有实例或示例性语言(如“例如”)的应用仅旨在更好地说明本披露,而不对另外要求保护的本披露范围做出限制。
[0958]
本披露的一种或多种化合物的任何非对称中心(例如,碳等)可以以外消旋或对映异构体富集的形式存在,例如,(r)-、(s)-或(r,s)-构型。在某些实施例中,例如呈对映异构体的混合物,每个不对称中心以至少10%对映异构体过量、至少20%对映异构体过量、至少30%对映异构体过量、至少40%对映异构体过量、至少50%对映异构体过量、至少60%对映异构体过量、至少70%对映异构体过量、至少80%对映异构体过量、至少90%对映异构体过量、至少95%对映异构体过量、或至少99%对映异构体过量存在。在某些实施例中,例如呈对映异构体富集形式,每个不对称中心以至少50%对映异构体过量、至少60%对映异构体过量、至少70%对映异构体过量、至少80%对映异构体过量、至少90%对映异构体过量、至少95%对映异构体过量、或至少99%对映异构体过量存在。因此,本披露的化合物可以以外消旋混合物或对映异构体富集形式或对映异构体形式存在,或呈非对映异构体的混合物。
[0959]
在一个实施例中,具有式(i’)的化合物包括具有式(i-i-a)、(i-i-b)、(i-ii-a)、或(i-ii-b)的化合物:
[0960][0961]
或者其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体。
[0962]
在一个实施例中,具有式(i-i-a)的化合物包括具有式(i-i-ai)或(i-i-aii)的化合物:
[0963][0964]
或者其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体。
[0965]
在一个实施例中,具有式(i-i-b)的化合物包括具有式(i-i-bi)或(i-i-bii)的化合物:
[0966][0967]
或者其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体。
[0968]
在一个实施例中,具有式(i-ii-a)的化合物包括具有式(i-ii-ai)或(i-ii-aii)的化合物:
[0969][0970]
或者其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体。
[0971]
在一个实施例中,具有式(i-ii-b)的化合物包括具有式(i-ii-bi)或(i-ii-bii)的化合物:
[0972][0973]
或者其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体。
[0974]
在另一个实施例中,具有式(i’)的化合物包括具有式(i-i)或(i-ii)的化合物:
[0975][0976]
或者其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体。
[0977]
在本技术的式中,在c-sp3上的术语指示绝对的立体化学,(r)或(s)。在本技术的式中,在c-sp3上的术语指示绝对的立体化学,(r)或(s)。在本技术的式中,在c-sp3上的术语“/”表示共价键,其中没有定义所述键的立体化学。这意指,在c-sp3上的术语“/”包括各自手性中心的(s)构型或(r)构型。此外,也可以存在混合物。因此,本披露涵盖立体异构体的混合物,例如对映异构体的混合物(如外消旋体),和/或非对映异构体的混合物。
[0978]
为避免疑义,对于任何r基团(例如式(i-i)或(i-ii)中的r1),当描绘具有未明确的立体化学的化合物结构时,如用键(/)表示,这意指不对称中心具有(r)-或(s)-构型,或作为其混合物存在并如此陈述。
[0979]
因此,如本文所用,本披露的化合物可以呈可能的立体异构体、旋转异构体、阻转异构体、互变异构体或其混合物之一的形式,例如,呈基本上纯的几何(顺式或反式)立体异构体、非对映异构体、光学异构体、外消旋体、或其混合物。
[0980]
可以基于组分的物理化学差异,例如通过色谱法和/或分级结晶法将任何所得的立体异构体混合物分离成纯的或基本上纯的几何或光学异构体、非对映异构体、外消旋体。
[0981]
可以通过已知方法将任何所得的本披露的化合物或中间体的外消旋体拆分成光学异构体(对映异构体),例如通过将用光学活性酸或碱得到的其非对映异构体盐进行分
离,并释放出光学活性的酸性或碱性化合物。特别地,因此可以采用碱性部分将本披露的化合物拆分成它们的光学对映体,例如通过分级结晶用光学活性酸,例如酒石酸、二苯甲酰基酒石酸、二乙酰基酒石酸、二-o,o'-对甲苯酰基酒石酸、扁桃酸、苹果酸或樟脑-10-磺酸形成的盐来拆分。本披露的外消旋化合物或外消旋中间体还可以通过手性色谱法(例如,使用手性吸附剂的高压液相色谱法(hplc))拆分。
[0982]
此外,本披露的化合物(包括其盐)也可以以其水合物的形式获得,或包括用于其结晶的其他溶剂。本披露的化合物可以固有地或通过设计与药学上可接受的溶剂(包括水)形成溶剂化物;因此,旨在将本披露包括溶剂化形式和非溶剂化形式两者。术语“溶剂化物”是指本披露化合物(包括其药学上可接受的盐)与一种或多种溶剂分子的分子复合物。此类溶剂分子(例如,水、乙醇等)是制药领域常用的那些,已知它们对接受者是无害的。术语“水合物”是指溶剂分子为水的复合物。本领域技术人员可以使用工具(例如nmr)来鉴定溶剂化物的存在。
[0983]
本披露的化合物(包括其盐、水合物和溶剂化物)可以固有地或通过设计形成多晶型物。
[0984]
在本披露的化合物中,戊二酰亚胺部分的c-3处的立体中心(用*标记)在碱性条件下可能倾向于差向异构化。
[0985][0986]
可以根据本领域已知的手性分离技术实现该位置处的非对映异构体(或视情况而定为对映异构体)的分离。特别地,可根据实例26进行分离。
[0987]
在本披露的化合物的一个实施例中,戊二酰亚胺立体中心处的绝对构型(用上述*标记)是s。
[0988]
在本披露的化合物的另一个实施例中,戊二酰亚胺立体中心处的绝对构型(用上述*标记)是r。
[0989]
在一个实施例中,提供了一种如实例中任一项或根据实施例1至82中任一项所述的化合物,其中戊二酰亚胺立体中心处的绝对构型(用上述*标记)是s。
[0990]
在另一个实施例中,提供了一种如实例中任一项或根据实施例1至82中任一项所述的化合物,其中戊二酰亚胺立体中心处的绝对构型(用上述*标记)是r。
[0991]
制备方法
[0992]
本披露的化合物可以以有机合成领域技术人员熟知的许多方法制备。举例来说,本披露的化合物可以使用下述方法,以及合成有机化学领域中已知的合成方法,或如本领域技术人员所理解的其变体来合成。
[0993]
通常,具有式(i’)和式(i)的化合物可根据下文提供的方案制备。
[0994]
通用方案1
[0995][0996]
以上反应方案的起始材料是可商购的,或可以根据本领域技术人员已知的方法或通过本文披露的方法来制备。一般地,本披露的化合物按照上述反应方案1如下制备:
[0997]
在步骤1中,在极性溶剂(例如乙腈(acn))存在下,金属光氧化还原反应(例如铱(ir)催化的int-1与式int-1a的醇配偶体的光氧化还原偶联)可以提供交叉偶联的醚产物int-2。在酸性条件下除去保护基团(例如boc)可以提供游离胺(i)-1(步骤2),然后可以将其在硼氢化物试剂(例如乙酸硼氢化钠)存在下、通过与适当的醛进行还原胺化(步骤3-i),或在胺碱和极性溶剂(例如二异丙基乙胺(dipea)和二甲基甲酰胺(dmf))存在下、通过与适当的甲磺酸烷基酯进行烷基化反应(步骤3-ii)而转化为(i)-2。当具有式(i)-2的化合物含有n保护的部分(例如n保护的哌嗪基团)时,这些化合物可以在酸性条件下通过脱保护(例如boc)在步骤4中进一步转化为(i)-3,随后用适当的醛和硼氢化钠试剂进行还原胺化,或用适当的烷基化试剂进行烷基化反应,或用适当的活化剂和碱进行酰胺偶联,以提供具有式(i)-4的化合物。对于方案1,r2、r
6a
、r
6b
和r
6c
如本文所定义,特别是根据列举的实施例1至80中任一项所定义。
[0998]
通用方案2
[0999][1000]
以上反应方案的起始材料是可商购的,或可以根据本领域技术人员已知的方法或通过本文披露的方法来制备。一般地,本披露的化合物按照上述反应方案2如下制备:可以将具有式(i)-1的化合物在硼氢化物试剂(例如乙酸硼氢化钠)存在下、通过与适当的酮进行还原胺化(步骤3-i)而转化为(i)-5,或在碱(例如k2co3)和极性溶剂(例如二甲基乙酰胺(dma))存在下、通过与适当的烷基碘化物进行烷基化反应而转化为(i)-6。对于方案2,r2如本文所定义,特别是根据列举的实施例1至80中任一项所定义。
[1001]
通用方案3
[1002][1003]
以上反应方案的起始材料是可商购的,或可以根据本领域技术人员已知的方法或通过本文披露的方法来制备。一般地,本披露的化合物按照上述反应方案3如下制备:化合物(i)-1与适当的羧酸、活化剂(例如hatu)和碱(例如dipea或nmm)进行的酰胺偶联反应提供了酰胺产物(i)-7。对于方案3,r3如本文所定义,特别是根据列举的实施例1至80中任一项所定义。
[1004]
通用方案4
[1005][1006]
以上反应方案的起始材料是可商购的,或可以根据本领域技术人员已知的方法或通过本文披露的方法来制备。一般地,本披露的化合物按照上述反应方案4如下制备:
[1007]
在步骤1中,在极性溶剂(例如乙腈(acn))存在下,金属光氧化还原反应(例如铱(ir)催化的(int-3)与式(int-1b)的醇配偶体的光氧化还原偶联)可以提供交叉偶联的醚产物(4)-i。在酸性条件下除去保护基团(例如boc)可以提供游离胺(4)-ii(步骤2),然后可以将其在硼氢化物试剂(例如乙酸硼氢化钠)存在下、通过与合适的醛进行还原胺化(步骤3-i)而转化为(4)-iii。可替代地,如通用方案1和2所述,可以将(4)-ii在胺碱和极性溶剂(例如二异丙基乙胺(dipea)和二甲基甲酰胺(dmf))存在下、通过与适当的甲磺酸烷基酯或烷基卤化物进行烷基化反应(步骤3-ii)而转化为4-(iii)。可替代地,如通用方案1和3所述,可以将(4)-ii在极性溶剂(例如dmf)中、通过与适当的羧酸、活化剂(例如hatu)和碱(例如dipea或nmm)进行酰胺偶联反应(步骤3-iii)而转化为4-(iii)。用合适的试剂(例如socl2)氯化内酯(4)-iii并开环得到(4)-iv。随后,通过在酸性条件下使用int-ic进行酰胺化和亲核取代来闭环,产生了具有式(i’)或式(i)的最终产物。对于方案4,y、z、r
x1
、r
x2
、r
y1
、r
y2
、r
z1
、r
z2
、r1和r2如本文所定义,特别是根据列举的实施例1至80中任一项所定义。
[1008]
通用方案5a和5b:氘化的本披露的化合物
[1009]
方案5a:
[1010][1011]
方案5b:
[1012][1013]
化合物(4)-iv可以根据通用方案4来制备。随后,通过在酸性条件下使用氘化的int-xx-d(根据wo 2012/068512制备)或氘化的int-xx-d-i(根据wo 2012/079022制备)进行酰胺化和亲核取代来闭环,产生了最终氘化的具有式(i’)的化合物,其中y、z、r1、r2、r
x1
、r
x2
、r
y1
、r
y2
、r
z1
、r
z2
如根据实施例1至80中任一项所定义。
[1014]
在一个实施例中,提供了具有式int-2的化合物或其盐。在另一个实施例中,提供了具有式(i)-1的化合物或其盐。
[1015]
在一个另外的实施例中,提供了具有式(x)的化合物或其盐,
[1016][1017]
其中:
[1018]
y选自o、和ch2、cf2以及chf;
[1019]
z是从0至2的整数;
[1020]rx1
和r
x2
各自独立地选自氢和c
1-c6烷基;
[1021]ry1
和r
y2
各自独立地选自氢和c
1-c6烷基;
[1022]rz1
和r
z2
都是氢
[1023]
或
[1024]rz1
和r
z2
中的1个以及r
y1
和r
y2
中的1个一起形成c
1-c2亚烷基桥接基团,并且r
z1
和r
z2
以及r
y1
和r
y2
中的另一个都是氢;
[1025]
r1选自氢和c
1-c6烷基;
[1026]
r2选自氢、氮保护基团(pg)(适当地,氨基甲酸叔丁酯(boc))、-c(=o)-r3、c
3-c8环烷基、c
1-c6卤代烷基、和c
1-c
10
烷基,其中所述烷基被独立地选自以下的0-1个取代基取代:c
6-c
10
芳基,包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基,包含独立地选自n、o和s的1-2个杂原子的4元至11元杂环基,c
3-c8环烷基和-o-(r
2a
),
[1027]
并且其中所述芳基、杂芳基、杂环基和环烷基各自独立地被0-5个r4取代;
[1028]r2a
是c
1-c6烷基,其中所述烷基被独立地选自c
6-c
10
芳基的0-1个取代基取代;
[1029]
r3选自-ch=cr
3ar3b
,c
6-c
10
芳基,包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基,包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基,c
3-c8环烷基,和c
1-c6烷基,其中所述烷基被0-3个r
3c
取代,并且
[1030]
其中所述芳基、杂芳基、杂环基和环烷基各自独立地被0-5个r4取代;
[1031]r3a
和r
3b
连同它们所附接的碳原子一起形成c
3-c8环烷基环;
[1032]
每个r
3c
在每次出现时独立地选自-c(=o)-r
3d
,nr
3er3f
,c
1-c6烷氧基,-o-r
3d
,羟基,-o-c
6-c
10
芳基,c
1-c6芳基c
6-c
10
烷基-o-,-o-(包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基),c
6-c
10
芳基,包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基,包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基,和c
3-c8环烷基,
[1033]
其中所述-o-芳基、芳基烷基-o-、和-o-杂芳基各自独立地被0-3个r
4a
取代,并且
[1034]
其中所述芳基、杂芳基、杂环基和环烷基各自独立地被0-5个r4取代;
[1035]r3d
是包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基;
[1036]r3e
和r
3f
各自独立地选自氢和c
1-c6烷基;
[1037]
每个r4在每次出现时独立地选自c
6-c
10
芳基,-o-c
6-c
10
芳基,c
1-c6芳基c
6-c
10
烷基-o-,-o-(包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基),包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基,包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基,c
1-c
10
烷基,c
1-c6烷氧基,c
1-c6卤代烷基,-so2r
4c
,卤素,羟基,-cn,-o-包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基,氧代,c
1-c6卤代烷氧基,-c(=o)-o-(r5),-c(=o)-(r5),-c(=o)-nr
6ar6b
,nr
6ar6b
,-nh-c(=o)-o-(c
1-c6烷基),和c
3-c8环烷基,其中所述芳基、-o-芳基、芳基烷基-o-、-o-杂芳基、杂芳基和杂环基各自独立地被0-3个r
4a
取代,
[1038]
其中所述烷基和烷氧基各自独立地被0-1个r
4b
取代,并且
[1039]
其中所述环烷基被各自独立地选自以下的0-3个取代基取代:-cn、c
1-c6烷基、c
1-c6烷氧基、羟基和c
1-c6卤代烷基;
[1040]
每个r
4a
在每次出现时独立地选自-cn,c
1-c6烷氧基,c
1-c6卤代烷基,卤素,羟基,-c(=o)-o-(r5),包含独立地选自n、o和s的1-4个杂原子的5元至10元杂芳基,二(c
1-c6烷基)氨基c
1-c6烷基,c
1-c6烷基,包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基,和c
3-c6环烷基,其中所述烷基被0-1个r
4b
取代,并且其中所述杂芳基被0-3个r
4a-1
取代;
[1041]
每个r
4a-1
在每次出现时独立地选自c
1-c6烷基、二(c
1-c6烷基)氨基c
1-c6烷基、-cn、c
1-c6烷氧基、和c
1-c6卤代烷基;
[1042]
每个r
4b
在每次出现时独立地选自-cn,卤素,-c(=o)nr
6ar6b
,nr
6ar6b
,包含独立地
选自n、o和s的1-4个杂原子的5元至10元杂芳基,-c(=o)-oh,c
1-c6烷氧基,包含独立地选自n、o和s的1个或2个杂原子的4元至6元杂环基,c
3-c8环烷基,c
2-c4炔基,和c
6-c
10
芳基,其中所述芳基被各自独立地选自以下的0-1个取代基取代:-cn、c
1-c6卤代烷基、和c
1-c6烷基;
[1043]r4c
选自c
6-c
10
芳基、羟基、nh2、和卤素;
[1044]
r5选自c
1-c6烷基、c
6-c
10
芳基、和c
6-c
10
芳基c
1-c6烷基;
[1045]r6a
和r
6b
各自独立地选自氢和c
1-c6烷基;
[1046]
或r
6a
和r
6b
连同它们所附接的氮原子一起形成包含选自n、o和s的0-1个另外的杂原子的5元或6元杂环基,其中所述杂环基被0-2个r
6c
取代;
[1047]
每个r
6c
在每次出现时独立地选自c
6-c
10
芳基c
1-c6烷基、-c(=o)-o-(c
1-c6烷基)、-c(=o)-(c
1-c6烷基)、氧代、和c
1-c6烷基,其中所述烷基被独立地选自以下的0-1个取代基取代:-cn和包含独立地选自n、o和s的1-2个杂原子的4元至6元杂环基。
[1048]
在一个实施例中,z是1;并且r
z1
和r
z2
中的1个以及r
y1
和r
y2
中的1个一起形成c
1-c2亚烷基桥接基团,并且r
z1
和r
z2
以及r
y1
和r
y2
中的另一个都是氢。
[1049]
在一个实施例中,z是1;并且r
z1
和r
z2
中的1个以及r
y1
和r
y2
中的1个一起形成c1亚烷基桥接基团,并且r
z1
和r
z2
以及r
y1
和r
y2
中的另一个都是氢。
[1050]
在一个实施例中,r
z1
和r
z2
均为氢。
[1051]
在一个实施例中,r1是氢。
[1052]
在一个实施例中,r
z1
和r
z2
均为氢,并且r1是氢。
[1053]
在一个实施例中,r
z1
和r
z2
均为氢,并且r1是氢且r2是氢。
[1054]
在一个另外的实施例中,r1、r2、r
y1
、r
y2
、r
x1
、r
x2
、r
z1
、r
z2
、y和z如列举的实施例1至80中任一项所定义。另外,r2可以是氮保护基团(pg)(例如氨基甲酸叔丁酯(boc))。
[1055]
在一个另外的实施例中,具有式(x)的化合物具有式(x)-i
[1056][1057]
其中r1、r2、r
x1
、r
x2
、r
y1
、r
y2
、r
z1
、r
z2
、y和z是根据上述式(x)定义的。
[1058]
在一个另外的实施例中,具有式(x)的化合物具有式(x)-ii
[1059][1060]
其中r1、r2、r
x1
、r
x2
、r
y1
、r
y2
、r
z1
、r
z2
、y和z是根据上述式(x)定义的。
[1061]
在式(x)(或式(x)-i或式(x)-ii)的一个另外的实施例中,提供了一种化合物,其选自:
[1062]
(r)-5-((1-乙基哌啶-2-基)甲氧基)异苯并呋喃-1(3h)-酮;
[1063]
(s)-5-((1-乙基哌啶-2-基)甲氧基)异苯并呋喃-1(3h)-酮;
[1064]
5-((r)-1-((s)-1-乙基哌啶-2-基)乙氧基)异苯并呋喃-1(3h)-酮;
[1065]
5-((s)-1-((s)-1-乙基哌啶-2-基)乙氧基)异苯并呋喃-1(3h)-酮;
[1066]
5-((s)-1-((r)-1-乙基哌啶-2-基)乙氧基)异苯并呋喃-1(3h)-酮;和
[1067]
5-((r)-1-((r)-1-乙基哌啶-2-基)乙氧基)异苯并呋喃-1(3h)-酮。
[1068]
在一个另外的实施例中,提供了一种式(y)的化合物
[1069][1070]
其中r1、r
x1
、r
x2
、r
y1
、r
y2
、r
z1
、r
z2
、y和z是根据上述式(x)定义的,并且如本文所定义,pg1和pg2均为氮保护基团。
[1071]
在一个实施例中,pg1是碱不稳定的保护基团,并且pg2是酸不稳定的保护基团。
[1072]
在一个实施例中,pg1是sem保护基团(三甲基甲硅烷基乙氧基甲基),并且pg2是boc保护基团(叔丁氧基羰基)。
[1073]
在一个另外的实施例中,式(y)的化合物具有(y)-i
[1074][1075]
其中r1、r
x1
、r
x2
、r
y1
、r
y2
、r
z1
、r
z2
、y、z、pg1和pg2是根据上述式(y)定义的。
[1076]
在一个另外的实施例中,式(y)的化合物具有(y)-ii
[1077][1078]
其中r1、r
x1
、r
x2
、r
y1
、r
y2
、r
z1
、r
z2
、y、z、pg1和pg2是根据上述式(y)定义的。
[1079]
在式(x)(或式(x)-i或式(x)-ii)的一个另外的实施例中,提供了一种化合物,其选自:
[1080]
叔丁基(2r)-2-(((2-(2,6-二氧代-1-((2-(三甲基甲硅烷基)乙氧基)甲基)哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)哌啶-1-甲酸酯;和
[1081]
叔丁基(2s)-2-(((2-(2,6-二氧代-1-((2-(三甲基甲硅烷基)乙氧基)甲基)哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)哌啶-1-甲酸酯。
[1082]
在一个另外的方面,本披露提供了用于制备呈游离形式或呈药学上可接受的盐形式的具有式(i’)或式(i)的化合物的方法,所述方法包括以下步骤:
[1083]
1)在光氧化还原偶联条件下,将具有式(int-1)或式(int-3)的芳基溴化物与具有式(int-1a)或(int-1b)的醇偶联,以给出如本文所定义的具有式(int-2)或式(4)-i的化合物。
[1084]
在一个另外的方面,本披露提供了用于制备呈游离形式或呈药学上可接受的盐形式的具有式(i’)或式(i)的化合物的方法,所述方法包括以下步骤:
[1085]
1)在光氧化还原偶联条件下,将具有式(int-3)的芳基溴化物与具有式(int-1b)的醇偶联,以给出如本文所定义的具有式(4)-i的化合物;
[1086]
2)将具有式(4)-i的化合物脱保护,以给出如本文所定义的具有式(4)-ii的化合物;
[1087]
3)在还原胺化条件下,使具有式(4)-ii的化合物反应,以给出如本文所定义的具有式(4)-iii的化合物;
[1088]
4)用亲核氯化试剂(例如socl2)将具有式(4)-iii的化合物氯化,以给出如本文所
定义的具有式(4)-iv的化合物;
[1089]
5)使具有式(4)-iv的化合物与具有式(int-1c)的化合物反应,以给出如本文所定义的具有式(i’)或式(i)(或如通用方案4所描绘的式(i)-8)的化合物;和
[1090]
6)任选地将如本文所定义的具有式(i’)或式(i)(或如通用方案4所描绘的式(i)-8)的化合物纯化。
[1091]
在一个另外的方面,本披露提供了用于制备呈游离形式或呈药学上可接受的盐形式的具有式(i’)或式(i)的化合物的方法,所述方法包括以下步骤:
[1092]
1)在光氧化还原偶联条件下,将具有式(int-1)的芳基溴化物与具有式(int-1a)的醇偶联,以给出如本文所定义的具有式(int-2)的化合物;
[1093]
2)将具有式(int-2)的化合物脱保护,以给出如本文所定义的具有式(i)-1(或式(i’)或式(i))的化合物;
[1094]
3-i)任选地,在还原胺化条件下,使具有式(i)-1的化合物反应,以给出如本文所定义的具有式(i)-2(或式(i’)或式(i))的化合物;或
[1095]
3-ii)任选地,在烷基化条件下,使具有式(i)-1的化合物反应,以给出如本文所定义的具有式(i)-2(或式(i’)或式(i))的化合物;或
[1096]
3-iii)任选地,在酰胺偶联条件下,使具有式(i)-1的化合物反应,以给出如本文所定义的具有式(i)-7(或式(i’)或式(i))的化合物;
[1097]
4)任选地,将具有式(i)-2的化合物脱保护,以给出如本文所定义的具有式(i)-3(或式(i’)或式(i))的化合物;和
[1098]
5)任选地,在还原胺化条件下,使具有式(i)-3的化合物反应,以给出如本文所定义的具有式(i)-4(或式(i’)或式(i))的化合物。
[1099]
用于任何前述方法步骤或下文的光氧化还原偶联反应条件涉及使用ir(iii)催化剂(例如[ir{df(cf3)ppy}2{dtbbpy}]pf6)、ni(ii)络合物(例如[nicl2·
dtbbpy])、碱(例如tmp)、合适的溶剂(例如乙腈)、光源(例如34w蓝色led),反应在室温(r.t.)下进行合适的时间,例如12小时。
[1100]
用于任何前述方法步骤或下文的还原胺化条件涉及使用相应的醛、合适的氢化物试剂(例如nabh(oac)3)、合适的溶剂(例如dmf),反应在室温(r.t.)下进行。
[1101]
用于任何前述方法步骤或下文的烷基化反应条件涉及使用相应的磺酸酯(例如相应的甲磺酸酯)、合适的碱(例如dipea)、合适的溶剂(例如dmf),反应在合适的温度(例如100℃)在微波下进行。
[1102]
用于任何前述方法步骤或下文的酰胺偶联反应条件涉及使用相应的羧酸、活化剂(例如hatu)、合适的碱(例如dipea或nmm)、合适的溶剂(例如dmf),反应在合适的温度(例如室温)下进行合适的时间,例如12小时。
[1103]
在一个另外的实施例中,提供了根据通用方案1至4中任一项所述制备具有式(i’)、(i)、(i-i)、(i-i-a)、(i-i-b)、(i-i-c)、(i-i-d)、(i-i-e)、(i-i-f)、(i-ii)、(i-ii-a)、(i-ii-b)、(i-ii-c)、(i-ii-d)、(i-ii-e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、(ia-xiii)、(ia-xiv)、(ie)、(if)、(ig)、(ih)、(ih-i)和(ih-ii)的化合物的方法,该化合物呈游离形式或呈药学上可接受的盐形式。
[1104]
如本文所定义的具有式(int-1)、(i)-i和(x)的化合物用于制备本披露的化合物,例如具有式(i’)、(i)、(i-i)、(i-i-a)、(i-i-b)、(i-i-c)、(i-i-d)、(i-i-e)、(i-i-f)、(i-ii)、(i-ii-a)、(i-ii-b)、(i-ii-c)、(i-ii-d)、(i-ii-e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、(ia-xiii)、(ia-xiv)、(ie)、(if)、(ig)、(ih)、(ih-i)和(ih-ii)的化合物。因此,在一个方面,本披露涉及具有式(int-1)或(i)-i或(x)的化合物或其盐。在另一个方面,本披露涉及具有式(int-1)或(i)-i或(x)的化合物或其盐在制造具有式(i’)、(i)、(i-i)、(i-i-a)、(i-i-b)、(i-i-c)、(i-i-d)、(i-i-e)、(i-i-f)、(i-ii)、(i-ii-a)、(i-ii-b)、(i-ii-c)、(i-ii-d)、(i-ii-e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、(ia-xiii)、(ia-xiv)、(ie)、(if)、(ig)、(ih)、(ih-i)和(ih-ii)的化合物中的用途。本披露进一步包括本披露方法的任何变型,其中将可在其任何阶段获得的中间体产物用作起始材料并且进行其余步骤,或其中起始材料在反应条件下原位形成,或其中将反应组分以其盐或光学纯物质的形式使用。
[1105]
药物组合物
[1106]
在另一方面,本披露提供了药物组合物,所述药物组合物包含本文所述的一种或多种化合物或者其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,以及一种或多种药学上可接受的载体。如本文所用,术语“药物组合物”是指呈适于口服或肠胃外施用的形式的本披露的化合物、或其药学上可接受的盐、以及至少一种药学上可接受的载体。
[1107]
如本文所用,术语“药学上可接受的载体”是指可用于制备或使用药物组合物的物质,并且包括例如合适的稀释剂、溶剂、分散介质、表面活性剂、抗氧化剂、防腐剂、等渗剂、缓冲剂、乳化剂、吸收延迟剂、盐、药物稳定剂、粘合剂、赋形剂、崩解剂、润滑剂、润湿剂、甜味剂、调味剂、染料、及其组合,如本领域技术人员已知的(参见例如remington the science and practice of pharmacy[雷明顿:药物科学与实践],第22版,pharmaceutical press[药物出版社],2013,第1049至1070页)。
[1108]
在本披露的一个方面,提供了一种药物组合物,该药物组合物包含有效降低wiz蛋白表达水平和/或诱导胎儿血红蛋白(hbf)表达的药剂。此类组合物包括但不限于小分子化合物(例如,可以例如通过e3泛素途径靶向wiz蛋白进行降解的小分子化合物,例如如本文所述的化合物)、sirna、shrna、aso、mirna、amo。
[1109]
在另一方面,本披露提供了药物组合物,所述药物组合物包含本披露的化合物、或其药学上可接受的盐、和药学上可接受的载体。在一个另外的实施例中,所述组合物包含至少两种药学上可接受的载体,例如本文所述的那些。出于本披露的目的,除非另有指定,溶剂化物和水合物通常被认为是组合物。优选地,药学上可接受的载体是无菌的。可以将药物组合物配制成用于特定的施用途径,如口服施用、肠胃外施用和直肠施用等。另外,本披露的药物组合物可以以固体形式(包括但不限于胶囊、片剂、丸剂、颗粒、粉末或栓剂)、或以液体形式(包括但不限于溶液、悬浮液或乳液)制成。可以对药物组合物进行常规的制药操作,如灭菌,和/或可以使其含有常规的惰性稀释剂、润滑剂或缓冲剂,以及辅助剂(如防腐剂、稳定剂、润湿剂、乳化剂和缓冲剂等)。
[1110]
通常,药物组合物是包含活性成分及以下中的一种或多种的片剂或明胶胶囊:
[1111]
a)稀释剂,例如乳糖、右旋糖、蔗糖、甘露糖醇、山梨糖醇、纤维素和/或甘氨酸;
[1112]
b)润滑剂,例如二氧化硅、滑石、硬酯酸、其镁盐或钙盐和/或聚乙二醇;
[1113]
c)粘合剂,例如硅酸镁铝、淀粉糊、明胶、黄芪胶、甲基纤维素、羧甲基纤维素钠和/或聚乙烯基吡咯烷酮;
[1114]
d)崩解剂,例如淀粉、琼脂、海藻酸或其钠盐,或泡腾混合物;和
[1115]
e)吸附剂、着色剂、风味剂和甜味剂。
[1116]
在一个实施例中,所述药物组合物是仅包含活性成分的胶囊。
[1117]
片剂可根据本领域已知的方法进行薄膜包衣或肠溶包衣。
[1118]
合适的用于口服施用的组合物包括有效量呈片剂、锭剂、水性或油性悬浮液、可分散粉末或颗粒、乳液、硬或软胶囊、或糖浆或酏剂、溶液或固体分散体的本发露化合物。将旨在用于口服使用的组合物根据本领域已知的用于制造药物组合物的任何方法来制备,并且为了提供药学上精致的并且适口的制剂,此类组合物可以包含一种或多种选自下组的试剂,该组由以下组成:甜味剂、调味剂、着色剂以及防腐剂。片剂可以含有与适用于制造片剂的非毒性、药学上可接受的赋形剂混合的活性成分。这些赋形剂是,例如,惰性稀释剂,如碳酸钙、碳酸钠、乳糖、磷酸钙或磷酸钠;造粒剂及崩解剂,例如,玉米淀粉或海藻酸;粘合剂,例如,淀粉、明胶或阿拉伯胶;以及润滑剂,例如硬脂酸镁、硬脂酸或滑石。片剂是未包衣的,或者根据已知技术进行包衣以延缓在胃肠道中的崩解和吸收,从而在较长的时间段内提供持久的作用。例如,可采用时间延迟材料,如单硬脂酸甘油酯或二硬脂酸甘油酯。用于口服使用的配制品可呈现为硬质明胶胶囊,其中活性成分与惰性固体稀释剂(例如,碳酸钙、磷酸钙或高岭土)混合,或呈现为软质明胶胶囊,其中活性成分与水或油介质(例如,花生油、液体石蜡或橄榄油)混合。
[1119]
某些可注射的组合物是水性等渗溶液或悬浮液,并且栓剂有利地由脂肪乳剂或悬浮液制备。所述组合物可以是灭菌的和/或含有辅助剂,例如防腐剂、稳定剂、润湿剂或乳化剂、溶液促进剂、用于调节渗透压的盐和/或缓冲剂。此外,所述组合物还可含有其他有治疗价值的物质。所述组合物分别根据常规的混合、制粒或包衣方法制备,并含有约0.1%-75%或约1%-50%的活性成分。
[1120]
用于透皮应用的合适组合物包括有效量的本披露化合物和合适的载体。适于透皮递送的载体包括可吸收的药理学上可接受的溶剂,以帮助通过宿主的皮肤。例如,透皮设备呈绷带的形式,所述绷带包含背衬构件、含有化合物以及任选地载体的贮存器、任选地控制速率的屏障以在长时间段内以受控和预定的速率将化合物递送至宿主皮肤、以及将所述设备固定在皮肤上的装置。
[1121]
适用于局部应用(例如,应用至皮肤和眼睛)的组合物包括水溶液、悬浮液、软膏剂、霜剂、凝胶或可喷雾配制品,例如,用于通过气溶胶等递送。这些局部递送系统将尤其适用于真皮应用,例如,用于治疗皮肤癌,例如,用于防晒霜、洗剂、喷雾等中的预防用途。因此它尤其适用于局部使用,包括本领域中熟知的化妆品、配制品。此类系统可含有增溶剂、稳定剂、张力增强剂、缓冲剂和防腐剂。
[1122]
如本文所用,局部应用还可以涉及吸入或鼻内应用。它们可以在使用或不使用合适推进剂的情况下,自干粉吸入器以干粉形式(单独的作为混合物,例如与乳糖的干掺混
物,或经混合的组分颗粒,例如与磷脂混合的组分颗粒)或自加压容器、泵、喷雾、喷雾器或雾化器以气溶胶喷雾形式便利地递送。
[1123]
呈游离形式或呈药学上可接受的盐形式的具有式(i’)、(i)、(i-i)、(i-i-a)、(i-i-b)、(i-i-c)、(i-i-d)、(i-i-e)、(i-i-f)、(i-ii)、(i-ii-a)、(i-ii-b)、(i-ii-c)、(i-ii-d)、(i-ii-e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、(ia-xiii)、(ia-xiv)、(ie)、(if)、(ig)、(ih)、(ih-i)和(ih-ii)的化合物表现出有价值的药理性质,例如wiz调节性能或wiz降解性能或hbf诱导性能,例如,如在实例中提供的体外测试中所示,因此被指示用于治疗或用作研究化学品,例如用作工具化合物。
[1124]
所披露的化合物的另外的性能包括在本文所述的生物学测定中具有良好的效力,有利的安全性,以及有利的药代动力学性能。
[1125]
疾病和障碍
[1126]
在本披露的一个实施例中,提供了一种治疗剂,该治疗剂有效降低wiz蛋白表达水平和/或诱导胎儿血红蛋白(hbf)表达。在一个另外的实施例中,该药剂是小分子(例如,可以例如通过e3泛素途径靶向wiz蛋白进行降解的小分子化合物,例如如本文所述的化合物)、sirna、shrna、aso、mirna、amo。在一个实施例中,降低wiz蛋白表达水平和/或诱导胎儿血红蛋白(hbf)表达的方法用于治疗血红蛋白病,例如β血红蛋白病,包括镰状细胞病(scd)和β-地中海贫血。
[1127]
本披露的化合物可以用于治疗下文所述的一种或多种疾病或障碍。在一个实施例中,该疾病或障碍受wiz蛋白表达水平降低和/或胎儿血红蛋白蛋白表达水平诱导影响。在另一个实施例中,该疾病或障碍是血红蛋白病,例如β血红蛋白病,包括镰状细胞病(scd)和β-地中海贫血。
[1128]
使用方法
[1129]
在本披露的一个方面,提供了一种降低wiz蛋白表达水平和/或诱导胎儿血红蛋白(hbf)表达的方法,该方法包括向受试者施用治疗有效量的药剂,例如小分子(例如,可以例如通过e3泛素途径靶向wiz蛋白进行降解的小分子化合物,例如如本文所述的化合物)、sirna、shrna、aso、mirna、amo。在一个实施例中,降低wiz蛋白表达水平和/或诱导胎儿血红蛋白(hbf)表达的方法用于治疗血红蛋白病,例如β血红蛋白病,包括镰状细胞病(scd)和β-地中海贫血。
[1130]
所有涉及降低wiz蛋白表达水平和/或诱导胎儿血红蛋白(hbf)表达的方法的前述实施例和下文实施例同样适用于:
[1131]
用于降低wiz蛋白表达水平和/或诱导胎儿血红蛋白(hbf)表达的方法中的治疗剂,例如小分子(例如,可以例如通过e3泛素途径靶向wiz蛋白进行降解的小分子化合物,例如如本文所述的化合物)、sirna、shrna、aso、mirna、amo;
[1132]
用于治疗根据本披露的上述疾病或障碍的治疗剂,例如小分子(例如,可以例如通过e3泛素途径靶向wiz蛋白进行降解的小分子化合物,例如如本文所述的化合物)、sirna、shrna、aso、mirna、amo;
[1133]
药剂例如小分子(例如如本文所述的化合物)、sirna、shrna、aso、mirna、amo在治疗根据本披露的上述疾病或障碍中的用途;和
[1134]
用于治疗根据本披露的上述疾病或障碍的药物组合物,该药物组合物包含药剂例如小分子(例如,可以例如通过e3泛素途径靶向wiz蛋白进行降解的小分子化合物,例如如本文所述的化合物)、sirna、shrna、aso、mirna、amo。
[1135]
考虑到这些化合物作为wiz调节剂或降解剂的活性,呈游离形式或呈药学上可接受的盐形式的具有式(i’)、(i)、(i-i)、(i-i-a)、(i-i-b)、(i-i-c)、(i-i-d)、(i-i-e)、(i-i-f)、(i-ii)、(i-ii-a)、(i-ii-b)、(i-ii-c)、(i-ii-d)、(i-ii-e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、(ia-xiii)、(ia-xiv)、(ie)、(if)、(ig)、(ih)、(ih-i)和(ih-ii)的化合物可用于治疗如下病症,所述病症可以通过调节wiz蛋白表达水平、降低wiz蛋白表达水平、或诱导胎儿血红蛋白(hbf)来治疗,例如血液病,例如遗传性血液病,例如镰状细胞病、或β-地中海贫血。在一个方面,本披露提供了治疗或预防有需要的受试者的疾病或障碍的方法,该方法包括向受试者施用治疗有效量的具有式(i’)、(i)、(i-i)、(i-i-a)、(i-i-b)、(i-i-c)、(i-i-d)、(i-i-e)、(i-i-f)、(i-ii)、(i-ii-a)、(i-ii-b)、(i-ii-c)、(i-ii-d)、(i-ii-e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、(ia-xiii)、(ia-xiv)、(ie)、(if)、(ig)、(ih)、(ih-i)和(ih-ii)的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体。
[1136]
在另一个方面,本披露提供了治疗或预防有需要的受试者的受wiz蛋白水平降低影响的障碍的方法,该方法包括向受试者施用治疗有效量的具有式(i’)、(i)、(i-i)、(i-i-a)、(i-i-b)、(i-i-c)、(i-i-d)、(i-i-e)、(i-i-f)、(i-ii)、(i-ii-a)、(i-ii-b)、(i-ii-c)、(i-ii-d)、(i-ii-e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、(ia-xiii)、(ia-xiv)、(ie)、(if)、(ig)、(ih)、(ih-i)和(ih-ii)的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体。
[1137]
在另一个方面,本披露提供了抑制有需要的受试者的wiz蛋白表达的方法,该方法包括向受试者施用治疗有效量的具有式(i’)、(i)、(i-i)、(i-i-a)、(i-i-b)、(i-i-c)、(i-i-d)、(i-i-e)、(i-i-f)、(i-ii)、(i-ii-a)、(i-ii-b)、(i-ii-c)、(i-ii-d)、(i-ii-e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、(ia-xiii)、(ia-xiv)、(ie)、(if)、(ig)、(ih)、(ih-i)和(ih-ii)的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体。
[1138]
在另一个方面,本披露提供了降解有需要的受试者的wiz蛋白的方法,该方法包括向受试者施用治疗有效量的具有式(i’)、(i)、(i-i)、(i-i-a)、(i-i-b)、(i-i-c)、(i-i-d)、(i-i-e)、(i-i-f)、(i-ii)、(i-ii-a)、(i-ii-b)、(i-ii-c)、(i-ii-d)、(i-ii-e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、(ia-xiii)、(ia-xiv)、(ie)、(if)、(ig)、(ih)、(ih-i)和(ih-ii)的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体。
[1139]
在另一个方面,本披露提供了抑制、降低、或消除wiz蛋白的活性或wiz蛋白表达的
方法,该方法包括向受试者施用具有式(i’)、(i)、(i-i)、(i-i-a)、(i-i-b)、(i-i-c)、(i-i-d)、(i-i-e)、(i-i-f)、(i-ii)、(i-ii-a)、(i-ii-b)、(i-ii-c)、(i-ii-d)、(i-ii-e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、(ia-xiii)、(ia-xiv)、(ie)、(if)、(ig)、(ih)、(ih-i)和(ih-ii)的化合物或药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体。
[1140]
在另一个方面,本披露提供了诱导或促进有需要的受试者的胎儿血红蛋白的方法,该方法包括向受试者施用治疗有效量的具有式(i’)、(i)、(i-i)、(i-i-a)、(i-i-b)、(i-i-c)、(i-i-d)、(i-i-e)、(i-i-f)、(i-ii)、(i-ii-a)、(i-ii-b)、(i-ii-c)、(i-ii-d)、(i-ii-e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、(ia-xiii)、(ia-xiv)、(ie)、(if)、(ig)、(ih)、(ih-i)和(ih-ii)的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体。
[1141]
在另一个方面,本披露提供了重新激活有需要的受试者的胎儿血红蛋白产生或表达的方法,该方法包括向受试者施用治疗有效量的具有式(i’)、(i)、(i-i)、(i-i-a)、(i-i-b)、(i-i-c)、(i-i-d)、(i-i-e)、(i-i-f)、(i-ii)、(i-ii-a)、(i-ii-b)、(i-ii-c)、(i-ii-d)、(i-ii-e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、(ia-xiii)、(ia-xiv)、(ie)、(if)、(ig)、(ih)、(ih-i)和(ih-ii)的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体。
[1142]
在另一个方面,本披露提供了增加有需要的受试者的胎儿血红蛋白表达的方法,该方法包括向受试者施用治疗有效量的具有式(i’)、(i)、(i-i)、(i-i-a)、(i-i-b)、(i-i-c)、(i-i-d)、(i-i-e)、(i-i-f)、(i-ii)、(i-ii-a)、(i-ii-b)、(i-ii-c)、(i-ii-d)、(i-ii-e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、(ia-xiii)、(ia-xiv)、(ie)、(if)、(ig)、(ih)、(ih-i)和(ih-ii)的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体。
[1143]
在另一个方面,本披露提供了治疗有需要的受试者的血红蛋白病,例如β-血红蛋白病的方法,该方法包括向受试者施用治疗有效量的具有式(i’)、(i)、(i-i)、(i-i-a)、(i-i-b)、(i-i-c)、(i-i-d)、(i-i-e)、(i-i-f)、(i-ii)、(i-ii-a)、(i-ii-b)、(i-ii-c)、(i-ii-d)、(i-ii-e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、(ia-xiii)、(ia-xiv)、(ie)、(if)、(ig)、(ih)、(ih-i)和(ih-ii)的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体。
[1144]
在另一个方面,本披露提供了治疗有需要的受试者的镰状细胞病的方法,该方法包括向受试者施用治疗有效量的具有式(i’)、(i)、(i-i)、(i-i-a)、(i-i-b)、(i-i-c)、(i-i-d)、(i-i-e)、(i-i-f)、(i-ii)、(i-ii-a)、(i-ii-b)、(i-ii-c)、(i-ii-d)、(i-ii-e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、(ia-xiii)、(ia-xiv)、(ie)、(if)、
(ig)、(ih)、(ih-i)和(ih-ii)的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体。
[1145]
在另一个方面,本披露提供了治疗有需要的受试者的β-地中海贫血的方法,该方法包括向受试者施用治疗有效量的具有式(i’)、(i)、(i-i)、(i-i-a)、(i-i-b)、(i-i-c)、(i-i-d)、(i-i-e)、(i-i-f)、(i-ii)、(i-ii-a)、(i-ii-b)、(i-ii-c)、(i-ii-d)、(i-ii-e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、(ia-xiii)、(ia-xiv)、(ie)、(if)、(ig)、(ih)、(ih-i)和(ih-ii)的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体。
[1146]
在一个实施例中,重型或中度β-地中海贫血是纯合无效突变或复合杂合突变的结果,其导致β-球蛋白缺乏和β-地中海贫血的表型并发症,无论是否是输血依赖型的。
[1147]
在另一个方面,本披露提供了具有式(i’)、(i)、(i-i)、(i-i-a)、(i-i-b)、(i-i-c)、(i-i-d)、(i-i-e)、(i-i-f)、(i-ii)、(i-ii-a)、(i-ii-b)、(i-ii-c)、(i-ii-d)、(i-ii-e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、(ia-xiii)、(ia-xiv)、(ie)、(if)、(ig)、(ih)、(ih-i)和(ih-ii)的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,用于在治疗或预防有需要的受试者的疾病或障碍的方法中使用,该方法包括向受试者施用治疗有效量的具有式(i’)、(i)、(i-i)、(i-i-a)、(i-i-b)、(i-i-c)、(i-i-d)、(i-i-e)、(i-i-f)、(i-ii)、(i-ii-a)、(i-ii-b)、(i-ii-c)、(i-ii-d)、(i-ii-e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、(ia-xiii)、(ia-xiv)、(ie)、(if)、(ig)、(ih)、(ih-i)和(ih-ii)的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体。
[1148]
在另一个方面,本披露提供了具有式(i’)、(i)、(i-i)、(i-i-a)、(i-i-b)、(i-i-c)、(i-i-d)、(i-i-e)、(i-i-f)、(i-ii)、(i-ii-a)、(i-ii-b)、(i-ii-c)、(i-ii-d)、(i-ii-e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、(ia-xiii)、(ia-xiv)、(ie)、(if)、(ig)、(ih)、(ih-i)和(ih-ii)的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,用于在治疗或预防有需要的受试者的受wiz蛋白水平降低影响的障碍的方法中使用,该方法包括向受试者施用治疗有效量的具有式(i’)、(i)、(i-i)、(i-i-a)、(i-i-b)、(i-i-c)、(i-i-d)、(i-i-e)、(i-i-f)、(i-ii)、(i-ii-a)、(i-ii-b)、(i-ii-c)、(i-ii-d)、(i-ii-e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、(ia-xiii)、(ia-xiv)、(ie)、(if)、(ig)、(ih)、(ih-i)和(ih-ii)的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体。
[1149]
在另一个方面,本披露提供了具有式(i’)、(i)、(i-i)、(i-i-a)、(i-i-b)、(i-i-c)、(i-i-d)、(i-i-e)、(i-i-f)、(i-ii)、(i-ii-a)、(i-ii-b)、(i-ii-c)、(i-ii-d)、(i-ii-e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、(ia-xiii)、(ia-xiv)、
(ie)、(if)、(ig)、(ih)、(ih-i)和(ih-ii)的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,用于在抑制有需要的受试者的wiz蛋白表达的方法中使用,该方法包括向受试者施用治疗有效量的具有式(i’)、(i)、(i-i)、(i-i-a)、(i-i-b)、(i-i-c)、(i-i-d)、(i-i-e)、(i-i-f)、(i-ii)、(i-ii-a)、(i-ii-b)、(i-ii-c)、(i-ii-d)、(i-ii-e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、(ia-xiii)、(ia-xiv)、(ie)、(if)、(ig)、(ih)、(ih-i)和(ih-ii)的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体。
[1150]
在另一个方面,本披露提供了具有式(i’)、(i)、(i-i)、(i-i-a)、(i-i-b)、(i-i-c)、(i-i-d)、(i-i-e)、(i-i-f)、(i-ii)、(i-ii-a)、(i-ii-b)、(i-ii-c)、(i-ii-d)、(i-ii-e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、(ia-xiii)、(ia-xiv)、(ie)、(if)、(ig)、(ih)、(ih-i)和(ih-ii)的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,用于在降解有需要的受试者的wiz蛋白的方法中使用,该方法包括向受试者施用治疗有效量的具有式(i’)、(i)、(i-i)、(i-i-a)、(i-i-b)、(i-i-c)、(i-i-d)、(i-i-e)、(i-i-f)、(i-ii)、(i-ii-a)、(i-ii-b)、(i-ii-c)、(i-ii-d)、(i-ii-e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、(ia-xiii)、(ia-xiv)、(ie)、(if)、(ig)、(ih)、(ih-i)和(ih-ii)的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体。
[1151]
在另一个方面,本披露提供了具有式(i’)、(i)、(i-i)、(i-i-a)、(i-i-b)、(i-i-c)、(i-i-d)、(i-i-e)、(i-i-f)、(i-ii)、(i-ii-a)、(i-ii-b)、(i-ii-c)、(i-ii-d)、(i-ii-e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、(ia-xiii)、(ia-xiv)、(ie)、(if)、(ig)、(ih)、(ih-i)和(ih-ii)的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,用于在抑制、降低、或消除wiz蛋白的活性或wiz蛋白表达的方法中使用,该方法包括向受试者施用具有式(i’)、(i)、(i-i)、(i-i-a)、(i-i-b)、(i-i-c)、(i-i-d)、(i-i-e)、(i-i-f)、(i-ii)、(i-ii-a)、(i-ii-b)、(i-ii-c)、(i-ii-d)、(i-ii-e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、(ia-xiii)、(ia-xiv)、(ie)、(if)、(ig)、(ih)、(ih-i)和(ih-ii)的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体。
[1152]
在另一个方面,本披露提供了具有式(i’)、(i)、(i-i)、(i-i-a)、(i-i-b)、(i-i-c)、(i-i-d)、(i-i-e)、(i-i-f)、(i-ii)、(i-ii-a)、(i-ii-b)、(i-ii-c)、(i-ii-d)、(i-ii-e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、(ia-xiii)、(ia-xiv)、(ie)、(if)、(ig)、(ih)、(ih-i)和(ih-ii)的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,用于在诱导或促进有需要的受试者的胎儿血红蛋白的方法中使用,该方法包括向受试者施用治疗有效量的具有式(i’)、(i)、(i-i)、(i-i-a)、
(i-i-b)、(i-i-c)、(i-i-d)、(i-i-e)、(i-i-f)、(i-ii)、(i-ii-a)、(i-ii-b)、(i-ii-c)、(i-ii-d)、(i-ii-e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、(ia-xiii)、(ia-xiv)、(ie)、(if)、(ig)、(ih)、(ih-i)和(ih-ii)的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体。
[1153]
在另一个方面,本披露提供了具有式(i’)、(i)、(i-i)、(i-i-a)、(i-i-b)、(i-i-c)、(i-i-d)、(i-i-e)、(i-i-f)、(i-ii)、(i-ii-a)、(i-ii-b)、(i-ii-c)、(i-ii-d)、(i-ii-e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、(ia-xiii)、(ia-xiv)、(ie)、(if)、(ig)、(ih)、(ih-i)和(ih-ii)的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,用于在重新激活有需要的受试者的胎儿血红蛋白产生或表达的方法中使用,该方法包括向受试者施用治疗有效量的具有式(i’)、(i)、(i-i)、(i-i-a)、(i-i-b)、(i-i-c)、(i-i-d)、(i-i-e)、(i-i-f)、(i-ii)、(i-ii-a)、(i-ii-b)、(i-ii-c)、(i-ii-d)、(i-ii-e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、(ia-xiii)、(ia-xiv)、(ie)、(if)、(ig)、(ih)、(ih-i)和(ih-ii)的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体。
[1154]
在另一个方面,本披露提供了具有式(i’)、(i)、(i-i)、(i-i-a)、(i-i-b)、(i-i-c)、(i-i-d)、(i-i-e)、(i-i-f)、(i-ii)、(i-ii-a)、(i-ii-b)、(i-ii-c)、(i-ii-d)、(i-ii-e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、(ia-xiii)、(ia-xiv)、(ie)、(if)、(ig)、(ih)、(ih-i)和(ih-ii)的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,用于在增加有需要的受试者的胎儿血红蛋白表达的方法中使用,该方法包括向受试者施用治疗有效量的具有式(i’)、(i)、(i-i)、(i-i-a)、(i-i-b)、(i-i-c)、(i-i-d)、(i-i-e)、(i-i-f)、(i-ii)、(i-ii-a)、(i-ii-b)、(i-ii-c)、(i-ii-d)、(i-ii-e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、(ia-xiii)、(ia-xiv)、(ie)、(if)、(ig)、(ih)、(ih-i)和(ih-ii)的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体。
[1155]
在另一个方面,本披露提供了具有式(i’)、(i)、(i-i)、(i-i-a)、(i-i-b)、(i-i-c)、(i-i-d)、(i-i-e)、(i-i-f)、(i-ii)、(i-ii-a)、(i-ii-b)、(i-ii-c)、(i-ii-d)、(i-ii-e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、(ia-xiii)、(ia-xiv)、(ie)、(if)、(ig)、(ih)、(ih-i)和(ih-ii)的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,用于在治疗有需要的受试者的血红蛋白病,例如β-血红蛋白病的方法中使用,该方法包括向受试者施用治疗有效量的具有式(i’)、(i)、(i-i)、(i-i-a)、(i-i-b)、(i-i-c)、(i-i-d)、(i-i-e)、(i-i-f)、(i-ii)、(i-ii-a)、(i-ii-b)、(i-ii-c)、(i-ii-d)、(i-ii-e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、
(ia-xiii)、(ia-xiv)、(ie)、(if)、(ig)、(ih)、(ih-i)和(ih-ii)的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体。
[1156]
在另一个方面,本披露提供了具有式(i’)、(i)、(i-i)、(i-i-a)、(i-i-b)、(i-i-c)、(i-i-d)、(i-i-e)、(i-i-f)、(i-ii)、(i-ii-a)、(i-ii-b)、(i-ii-c)、(i-ii-d)、(i-ii-e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、(ia-xiii)、(ia-xiv)、(ie)、(if)、(ig)、(ih)、(ih-i)和(ih-ii)的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,用于在治疗有需要的受试者的镰状细胞病的方法中使用,该方法包括向受试者施用治疗有效量的具有式(i’)、(i)、(i-i)、(i-i-a)、(i-i-b)、(i-i-c)、(i-i-d)、(i-i-e)、(i-i-f)、(i-ii)、(i-ii-a)、(i-ii-b)、(i-ii-c)、(i-ii-d)、(i-ii-e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、(ia-xiii)、(ia-xiv)、(ie)、(if)、(ig)、(ih)、(ih-i)和(ih-ii)的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体。
[1157]
在另一个方面,本披露提供了具有式(i’)、(i)、(i-i)、(i-i-a)、(i-i-b)、(i-i-c)、(i-i-d)、(i-i-e)、(i-i-f)、(i-ii)、(i-ii-a)、(i-ii-b)、(i-ii-c)、(i-ii-d)、(i-ii-e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、(ia-xiii)、(ia-xiv)、(ie)、(if)、(ig)、(ih)、(ih-i)和(ih-ii)的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体,用于在治疗有需要的受试者的β-地中海贫血的方法中使用,该方法包括向受试者施用治疗有效量的具有式(i’)、(i)、(i-i)、(i-i-a)、(i-i-b)、(i-i-c)、(i-i-d)、(i-i-e)、(i-i-f)、(i-ii)、(i-ii-a)、(i-ii-b)、(i-ii-c)、(i-ii-d)、(i-ii-e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、(ia-xiii)、(ia-xiv)、(ie)、(if)、(ig)、(ih)、(ih-i)和(ih-ii)的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体。
[1158]
在一个实施例中,重型或中度β-地中海贫血是纯合无效突变或复合杂合突变的结果,其导致β-球蛋白缺乏和β-地中海贫血的表型并发症,无论是否是输血依赖型的。
[1159]
剂量
[1160]
对于约50-70kg的受试者,本披露的药物组合物或组合可以处于约1-1000mg一种或多种活性成分、或约1-500mg或约1-250mg或约1-150mg或约0.5-100mg、或约1-50mg的活性成分的单位剂量。化合物、药物组合物或其组合的治疗有效剂量取决于治疗中的受试者的物种、体重、年龄及个体情况、障碍或疾病或其严重程度。
[1161]
使用有利的哺乳动物(例如,小鼠、大鼠、狗、猴)或其分离的器官、组织和制品在体外和体内测试中可证明上述剂量特性。本披露的化合物能以溶液(例如水溶液)的形式体外应用,以及例如以悬浮液或以水溶液的形式肠内、肠胃外(有利地,静脉内)体内应用。体外剂量可在约10-3
摩尔和10-9
摩尔浓度之间的范围内。取决于施用途径,体内治疗有效量可以在约0.1-500mg/kg之间、或约1-100mg/kg之间的范围内。
[1162]
可以通过实例中所述的体外方法对根据本披露的化合物的活性进行评估。
[1163]
组合疗法
[1164]
在另一个方面,本披露提供了药物组合,该药物组合包含具有式(i’)、(i)、(i-i)、(i-i-a)、(i-i-b)、(i-i-c)、(i-i-d)、(i-i-e)、(i-i-f)、(i-ii)、(i-ii-a)、(i-ii-b)、(i-ii-c)、(i-ii-d)、(i-ii-e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、(ia-xiii)、(ia-xiv)、(ie)、(if)、(ig)、(ih)、(ih-i)和(ih-ii)的化合物或其药学上可接受的盐、水合物、溶剂化物、前药、立体异构体、或互变异构体以及一种或多种另外的治疗剂,用于在治疗中同时、分开或顺序使用。在一个实施例中,另外的治疗剂是骨髓抑制剂,例如羟基脲。
[1165]
组合疗法包括将主题化合物进一步与其他生物学活性成分(例如但不限于第二且不同的抗肿瘤药剂,或靶向hbf或另一种癌症靶标的治疗剂)和非药物疗法(例如但不限于手术或辐射治疗)组合施用。例如,本技术的化合物可以与其他药物活性化合物(优选地,能够增强本技术的化合物的作用的化合物)组合使用。
[1166]
本披露的化合物可以与一种或多种其他的治疗剂同时施用或在所述治疗剂之前或之后施用。本披露的化合物可以通过相同或不同的施用途径分开施用,或在与其他药剂相同的药物组合物中一起施用。治疗剂是例如化学化合物、肽、抗体、抗体片段或核酸,所述治疗剂当与本披露的化合物组合施用至患者时具有治疗活性或增强治疗活性。因此,在一个实施例中,本披露提供了组合,该组合包含治疗有效量的具有式(i’)、(i)、(i-i)、(i-i-a)、(i-i-b)、(i-i-c)、(i-i-d)、(i-i-e)、(i-i-f)、(i-ii)、(i-ii-a)、(i-ii-b)、(i-ii-c)、(i-ii-d)、(i-ii-e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、(ia-xiii)、(ia-xiv)、(ie)、(if)、(ig)、(ih)、(ih-i)和(ih-ii)的化合物或其药学上可接受的盐以及一种或多种另外的治疗活性剂。
[1167]
在一个实施例中,本披露提供了产品,该产品包含具有式(i’)、(i)、(i-i)、(i-i-a)、(i-i-b)、(i-i-c)、(i-i-d)、(i-i-e)、(i-i-f)、(i-ii)、(i-ii-a)、(i-ii-b)、(i-ii-c)、(i-ii-d)、(i-ii-e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、(ia-xiii)、(ia-xiv)、(ie)、(if)、(ig)、(ih)、(ih-i)和(ih-ii)的化合物以及至少一种其他治疗剂,作为组合制剂用于在治疗中同时、分开或顺序使用。在一个实施例中,所述疗法是治疗由wiz调节的疾病或病症。作为组合制剂提供的产品包括组合物,该组合物包含具有式(i’)、(i)、(i-i)、(i-i-a)、(i-i-b)、(i-i-c)、(i-i-d)、(i-i-e)、(i-i-f)、(i-ii)、(i-ii-a)、(i-ii-b)、(i-ii-c)、(i-ii-d)、(i-ii-e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、(ia-xiii)、(ia-xiv)、(ie)、(if)、(ig)、(ih)、(ih-i)和(ih-ii)的化合物以及在同一药物组合物中一起存在的其他一种或多种治疗剂,或包含具有式(i’)、(i)、(i-i)、(i-i-a)、(i-i-b)、(i-i-c)、(i-i-d)、(i-i-e)、(i-i-f)、(i-ii)、(i-ii-a)、(i-ii-b)、(i-ii-c)、(i-ii-d)、(i-ii-e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、(ia-xiii)、(ia-xiv)、(ie)、(if)、(ig)、(ih)、(ih-i)和(ih-ii)的化合物以及呈分开
形式(例如呈试剂盒的形式)的其他一种或多种治疗剂。
[1168]
在一个实施例中,本披露提供了药物组合物,所述药物组合物包含具有式(i’)、(i)、(i-i)、(i-i-a)、(i-i-b)、(i-i-c)、(i-i-d)、(i-i-e)、(i-i-f)、(i-ii)、(i-ii-a)、(i-ii-b)、(i-ii-c)、(i-ii-d)、(i-ii-e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、(ia-xiii)、(ia-xiv)、(ie)、(if)、(ig)、(ih)、(ih-i)和(ih-ii)的化合物以及其他一种或多种治疗剂。任选地,所述药物组合物可以包含如上所述的药学上可接受的载体。
[1169]
在一个实施例中,本披露提供了试剂盒,所述试剂盒包含两种或更多种分开的药物组合物,其中至少一种药物组合物含有具有式(i’)、(i)、(i-i)、(i-i-a)、(i-i-b)、(i-i-c)、(i-i-d)、(i-i-e)、(i-i-f)、(i-ii)、(i-ii-a)、(i-ii-b)、(i-ii-c)、(i-ii-d)、(i-ii-e)、(i-ii-f)、(ia)、(ib)、(ic)、(id)、(ia-i)、ia-ii)、(ia-iii)、(ia-iv)、(ia-v)、(ia-vi)、(ia-vii)、(ia-viii)、(ia-ix)、(ia-x)、(ia-xi)、(ia-xii)、(ia-xiii)、(ia-xiv)、(ie)、(if)、(ig)、(ih)、(ih-i)和(ih-ii)的化合物。在一个实施例中,所述试剂盒包含用于分开保留所述组合物的装置(例如容器、分隔瓶或分隔箔包)。这种试剂盒的实例是泡罩包装,如通常用于包装片剂、胶囊及类似物的泡罩包装。
[1170]
本披露的试剂盒可用于施用不同的剂型,例如口服和肠胃外剂型,用于以不同的剂量间隔施用分开的组合物,或用于相互滴定分开的组合物。为了促进依从性,本披露的试剂盒通常包含施用说明书。
[1171]
在本披露的组合疗法中,本披露的化合物和其他治疗剂可以由相同或不同的制造商生产和/或配制。此外,本发明的化合物和其他治疗剂可以在以下情况下放在一起组合成组合疗法:(i)在向医师发布组合产品(例如,在包含本披露的化合物和另一种治疗剂的试剂盒的情况下)之前进行;(ii)在施用之前不久,由医师自身(或在医师的指导下)进行;(iii)在患者本身中,例如在顺序施用本披露的化合物和另一种治疗剂期间进行。
[1172]
化合物的制备
[1173]
应当理解,在以下描述中,仅当所描绘式的取代基和/或变量的组合产生稳定化合物时,此类组合才是被允许的。
[1174]
本领域技术人员还应理解,在下文所述的方法中,中间体化合物的官能团可能需要通过合适的保护基团保护。此类官能团包括羟基、酚、氨基和羧酸。用于羟基或酚的合适保护基团包括三烷基甲硅烷基或二芳基烷基甲硅烷基(例如,叔丁基二甲基甲硅烷基、叔丁基二苯基甲硅烷基或三甲基甲硅烷基)、四氢吡喃基、苄基、经取代的苄基、甲基等等。用于氨基、脒基和胍基的合适保护基团包括叔丁氧基羰基、苄氧基羰基等等。用于羧酸的合适保护基团包括烷基酯、芳基酯或芳基烷基酯。
[1175]
保护基团可以根据标准技术添加或除去,所述标准技术是本领域技术人员熟知的并且如本文所述。保护基团的用途详细地描述于j.f.w.mcomie,“protective groups in organic chemistry[有机化学中的保护基团]”,plenum press[plenum出版社],伦敦和纽约1973;t.w.greene和p.g.m.wuts,“greene's protective groups in organic synthesis[格林有机合成中的保护基团]”,第四版,wiley[威利出版社],纽约2007;p.j.kocienski,“protecting groups[保护基团]”,第三版,georg thieme verlag[格奥尔格蒂梅出版社],斯图加特和纽约2005;以及在"methoden der organischen chemie"
(methods of organic chemistry)[有机化学方法],houben weyl,第4版,第15卷/i,georg thieme verlag[格奥尔格蒂梅出版社],斯图加特1974。
[1176]
所述保护基团也可以是聚合物树脂,例如王氏(wang)树脂或2-氯三苯甲基-氯树脂。
[1177]
以下反应方案说明了制备本披露化合物的方法。应当理解,本领域技术人员将能够通过类似的方法或通过本领域技术人员已知的方法来制造这些化合物。一般来讲,起始组分和试剂可以从以下来源获得,例如西格玛奥德里奇公司(sigma aldrich)、兰开斯特合成有限公司(lancaster synthesis,inc.)、五月桥公司(maybridge)、矩阵科学公司(matrix scientific)、tci公司、美国氟化学公司(fluorochem usa)、strem公司、其他商业供应商,或可以根据本领域技术人员已知的来源合成,或根据本披露所述进行制备。
[1178]
分析方法、材料和仪器
[1179]
除非另有说明,否则使用从商业供应商处收到的试剂和溶剂。除非另有说明,否则在bruker avance光谱仪或varian oxford 400mhz光谱仪上获得质子核磁共振(nmr)光谱。光谱以ppm(δ)给出,并且以赫兹报告偶联常数j。将四甲基硅烷(tms)用作内标。相对于二甲基亚砜(δ2.50)、甲醇(δ3.31)、氯仿(δ7.26)或nmr光谱数据中所示的其他溶剂,以ppm报告化学位移。将少量干燥样品(2-5mg)溶于适当的氘代溶剂(1ml)中。化学名称使用来自cambridgesoft的chembiodraw ultra v12生成。
[1180]
使用waters系统(acquity uplc和micromass zq质谱仪)或agilent-1260infinity(6120四极杆)收集质谱(esi-ms);除非另有说明,否则报告的所有质量均为质子化的母离子的m/z。将样品溶解于合适的溶剂(如mecn、dmso、或meoh)中,并且使用自动样品处理器将其直接注入柱中。在waters acquity uplc系统上进行分析(柱:waters acquity uplc beh c18 1.7μm,2.1x30mm;流速:1ml/min;55℃(柱温);溶剂a:水中的0.05%甲酸,溶剂b:meoh中的0.04%甲酸;梯度:从0至0.10min,95%溶剂a;从0.10至0.50min,95%溶剂a至20%溶剂a;从0.50至0.60min,20%溶剂a至5%溶剂a;从0.6至0.8min,保持在5%溶剂a;从0.80至0.90min,5%溶剂a至95%溶剂a;以及从0.90至1.15min,保持在95%溶剂a)。
[1181]
缩写:
[1182]
acn
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
乙腈
[1183]
acoh
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
乙酸
[1184]
aibn
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
偶氮二异丁腈
[1185]
aq.
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
水性
[1186]
b2pin2ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
双(频哪醇)二硼
[1187]
boc2o
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
二碳酸二叔丁酯
[1188]
bn
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
苄基
[1189]
bnbr
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
苄基溴
[1190]
br
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
宽峰
[1191]dꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
双重峰
[1192]
dd
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
双二重峰
[1193]
ddd
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
双重双重双重峰
[1194]
ddq
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
双重双重四重峰
[1195]
ddt
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
双重双重三重峰
[1196]
dq
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
双四重峰
[1197]
dt
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
双三重峰
[1198]
dtbbpy
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
4,4
′‑
二-叔丁基-2,2
′‑
二吡啶基
[1199]
dtd
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
双重三重双重峰
[1200]
cs2co3ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
碳酸铯
[1201]
dce
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
1,2-二氯乙烷
[1202]
dcm
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
二氯甲烷
[1203]
dhp
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
二氢吡喃
[1204]
dibal-h
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
氢化二异丁基铝
[1205]
dipea(diea)
ꢀꢀꢀꢀꢀꢀ
二异丙基乙胺
[1206]
dipea
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
n,n-二异丙基乙胺
[1207]
dma
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
n,n-二甲基乙酰胺
[1208]
dmap
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
4-二甲基氨基吡啶
[1209]
dme
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
1,2-二甲氧基乙烷
[1210]
dmf
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
n,n-二甲基甲酰胺
[1211]
dmp
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
戴斯-马丁高碘烷或1,1,1-三(乙酰氧基)-1,1-二氢-1,2-苯碘酰-3-(1h)-酮
[1212]
dmso
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
二甲亚砜
[1213]
ec
50
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
半数最大有效浓度
[1214]
elsd
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
蒸发光散射检测器
[1215]
etoh
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
乙醇
[1216]
et2o
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
二乙醚
[1217]
et3n
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
三乙胺
[1218]
etoac
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
乙酸乙酯
[1219]
hatu
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
1-[双(二甲基氨基)亚甲基]-1h-1,2,3-三唑并[4,5-b]吡啶鎓3-氧化物六氟磷酸盐
[1220]
hcl
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
氯化氢
[1221]
hept
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
七重峰
[1222]
hplc
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
高效液相色谱法
[1223]
h或hr
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
小时
[1224]
hrms
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
高分辨质谱法
[1225]gꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
克
[1226]
g/min
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
克/分钟
[1227]
ic
50
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
半数最大抑制浓度
[1228]
ipa(iproh)
ꢀꢀꢀꢀꢀꢀꢀ
异丙醇
[1229]
ir[(df(cf3)ppy)2dtbbpy]pf
6 [4,4
′‑
双(1,1-二甲基乙基)-2,2
′‑
二吡啶-n1,n1
′
]双[3,5-二氟-2-[5-(三氟甲基)-2-吡啶基-n]苯基-c]铱(iii)六氟磷酸盐
[1230]
k2co3ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
碳酸钾
[1231]
ki
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
碘化钾
[1232]
koac
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
乙酸钾
[1233]
k3po4ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
磷酸三钾
[1234]
lcms
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
液相色谱质谱法
[1235]
lda
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
二异丙基氨基锂
[1236]mꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
多重峰
[1237]
mecn
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
乙腈
[1238]
meoh
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
甲醇
[1239]
mg
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
毫克
[1240]
mhz
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
兆赫
[1241]
min
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
分钟
[1242]
ml
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
毫升
[1243]
mmol
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
毫摩尔
[1244]mꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
摩尔
[1245]
ms
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
质谱法
[1246]
nah
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
氢化钠
[1247]
nahco3ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
碳酸氢钠
[1248]
nabh(oac)3ꢀꢀꢀꢀꢀꢀꢀ
三乙酰氧基硼氢化钠
[1249]
na2so4ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
硫酸钠
[1250]
nbs
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
n-溴代琥珀酰亚胺
[1251]
nmm
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
n-甲基吗啉
[1252]
nmp
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
n-甲基-2-吡咯烷酮
[1253]
nmr
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
核磁共振
[1254]
on
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
过夜
[1255]
pd/c
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
钯碳
[1256]
pdcl2(dppf)
·
dcm 与二氯甲烷复合的[1,1'-双(二苯基膦基)二茂铁]二氯钯(ii)二氯甲烷
[1257]
pd(pph3)4ꢀꢀꢀꢀꢀꢀꢀꢀ
四(三苯基膦)钯(0)
[1258]
pmb
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
对甲氧基苄基
[1259]qꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
四重峰
[1260]
qd
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
四重双重峰
[1261]
quint
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
五重峰
[1262]
quintd
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
五重双重峰
[1263]
rbf
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
圆底烧瓶
[1264]
rockphos g3 pd
ꢀꢀꢀ
[(2-二-叔丁基膦基-3-甲氧基-6-甲基-2
′
,4
′
,6
′‑
三异丙基-1,1
′‑
联苯)-2-(2-氨基联苯)]甲磺酸钯(ii)
[1265]
rt或r.t.
ꢀꢀꢀꢀꢀꢀꢀꢀꢀ
室温
[1266]
rt
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
保留时间
[1267]sꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
单峰
[1268]
sem
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
2-(三甲基甲硅烷基)乙氧基甲基
[1269]
snbu3ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
三丁基锡
[1270]
t
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
三重峰
[1271]
td
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
三重双重峰
[1272]
tdd
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
三重双重双重峰
[1273]
tbai
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
四丁基碘化铵
[1274]
tea(net3)
ꢀꢀꢀꢀꢀꢀꢀꢀ
三乙胺
[1275]
tfa
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
三氟乙酸
[1276]
tfoh
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
三氟甲磺酸
[1277]
thf
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
四氢呋喃
[1278]
thp
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
四氢吡喃
[1279]
tmp
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
2,2,6,6-四甲基哌啶
[1280]
ts
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
甲苯磺酰基
[1281]
tt
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
三重三重峰
[1282]
ttd
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
三重三重双重峰
[1283]
tlc
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
薄层色谱法
[1284]
uplc
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
超高效液相色谱法
[1285]
xphos pd g2
ꢀꢀꢀꢀꢀꢀ
氯(2-二环己基膦基-2’,4’,6
’‑
三异丙基-1,1
’‑
联苯)[2-(2
’‑
氨基-1,1
’‑
联苯)]钯(ii)
[1286]
μw或uw
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
微波
[1287]
通用方法i-用内酯进行光氧化还原催化的代表性程序
[1288]
向40ml小瓶中装入5-溴异苯并呋喃-1(3h)-酮(5-i)(1当量)、醇结构单元(1当量)、nicl2(甘醇二甲醚)(0.05当量)、dtbbpy(0.05当量)和ir[(df(cf3)ppy)2dtbbpy]pf6(0.01当量)。然后添加acn(0.186m),随后添加2,2,6,6-四甲基哌啶(1当量)。将反应烧瓶抽真空并用氮气回填三次。将所得混合物放置于macmillian蓝色led光反应器中18小时。然后将反应混合物过滤并将固体用二氯甲烷洗涤。将滤液浓缩并通过反相hplc或硅胶色谱法纯化。
[1289]
通用方法ii-boc脱保护的代表性程序
[1290]
将氨基-醚内酯实例(4)-i(1当量)悬浮于二噁烷(0.2m)。然后添加二噁烷中的4m hcl(6当量),并将所得混合物在40℃下搅拌2小时。将反应混合物在减压下浓缩以提供游离氨基-醚内酯实例。(4)-ii。将获得的产物不经纯化用于下个步骤。
[1291]
通用方法iii-减少胺化的代表性程序
[1292]
将游离氨基-醚内酯实例(4)-ii(1当量)悬浮于dmf(0.2m)。添加醛(3当量)。将反应在室温下搅拌5分钟,然后添加nabh(oac)3(3当量)。将反应在室温下搅拌18小时。将反应用饱和水性碳酸氢钠淬灭并用二氯甲烷萃取三次。将有机相合并,通过相分离器并浓缩。将粗材料通过硅胶色谱法纯化。
[1293]
通用方法iv-开socl2内酯的代表性程序
[1294]
向在70℃下搅拌的内酯(1当量)在二氯乙烷(0.2m)和etoh(0.2m)中的溶液逐滴添
加亚硫酰氯(12当量),并将所得混合物在70℃下搅拌过夜。将反应混合物冷却至室温,用水稀释,并用饱和水性碳酸氢钠淬灭。将反应混合物用etoac萃取三次,并将合并的有机相通过相分离器并浓缩到上。将粗材料通过硅胶色谱法纯化。
[1295]
通用方法v-内酰胺环闭合的代表性程序
[1296]
在2ml微波小瓶中,将3-氨基哌啶-2,6-二酮盐酸盐(2当量)溶解于dmf(0.2m)中。然后添加dipea(5当量)并且将所得混合物在室温下搅拌15分钟。将α-氯酯(1当量)溶解于dmf(0.2m)中并添加,并且在85℃下继续搅拌18小时,然后在150℃在微波辐射下搅拌2小时。将反应混合物浓缩到上并通过硅胶柱色谱法纯化。
[1297]
通用方法vi-用3-(5-溴-1-氧代异吲哚啉-2-基)-1-((2-(三甲基甲硅烷基)乙氧基)甲基)哌啶-2,6-二酮进行光氧化还原催化的代表性程序
[1298]
向8ml红色加盖的小瓶中添加3-(5-溴-1-氧代异吲哚啉-2-基)-1-((2-(三甲基甲硅烷基)乙氧基)甲基)哌啶-2,6-二酮int-xxx(1当量)、醇结构单元(1.2当量)、dtbbpy(0.05当量)、nicl2(甘醇二甲醚)(0.05当量)和ir[(df(cf3)ppy)2dtbbpy]pf6(0.01当量)。然后添加acn(0.3m),随后添加2,2,6,6-四甲基哌啶(1.05当量)。将反应烧瓶抽真空并用氮气回填三次。将反应混合物放置于蓝色led光下的光反应器板中18小时,然后过滤并浓缩。
[1299]
通用方法vii-整体脱保护的代表性程序
[1300]
向sem保护的戊二酰亚胺、boc保护的胺和异吲哚啉衍生物(实例int-2)(1当量)在acn(0.11m)中的溶液添加甲磺酸(11.2当量)。将所得混合物在室温下搅拌72小时,并且然后冷却至0℃。然后添加三乙胺(13.04当量),随后添加n1,n2-二甲基乙烷-1,2-二胺(1.5当量)。然后将反应混合物在室温下搅拌4小时,浓缩,并通过反相hplc纯化。
[1301]
int-xxx的制备方法:
[1302]
3-(5-溴-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(int-xx)
[1303][1304]
步骤1.乙基4-溴-2-(氯甲基)苯甲酸酯(1-1b)
[1305]
将5-溴苯酞1-1a(1200g,5.633mol)在etoh(12l)中的搅拌的悬浮液加热至68℃-72℃。然后经7h的时间逐滴添加socl2(2.40l,33.0mol)。将反应混合物在减压下浓缩至约4l,然后添加水(5l)和mtbe(5l)。将所得混合物搅拌40min。分离各相,并将水相用mtbe(1x5l)萃取。将合并的有机层用5%水性nahco3(5l)洗涤,经na2so4干燥,过滤并浓缩至干燥,以提供呈浅棕色固体的1-1b(1450g,5.25mol,93%产率)。ms[m na]
=298.9。1h nmr(400mhz,氯仿-d)δ7.85(d,j=8.4hz,1h),7.72(d,j=2.0hz,1h),7.52(dd,j=8.3,2.0hz,1h),5.00(s,2h),4.38(q,j=7.1hz,2h),1.40(t,j=7.1hz,3h)。
[1306]
步骤2. 3-(5-溴-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(int-xx)
[1307]
向3-氨基哌啶-2,6-二酮盐酸盐1-1c(596.3g,3.623mol)和i-pr2net(2.50l,14.3mol)在dmf(5.0l)中的搅拌的悬浮液添加1-1b(1000g,3.623mmol),并将所得反应混合物在85℃-90℃下搅拌24h。然后允许反应混合物冷却至室温,添加水(20l),并将所得混合
物搅拌12h。将形成的沉淀过滤,并用水(5l)和meoh(2l)洗涤。将粗固体在meoh(5l)中浆化1h,过滤,并用meoh(2l)洗涤。然后将所得固体置于etoac(10l)中并搅拌1h。然后将所获得的悬浮液过滤,用etoac(5l)洗涤,并在减压下在45℃-50℃干燥以得到呈灰白色固体的int-xx(740g,2.29mol,63%产率)。ms[m 1]
=323.2。1h nmr(400mhz,dmso-d6)δ10.99(s,1h),7.91-7.88(m,1h),7.72(dd,j=8.1,1.6hz,1h),7.67(d,j=8.0hz,1h),5.11(dd,j=13.3,5.1hz,1h),4.47(d,j=17.7hz,1h),4.34(d,j=17.7hz,1h),2.98-2.83(m,1h),2.65-2.55(m,1h),2.45-2.29(m,1h),2.01(dtd,j=12.7,5.3,2.3hz,1h)。
[1308]
3-(5-溴-1-氧代异吲哚啉-2-基)-1-((2-(三甲基甲硅烷基)乙氧基)甲基)哌啶-2,6-二酮(int-xxx)
[1309][1310]
在0℃下,向int-xx(10.0g,30.9mmol)和dbu(6.9ml,46mmol)在dmf(95ml)中的搅拌溶液中添加semcl(6.6ml,37mmol),并允许所得反应混合物升温至室温然后搅拌5h。添加另外部分的dbu(3.5ml,23mmol)和semcl(3.3ml,19mmol)并继续再搅拌2h。然后将反应混合物用饱和水性nh4cl(250ml)淬灭并且用etoac(x 3)萃取。将合并的有机相经na2so4干燥,过滤,并浓缩至干燥。将粗材料溶解于最少量的etoac(约50ml)中,并添加et2o:庚烷(v/v=1:2,400ml)。将所得混浊溶液在-5℃静置过夜。将形成的沉淀过滤,用庚烷洗涤(x3),并在真空下干燥以得到呈灰白色固体的int-xxx(11.53g,25.4mmol,82%产率)。ms[m h]
=453.4。1h nmr(400mhz,氯仿-d)δ7.75(d,j=8.6hz,1h),7.66-7.61(m,2h),5.37-5.09(m,3h),4.48(d,j=16.2hz,1h),4.32(d,j=16.2hz,1h),3.74-3.50(m,2h),3.11-2.98(m,1h),2.94-2.83(m,1h),2.33(qd,j=13.2,4.7hz,1h),2.24-2.15(m,1h),0.97-0.90(m,2h),0.00(s,9h)。
[1311]
实例1:叔丁基2-(1-羟基乙基)哌啶-1-甲酸酯(int-1)的非对映异构体混合物
[1312][1313]
向20ml小瓶中装入1-(哌啶-2-基)乙醇(0.5g,3.87mmol)、二碳酸二叔丁酯(0.98ml,4.26mmol)、k2co3(0.59g,4.26mmol)和thf(20ml),并将所得混合物在室温下剧烈搅拌48小时。将反应混合物用盐水稀释,并用etoac萃取三次。将有机相合并,通过相分离器并浓缩到上。将残余物通过硅胶色谱法(用在庚烷中的0-100%乙酸乙酯洗脱,使用elsd检测)纯化,以提供呈澄清油状物的叔丁基2-(1-羟基乙基)哌啶-1-甲酸酯int-1(680mg,2.97mmol,77%产率)的非对映异构体混合物。1h nmr(400mhz,氯仿-d)δ4.17-3.90(m,3h),2.99-2.68(m,1h),2.05-1.98(m,1h),1.85-1.54(m,5h),1.49(s,9h),1.23(dd,j=9.3,6.1hz,3h)。
[1314]
实例2:5-(1-(1-乙基哌啶-2-基)乙氧基)异苯并呋喃-1(3h)-酮(int-3)的非对映异构体
[1315][1316]
步骤1:叔丁基2-(1-((1-氧代-1,3-二氢异苯并呋喃-5-基)氧基)乙基)哌啶-1-甲酸酯(1)的非对映异构体混合物
[1317]
5-((r)-1-((s)-1-乙基哌啶-2-基)乙氧基)异苯并呋喃-1(3h)-酮,5-((s)-1-((s)-1-乙基哌啶-2-基)乙氧基)异苯并呋喃-1(3h)-酮,
[1318]
5-((s)-1-((r)-1-乙基哌啶-2-基)乙氧基)异苯并呋喃-1(3h)-酮,5-((r)-1-((r)-1-乙基哌啶-2-基)乙氧基)异苯并呋喃-1(3h)-酮。
[1319]
根据通用方法i,从5-溴异苯并呋喃-1(3h)-酮和叔丁基2-(1-羟基乙基)哌啶-1-甲酸酯int-1(0.67g,2.93mmol)的非对映异构体混合物开始制备产物。将反应混合物过滤,并且将固体用二氯甲烷洗涤。将滤液浓缩,并将粗材料溶解于最少的甲醇中并通过反相elsd/uv触发的硅胶色谱法(用均含有5mm nh4oac作为改性剂的5-50%95:5acn:h2o至95:5h2o:acn洗脱)纯化,以提供呈橙色固体的叔丁基2-(1-((1-氧代-1,3-二氢异苯并呋喃-5-基)氧基)乙基)哌啶-1-甲酸酯1的非对映异构体混合物(533mg,1.46mmol,50.3%产率)。可替代地,可以将粗材料通过硅胶色谱法(用在庚烷中的含1%tea的0-100%3:1etoac:etoh洗脱)纯化,以提供所希望的产物。lcms[m h-叔丁基]
:306.1。1h nmr(400mhz,氯仿-d)δ7.69(d,j=8.5hz,1h),6.91(dd,j=8.5,2.1hz,1h),6.79(dd,j=6.9,2.0hz,1h),5.12(d,j=6.0hz,2h),4.64(ddd,j=14.1,8.3,6.2hz,1h),4.32-4.14(m,1h),2.69-2.48(m,1h),1.90-1.81(m,1h),1.69-1.58(m,1h),1.54-1.40(m,4h),1.34(s,10h),1.19(d,j=6.1hz,3h)。
[1320]
步骤2:5-(1-(哌啶-2-基)乙氧基)异苯并呋喃-1(3h)-酮(2)的非对映异构体混合物
[1321]
根据通用方法ii,从叔丁基2-(1-((1-氧代-1,3-二氢异苯并呋喃-5-基)氧基)乙基)哌啶-1-甲酸酯1(0.53g,1.46mmol)的非对映异构体混合物开始制备产物。将反应混合物浓缩,以提供呈粗橙色固体的5-(1-(哌啶-2-基)乙氧基)异苯并呋喃-1(3h)-酮2的非对映异构体混合物。将粗产物不经纯化用于下个步骤。lcms[m h]
:262.1。
[1322]
步骤3:非对映异构体5-(1-(1-乙基哌啶-2-基)乙氧基)异苯并呋喃-1(3h)-酮(int-3):
[1323]
根据通用方法iii,从5-(1-(哌啶-2-基)乙氧基)异苯并呋喃-1(3h)-酮2(0.39g,
1.48mmol)和乙醛(0.25ml,4.42mmol)的非对映异构体混合物开始制备产物。将反应混合物用饱和水性碳酸氢钠淬灭,并用用二氯甲烷萃取三次。将有机相合并,通过相分离器并浓缩。将粗材料通过硅胶色谱法(用在二氯甲烷中的0-20%甲醇洗脱)纯化,以提供呈棕色油状物的5-(1-(1-乙基哌啶-2-基)乙氧基)异苯并呋喃-1(3h)-酮int-3的非对映异构体混合物(372mg,1.29mmol,87%产率)。lcms[m h]
:290.2。1h nmr(400mhz,氯仿-d)δ7.81(dd,j=8.5,1.9hz,1h),7.03(dd,j=8.5,2.1hz,1h),6.92(s,1h),5.24(s,2h),4.93-4.62(m,1h),3.06-2.81(m,2h),2.60-2.43(m,2h),2.32-2.17(m,1h),1.77(dd,j=27.1,14.7hz,2h),1.66-1.48(m,3h),1.35(dd,j=11.4,6.3hz,4h),1.11-0.97(m,3h)。将异构体的非对映异构体混合物通过手性sfc[柱21x250mm chiralpak ic;含10mm nh3的co2助溶剂30%ipa;以80g/min在125巴在25℃下]分离,以提供两种非对映异构体的混合物以及两种干净单一的非对映异构体:峰3:呈橙色固体的5-(1-(1-乙基哌啶-2-基)乙氧基)异苯并呋喃-1(3h)-酮的非对映异构体3(101mg,0.349mmol,23.7%)。手性sfc rt 14min。峰4:呈橙色固体的5-(1-(1-乙基哌啶-2-基)乙氧基)异苯并呋喃-1(3h)-酮的非对映异构体4(105mg,0.363mmol,24.6%)。手性sfc rt 19min。将异构体的混合物进一步通过手性sfc[柱21x250mm chiralpak ig;含10mm nh3的co2助溶剂25%1:1meoh:ipa;以80g/min在125巴在25℃下]分离,以提供另外两种非对映异构体:峰1:呈橙色固体的5-(1-(1-乙基哌啶-2-基)乙氧基)异苯并呋喃-1(3h)-酮的非对映异构体1(30.4mg,0.105mmol,7.1%)。手性sfc rt 4.9min。峰2:呈橙色固体的5-(1-(1-乙基哌啶-2-基)乙氧基)异苯并呋喃-1(3h)-酮的非对映异构体2(35mg,0.121mmol,8.2%)。手性sfc rt 4.7min。
[1324]
实例3:3-(5-(1-(1-乙基哌啶-2-基)乙氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-5)的非对映异构体
[1325][1326]
步骤1:乙基2-(氯甲基)-4-(1-(1-乙基哌啶-2-基)乙氧基)苯甲酸酯(4)的单一非对映异构体
[1327]
根据通用方法iv,从单一非对映异构体5-(1-(1-乙基哌啶-2-基)乙氧基)异苯并呋喃-1(3h)-酮int-3峰3(0.1g,0.346mmol)开始制备产物(4)。将粗材料通过硅胶色谱法
(用在庚烷中的0-100%乙酸乙酯洗脱)纯化,以提供呈橙色油状物的单一非对映异构体乙基2-(氯甲基)-4-(1-(1-乙基哌啶-2-基)乙氧基)苯甲酸酯4(102mg,0.288mmol,83%产率)。lcms[m h]
:354.6。1h nmr(400mhz,氯仿-d)δ7.98(d,j=8.7hz,1h),7.07(d,j=2.6hz,1h),6.85(dd,j=8.8,2.6hz,1h),5.05(s,2h),4.65(qd,j=6.4,2.8hz,1h),4.35(q,j=7.1hz,2h),3.02-2.89(m,2h),2.58-2.49(m,1h),2.45(dt,j=10.2,2.9hz,1h),2.23(ddd,j=12.0,10.8,3.2hz,1h),1.83-1.68(m,2h),1.63-1.45(m,3h),1.39(t,j=7.1hz,3h),1.36-1.21(m,4h),1.02(t,j=7.1hz,3h)。
[1328]
步骤2:非对映异构体3-(5-(1-(1-乙基哌啶-2-基)乙氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-5)
[1329]
根据通用方法v,从单一非对映异构体乙基2-(氯甲基)-4-(1-(1-乙基哌啶-2-基)乙氧基)苯甲酸酯4(102mg,0.288mmol)开始制备化合物i-5。将反应混合物通过硅胶色谱法(用在etoac中的含1%tea的0-100%3:1etoac:etoh洗脱)纯化,以提供呈白色固体的单一非对映异构体3-(5-(1-(1-乙基哌啶-2-基)乙氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-5(28.4mg,0.069mmol,23.92%产率)。lcms[m h]
:400.3。1h nmr(400mhz,dmso-d6)δ10.97(s,1h),7.61(d,j=8.4hz,1h),7.18(d,j=2.2hz,1h),7.03(dd,j=8.4,2.2hz,1h),5.07(dd,j=13.3,5.1hz,1h),4.77-4.68(m,1h),4.39(d,j=17.2hz,1h),4.26(d,j=17.1hz,1h),2.96-2.83(m,3h),2.64-2.54(m,1h),2.45-2.30(m,2h),2.26-2.13(m,1h),2.01-1.92(m,1h),1.70(d,j=10.2hz,2h),1.55-1.22(m,8h),0.94(t,j=7.0hz,3h)。
[1330]
实例4:非对映异构体3-(5-(1-(1-乙基哌啶-2-基)乙氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-7)
[1331][1332]
步骤1:单一非对映异构体乙基2-(氯甲基)-4-(1-(1-乙基哌啶-2-基)乙氧基)苯甲酸酯(6)
[1333]
根据通用方法iv,从单一非对映异构体5-(1-(1-乙基哌啶-2-基)乙氧基)异苯并呋喃-1(3h)-酮int-3峰4(0.1g,0.346mmol)开始制备中间体6。将粗材料通过反相硅胶色谱法(用在含0.1%tfa作为改性剂的水中的5%-60%acn洗脱)纯化。将含有产物的级分合并并且浓缩至最少水相。将水相用二氯甲烷萃取三次。将有机相合并,通过相分离器并浓缩,
以提供呈橙色油状物的单一非对映异构体乙基2-(氯甲基)-4-(1-(1-乙基哌啶-2-基)乙氧基)苯甲酸酯6(104mg,0.294mmol,85%产率)。lcms[m h]
:354.3。
[1334]
步骤2:非对映异构体3-(5-(1-(1-乙基哌啶-2-基)乙氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-7)
[1335]
根据通用方法v,从乙基2-(氯甲基)-4-(1-(1-乙基哌啶-2-基)乙氧基)苯甲酸酯6(104mg,0.294mmol)开始制备化合物i-7。将粗材料通过硅胶色谱法(用在etoac中的含1%三乙胺的0-100%3:1etoac:etoh洗脱)纯化,以提供呈灰色固体的单一非对映异构体3-(5-(1-(1-乙基哌啶-2-基)乙氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-7(40.5mg,0.096mmol,32.8%产率)。lcms[m h]
:400.3。1h nmr(400mhz,dmso-d6)δ10.99(s,1h),7.65(d,j=8.4hz,1h),7.19(d,j=2.1hz,1h),7.06(dd,j=8.5,2.2hz,1h),5.04(dd,j=13.3,5.1hz,1h),4.75(dd,j=6.3,3.1hz,1h),4.41(d,j=17.3hz,1h),4.28(d,j=17.3hz,1h),2.96-2.82(m,3h),2.67-2.59(m,1h),2.50-2.32(m,2h),2.24(t,j=11.2hz,1h),2.05-1.96(m,1h),1.77-1.67(m,2h),1.58-1.19(m,8h),0.95(t,j=7.0hz,3h)。
[1336]
实例5:非对映异构体3-(5-(1-(1-乙基哌啶-2-基)乙氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-9)
[1337][1338]
步骤1:单一非对映异构体乙基2-(氯甲基)-4-(1-(1-乙基哌啶-2-基)乙氧基)苯甲酸酯(8)
[1339]
根据通用方法iv,从5-(1-(哌啶-2-基)乙氧基)异苯并呋喃-1(3h)-酮int-3峰2(43.1mg,0.149mmol)开始制备中间体8。将粗材料通过反相硅胶色谱法(在含有0.1%tfa作为改性剂的水中的5%-50%acn)纯化。将含有产物的级分合并并且浓缩成最少水相。将水相用二氯甲烷萃取三次。将有机相合并,通过相分离器,并浓缩,以提供呈黄色油状物的单一非对映异构体乙基2-(氯甲基)-4-(1-(1-乙基哌啶-2-基)乙氧基)苯甲酸酯8(52mg,0.147mmol,99%产率)。lcms[m h]
:354.3。
[1340]
步骤2:非对映异构体3-(5-(1-(1-乙基哌啶-2-基)乙氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-9)
[1341]
根据通用方法v,从单一非对映异构体乙基2-(氯甲基)-4-(1-(1-乙基哌啶-2-基)
乙氧基)苯甲酸酯8(0.052g,0.147mmol)开始制备化合物i-9。将反应混合物通过硅胶(用在etoac中的含1%tea的0-100%3:1etoac:etoh洗脱)纯化,以提供呈奶油色固体的单一非对映异构体3-(5-(1-(1-乙基哌啶-2-基)乙氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-9(16.6mg,37μmol,25.5%产率)。lcms[m h]
:400.1。1h nmr(400mhz,dmso-d6)δ10.97(s,1h),7.61(d,j=8.4hz,1h),7.21(d,j=2.1hz,1h),7.06(dd,j=8.4,2.2hz,1h),5.07(dd,j=13.3,5.1hz,1h),4.98(p,j=6.1hz,1h),4.39(d,j=17.1hz,1h),4.26(d,j=17.1hz,1h),2.96-2.81(m,2h),2.78-2.71(m,1h),2.63-2.55(m,1h),2.48-2.31(m,3h),2.18-2.10(m,1h),2.02-1.92(m,1h),1.79-1.65(m,2h),1.57-1.51(m,1h),1.44-1.27(m,2h),1.22(dd,j=6.2,1.3hz,3h),1.19-1.11(m,1h),0.96(t,j=7.1hz,3h)。
[1342]
实例6:非对映异构体3-(5-(1-(1-乙基哌啶-2-基)乙氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-11)
[1343][1344]
步骤1:单一非对映异构体乙基2-(氯甲基)-4-(1-(1-乙基哌啶-2-基)乙氧基)苯甲酸酯(10)
[1345]
根据通用方法iv,从单一非对映异构体5-(1-(哌啶-2-基)乙氧基)异苯并呋喃-1(3h)-酮int-3峰1(38mg,0.131mmol)开始制备中间体10。将粗材料通过硅胶色谱法(用在庚烷中的0-100%乙酸乙酯洗脱)纯化,以提供呈黄色油状物的单一非对映异构体乙基2-(氯甲基)-4-(1-(1-乙基哌啶-2-基)乙氧基)苯甲酸酯10(43mg,0.122mmol,93%产率)。lcms[m h]
:354.1。1h nmr(400mhz,氯仿-d)δ7.99(d,j=8.8hz,1h),7.10(d,j=2.5hz,1h),6.87(dd,j=8.7,2.6hz,1h),5.06(s,2h),4.92-4.83(m,1h),4.37(q,j=7.1hz,2h),2.94(dtd,j=11.7,3.8,1.3hz,1h),2.86-2.75(m,1h),2.59-2.50(m,2h),2.24(td,j=11.5,3.2hz,1h),1.88-1.81(m,1h),1.81-1.73(m,1h),1.67-1.47(m,2h),1.43-1.38(m,4h),1.33(d,j=6.3hz,3h),1.30-1.21(m,1h),1.07(t,j=7.1hz,3h)。
[1346]
步骤2:非对映异构体3-(5-(1-(1-乙基哌啶-2-基)乙氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-11)
[1347]
根据通用方法v,从单一非对映异构体乙基2-(氯甲基)-4-(1-(1-乙基哌啶-2-基)乙氧基)苯甲酸酯10(43mg,0.122mmol)开始制备化合物i-11。将反应混合物通过硅胶(用在乙酸乙酯中的含1%tea的0-100%3:etoac:etoh洗脱)纯化,以提供呈奶油色固体的3-(5-(1-(1-乙基哌啶-2-基)乙氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-11(22.2mg,56μ
mol,45.7%产率)。lcms[m h]
:400.2。1h nmr(400mhz,dmso-d6)δ10.97(s,1h),7.61(d,j=8.4hz,1h),7.21(d,j=2.1hz,1h),7.06(dd,j=8.4,2.2hz,1h),5.07(dd,j=13.3,5.1hz,1h),4.98(p,j=6.1hz,1h),4.39(d,j=16.9hz,1h),4.26(d,j=17.1hz,1h),2.98-2.81(m,2h),2.80-2.69(m,1h),2.65-2.55(m,1h),2.41(ddd,j=26.6,13.6,5.7hz,3h),2.20-2.08(m,1h),1.98(ddd,j=10.3,5.2,2.8hz,1h),1.81-1.65(m,2h),1.59-1.50(m,1h),1.45-1.27(m,2h),1.22(dd,j=6.2,1.3hz,3h),1.19-1.11(m,1h),0.96(t,j=7.0hz,3h)。
[1348]
实例7:外消旋-叔丁基2-(羟基甲基)-3,3-二甲基哌啶-1-甲酸酯(int-12)
[1349][1350]
将外消旋1-(叔丁氧基羰基)-3,3-二甲基哌啶-2-甲酸(0.3g,1.17mmol)溶解于thf(3.9ml)中,并将所得混合物冷却至0℃。逐滴添加在thf中的1m硼烷四氢呋喃复合物(3.50ml,3.50mmol),并将反应混合物在室温下搅拌过夜,然后冷却至0℃并用甲醇(3ml,74.2mmol)淬灭,并在室温下搅拌2小时。将反应混合物浓缩至干燥,然后溶解于甲醇(5ml)中并在室温下搅拌过夜。将反应混合物浓缩到上,并通过硅胶色谱法(用在庚烷中的0-100%乙酸乙酯洗脱,使用elsd检测)纯化,以提供呈澄清油状物的外消旋-叔丁基2-(羟基甲基)-3,3-二甲基哌啶-1-甲酸酯int-12(210mg,0.863mmol,74.0%产率)。lcms[m h-叔丁基]
:188.3。1h nmr(400mhz,氯仿-d)δ4.22-3.88(m,2h),3.86-3.70(m,2h),2.96-2.62(m,1h),1.79-1.58(m,2h),1.50-1.42(m,10h),1.36-1.25(m,2h),1.03(s,3h),0.92(s,3h)。
[1351]
实例8:对映异构体3-(5-((1-乙基-3,3-二甲基哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(int-15)
[1352][1353]
步骤1:外消旋-叔丁基3,3-二甲基-2-(((1-氧代-1,3-二氢异苯并呋喃-5-基)氧基)甲基)哌啶-1-甲酸酯(13)
[1354]
根据通用方法i,从叔丁基2-(羟基甲基)-3,3-二甲基哌啶-1-甲酸酯int-12的对映异构体混合物(0.21g,0.863mmol)开始制备中间体13。将反应混合物通过硅胶色谱法(用在庚烷中的0-100%乙酸乙酯洗脱)纯化,以提供呈黄色油状物的外消旋-叔丁基3,3-二甲
基-2-(((1-氧代-1,3-二氢异苯并呋喃-5-基)氧基)甲基)哌啶-1-甲酸酯13(342mg,0.911mmol,108%产率)。lcms[m h-叔丁基]
:320.2。1h nmr(400mhz,氯仿-d)δ7.72-7.64(m,1h),6.94(dd,j=8.5,2.1hz,1h),6.89-6.83(m,1h),5.16(s,2h),4.28-3.68(m,5h),1.69-1.51(m,2h),1.45-1.29(m,11h),1.00(s,3h),0.95(s,3h)。
[1355]
步骤2:外消旋-5-((3,3-二甲基哌啶-2-基)甲氧基)异苯并呋喃-1(3h)-酮(14)
[1356]
根据通用方法ii,从叔丁基3,3-二甲基-2-(((1-氧代-1,3-二氢异苯并呋喃-5-基)氧基)甲基)哌啶-1-甲酸酯13的对映异构体混合物(342mg,0.911mmol)开始制备中间体14,以提供呈白色固体的外消旋-5-((3,3-二甲基哌啶-2-基)甲氧基)异苯并呋喃-1(3h)-酮14。将粗产物不经纯化用于下个步骤。lcms[m h]
:276.2。
[1357]
步骤3:对映异构体5-((1-乙基-3,3-二甲基哌啶-2-基)甲氧基)异苯并呋喃-1(3h)-酮(int-15)
[1358]
根据通用方法iii,从外消旋-5-((3,3-二甲基哌啶-2-基)甲氧基)异苯并呋喃-1(3h)-酮14(251mg,0.911mmol)和乙醛(0.31ml,5.47mmol)开始制备int-15。将粗材料通过硅胶色谱法(用在庚烷中的0-100%乙酸乙酯洗脱)纯化,以提供呈橙色油状物的外消旋-5-((1-乙基-3,3-二甲基哌啶-2-基)甲氧基)异苯并呋喃-1(3h)-酮int-15(143mg,0.471mmol,51.7%产率)。lcms[m h]
:304.4。1h nmr(400mhz,氯仿-d)δ7.84(d,j=8.5hz,1h),7.06(dd,j=8.5,2.1hz,1h),6.99-6.90(m,1h),5.27(s,2h),4.20-4.04(m,2h),2.98(s,3h),2.91(s,3h),2.78-2.64(m,2h),2.62-2.52(m,2h),2.46-2.35(m,1h),1.68-1.59(m,2h),1.50-1.39(m,1h),1.35-1.25(m,1h),1.06(t,j=7.0hz,3h)。将异构体的对映体混合物通过手性sfc[柱21x250mm chiralpak ig;含10mm nh3的co2助溶剂25%meoh;以80g/min在125巴在25℃下]分离,以提供对映异构体:峰1:呈黄色油状物的5-((1-乙基-3,3-二甲基哌啶-2-基)甲氧基)异苯并呋喃-1(3h)-酮(65.2mg,0.215mmol,23.59%产率)的对映异构体1。手性sfc rt 3.8min。峰2:呈橙色油状物的5-((1-乙基-3,3-二甲基哌啶-2-基)甲氧基)异苯并呋喃-1(3h)-酮(71mg,0.234mmol,25.7%产率)的对映异构体2。手性sfc rt 5.9min。
[1359]
实例9:非对映异构体3-(5-((1-乙基-3,3-二甲基哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-17)
[1360]
[1361]
步骤1:单一对映异构体乙基2-(氯甲基)-4-((1-乙基-3,3-二甲基哌啶-2-基)甲氧基)苯甲酸酯(16)
[1362]
根据通用方法iv,从5-((3,3-二甲基哌啶-2-基)甲氧基)异苯并呋喃-1(3h)-酮int-15峰1的单一对映异构体(65.2mg,0.215mmol)开始制备中间体16,以提供呈棕色油状物的乙基2-(氯甲基)-4-((1-乙基-3,3-二甲基哌啶-2-基)甲氧基)苯甲酸酯16的单一对映异构体。将粗材料无需纯化即可用于下个步骤。lcms[m h]
:368.3。
[1363]
步骤2:非对映异构体3-(5-((1-乙基-3,3-二甲基哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-17)
[1364]
根据通用方法v,从单一对映异构体乙基2-(氯甲基)-4-((1-乙基-3,3-二甲基哌啶-2-基)甲氧基)苯甲酸酯16(79mg,0.215mmol)开始制备化合物i-17。将反应混合物通过硅胶色谱法(用在庚烷中的含1%tea作为改性剂的0-100%3:1etoac:etoh洗脱)纯化。将含有所希望的产物的级分合并,浓缩并冻干,以提供呈浅紫色固体的3-(5-((1-乙基-3,3-二甲基哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-17的单一非对映异构体(37.7mg,0.090mmol,42.0%产率)。lcms[m h]
:414.5。1h nmr(400mhz,dmso-d6)δ10.89(s,1h),7.55(d,j=8.3hz,1h),7.20-7.12(m,1h),6.99(dd,j=8.4,2.2hz,1h),5.00(dd,j=13.4,5.1hz,1h),4.32(d,j=17.3hz,1h),4.26-4.07(m,2h),4.05-3.93(m,1h),2.84(ddd,j=17.2,13.6,5.4hz,1h),2.63-2.48(m,4h),2.37-2.19(m,3h),1.95-1.85(m,1h),1.51-1.41(m,2h),1.39-1.31(m,1h),1.18-1.11(m,1h),0.99(s,3h),0.91(t,j=7.0hz,3h),0.86(s,3h)。
[1365]
实例10:非对映异构体3-(5-((1-乙基-3,3-二甲基哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-19)
[1366][1367]
步骤1:单一对映异构体乙基2-(氯甲基)-4-((1-乙基-3,3-二甲基哌啶-2-基)甲氧基)苯甲酸酯(18)
[1368]
根据通用方法iv,从5-((3,3-二甲基哌啶-2-基)甲氧基)异苯并呋喃-1(3h)-酮int-15峰2的单一对映异构体(71mg,0.234mmol)开始制备中间体18,以提供呈棕色油状物的乙基2-(氯甲基)-4-((1-乙基-3,3-二甲基哌啶-2-基)甲氧基)苯甲酸酯18的单一对映异构体。将粗材料无需纯化即可用于下个步骤。lcms[m h]
:368.2。
[1369]
步骤2:非对映异构体3-(5-((1-乙基-3,3-二甲基哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-19)
[1370]
根据通用方法v,从单一对映异构体乙基2-(氯甲基)-4-((1-乙基-3,3-二甲基哌啶-2-基)甲氧基)苯甲酸酯18(86mg,0.234mmol)开始制备化合物i-19。将反应混合物通过硅胶色谱法(用在庚烷中的含1%tea作为改性剂的0-100%3:1etoac:etoh洗脱)纯化。将含有所希望的产物的级分合并,浓缩并冻干,以提供呈浅紫色固体的3-(5-((1-乙基-3,3-二甲基哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-19的非对映异构体的混合物(45.6mg,0.109mmol,46.7%产率)。lcms[m h]
:414.3。1h nmr(400mhz,dmso-d6)δ10.97(s,1h),7.63(d,j=8.3hz,1h),7.23(d,j=2.2hz,1h),7.07(dd,j=8.4,2.3hz,1h),5.08(dd,j=13.3,5.1hz,1h),4.40(d,j=17.1hz,1h),4.27(d,j=17.3hz,1h),4.23-4.16(m,1h),4.13-4.02(m,1h),2.91(ddd,j=17.1,13.6,5.4hz,1h),2.70-2.56(m,4h),2.47-2.27(m,3h),2.03-1.93(m,1h),1.57-1.47(m,2h),1.47-1.38(m,1h),1.27-1.18(m,1h),1.06(s,3h),0.99(t,j=7.0hz,3h),0.94(s,3h)。
[1371]
实例11:非对映异构体混合物叔丁基(2s)-2-(1-羟基乙基)吡咯烷-1-甲酸酯(int-20)
[1372][1373]
向100ml rbf添加n-boc-l-脯氨醛(0.5ml,2.67mmol),并将其溶解于thf(21.3ml)中,并将所得混合物冷却至-78℃。逐滴添加在二乙醚中的3m甲基溴化镁(1.78ml,5.34mmol),并将反应混合物在室温下搅拌2小时,然后冷却至-78℃。添加另外的在二乙醚中的3m甲基溴化镁(1ml,3.00mmol),在室温下继续搅拌2小时。将反应混合物冷却至0℃,用饱和水性氯化铵淬灭,并用乙酸乙酯萃取三次。将有机相合并,通过相分离器并浓缩到上。将粗材料通过硅胶色谱法(用在庚烷中的0-100%乙酸乙酯洗脱,使用elsd检测器)纯化,以提供呈澄清油状物的叔丁基(2s)-2-(1-羟基乙基)吡咯烷-1-甲酸酯int-20的非对映异构体混合物(541mg,2.51mmol,84%产率)。lcms[m h-叔丁基]
:160.1。1h nmr(400mhz,氯仿-d)δ4.01-3.90(m,1h),3.78-3.64(m,1h),3.62-3.47(m,1h),3.34-3.22(m,1h),2.07-1.93(m,1h),1.91-1.59(m,3h),1.49(s,9h),1.14(dd,j=25.7,6.2hz,3h)。
[1374]
实例12:非对映异构体5-((s)-1-((s)-1-乙基吡咯烷-2-基)乙氧基)异苯并呋喃-1(3h)-酮
2-基)乙氧基)异苯并呋喃-1(3h)-酮(116.5mg,0.423mmol,20.53%产率)的非对映异构体2。手性sfc rt 11.6min。1h nmr(400mhz,氯仿-d)δ7.71(d,j=8.5hz,1h),6.97(dd,j=8.5,2.1hz,1h),6.90(d,j=2.0hz,1h),5.18(s,2h),4.45(p,j=6.2hz,1h),3.11(dt,j=9.2,4.6hz,1h),2.92(dq,j=12.0,7.4hz,1h),2.74(dt,j=8.6,5.5hz,1h),2.35(dq,j=11.8,7.0hz,1h),2.20(q,j=8.3hz,1h),1.89-1.77(m,1h),1.74-1.62(m,3h),1.25(d,j=6.2hz,3h),1.00(t,j=7.2hz,3h)。
[1382]
实例13:非对映异构体3-(5-(1-((s)-1-乙基吡咯烷-2-基)乙氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮
[1383][1384]
步骤1:单一非对映异构体乙基2-(氯甲基)-4-(1-((s)-1-乙基吡咯烷-2-基)乙氧基)苯甲酸酯(24)
[1385]
根据通用方法iv,从5-(1-((s)-1-乙基吡咯烷-2-基)乙氧基)异苯并呋喃-1(3h)-酮int-23峰2(145.1mg,0.527mmol)开始制备中间体24。将粗材料通过硅胶色谱法(用在庚烷中的0-100%乙酸乙酯洗脱)纯化,以提供呈棕色油状物的乙基2-(氯甲基)-4-(1-((s)-1-乙基吡咯烷-2-基)乙氧基)苯甲酸酯24(152mg,0.447mmol,85%产率)。lcms[m h]
:340.2。1h nmr(400mhz,氯仿-d)δ7.97(d,j=8.7hz,1h),7.08(d,j=2.6hz,1h),6.87(dd,j=8.8,2.6hz,1h),5.05(s,2h),4.50(p,j=6.1hz,1h),4.35(q,j=7.1hz,2h),3.20-3.12(m,1h),2.97(dq,j=12.0,7.4hz,1h),2.77(dt,j=8.5,5.6hz,1h),2.39(dq,j=12.0,7.0hz,1h),2.28-2.19(m,1h),1.92-1.68(m,4h),1.39(t,j=7.1hz,3h),1.29(d,j=6.2hz,3h),1.07(t,j=7.2hz,3h)。
[1386]
步骤2:非对映异构体3-(5-(1-((s)-1-乙基吡咯烷-2-基)乙氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-25)
[1387]
根据通用方法v,从乙基2-(氯甲基)-4-(1-((s)-1-乙基吡咯烷-2-基)乙氧基)苯甲酸酯24(152mg,0.447mmol)开始制备化合物i-25。将反应混合物通过硅胶(用在乙酸乙酯中的含1%tea的100%3:1etoac:etoh洗脱)纯化,以提供呈灰白色固体的非对映异构体3-(5-(1-((s)-1-乙基吡咯烷-2-基)乙氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-25(95.9mg,0.246mmol,55.1%产率)。lcms[m h]
:386.2。1h nmr(400mhz,dmso-d6)δ10.97(s,
1h),7.60(d,j=8.4hz,1h),7.17(d,j=2.1hz,1h),7.03(dd,j=8.4,2.2hz,1h),5.07(dd,j=13.3,5.1hz,1h),4.59(p,j=6.1hz,1h),4.38(dd,j=17.1,4.9hz,1h),4.25(dd,j=17.2,4.2hz,1h),3.10-3.02(m,1h),3.00-2.85(m,2h),2.76-2.68(m,1h),2.64-2.55(m,1h),2.45-2.25(m,2h),2.19-2.11(m,1h),2.04-1.93(m,1h),1.84-1.57(m,4h),1.21(dd,j=6.2,1.1hz,3h),0.99(t,j=7.2hz,3h)。
[1388]
实例14:非对映异构体3-(5-(1-((s)-1-乙基吡咯烷-2-基)乙氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-27)
[1389][1390]
步骤1:单一非对映异构体乙基2-(氯甲基)-4-(1-((s)-1-乙基吡咯烷-2-基)乙氧基)苯甲酸酯(26)
[1391]
根据通用方法iv,从5-(1-((s)-1-乙基吡咯烷-2-基)乙氧基)异苯并呋喃-1(3h)-酮int-23峰1(116.5mg,0.423mmol)开始制备中间体26。将粗材料通过硅胶色谱法(用在庚烷中的0-100%乙酸乙酯洗脱)纯化,以提供呈棕色油状物的单一非对映异构体乙基2-(氯甲基)-4-(1-((s)-1-乙基吡咯烷-2-基)乙氧基)苯甲酸酯26(117mg,0.344mmol,81%产率)。lcms[m h]
:340.1。1h nmr(400mhz,氯仿-d)δ7.96(d,j=8.8hz,1h),7.08(d,j=2.6hz,1h),6.86(dd,j=8.8,2.6hz,1h),5.04(s,2h),4.46(qd,j=6.3,3.9hz,1h),4.34(q,j=7.1hz,2h),3.15(ddd,j=9.0,5.8,2.9hz,1h),2.93(dq,j=12.0,7.4hz,1h),2.64(ddd,j=7.7,6.3,3.8hz,1h),2.35(dq,j=12.0,7.0hz,1h),2.25-2.17(m,1h),1.90-1.69(m,4h),1.38(t,j=7.1hz,3h),1.30(d,j=6.2hz,3h),1.08(t,j=7.2hz,3h)。
[1392]
步骤2:非对映异构体3-(5-(1-((s)-1-乙基吡咯烷-2-基)乙氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-27)
[1393]
根据通用方法v,从乙基2-(氯甲基)-4-(1-((s)-1-乙基吡咯烷-2-基)乙氧基)苯甲酸酯26(117mg,0.344mmol)开始制备化合物i-27。将粗材料通过硅胶(用在乙酸乙酯中的含1%tea的0-100%3:1etoac:etoh洗脱)纯化,以提供呈灰白色固体的3-(5-(1-((s)-1-乙基吡咯烷-2-基)乙氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-27(68mg,0.162mmol,47.1%产率)。lcms[m h]
:386.1。1h nmr(400mhz,dmso-d6)δ10.96(s,1h),7.59(d,j=8.4hz,1h),7.15(d,j=2.2hz,1h),7.02(dd,j=8.4,2.2hz,1h),5.07(dd,j=13.3,5.1hz,1h),4.60-4.48(m,1h),4.37(dd,j=17.2,5.9hz,1h),4.31-4.19(m,1h),3.06-2.99(m,1h),2.96-2.85(m,2h),2.68-2.55(m,2h),2.43-2.22(m,2h),2.18-2.11(m,1h),2.02-1.94
(m,1h),1.88-1.78(m,1h),1.77-1.62(m,3h),1.26-1.21(m,3h),0.98(t,j=7.2hz,3h)。
[1394]
实例15:非对映异构体混合物叔丁基(2s)-2-(1-羟基丙基)吡咯烷-1-甲酸酯(int-28)
[1395]
向冷却至-78℃的100ml rbf添加n-boc-l-脯氨醛(1ml,5.34mmol),并溶解于thf(42.7ml)中。然后逐滴添加在thf中的1m乙基溴化镁(16.0ml,16.01mmol),将所得混合物在室温下搅拌3小时,冷却至0℃,用饱和水性氯化铵淬灭,并用乙酸乙酯萃取三次。将有机相合并,通过相分离器并浓缩到上。将粗材料通过硅胶色谱法(用在庚烷中的0-100%乙酸乙酯洗脱,使用elsd检测器)纯化,以提供呈澄清油状物的叔丁基(2s)-2-(1-羟基丙基)吡咯烷-1-甲酸酯int-28(1.09g,4.75mmol,89%产率)。lcms[m h-叔丁基]
:174.1。1h nmr(400mhz,氯仿-d)δ3.95-3.71(m,2h),3.61-3.39(m,2h),3.35-3.22(m,1h),2.03-1.52(m,5h),1.49(s,9h),1.44-1.31(m,1h),1.03(td,j=7.4,2.4hz,3h)。
[1396]
实例16:非对映异构体5-(1-((s)-1-乙基吡咯烷-2-基)丙氧基)异苯并呋喃-1(3h)-酮
[1397][1398]
步骤1:非对映异构体混合物叔丁基(2s)-2-(1-((1-氧代-1,3-二氢异苯并呋喃-5-基)氧基)丙基)吡咯烷-1-甲酸酯(29)
[1399]
根据通用方法i,从叔丁基(2s)-2-(1-羟基丙基)吡咯烷-1-甲酸酯int-28(538mg,2.347mmol)开始制备中间体29。将反应混合物通过硅胶色谱法(用在庚烷中的0-100%乙酸乙酯洗脱)纯化,以提供呈黄色油状物的叔丁基(2s)-2-(1-((1-氧代-1,3-二氢异苯并呋喃-5-基)氧基)丙基)吡咯烷-1-甲酸酯29的非对映异构体混合物(526mg,1.455mmol,62.0%产率)。lcms[m h]
:362.2。
[1400]
步骤2:非对映异构体混合物5-(1-((s)-吡咯烷-2-基)丙氧基)异苯并呋喃-1(3h)-酮(30)
[1401]
根据通用方法ii,从叔丁基(2s)-2-(1-((1-氧代-1,3-二氢异苯并呋喃-5-基)氧基)丙基)吡咯烷-1-甲酸酯29的非对映异构体混合物(526mg,1.46mmol)开始制备中间体30,以提供呈橙色固体的非对映异构体混合物5-(1-((s)-吡咯烷-2-基)丙氧基)异苯并呋喃-1(3h)-酮30。粗材料无需纯化即可直接用于下个反应。lcms[m h]
:262.2。
[1402]
步骤3:非对映异构体5-(1-((s)-1-乙基吡咯烷-2-基)丙氧基)异苯并呋喃-1(3h)-酮(int-31)
[1403]
根据通用方法iii,从非对映异构体混合物5-(1-((s)-吡咯烷-2-基)丙氧基)异苯并呋喃-1(3h)-酮(380mg,1.46mmol)和乙醛(0.25ml,4.27mmol)开始制备int-31。将粗材料通过硅胶色谱法(用在庚烷中的0-100%乙酸乙酯洗脱)纯化,以提供呈黄色油状物的5-(1-((s)-1-乙基吡咯烷-2-基)丙氧基)异苯并呋喃-1(3h)-酮int-31的非对映异构体混合物(221mg,0.764mmol,52.5%产率)。lcms[m h]
:290.2。将异构体的混合物通过手性sfc[柱21x250mm chiralpak ig;含10mm nh3的co2助溶剂18%meoh;以80g/min在150巴在25℃下]分离,以提供非对映异构体:峰1:呈橙色油状物的5-(1-((s)-1-乙基吡咯烷-2-基)丙氧基)异苯并呋喃-1(3h)-酮的非对映异构体1(92.8mg,0.321mmol,22.04%产率)。手性sfc rt 3.8min。1h nmr(400mhz,氯仿-d)δ7.74(d,j=8.5hz,1h),7.04(dd,j=8.5,2.1hz,1h),6.97(d,j=2.1hz,1h),5.20(s,2h),4.32(ddd,j=7.7,5.1,2.7hz,1h),3.06(dt,j=9.1,4.3hz,1h),2.86(dq,j=11.9,7.4hz,1h),2.66(ddd,j=8.7,5.7,2.8hz,1h),2.27(dq,j=11.9,7.0hz,1h),2.12(q,j=8.6hz,1h),1.93-1.57(m,6h),1.01(t,j=7.2hz,3h),0.95(t,j=7.4hz,3h)。峰2:呈橙色油状物的5-(1-((s)-1-乙基吡咯烷-2-基)丙氧基)异苯并呋喃-1(3h)-酮的非对映异构体2(116.3mg,0.402mmol,27.6%产率)。手性sfc rt 5.1min。1h nmr(400mhz,氯仿-d)δ7.73(d,j=8.5hz,1h),7.04(dd,j=8.5,2.1hz,1h),6.97(s,1h),5.20(s,2h),4.34-4.18(m,1h),3.11(dt,j=9.1,4.5hz,1h),2.94-2.82(m,1h),2.78(dt,j=8.4,5.2hz,1h),2.32(dq,j=13.6,7.0hz,1h),2.18(q,j=8.1hz,1h),1.89-1.75(m,2h),1.75-1.52(m,4h),1.01-0.88(m,6h)。
[1404]
实例17:非对映异构体3-(5-(1-((s)-1-乙基吡咯烷-2-基)丙氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮
[1405][1406]
步骤1:单一非对映异构体乙基2-(氯甲基)-4-(1-((s)-1-乙基吡咯烷-2-基)丙氧基)苯甲酸酯(32)
[1407]
根据通用方法iv,从5-(1-((s)-1-乙基吡咯烷-2-基)丙氧基)异苯并呋喃-1(3h)-酮int-31峰2(116.3mg,0.402mmol)开始制备中间体32。将粗材料通过硅胶色谱法(用在庚烷中的0-100%乙酸乙酯洗脱)纯化,以提供呈棕色油状物的乙基2-(氯甲基)-4-(1-((s)-1-乙基吡咯烷-2-基)丙氧基)苯甲酸酯32(113mg,0.319mmol,79%产率)。lcms[m h]
:354.6。1h nmr(400mhz,氯仿-d)δ7.98(d,j=8.8hz,1h),7.15(d,j=2.6hz,1h),6.92(dd,j
=8.8,2.6hz,1h),5.06(s,2h),4.40-4.25(m,3h),3.15(ddd,j=9.4,6.2,3.6hz,1h),2.93(dq,j=11.9,7.4hz,1h),2.81(dt,j=8.2,5.4hz,1h),2.36(dq,j=11.9,7.0hz,1h),2.26-2.15(m,1h),1.93-1.57(m,6h),1.40(t,j=7.1hz,3h),1.03(t,j=7.2hz,3h),0.98(t,j=7.4hz,3h)。
[1408]
步骤2:非对映异构体3-(5-(1-((s)-1-乙基吡咯烷-2-基)丙氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-33)
[1409]
根据通用方法v,从乙基2-(氯甲基)-4-(1-((s)-1-乙基吡咯烷-2-基)丙氧基)苯甲酸酯32(113mg,0.319mmol)开始制备化合物i-33。将粗材料通过硅胶(用在乙酸乙酯中的含1%tea的0-100%3:1etoac:etoh洗脱)纯化,以提供不纯产物。将材料进一步通过碱性物质触发的反相hplc(在含有5mm nh4oh的水中的25%-50%acn)纯化。在收集前,级分管中含有3滴甲酸。将含有纯的所希望的产物的级分合并,浓缩并冻干,以提供呈白色固体的非对映异构体3-(5-(1-((s)-1-乙基吡咯烷-2-基)丙氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-33(37.9mg,73μmol,23%产率)。lcms[m h]
:400.5。1h nmr(400mhz,dmso-d6)δ8.32(s,1h),7.61(d,j=8.4hz,1h),7.20(d,j=2.1hz,1h),7.08(dd,j=8.4,2.1hz,1h),5.07(dd,j=13.3,5.1hz,1h),4.48-4.34(m,2h),4.26(d,j=17.2hz,1h),3.13-3.06(m,1h),3.00-2.78(m,3h),2.60(ddd,j=17.3,4.4,2.3hz,1h),2.44-2.28(m,2h),2.24-2.16(m,1h),2.02-1.94(m,1h),1.86-1.62(m,5h),1.55(dt,j=14.6,7.4hz,1h),0.94(dt,j=16.2,7.2hz,6h)。
[1410]
实例18:非对映异构体3-(5-(1-((s)-1-乙基吡咯烷-2-基)丙氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-35)
[1411][1412]
步骤1:单一非对映异构体乙基2-(氯甲基)-4-(1-((s)-1-乙基吡咯烷-2-基)丙氧基)苯甲酸酯(34)
[1413]
根据通用方法iv,从5-(1-((s)-1-乙基吡咯烷-2-基)丙氧基)异苯并呋喃-1(3h)-酮int-31峰1(92.8mg,0.321mmol)开始制备中间体34。将粗材料通过硅胶色谱法(用在庚烷中的0-100%乙酸乙酯洗脱)纯化,以提供呈棕色油状物的乙基2-(氯甲基)-4-(1-((s)-1-乙基吡咯烷-2-基)丙氧基)苯甲酸酯34的单一非对映异构体(90mg,0.254mmol,79%产率)。lcms[m h]
:354.1。1h nmr(400mhz,氯仿-d)δ7.97(d,j=8.7hz,1h),7.15(d,j=2.6hz,
1h),6.91(dd,j=8.8,2.6hz,1h),5.06(s,2h),4.42-4.29(m,3h),3.12(ddd,j=9.0,5.1,3.2hz,1h),2.91(dq,j=11.9,7.4hz,1h),2.68(ddd,j=8.8,5.6,3.0hz,1h),2.30(dq,j=11.9,7.0hz,1h),2.20-2.11(m,1h),1.94-1.63(m,6h),1.40(t,j=7.1hz,3h),1.07(t,j=7.2hz,3h),0.98(t,j=7.4hz,3h)。
[1414]
步骤2:非对映异构体3-(5-(1-((s)-1-乙基吡咯烷-2-基)丙氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-35)
[1415]
根据通用方法v,从乙基2-(氯甲基)-4-(1-((s)-1-乙基吡咯烷-2-基)丙氧基)苯甲酸酯34的单一非对映异构体(90mg,0.254mmol)开始制备化合物i-35。将反应混合物通过硅胶(用在乙酸乙酯中的含1%tea的0-100%3:1etoac:etoh洗脱)纯化,以提供不纯产物。将产物进一步通过碱性物质触发的反相hplc(用在含有5mm nh4oh的水中的25%-50%acn洗脱)纯化。在收集前,级分管中含有3滴甲酸。将含有纯的所希望的产物的级分合并,浓缩并冻干,以提供呈白色固体的非对映异构体3-(5-(1-((s)-1-乙基吡咯烷-2-基)丙氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-35(19.6mg,0.040mmol,15.63%产率)。lcms[m h]
:400.3。1h nmr(400mhz,dmso-d6)δ8.30(s,1h),7.58(d,j=8.4hz,1h),7.19(d,j=2.1hz,1h),7.06(dt,j=8.5,1.8hz,1h),5.06(dd,j=13.3,5.1hz,1h),4.49-4.31(m,2h),4.24(dd,j=17.1,6.0hz,1h),3.02-2.84(m,3h),2.67(td,j=7.3,2.6hz,1h),2.63-2.56(m,1h),2.37(qd,j=13.2,4.4hz,1h),2.21(dq,j=11.8,6.9hz,1h),2.13-2.04(m,1h),2.02-1.93(m,1h),1.84-1.75(m,2h),1.71-1.57(m,4h),0.98-0.90(m,6h)。
[1416]
实例19:非对映异构体(2s)-叔丁基2-(1-((1-氧代-1,3-二氢异苯并呋喃-5-基)氧基)丙基)吡咯烷-1-甲酸酯(int-36)
[1417][1418]
根据通用方法i,从(s)-叔丁基2-((s)-1-羟基丙基)吡咯烷-1-甲酸酯int-28(541mg,2.361mmol)开始制备int-36。将粗产物通过硅胶色谱法(用在庚烷中的0-100%乙酸乙酯洗脱)纯化,以提供呈黄色油状物的非对映异构体(2s)-叔丁基2-(1-((1-氧代-1,3-二氢异苯并呋喃-5-基)氧基)丙基)吡咯烷-1-甲酸酯int-36的稍微不纯的混合物(774mg,1.820mmol,77%产率)。lcms[m h]
:362.2。将异构体的混合物通过手性sfc[柱21x250mm phenomenx i-cellulose-5;co2助溶剂20%meoh;以80g/min在150巴在25℃下]分离,以提供两种非对映异构体:峰1:呈粘稠黄色油状物的(2s)-叔丁基2-(1-((1-氧代-1,3-二氢异苯并呋喃-5-基)氧基)丙基)吡咯烷-1-甲酸酯的非对映异构体1(124.2mg,0.343mmol,14.6%产率)。手性sfc rt 5.2min。峰2:呈粘稠黄色油状物的(2s)-叔丁基2-(1-((1-氧代-1,3-二氢异苯并呋喃-5-基)氧基)丙基)吡咯烷-1-甲酸酯的非对映异构体2(390.6mg,1.08mmol,45.8%产率)。手性sfc rt 6.5min。
[1419]
实例20:非对映异构体3-(5-(1-((s)-1-苄基吡咯烷-2-基)丙氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-39)
[1420][1421]
步骤1:单一非对映异构体5-(1-((s)-吡咯烷-2-基)丙氧基)异苯并呋喃-1(3h)-酮(36)
[1422]
根据通用方法ii,从(2s)-叔丁基2-(1-((1-氧代-1,3-二氢异苯并呋喃-5-基)氧基)丙基)吡咯烷-1-甲酸酯int-36峰1(124.2mg,0.343mmol)开始制备中间体36,以提供呈棕色油状物的5-(1-((s)-吡咯烷-2-基)丙氧基)异苯并呋喃-1(3h)-酮36。粗材料无需纯化即可用于下个反应。lcms[m h]
:262.4。
[1423]
步骤2:单一非对映异构体5-(1-((s)-1-苄基吡咯烷-2-基)丙氧基)异苯并呋喃-1(3h)-酮(37)
[1424]
根据通用方法iii,从5-(1-((s)-吡咯烷-2-基)丙氧基)异苯并呋喃-1(3h)-酮36(90mg,0.343mmol)和苯甲醛(0.10ml,1.030mmol)开始制备中间体37。将粗材料通过硅胶色谱法(用在庚烷中的0-100%乙酸乙酯洗脱)纯化,以提供呈黄色油状物的5-(1-((s)-1-苄基吡咯烷-2-基)丙氧基)异苯并呋喃-1(3h)-酮37(150mg,0.427mmol,定量产率)。lcms[m h]
:352.1。1h nmr(400mhz,氯仿-d)δ7.79(d,j=8.5hz,1h),7.37-7.36(m,1h),7.24(ddd,j=5.3,4.2,2.4hz,2h),7.16(dd,j=7.4,2.2hz,2h),7.07(dd,j=8.5,2.1hz,1h),6.94(d,j=2.0hz,1h),5.19(d,j=15.2hz,1h),5.12(d,j=15.2hz,1h),4.36(ddd,j=7.6,4.9,2.3hz,1h),4.06(d,j=13.4hz,1h),3.42(d,j=13.4hz,1h),2.94(ddd,j=9.1,5.5,3.6hz,1h),2.88(ddd,j=9.2,5.5,2.3hz,1h),2.20(td,j=9.1,7.7hz,1h),2.05-1.66(m,6h),1.01(t,j=7.5hz,3h)。
[1425]
步骤3:单一非对映异构体乙基4-(1-((s)-1-苄基吡咯烷-2-基)丙氧基)-2-(氯甲基)苯甲酸酯(38)
[1426]
根据通用方法iv,从5-(1-((s)-1-苄基吡咯烷-2-基)丙氧基)异苯并呋喃-1(3h)-酮37(150mg,0.427mmol)开始制备中间体38。将粗材料通过硅胶色谱法(用在庚烷中的0-100%乙酸乙酯洗脱)纯化,以提供呈橙色油状物的乙基2-(氯甲基)-4-(1-((s)-1-乙基吡咯烷-2-基)丙氧基)苯甲酸酯38(134mg,0.322mmol,75%产率)。lcms[m h]
:416.3。1h nmr(400mhz,氯仿-d)δ7.99(d,j=8.7hz,1h),7.33-7.18(m,5h),7.13(d,j=2.6hz,1h),6.91(dd,j=8.8,2.6hz,1h),5.11-4.99(m,2h),4.40(q,j=7.1hz,2h),4.33(td,j=4.9,2.4hz,1h),4.08(d,j=13.2hz,1h),3.40(d,j=13.2hz,1h),2.97-2.84(m,2h),2.20(td,j=9.3,7.0hz,1h),2.01-1.65(m,6h),1.43(t,j=7.1hz,3h),1.00(t,j=7.4hz,3h)。
[1427]
步骤4:非对映异构体3-(5-(1-((s)-1-苄基吡咯烷-2-基)丙氧基)-1-氧代异吲哚
啉-2-基)哌啶-2,6-二酮(i-39)
[1428]
根据通用方法v,从乙基2-(氯甲基)-4-(1-((s)-1-乙基吡咯烷-2-基)丙氧基)苯甲酸酯38(134mg,0.322mmol)开始制备化合物i-39。将粗材料通过硅胶(用在乙酸乙酯中的含1%tea的0-100%3:1etoac:etoh洗脱)纯化,以提供呈白色固体的3-(5-(1-((s)-1-苄基吡咯烷-2-基)丙氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-39(7.4mg,0.016mmol,4.83%产率)。lcms[m h]
:462.4。1h nmr(400mhz,dmso-d6)δ10.97(s,1h),7.58(d,j=8.4hz,1h),7.26-7.13(m,4h),7.13-7.00(m,3h),5.08(dd,j=13.4,5.1hz,1h),4.60-4.51(m,1h),4.42-4.32(m,1h),4.24(d,j=6.9hz,1h),4.10(dd,j=13.4,3.6hz,1h),3.28-3.19(m,1h),2.91(ddd,j=18.3,13.6,5.4hz,1h),2.85-2.77(m,1h),2.72-2.64(m,1h),2.64-2.54(m,1h),2.42-2.31(m,1h),2.12-1.94(m,2h),1.90-1.80(m,2h),1.75-1.58(m,4h),0.96(td,j=7.4,3.4hz,3h)。
[1429]
实例21:非对映异构体3-(5-(1-((s)-1-苄基吡咯烷-2-基)丙氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-43)
[1430][1431]
步骤1:单一非对映异构体5-(1-((s)-吡咯烷-2-基)丙氧基)异苯并呋喃-1(3h)-酮(40)
[1432]
根据通用方法ii,从(2s)-叔丁基2-(1-((1-氧代-1,3-二氢异苯并呋喃-5-基)氧基)丙基)吡咯烷-1-甲酸酯int-36峰2(290.6mg,0.804mmol)开始制备中间体40。将反应混合物浓缩,以提供呈棕色油状物的5-(1-((s)-吡咯烷-2-基)丙氧基)异苯并呋喃-1(3h)-酮40。粗材料无需纯化即可用于下个反应。lcms[m h]
:262.2。
[1433]
步骤2:单一非对映异构体5-(1-((s)-1-苄基吡咯烷-2-基)丙氧基)异苯并呋喃-1(3h)-酮(41)
[1434]
根据通用方法iii,从5-(1-((s)-吡咯烷-2-基)丙氧基)异苯并呋喃-1(3h)-酮40(210mg,0.804mmol)和苯甲醛(0.24ml,2.41mmol)开始制备中间体41。将粗材料通过硅胶色谱法(用在庚烷中的0-100%乙酸乙酯洗脱)纯化,以提供不纯产物。将材料进一步通过硅胶色谱法(用在庚烷中的0-100%乙酸乙酯洗脱)纯化,以提供呈黄色油状物的5-(1-((s)-1-苄基吡咯烷-2-基)丙氧基)异苯并呋喃-1(3h)-酮41(155mg,0.441mmol,54.9%产率)。lcms[m h]
:352.2。1h nmr(400mhz,氯仿-d)δ7.74(d,j=8.5hz,1h),7.35-7.20(m,5h),6.92(dd,j=8.5,2.2hz,1h),6.70(d,j=2.0hz,1h),5.24-5.11(m,2h),4.17(ddd,j=8.7,5.8,2.7hz,1h),3.96(d,j=13.1hz,1h),3.64(d,j=13.1hz,1h),3.08-2.92(m,2h),2.40-2.31
(m,1h),2.01-1.55(m,6h),0.96(t,j=7.4hz,3h)。
[1435]
步骤3:单一非对映异构体乙基4-(1-((s)-1-苄基吡咯烷-2-基)丙氧基)-2-(氯甲基)苯甲酸酯(42)
[1436]
根据通用方法iv,从5-(1-((s)-1-苄基吡咯烷-2-基)丙氧基)异苯并呋喃-1(3h)-酮41(155mg,0.441mmol)开始制备中间体42。将粗材料通过硅胶色谱法(用在庚烷中的0-100%乙酸乙酯洗脱)纯化,以提供呈橙色油状物的乙基4-(1-((s)-1-苄基吡咯烷-2-基)丙氧基)-2-(氯甲基)苯甲酸酯42(133mg,0.320mmol,72.5%产率)。lcms[m h]
:416.7。1h nmr(400mhz,氯仿-d)δ7.96(d,j=8.7hz,1h),7.36-7.23(m,5h),7.04(d,j=2.6hz,1h),6.79(dd,j=8.8,2.6hz,1h),5.14-4.97(m,2h),4.39(q,j=7.1hz,2h),4.19(ddd,j=8.6,5.6,2.7hz,1h),4.02(d,j=13.1hz,1h),3.61(d,j=13.1hz,1h),3.07-2.93(m,2h),2.33(dt,j=9.1,8.3hz,1h),2.04-1.59(m,6h),1.43(t,j=7.1hz,3h),0.97(t,j=7.4hz,3h)。
[1437]
步骤4:非对映异构体3-(5-(1-((s)-1-苄基吡咯烷-2-基)丙氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-43)
[1438]
根据通用方法v,从乙基4-(1-((s)-1-苄基吡咯烷-2-基)丙氧基)-2-(氯甲基)苯甲酸酯42(133mg,0.320mmol)开始制备化合物i-43。将粗材料通过硅胶色谱法(用在庚烷中的含1%tea的0-50%3:1etoac:etoh洗脱)纯化,以提供呈白色固体的3-(5-(1-((s)-1-苄基吡咯烷-2-基)丙氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-43(10mg,0.021mmol,6.71%产率)。lcms[m h]
:462.3。1h nmr(400mhz,dmso-d6)δ11.02-10.90(m,1h),7.57(d,j=8.3hz,1h),7.35-7.15(m,5h),7.09-6.90(m,2h),5.07(ddd,j=13.3,5.1,3.2hz,1h),4.44-4.15(m,3h),4.02(d,j=13.1hz,1h),3.49(d,j=13.1hz,1h),2.97-2.81(m,3h),2.67-2.53(m,1h),2.46-2.30(m,1h),2.26-2.18(m,1h),2.03-1.84(m,2h),1.82-1.72(m,2h),1.68-1.50(m,3h),0.94-0.85(m,3h)。
[1439]
实例22:非对映异构体3-(1-氧代-5-(1-((s)-吡咯烷-2-基)丙氧基)异吲哚啉-2-基)哌啶-2,6-二酮
[1440]
将3-(5-(1-((s)-1-苄基吡咯烷-2-基)丙氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-39(76.8mg,0.166mmol)溶解于dmf(2ml)中,并将所得混合物用氮气吹扫5分钟。添加pd-c(1.8mg,0.017mmol),并将反应混合物用氢气吹扫5分钟。将氢气气球放置于反应混合物的顶部,并将反应混合物在室温下搅拌18小时。将反应混合物用氮气吹扫5分钟,通过注射器过滤器用乙腈过滤,并浓缩。将粗材料通过碱性物质触发的反相hplc(用在含有5mm nh4oh的水中的15%-40%acn洗脱)纯化。在收集前,级分管中含有3滴甲酸。将含有纯的所希望的产物的级分合并,浓缩并冻干,以提供呈白色固体的非对映异构体3-(1-氧代-5-(1-((s)-吡咯烷-2-基)丙氧基)异吲哚啉-2-基)哌啶-2,6-二酮i-44(19.7mg,0.045mmol,27.2%产率)。lcms[m h]
:372.1。1h nmr(400mhz,dmso-d6)δ10.97(s,1h),8.19,(s,1h),7.61(d,j=8.4hz,1h),7.21(s,1h),7.08(d,j=8.6hz,1h),5.07(dd,j=13.3,5.1hz,1h),4.38(dd,j=17.0,4.5hz,2h),4.25(dd,j=17.1,4.0hz,1h),3.41-3.37(m,1h),2.97-2.85(m,3h),2.64-2.54(m,2h),2.43-2.31(m,1h),2.02-1.94(m,1h),1.92-1.82(m,1h),1.77-1.58(m,5h),0.90(t,j=7.4hz,3h)。
[1441]
实例23:非对映异构体3-(1-氧代-5-(1-((s)-吡咯烷-2-基)丙氧基)异吲哚啉-2-基)哌啶-2,6-二酮(i-45)
[1442]
将3-(5-(1-((s)-1-苄基吡咯烷-2-基)丙氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-43(73.6mg,0.159mmol)溶解于dmf(2ml)中,并将所得混合物用氮气吹扫5分钟。添加pd-c(1.7mg,0.016mmol),并将反应混合物用氢气吹扫5分钟。将氢气气球放置于反应物的顶部,并将反应混合物在室温下搅拌18小时。将反应混合物用氮气吹扫5分钟,通过注射器过滤器用乙腈过滤,并浓缩。将粗材料通过碱性物质触发的反相hplc(用在含有5mm nh4oh的水中的15%-40%acn洗脱)纯化。在收集前,级分管中含有3滴甲酸。将含有纯的所希望的产物的级分合并,浓缩并冻干,以提供呈白色固体的3-(1-氧代-5-(1-((s)-吡咯烷-2-基)丙氧基)异吲哚啉-2-基)哌啶-2,6-二酮i-45(27.7mg,0.061mmol,38.4%产率)的非对映异构体的混合物。lcms[m h]
:372.1。1h nmr(400mhz,dmso-d6)δ10.97(s,1h),8.24(s,1h)7.62(d,j=8.4hz,1h),7.23(s,1h),7.10(d,j=8.5hz,1h),5.07(dd,j=13.3,5.1hz,1h),4.51-4.34(m,2h),4.26(dd,j=17.2,5.7hz,1h),3.48-3.43(m,1h),3.02-2.85(m,4h),2.63-2.55(m,1h),2.38(dd,j=13.1,4.5hz,1h),2.02-1.94(m,1h),1.89(s,1h),1.78(dq,j=13.9,7.1hz,3h),1.61(dt,j=14.2,6.9hz,1h),1.51(q,j=10.2,9.6hz,1h),0.90(t,j=7.4hz,3h)。
[1443]
实例24:非对映异构体3-(1-氧代-5-(((r)-哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮(i-47)
[1444][1445]
步骤1:非对映异构体叔丁基(2r)-2-(((2-(2,6-二氧代-1-((2-(三甲基甲硅烷基)乙氧基)甲基)哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)哌啶-1-甲酸酯(46)
[1446]
根据通用方法vi,从(r)-1-n-boc-2-羟基甲基哌啶(28mg,0.132mmol)和3-(5-溴-1-氧代异吲哚啉-2-基)-1-((2-(三甲基甲硅烷基)乙氧基)甲基)哌啶-2,6-二酮int-xxx开始制备中间体46。将反应混合物过滤并浓缩,以提供呈棕色固体的非对映异构体叔丁基(2r)-2-(((2-(2,6-二氧代-1-((2-(三甲基甲硅烷基)乙氧基)甲基)哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)哌啶-1-甲酸酯46。将粗材料无需纯化即可用于下个步骤。lcms[m h-156.3(tmsch2ch2,叔丁基)]
:432.26。
[1447]
步骤2:非对映异构体3-(1-氧代-5-(((r)-哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮(i-47)
[1448]
根据通用方法vii,从叔丁基(2r)-2-(((2-(2,6-二氧代-1-((2-(三甲基甲硅烷基)乙氧基)甲基)哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)哌啶-1-甲酸酯46(64.7mg,0.11mmol)开始制备化合物i-47。将反应混合物浓缩,溶解于dmso中,并通过碱性
物质触发的反相hplc(用在含有5mm nh4oh作为改性剂的水中的10%-30%acn洗脱)纯化。在收集前,每个测试管中含有3滴甲酸。将纯的级分合并,浓缩并冻干,以提供呈奶油色固体的非对映异构体3-(1-氧代-5-(((r)-哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮i-47(4.55mg,9.62μmol,8.74%产率)。lcms[m h]
:358.3。1h nmr(400mhz,dmso-d6)δ10.95(s,1h),8.29(s,1h),7.62(d,j=8.4hz,1h),7.18(d,j=2.3hz,1h),7.06(dd,j=8.5,2.2hz,1h),5.07(dd,j=13.3,5.0hz,1h),4.39(d,j=17.1hz,1h),4.26(d,j=17.3hz,1h),3.98(dd,j=9.5,4.6hz,1h),3.88(ddd,j=9.2,7.2,1.6hz,1h),3.03-2.83(m,3h),2.68-2.55(m,2h),2.44-2.29(m,1h),2.03-1.92(m,1h),1.80-1.61(m,2h),1.59-1.52(m,1h),1.49-1.43(m,1h),1.38-1.29(m,2h),1.21-1.10(m,1h)。
[1449]
实例25:非对映异构体1-(羟基甲基)-3-(1-氧代-5-(((s)-哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮(i-49)
[1450][1451]
步骤1:非对映异构体叔丁基(2s)-2-(((2-(2,6-二氧代-1-((2-(三甲基甲硅烷基)乙氧基)甲基)哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)哌啶-1-甲酸酯(48)
[1452]
根据通用方法vi,从(s)-n-boc-哌啶-2-甲醇(28mg,0.132mmol)和3-(5-溴-1-氧代异吲哚啉-2-基)-1-((2-(三甲基甲硅烷基)乙氧基)甲基)哌啶-2,6-二酮int-xxx开始制备中间体48。将反应混合物过滤并浓缩,以提供呈棕色油状物的叔丁基(2s)-2-(((2-(2,6-二氧代-1-((2-(三甲基甲硅烷基)乙氧基)甲基)哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)哌啶-1-甲酸酯48。粗材料无需纯化即可用于下个反应。lcms[m h-156.3(tmsch2ch2,叔丁基)]
:432.2。
[1453]
步骤2:非对映异构体3-(1-氧代-5-(((s)-哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮(i-49)
[1454]
根据通用方法vii,从叔丁基(2s)-2-(((2-(2,6-二氧代-1-((2-(三甲基甲硅烷基)乙氧基)甲基)哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)哌啶-1-甲酸酯48(64.7mg,0.11mmol)开始制备化合物i-49。将反应混合物浓缩并将三分之一的材料通过碱性物质触发的反相hplc(用在含有5mm nh4oh作为改性剂的水中的10%-30%acn洗脱)纯化。在收集前,每个测试管中含有3滴甲酸。将纯的级分合并,浓缩并冻干,以提供呈奶油色固体的非对映异构体3-(1-氧代-5-(((s)-哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮i-49(3.94mg,8.33μmol,4.48%产率)。其余物质无需纯化即可用于下个反应。lcms[m h]
:358.2。1h nmr(400mhz,dmso-d6)δ10.92(s,1h),7.62(d,j=8.4hz,1h),7.21-7.15(m,
1h),7.06(dd,j=8.4,2.3hz,1h),5.07(dd,j=13.3,5.0hz,1h),4.39(d,j=17.3hz,1h),4.26(d,j=17.3hz,1h),4.05-3.96(m,1h),3.96-3.83(m,1h),3.02-2.87(m,3h),2.63-2.54(m,2h),2.45-2.33(m,1h),2.03-1.91(m,1h),1.80-1.59(m,2h),1.59-1.50(m,1h),1.49-1.43(m,2h),1.38-1.31(m,1h),1.21-1.09(m,1h)。
[1455]
实例26:3-(5-(((r)-1-乙基哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮
[1456][1457]
根据通用方法iii,从1-(羟基甲基)-3-(1-氧代-5-(((r)-哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮i-47(26mg,0.073mmol)和乙醛(0.5ml,8.85mmol)开始制备化合物i-50。将反应混合物用饱和水性碳酸氢钠淬灭并用4:1二氯甲烷:异丙醇萃取4次。将有机相合并,通过相分离器并浓缩。将粗材料通过碱性物质触发的反相hplc(用在含有5mm nh4oh作为改性剂的水中的15%-40%acn洗脱)纯化。在样品收集前,每个测试管中含有3滴甲酸。将纯的级分合并,浓缩并冻干,以提供呈橙色固体的3-(5-(((r)-1-乙基哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-50(4.59mg,9.90μmol,13.56%产率)。lcms[m h]
:386.3。1h nmr(400mhz,dmso-d6)δ10.96(s,1h),8.23(s,1h),7.62(d,j=8.4hz,1h),7.23-7.14(m,1h),7.05(dd,j=8.4,2.2hz,1h),5.07(dd,j=13.3,5.1hz,1h),4.39(d,j=17.2hz,1h),4.26(d,j=17.2hz,1h),4.21-4.11(m,1h),4.07-3.95(m,1h),2.91(ddd,j=18.0,13.6,5.5hz,1h),2.81-2.55(m,3h),2.44-2.32(m,2h),2.24(td,j=11.6,10.6,3.2hz,1h),2.17-2.10(m,1h),2.02-1.93(m,1h),1.78-1.70(m,1h),1.70-1.61(m,1h),1.58-1.51(m,1h),1.50-1.40(m,2h),1.35-1.22(m,1h),0.97(t,j=7.1hz,3h)。
[1458]
将i-50的非对映异构体混合物通过手性sfc[柱21x250mm chiralpak ih;含10mm nh3的co2助溶剂30%ipa;以100g/min在125巴在25℃下]分离,以提供单一非对映异构体:峰1:呈白色固体的3-(5-(((r)-1-乙基哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮的非对映异构体1(32.1mg,0.082mmol,31.80%产率)。手性sfc rt 3.6min。1h nmr(400mhz,dmso-d6)δ7.62(d,j=8.4hz,1h),7.19(d,j=2.2hz,1h),7.06(dd,j=8.4,2.2hz,1h),5.07(dd,j=13.3,5.1hz,1h),4.39(d,j=17.2hz,1h),4.26(d,j=17.2hz,1h),4.18(dd,j=10.3,4.7hz,1h),4.02(dd,j=10.2,5.0hz,1h),2.98-2.65(m,4h),2.64-2.53(m,1h),2.37(td,j=12.9,4.3hz,2h),2.31-2.22(m,1h),2.03-1.94(m,1h),1.80-1.36(m,6h),0.97(t,j=7.1hz,3h)。
[1459]
峰2:呈白色固体的3-(5-(((r)-1-乙基哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮的非对映异构体2(16.2mg,0.042mmol,16.04%产率)。手性sfc rt 6.5min。1h nmr(400mhz,dmso-d6)δ10.97(s,1h),7.63(d,j=8.4hz,1h),7.19(d,j=2.2hz,
1h),7.06(dd,j=8.4,2.2hz,1h),5.07(dd,j=13.3,5.1hz,1h),4.39(d,j=17.2hz,1h),4.26(d,j=17.2hz,1h),4.18(dd,j=10.3,4.7hz,1h),4.05(dd,j=10.3,4.9hz,1h),2.96-2.73(m,4h),2.58(dd,j=13.5,6.8hz,2h),2.38(dd,j=13.4,4.6hz,1h),2.33(s,1h),2.02-1.93(m,1h),1.76(d,j=12.7hz,1h),1.71-1.63(m,1h),1.56(s,1h),1.47(d,j=11.1hz,3h),0.99(t,j=7.1hz,3h)。
[1460]
根据实例26,从实例24(i-47)或实例25(i-49)的最终产物开始制备以下化合物。
[1461]
[1462]
[1463]
[1464]
[1465]
[1466]
[1467]
[1468]
[1469]
[1470]
[1471]
[1472]
[1473]
[1474]
[1475]
[1476]
[1477]
[1478]
[1479]
[1480]
[1481]
[1482]
[1483]
[1484]
[1485]
[1486]
[1487]
[1488]
[1489]
[1490]
[1491]
[1492]
[1493]
[1494]
[1495]
[1496]
[1497]
[1498]
[1499]
[1500]
[1501]
[1502]
[1503][1504]
实例27:(3,3-二氟环丁基)甲磺酸甲酯(int-51)
[1505][1506]
向(3,3-二氟环丁基)甲醇(0.16g,1.310mmol)在dcm(1.4ml)中的溶液逐滴添加dipea(0.46ml,2.62mmol)、1-甲基-1h-咪唑(0.21ml,2.62mmol)和甲磺酰氯(0.15ml,
1.96mmol)。将所得混合物在室温下搅拌18小时,然后用dcm(30ml)稀释。将有机相用1m水性hcl洗涤三次,并用饱和水性碳酸氢钠洗涤两次。将合并的有机相通过相分离器并浓缩,以提供呈橙色油状物的(3,3-二氟环丁基)甲磺酸甲酯int-51(227mg,1.134mmol,87%产率)。1h nmr(400mhz,氯仿-d)δ4.33-4.24(m,2h),3.07(s,3h),2.82-2.68(m,2h),2.67-2.53(m,1h),2.52-2.36(m,2h)。
[1507]
实例28:非对映异构体3-(5-(((r)-1-((3,3-二氟环丁基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮
[1508][1509]
将(3,3-二氟环丁基)甲磺酸甲酯int-51(101mg,0.504mmol)添加至40ml小瓶,并溶解于dmf(2.1ml)中。添加1-(羟基甲基)-3-(1-氧代-5-(((r)-哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮i-47(0.15g,0.420mmol),随后添加dipea(0.15ml,0.839mmol)。将所得混合物在室温下搅拌72小时,在50℃下搅拌18小时,在60℃下搅拌24小时,然后在100℃下搅拌24小时。将反应混合物用饱和水性碳酸氢钠淬灭并用4:1dcm:iproh萃取三次。将有机相合并,通过相分离器并浓缩到上。将粗材料通过硅胶色谱法(用在庚烷中的含1%tea的0-100%3:1etoac:etoh洗脱)纯化,以提供呈白色固体的3-(5-(((r)-1-((3,3-二氟环丁基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-52(38.9mg,0.081mmol,19.28%产率)。lcms[m h]
:462.5。1h nmr(400mhz,dmso-d6)δ10.97(s,1h),7.64(d,j=8.4hz,1h),7.20(d,j=2.3hz,1h),7.07(dd,j=8.4,2.3hz,1h),5.08(dd,j=13.3,5.2hz,1h),4.40(d,j=17.1hz,1h),4.28(d,j=17.3hz,1h),4.23-4.13(m,1h),4.13-4.01(m,1h),2.98-2.77(m,3h),2.74-2.57(m,4h),2.45-2.13(m,6h),2.04-1.93(m,1h),1.77-1.60(m,2h),1.58-1.27(m,4h)。
[1510]
实例29:3-(5-(((r)-1-异丙基哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-53)
[1511][1512]
将3-(1-氧代-5-(((r)-哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮i-47(68mg,0.190mmol)悬浮于dma(1.90ml)。添加k2co3(39mg,0.285mmol),并将所得混合物抽真空并用氮气回填3次。添加2-碘丙烷(0.10ml,0.95mmol),并在微波辐射下,将反应混合物在100℃下加热3小时。将反应混合物用50%饱和水性碳酸氢钠淬灭并用4:1dcm:iproh萃取三
次。将有机相合并,通过相分离器并浓缩到上。将粗材料通过硅胶色谱法(用在庚烷中的含1%tea的0-100%3:1乙酸乙酯:乙醇洗脱)纯化。将纯的级分合并,浓缩并冻干,以提供呈白色固体的3-(5-(((r)-1-异丙基哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-53(52.96mg,0.130mmol,68.3%产率)。lcms[m h]
:400.6。1h nmr(400mhz,dmso-d6)δ10.96(s,1h),7.62(d,j=8.3hz,1h),7.19(d,j=2.3hz,1h),7.05(dd,j=8.7,2.1hz,1h),5.07(dd,j=13.3,5.2hz,1h),4.39(d,j=17.1hz,1h),4.26(d,j=17.2hz,1h),4.20-3.92(m,2h),3.25-3.09(m,1h),2.97-2.70(m,3h),2.59(ddd,j=17.2,4.7,2.2hz,1h),2.45-2.31(m,1h),2.15(s,1h),2.02-1.91(m,1h),1.82-1.64(m,2h),1.62-1.52(m,1h),1.44-1.22(m,3h),1.12-0.98(m,3h),0.96-0.86(m,3h)。
[1513]
实例30:对映异构体5-((4-乙基-6,6-二甲基吗啉-3-基)甲氧基)异苯并呋喃-1(3h)-酮(int-56)
[1514][1515]
步骤1:外消旋-叔丁基2,2-二甲基-5-(((1-氧代-1,3-二氢异苯并呋喃-5-基)氧基)甲基)吗啉-4-甲酸酯(54)
[1516]
根据通用方法i,从4-boc-5-羟基甲基-2,2-二甲基-吗啉(507mg,2.065mmol)开始制备中间体54。将粗材料通过硅胶色谱法(用在庚烷中的0-100%乙酸乙酯洗脱)纯化,以提供呈奶油色固体的外消旋-叔丁基2,2-二甲基-5-(((1-氧代-1,3-二氢异苯并呋喃-5-基)氧基)甲基)吗啉-4-甲酸酯54(587mg,1.555mmol,83%产率)。lcms[m h]
:322.1(不含叔丁基的质量)。1h nmr(400mhz,氯仿-d)δ7.73(d,j=8.5hz,1h),7.00(dd,j=8.5,2.2hz,1h),6.93(d,j=2.1hz,1h),5.19(s,2h),4.29-4.06(m,2h),3.94-3.54(m,5h),1.41(s,9h),1.20(s,3h),1.16(s,3h)。
[1517]
步骤2:外消旋-5-((6,6-二甲基吗啉-3-基)甲氧基)异苯并呋喃-1(3h)-酮(55)
[1518]
根据通用方法ii,从叔丁基2,2-二甲基-5-(((1-氧代-1,3-二氢异苯并呋喃-5-基)氧基)甲基)吗啉-4-甲酸酯54(0.587g,1.555mmol)开始制备中间体55。将反应混合物浓缩,以提供呈白色固体的5-((6,6-二甲基吗啉-3-基)甲氧基)异苯并呋喃-1(3h)-酮55。粗材料无需纯化即可用于下个反应。lcms[m h]
:278.3。
[1519]
步骤3:对映异构体5-((4-乙基-6,6-二甲基吗啉-3-基)甲氧基)异苯并呋喃-1(3h)-酮(int-56)
[1520]
根据通用方法iii,从5-((6,6-二甲基吗啉-3-基)甲氧基)异苯并呋喃-1(3h)-酮
55(1.11g,4.0mmol)和乙醛(0.5ml,9.33mmol)开始制备int-56。将粗材料通过硅胶色谱法(用在庚烷中的含1%tea的0-100%3:1etoac:etoh洗脱)纯化,以提供呈粉色固体的5-((4-乙基-6,6-二甲基吗啉-3-基)甲氧基)异苯并呋喃-1(3h)-酮int-56(275mg,0.901mmol,22.51%产率)。lcms[m h]
:306.5。1h nmr(400mhz,氯仿-d)δ7.79(d,j=8.5hz,1h),7.03(dd,j=8.5,2.2hz,1h),6.95-6.89(m,1h),5.23(s,2h),4.20(dd,j=9.5,4.4hz,1h),4.07(dd,j=9.5,6.4hz,1h),3.85(dd,j=11.6,3.5hz,1h),3.70(dd,j=11.6,7.0hz,1h),2.92-2.79(m,1h),2.79-2.66(m,1h),2.62-2.47(m,2h),2.23(d,j=11.5hz,1h),1.28(s,3h),1.25(s,3h),1.05(t,j=7.1hz,3h)。将异构体的混合物通过手性sfc[柱21x250mm chiralpak if;co2助溶剂25%meoh;以80g/min在125巴在25℃下]分离,以提供两种对映异构体:峰1:呈浅黄色固体的5-((4-乙基-6,6-二甲基吗啉-3-基)甲氧基)异苯并呋喃-1(3h)-酮的对映异构体1(99mg,0.324mmol,8.10%产率)。手性sfc rt 2.5min。峰2:呈浅红色固体的5-((4-乙基-6,6-二甲基吗啉-3-基)甲氧基)异苯并呋喃-1(3h)-酮的对映异构体2(111.5mg,0.365mmol,9.13%产率)。手性sfc rt 3.7min。
[1521]
实例31:非对映异构体3-(5-((4-乙基-6,6-二甲基吗啉-3-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-58)
[1522][1523]
步骤1:单一对映异构体乙基2-(氯甲基)-4-((4-乙基-6,6-二甲基吗啉-3-基)甲氧基)苯甲酸酯(57)
[1524]
根据通用方法iv,从5-((6,6-二甲基吗啉-3-基)甲氧基)异苯并呋喃-1(3h)-酮int-56峰1(99mg,0.324mmol)开始制备中间体57,以提供呈棕色油状物的单一对映异构体乙基2-(氯甲基)-4-((4-乙基-6,6-二甲基吗啉-3-基)甲氧基)苯甲酸酯57。将粗材料无需纯化即可用于下个步骤。lcms[m h]
:370.4。
[1525]
步骤2:非对映异构体3-(5-((4-乙基-6,6-二甲基吗啉-3-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-58)
[1526]
根据通用方法v,从乙基2-(氯甲基)-4-((4-乙基-6,6-二甲基吗啉-3-基)甲氧基)苯甲酸酯57(120mg,0.324mmol)开始制备化合物i-58。将粗材料通过硅胶色谱法(用在庚烷中的含有1%tea作为改性剂的0-100%3:1乙酸乙酯:乙醇洗脱)纯化。将含有所希望的产物的级分合并,浓缩并冻干,以提供呈浅紫色固体的3-(5-((4-乙基-6,6-二甲基吗啉-3-基)
甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-58(71mg,0.169mmol,52.2%产率)。lcms[m h]
:416.6。1h nmr(400mhz,dmso-d6)δ10.97(s,1h),7.63(d,j=8.3hz,1h),7.26-7.15(m,1h),7.08(dd,j=8.4,2.3hz,1h),5.08(dd,j=13.3,5.2hz,1h),4.40(dd,j=17.4,1.8hz,1h),4.34-4.15(m,2h),4.12-4.00(m,1h),3.74(dd,j=11.6,3.4hz,1h),3.57(dd,j=11.4,7.4hz,1h),2.91(ddd,j=17.3,13.6,5.4hz,1h),2.78-2.65(m,2h),2.64-2.49(m,2h),2.48-2.31(m,2h),2.13(d,j=11.4hz,1h),2.03-1.93(m,1h),1.21(s,3h),1.16(s,3h),0.98(t,j=7.1hz,3h)。
[1527]
实例32:非对映异构体3-(5-((4-乙基-6,6-二甲基吗啉-3-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-60)
[1528][1529]
步骤1:单一对映异构体乙基2-(氯甲基)-4-((4-乙基-6,6-二甲基吗啉-3-基)甲氧基)苯甲酸酯(59)
[1530]
根据通用方法iv,从5-((6,6-二甲基吗啉-3-基)甲氧基)异苯并呋喃-1(3h)-酮int-56峰2(111.5mg,0.365mmol)开始制备中间体59,以提供呈棕色油状物的乙基2-(氯甲基)-4-((4-乙基-6,6-二甲基吗啉-3-基)甲氧基)苯甲酸酯59。将粗材料无需纯化即可用于下个步骤。lcms[m h]
:370.4。
[1531]
步骤2:非对映异构体(5-((4-乙基-6,6-二甲基吗啉-3-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-60)
[1532]
根据通用方法v,从乙基2-(氯甲基)-4-((4-乙基-6,6-二甲基吗啉-3-基)甲氧基)苯甲酸酯59(135mg,0.365mmol)开始制备化合物i-60。将粗材料通过硅胶色谱法(用在庚烷中的含有1%tea作为改性剂的0-100%3:1乙酸乙酯:乙醇洗脱)纯化。将含有所希望的产物的级分合并,浓缩并冻干,以提供呈浅紫色固体的(5-((4-乙基-6,6-二甲基吗啉-3-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-60(68.1mg,0.161mmol,44.0%产率)。lcms[m h] :416.4。1h nmr(400mhz,dmso-d6)δ10.97(s,1h),7.63(d,j=8.5hz,1h),7.25-7.17(m,1h),7.08(dd,j=8.5,2.2hz,1h),5.08(dd,j=13.3,5.0hz,1h),4.40(dd,j=17.6,1.8hz,1h),4.34-4.16(m,2h),4.12-4.01(m,1h),3.74(dd,j=11.3,3.4hz,1h),3.57(dd,j=11.6,7.4hz,1h),2.91(ddd,j=17.2,13.6,5.4hz,1h),2.78-2.64(m,2h),2.63-2.54(m,2h),2.48-2.31(m,2h),2.17-2.10(m,1h),2.03-1.92(m,1h),1.21(s,3h),1.16(s,3h),
0.98(t,j=7.1hz,3h)。
[1533]
实例33:叔丁基(r)-3-(羟基甲基)吗啉-4-甲酸酯(int-61)
[1534][1535]
将(s)-4-(叔丁氧基羰基)吗啉-3-甲酸(0.2g,0.865mmol)溶解于thf(2.9ml)中并冷却至0℃。逐滴添加在thf中的1m硼烷四氢呋喃复合物(2.6ml,2.59mmol)。将所得混合物在室温下搅拌过夜,然后冷却至0℃,用甲醇(2ml,49.4mmol)淬灭并在室温下搅拌2小时。将反应混合物浓缩至干燥,溶解于甲醇(5ml)中并在室温下搅拌过夜。将反应混合物浓缩到上,并通过硅胶色谱法(用在庚烷中的0-100%乙酸乙酯洗脱,使用elsd检测)纯化,以提供呈白色固体的叔丁基(r)-3-(羟基甲基)吗啉-4-甲酸酯int-61(85mg,0.391mmol,45.2%产率)。1h nmr(400mhz,氯仿-d)δ4.04(s,1h),3.94(d,j=12.0hz,1h),3.91-3.81(m,3h),3.77(d,j=13.8hz,1h),3.60(dd,j=11.9,3.5hz,1h),3.49(td,j=11.8,3.1hz,1h),3.21(t,j=12.6hz,1h),1.50(s,9h)。
[1536]
实例34:非对映异构体3-(5-(((s)-4-乙基吗啉-3-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-64)
[1537][1538]
步骤1:叔丁基(3s)-3-(((2-(2,6-二氧代-1-((2-(三甲基甲硅烷基)乙氧基)甲基)哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)吗啉-4-甲酸酯(62)
[1539]
根据通用方法vi,从叔丁基(r)-3-(羟基甲基)吗啉-4-甲酸酯int-61(58mg,0.265mmol)开始制备中间体62。将粗材料通过硅胶色谱法(用在庚烷中的0-100%乙酸乙酯洗脱)纯化,以提供呈白色粘稠固体的叔丁基(3s)-3-(((2-(2,6-二氧代-1-((2-(三甲基甲硅烷基)乙氧基)甲基)哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)吗啉-4-甲酸酯62(119mg,0.202mmol,91%产率)。lcms[m h-156.3(tmsch2ch2,叔丁基)]
:434.4。1h nmr(400mhz,氯仿-d)δ7.79(d,j=8.4hz,1h),7.03(dd,j=8.4,2.2hz,1h),6.98(s,1h),5.29-5.13(m,3h),4.43(d,j=15.9hz,1h),4.32-4.23(m,3h),4.18-4.02(m,2h),3.96-3.71(m,2h),3.67-3.57(m,3h),3.51(td,j=11.9,3.0hz,1h),3.13(t,j=12.7hz,1h),3.02(ddd,j=17.8,4.7,2.5hz,1h),2.89(ddd,j=18.1,13.3,5.5hz,1h),2.32(qd,j=13.2,4.7hz,
1h),2.18(dtd,j=12.8,5.3,2.4hz,1h),1.49(s,9h),0.94(dd,j=9.2,7.3hz,2h),0.00(s,9h)。
[1540]
步骤2:3-(5-(((s)-吗啉-3-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(63)
[1541]
根据通用方法vii,从叔丁基(3s)-3-(((2-(2,6-二氧代-1-((2-(三甲基甲硅烷基)乙氧基)甲基)哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)吗啉-4-甲酸酯62(119mg,0.202mmol)开始制备中间体63。将粗材料通过硅胶色谱法(用在二氯甲烷中的含有1%tea的0-100%乙醇洗脱)纯化,以提供呈白色固体的3-(5-(((s)-吗啉-3-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮63(54.5mg,0.152mmol,75%产率)。lcms[m h]
:360.3。1h nmr(400mhz,氯仿-d)δ7.76(d,j=8.4hz,1h),6.97(dd,j=8.4,2.2hz,1h),6.93-6.87(m,1h),5.15(ddd,j=13.2,5.2,1.2hz,1h),4.38(d,j=15.9hz,1h),4.24(d,j=15.9hz,1h),4.00-3.85(m,3h),3.85-3.77(m,1h),3.63-3.51(m,1h),3.42(ddd,j=11.0,9.3,3.1hz,1h),3.35-3.24(m,1h),3.02-2.92(m,3h),2.90-2.72(m,2h),2.28(qd,j=12.9,5.2hz,1h),2.21-2.11(m,1h)。
[1542]
步骤3:3-(5-(((s)-4-乙基吗啉-3-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-64)
[1543]
根据通用方法iii,从3-(5-(((s)-吗啉-3-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮63(54.5mg,0.152mmol)和乙醛(0.05ml,0.91mmol)的溶液开始制备化合物i-64。将粗材料通过硅胶色谱法(用在庚烷中的含1%tea的0-100%3:1乙酸乙酯:乙醇洗脱)纯化。将纯的级分合并,浓缩并冻干,以提供呈橙色固体的3-(5-(((s)-4-乙基吗啉-3-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-64(24.6mg,0.062mmol,40.6%产率)。lcms[m h]
:388.5。1h nmr(400mhz,dmso-d6)δ10.89(s,1h),7.55(d,j=8.3hz,1h),7.18-7.06(m,1h),7.00(dd,j=8.4,2.2hz,1h),5.00(dd,j=13.3,5.0hz,1h),4.32(d,j=17.2hz,1h),4.24-4.09(m,2h),3.98(ddd,j=9.8,6.2,1.9hz,1h),3.72(dd,j=11.1,3.0hz,1h),3.65-3.55(m,1h),3.55-3.45(m,1h),3.41(dd,j=11.0,7.3hz,1h),2.91-2.76(m,1h),2.75-2.56(m,3h),2.57-2.48(m,1h),2.38-2.21(m,3h),1.95-1.87(m,1h),0.93(t,j=7.1hz,3h)。
[1544]
实例35:叔丁基2-(羟基甲基)氮杂环庚烷-1-甲酸酯,2-(羟基甲基)氮杂环庚烷-1-甲酸(int-65)
[1545][1546]
将1-(叔丁氧基羰基)氮杂环庚烷-2-甲酸(0.3g,1.233mmol)溶解于thf(4.1ml)中并冷却至0℃。逐滴添加在thf中的1m硼烷四氢呋喃复合物(3.70ml,3.70mmol)。将所得混合物在室温下搅拌过夜,冷却至0℃并用甲醇(3ml,74.2mmol)淬灭,并在室温下搅拌2小时。将反应混合物浓缩至干燥,然后重新溶解于甲醇(5ml)中,在室温下搅拌过夜。将反应混合物浓缩到上,并通过硅胶色谱法(用在庚烷中的0-100%乙酸乙酯洗脱,使用elsd检测器)纯化,以提供呈澄清油状物的叔丁基2-(羟基甲基)氮杂环庚烷-1-甲酸酯int-65
(209mg,0.911mmol,73.9%产率)。lcms[m h-叔丁基]
:174.2。1h nmr(400mhz,氯仿-d)δ4.10-3.97(m,1h),3.95-3.65(m,1h),3.62-3.52(m,1h),3.51-3.33(m,2h),3.21(s,1h),2.76-2.63(m,1h),1.99-1.86(m,1h),1.78-1.66(m,2h),1.63-1.55(m,1h),1.42-1.33(m,9h),1.25-1.10(m,2h)。
[1547]
实例36:对映异构体5-((1-乙基氮杂环庚烷-2-基)甲氧基)异苯并呋喃-1(3h)-酮(int-68)
[1548][1549]
步骤1:外消旋-叔丁基2-(((1-氧代-1,3-二氢异苯并呋喃-5-基)氧基)甲基)氮杂环庚烷-1-甲酸酯(66)
[1550]
根据通用方法i,从叔丁基2-(羟基甲基)氮杂环庚烷-1-甲酸酯int-65(209mg,0.912mmol)开始制备中间体66。将粗材料通过硅胶色谱法(用在庚烷中的0-100%乙酸乙酯洗脱)纯化,以提供呈粘稠黄色固体的叔丁基2-(((1-氧代-1,3-二氢异苯并呋喃-5-基)氧基)甲基)氮杂环庚烷-1-甲酸酯66(245mg,0.678mmol,78%产率)。lcms[m h-6.3(tmsch2ch2,叔丁基)]
:306.3。1h nmr(400mhz,氯仿-d)δ7.77-7.70(m,1h),6.99(dt,j=8.5,2.4hz,1h),6.91(dd,j=14.4,2.1hz,1h),5.23-5.12(m,2h),4.40-4.21(m,1h),4.06-3.89(m,2h),3.87-3.65(m,1h),2.93-2.77(m,1h),2.21-2.03(m,1h),1.91-1.74(m,2h),1.73-1.64(m,1h),1.62-1.46(m,1h),1.45-1.39(m,9h),1.28-1.17(m,3h)。
[1551]
步骤2:外消旋-5-(氮杂环庚烷-2-基甲氧基)异苯并呋喃-1(3h)-酮(67)
[1552]
根据通用方法ii,从叔丁基2-(((1-氧代-1,3-二氢异苯并呋喃-5-基)氧基)甲基)氮杂环庚烷-1-甲酸酯66(245mg,0.678mmol)开始制备中间体67,以提供呈白色固体的5-(氮杂环庚烷-2-基甲氧基)异苯并呋喃-1(3h)-酮67。粗物质无需纯化即可用于下一步。lcms[m h]
:262.2。
[1553]
步骤3:5-((1-乙基氮杂环庚烷-2-基)甲氧基)异苯并呋喃-1(3h)-酮(int-68)的对映异构体
[1554]
根据通用方法iii,从5-(氮杂环庚烷-2-基甲氧基)异苯并呋喃-1(3h)-酮67(0.18g,0.678mmol)和乙醛(0.23ml,4.07mmol)开始制备int-68。将粗材料通过硅胶色谱法(用在庚烷中的0-100%乙酸乙酯洗脱)纯化,以提供呈奶油色固体的对映异构体混合物5-((1-乙基氮杂环庚烷-2-基)甲氧基)异苯并呋喃-1(3h)-酮int-68(101mg,0.349mmol,51.5%产率)。lcms[m h]
:290.4。1h nmr(400mhz,氯仿-d)δ7.81(d,j=8.5hz,1h),7.05
(dd,j=8.5,2.1hz,1h),6.94-6.88(m,1h),5.25(s,2h),3.99(dd,j=9.1,4.9hz,1h),3.82(dd,j=9.1,7.7hz,1h),3.09-3.00(m,1h),2.93-2.87(m,2h),2.84-2.69(m,2h),2.07-1.97(m,1h),1.85-1.75(m,1h),1.74-1.34(m,6h),1.09(t,j=7.1hz,3h)。将异构体的混合物通过手性sfc[柱2.1x25.0cm chiralcel od-h;含0.25%异丙胺的co2助溶剂15%ipa;以100g/min在100巴在25℃下]分离,以提供两种对映异构体:峰1:呈白色固体的5-((1-乙基氮杂环庚烷-2-基)甲氧基)异苯并呋喃-1(3h)-酮的对映异构体1(27.7mg,0.096mmol,14.12%产率)。手性sfc rt 1.84min。峰2:呈白色固体的5-((1-乙基氮杂环庚烷-2-基)甲氧基)异苯并呋喃-1(3h)-酮的对映异构体2(30mg,0.104mmol,15.29%产率)。手性sfc rt2.05min。
[1555]
实例37:3-(5-((1-乙基氮杂环庚烷-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-70)
[1556][1557]
步骤1:单一对映异构体乙基2-(氯甲基)-4-((1-乙基氮杂环庚烷-2-基)甲氧基)苯甲酸酯(69)
[1558]
根据通用方法iv,从5-(氮杂环庚烷-2-基甲氧基)异苯并呋喃-1(3h)-酮int68峰2(30mg,0.104mmol)开始制备中间体69,以提供呈棕色油状物的乙基2-(氯甲基)-4-((1-乙基氮杂环庚烷-2-基)甲氧基)苯甲酸酯69。将粗材料无需纯化即可用于下个步骤。lcms[m h]
:354.1。
[1559]
步骤2:非对映异构体混合物3-(5-((1-乙基氮杂环庚烷-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-70)
[1560]
根据通用方法v,从乙基2-(氯甲基)-4-((1-乙基氮杂环庚烷-2-基)甲氧基)苯甲酸酯69(36.8mg,0.104mmol)开始制备化合物i-70。将粗材料通过硅胶色谱法(用在庚烷中的含有1%三乙胺作为改性剂的0-100%3:1乙酸乙酯:乙醇洗脱)纯化。将含有所希望的产物的级分合并,浓缩并冻干,以提供不纯产物。将粗材料进一步通过碱性反相hplc(用在含有5mm nh4oh为改性剂的水中的35%-60%acn洗脱)纯化。将纯的级分冻干,以提供呈白色固体的3-(5-((1-乙基氮杂环庚烷-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮
i-70(3.95mg,9.00μmol,8.65%产率)。lcms[m h]
:400.2。1h nmr(400mhz,dmso-d6)δ10.89(s,1h),7.54(d,j=8.4hz,1h),7.12-7.04(m,1h),6.97(dd,j=8.4,2.3hz,1h),5.00(dd,j=13.3,5.0hz,1h),4.31(d,j=17.2hz,1h),4.19(d,j=17.2hz,1h),3.96-3.65(m,2h),2.98-2.60(m,5h),2.57-2.49(m,1h),2.37-2.26(m,1h),1.95-1.83(m,2h),1.68-1.19(m,8h),0.93(t,j=7.2hz,3h)。
[1561]
实例38:3-(5-(((r)-1-苯甲酰基哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-71)
[1562][1563]
将苯甲酸(9.16mg,0.075mmol)溶解于dmf(0.75ml)中。添加hatu(34mg,0.090mmol)和dipea(0.03ml,0.15mmol),并将所得混合物在室温下搅拌15分钟。添加3-(1-氧代-5-(((r)-哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮i-47(27mg,0.075mmol)在dmf(0.75ml)中的溶液,并在室温下继续搅拌过夜。将反应混合物浓缩,并通过酸性反相hplc(用在含有0.1%甲酸作为改性剂的水中的15%-40%acn洗脱)纯化。将纯的级分合并并冻干,以提供呈白色固体的3-(5-(((r)-1-苯甲酰基哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-71(21.3mg,0.046mmol,61.5%产率)。lcms[m h] :462.3。1h nmr(400mhz,dmso-d6)δ10.97(s,1h),7.61(d,j=8.3hz,1h),7.48-6.86(m,7h),5.08(dd,j=13.2,5.2hz,1h),4.60-3.94(m,5h),3.31-3.25(m,2h),2.91(ddd,j=17.3,13.6,5.4hz,1h),2.59(dt,j=16.6,3.5hz,1h),2.45-2.35(m,1h),2.03-1.94(m,1h),1.86-1.55(m,5h),1.50-1.33(m,1h)。
[1564]
根据实例38,从实例24(i-47)或实例25(i-49)的最终产物开始制备以下化合物。
[1565]
[1566][1567]
实例39:3-(5-(((s)-1-(2-(萘-2-基氧基)乙酰基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-72)
[1568][1569]
向含有在dmf(200μl)中的2-(萘-2-基氧基)乙酸(11.9mg,0.059mmol)的反应小瓶中添加hatu(22.3mg,0.059mmol)在dmf(200μl)中的溶液,随后添加3-(1-氧代-5-(((s)-哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮i-49(12mg,0.034mmol)和nmm(0.02ml,0.168mmol)在dmf(600μl)中的混合物。将所得混合物在室温下搅拌过夜。将反应混合物浓缩,并通过酸性反相hplc(用在含有0.1%甲酸作为改性剂的水中的10%-90%acn洗脱)纯化,以提供3-(5-(((s)-1-(2-(萘-2-基氧基)乙酰基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-72(10.9mg,0.019mmol,55.9%产率)。lcms[m h] :542.3,rt 0.62min。
[1570]
根据实例39,从实例24(i-47)或实例25(i-49)的最终产物开始制备以下化合物。
[1571]
[1572]
[1573]
[1574]
[1575]
[1576]
[1577]
[1578]
[1579]
[1580]
[1581]
[1582]
[1583]
[1584]
[1585]
[1586]
[1587]
[1588]
[1589]
[1590]
[1591]
[1592]
[1593]
[1594]
[1595]
[1596]
[1597]
[1598]
[1599]
[1600]
[1601]
[1602]
[1603]
[1604]
[1605]
[1606]
[1607]
[1608]
[1609]
[1610]
[1611]
[1612]
[1613]
[1614]
[1615]
[1616]
[1617]
[1618]
[1619]
[1620]
[1621]
[1622]
[1623]
[1624]
[1625]
[1626]
[1627]
[1628]
[1629]
[1630]
[1631]
[1632]
[1633]
[1634]
[1635]
[1636][1637]
实例40:叔丁基4-(4-(((2r)-2-(((2-(2,6-二氧代哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)哌啶-1-基)甲基)苯基)哌嗪-1-甲酸酯(i-73)
[1638][1639]
根据通用方法iii,从3-(1-氧代-5-(((r)-哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮i-47(0.45g,1.259mmol)和1-boc-4-(4-甲酰基苯基)哌嗪(550mg,1.894mmol)开始制备化合物i-73。将粗材料通过硅胶色谱法(用在庚烷中的含1%tea的0-100%3:1乙酸乙酯:乙醇洗脱)纯化。将纯的级分合并,浓缩并冻干,以提供呈白色固体的叔丁基4-(4-(((2r)-2-(((2-(2,6-二氧代哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)哌啶-1-基)甲基)苯基)哌嗪-1-甲酸酯i-73(599mg,0.948mmol,75%产率)。lcms[m h]
:632.6。1h nmr(400mhz,氯仿-d)δ7.98(d,j=14.3hz,1h),7.81(d,j=8.4hz,1h),7.25(d,j=8.2hz,2h),
7.03(dd,j=8.3,2.2hz,1h),6.95(s,1h),6.89(d,j=8.4hz,2h),5.22(dd,j=13.2,5.2hz,1h),4.46(d,j=15.8hz,1h),4.32-4.19(m,2h),4.09(dd,j=9.8,4.8hz,1h),3.99(d,j=13.6hz,1h),3.63-3.53(m,4h),3.39(d,j=13.6hz,1h),3.16-3.06(m,4h),2.99-2.74(m,4h),2.36(qd,j=13.0,5.0hz,1h),2.27-2.12(m,2h),1.91-1.80(m,1h),1.76-1.70(m,1h),1.68-1.46(m,13h)。
[1640]
实例41:3-(1-氧代-5-(((r)-1-(4-(哌嗪-1-基)苄基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮(int-74)
[1641][1642]
将叔丁基4-(4-(((2r)-2-(((2-(2,6-二氧代哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)哌啶-1-基)甲基)苯基)哌嗪-1-甲酸酯i-73(0.599g,0.948mmol)悬浮于二噁烷(体积:4ml,比率:1.333)并溶解于三氟乙醇(体积:3ml,比率:1.000)中。添加在二噁烷中的4m hcl(1.422ml,5.69mmol),并将所得混合物在室温下搅拌过夜。将反应混合物浓缩,以提供呈粉色固体的稍微不纯的3-(1-氧代-5-(((r)-1-(4-(哌嗪-1-基)苄基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮int-74(700mg,1.317mmol)。粗物质无需纯化即可用于下一步。lcms[m h]
:532.5。
[1643]
实例42:3-(5-(((r)-1-(4-(4-乙基哌嗪-1-基)苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-75)
[1644][1645]
根据通用方法iii,从3-(1-氧代-5-(((r)-1-(4-(哌嗪-1-基)苄基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮int-74(0.1g,0.188mmol)和乙醛(50mg,1.129mmol)
开始制备int-74。将粗材料通过硅胶色谱法(用在庚烷中的含1%tea的0-100%3:1乙酸乙酯:乙醇洗脱)纯化。将纯的级分合并,浓缩并冻干,以提供呈白色固体的3-(5-(((r)-1-(4-(4-乙基哌嗪-1-基)苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-75(41.77mg,0.073mmol,38.9%产率)。lcms[m h]
:560.3。1h nmr(400mhz,dmso-d6)δ10.90(s,1h),7.54(d,j=8.4hz,1h),7.14-7.02(m,3h),6.99(dd,j=8.4,2.3hz,1h),6.78(d,j=8.4hz,2h),5.00(dd,j=13.3,5.2hz,1h),4.32-4.11(m,3h),4.05(dd,j=10.3,5.5hz,1h),3.81(d,j=13.5hz,1h),3.23-3.18(m,1h),3.01(t,j=5.0hz,4h),2.84(ddd,j=17.2,13.6,5.4hz,1h),2.69-2.56(m,2h),2.56-2.48(m,1h),2.42-2.23(m,7h),2.07-1.97(m,1h),1.96-1.85(m,1h),1.74-1.66(m,1h),1.62-1.53(m,1h),1.49-1.36(m,2h),1.36-1.21(m,2h),0.95(t,j=7.1hz,3h)。
[1646]
实例43:3-(5-(((r)-1-(4-(4-(氧杂环丁烷-3-基甲基)哌嗪-1-基)苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-76)
[1647][1648]
根据通用方法iii,从3-(1-氧代-5-(((r)-1-(4-(哌嗪-1-基)苄基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮int-74(0.15g,0.282mmol)和氧杂环丁烷-3-甲醛(49mg,0.564mmol)开始制备int-74。将粗材料通过硅胶色谱法(用在庚烷中的含1%tea的0-100%3:1乙酸乙酯:乙醇洗脱)纯化。将纯的级分合并,浓缩并冻干,以提供呈白色固体的3-(5-(((r)-1-(4-(4-(氧杂环丁烷-3-基甲基)哌嗪-1-基)苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-76(43.17mg,0.072mmol,25.4%产率)。lcms[m h]
:602.3。1h nmr(400mhz,dmso-d6)δ10.90(s,1h),7.54(d,j=8.4hz,1h),7.13-7.03(m,3h),6.99(dd,j=8.6,2.2hz,1h),6.77(d,j=8.4hz,2h),5.00(dd,j=13.2,5.0hz,1h),4.58(dd,j=7.8,5.8hz,2h),4.37-4.13(m,5h),4.05(dd,j=10.3,5.5hz,1h),3.81(d,j=13.2hz,1h),3.24-3.19(m,1h),3.18-3.07(m,1h),3.03-2.93(m,4h),2.84(ddd,j=17.3,13.6,5.4hz,1h),2.71-2.48(m,5h),2.39-2.28(m,5h),2.07-1.96(m,1h),1.96-1.86(m,1h),1.75-1.64(m,1h),1.63-1.51(m,1h),1.51-1.22(m,4h)。
[1649]
实例44:3-(5-(((r)-1-(4-(4-异丁基哌嗪-1-基)苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-77)
1-氧代异吲哚啉-5-基)氧基)甲基)吡咯烷-1-甲酸酯78。将粗材料无需处理或纯化即可用于下个步骤作为溶液。lcms[m h-156.3(tmsch2ch2,叔丁基)]
:418.2。
[1656]
步骤2:3-(1-氧代-5-(((s)-吡咯烷-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮(i-79)
[1657]
根据通用方法vii,从叔丁基(2s)-2-(((2-(2,6-二氧代-1-((2-(三甲基甲硅烷基)乙氧基)甲基)哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)吡咯烷-1-甲酸酯78(63mg,0.110mmol)开始制备化合物i-79。将反应混合物浓缩。将pl-hco3mp spe柱(聚合物实验室(polymer lab)(瓦里安公司(varian)),部件号pl3540-c603,在6ml试管中的500mg预填充树脂)用etoh(5ml)预洗涤。将粗材料溶解于etoh(3ml)中,并通过柱经施加正压进行过滤。将柱用etoh(5ml)洗涤,并将滤液浓缩,并通过碱性物质触发的反相hplc(用在含有5mm nh4oh作为改性剂的水中的10%-30%acn洗脱)纯化。在样品收集前,每个测试管中含有3滴甲酸。将纯的级分合并,浓缩并冻干,以提供呈奶油色固体的3-(1-氧代-5-(((s)-吡咯烷-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮i-79(18.9mg,0.047mmol,42.3%产率)。lcms[m h]
:344.2。1h nmr(400mhz,dmso-d6)δ10.96(s,1h),8.27(s,1h),7.63(d,j=8.4hz,1h),7.18(d,j=2.2hz,1h),7.06(dd,j=8.4,2.3hz,1h),5.07(dd,j=13.4,5.1hz,1h),4.39(d,j=17.2hz,1h),4.26(d,j=17.2hz,1h),4.06-3.93(m,2h),3.55(p,j=6.8hz,1h),2.96-2.85(m,3h),2.59(dd,j=16.8,3.4hz,1h),2.44-2.32(m,1h),2.03-1.87(m,2h),1.83-1.66(m,2h),1.59-1.47(m,1h)。
[1658]
实例46:3-(1-氧代-5-(((r)-吡咯烷-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮(i-81)
[1659][1660]
步骤1:叔丁基(2r)-2-(((2-(2,6-二氧代-1-((2-(三甲基甲硅烷基)乙氧基)甲基)哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)吡咯烷-1-甲酸酯(80)
[1661]
根据通用方法vi,从n-boc-d-脯氨醇(27mg,0.132mmol)和3-(5-溴-1-氧代异吲哚啉-2-基)-1-((2-(三甲基甲硅烷基)乙氧基)甲基)哌啶-2,6-二酮int-xxx开始制备中间体80,以提供叔丁基(2r)-2-(((2-(2,6-二氧代-1-((2-(三甲基甲硅烷基)乙氧基)甲基)哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)吡咯烷-1-甲酸酯80。将粗材料无需处理或纯化即可用于下个步骤作为溶液。lcms[m h-156.3(tmsch2ch2,叔丁基)]
:418.6。
[1662]
步骤2:46:3-(1-氧代-5-(((r)-吡咯烷-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮(i-81)
[1663]
根据通用方法vii,从叔丁基(2r)-2-(((2-(2,6-二氧代-1-((2-(三甲基甲硅烷基)乙氧基)甲基)哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)吡咯烷-1-甲酸酯80(63mg,0.110mmol)开始制备化合物i-81。将粗材料浓缩,并通过碱性物质触发的反相hplc(用在含有5mm nh4oh作为改性剂的水中的10%-30%acn洗脱)纯化。在样品收集前,每个测试管中含有3滴甲酸。将纯的级分合并,浓缩并冻干,以提供呈三乙胺盐的产物。将pl-hco3 mp spe柱(聚合物实验室(瓦里安公司),部件号pl3540-c603(或当量);在6ml试管中的500mg预填充树脂)用etoh(5ml)预洗涤。将产物溶解于etoh(3ml)中,并通过柱经施加较小压力进行过滤。将柱用etoh(5ml)洗涤,并将滤液浓缩并冻干,以提供呈白色固体的3-(1-氧代-5-(((r)-吡咯烷-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮i-81(7.3mg,0.021mmol,19.09%产率)。lcms[m h]
:344.3。1h nmr(400mhz,dmso-d6)δ10.93(s,1h),7.63(d,j=8.4hz,1h),7.17(d,j=2.2hz,1h),7.05(dd,j=8.3,2.3hz,1h),5.07(dd,j=13.3,5.1hz,1h),4.39(d,j=17.1hz,1h),4.26(d,j=17.2hz,1h),4.05-3.92(m,2h),3.54(p,j=6.8hz,1h),2.97-2.83(m,3h),2.59(ddd,j=17.2,4.6,2.2hz,1h),2.45-2.30(m,1h),2.03-1.86(m,2h),1.86-1.62(m,2h),1.59-1.44(m,2h)。
[1664]
实例47:苄基(2s)-2-(((2-(2,6-二氧代哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)吡咯烷-1-甲酸酯(i-82)
[1665][1666]
根据通用程序x制备化合物i-82:
[1667]
制备0.2m int-47a和在acn中的0.3m tmp 0.004m[ir]催化剂储备溶液:向100ml小瓶中装入int-47a(4.50g,9.92mmol)、tmp(2.6ml,14.8mmol)和ir[(df(cf3)ppy)2dtbbpy]pf6(122mg,0.10mmol),然后用acn稀释至总体积50ml。制备在acn中的0.025m[ni]催化剂溶液:在氮气下,向40ml小瓶中添加nicl2(甘醇二甲醚)(113mg,0.50mmol)和dtbbpy(138mg,0.50mmol),然后用acn稀释至总体积20ml。将获得的混合物剧烈搅拌直到均质。如果产生催化剂沉淀,则将反应混合物在70℃下加热15min,产生甚至在室温下仍保持均质的均质溶液。
[1668]
向1打兰小瓶中装入苄基(s)-2-(羟基甲基)吡咯烷-1-甲酸酯(35mg,0.15mmol)。接下来,添加int-47a tmp [ir]储备溶液在acn中的0.2m溶液(0.55ml,0.110mmol),随后添加在acn中的0.025m[ni]催化剂溶液(0.22ml,5.51μmol)。然后在室温下,在rayonet led反应器中,在蓝色led光的照射下,将反应混合物剧烈搅拌48小时。然后添加甲磺酸(0.072ml,1.103mmol),并将反应混合物在室温下搅拌过夜。在0℃下,同时添加tea(0.22ml,1.544mmol)和n1,n2-二甲基乙烷-1,2-二胺(0.014ml,0.132mmol),并在室温下继续搅拌过
夜。将反应混合物浓缩至干燥,并通过反相hplc(用在含有0.1%甲酸作为改性剂的水中的15%-95%acn洗脱)纯化,以提供苄基(2s)-2-(((2-(2,6-二氧代哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)吡咯烷-1-甲酸酯i-82(2.5mg,4.97μmol,4.5%产率)。lcms[m h]
:478.3,rt 0.61min。
[1669]
实例48:3-(5-(((r)-1-(2-甲氧基苯甲酰基)吡咯烷-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-83)
[1670][1671]
根据通用程序x,从(r)-(2-(羟基甲基)吡咯烷-1-基)(2-甲氧基苯基)甲酮(int-48a,35mg,0.15mmol)开始制备化合物i-83。将反应混合物浓缩至干燥,并通过反相hplc(用在含有0.1%甲酸作为改性剂的水中的15%-95%acn洗脱)纯化,以提供3-(5-(((r)-1-(2-甲氧基苯甲酰基)吡咯烷-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-83(25.1mg,0.050mmol,45.3%产率)。lcms[m h]
:478.3,rt 0.56min。
[1672]
实例49:3-(5-(((s)-4,4-二氟吡咯烷-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-84)
[1673][1674]
根据通用程序x,从叔丁基(s)-4,4-二氟-2-(羟基甲基)吡咯烷-1-甲酸酯(35.3mg,0.15mmol)开始制备int xxx。将反应混合物浓缩至干燥,并通过反相hplc(用在含有0.1%甲酸作为改性剂的水中的5%-95%acn洗脱)纯化,以提供3-(5-(((s)-4,4-二氟吡咯烷-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-84(11.2mg,0.025mmol,22.7%产率)。lcms[m h]
:380.2,rt 0.35min。
[1675]
实例50:3-(5-(((s)-1-苄基吡咯烷-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-90)
[1676][1677]
步骤1:(s)-叔丁基2-(((1-氧代-1,3-二氢异苯并呋喃-5-基)氧基)甲基)吡咯烷-1-甲酸酯(86)
[1678]
参考:angew.chem.int.ed.[应用化学国际版],2011,50,9943。向反应小瓶中添加5-溴苯酞(98.4mg,0.462mmol)、boc-l-脯氨醇(281.6mg,1.399mmol)、碳酸铯(231.1mg,0.709mmol)和rockphos g3 pd催化剂(27.6mg,0.033mmol),并将小瓶抽真空并用氮气回填三次。添加甲苯(2.0ml),并将所得混合物在90℃下搅拌6小时。将溶液用乙酸乙酯(80ml)稀释并用水(20ml)、饱和水性碳酸氢钠溶液(20ml)、和盐水(20ml)洗涤。将有机相经硫酸镁干燥,过滤,并浓缩。将粗产物用二氯甲烷稀释,并通过硅胶色谱法(用在庚烷中的0-100%etoac洗脱)纯化,以提供产物。将材料进一步通过碱性物质触发的反相hplc(用在含有10mm nh4oh作为改性剂的水中的35%-60%acn洗脱)纯化。将含有所希望的产物的级分合并并浓缩,以提供呈黄色固体的(s)-叔丁基2-(((1-氧代-1,3-二氢异苯并呋喃-5-基)氧基)甲基)吡咯烷-1-甲酸酯86(100.9mg,0.303mmol,65.5%产率)。lcms[m h]
:334.4。1h nmr(400mhz,二氯甲烷-d2)δ7.80(d,j=8.5hz,1h),7.12(dd,j=8.5,2.2hz,1h),7.04(s,1h),5.26(s,2h),4.26(s,1h),4.17(d,j=4.4hz,1h),4.03(s,1h),3.40(d,j=7.6hz,2h),2.13-2.02(m,2h),2.02-1.95(m,1h),1.95-1.85(m,1h),1.49(s,9h)。
[1679]
步骤2:(s)-5-(吡咯烷-2-基甲氧基)异苯并呋喃-1(3h)-酮(87)tfa盐
[1680]
向含有溶解于dcm(1ml)的(s)-叔丁基2-(((1-氧代-1,3-二氢异苯并呋喃-5-基)氧基)甲基)吡咯烷-1-甲酸酯86(100.9mg,0.303mmol)的反应小瓶中添加三氟乙酸(0.1ml,1.298mmol),并将所得混合物在室温下搅拌直到观察到起始物质完全消耗。然后将反应混合物浓缩,以提供呈透明胶状物的(s)-5-(吡咯烷-2-基甲氧基)异苯并呋喃-1(3h)-酮87tfa盐(150mg,0.643mmol)。lcms[m h]
:234.3。1h nmr(400mhz,dmso-d6)δ9.21(s,1h),8.76(s,1h),7.81(d,j=8.5hz,1h),7.25(t,j=1.4hz,1h),7.17(dd,j=8.5,2.3hz,1h),
5.36(s,2h),4.40(dd,j=10.7,3.5hz,1h),4.21(dd,j=10.8,8.4hz,1h),3.97(dt,j=9.0,3.4hz,1h),3.24(dtd,j=11.7,6.7,5.8,2.0hz,2h),2.15(dtd,j=12.7,7.8,4.9hz,1h),2.06-1.84(m,2h),1.75(dq,j=12.8,8.2hz,1h)。
[1681]
步骤3:(s)-5-((1-苄基吡咯烷-2-基)甲氧基)异苯并呋喃-1(3h)-酮(88)
[1682]
参考文献:heterocycles[杂环],2006,第67卷,第2期,第519-522页;bioorganic and medicinal chemistry[生物有机和药物化学],2001,第9卷,第2期,第237-243页。
[1683]
向含有溶解于dce(1.5ml)的(s)-5-(吡咯烷-2-基甲氧基)异苯并呋喃-1(3h)-酮87(70.6mg,0.303mmol)的反应小瓶中添加三乙胺(0.065ml,0.466mmol)。将所得混合物在室温下搅拌5分钟,然后添加苯甲醛(0.035ml,0.344mmol),并且继续在室温下搅拌1小时。添加三乙酰氧基硼氢化钠(92.0mg,0.434mmol),并将反应混合物在室温下搅拌过夜,然后用etoac(40ml)稀释,并用饱和水性碳酸氢钠洗涤两次并用盐水洗涤。将有机相经硫酸镁干燥,过滤,并浓缩。将粗材料用二氯甲烷稀释,并通过硅胶色谱法(用在庚烷中的含0.1%tea的0-80%etoac洗脱)纯化,以提供(s)-5-((1-苄基吡咯烷-2-基)甲氧基)异苯并呋喃-1(3h)-酮88(59.8mg,0.185mmol,61.1%产率)。lcms[m h]
:324.4。1h nmr(400mhz,二氯甲烷-d2)δ7.78(d,j=8.5hz,1h),7.43-7.30(m,4h),7.26(t,j=7.1hz,1h),7.03(dd,j=8.5,2.2hz,1h),6.89(s,1h),5.24(s,2h),4.17-4.08(m,1h),4.05(dd,j=9.3,5.2hz,1h),3.94(dd,j=9.3,6.4hz,1h),3.59(d,j=13.2hz,1h),3.13-3.03(m,1h),2.99(dd,j=8.6,5.2hz,1h),2.37(q,j=8.4hz,1h),2.14-2.04(m,1h),1.80(q,j=6.8,5.9hz,3h)。
[1684]
步骤4:(s)-乙基4-((1-苄基吡咯烷-2-基)甲氧基)-2-(氯甲基)苯甲酸酯(89)
[1685]
将含有溶解于乙醇(2ml)中的(s)-5-((1-苄基吡咯烷-2-基)甲氧基)异苯并呋喃-1(3h)-酮88(59.8mg,0.185mmol)的2颈圆底烧瓶配备有回流冷凝器,并加热至70℃。将回流冷凝器配备有碳酸氢钠洗涤器。将亚硫酰氯(0.08ml,1.096mmol)经由侧颈添加至反应,并将所得混合物在70℃下搅拌4小时。然后将溶液用水稀释,并用饱和水性碳酸氢钠中和。将水相用乙酸乙酯萃取三次。将有机相合并,用5%碳酸氢钠溶液、盐水洗涤,经硫酸镁干燥,过滤并浓缩,以提供呈棕色胶状物的(s)-乙基4-((1-苄基吡咯烷-2-基)甲氧基)-2-(氯甲基)苯甲酸酯89(59.7mg,0.139mmol,74.9%产率)。将物质无需纯化即可用于下一步骤。lcms[m h]
:388.3。1h nmr(400mhz,二氯甲烷-d2)δ8.00(d,j=8.7hz,1h),7.35(dt,j=14.6,7.5hz,4h),7.26(t,j=7.0hz,1h),7.07(d,j=2.6hz,1h),6.88(dd,j=8.8,2.6hz,1h),5.07(s,2h),4.37(q,j=7.1hz,2h),4.20-4.11(m,1h),4.03(d,j=7.6hz,1h),3.92(dd,j=14.4,6.0hz,1h),3.57(d,j=13.1hz,1h),3.02(d,j=29.4hz,2h),2.43-2.31(m,1h),2.08(dt,j=8.1,4.9hz,1h),1.80(s,3h),1.42(t,j=7.1hz,3h)。
[1686]
步骤5:3-(5-(((s)-1-苄基吡咯烷-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-90)
[1687]
向含有溶解于dmf(0.5ml)中的3-氨基哌啶-2,6-二酮盐酸盐(26.8mg,0.163mmol)的反应小瓶中添加dipea(0.07ml,0.401mmol),并将所得混合物在室温下搅拌15分钟。添加在dmf(0.5ml)中的(s)-乙基4-((1-苄基吡咯烷-2-基)甲氧基)-2-(氯甲基)苯甲酸酯89(59.7mg,0.154mmol),并将反应混合物在85℃下搅拌过夜。将溶液冷却至室温并浓缩。将粗材料通过酸性反相柱色谱法(用在含有0.1%甲酸作为改性剂的水中的10%-30%acn洗脱)纯化。将含有所希望的产物的级分合并并浓缩,以提供呈棕色固体的3-(5-(((s)-1-苄基吡
咯烷-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-90(22.7mg,0.045mmol,29.2%产率)。lcms[m h]
:434.5。1h nmr(400mhz,dmso-d6)δ10.96(s,1h),8.14(s,1h),7.60(d,j=8.4hz,1h),7.37-7.27(m,4h),7.23(ddt,j=8.5,5.1,2.6hz,1h),7.12(d,j=2.2hz,1h),7.02(ddd,j=8.5,2.2,0.9hz,1h),5.07(dd,j=13.3,5.1hz,1h),4.44-4.19(m,2h),4.18-4.04(m,2h),3.94(dd,j=9.7,6.5hz,1h),3.48(d,j=13.2hz,1h),2.98(d,j=20.2hz,1h),2.90-2.79(m,2h),2.64-2.55(m,1h),2.38(dd,j=13.2,4.3hz,1h),2.26(t,j=7.9hz,1h),1.99(dt,j=7.2,5.0hz,2h),1.69(q,j=9.5,8.9hz,3h)。
[1688]
实例51:3-(5-(((r)-1-((6-氟吡啶-3-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-91)
[1689][1690]
根据通用方法iii,从3-(1-氧代-5-(((r)-哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮i-47(0.15g,0.420mmol)和6-氟吡啶-3-甲醛(0.079g,0.630mmol)开始制备化合物i-47。将反应混合物用50%饱和水性碳酸氢钠在水中淬灭并用4:1二氯甲烷:异丙醇萃取4次。将有机相合并,通过相分离器并浓缩。将材料通过硅胶色谱法(用在庚烷中的含1%tea的0-100%3:1乙酸乙酯:乙醇洗脱)纯化。将纯的级分合并,浓缩并放置于高真空下过夜,以提供呈白色固体的3-(5-(((r)-1-((6-氟吡啶-3-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-91(69.7mg,0.134mmol,32.0%产率)。lcms[m h]
:467.2。1h nmr(400mhz,dmso-d6)δ11.00(s,1h),8.16(d,j=2.4hz,1h),8.07-7.82(m,1h),7.64(d,j=8.4hz,1h),7.21(d,j=2.2hz,1h),7.10(ddd,j=13.4,8.4,2.5hz,2h),5.10(dd,j=13.3,5.1hz,1h),4.48-4.24(m,3h),4.19-4.12(m,1h),4.08-3.97(m,1h),3.48(d,j=14.1hz,1h),2.99-2.87(m,1h),2.82-2.75(m,1h),2.72-2.58(m,2h),2.40(qd,j=13.3,4.5hz,1h),2.21-2.10(m,1h),2.05-1.95(m,1h),1.84-1.75(m,1h),1.72-1.62(m,1h),1.59-1.33(m,4h)。
[1691]
实例52:3-(5-(((r)-1-(4,4-二氟环己基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-92)
[1692]
[1693]
向40ml小瓶中装入3-(1-氧代-5-(((r)-哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮i-47(0.2g,0.560mmol)、4,4-二氟环己烷-1-酮(1.50g,11.19mmol)、mgso4(0.202g,1.679mmol)和dmf(2ml),并将所得悬浮液在室温下搅拌15min。然后添加nabh(oac)3(0.237g,1.119mmol)并在60℃下继续搅拌过夜。将反应混合物冷却至室温并用50%饱和水性碳酸氢钠淬灭,并用4:1dcm:iproh萃取三次。将有机相合并,通过相分离器并浓缩。将粗材料通过硅胶色谱法(用在庚烷中的含1%tea的0-100%3:1etoac:etoh洗脱)纯化,以提供呈奶油色固体的3-(5-(((r)-1-(4,4-二氟环己基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-92(60.19mg,0.123mmol,21.94%产率)。lcms[m h]
:476.2。1h nmr(400mhz,dmso-d6)δ10.99(s,1h),7.65(d,j=8.4hz,1h),7.20(s,1h),7.07(d,j=8.5hz,1h),5.09(dd,j=13.3,5.1hz,1h),4.40(dd,j=17.2,4.2hz,1h),4.34-4.11(m,2h),4.11-3.96(m,1h),2.97-2.87(m,3h),2.83-2.76(m,1h),2.65-2.56(m,1h),2.40(qd,j=12.9,4.3hz,1h),2.26(t,j=9.3hz,1h),2.09-1.95(m,3h),1.90-1.52(m,8h),1.48-1.24(m,4h)。
[1694]
实例53:(3-氰基双环[1.1.1]戊烷-1-基)甲磺酸甲酯(int-93)
[1695][1696]
向3-(羟基甲基)双环[1.1.1]戊烷-1-甲腈(0.117g,0.950mmol)在dcm(1.49ml)中的溶液中逐滴添加dipea(0.33ml,1.900mmol)、1-甲基-1h-咪唑(0.15ml,1.900mmol),随后逐滴添加甲磺酰氯(0.11ml,1.425mmol)。将所得混合物在室温下搅拌18小时。将反应混合物用dcm(30ml)稀释。将有机相用1m水性hcl洗涤三次,并用饱和水性碳酸氢钠洗涤两次。将有机相通过相分离器并浓缩,以提供呈米色固体的(3-氰基双环[1.1.1]戊烷-1-基)甲磺酸甲酯int-93(164mg,0.815mmol,86%产率)。1h nmr(400mhz,氯仿-d)δ4.12(s,2h),2.95(s,3h),2.23(s,6h)。
[1697]
实例54:3-(((2r)-2-(((2-(2,6-二氧代哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)哌啶-1-基)甲基)双环[1.1.1]戊烷-1-甲腈(i-94)
[1698][1699]
将(3-氰基双环[1.1.1]戊烷-1-基)甲磺酸甲酯int-93(81mg,0.403mmol)添加至2ml微波小瓶,并溶解于dmf(1.68ml)中。添加3-(1-氧代-5-(((r)-哌啶-2-基)甲氧基)异吲
哚啉-2-基)哌啶-2,6-二酮i-47(0.12g,0.336mmol),随后添加dipea(0.12ml,0.671mmol)。将所得混合物在100℃下在微波辐射下搅拌共计22小时。将反应混合物用50%饱和水性碳酸氢钠淬灭并用4:1dcm:iproh萃取三次。将有机相合并,通过相分离器并浓缩。将粗材料通过硅胶色谱法(用在庚烷中的含1%tea的0-100%3:1etoac:etoh洗脱)纯化,以提供呈白色固体的3-(((2r)-2-(((2-(2,6-二氧代哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)哌啶-1-基)甲基)双环[1.1.1]戊烷-1-甲腈i-94(18.3mg,0.036mmol,10.84%产率)。lcms[m h]
:463.2。1h nmr(400mhz,dmso-d6)δ10.90(s,1h),7.56(d,j=8.3hz,1h),7.11(d,j=2.3hz,1h),6.99(dd,j=8.3,2.4hz,1h),5.00(dd,j=13.3,5.0hz,1h),4.32(d,j=17.4hz,1h),4.20(d,j=17.3hz,1h),4.08-4.00(m,1h),3.96-3.82(m,1h),2.90-2.78(m,1h),2.75-2.63(m,3h),2.56-2.49(m,1h),2.35-2.22(m,3h),2.11-2.04(m,6h),1.96-1.87(m,1h),1.68-1.52(m,2h),1.47-1.19(m,4h)。
[1700]
实例55:((1r,3r)-3-甲氧基环丁基)甲磺酸甲酯(int-96)
[1701]
步骤1:((1r,3r)-3-甲氧基环丁基)甲醇(95)
[1702]
将反式-3-甲氧基环丁烷-1-甲酸(0.1g,0.768mmol)溶解于thf(2.56ml)中并冷却至0℃。逐滴添加在thf中的1m硼烷thf复合物(2.3ml,2.31mmol)。将反应在室温下搅拌过夜。将反应冷却至0℃并用甲醇(1.87ml,46.1mmol)淬灭,并在室温下搅拌2小时。将反应浓缩至干燥然后重新溶解于甲醇(5ml)中。将反应在室温下搅拌过夜。将反应浓缩,以提供呈澄清油状物的((1r,3r)-3-甲氧基环丁基)甲醇95(89mg,0.768mmol,100%产率)。将物质(假定定量产率)无需纯化即可用于下一步骤。
[1703]
步骤2:((1r,3r)-3-甲氧基环丁基)甲磺酸甲酯(int-96)
[1704]
向((1r,3r)-3-甲氧基环丁基)甲醇95(89mg,0.768mmol)在dcm(1.5ml)中的溶液逐滴添加dipea(268μl,1.536mmol)、1-甲基-1h-咪唑(122μl,1.536mmol),然后逐滴添加甲磺酰氯(90μl,1.152mmol)。将反应在室温下搅拌18小时。将反应用dcm(30ml)稀释。将有机层用1m水性hcl洗涤三次,并用饱和水性碳酸氢钠洗涤两次。将有机层通过相分离器并浓缩,以提供呈褐红色油状物的((1r,3r)-3-甲氧基环丁基)甲磺酸甲酯int-96(176mg,0.906mmol,118%产率)。将物质无需纯化即可用于下一步,由于存在杂质,其产率高于定量产率。1h nmr(400mhz,cdcl3)δ4.16(d,j=6.8hz,2h),3.94-3.82(m,1h),3.16(s,3h),2.96(s,3h),2.63-2.51(m,1h),2.09(t,j=6.8hz,4h)。
[1705]
实例56:3-(5-(((r)-1-(((1r,3r)-3-甲氧基环丁基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-97)
[1706][1707]
将((1r,3r)-3-甲氧基环丁基)甲磺酸甲酯int-96(112mg,575μmol)添加至2ml微
波小瓶,并溶解于dmf(1.92ml)中。添加3-(1-氧代-5-(((r)-哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮i-47(137mg,0.383mmol),随后添加dipea(0.13ml,0.767mmol)。将反应抽真空并用氮气回填三次。将反应在100℃下在微波辐射下搅拌共计15小时。添加另外的((1r,3r)-3-甲氧基环丁基)甲磺酸甲酯int-96(64mg,0.329mmol)和dipea(0.13ml,0.767mmol),并将反应抽真空并用氮气回填三次。将反应在100℃下在微波辐射下再搅拌12小时。将反应用饱和碳酸氢钠水溶液淬灭并用4:1dcm:iproh萃取三次。将有机层合并,通过相分离器并浓缩到celite上。将粗材料通过硅胶色谱法(在庚烷中的含1%tea的0-100%3:1etoac:etoh)纯化,以提供不纯产物。将材料进一步通过碱性物质触发的反相hplc(在含有5mm nh4oh作为改性剂的水中的25%-50%acn)纯化。在样品收集前,测试管中含有3滴甲酸。将纯的级分合并并冻干,以提供呈白色固体的甲酸盐3-(5-(((r)-1-(((1r,3r)-3-甲氧基环丁基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-97(44.6mg,0.089mmol,23.2%产率)。lcms[m h]
:456.1。1h nmr(400mhz,dmso-d6)δ10.84(s,1h),8.24(t,j=5.4hz,1h),7.56(d,j=8.4hz,1h),7.13(d,j=2.3hz,1h),6.99(dd,j=8.4,2.2hz,1h),5.00(dd,j=13.3,5.1hz,1h),4.32(d,j=17.2hz,1h),4.20(d,j=17.2hz,1h),4.15-4.04(m,1h),4.03-3.91(m,1h),3.73(p,j=6.3hz,1h),2.97(s,3h),2.84(ddd,j=17.1,13.6,5.4hz,1h),2.77-2.64(m,2h),2.63-2.48(m,2h),2.35-2.24(m,3h),2.13-2.04(m,1h),1.98-1.72(m,5h),1.68-1.52(m,2h),1.46-1.20(m,4h)。
[1708]
实例57:3-氟双环[1.1.1]戊烷-1-甲醛(int-99)
[1709]
步骤1:(3-氟双环[1.1.1]戊烷-1-基)甲醇(98)
[1710]
在氮气气氛下,将3-氟双环[1.1.1]戊烷-1-甲酸溶解于thf(ml)中并冷却至0℃。经10min逐滴添加在thf中的1m硼烷thf复合物(ml,mmol)。允许反应升温至室温并在室温下搅拌72小时。将反应冷却至0℃并逐滴添加meoh(1ml)。在气体逸出停止后,将溶剂浓缩,以提供(3-氟双环[1.1.1]戊烷-1-基)甲醇98(650mg,5.6mmol,143%产率)。该物质无需纯化即可直接用于下一步,由于杂质,其产率高于定量产率。
[1711]
步骤2:3-氟双环[1.1.1]戊烷-1-甲醛(int-99)
[1712]
向40ml小瓶中装入(3-氟双环[1.1.1]戊烷-1-基)甲醇98(454mg,3.91mmol)、nahco3(750mg,8.93mmol)和dcm(6ml)。添加戴斯-马丁高碘烷(2.49g,5.87mmol),并将反应混合物在室温下搅拌3小时。将乙醚(18ml)添加至反应,并将反应过滤两次。将滤液浓缩,添加乙醚(20ml),并将固体过滤。将滤液再次浓缩,以提供呈含有一些白色固体的黄色油状物的3-氟双环[1.1.1]戊烷-1-甲醛int-99(449mg,3.93mmol,100%产率)。制备在dmf中的1m溶液,将该物质(假定定量产率)无需纯化即可直接用于下一步。
[1713]
实例58:3-(5-(((r)-1-((3-氟双环[1.1.1]戊烷-1-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-100)
[1714][1715]
将在dmf中的1m 3-氟双环[1.1.1]戊烷-1-甲醛int-99(0.8ml,0.80mmol)添加至在dmf(1.8ml)中的3-(1-氧代-5-(((r)-哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮i-47(150mg,0.420mmol)。将反应混合物在室温下搅拌15min。添加三乙酰氧基硼氢化钠(205mg,0.965mmol)并将反应在室温下搅拌过夜。添加少量的分子筛和另外的在dmf中的1m 3-氟双环[1.1.1]戊烷-1-甲醛int-99(0.8ml,0.80mmol)。将反应在50℃下搅拌1小时。添加另外的三乙酰氧基硼氢化钠(205mg,0.965mmol),并将反应在50℃下搅拌过夜。将反应用50%饱和碳酸氢钠水溶液淬灭并用4:1dcm:iproh萃取三次。将粗材料通过硅胶色谱法(在含有0.1%tea的dcm中的含有1%tea的1%-25%etoh)纯化,以提供3-(5-(((r)-1-((3-氟双环[1.1.1]戊烷-1-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-100(17mg,0.036mmol,8.5%产率)。lcms[m h]
:456.5。1h nmr(400mhz,dmso-d6)δ10.96(s,1h),7.62(d,j=8.4hz,1h),7.18(d,j=2.3hz,1h),7.06(dd,j=8.6,2.2hz,1h),5.07(dd,j=13.3,5.2hz,1h),4.39(d,j=17.2hz,1h),4.27(d,j=17.1hz,1h),4.18-3.90(m,2h),3.30-3.28(m,1h),3.03-2.85(m,2h),2.84-2.71(m,3h),2.63-2.55(m,1h),2.44-2.35(m,2h),2.03-1.90(m,7h),1.75-1.59(m,2h),1.51-1.31(m,3h)。
[1716]
根据实例26,从实例24(i-47)的最终产物开始制备以下化合物。
[1717]
[1718]
[1719]
[1720]
[1721]
[1722][1723]
实例60:3-(5-(((r)-1-(4-(4-(环丙基甲基)哌嗪-1-基)苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-102)
[1724][1725]
根据通用方法iii,从3-(1-氧代-5-(((r)-1-(4-(哌嗪-1-基)苄基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮int-74(100mg,0.188mmol)和环丙烷甲醛(28μl,0.376mmol)开始制备化合物i-102。将反应用在水中的50%饱和水性碳酸氢钠淬灭,并用4:1二氯甲烷:异丙醇萃取4次。将有机层合并,通过相分离器并浓缩。将材料通过硅胶色谱法(在庚烷中含1%tea的0-100%3:1乙酸乙酯:乙醇)纯化。将纯的级分合并,浓缩并冻干,以提供呈白色固体的3-(5-(((r)-1-(4-(4-(环丙基甲基)哌嗪-1-基)苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-102(65.9mg,0.111mmol,59.2%产率)。lcms[m h]
:586.6。1h nmr(400mhz,dmso-d6)δ10.87(s,1h),7.52(d,j=8.4hz,1h),7.13-7.01(m,3h),6.97(dd,j=8.6,2.2hz,1h),6.76(d,j=8.3hz,2h),4.98(dd,j=13.3,5.1hz,1h),4.34-4.08(m,3h),4.02(dd,j=10.3,5.6hz,1h),3.79(d,j=13.5hz,1h),3.03-2.95
(m,4h),2.86-2.75(m,1h),2.65-2.56(m,2h),2.53-2.42(m,6h),2.35-2.22(m,1h),2.12(d,j=6.6hz,2h),2.02-1.95(m,1h),1.92-1.84(m,1h),1.71-1.63(m,1h),1.62-1.49(m,1h),1.46-1.16(m,4h),0.82-0.68(m,1h),0.42-0.35(m,2h),0.03
‑‑
0.04(m,2h)。
[1726]
实例61:(2-氧杂螺[3.3]庚烷-6-基)甲磺酸甲酯(int-103)
[1727]
向(2-氧杂螺[3.3]庚烷-6-基)甲醇(0.1g,0.780mmol)在dcm(1.5ml)中的溶液逐滴添加dipea(0.27ml,1.56mmol)、1-甲基-1h-咪唑(0.12ml,1.56mmol),然后逐滴添加甲磺酰氯(0.09ml,1.17mmol)。将反应在室温下搅拌18小时。将反应用dcm(30ml)稀释。将有机层用1m水性hcl洗涤三次,并用饱和水性碳酸氢钠洗涤两次。将有机层通过相分离器并浓缩,以提供呈棕色油状物的(2-氧杂螺[3.3]庚烷-6-基)甲磺酸甲酯int-103(137.5mg,0.667mmol,85%产率)。1h nmr(400mhz,cdcl3)δ4.73(s,2h),4.64(s,2h),4.15(d,j=6.2hz,2h),3.03(s,3h),2.59-2.49(m,1h),2.47-2.38(m,2h),2.13-2.03(m,2h)。
[1728]
实例62:3-(5-(((r)-1-((2-氧杂螺[3.3]庚烷-6-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-104)
[1729][1730]
将(2-氧杂螺[3.3]庚烷-6-基)甲磺酸甲酯int-103(95mg,0.462mmol)添加至2ml微波小瓶,并溶解于dmf(1.5ml)中。添加3-(1-氧代-5-(((r)-哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮i-47(0.11g,0.308mmol),随后添加dipea(0.11ml,0.616mmol)。将反应抽真空并用氮气回填三次。将反应100℃下在微波辐射下搅拌12小时。将反应用50%饱和水性碳酸氢钠淬灭并用4:1dcm:iproh萃取三次。将有机层合并,通过相分离器并浓缩到celite上。将粗材料通过硅胶色谱法(在庚烷中的含1%tea的0-100%3:1etoac:etoh)纯化,以提供呈白色固体的3-(5-(((r)-1-((2-氧杂螺[3.3]庚烷-6-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮int-104(46.1mg,0.094mmol,30.4%产率)。lcms[m h]
:468.5。1h nmr(400mhz,dmso-d6)δ10.97(s,1h),7.63(d,j=8.5hz,1h),7.19(d,j=2.3hz,1h),7.06(dd,j=8.4,2.3hz,1h),5.08(dd,j=13.3,5.0hz,1h),4.54(s,2h),4.43-4.33(m,3h),4.27(d,j=17.1hz,1h),4.16-4.10(m,1h),4.06-3.98(m,1h),2.91(ddd,j=17.2,13.5,5.4hz,1h),2.81-2.71(m,1h),2.65-2.56(m,3h),2.43-2.31(m,2h),2.29-2.20(m,3h),2.18-2.10(m,1h),2.02-1.95(m,1h),1.84-1.60(m,4h),1.54-1.25(m,4h)。
[1731]
实例63:叔丁基4-(2-(((2r)-2-(((2-(2,6-二氧代哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)哌啶-1-基)甲基)苯基)哌嗪-1-甲酸酯(i-105)
[1732][1733]
根据通用方法iii,从3-(1-氧代-5-(((r)-哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮i-47(100mg,0.280mmol)和叔丁基4-(2-甲酰基苯基)哌嗪-1-甲酸酯(122mg,0.420mmol)开始制备化合物i-105。将反应用50%饱和水性碳酸氢钠淬灭并用4:1dcm:iproh萃取三次。将有机层合并,通过相分离器并浓缩到celite上。将粗材料通过硅胶色谱法(在庚烷中的含1%tea的0-100%3:1etoac:etoh)纯化,以提供呈白色固体的叔丁基4-(2-(((2r)-2-(((2-(2,6-二氧代哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)哌啶-1-基)甲基)苯基)哌嗪-1-甲酸酯i-105(170.6mg,0.268mmol,95.4%产率)。lcms[m h]
:632.6。1h nmr(400mhz,dmso-d6)δ10.97(s,1h),7.61(d,j=8.3hz,1h),7.51-7.42(m,1h),7.22-7.12(m,2h),7.10-6.99(m,3h),5.08(dd,j=13.2,5.0hz,1h),4.42-4.19(m,3h),4.16-4.04(m,1h),3.95(d,j=13.8hz,1h),3.58(d,j=13.8hz,1h),3.49-3.36(m,4h),2.97-2.70(m,7h),2.63-2.55(m,1h),2.44-2.32(m,1h),2.28-2.18(m,1h),2.02-1.93(m,1h),1.83-1.72(m,1h),1.69-1.54(m,2h),1.50-1.37(m,12h)。
[1734]
实例64:3-(1-氧代-5-(((r)-1-(2-(哌嗪-1-基)苄基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮(i-106)
[1735][1736]
将叔丁基4-(2-(((2r)-2-(((2-(2,6-二氧代哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)哌啶-1-基)甲基)苯基)哌嗪-1-甲酸酯i-105(0.14g,0.222mmol)悬浮于二噁烷(0.89ml)中,并溶解于三氟乙醇(0.59ml)中。添加在二噁烷中的4m hcl(0.33ml,1.33mmol),并将反应在室温下搅拌过夜。将反应浓缩,然后用4:1dcm:iproh稀释。将反应用50%饱和水性碳酸氢钠淬灭。将水层用4:1dcm:iproh萃取4次。将有机层合并,通过相分离器并浓缩。将粗材料通过硅胶色谱法(在dcm中的含1%tea的0-100%etoh)纯化,以提供呈白色固体的3-(1-氧代-5-(((r)-1-(2-(哌嗪-1-基)苄基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮i-106(80.1mg,0.140mmol,63.2%产率)。lcms[m h]
:532.4。1h nmr(400mhz,dmso-d6)δ10.97(s,1h),7.61(d,j=8.6hz,1h),7.53-7.44(m,1h),7.22-7.10(m,2h),7.08-6.97(m,3h),5.08(dd,j=13.3,5.1hz,1h),4.44-4.19(m,3h),4.14-4.04(m,1h),3.93(d,j=13.9hz,1h),3.58(d,j=13.9hz,1h),2.97-2.66(m,11h),2.64-2.56(m,1h),2.45-2.33(m,1h),2.28-2.19(m,1h),2.03-1.94(m,1h),1.82-1.74(m,1h),1.70-1.62
(m,1h),1.60-1.36(m,4h)。
[1737]
实例65:3-(5-(((r)-1-(2-(4-异丁基哌嗪-1-基)苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-107)
[1738][1739]
根据通用方法iii,从3-(1-氧代-5-(((r)-1-(2-(哌嗪-1-基)苄基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮i-106(75mg,0.141mmol)和异丁醛(0.02ml,0.212mmol)开始制备化合物i-107。将反应用50%饱和水性碳酸氢钠淬灭并用4:1dcm:iproh萃取三次。将有机层合并,通过相分离器并浓缩到celite上。将粗材料通过硅胶色谱法(在庚烷中的含1%tea的0-100%3:1etoac:etoh)纯化,以提供呈白色固体的3-(5-(((r)-1-(2-(4-异丁基哌嗪-1-基)苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-107(53.8mg,0.090mmol,63.6%产率)。lcms[m h]
:588.2。1h nmr(400mhz,dmso-d6)δ10.97(s,1h),7.61(d,j=8.3hz,1h),7.47(dd,j=7.8,1.8hz,1h),7.23-7.09(m,2h),7.09-6.97(m,3h),5.08(dd,j=13.4,5.1hz,1h),4.43-4.20(m,3h),4.14-4.05(m,1h),3.93(d,j=13.8hz,1h),3.55(d,j=13.8hz,1h),2.97-2.76(m,6h),2.74-2.69(m,1h),2.62-2.56(m,1h),2.41(ddd,j=22.3,10.9,4.5hz,5h),2.27-2.18(m,1h),2.07-1.94(m,3h),1.82-1.72(m,2h),1.68-1.37(m,5h),0.86(d,j=6.4hz,6h)。
[1740]
实例66:3-(1-氧代-5-(((r)-1-(2-(4-((四氢-2h-吡喃-4-基)甲基)哌嗪-1-基)苄基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮(i-108)
[1741][1742]
根据通用方法iii,从3-(1-氧代-5-(((r)-1-(2-(哌嗪-1-基)苄基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮i-106(75mg,0.141mmol)和四氢-2h-吡喃-4-甲醛(22μl,0.212mmol)开始制备化合物i-108。将反应用50%饱和水性碳酸氢钠淬灭并用4:1dcm:iproh萃取三次。将有机层合并,通过相分离器并浓缩到celite上。将粗材料通过硅胶色谱法(在庚烷中的含1%tea的0-100%3:1etoac:etoh)纯化,以提供呈白色固体的3-(1-氧代-5-(((r)-1-(2-(4-((四氢-2h-吡喃-4-基)甲基)哌嗪-1-基)苄基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮i-108(61.5mg,0.095mmol,67.1%产率)。lcms[m h]
:630.6。1h nmr(400mhz,dmso-d6)δ10.89(s,1h),7.54(d,j=8.4hz,1h),7.45-7.35(m,1h),7.17-7.02(m,2h),7.02-6.90(m,3h),5.00(dd,j=13.3,5.2hz,1h),4.36-4.15(m,3h),4.09-3.97(m,
1h),3.85(d,j=13.8hz,1h),3.80-3.69(m,2h),3.47(d,j=13.9hz,1h),3.23-3.16(m,3h),2.90-2.63(m,6h),2.56-2.49(m,1h),2.39-2.27(m,4h),2.21-2.10(m,1h),2.08-2.03(m,2h),1.94-1.85(m,1h),1.75-1.26(m,10h),1.11-0.97(m,2h)。
[1743]
实例67:3-(1-氧代-5-(((r)-1-(4-(4-(四氢-2h-吡喃-4-基)哌嗪-1-基)苄基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮(i-109)
[1744][1745]
向40ml小瓶中装入3-(1-氧代-5-(((r)-1-(4-(哌嗪-1-基)苄基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮int-74(0.1g,0.188mmol)、四氢-4h-吡喃-4-酮(0.35ml,3.76mmol)、mgso4(68mg,0.564mmol)和dmf(1ml)。将悬浮液在室温下搅拌15min。添加nab(oac)3h(80mg,0.376mmol),并将反应混合物在60℃下搅拌过夜。将反应冷却至室温并用50%饱和水性碳酸氢钠淬灭,并用4:1dcm:iproh萃取三次。将有机层合并,通过相分离器并浓缩。将粗材料通过硅胶色谱法(在庚烷中的含1%tea的0-100%3:1etoac:etoh)纯化。将含有所希望的产物的级分合并并浓缩。将产物进一步通过碱性反相hplc(在含有5mm nh4oh作为改性剂的水中的25%-50%acn)纯化。在样品收集前,测试管中含有3滴甲酸。将含有纯的产物的级分合并并冻干,以提供呈白色固体的3-(1-氧代-5-(((r)-1-(4-(4-(四氢-2h-吡喃-4-基)哌嗪-1-基)苄基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮i-109(47.4mg,0.075mmol,39.7%产率)。lcms[m h]
:616.6。1h nmr(400mhz,dmso-d6)δ10.90(s,1h),7.55(d,j=8.3hz,1h),7.15-7.04(m,3h),7.00(d,j=8.3hz,1h),6.79(d,j=8.2hz,2h),5.00(dd,j=13.4,5.2hz,1h),4.36-4.12(m,3h),4.11-3.99(m,1h),3.83(dd,j=10.7,4.4hz,3h),3.23-3.18(m,4h),3.06-2.96(m,4h),2.91-2.77(m,1h),2.68-2.62(m,1h),2.57-2.51(m,3h),2.39-2.28(m,4h),2.06-1.97(m,1h),1.95-1.87(m,1h),1.76-1.62(m,3h),1.62-1.54(m,1h),1.51-1.24(m,6h)。
[1746]
实例68:叔丁基7-(((2r)-2-(((2-(2,6-二氧代哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)哌啶-1-基)甲基)吲哚啉-1-甲酸酯(i-110)
[1747][1748]
根据通用方法iii,从1-(羟基甲基)-3-(1-氧代-5-(((r)-哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮i-47(75mg,0.210mmol)和叔丁基7-甲酰基吲哚啉-1-甲酸酯(78mg,0.315mmol)开始制备化合物i-10。将反应用50%饱和水性碳酸氢钠淬灭并用4:1dcm:iproh萃取三次。将有机层合并,通过相分离器并浓缩到celite上。将粗材料通过硅胶色谱法(在庚烷中的含1%tea的0-100%3:1etoac:etoh)纯化,以提供呈白色固体的叔丁基7-(((2r)-2-(((2-(2,6-二氧代哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)哌啶-1-基)甲基)吲哚啉-1-甲酸酯i-110(87.3mg,0.148mmol,70.3%产率)。lcms[m h]
:589.2。1h nmr(400mhz,dmso-d6)δ10.97(s,1h),7.60(d,j=8.5hz,1h),7.35(d,j=7.7hz,1h),7.13-7.06(m,2h),7.02(t,j=7.6hz,2h),5.08(dd,j=13.3,5.0hz,1h),4.37(d,j=17.2hz,1h),4.31-4.18(m,2h),4.10-3.89(m,4h),3.50(d,j=15.1hz,1h),2.98-2.85(m,3h),2.79-2.70(m,1h),2.63-2.56(m,2h),2.44-2.31(m,1h),2.14-2.06(m,1h),2.03-1.93(m,1h),1.81-1.71(m,1h),1.65-1.33(m,14h)。
[1749]
实例69:3-(5-(((r)-1-(吲哚啉-7-基甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-111)
[1750][1751]
将叔丁基7-(((2r)-2-(((2-(2,6-二氧代哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)哌啶-1-基)甲基)吲哚啉-1-甲酸酯i-110(78.6mg,0.134mmol)悬浮于二噁烷(0.45ml),并溶解于三氟乙醇(0.45ml)中。添加在二噁烷中的4m hcl(0.20ml,0.801mmol),并将反应在室温下搅拌72小时。将反应浓缩,然后用4:1dcm:iproh稀释。将反应用50%饱和水性碳酸氢钠淬灭。将水层用4:1dcm:iproh萃取4次。将有机层合并,通过相分离器并浓缩,以提供呈白色固体的3-(5-(((r)-1-(吲哚啉-7-基甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-111(32.7mg,67μmol,50%产率)。该物质无需纯化即可用于下个步骤。将其余的材料通过碱性反相hplc(在含有5mm nh4oh作为改性剂的h2o中的35%-60%acn)纯化。在样品收集前,测试管中含有3滴甲酸。将含有产物的级分合并并冻干,以提供不纯产物。将材料进一步通过手性酸性反相hplc(在含有0.1%乙酸作为改性剂的h2o中的5%-95%acn,xbridge prep c18,19x50mm,5μm obd,在25℃下流速25ml/min)纯化,以提
供产物,将所述产物溶解于acn和水中并冻干,以提供呈白色固体的3-(5-(((r)-1-(吲哚啉-7-基甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-111(4mg,7.61μmol,5.70%产率)。lcms[m h]
:489.2。1h nmr(400mhz,dmso-d6)δ10.91(s,1h),7.62(dd,j=13.5,6.4hz,1h),7.22-6.91(m,4h),6.57-6.36(m,1h),5.02(dd,j=13.4,5.1hz,1h),4.60-4.33(m,3h),4.23(d,j=16.9hz,1h),4.10(ddd,j=8.9,5.8,3.1hz,1h),3.74(d,j=85.7hz,1h),3.46-3.37(m,2h),2.99(s,1h),2.92-2.82(m,2h),2.57-2.50(m,1h),2.34(dt,j=12.8,6.6hz,1h),1.94(t,j=9.1hz,1h),1.74-1.67(m,2h),1.52-1.39(m,1h),1.13(s,2h),1.11-1.07(m,3h),1.04(s,1h),0.98(d,j=6.2hz,1h)。
[1752]
实例70:3-(5-(((r)-1-((1-乙基吲哚啉-7-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-112)
[1753][1754]
根据通用方法iii,从3-(5-(((r)-1-(吲哚啉-7-基甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-111(32.7mg,67μmol)和乙醛(0.01ml,0.177mmol)开始制备化合物i-112。将反应用50%饱和水性碳酸氢钠淬灭并用4:1dcm:iproh萃取三次。将有机层合并,通过相分离器并浓缩到celite上。将粗材料通过硅胶色谱法(在庚烷中的含1%tea的0-100%3:1etoac:etoh)纯化,以提供呈白色固体的3-(5-(((r)-1-((1-乙基吲哚啉-7-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-112(25.5mg,0.047mmol,70.7%产率)。lcms[m-h]-:515.4。1h nmr(400mhz,dmso-d6)δ10.89(s,1h),7.54(d,j=8.4hz,1h),7.09(d,j=2.4hz,1h),6.97(dd,j=8.3,2.3hz,1h),6.93-6.79(m,2h),6.47(t,j=7.3hz,1h),5.00(dd,j=13.3,5.1hz,1h),4.31(d,j=17.6hz,1h),4.27-4.07(m,3h),3.91(d,j=13.2hz,1h),3.47-3.36(m,1h),3.29(d,j=10.8hz,2h),2.89-2.76(m,3h),2.72-2.65(m,1h),2.54(tt,j=15.0,3.0hz,2h),2.37-2.28(m,1h),2.10-1.87(m,3h),1.70-1.63(m,1h),1.60-1.48(m,2h),1.47-1.26(m,4h),0.92(t,j=7.0hz,3h)。
[1755]
实例74:((1s,3s)-3-甲氧基环丁基)甲磺酸甲酯(int-117)
[1756][1757]
步骤1:((1s,3s)-3-甲氧基环丁基)甲醇(116)
[1758]
将顺式-3-甲氧基环丁烷甲酸(0.1g,0.768mmol)溶解于thf(2.56ml)中并冷却至0℃。逐滴添加在thf中的1m硼烷thf复合物(2.31ml,2.31mmol)。将反应在室温下搅拌过夜。将反应冷却至0℃并用甲醇(1.87ml,46.1mmol)淬灭,并在室温下搅拌2小时。将反应浓缩至干燥并重新溶解于甲醇(5ml)中。将反应在室温下搅拌过夜。将反应浓缩,以提供呈澄清油
状物的((1s,3s)-3-甲氧基环丁基)甲醇116(89mg,0.768mmol,100%产率)。将物质(假定定量产率)无需纯化即可以粗品用于下一反应。1h nmr(400mhz,cdcl3)δ3.81(p,j=7.2hz,1h),3.63(d,j=6.2hz,2h),3.26(s,3h),2.42-2.33(m,2h),2.15-2.01(m,1h),1.73-1.63(m,3h)。
[1759]
步骤2:((1s,3s)-3-甲氧基环丁基)甲磺酸甲酯(int-117)
[1760]
向((1s,3s)-3-甲氧基环丁基)甲醇116(89mg,0.768mmol)在dcm(1.5ml)中的溶液中添加dipea(268μl,1.536mmol)、1-甲基-1h-咪唑(122μl,1.536mmol),然后逐滴添加甲磺酰氯(90μl,1.152mmol)。将反应在室温下搅拌18小时。将反应用dcm(30ml)稀释。将有机层用1m水性hcl洗涤三次,并用饱和水性碳酸氢钠洗涤两次。将有机层通过相分离器并浓缩,以提供呈棕色油状物的((1s,3s)-3-甲氧基环丁基)甲磺酸甲酯int-117(121mg,0.623mmol,81%产率)。1h nmr(400mhz,cdcl3)δ4.22(d,j=6.4hz,2h),3.82(p,j=7.2hz,1h),3.25(s,3h),3.03(s,3h),2.50-2.39(m,2h),2.34-2.21(m,1h),1.81-1.68(m,2h)。
[1761]
实例75:3-(5-(((r)-1-(((1s,3s)-3-甲氧基环丁基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-118)
[1762][1763]
将((1s,3s)-3-甲氧基环丁基)甲磺酸甲酯int-117(121mg,0.623mmol)添加至2ml微波小瓶并溶解于dmf(1.92ml)中。添加3-(1-氧代-5-(((r)-哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮i-47(137mg,0.383mmol),随后添加dipea(0.15ml,0.843mmol)。将反应抽真空并用氮气回填三次。将反应100℃下在微波辐射下搅拌12小时。将反应用50%饱和水性碳酸氢钠淬灭并用4:1dcm:iproh萃取三次。将有机层合并,通过相分离器并浓缩到celite上。将粗材料通过硅胶色谱法(在庚烷中的含1%tea的0-100%3:1etoac:etoh)纯化,以提供稍微不纯的产物。将材料进一步通过碱性物质触发的反相hplc(在含有5mm nh4oh作为改性剂的水中的25%-50%acn)纯化。在样品收集前,测试管中含有3滴甲酸。将纯的级分合并并冻干,以提供呈白色固体的3-(5-(((r)-1-(((1s,3s)-3-甲氧基环丁基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-118的甲酸盐(44.2mg,0.087mmol,22.76%产率)。lcms[m h]
:456.5。1h nmr(400mhz,dmso-d6)δ10.89(s,1h),8.16(s,1h),7.55(d,j=8.3hz,1h),7.12(d,j=2.2hz,1h),6.98(dd,j=8.4,2.3hz,1h),5.00(dd,j=13.3,5.1hz,1h),4.32(d,j=17.2hz,1h),4.20(d,j=17.1hz,1h),4.13-4.02(m,1h),3.96-3.88(m,1h),3.57(p,j=7.3hz,2h),2.99(s,3h),2.89-2.78(m,1h),2.76-2.68(m,1h),2.67-2.48(m,3h),2.40-2.35(m,1h),2.31(dd,j=13.2,4.5hz,1h),2.27-2.16(m,2h),2.16-2.07(m,1h),1.97-1.84(m,2h),1.70-1.50(m,2h),1.49-1.15(m,5h)。
[1764]
实例77:叔丁基4-(2-甲酰基苯基)哌啶-1-甲酸酯(int-121)
(((2r)-2-(((2-(2,6-二氧代哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)哌啶-1-基)甲基)苯基)哌啶-1-甲酸酯i-122(208mg,0.330mmol,78.5%产率)。lcms[m h]
:631.4。1h nmr(400mhz,dmso-d6)δ10.97(s,1h),7.63(d,j=8.4hz,1h),7.27-7.17(m,4h),7.10(td,j=8.6,7.9,2.1hz,2h),5.08(dd,j=13.3,5.1hz,1h),4.42-4.32(m,2h),4.30-4.22(m,2h),4.15-3.99(m,3h),3.42-3.35(m,1h),3.20-3.10(m,1h),2.97-2.77(m,3h),2.64-2.56(m,2h),2.42-2.35(m,1h),2.14-2.05(m,1h),2.03-1.94(m,1h),1.42(s,20h)。
[1773]
实例79:3-(5-(((r)-1-(2-(1-乙基哌啶-4-基)苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-124)
[1774][1775]
步骤1:3-(1-氧代-5-(((r)-1-(2-(哌啶-4-基)苄基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮(123)
[1776]
将叔丁基4-(2-(((2r)-2-(((2-(2,6-二氧代哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)哌啶-1-基)甲基)苯基)哌啶-1-甲酸酯i-122(191mg,0.303mmol)悬浮于二噁烷(1.0ml),并溶解于三氟乙醇(1.0ml)中。添加在二噁烷中的4m hcl(0.45ml,1.817mmol),并将反应在室温下搅拌72小时。将反应浓缩,然后用4:1dcm:iproh稀释。将反应用50%饱和水性碳酸氢钠淬灭。将水层用4:1dcm:iproh萃取4次。将有机层合并,通过相分离器并浓缩,以提供呈白色粘稠固体的3-(1-氧代-5-(((r)-1-(2-(哌啶-4-基)苄基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮123(159mg,0.300mmol,99%产率)。lcms[m h]
:531.5。
[1777]
步骤2:3-(5-(((r)-1-(2-(1-乙基哌啶-4-基)苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-124)
[1778]
根据通用方法iii,从3-(1-氧代-5-(((r)-1-(2-(哌啶-4-基)苄基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮123(159mg,0.300mmol)和乙醛(0.03ml,0.531mmol)开始制备化合物i-124。将反应用50%饱和水性碳酸氢钠淬灭并用4:1dcm:iproh萃取三次。将有机层合并,通过相分离器并浓缩到celite上。将粗材料通过硅胶色谱法(在庚烷中的含1%tea的0-100%3:1etoac:etoh)纯化,以提供呈白色固体的3-(5-(((r)-1-(2-(1-乙基哌啶-4-基)苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-124(58mg,0.102mmol,34.0%产率)。lcms[m h]-
:559.6。1h nmr(400mhz,dmso-d6)δ10.89(s,1h),7.56(d,j=8.4hz,1h),7.21-7.11(m,4h),7.03(dd,j=8.1,1.9hz,2h),5.01(dd,j=13.4,5.1hz,1h),4.35-4.26(m,2h),4.23-4.12(m,2h),4.03(d,j=13.0hz,1h),3.32-3.26(m,1h),2.95-2.77(m,4h),2.77-2.69(m,1h),2.57-2.47(m,2h),2.35-2.22(m,3h),2.05-1.96(m,1h),1.95-1.86(m,2h),1.80-1.72(m,1h),1.70-1.45(m,7h),1.41-1.24(m,3h),0.94(t,j=7.1hz,3h)。
[1779]
实例80:叔丁基4-(4-甲酰基苯基)哌啶-1-甲酸酯,4-(4-甲酰基苯基)哌啶-1-甲
酸,4-(哌啶-4-基)苯甲醛(int-126)
[1780]
步骤1:叔丁基4-(4-(羟基甲基)苯基)哌啶-1-甲酸酯,(4-(哌啶-4-基)苯基)甲醇(125)
[1781]
将4-(1-(叔丁氧基羰基)哌啶-4-基)苯甲酸(0.2g,0.655mmol)溶解于thf(2.18ml)中并冷却至0℃。逐滴添加在thf中的1m硼烷thf复合物(1.97ml,1.97mmol)。将反应在室温下搅拌过夜。将反应冷却至0℃并用甲醇(1.59ml,39.3mmol)淬灭,并在室温下搅拌2小时。将反应浓缩至干燥并重新溶解于甲醇(5ml)中。将反应在室温下搅拌过夜。将反应浓缩,以提供呈澄清胶粘性油状物的叔丁基4-(4-(羟基甲基)苯基)哌啶-1-甲酸酯125(191mg,0.655mmol,100%产率)。物质(假定定量产率)以粗制品用于下一步。lcms[m h-叔丁基]
:192.3。1h nmr(400mhz,cd3od)δ7.18(d,j=8.0hz,2h),7.10(d,j=8.1hz,2h),4.46(s,2h),4.13-4.04(m,2h),2.89-2.66(m,2h),2.66-2.55(m,1h),1.70(d,j=12.4hz,2h),1.54-1.42(m,3h),1.38(s,9h)。
[1782]
步骤2:叔丁基4-(4-甲酰基苯基)哌啶-1-甲酸酯,4-(4-甲酰基苯基)哌啶-1-甲酸,4-(哌啶-4-基)苯甲醛(int-126)
[1783]
将叔丁基4-(4-(羟基甲基)苯基)哌啶-1-甲酸酯125(191mg,0.655mmol)溶解于dcm(3.28ml)中。添加mno2(569mg,6.55mmol),并将反应混合物在室温下搅拌3小时。添加另外的mno2(569mg,6.55mmol),并将反应在室温下搅拌18小时。将反应用dcm稀释并通过celite层。将滤液浓缩,以提供呈黄色油状物的叔丁基4-(4-甲酰基苯基)哌啶-1-甲酸酯int-126(208mg,0.719mmol,110%产率)。物质无需纯化即可以粗品用于下一步,由于存在杂质,产率大于100%。lcms[m h-叔丁基]
:190.2。1h nmr(400mhz,cdcl3)δ9.91(s,1h),7.82-7.70(m,2h),7.34-7.27(m,2h),4.33-4.12(m,2h),2.82-2.63(m,2h),1.83-1.73(m,2h),1.66-1.54(m,3h),1.42(s,9h)。
[1784]
实例81:叔丁基4-(4-(((2r)-2-(((2-(2,6-二氧代哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)哌啶-1-基)甲基)苯基)哌啶-1-甲酸酯(i-127)
[1785][1786]
根据通用方法iii,从3-(1-氧代-5-(((r)-哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮i-47(150mg,0.420mmol)和叔丁基4-(4-甲酰基苯基)哌啶-1-甲酸酯int-126(182mg,0.630mmol)开始制备化合物i-127。将反应用50%饱和水性碳酸氢钠淬灭并用4:1dcm:iproh萃取三次。将有机层合并,通过相分离器并浓缩。将粗材料通过硅胶色谱法(在
基)哌啶-2,6-二酮(i-133)
[1800][1801]
根据通用方法iii,从3-(1-氧代-5-(((r)-哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮i-47(150mg,0.420mmol)和2-甲氧基苯甲醛int-132(86mg,0.630mmol)开始制备化合物i-133。将反应用50%饱和水性碳酸氢钠淬灭并用4:1dcm:iproh萃取三次。将有机层合并,通过相分离器并浓缩。将粗材料通过硅胶色谱法(在庚烷中的含1%tea的0-100%3:1etoac:etoh)纯化,以提供呈白色固体的3-(5-(((r)-1-(2-甲氧基苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-133(75mg,0.151mmol,35.9%产率)。lcms[m h]
:478.4。1h nmr(400mhz,dmso-d6)δ10.97(s,1h),7.62(d,j=8.4hz,1h),7.38(dd,j=7.3,1.8hz,1h),7.23-7.16(m,2h),7.06(dd,j=8.3,2.3hz,1h),6.98-6.87(m,2h),5.08(dd,j=13.3,5.1hz,1h),4.42-4.24(m,3h),4.10(dd,j=10.2,5.4hz,1h),3.93(d,j=14.6hz,1h),3.74(s,3h),3.44(d,j=14.5hz,1h),2.97-2.87(m,1h),2.81-2.71(m,2h),2.64-2.56(m,1h),2.39(qd,j=13.1,4.3hz,1h),2.21-2.14(m,1h),2.04-1.95(m,1h),1.85-1.78(m,1h),1.73-1.63(m,1h),1.57-1.33(m,4h)。
[1802]
实例88:2,3-二氢苯并[b][1,4]二噁英-5-甲醛(int-134)
[1803]
将(2,3-二氢苯并[b][1,4]二噁英-5-基)甲醇(0.1g,0.602mmol)溶解于dcm(3.01ml)中。添加mno2(1.05g,12.0mmol),并将反应混合物在室温下搅拌3小时。添加另外的mno2(1.05g,12.0mmol),并将反应在室温下搅拌18小时。将反应用dcm稀释并通过celite层。将滤液浓缩,以提供呈白色固体的2,3-二氢苯并[b][1,4]二噁英-5-甲醛int-134(75mg,0.457mmol,76%产率)。将物质无需纯化即可用于下一步骤。lcms[m h]
:165.2。1h nmr(400mhz,cdcl3)δ10.39(s,1h),7.42(dd,j=7.8,1.6hz,1h),7.12(dd,j=8.0,1.6hz,1h),6.93(t,j=7.9hz,1h),4.45-4.38(m,2h),4.38-4.30(m,2h)。
[1804]
实例89:3-(5-(((r)-1-((2,3-二氢苯并[b][1,4]二噁英-5-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-135)
[1805][1806]
根据通用方法iii,从3-(1-氧代-5-(((r)-哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮i-47(110mg,0.308mmol)和2,3-二氢苯并[b][1,4]二噁英-5-甲醛int-134
(76mg,0.462mmol)开始制备化合物i-135。将反应用50%饱和水性碳酸氢钠淬灭并用4:1dcm:iproh萃取三次。将有机层合并,通过相分离器并浓缩。将粗材料通过硅胶色谱法(在庚烷中的0-100%3:1:0.01etoac:etoh:tea)纯化,以提供呈白色固体的3-(5-(((r)-1-((2,3-二氢苯并[b][1,4]二噁英-5-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-135(84.7mg,0.164mmol,53.3%产率)。lcms[m h]
:506.5。1h nmr(400mhz,dmso-d6)δ10.97(s,1h),7.62(d,j=8.4hz,1h),7.18(d,j=2.4hz,1h),7.06(dd,j=8.4,2.3hz,1h),6.94(dd,j=7.4,1.8hz,1h),6.77(t,j=7.8hz,1h),6.73-6.67(m,1h),5.08(dd,j=13.3,5.0hz,1h),4.45-4.24(m,3h),4.19(d,j=2.7hz,4h),4.10(dd,j=10.2,5.4hz,1h),3.90(d,j=14.4hz,1h),3.43(d,j=14.6hz,1h),2.97-2.86(m,1h),2.81-2.74(m,2h),2.64-2.56(m,1h),2.39(qd,j=13.1,4.3hz,1h),2.21-2.14(m,1h),2.03-1.95(m,1h),1.85-1.76(m,1h),1.71-1.63(m,1h),1.56-1.33(m,4h)。
[1807]
实例90:苯并[d][1,3]间二氧杂环戊烯-5-甲醛(int-136)
[1808]
将胡椒醇(0.1g,0.657mmol)溶解于dcm(3.29ml)中。添加mno2(1.14g,13.2mmol),并将反应混合物在室温下搅拌3小时。添加另外的mno2(1.14g,13.2mmol),并将反应在室温下搅拌18小时。将反应用dcm稀释并通过celite层。将滤液浓缩,以提供呈澄清油状物的苯并[d][1,3]间二氧杂环戊烯-5-甲醛int-136(87mg,0.579mmol,88%产率)。将物质无需纯化即可用于下一步骤。lcms[m h]
:151.1。1h nmr(400mhz,cdcl3)δ9.84(s,1h),7.44(dd,j=7.9,1.6hz,1h),7.37(d,j=1.6hz,1h),6.96(d,j=7.9hz,1h),6.10(s,2h)。
[1809]
实例91:3-(5-(((r)-1-(苯并[d][1,3]间二氧杂环戊烯-5-基甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-137)
[1810][1811]
根据通用方法iii,从3-(1-氧代-5-(((r)-哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮i-47(130mg,0.364mmol)和苯并[d][1,3]间二氧杂环戊烯-5-甲醛int-136(82mg,0.546mmol)开始制备化合物i-137。将反应用50%饱和水性碳酸氢钠淬灭并用4:1dcm:iproh萃取三次。将有机层合并,通过相分离器并浓缩。将粗材料通过硅胶色谱法(在庚烷中的含1%tea的0-100%3:1etoac:etoh)纯化,以提供呈白色固体的3-(5-(((r)-1-(苯并[d][1,3]间二氧杂环戊烯-5-基甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-137(68mg,0.137mmol,37.7%产率)。lcms[m h]
:492.2。1h nmr(400mhz,dmso-d6)δ10.89(s,1h),7.54(d,j=8.4hz,1h),7.16-7.04(m,1h),6.99(dd,j=8.4,2.2hz,1h),6.81(d,j=1.5hz,1h),6.76-6.66(m,2h),5.89(s,2h),5.00(dd,j=13.3,5.1hz,1h),4.37-4.11(m,3h),4.05(dd,j=11.2,5.2hz,1h),3.82(d,j=13.6hz,1h),3.24-3.21(m,1h),2.89-2.76(m,1h),2.71-2.58(m,2h),2.56-2.47(m,1h),2.37-2.24(m,
1h),2.07-1.99(m,1h),1.95-1.86(m,1h),1.74-1.66(m,1h),1.63-1.55(m,1h),1.49-1.22(m,4h)。
[1812]
实例92:(1r,3r)-3-((叔丁基二苯基甲硅烷基)氧基)环丁烷-1-甲醛(int-139)
[1813][1814]
步骤1:((1r,3r)-3-((叔丁基二苯基甲硅烷基)氧基)环丁基)甲醇(138)
[1815]
将(1r,3r)-3-((叔丁基二苯基甲硅烷基)氧基)环丁烷-1-甲酸(1.77g,4.99mmol)溶解于thf(16.6ml)中并冷却至0℃。逐滴添加在thf中的1m硼烷thf复合物(15ml,15mmol)。将反应在室温下搅拌过夜。将反应冷却至0℃并用甲醇(12.1ml,299mmol)淬灭并在室温下搅拌2小时。将反应浓缩至干燥并重新溶解于甲醇(5ml)中。将反应在室温下搅拌过夜。将反应浓缩,以提供稍微不纯的产物。将材料通过硅胶色谱法(在庚烷中的0-100%etoac)纯化,以提供呈澄清油状物的((1r,3r)-3-((叔丁基二苯基甲硅烷基)氧基)环丁基)甲醇138(1.12g,3.29mmol,65.9%产率)。lcms[m h]
:341.4。1h nmr(400mhz,cdcl3)δ7.76-7.66(m,4h),7.50-7.37(m,6h),4.41(p,j=6.9hz,1h),3.50(d,j=7.1hz,2h),2.42-2.19(m,3h),2.11-1.98(m,2h),1.08(s,9h)。
[1816]
步骤2:(1r,3r)-3-((叔丁基二苯基甲硅烷基)氧基)环丁烷-1-甲醛(int-139)
[1817]
在40ml小瓶中,添加dcm(0.73ml),随后添加草酰氯(0.02ml,0.228mmol),然后冷却至-78℃。逐滴添加在dcm(0.73ml)中的dmso(0.03ml,0.423mmol),并将反应混合物在-78℃下继续搅拌30min。逐滴添加在dcm(1.47ml)中的((1r,3r)-3-((叔丁基二苯基甲硅烷基)氧基)环丁基)甲醇138(50mg,0.147mmol),并将反应混合物在-78℃下继续搅拌1小时。添加三乙胺(102μl,0.734mmol),并将反应放置在室温下1小时。将反应用饱和水性氯化铵淬灭,并用dcm萃取三次。将有机层合并,通过相分离器并真空浓缩,以提供呈粘稠奶油色固体的(1r,3r)-3-((叔丁基二苯基甲硅烷基)氧基)环丁烷-1-甲醛int-139(66mg,0.195mmol,133%产率)。将物质无需纯化即可用于下一步骤。1h nmr(400mhz,cdcl3)δ9.61(d,j=1.9hz,1h),7.60-7.53(m,4h),7.36-7.27(m,6h),4.31-4.19(m,1h),2.97-2.86(m,1h),2.43-2.32(m,2h),2.32-2.18(m,2h),0.96(s,9h)。
[1818]
实例93:3-(5-(((r)-1-(((1r,3r)-3-羟基环丁基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮和3-(5-(((r)-1-(((1s,3s)-3-羟基环丁基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-141a和i-141b)
[1819][1820]
步骤1:3-(5-(((r)-1-(((1r,3r)-3-((叔丁基二苯基甲硅烷基)氧基)环丁基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮和3-(5-(((r)-1-(((1s,3s)-3-((叔丁基二苯基甲硅烷基)氧基)环丁基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(140a和140b)
[1821]
根据通用方法iii,从3-(1-氧代-5-(((r)-哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮i-47(45mg,0.126mmol)和(1r,3r)-3-((叔丁基二苯基甲硅烷基)氧基)环丁烷-1-甲醛int-139(50mg,0.148mmol)开始制备化合物i-140a。将反应用50%饱和水性碳酸氢钠淬灭并用4:1dcm:iproh萃取三次。将有机层合并,通过相分离器并浓缩。将粗材料通过硅胶色谱法(在庚烷中的含1%tea的0-100%3:1etoac:etoh)纯化,以提供均呈透明油状物的3-(5-(((r)-1-(((1r,3r)-3-((叔丁基二苯基甲硅烷基)氧基)环丁基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮140a(45mg,0.066mmol,52.6%产率)和3-(5-(((r)-1-(((1s,3s)-3-((叔丁基二苯基甲硅烷基)氧基)环丁基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮140b(27mg,0.040mmol,31.5%产率)。lcms[m h]
:680.3。
[1822]
步骤2:3-(5-(((r)-1-(((1r,3r)-3-羟基环丁基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮和3-(5-(((r)-1-(((1s,3s)-3-羟基环丁基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-141a和i-141b)
[1823]
将3-(5-(((r)-1-(((1r,3r)-3-((叔丁基二苯基甲硅烷基)氧基)环丁基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮140a(45mg,0.066mmol)溶解于tfa(1.32ml)中,并转移到2ml微波小瓶中。将反应80℃下在微波辐射下搅拌2小时。将物质溶解于4:1dcm:iproh中并用饱和水性碳酸氢钠淬灭。将水层用4:1dcm:iproh萃取三次。将有机层合并,通过相分离器并浓缩。将粗材料通过碱性物质触发的反相hplc(在含有5mm nh4oh作为改性剂的水中的15%-40%acn)纯化。在样品收集前,测试管中含有3滴甲酸。将含有所希望的产物的级分合并并冻干,以提供6.7:1的反式:顺式比的3-(5-(((r)-1-(((1r,3r)-3-羟基环丁基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮和3-(5-(((r)-1-(((1s,3s)-3-羟基环丁基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-141a和i-141b(17mg,0.039mmol,58.2%产率)。lcms[m h]
:442.4。1h nmr(400mhz,dmso-d6)δ10.90(s,1h),7.56(d,j=8.4hz,1h),7.12(d,j=2.4hz,1h),6.99(dd,j=8.5,2.2hz,1h),5.01(dd,j=13.3,5.1hz,1h),4.77(s,1h),4.33(d,j=
17.2hz,1h),4.20(d,j=17.2hz,1h),4.14-3.92(m,3h),2.89-2.79(m,1h),2.77-2.65(m,2h),2.58-2.48(m,2h),2.38-2.16(m,3h),2.11-2.03(m,1h),1.95-1.85(m,2h),1.84-1.73(m,3h),1.68-1.52(m,2h),1.46-1.23(m,4h)。
[1824]
实例94:3-(5-(((r)-1-(3-氟-4-甲氧基苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-142)
[1825][1826]
向3-(1-氧代-5-(((r)-哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮i-47(100mg,0.27mmol)在dmf(3ml)中的搅拌溶液添加4-氟-3-甲氧基苯甲醛(84mg,0.55mmol)和acoh(0.01ml)。将反应在室温下搅拌30min。添加三乙酰氧基硼氢化钠(116mg,0.55mmol),并将反应在80℃下搅拌16小时。将反应用50%饱和水性碳酸氢钠淬灭并用4:1dcm:iproh萃取。将有机层浓缩,并将粗材料通过硅胶色谱法(在己烷中的80%etoac)纯化,以提供呈浅黄色粘性固体的3-(5-(((r)-1-(3-氟-4-甲氧基苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-142(15mg,0.03mmol,11.1%产率)。lcms[m h]
:496.15。1h nmr(300mhz,dmso-d6):δ7.69(d,j=8.7hz,1h),7.11-7.07(m,3h),7.00-6.93(m,1h),6.88-6.86(m,1h),5.14-5.08(m,1h),4.43-4.42(m,2h),4.28-4.20(m 2h),4.02(d,j=13.2hz,1h),3.81(s,3h),3.39(d,j=13.8hz,1h),2.90-2.74(m,4h),2.55-2.45(m 1h),2.18-2.13(m,2h),1.82(m,2h),1.65-1.55(m,3h),1.39(m 1h)。
[1827]
根据实例94,从实例24(i-47)的最终产物开始制备以下化合物。
[1828]
[1829]
[1830]
[1831]
[1832]
[1833][1834]
实例105:叔丁基4-(2-乙基-4-甲酰基苯基)哌啶-1-甲酸酯(int-154)
[1835]
将叔丁基4-(2-乙基-4-(羟基甲基)苯基)哌啶-1-甲酸酯153(147.6mg,0.462mmol)和二氧化锰(415.7mg,4.78mmol)悬浮于dcm(2ml)。将反应在室温下搅拌22小时。将反应通过celite过滤并用二氯甲烷洗涤。将滤液浓缩,并通过硅胶色谱法(在庚烷中的0-60%etoac)纯化,以提供呈透明液体的叔丁基4-(2-乙基-4-甲酰基苯基)哌啶-1-甲酸酯int-154(157mg,0.485mmol,105%产率)。lcms[m h-叔丁基]
:262.2。1h nmr(400mhz,cd2cl2)δ9.94(s,1h),7.72-7.64(m,2h),7.37(d,j=7.9hz,1h),4.25(dp,j=13.5,1.9hz,2h),2.98(tt,j=11.6,3.9hz,1h),2.90-2.72(m,4h),1.80-1.55(m,4h),1.47(s,9h),1.32-1.25(m,3h)。
[1836]
实例106:叔丁基4-(4-(((2r)-2-(((2-(2,6-二氧代哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)哌啶-1-基)甲基)-2-乙基苯基)哌啶-1-甲酸酯(i-155)
[1837][1838]
将3-(1-氧代-5-(((r)-哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮i-47
(57.8mg,0.162mmol)和叔丁基4-(2-乙基-4-甲酰基苯基)哌啶-1-甲酸酯int-154(72.3mg,0.228mmol)溶解于dmf(1ml)中。添加三乙酰氧基硼氢化钠(78.6mg,0.371mmol)并将反应在室温下搅拌过夜。将反应用50%饱和水性碳酸氢钠淬灭。将反应用4:1二氯甲烷:异丙醇萃取。将有机层合并,通过相分离器并真空浓缩。将粗材料通过硅胶色谱法(在dcm中的含1%tea的0-80%3:1etoac:etoh)纯化,以提供呈白色固体的叔丁基4-(4-(((2r)-2-(((2-(2,6-二氧代哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)哌啶-1-基)甲基)-2-乙基苯基)哌啶-1-甲酸酯i-155(36.9mg,0.055mmol,34%产率)。lcms[m h]
:659.6。1h nmr(400mhz,dmso-d6)δ10.95(s,1h),7.60(d,j=8.4hz,1h),7.17(d,j=2.2hz,1h),7.14-7.00(m,4h),5.07(dd,j=13.3,5.1hz,1h),4.43-4.18(m,3h),4.16-3.98(m,3h),3.92(d,j=13.8hz,1h),2.98-2.65(m,8h),2.65-2.55(m,3h),2.44-2.33(m,1h),2.11(t,j=9.5hz,1h),2.03-1.93(m,1h),1.86-1.72(m,1h),1.71-1.29(m,17h),1.16-1.07(m,3h)。
[1839]
实例107:3-(5-(((r)-1-(3-乙基-4-(哌啶-4-基)苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-156)
[1840][1841]
将叔丁基4-(4-(((2r)-2-(((2-(2,6-二氧代哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)哌啶-1-基)甲基)-2-乙基苯基)哌啶-1-甲酸酯i-155(30mg,0.046mmol)溶解于在二噁烷中的4m hcl(1ml,4.00mmol)中并在室温下搅拌过夜。将反应浓缩,用二乙醚研磨,过滤,并放置于高真空下过夜,以提供呈白色固体的3-(5-(((r)-1-(3-乙基-4-(哌啶-4-基)苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-156(25mg,0.038mmol,83%产率)。lcms[m h]
:559.8。1h nmr(400mhz,dmso-d6)δ10.97(s,1h),10.32-10.07(m,1h),8.83-8.59(m,2h),7.69(d,j=8.4hz,1h),7.49-7.33(m,2h),7.26(s,1h),7.22-7.07(m,2h),5.09(dd,j=13.3,5.1hz,1h),4.73-4.48(m,3h),4.48-4.24(m,4h),4.16(dd,j=13.2,7.0hz,1h),3.37-3.30(m,2h),3.13-2.88(m,5h),2.68-2.61(m,2h),2.44-2.36(m,1h),2.11-1.65(m,10h),1.19-1.13(m,3h)。
[1842]
实例108:3-(5-(((r)-1-(3-乙基-4-(1-乙基哌啶-4-基)苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-157)
[1843][1844]
将3-(5-(((r)-1-(3-乙基-4-(哌啶-4-基)苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-156(25mg,0.040mmol)和乙醛(3.11μl,0.055mmol)溶解于2,2,2-三氟乙醇(0.5ml)中并搅拌5分钟。添加三乙酰氧基硼氢化钠(16.78mg,0.079mmol)并将反应在室温下搅拌过夜。将反应用50%饱和水性碳酸氢钠淬灭。将反应用4:1二氯甲烷:异丙醇萃取。将有机层合并,通过相分离器并真空浓缩。将粗材料通过硅胶色谱法(在dcm中的含1%tea的0-60%3:1etoac:etoh)纯化,以提供呈白色固体的3-(5-(((r)-1-(3-乙基-4-(1-乙基哌啶-4-基)苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-157(11.8mg,0.020mmol,50%产率)。lcms[m h]
:587.8。1h nmr(400mhz,dmso-d6)δ10.96(s,1h),7.60(d,j=8.4hz,1h),7.26-6.91(m,5h),5.07(dd,j=13.3,5.1hz,1h),4.47-4.18(m,3h),4.11(dd,j=10.3,5.3hz,1h),3.92(d,j=13.8hz,1h),3.03-2.84(m,3h),2.74(dt,j=8.9,4.7hz,2h),2.58(q,j=7.3hz,4h),2.43-2.32(m,3h),2.11(ddd,j=11.5,8.6,3.1hz,1h),2.01-1.89(m,3h),1.78(d,j=11.3hz,1h),1.72-1.30(m,10h),1.10(t,j=7.5hz,3h),1.01(t,j=7.1hz,3h)。
[1845]
实例110:4-(哌啶-1-基)苯甲醛(int-160)
[1846]
步骤1:(4-(哌啶-1-基)苯基)甲醇(159)
[1847]
在0℃下,将在甲苯中的1m dibal-h(259mg,1.824mmol)添加至甲基4-(哌啶-1-基)苯甲酸酯(200mg,0.912mmol)在thf(4.5ml)中的的混合物。经17小时将反应缓慢升温至室温。添加另外的在甲苯中的1m dibal-h(259mg,1.824mmol),并将溶液在室温下搅拌2.5小时。将反应用饱和水性罗谢尔盐淬灭,进一步用水稀释,并用etoac萃取。将有机层合并,用盐水洗涤,经na2so4干燥,过滤并真空浓缩。将粗材料通过硅胶色谱法(在庚烷中的0-100%etoac)纯化,以提供呈澄清油状物的(4-(哌啶-1-基)苯基)甲醇159(90.5mg,0.473mmol,52%产率)。lcms[m h]
:192.3。1h nmr(400mhz,cdcl3)δ7.25(d,j=8.3hz,2h),6.93(d,j=8.2hz,2h),4.59(d,j=4.9hz,2h),3.20-3.10(m,4h),1.71(p,j=5.7hz,4h),1.58(p,j=5.7,5.3hz,2h),1.46(t,j=5.7hz,1h)。
[1848]
步骤2:4-(哌啶-1-基)苯甲醛(int-160)
[1849]
将(4-(哌啶-1-基)苯基)甲醇159(90.5mg,0.473mmol)和二氧化锰(411mg,4.73mmol)悬浮于dcm(2ml)。将反应在室温下搅拌过夜。将反应通过celite过滤并用二氯甲烷冲洗。将滤液真空浓缩。将粗材料通过硅胶色谱法(在庚烷中的0-60%etoac)纯化,以提供呈透明液体的4-(哌啶-1-基)苯甲醛int-160(73.9mg,0.387mmol,82%产率),其结晶成
白色固体。lcms[m h]
:190.0。1h nmr(400mhz,cd2cl2)δ9.74(s,1h),7.81-7.66(m,2h),7.01(d,j=8.5hz,2h),3.47-3.33(m,4h),1.80-1.61(m,6h)。
[1850]
实例111:3-(1-氧代-5-(((r)-1-(4-(哌啶-1-基)苄基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮(i-161)
[1851][1852]
将3-(1-氧代-5-(((r)-哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮i-47(26.5mg,0.074mmol)和4-(哌啶-1-基)苯甲醛int-160(16.6mg,0.088mmol)溶解于dmf(0.5ml)中。添加三乙酰氧基硼氢化钠(44mg,0.208mmol)并将反应在室温下搅拌过夜。将反应用50%饱和水性碳酸氢钠淬灭。将反应用4:1二氯甲烷:异丙醇萃取。将有机层合并,通过相分离器并真空浓缩。将粗材料通过硅胶色谱法(在dcm中的含1%tea的0-100%3:1etoac:etoh)纯化,以提供呈白色固体的3-(1-氧代-5-(((r)-1-(4-(哌啶-1-基)苄基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮i-161(15.9mg,0.029mmol,39%产率)。lcms[m h]
:531.4。1h nmr(400mhz,dmso-d6)δ10.96(s,1h),7.61(d,j=8.4hz,1h),7.17(s,1h),7.12(d,j=8.5hz,2h),7.06(dd,j=8.4,2.2hz,1h),6.90-6.79(m,2h),5.07(dd,j=13.3,5.1hz,1h),4.46-4.18(m,3h),4.17-4.08(m,1h),3.87(d,j=13.3hz,1h),3.06(t,j=5.4hz,4h),2.91(ddd,j=18.0,13.6,5.4hz,1h),2.77-2.66(m,2h),2.59(d,j=17.5hz,1h),2.38(dd,j=13.2,4.4hz,1h),2.08(t,j=9.8hz,1h),1.97(d,j=10.6hz,1h),1.76(d,j=4.4hz,1h),1.70-1.43(m,10h),1.35(q,j=11.8hz,2h)。
[1853]
实例112:3-甲氧基双环[1.1.1]戊烷-1-甲醛(int-162)
[1854]
在40ml小瓶中,添加dcm(1.5ml),随后添加草酰氯(0.08ml,0.914mmol),然后冷却至-78℃。逐滴添加在dcm(1.5ml)中的dmso(0.15ml,2.11mmol),并将反应混合物在-78℃下继续搅拌30min。逐滴添加在dcm(3ml)中的(3-甲氧基双环[1.1.1]戊烷-1-基)甲醇(89.2mg,0.696mmol),并将反应混合物在-78℃下继续搅拌1小时。添加三乙胺(500μl,3.59mmol),并将反应升温至室温过夜。将反应用饱和水性氯化铵淬灭,并用dcm萃取三次。将有机层合并,通过相分离器并真空浓缩。将粗材料通过硅胶色谱法(在庚烷中的0-100%etoac)纯化,以提供呈透明液体的3-甲氧基双环[1.1.1]戊烷-1-甲醛int-162(27.6mg,0.208mmol,30%产率)。1h nmr(400mhz,cd2cl2)δ9.71(s,1h),3.28(s,3h),2.13(s,6h)。
[1855]
实例113:3-(5-(((r)-1-((3-甲氧基双环[1.1.1]戊烷-1-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-163)
[1856][1857]
将3-(1-氧代-5-(((r)-哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮i-47(48.3mg,0.135mmol)和3-甲氧基双环[1.1.1]戊烷-1-甲醛int-162(27.6mg,0.219mmol)溶解于dmf(0.5ml)中。添加三乙酰氧基硼氢化钠(93mg,0.439mmol)并将反应在室温下搅拌过夜。将反应用50%饱和水性碳酸氢钠淬灭。将反应用4:1二氯甲烷:异丙醇萃取。将有机层合并,通过相分离器并真空浓缩。将粗材料通过硅胶色谱法(在dcm中的含1%tea的0-80%3:1etoac:etoh)纯化,以提供呈灰白色固体的3-(5-(((r)-1-((3-甲氧基双环[1.1.1]戊烷-1-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-163(33.6mg,0.070mmol,52.1%产率)。lcms[m h]
:468.5。1h nmr(400mhz,dmso-d6)δ10.96(s,1h),7.62(d,j=8.4hz,1h),7.18(d,j=2.2hz,1h),7.05(dd,j=8.4,2.2hz,1h),5.07(dd,j=13.3,5.1hz,1h),4.44-4.22(m,2h),4.14(ddd,j=10.1,4.7,2.6hz,1h),3.99(ddd,j=10.0,5.4,2.1hz,1h),3.14(s,3h),2.97-2.84(m,2h),2.85-2.74(m,2h),2.70-2.64(m,1h),2.63-2.54(m,1h),2.45-2.35(m,2h),2.04-1.93(m,1h),1.78-1.68(m,7h),1.68-1.58(m,1h),1.57-1.25(m,4h)。
[1858]
实例114:叔丁基4-(4-氟-2-甲酰基苯基)哌嗪-1-甲酸酯(int-166)
[1859][1860]
步骤1:2-(4-(叔丁氧基羰基)哌嗪-1-基)-5-氟苯甲酸(164)
[1861]
将5-氟-2-(哌嗪-1-基)苯甲酸(300.9mg,1.342mmol)、boc-酸酐(352.4mg,1.615mmol)和碳酸氢钠(353.0mg,4.20mmol)悬浮于thf(4.5ml)。将反应在室温下搅拌过夜。将反应用水淬灭并用dcm洗涤。分离并弃去dcm层。将水层用1n hcl酸化至ph 5并用dcm萃取三次。将有机层合并,经硫酸镁干燥,过滤并真空浓缩,以提供呈白色泡沫状的2-(4-(叔丁氧基羰基)哌嗪-1-基)-5-氟苯甲酸164(46.0mg,0.140mmol,10.5%产率)。lcms[m h]
:325.6。1h nmr(400mhz,dmso-d6)δ7.72(dd,j=8.9,4.9hz,1h),7.67(dd,j=9.1,3.1hz,1h),7.50(ddd,j=8.9,8.0,3.2hz,1h),3.52(t,j=5.0hz,4h),3.02(t,j=5.0hz,4h),1.43(s,9h)。
[1862]
步骤2:叔丁基4-(4-氟-2-(羟基甲基)苯基)哌嗪-1-甲酸酯(165)
[1863]
将2-(4-(叔丁氧基羰基)哌嗪-1-基)-5-氟苯甲酸164(46mg,0.142mmol)溶解于thf(0.5ml)中并冷却至0℃。添加在thf中的1m硼烷四氢呋喃复合物(0.5ml,0.500mmol),并
将反应升温至室温过夜。将反应冷却至0℃并用甲醇(0.3ml)淬灭。然后将溶液浓缩至干燥并在meoh(1.000ml)中重构,并在室温下搅拌过夜。将反应真空浓缩,并通过硅胶色谱法(在庚烷中的0-80%etoac)纯化,以提供呈透明、粘稠液体的叔丁基4-(4-氟-2-(羟基甲基)苯基)哌嗪-1-甲酸酯165(41.7mg,0.134mmol,95%产率)。lcms[m h]
:311.2。1h nmr(400mhz,cd2cl2)δ7.22-7.12(m,1h),7.06-6.94(m,2h),4.76(s,2h),3.61(t,j=5.0hz,4h),2.91(t,j=5.0hz,4h),1.46(s,9h)。
[1864]
步骤3:叔丁基4-(4-氟-2-甲酰基苯基)哌嗪-1-甲酸酯(int-166)
[1865]
将叔丁基4-(4-氟-2-(羟基甲基)苯基)哌嗪-1-甲酸酯165(41.7mg,0.134mmol)和二氧化锰(122.4mg,1.408mmol)悬浮于dcm(1ml)。将反应在室温下搅拌4天。将反应用celite过滤并用dcm冲洗。将滤液真空浓缩,并通过硅胶色谱法(在庚烷中的0-60%etoac)纯化,以提供呈黄色粘稠胶状物的叔丁基4-(4-氟-2-甲酰基苯基)哌嗪-1-甲酸酯int-166(26.3mg,0.085mmol,63.5%产率)。lcms[m h]
:309.5。1h nmr(400mhz,cd2cl2)δ10.37(d,j=2.9hz,1h),7.53-7.46(m,1h),7.28(ddd,j=8.9,7.7,3.1hz,1h),7.25-7.19(m,1h),3.65-3.58(m,4h),3.04-2.96(m,4h),1.46(s,9h)。
[1866]
实例115:叔丁基4-(2-(((2r)-2-(((2-(2,6-二氧代哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)哌啶-1-基)甲基)-4-氟苯基)哌嗪-1-甲酸酯(i-167)
[1867][1868]
将3-(1-氧代-5-(((r)-哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮i-47(25.8mg,0.072mmol)和叔丁基4-(4-氟-2-甲酰基苯基)哌嗪-1-甲酸酯int-166(26.3mg,0.085mmol)溶解于dmf(0.5ml)中。添加三乙酰氧基硼氢化钠(50.6mg,0.239mmol),并将反应在室温下搅拌36小时。将反应用50%饱和水性碳酸氢钠淬灭。将反应用4:1二氯甲烷:异丙醇萃取。将有机层合并,通过相分离器并真空浓缩。将粗材料通过硅胶色谱法(在dcm中的含1%tea的0-80%3:1etoac:etoh)纯化,以提供分离为白色固体的叔丁基4-(2-(((2r)-2-(((2-(2,6-二氧代哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)哌啶-1-基)甲基)-4-氟苯基)哌嗪-1-甲酸酯i-167(20.3mg,0.030mmol,42.0%产率)。lcms[m h]
:468.5。1h nmr(400mhz,dmso-d6)δ10.96(s,1h),7.62(d,j=8.4hz,1h),7.18(d,j=2.2hz,1h),7.05(dd,j=8.4,2.2hz,1h),5.07(dd,j=13.3,5.1hz,1h),4.44-4.22(m,2h),4.14(ddd,j=10.1,4.7,2.6hz,1h),3.99(ddd,j=10.0,5.4,2.1hz,1h),3.14(s,3h),2.97-2.84(m,2h),2.85-2.74(m,2h),2.70-2.64(m,1h),2.63-2.54(m,1h),2.45-2.35(m,2h),2.04-1.93(m,1h),1.78-1.68(m,7h),1.68-1.58(m,1h),1.57-1.25(m,4h)。
[1869]
实例116:3-(5-(((r)-1-(5-氟-2-(哌嗪-1-基)苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-168)
[1870][1871]
将叔丁基4-(2-(((2r)-2-(((2-(2,6-二氧代哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)哌啶-1-基)甲基)-4-氟苯基)哌嗪-1-甲酸酯i-167(18.0mg,0.028mmol)溶解于在二噁烷中的4m hcl(0.8ml,3.20mmol)中,并在室温下搅拌过夜。将反应浓缩并用二乙醚研磨,过滤,并在高真空下干燥过夜,以提供呈白色固体的3-(5-(((r)-1-(5-氟-2-(哌嗪-1-基)苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-168的hcl盐(14.8mg,0.024mmol,86%产率)。lcms[m h]
:550.5。1h nmr(400mhz,dmso-d6)δ10.98(s,1h),10.12-9.72(m,1h),9.06(s,2h),7.77-7.57(m,2h),7.43-7.22(m,3h),7.21-7.09(m,1h),5.10(ddd,j=13.2,5.2,2.2hz,1h),4.65(t,j=11.5hz,1h),4.58-4.24(m,4h),3.90(d,j=33.5hz,1h),3.30-3.11(m,4h),3.10-2.86(m,5h),2.67-2.57(m,1h),2.47-2.36(m,1h),2.21-1.88(m,3h),1.88-1.69(m,3h),1.69-1.52(m,1h),1.10(t,j=7.0hz,3h)。
[1872]
实例117:3-(5-(((r)-1-(2-(4-乙基哌嗪-1-基)-5-氟苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-169)
[1873][1874]
将3-(5-(((r)-1-(5-氟-2-(哌嗪-1-基)苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-168(13.5mg,0.023mmol)和乙醛(1.81μl,0.032mmol)溶解于2,2,2-三氟乙醇(0.5ml)中,并搅拌5分钟。一次性添加三乙酰氧基硼氢化钠(9.76mg,0.046mmol),并在室温下搅拌2小时。将反应用50%饱和水性碳酸氢钠淬灭。将反应用4:1二氯甲烷:异丙醇萃取。将有机层合并,通过相分离器并真空浓缩。将粗材料通过硅胶色谱法(在dcm中的含1%tea的0-60%3:1etoac:etoh)纯化,以提供呈白色固体的3-(5-(((r)-1-(2-(4-乙基哌嗪-1-基)-5-氟苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-169(9.1mg,0.015mmol,67%产率)。lcms[m h]
:578.5。1h nmr(400mhz,dmso-d6)δ10.95(s,1h),7.60(d,j=8.4hz,1h),7.28(dd,j=10.2,3.2hz,1h),7.15-7.10(m,1h),7.07(dd,j=8.8,5.3hz,1h),7.04-6.88(m,2h),5.07(dd,j=13.3,5.1hz,1h),4.42-4.19(m,3h),4.12-4.04(m,1h),3.92(d,j=14.7hz,1h),3.56(d,j=14.7hz,1h),2.98-2.69(m,6h),2.64-2.54(m,1h),2.47-2.28(m,8h),2.26-2.16(m,1h),2.01-1.92(m,1h),1.84-1.71(m,1h),1.71-1.34(m,5h),1.00(t,j=7.1hz,3h)。
[1875]
实例118:4-(1-(三氟甲基)环丙基)苯甲醛(int-172)
[1876][1877]
170来自acs medicinal chemistry letters[acs药物化学快报],2013,第4(6)卷,第514-516页;doi:10.1021/ml400045j
[1878]
步骤1:(4-(1-(三氟甲基)环丙基)苯基)甲醇(171)
[1879]
将4-(1-(三氟甲基)环丙基)苯甲酸170(257.4mg,1.118mmol)溶解于thf(3.5ml)中并冷却至0℃。添加在thf中的1m硼烷四氢呋喃复合物(3.1ml,3.10mmol),并将反应升温至室温过夜。将反应冷却至0℃并用甲醇(2.2ml)淬灭。将反应浓缩至干燥,在meoh(7ml)中重构并在室温下搅拌过夜。将反应真空浓缩,并通过硅胶色谱法(在庚烷中的0-80%etoac)纯化,以提供呈透明液体的(4-(1-(三氟甲基)环丙基)苯基)甲醇171(163.7mg,0.757mmol,67.7%产率)。1h nmr(400mhz,cd2cl2)δ7.50(d,j=8.1hz,2h),7.42-7.34(m,2h),4.71(s,2h),1.42-1.36(m,2h),1.12-1.04(m,2h)。
[1880]
步骤2:4-(1-(三氟甲基)环丙基)苯甲醛(int-172)
[1881]
将(4-(1-(三氟甲基)环丙基)苯基)甲醇171(163.7mg,0.757mmol)和二氧化锰(659.7mg,7.59mmol)悬浮于dcm(5ml)。在室温下搅拌36小时。将反应通过celite过滤并用dcm冲洗。将滤液真空浓缩,并通过硅胶色谱法(在庚烷中的0-60%etoac)纯化,以提供呈透明液体的4-(1-(三氟甲基)环丙基)苯甲醛int-172(114.4mg,0.529mmol,69.8%产率)。lcms[m h]
:215.1。1h nmr(400mhz,cd2cl2)δ10.02(s,1h),7.91-7.82(m,2h),7.71-7.59(m,2h),1.47-1.40(m,2h),1.14-1.08(m,2h)。
[1882]
实例119:3-(1-氧代-5-(((r)-1-(4-(1-(三氟甲基)环丙基)苄基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮(i-173)
[1883][1884]
将3-(1-氧代-5-(((r)-哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮i-47(133.2mg,0.373mmol)和4-(1-(三氟甲基)环丙基)苯甲醛int-172(114.4mg,0.534mmol)溶解于dmf(2ml)中。添加三乙酰氧基硼氢化钠(246mg,1.161mmol)并将反应在室温下搅拌过夜。将反应用50%饱和水性碳酸氢钠淬灭。将反应用4:1二氯甲烷:异丙醇萃取。将有机层合
并,通过相分离器并真空浓缩。将粗材料通过硅胶色谱法(在dcm中的含1%tea的0-80%3:1etoac:etoh)纯化,以提供分离为白色固体的3-(1-氧代-5-(((r)-1-(4-(1-(三氟甲基)环丙基)苄基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮i-173(138.9mg,0.248mmol,66.4%产率)。lcms[m h]
:556.2。1h nmr(400mhz,dmso-d6)δ10.95(s,1h),7.60(d,j=8.4hz,1h),7.41-7.28(m,4h),7.20-7.13(m,1h),7.04(dd,j=8.4,2.2hz,1h),5.07(dd,j=13.3,5.1hz,1h),4.44-4.20(m,3h),4.16-4.06(m,1h),4.00(d,j=14.1hz,1h),3.41(d,j=14.1hz,1h),2.90(ddd,j=17.2,13.4,5.4hz,1h),2.81-2.64(m,2h),2.64-2.54(m,1h),2.44-2.32(m,1h),2.19-2.08(m,1h),2.03-1.90(m,1h),1.86-1.74(m,1h),1.72-1.61(m,1h),1.60-1.32(m,4h),1.32-1.26(m,2h),1.09-1.01(m,2h)。
[1885]
实例120:3,4-二氢-2h-苯并[b][1,4]噁嗪-5-甲醛(int-176)和3-氧代-3,4-二氢-2h-苯并[b][1,4]噁嗪-5-甲醛(int-177)
[1886][1887]
步骤1:3,4-二氢-2h-苯并[b][1,4]噁嗪-5-甲酸(174)
[1888]
将甲基3,4-二氢-2h-苯并[b][1,4]噁嗪-5-甲酸酯(207.6mg,1.08mmol)溶解于meoh(1.5ml)和水(1ml)中。添加1m水性氢氧化钠(2.2ml,2.200mmol),并将反应在55℃下搅拌25小时。将反应部分浓缩以除去甲醇,然后用1m hcl溶液酸化至约ph 2。通过过滤收集沉淀物,并用二乙醚洗涤,以提供呈白色固体的3,4-二氢-2h-苯并[b][1,4]噁嗪-5-甲酸174(61.9mg,0.339mmol,31.5%产率)。将物质无需纯化即可用于下一步骤。lcms[m h]
=180.1。1h nmr(400mhz,dmso-d6)δ12.54(s,1h),8.51-7.37(m,1h),7.34(dd,j=8.1,1.5hz,1h),6.83(dd,j=7.7,1.5hz,1h),6.43(t,j=7.9hz,1h),4.18-4.02(m,2h),3.51-3.40(m,2h)。
[1889]
步骤2:(3,4-二氢-2h-苯并[b][1,4]噁嗪-5-基)甲醇(175)
[1890]
将3,4-二氢-2h-苯并[b][1,4]噁嗪-5-甲酸174(61.9mg,0.345mmol)溶解于thf(1ml)中并冷却至0℃。将在thf中的1m硼烷四氢呋喃复合物(1ml,1.00mmol)添加至反应。将反应升温至室温过夜。将反应冷却至0℃并用甲醇(0.7ml)淬灭。将反应浓缩至干燥,在meoh(2ml)中重构并在室温下搅拌过夜。将反应浓缩,并通过硅胶色谱法(在庚烷中的0-100%etoac)纯化,以提供呈不透明、粘稠液体的(3,4-二氢-2h-苯并[b][1,4]噁嗪-5-基)甲醇175(62.5mg,0.341mmol,99%产率)。lcms[m h]
=166.2。1h nmr(400mhz,cd2cl2)δ6.73(dd,j=7.9,1.6hz,1h),6.71-6.67(m,1h),6.64-6.56(m,1h),4.63(s,2h),4.25-4.17(m,2h),3.51-3.42(m,2h)。
[1891]
步骤3:3,4-二氢-2h-苯并[b][1,4]噁嗪-5-甲醛(int-176)和3-氧代-3,4-二氢-2h-苯并[b][1,4]噁嗪-5-甲醛(int-177)
[1892]
将(3,4-二氢-2h-苯并[b][1,4]噁嗪-5-基)甲醇175(57.1mg,0.346mmol)和二氧化锰(306.5mg,3.53mmol)悬浮于dcm(2ml)。将反应在室温下搅拌过夜。将反应物用celite过滤并且用dcm洗涤。将滤液浓缩,并通过硅胶色谱法(在庚烷中的0-60%etoac)纯化,以提
供呈黄色液体的3,4-二氢-2h-苯并[b][1,4]噁嗪-5-甲醛int-176(11.5mg,0.070mmol,20.2%产率)和呈橙色固体的3-氧代-3,4-二氢-2h-苯并[b][1,4]噁嗪-5-甲醛int-177(12.2mg,0.067mmol,19.3%产率)。
[1893]
3,4-二氢-2h-苯并[b][1,4]噁嗪-5-甲醛int-176:lcms[m h]
=164.2。1h nmr(400mhz,cd2cl2)δ9.86(s,1h),8.57-7.27(m,1h),7.16(dd,j=7.8,1.5hz,1h),6.95(dd,j=7.7,1.5hz,1h),6.64(t,j=7.8hz,1h),4.29-4.21(m,2h),3.63-3.53(m,2h)。
[1894]
3-氧代-3,4-二氢-2h-苯并[b][1,4]噁嗪-5-甲醛int-177:lcms[m h]
=178.2。1h nmr(400mhz,cd2cl2)δ10.37(s,1h),9.96(s,1h),7.40(dd,j=7.6,1.4hz,1h),7.23(ddd,j=8.1,1.4,0.7hz,1h),7.17-7.09(m,1h),4.66(s,2h)。
[1895]
实例121:3-(5-(((r)-1-((3,4-二氢-2h-苯并[b][1,4]噁嗪-5-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-178)
[1896][1897]
将3-(1-氧代-5-(((r)-哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮i-47(18.3mg,0.051mmol)和3,4-二氢-2h-苯并[b][1,4]噁嗪-5-甲醛int-176(11.5mg,0.070mmol)溶解于dmf(0.5ml)中。添加三乙酰氧基硼氢化钠(34.5mg;0.163mmol)并且将反应在室温下搅拌5天。将反应用50%饱和水性碳酸氢钠淬灭。将反应用4:1二氯甲烷:异丙醇萃取三次。将有机层合并,通过相分离器并真空浓缩。将粗材料通过硅胶色谱法(在dcm中的含1%tea的0-80%3:1etoac:etoh)纯化,以提供呈白色固体的3-(5-(((r)-1-((3,4-二氢-2h-苯并[b][1,4]噁嗪-5-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-178(7.9mg,0.015mmol,29.0%产率)。lcms[m h]
:468.5。1h nmr(400mhz,dmso-d6)δ10.96(s,1h),7.63(d,j=8.4hz,1h),7.19(d,j=2.2hz,1h),7.08(dd,j=8.4,2.2hz,1h),6.58(ddd,j=12.3,7.7,1.5hz,2h),6.42(dd,j=8.0,7.3hz,1h),5.92(s,1h),5.07(dd,j=13.3,5.1hz,1h),4.49-4.18(m,4h),4.15-3.93(m,3h),3.45-3.36(m,1h),3.23(dd,j=12.8,3.3hz,1h),2.97-2.84(m,1h),2.73-2.70(m,1h),2.70-2.64(m,2h),2.63-2.54(m,1h),2.38(dd,j=13.2,4.5hz,1h),2.11-1.94(m,2h),1.70(dd,j=21.6,11.9hz,3h),1.59-1.45(m,1h),1.45-1.32(m,2h)。
[1898]
实例122:3-(5-(((r)-1-((4-乙基-3,4-二氢-2h-苯并[b][1,4]噁嗪-5-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-179)
基)哌啶-2,6-二酮i-180(3.1mg,5.80μmol,7.73%产率)。lcms[m h]
:519.3。1h nmr(400mhz,cdcl3)δ10.62(s,1h),7.94(d,j=6.2hz,1h),7.79(d,j=8.5hz,1h),7.24-7.14(m,1h),7.10(dt,j=8.5,1.9hz,1h),6.92-6.77(m,2h),6.77-6.68(m,1h),5.18(ddd,j=13.3,5.3,1.5hz,1h),4.67-4.19(m,6h),4.03(ddd,j=10.2,4.8,3.2hz,1h),3.31(d,j=13.3hz,1h),2.98-2.75(m,3h),2.71-2.58(m,1h),2.33(qd,j=13.1,5.0hz,1h),2.25-2.14(m,1h),2.13-2.06(m,1h),2.00-1.88(m,1h),1.86-1.78(m,1h),1.78-1.67(m,1h),1.50-1.37(m,2h)。
[1904]
实例124:2-(苄氧基)乙醛(int-182)
[1905][1906]
步骤1:2-(苄氧基)乙-1-醇(181)
[1907]
将2-(苄氧基)乙酸(319.6mg,1.923mmol)溶解于thf(4ml)中并冷却至0℃。添加在thf中的1m硼烷四氢呋喃复合物(5.3ml,5.30mmol),并将反应升温至室温过夜。将反应冷却至0℃并用甲醇(4ml)淬灭。将反应浓缩至干燥,并在meoh(8.00ml)中重构并在室温下搅拌过夜。将反应浓缩,并通过硅胶色谱法(在庚烷中的0-100%etoac)纯化,以提供呈透明液体的2-(苄氧基)乙-1-醇181。1h nmr(400mhz,cd2cl2)δ7.39-7.25(m,5h),4.55(s,2h),3.74-3.67(m,2h),3.62-3.53(m,2h)。
[1908]
步骤2:2-(苄氧基)乙醛
[1909]
在40ml小瓶中,添加dcm(3.0ml),随后添加草酰氯(0.2ml,2.29mmol),然后冷却至-78℃。逐滴添加在dcm(3.0ml)中的dmso(0.4ml,5.64mmol),并将反应混合物在-78℃下继续搅拌30min。逐滴添加在dcm(6ml)中的2-(苄氧基)乙-1-醇181(293mg,1.925mmol),并将反应混合物在-78℃下继续搅拌1小时。添加三乙胺(1.3ml,9.33mmol),并将反应升温至室温过夜。将反应用饱和水性氯化铵淬灭,并用dcm萃取三次。将有机层合并,通过相分离器并真空浓缩。将粗材料通过硅胶色谱法(在庚烷中的0-100%etoac)纯化,以提供呈黄色液体的2-(苄氧基)乙醛int-182(57.0mg,0.380mmol,19.7%产率)。1h nmr(400mhz,cd2cl2)δ9.71(s,1h),3.28(s,3h),2.13(s,6h)。
[1910]
实例125:3-(5-(((r)-1-(2-(苄氧基)乙基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-183)
[1911]
[1912]
将3-(1-氧代-5-(((r)-哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮i-47(42.5mg,0.119mmol)和2-(苄氧基)乙醛int-182(57.0mg,0.380mmol)溶解于dmf(0.8ml)中。添加三乙酰氧基硼氢化钠(83.9mg,0.396mmol)并将反应在室温下搅拌过夜。将反应用50%饱和水性碳酸氢钠淬灭。将反应用4:1二氯甲烷:异丙醇萃取三次。将有机层合并,通过相分离器并真空浓缩。将粗材料通过硅胶色谱法(在dcm中的含1%tea的0-80%3:1etoac:etoh)纯化,以提供呈白色固体的3-(5-(((r)-1-(2-(苄氧基)乙基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-183(33.3mg,0.065mmol,54.7%产率)。lcms[m h]
:492.7。1h nmr(400mhz,dmso-d6)δ10.96(s,1h),7.60(d,j=8.4hz,1h),7.36-7.21(m,5h),7.14(d,j=2.2hz,1h),7.03(dd,j=8.4,2.2hz,1h),5.07(dd,j=13.3,5.1hz,1h),4.45(s,2h),4.42-4.15(m,3h),4.05-3.98(m,1h),3.60-3.46(m,2h),2.98-2.80(m,3h),2.78-2.55(m,3h),2.41-2.29(m,2h),2.04-1.93(m,1h),1.79-1.69(m,1h),1.69-1.58(m,1h),1.58-1.36(m,3h),1.36-1.22(m,1h)。
[1913]
实例127:6-吗啉代烟醛(int-185)
[1914]
将(6-吗啉代吡啶-3-基)甲醇(150mg,0.772mmol)溶解于dcm(3.9ml)中。添加mno2(1.34g,15.45mmol),并将反应混合物在室温下搅拌36小时。将反应用dcm稀释并通过celite层。将滤液真空浓缩,以提供呈浅黄色固体的6-吗啉代烟醛int-185(121.5mg,0.632mmol,82%产率)。lcms[m h]
:193.2。1h nmr(400mhz,dmso-d6)δ9.76(s,1h),8.61(d,j=2.3hz,1h),7.91(dd,j=9.1,2.4hz,1h),6.96(d,j=9.0hz,1h),3.69(s,8h)。
[1915]
实例128:3-(5-(((r)-1-((6-吗啉代吡啶-3-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-186)
[1916][1917]
根据通用方法iii,从3-(1-氧代-5-(((r)-哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮i-47(0.1g,0.280mmol)和6-吗啉代烟醛int-185(81mg,0.420mmol)开始制备化合物i-186。将反应用50%饱和水性碳酸氢钠淬灭并用4:1dcm:iproh萃取三次。将有机层合并,通过相分离器并浓缩。将粗材料通过硅胶色谱法(在庚烷中的0-100%3:1:0.01etoac:etoh:tea)纯化。将含有所希望的产物的级分浓缩并冻干,以提供呈白色固体的3-(5-(((r)-1-((6-吗啉代吡啶-3-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-186(73.6mg,0.138mmol,49.3%产率)。lcms[m h]
:534.5。1h nmr(400mhz,dmso-d6)δ10.89(s,1h),7.96(d,j=2.3hz,1h),7.55(d,j=8.4hz,1h),7.43(dd,j=8.7,2.3hz,1h),7.13(s,1h),7.00(dd,j=8.4,2.3hz,1h),6.70(d,j=8.7hz,1h),5.00
(4-(3,6-二氢-2h-吡喃-4-基)苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-188(159mg,0.300mmol,42.9%产率)。lcms[m h]
:530.1。1h nmr(400mhz,dmso-d6)δ10.89(s,1h),7.54(d,j=8.4hz,1h),7.30(d,j=8.2hz,2h),7.23(d,j=8.0hz,2h),7.10(d,j=2.4hz,1h),6.99(dd,j=8.4,2.3hz,1h),6.16-6.09(m,1h),5.00(dd,j=13.3,5.0hz,1h),4.33-4.09(m,5h),4.06(dd,j=10.3,5.4hz,1h),3.91(d,j=13.9hz,1h),3.74(t,j=5.4hz,2h),3.33(d,j=13.8hz,1h),2.84(ddd,j=17.2,13.6,5.4hz,1h),2.72-2.57(m,2h),2.57-2.48(m,1h),2.38-2.28(m,3h),2.11-2.01(m,1h),1.96-1.86(m,1h),1.75-1.68(m,1h),1.64-1.52(m,1h),1.51-1.25(m,4h)。
[1924]
实例131:叔丁基4-(5-(((2r)-2-(((2-(2,6-二氧代哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)哌啶-1-基)甲基)吡啶-2-基)哌嗪-1-甲酸酯(i-189)
[1925][1926]
根据通用方法iii,从3-(1-氧代-5-(((r)-哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮i-47(0.121g,0.339mmol)和n1-boc保护的4-(5-甲酰基吡啶-2-基)哌嗪(0.148g,0.508mmol)开始制备化合物i-189。将反应用50%饱和水性碳酸氢钠淬灭并用4:1dcm:iproh萃取三次。将有机层合并,通过相分离器并真空浓缩。将粗材料通过硅胶色谱法(在庚烷中的0-100%3:1:0.01etoac:etoh:tea)纯化,以提供呈白色固体的叔丁基4-(5-(((2r)-2-(((2-(2,6-二氧代哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)哌啶-1-基)甲基)吡啶-2-基)哌嗪-1-甲酸酯i-189(104mg,0.164mmol,48.5%产率)。lcms[m h]
:633.6。1h nmr(400mhz,dmso-d6)δ10.97(s,1h),8.03(d,j=2.4hz,1h),7.62(d,j=8.5hz,1h),7.50(dd,j=8.7,2.3hz,1h),7.21(d,j=2.2hz,1h),7.08(dd,j=8.4,2.2hz,1h),6.80(d,j=8.7hz,1h),5.08(dd,j=13.3,5.1hz,1h),4.43-4.23(m,4h),4.14(dd,j=10.3,5.3hz,1h),3.85(d,j=13.6hz,1h),2.96-2.78(m,3h),2.76-2.69(m,2h),2.63-2.56(m,1h),2.43-2.37(m,1h),2.15-2.04(m,1h),2.02-1.94(m,1h),1.82-1.73(m,2h),1.69-1.59(m,2h),1.53-1.46(m,4h),1.45-1.40(m,11h),1.38-1.32(m,2h)。
[1927]
实例132:3-(5-(((r)-1-((6-(4-乙基哌嗪-1-基)吡啶-3-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-191)
[1928][1929]
步骤1:3-(1-氧代-5-(((r)-1-((6-(哌嗪-1-基)吡啶-3-基)甲基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮(190)
[1930]
将叔丁基4-(5-(((2r)-2-(((2-(2,6-二氧代哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)哌啶-1-基)甲基)吡啶-2-基)哌嗪-1-甲酸酯i-189(0.104g,0.164mmol)悬浮于二噁烷(0.55ml),并溶解于三氟乙醇(0.55ml)中。添加在二噁烷中的4m hcl(0.25ml,0.986mmol),并将反应在室温下搅拌96小时。然后将反应浓缩,用4:1dcm:iproh稀释。将反应用50%饱和水性碳酸氢钠淬灭。将水层用4:1dcm:iproh萃取4次。将有机层合并,通过相分离器并浓缩,以提供呈奶油色固体的3-(1-氧代-5-(((r)-1-((6-(哌嗪-1-基)吡啶-3-基)甲基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮190。将物质无需纯化即可用于下一步骤。lcms[m h]
:533.5。
[1931]
步骤2:3-(5-(((r)-1-((6-(4-乙基哌嗪-1-基)吡啶-3-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-191)
[1932]
向3-(1-氧代-5-(((r)-1-((6-(哌嗪-1-基)吡啶-3-基)甲基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮190(93.6mg,0.176mmol)在dmf(1ml)中的溶液添加三乙酰氧基硼氢化钠(74mg,0.351mmol)。然后添加乙醛(0.015ml,0.264mmol)。将反应在室温下搅拌36小时。将反应用50%饱和水性碳酸氢钠淬灭并用4:1dcm:iproh萃取三次。将有机层合并,通过相分离器并浓缩到celite上。将粗材料通过硅胶色谱法(在庚烷中的含1%tea的0-100%3:1etoac:etoh)纯化,以提供呈白色固体的3-(5-(((r)-1-((6-(4-乙基哌嗪-1-基)
吡啶-3-基)甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-191(61.4mg,0.108mmol,61.7%产率)。lcms[m h]
:561.6。1h nmr(400mhz,dmso-d6)δ10.89(s,1h),7.93(d,j=2.3hz,1h),7.55(d,j=8.4hz,1h),7.40(dd,j=8.3,2.3hz,1h),7.18-7.09(m,1h),7.00(dd,j=8.3,2.3hz,1h),6.70(d,j=8.6hz,1h),5.00(dd,j=13.2,5.0hz,1h),4.36-4.14(m,3h),4.06(dd,j=10.3,5.4hz,1h),3.76(d,j=13.5hz,1h),3.40-3.30(m,4h),3.23-3.19(m,1h),2.84(ddd,j=17.2,13.6,5.5hz,1h),2.64(dt,j=9.0,4.5hz,2h),2.56-2.48(m,1h),2.38-2.25(m,7h),2.06-1.98(m,1h),1.95-1.86(m,1h),1.74-1.66(m,1h),1.61-1.52(m,1h),1.48-1.37(m,2h),1.35-1.21(m,2h),0.96(t,j=7.2hz,3h)。
[1933]
实例135:5-甲酰基-2-甲氧基苯甲腈(int-195)
[1934][1935]
步骤1:5-(羟基甲基)-2-甲氧基苯甲腈,(3-(氨基甲基)-4-甲氧基苯基)甲醇(194)
[1936]
将甲基3-氰基-4-甲氧基苯甲酸酯(0.15g,0.785mmol)溶解于thf(3.92ml)中并冷却至0℃。逐滴添加在thf中的2m libh4(1.57ml,3.14mmol),并将反应在室温下搅拌36小时。将反应冷却至0℃并用meoh(10ml)淬灭。将反应在室温下搅拌2小时。将反应浓缩,用etoac稀释并用饱和水性氯化铵洗涤。将水层用etoac萃取三次。将有机层合并,通过相分离器并浓缩,以提供呈透明浅黄色油状物的5-(羟基甲基)-2-甲氧基苯甲腈194。将物质无需纯化即可用于下一步骤。1h nmr(400mhz,cd3od)δ7.53-7.42(m,2h),7.02(d,j=8.6hz,1h),4.44(s,2h),3.82(s,3h)。
[1937]
步骤2:5-甲酰基-2-甲氧基苯甲腈(int-195)
[1938]
将5-(羟基甲基)-2-甲氧基苯甲腈194(0.137g,0.840mmol)溶解于dcm(4.2ml)中。添加mno2(1.46g,16.79mmol),并将反应混合物在室温下搅拌18小时。将反应用dcm稀释并通过celite层。将滤液浓缩,以提供呈浅奶油色固体的5-甲酰基-2-甲氧基苯甲腈int-195(101mg,0.627mmol,74.6%产率)。将物质无需纯化即可用于下一步骤。1h nmr(400mhz,cdcl3)δ9.83(s,1h),8.06-7.98(m,2h),7.06(d,j=8.5hz,1h),3.98(s,3h)。
[1939]
实例136:5-(((2r)-2-(((2-(2,6-二氧代哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)哌啶-1-基)甲基)-2-甲氧基苯甲腈(i-196)
[1940]
[1941]
根据通用方法iii,从3-(1-氧代-5-(((r)-哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮i-47(0.17g,0.476mmol)和5-甲酰基-2-甲氧基苯甲腈int-195(0.101g,0.627mmol)开始制备化合物i-196。将反应用50%饱和水性碳酸氢钠淬灭并用4:1dcm:iproh萃取三次。将有机层合并,通过相分离器并浓缩到celite上。将粗材料通过硅胶色谱法(在庚烷中的含1%tea的0-100%3:1etoac:etoh)纯化,以提供呈白色固体的5-(((2r)-2-(((2-(2,6-二氧代哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)哌啶-1-基)甲基)-2-甲氧基苯甲腈i-196(60.8mg,0.121mmol,25.4%产率)。lcms[m h]-
:503.2。1h nmr(400mhz,dmso-d6)δ10.89(s,1h),7.61-7.45(m,3h),7.12-7.02(m,2h),6.97(dt,j=8.3,2.4hz,1h),5.00(dd,j=13.3,5.0hz,1h),4.31(d,j=17.1hz,1h),4.26-4.13(m,2h),4.10-4.00(m,1h),3.85(d,j=14.0hz,1h),3.79(d,j=1.5hz,3h),3.33(d,j=13.9hz,1h),2.84(ddd,j=17.2,13.5,5.4hz,1h),2.70-2.60(m,2h),2.56-2.49(m,1h),2.38-2.24(m,1h),2.11-2.03(m,1h),1.95-1.87(m,1h),1.74-1.67(m,1h),1.64-1.54(m,1h),1.51-1.25(m,4h)。
[1942]
实例137:3-(1-氧代-5-(((r)-1-(4-(1-((四氢-2h-吡喃-4-基)甲基)哌啶-4-基)苄基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮(i-197)
[1943][1944]
向3-(1-氧代-5-(((r)-1-(4-(哌啶-4-基)苄基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮int-128(75mg,0.141mmol)在acn(1ml)中的悬浮液添加4-(溴甲基)四氢-2h-吡喃(0.028ml,0.212mmol)。添加dipea(0.074ml,0.424mmol),并将反应在60℃搅拌过夜。将反应用50%饱和水性碳酸氢钠淬灭并用4:1dcm:iproh萃取三次。将有机层合并,通过相分离器并浓缩到celite上。将粗材料通过硅胶色谱法(在庚烷中的含1%tea的0-100%3:1etoac:etoh)纯化,以提供呈白色固体的3-(1-氧代-5-(((r)-1-(4-(1-((四氢-2h-吡喃-4-基)甲基)哌啶-4-基)苄基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮i-197(22.6mg,0.033mmol,23.40%产率)。lcms[m h]-
:629.6。1h nmr(400mhz,dmso-d6)δ10.89(s,1h),7.53(d,j=8.4hz,1h),7.16(d,j=7.9hz,2h),7.13-7.05(m,3h),6.98(dd,j=8.4,2.2hz,1h),5.00(dd,j=13.3,5.1hz,1h),4.34-4.10(m,3h),4.05(dd,j=10.3,5.3hz,1h),3.88(d,j=13.7hz,1h),3.81-3.70(m,2h),3.23-3.21(m,2h),2.90-2.77(m,3h),2.71-2.62(m,2h),2.56-2.48(m,1h),2.36-2.28(m,2h),2.09-1.99(m,3h),1.96-1.81
(m,3h),1.77-1.24(m,14h),1.06(dd,j=12.7,8.5hz,2h)。
[1945]
实例138:3-(5-(((r)-1-(4-(1-(2-氟乙基)哌啶-4-基)苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-198)
[1946][1947]
向3-(1-氧代-5-(((r)-1-(4-(哌啶-4-基)苄基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮int-128(75mg,0.141mmol)在acn(1ml)中的悬浮液添加1-溴-2-氟乙烷(0.016ml,0.212mmol)。然后添加dipea(0.074ml,0.424mmol)。将反应在60℃下搅拌过夜。将反应用50%饱和水性碳酸氢钠淬灭并用4:1dcm:iproh萃取三次。将有机层合并,通过相分离器并浓缩到celite上。将粗材料通过硅胶色谱法(在庚烷中的含1%tea的0-100%3:1etoac:etoh)纯化,以提供呈白色固体的3-(5-(((r)-1-(4-(1-(2-氟乙基)哌啶-4-基)苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-198(48.9mg,0.083mmol,58.8%产率)。lcms[m h]-
:577.6。1h nmr(400mhz,dmso-d6)δ10.89(s,1h),7.54(d,j=8.4hz,1h),7.16(d,j=8.1hz,2h),7.12-7.05(m,3h),6.98(dd,j=8.7,2.3hz,1h),5.00(dd,j=13.3,5.1hz,1h),4.53(t,j=4.9hz,1h),4.41(t,j=4.9hz,1h),4.36-4.14(m,3h),4.05(dd,j=10.3,5.3hz,1h),3.89(d,j=13.8hz,1h),2.95-2.78(m,3h),2.72-2.57(m,3h),2.56-2.48(m,2h),2.38-2.27(m,2h),2.10-1.97(m,3h),1.95-1.86(m,1h),1.76-1.23(m,11h)。
[1948]
实例139:苯并[d]噁唑-5-甲醛(int-200)
[1949][1950]
步骤1:苯并[d]噁唑-5-基甲醇(199)
[1951]
将苯并[d]噁唑-5-甲酸(0.1g,0.613mmol)溶解于thf(2.04ml)中并冷却至0℃。逐滴添加在thf中的1m硼烷四氢呋喃复合物(1.84ml,1.84mmol)。将反应在室温下搅拌36小时。将反应冷却至0℃并用甲醇(1.5ml)淬灭并在室温下搅拌2小时。将反应浓缩至干燥,然
后重新溶解于甲醇(5ml)中。将反应在室温下搅拌96小时。将反应浓缩,以提供呈棕色油状物的苯并[d]噁唑-5-基甲醇199。将物质(假定定量产率)无需纯化即可用于下一步骤。lcms[m h]
:150.1。
[1952]
步骤2:苯并[d]噁唑-5-甲醛(int-200)
[1953]
将苯并[d]噁唑-5-基甲醇199(91mg,0.613mmol)溶解于dcm(3.9ml)中。添加mno2(1.07g,12.3mmol),并将反应混合物在室温下搅拌36小时。将反应用dcm稀释并通过celite层。将滤液浓缩,以提供呈红棕色固体的苯并[d]噁唑-5-甲醛int-200(46.5mg,0.316mmol,51.6%产率)。lcms[m h]
:148.1。1h nmr(400mhz,cdcl3)δ10.05(s,1h),8.26(d,j=1.6hz,1h),8.15(s,1h),7.94(dd,j=8.4,1.6hz,1h),7.67(d,j=8.5hz,1h)。
[1954]
实例140:3-(5-(((r)-1-(苯并[d]噁唑-5-基甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-201)
[1955][1956]
根据通用方法iii,从3-(1-氧代-5-(((r)-哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮i-47(0.08g,0.224mmol)和苯并[d]噁唑-5-甲醛int-200(46.5mg,0.316mmol)开始制备化合物i-201。将反应用50%饱和水性碳酸氢钠淬灭并用4:1dcm:iproh萃取三次。将有机层合并,通过相分离器并真空浓缩。将粗材料通过硅胶色谱法(在庚烷中的0-100%3:1:0.01etoac:etoh:tea)纯化。将产物进一步通过反相hplc(在含有5mm nh4oh作为改性剂的h2o中的25%-50%acn)纯化。在样品收集前,级分中含有3滴甲酸。将含有纯的产物的级分合并并冻干,以提供呈浅米色固体的3-(5-(((r)-1-(苯并[d]噁唑-5-基甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-201的甲酸盐(3.17mg,5.63μmol,2.52%产率)。lcms[m h]
:489.4。1h nmr(400mhz,dmso-d6)δ10.89(s,1h),8.61(d,j=1.4hz,1h),8.20(s,1h),7.66(d,j=1.5hz,1h),7.60(d,j=8.3hz,1h),7.53(d,j=8.4hz,1h),7.35(dd,j=8.5,1.5hz,1h),7.11(t,j=2.7hz,1h),7.05-6.96(m,1h),5.00(dd,j=13.3,5.1hz,1h),4.35-4.24(m,2h),4.24-3.98(m,3h),3.47(d,j=13.7hz,1h),2.89-2.79(m,1h),2.76-2.69(m,1h),2.69-2.63(m,1h),2.56-2.49(m,1h),2.37-2.27(m,1h),2.15-2.06(m,1h),1.95-1.89(m,1h),1.79-1.70(m,1h),1.64-1.56(m,1h),1.51-1.27(m,4h)。
[1957]
实例142:3-(5-(((r)-1-(4-(1-(氧杂环丁烷-3-基甲基)哌啶-4-基)苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-203)
[1958][1959]
根据通用方法iii,从3-(1-氧代-5-(((r)-1-(4-(哌啶-4-基)苄基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮int-128(0.078g,0.147mmol)和氧杂环丁烷-3-甲醛(0.015ml,0.220mmol)开始制备化合物i-203。将反应用50%饱和水性碳酸氢钠淬灭并用4:1dcm:iproh萃取三次。将有机层合并,通过相分离器并浓缩到celite上。将粗材料通过硅胶色谱法(在庚烷中的含1%tea的0-100%3:1etoac:etoh)纯化,以提供呈白色固体的3-(5-(((r)-1-(4-(1-(氧杂环丁烷-3-基甲基)哌啶-4-基)苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-203(40.2mg,0.066mmol,45.1%产率)。lcms[m h]-
:601.3。1h nmr(400mhz,dmso-d6)δ10.97(s,1h),7.61(d,j=8.4hz,1h),7.23(d,j=7.8hz,2h),7.21-7.10(m,3h),7.06(dd,j=8.4,2.2hz,1h),5.08(dd,j=13.4,5.1hz,1h),4.65(dd,j=7.8,5.8hz,2h),4.42-4.21(m,5h),4.12(dd,j=10.2,5.3hz,1h),3.96(d,j=13.8hz,1h),3.24-3.14(m,1h),2.96-2.80(m,3h),2.78-2.70(m,2h),2.66-2.56(m,3h),2.45-2.36(m,2h),2.16-2.06(m,1h),2.03-1.93(m,3h),1.84-1.74(m,1h),1.72-1.30(m,10h)。
[1960]
实例143:四氢呋喃-3-甲醛(int-205)
[1961][1962]
步骤1:(四氢呋喃-3-基)甲醇(204)
[1963]
将四氢呋喃-3-甲酸(304mg,2.62mmol)溶解于thf(4ml)中并冷却至0℃。添加在thf中的1m硼烷四氢呋喃复合物(7.9ml,7.90mmol),并将反应升温至室温过夜。然后将反应冷却至0℃并用甲醇(5ml)淬灭。将反应浓缩至干燥,在meoh(8.00ml)中重构并在室温下搅拌过夜。将反应浓缩,并通过硅胶色谱法(在二氯甲烷中的0-80%3:1:0.01etoac:etoh:tea)纯化,以提供呈透明液体的(四氢呋喃-3-基)甲醇204(162.2mg,1.59mmol,60.6%产率)。1h nmr(400mhz,cdcl3)δ3.91-3.80(m,2h),3.74(ddd,j=8.5,7.6,6.9hz,1h),3.68-3.54(m,3h),2.55-2.37(m,1h),2.10-1.96(m,1h),1.64(dddd,j=12.5,8.0,7.0,5.6hz,1h)。
[1964]
步骤2:四氢呋喃-3-甲醛(int-205)
[1965]
在40ml小瓶中,添加dcm(2.0ml),随后添加草酰氯(0.18ml,2.056mmol),然后冷却
至-78℃。逐滴添加在dcm(2.0ml)中的dmso(0.35ml,4.93mmol),并将反应混合物在-78℃下继续搅拌30min。逐滴添加在dcm(3ml)中的(四氢呋喃-3-基)甲醇204(162.2mg,1.59mmol),并将反应混合物在-78℃下继续搅拌1小时。添加三乙胺(1.1ml,7.89mmol),并将反应升温至室温过夜。将反应用饱和水性氯化铵淬灭,并用dcm萃取三次。将有机层合并,通过相分离器并浓缩,以提供含有白色沉淀物的呈黄色液体的四氢呋喃-3-甲醛int-205。将物质无需纯化即可用于下一步骤。
[1966]
实例144:非对映异构体5-(((2r)-1-((四氢呋喃-3-基)甲基)哌啶-2-基)甲氧基)异苯并呋喃-1(3h)-酮(int-209)
[1967][1968]
步骤1:苄基(r)-2-(羟基甲基)哌啶-1-甲酸酯(206)
[1969]
在0℃-5℃下,向(r)-1-((苄氧基)羰基)哌啶-2-甲酸(5g,19mmol)在thf(76ml)中的溶液逐滴添加在在thf中的1m硼烷-四氢呋喃复合物(3.1g,36.1mmol),保持内部温度低于5℃。将反应升温至室温并在室温下搅拌过夜。将冰缓慢添加至反应,并允许反应达到至室温。将反应用etoac萃取两次。将有机层合并,用盐水洗涤,经无水na2so4干燥,过滤并真空浓缩。将粗材料通过硅胶色谱法(在庚烷中的0-100%etoac)纯化,以提供呈油状物的苄基(r)-2-(羟基甲基)哌啶-1-甲酸酯206(4.15g,16.7mmol,88%产率)。lcms[m h]-
:250.2。
[1970]
步骤2:苄基(r)-2-(((1-氧代-1,3-二氢异苯并呋喃-5-基)氧基)甲基)哌啶-1-甲酸酯(207)
[1971]
将csf(1.23g,8.06mmol)、bppyphos(68mg,0.134mmol)、pd2dba3(62mg,0.067mmol)和5-溴异苯并呋喃-1(3h)-酮(687mg,3.22mmol)悬浮于甲苯(13.4ml),并用氮气吹扫。将反应混合物在90℃下搅拌直到看见颜色变化。添加苄基(r)-2-(羟基甲基)哌啶-1-甲酸酯206(670mg,2.69mmol),并将反应在90℃下搅拌过夜。将反应混合物冷却至室温,并通过celite垫过滤。将混合物用饱和水性nahco3、盐水洗涤,经na2so4干燥,过滤并真空浓缩。将粗材料
通过硅胶色谱法(在庚烷中的10%-60%etoac)纯化,以提供苄基(r)-2-(((1-氧代-1,3-二氢异苯并呋喃-5-基)氧基)甲基)哌啶-1-甲酸酯207(880mg,2.31mmol,86%产率)。lcms[m h]-
:382.4。
[1972]
步骤3:(r)-5-(哌啶-2-基甲氧基)异苯并呋喃-1(3h)-酮(208)
[1973]
将苄基(r)-2-(((1-氧代-1,3-二氢异苯并呋喃-5-基)氧基)甲基)哌啶-1-甲酸酯207(0.880g,2.307mmol)溶解于etoh(23.1ml)中。将反应用氮气吹扫5分钟。然后添加10%湿的pd碳(0.246g,0.231mmol)。将反应用氢气气球吹扫10分钟。将反应在室温下用氢气气球在顶部搅拌24小时。将反应用氮气吹扫5分钟,然后通过用dcm冲洗的celite塞。将滤液浓缩,以提供呈奶油色固体的(r)-5-(哌啶-2-基甲氧基)异苯并呋喃-1(3h)-酮208(556.7mg,2.251mmol,98%产率)。将物质无需纯化即可用于下一步骤。lcms[m h]
:248.3。
[1974]
步骤4:非对映异构体5-(((2r)-1-((四氢呋喃-3-基)甲基)哌啶-2-基)甲氧基)异苯并呋喃-1(3h)-酮(int-209)
[1975]
将(r)-5-(哌啶-2-基甲氧基)异苯并呋喃-1(3h)-酮208(112.6mg,0.455mmol)和四氢呋喃-3-甲醛int-205(325.8mg,1.627mmol)溶解于dmf(1.5ml)中。添加三乙酰氧基硼氢化钠(280mg,1.321mmol)并将反应在室温下搅拌48小时。将反应用50%饱和碳酸氢钠水溶液淬灭并用4:1dcm:iproh萃取三次。将有机层合并,通过相分离器并浓缩到celite上。将粗材料通过硅胶色谱法(在庚烷中的含1%tea的0-80%3:1etoac:etoh)纯化,以提供呈黄色液体的非对映异构体5-(((2r)-1-((四氢呋喃-3-基)甲基)哌啶-2-基)甲氧基)异苯并呋喃-1(3h)-酮int-209的混合物(187.1mg,0.565mmol)。lcms[m h]
:332.2。将非对映异构体的混合物通过手性sfc[柱chiralcel oj-h 21x250mm 5um,含10mm nh3的co2助溶剂10%-30%meoh;以80g/min在125巴下]分离,以提供非对映异构体:峰1:5-(((2r)-1-((四氢呋喃-3-基)甲基)哌啶-2-基)甲氧基)异苯并呋喃-1(3h)-酮的非对映异构体1(30.5mg,0.092mmol)。手性sfc rt 1.35min。1h nmr(400mhz,cd2cl2)δ7.86-7.71(m,1h),7.16-6.89(m,2h),5.27-5.19(m,2h),4.24-4.09(m,1h),4.07-3.92(m,1h),3.87-3.61(m,3h),3.61-3.09(m,2h),3.00-2.81(m,1h),2.79-2.59(m,2h),2.52-2.15(m,3h),2.10-1.82(m,2h),1.81-1.34(m,5h)。峰2:5-(((2r)-1-((四氢呋喃-3-基)甲基)哌啶-2-基)甲氧基)异苯并呋喃-1(3h)-酮的非对映异构体2(28.6mg,0.086mmol)。手性sfc rt 1.43min。1h nmr(400mhz,cd2cl2)δ7.77(d,j=8.5hz,1h),7.13-6.87(m,2h),5.23(s,2h),4.22-4.09(m,1h),4.09-3.96(m,1h),3.83-3.61(m,3h),3.49-3.36(m,1h),2.95-2.83(m,1h),2.83-2.63(m,2h),2.49-2.22(m,3h),2.02-1.87(m,1h),1.84-1.72(m,1h),1.71-1.52(m,5h),1.47-1.34(m,1h)。
[1976]
实例145:非对映异构体3-(1-氧代-5-(((2r)-1-((四氢呋喃-3-基)甲基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮(i-211)
[1977][1978]
步骤1:单一非对映异构体乙基2-(氯甲基)-4-(((2r)-1-((四氢呋喃-3-基)甲基)哌啶-2-基)甲氧基)苯甲酸酯(210)
[1979]
根据通用方法iv,从5-(((2r)-1-((四氢呋喃-3-基)甲基)哌啶-2-基)甲氧基)异苯并呋喃-1(3h)-酮int-209峰1(30.5mg,0.092mmol)开始制备化合物210。将反应冷却至室温,用水稀释,并用饱和碳酸氢钠淬灭。将反应用乙酸乙酯萃取3次。将有机层合并,通过相分离器并浓缩,以提供呈棕色油状物的单一非对映异构体乙基2-(氯甲基)-4-(((2r)-1-((四氢呋喃-3-基)甲基)哌啶-2-基)甲氧基)苯甲酸酯(36.4mg,0.092mmol,100%产率)210。将物质(假定定量产率)无需纯化即可用于下一步骤。lcms[m h]
:396.3。
[1980]
步骤2:非对映异构体3-(1-氧代-5-(((2r)-1-((四氢呋喃-3-基)甲基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮(i-211)
[1981]
根据通用方法v,从单一非对映异构体乙基2-(氯甲基)-4-(((2r)-1-((四氢呋喃-3-基)甲基)哌啶-2-基)甲氧基)苯甲酸酯210(36.4mg,0.092mmol)开始制备化合物i-211。将反应浓缩,并通过硅胶色谱法(在庚烷中的含1%tea的0-100%3:1etoac:etoh)纯化,以提供呈奶油色固体的非对映异构体3-(1-氧代-5-(((2r)-1-((四氢呋喃-3-基)甲基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮i-211(18.2mg,0.039mmol,42.6%产率)。lcms[m h]
:442.3。1h nmr(400mhz,dmso-d6)δ10.89(s,1h),7.55(d,j=8.3hz,1h),7.12(d,j=2.2hz,1h),6.98(dd,j=8.4,2.1hz,1h),5.00(dd,j=13.3,5.2hz,1h),4.32(d,j=17.2hz,1h),4.19(d,j=17.2hz,1h),4.14-4.04(m,1h),4.02-3.92(m,1h),3.66-3.53(m,2h),3.49(q,j=7.6hz,1h),3.31(dd,j=8.3,5.8hz,1h),2.85-2.78(m,1h),2.61-2.49(m,3h),2.36-2.25(m,3h),2.14-2.05(m,1h),1.95-1.79(m,3h),1.68-1.53(m,2h),1.49-1.23(m,5h)。
[1982]
实例146:非对映异构体3-(1-氧代-5-(((2r)-1-((四氢呋喃-3-基)甲基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮(i-213)
[1983][1984]
步骤1:单一非对映异构体乙基2-(氯甲基)-4-(((2r)-1-((四氢呋喃-3-基)甲基)哌啶-2-基)甲氧基)苯甲酸酯(212)
[1985]
根据通用方法iv,从5-(((2r)-1-((四氢呋喃-3-基)甲基)哌啶-2-基)甲氧基)异苯并呋喃-1(3h)-酮int-209峰2(28.6mg,0.086mmol)开始制备化合物212。将反应冷却至室温,用水稀释,并用饱和碳酸氢钠淬灭。将反应用乙酸乙酯萃取3次。将有机层合并,通过相分离器并浓缩,以提供呈棕色油状物的单一非对映异构体乙基2-(氯甲基)-4-(((2r)-1-((四氢呋喃-3-基)甲基)哌啶-2-基)甲氧基)苯甲酸酯212(34mg,0.086mmol,100%产率)。将物质(假定定量产率)无需纯化即可用于下一步骤。lcms[m h]
:396.5。
[1986]
步骤2:非对映异构体3-(1-氧代-5-(((2r)-1-((四氢呋喃-3-基)甲基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮(i-213)
[1987]
根据通用方法v,从单一非对映异构体乙基2-(氯甲基)-4-(((2r)-1-((四氢呋喃-3-基)甲基)哌啶-2-基)甲氧基)苯甲酸酯212(34.0mg,0.086mmol)开始制备化合物i-213。将反应浓缩,并通过硅胶色谱法(在庚烷中的含1%tea的0-100%3:1etoac:etoh)纯化,以提供呈奶油色固体的非对映异构体3-(1-氧代-5-(((2r)-1-((四氢呋喃-3-基)甲基)哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮i-213(17.6mg,0.038mmol,44.0%产率)。lcms[m h]
:442.4。1h nmr(400mhz,dmso-d6)δ10.97(s,1h),7.63(d,j=8.4hz,1h),7.20(d,j=2.2hz,1h),7.06(dd,j=8.8,2.0hz,1h),5.08(dd,j=13.3,5.2hz,1h),4.40(d,j=17.1hz,1h),4.27(d,j=17.1hz,1h),4.21-4.12(m,1h),4.12-4.02(m,1h),3.75-3.52(m,3h),2.98-2.82(m,2h),2.77-2.65(m,2h),2.65-2.55(m,1h),2.43-2.36(m,2h),2.31-2.21(m,2h),2.02-1.83(m,3h),1.76-1.45(m,6h),1.40-1.31(m,1h)。
[1988]
实例147:3-(5-(((r)-1-(环丙基甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-214)
[1989][1990]
向3-(1-氧代-5-(((r)-哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮i-47(100mg,0.280mmol)在etoh(1.5ml)中的溶液添加三乙酰氧基硼氢化钠(119mg,0.560mmol),然后添加环丙烷甲醛(29mg,0.420mmol)。将反应在室温下搅拌,并在1小时后,添加另外的环丙烷甲醛(14mg,0.167mmol),并将反应在室温下搅拌过夜。添加另外的etoh(1ml),随后添加三乙酰氧基硼氢化钠(80mg,0.377mmol)和环丙烷甲醛(14mg,0.167mmol)。将反应在室温下再搅拌1小时。将反应浓缩到isolute上,并通过硅胶色谱法(在dcm中的含1%tea的0-100%3:1etoac:etoh)纯化。将产物浓缩,用1:1水:乙腈稀释,并冻干,以提供3-(5-(((r)-1-(环丙基甲基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-214(67mg,0.155mmol,55.3%产率)。lcms[m h]
=412.7。1h nmr(400mhz,dmso-d6)δ10.96(s,1h),7.61(d,j=8.4hz,1h),7.19(d,j=2.2hz,1h),7.05(dd,j=8.4,2.3hz,1h),5.07(dd,j=13.3,5.0hz,1h),4.44-4.21(m,2h),4.17(ddd,j=10.3,4.8,2.2hz,1h),4.02(dd,j=10.2,5.3hz,1h),3.05-2.83(m,2h),2.75-2.64(m,1h),2.64-2.52(m,2h),2.43-2.25(m,3h),2.05-1.91(m,1h),1.82-1.70(m,1h),1.65(dt,j=8.8,4.3hz,1h),1.55(dt,j=8.3,4.1hz,1h),1.50-1.37(m,2h),1.37-1.25(m,1h),0.91-0.77(m,1h),0.43(dt,j=7.7,3.5hz,2h),0.05(q,j=4.0hz,2h)。
[1991]
实例148:5-(1-(1-(((1r,4r)-4-甲氧基环己基)甲基)哌啶-2-基)乙氧基)异苯并呋喃-1(3h)-酮(int-215)
[1992][1993]
根据通用方法iii,从5-(1-(哌啶-2-基)乙氧基)异苯并呋喃-1(3h)-酮2(0.62g,1.19mmol)和(1r,4r)-4-甲氧基环己烷-1-甲醛(0.227g,1.596mmol)开始制备化合物int-215。将粗材料通过硅胶色谱法(在庚烷中的0-100%乙酸乙酯)纯化,以提供来自主峰int-215的呈橙色油状物的非对映异构体5-(1-(1-((4-甲氧基环己基)甲基)哌啶-2-基)乙氧基)异苯并呋喃-1(3h)-酮的混合物(227mg,0.586mmol,49.4%产率)和来自次要峰的呈橙色油状物的非对映异构体5-(1-(1-((4-甲氧基环己基)甲基)哌啶-2-基)乙氧基)异苯并呋喃-1(3h)-酮的混合物(32.5mg,0.084mmol,7.07%产率)。lcms[m h]
:388.6。
[1994]
首先,将来自主峰的非对映异构体的混合物通过手性sfc[柱chiralpak ib 5um 21x250mm,含10mm nh3的co2助溶剂15%meoh;以80g/min在125巴下]分离,以提供两个峰。将
峰1进一步通过手性sfc[柱chiralpak ia 21x250mm,含10mm nh3的co2助溶剂10%1:1meoh:ipa;以80g/min在125巴下]分离,以提供非对映异构体:级分10:5-(1-(1-((4-甲氧基环己基)甲基)哌啶-2-基)乙氧基)异苯并呋喃-1(3h)-酮的非对映异构体1(32.5mg,0.084mmol)。手性sfc rt 1.72min。级分12:5-(1-(1-((4-甲氧基环己基)甲基)哌啶-2-基)乙氧基)异苯并呋喃-1(3h)-酮的非对映异构体2(29.6mg,0.076mmol)。手性sfc rt 1.79min。将峰2进一步通过手性sfc[柱chiralpak ig 21x250mm,含10mm nh4oh的co2助溶剂15%1meoh;以80g/min在125巴下]分离,以提供非对映异构体:级分5:5-(1-(1-((4-甲氧基环己基)甲基)哌啶-2-基)乙氧基)异苯并呋喃-1(3h)-酮的非对映异构体3(11.1mg,0.029mmol)。手性sfc rt 2.44min。级分7:5-(1-(1-((4-甲氧基环己基)甲基)哌啶-2-基)乙氧基)异苯并呋喃-1(3h)-酮的非对映异构体4(11.3mg,0.029mmol)。手性sfc rt 2.55min。
[1995]
实例149:非对映异构体3-(5-(1-(1-((4-甲氧基环己基)甲基)哌啶-2-基)乙氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-217)
[1996][1997]
步骤1:单一非对映异构体乙基2-(氯甲基)-4-(1-(1-((4-甲氧基环己基)甲基)哌啶-2-基)乙氧基)苯甲酸酯(216)
[1998]
根据通用方法iv,从5-(1-(1-(((1r,4r)-4-甲氧基环己基)甲基)哌啶-2-基)乙氧基)异苯并呋喃-1(3h)-酮int-215级分10(32.5g,0.084mmol)开始制备化合物216。将反应冷却至室温,用水稀释,并用饱和碳酸氢钠淬灭。将反应用乙酸乙酯萃取3次。将有机层合并,通过相分离器并浓缩,以提供呈棕色油状物的单一非对映异构体乙基2-(氯甲基)-4-(1-(1-((4-甲氧基环己基)甲基)哌啶-2-基)乙氧基)216(38mg,0.084mmol)。将物质(假定定量产率)无需纯化即可用于下个步骤。lcms[m h]
:452.2。
[1999]
步骤2:非对映异构体3-(5-(1-(1-((4-甲氧基环己基)甲基)哌啶-2-基)乙氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-217)
[2000]
根据通用方法v,从乙基2-(氯甲基)-4-(1-(1-((4-甲氧基环己基)甲基)哌啶-2-基)乙氧基)苯甲酸酯216(38.0mg,0.084mmol)开始制备化合物i-217。将反应浓缩,并通过硅胶色谱法(在庚烷中的含有1%三乙胺的0-100%3:1乙酸乙酯:乙醇)纯化,以提供不纯产物。将材料进一步通过碱性物质触发的反相hplc(在含有5mm nh4oh作为改性剂的水中的35%-60%acn)纯化。在样品收集前,测试管中含有3滴甲酸。将含有纯的产物的级分合并并冻干,以提供呈白色固体的非对映异构体3-(5-(1-(1-((4-甲氧基环己基)甲基)哌啶-2-基)乙氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-217的甲酸盐(8.07mg,0.015mmol,17.38%产率)。lcms[m h]
:498.2。1h nmr(400mhz,dmso-d6)δ10.89(s,1h),8.18(s,1h),7.54(d,j=8.4hz,1h),7.12(d,j=2.3hz,1h),6.96(dd,j=8.5,2.1hz,1h),5.00(dd,j=13.3,5.0hz,1h),4.70(p,j=6.0hz,1h),4.31(dd,j=17.1,4.9hz,1h),4.19(dd,j=17.3,3.3hz,1h),2.99-2.75(m,3h),2.61-2.48(m,3h),2.37-2.24(m,4h),2.14-1.98(m,2h),1.94-1.81(m,3h),1.79-1.52(m,4h),1.46-1.37(m,2h),1.32-1.17(m,6h),1.01-0.86(m,2h),0.85-0.63(m,2h)。
[2001]
实例150:非对映异构体3-(5-(1-(1-((4-甲氧基环己基)甲基)哌啶-2-基)乙氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-219)
[2002][2003]
按照与实例149相同的方式从int-215级分12开始制备化合物i-219。将步骤2的反应浓缩,并通过硅胶色谱法(在庚烷中的含有1%三乙胺作为改性剂的0-100%3:1乙酸乙酯:乙醇)纯化。将含有所希望的产物的级分合并,浓缩并冻干,以提供呈灰色固体的3-(5-(1-(1-((4-甲氧基环己基)甲基)哌啶-2-基)乙氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-219(15.8mg,0.030mmol,39.7%产率)。lcms[m h]
:498.2。1h nmr(400mhz,dmso-d6)δ10.89(s,1h),7.54(d,j=8.3hz,1h),7.12(d,j=2.3hz,1h),6.96(dd,j=8.4,2.2hz,1h),5.00(dd,j=13.3,5.1hz,1h),4.70(p,j=6.1hz,1h),4.31(dd,j=17.1,4.9hz,1h),4.19(dd,j=17.4,3.4hz,1h),2.99-2.78(m,3h),2.71-2.48(m,4h),2.39-2.27(m,3h),2.14-1.97(m,2h),1.96-1.81(m,3h),1.78-1.53(m,4h),1.46-1.36(m,2h),1.32-1.17(m,6h),
1.01-0.87(m,2h),0.83-0.64(m,2h)。
[2004]
实例151:3-(5-(((1r,3s,4s)-2-乙基-2-氮杂双环[2.2.1]庚烷-3-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-223)
[2005][2006]
步骤1:叔丁基(1r,3s,4s)-3-(羟基甲基)-2-氮杂双环[2.2.1]庚烷-2-甲酸酯(220)
[2007]
将(1r,3s,4s)-2-(叔丁氧基羰基)-2-氮杂双环[2.2.1]庚烷-3-甲酸(0.113g,0.468mmol)溶解于thf(1.56ml)中并冷却至0℃。逐滴添加在thf中给的2m氢化铝锂(0.35ml,0.702mmol),并将反应在室温下搅拌2小时。将反应用饱和罗谢尔盐淬灭并在室温下搅拌1小时。将反应用dcm萃取3次并用etoac萃取2次。将有机层合并并浓缩,以提供呈澄清油状物的叔丁基(1r,3s,4s)-3-(羟基甲基)-2-氮杂双环[2.2.1]庚烷-2-甲酸酯220(98mg,0.431mmol,92%产率)。
[2008]
步骤2:叔丁基(1r,3s,4s)-3-(((2-(2,6-二氧代-1-((2-(三甲基甲硅烷基)乙氧基)甲基)哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)-2-氮杂双环[2.2.1]庚烷-2-甲酸酯(221)
[2009]
根据通用方法vi,从3-(5-溴-1-氧代异吲哚啉-2-基)-1-((2-(三甲基甲硅烷基)乙氧基)甲基)哌啶-2,6-二酮(0.12g,0.265mmol)和叔丁基(1r,3s,4s)-3-(羟基甲基)-2-氮杂双环[2.2.1]庚烷-2-甲酸酯220(98mg,0.431mmol)开始制备化合物221。将反应浓缩,并通过硅胶色谱法(在庚烷中的0-100%etoac)纯化,以提供呈黄色油状物的叔丁基(1r,3s,4s)-3-(((2-(2,6-二氧代-1-((2-(三甲基甲硅烷基)乙氧基)甲基)哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)-2-氮杂双环[2.2.1]庚烷-2-甲酸酯221(134mg,0.223mmol,84%产率)。lcms[m h-156.3(tmsch2ch2,叔丁基)]
:444.4。
[2010]
步骤3:3-(5-(((1r,3s,4s)-2-氮杂双环[2.2.1]庚烷-3-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(222)
[2011]
根据通用方法vii,从叔丁基(1r,3s,4s)-3-(((2-(2,6-二氧代-1-((2-(三甲基甲硅烷基)乙氧基)甲基)哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)-2-氮杂双环[2.2.1]庚烷-2-甲酸酯221(134mg,0.223mmol)开始制备化合物222。将反应用50%饱和水性碳酸氢钠淬灭并用4:1dcm:iproh萃取四次。将有机层合并,通过相分离器并浓缩,以提供呈黄色固体的3-(5-(((1r,3s,4s)-2-氮杂双环[2.2.1]庚烷-3-基)甲氧基)-1-氧代异吲哚
啉-2-基)哌啶-2,6-二酮222(105mg,0.284mmol,127%产率)。lcms[m h]
:370.4。
[2012]
步骤4:3-(5-(((1r,3s,4s)-2-乙基-2-氮杂双环[2.2.1]庚烷-3-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-223)
[2013]
根据通用方法iii,从3-(5-(((1r,3s,4s)-2-氮杂双环[2.2.1]庚烷-3-基)甲氧基)-1-氧代异吲哚啉-2-基)-1-(羟基甲基)哌啶-2,6-二酮222(105mg,0.284mmol)和乙醛(0.08ml,1.42mmol)开始制备化合物i-223。将反应用在水中的50%饱和水性碳酸氢钠淬灭,并用4:1二氯甲烷:异丙醇萃取4次。将有机层合并,通过相分离器并浓缩。将粗材料通过硅胶色谱法(在庚烷中含1%tea的0-100%3:1乙酸乙酯:乙醇)纯化。将级分合并,浓缩并高真空过夜,以提供稍微不纯的产物。将材料进一步通过碱性反相hplc(在含有5mm nh4oh作为改性剂的水中的25%-50%acn)纯化。在样品收集前,测试管中含有3滴甲酸。将级分合并并冻干,以提供呈白色固体的3-(5-(((1r,3s,4s)-2-乙基-2-氮杂双环[2.2.1]庚烷-3-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-223的甲酸盐(4.95mg,10.60μmol,3.73%产率)。lcms[m h]
:398.3。1h nmr(400mhz,dmso-d6)δ10.89(s,1h),8.18(s,1h),7.53(d,j=8.4hz,1h),7.09(d,j=2.2hz,1h),6.97(dd,j=8.6,2.2hz,1h),5.00(dd,j=13.3,5.1hz,1h),4.31(d,j=17.3hz,1h),4.18(d,j=17.1hz,1h),3.77-3.69(m,1h),3.69-3.61(m,1h),2.84(ddd,j=17.1,13.5,5.4hz,1h),2.64-2.47(m,2h),2.39-2.25(m,2h),2.22-2.15(m,2h),1.95-1.85(m,1h),1.81-1.70(m,1h),1.60(d,j=9.6hz,1h),1.57-1.46(m,1h),1.26-1.10(m,4h),0.92(t,j=7.2hz,3h)。
[2014]
实例152:1-(4-(氯甲基)苯基)-4-异丙基哌嗪(int-226)
[2015][2016]
步骤1:4-(4-异丙基哌嗪-1-基)苯甲醛(224):
[2017]
向4-氟苯甲醛(1.00g,8.06mmol)在dmf(10ml)中的溶液添加1-异丙基哌嗪(1.24g,9.67mmol)、k2co3(1.67g,12.09mmol)。将反应混合物在130℃下搅拌16小时。将反应用h2o(40ml)淬灭并用乙酸乙酯萃取三次。将有机层合并,用饱和水性氯化钠洗涤,经na2so4干燥,过滤,并真空浓缩,以提供呈黄色固体的4-(4-异丙基哌嗪-1-基)苯甲醛224。将物质无需纯化即可用于下个步骤。1h nmr(400mhz,dmso-d6)δ=9.71(s,1h),7.76-7.60(m,2h),7.02(d,j=8.8hz,2h),3.37-3.34(m,4h),2.70-2.63(m,1h),2.57-2.51(m,4h),0.99(d,j=6.4hz,6h)。
[2018]
步骤2:(4-(4-异丙基哌嗪-1-基)苯基)甲醇(225):
[2019]
在0℃在n2气氛下,向4-(4-异丙基哌嗪-1-基)苯甲醛224(500mg,2.15mmol)在meoh(5ml)中的溶液缓慢添加nabh4(122.1mg,3.23mmol)。将反应放置于室温下并搅拌2小时。将反应过滤以除去不溶物质并真空浓缩,以提供呈白色固体的(4-(4-异丙基哌嗪-1-基)苯基)甲醇225(0.5g,2.13mmol,99%产率)。将粗产物直接用于下一步骤。lcms[m h]
:235.2。
[2020]
步骤3:1-(4-(氯甲基)苯基)-4-异丙基哌嗪(int-226):
[2021]
在25℃下,向(4-(4-异丙基哌嗪-1-基)苯基)甲醇225(500mg,2.13mmol)在dcm(5ml)中的溶液添加socl2(0.76ml,10.67mmol)。将反应在40℃下搅拌2小时。将反应在减压下浓缩,以提供呈黄色固体的1-(4-(氯甲基)苯基)-4-异丙基哌嗪int-226(0.5g,1.98mmol,93%产率)。将粗产物直接用于下一步骤。
[2022]
实例153:3-(5-(((r)-1-(4-(4-异丙基哌嗪-1-基)苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-227)
[2023][2024]
在25℃下,向3-(1-氧代-5-(((r)-哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮i-47(200mg,0.7mmol)和1-(4-(氯甲基)苯基)-4-异丙基哌嗪int-226(283mg,1.12mmol)在ch3cn(2ml)中的溶液添加nahco3(199mg,2.3mmol)。将反应在60℃下搅拌12小时。将反应过滤以除去不溶物质。将滤液真空浓缩。将粗材料通过反相hplc(柱:waters xbridge 150*25mm*5um;流动相:a表示h2o(10mm nh4hco3)以及b表示乙腈;梯度:在10min内呈线性地b 35%-65%;流速:25ml/min;柱温:室温,波长:220nm/254nm)纯化,以提供3-(5-(((r)-1-(4-(4-异丙基哌嗪-1-基)苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-227的甲酸盐(42.31mg,0.08mmol,27%产率,100%纯度)。lcms[m h]
:574.2。1h nmr(400mhz,dmso-d6)δ=10.97(s,1h),8.20(s,1h),7.62(d,j=8.4hz,1h),7.22-7.11(m,3h),7.10-7.05(m,1h),6.86(m,2h),5.08(m,1h),4.35-4.27(m,2h),4.13(m,2h),3.89(m,2h),3.32(m,2h),3.09(m,4h),2.77-2.69(m,4h),2.61(m,2h),2.43-2.32(m,2h),2.15-2.08(m,1h),2.03-1.95(m,1h),1.82-1.75(m,1h),1.65(m,1h),1.56-1.46(m,2h),1.42-1.31(m,2h),1.02(d,j=6.4hz,6h)。
[2025]
实例154:4-(4-(叔丁基)哌嗪-1-基)苯甲醛(int-228)。
[2026]
向4-氟苯甲醛(1.00g,8.06mmol)在dmf(10ml)中的溶液添加1-(叔丁基)哌嗪(1.65g,12.0mmol)、k2co3(1.67g,12.09mmol)。将反应混合物在130℃下搅拌16小时。将反应用h2o(40ml)淬灭并用乙酸乙酯萃取三次。将有机层合并,用饱和水性氯化钠洗涤,经na2so4干燥,过滤,并真空浓缩,以提供呈黄色固体的4-(4-(叔丁基)哌嗪-1-基)苯甲醛int-228(1.5g,6.09mmol,76.1%产率)。将物质无需纯化即可用于下个步骤。1hnmr(400mhz,dmso-d6)δ=9.70(s,1h),7.70(d,j=8.8hz,2h),7.02(d,j=8.8hz,2h),3.36(br s,4h),2.64-2.57(m,4h),1.04(s,9h)。
[2027]
实例155:3-(5-(((r)-1-(4-(4-(叔丁基)哌嗪-1-基)苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-229)
[2028][2029]
在室温下,向3-(1-氧代-5-(((r)-哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮i-47(200mg,0.55mmol,甲酸盐)和4-(4-(叔丁基)哌嗪-1-基)苯甲醛int-228(275mg,1.12mmol)在dmf(2ml)中的溶液添加nabh3cn(70mg,1.12mmol)。将反应在60℃下搅拌12小时。将反应用水(2ml)稀释并用乙酸乙酯萃取三次。将有机层合并,用饱和水性氯化钠洗涤,经na2so4干燥,过滤,并真空浓缩。将粗材料通过反相hplc(仪器:acs-wh-gx-f;柱:phenomenex luna c18 150*25mm*10um;流动相:a表示h2o(0.225%fa)以及b表示乙腈;梯度:在10min内呈线性地b 6%-36%;流速:25ml/min;柱温:室温,波长:220nm/254nm)纯化,以提供呈黄色油状物的3-(5-(((r)-1-(4-(4-(叔丁基)哌嗪-1-基)苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-229s0-ee-stcj(59.33mg,0.10mmol,18%产率)。lcms[m h]
:588.7。1h nmr(400mhz,dmso-d6)δ8.37-8.24(m,1h),7.61(d,j=8.4hz,1h),7.22-7.11(m,3h),7.08-7.04(m,1h),6.84(d,j=8.4hz,2h),5.10-5.04(m,1h),4.41-4.21(m,4h),4.14-4.09(m,1h),3.90-3.86(m,1h),3.31-3.27(m,1h),3.12-2.99(m,4h),2.96-2.84(m,1h),2.76-2.58(m,6h),2.40-2.35(m,1h),2.12-2.04(m,1h),2.02-1.93(m,1h),1.82-1.72(m,1h),1.70-1.57(m,1h),1.55-1.28(m,4h),1.04(s,9h)。
[2030]
实例156:1-(4-(氯甲基)苯基)-4-环丙基哌嗪(int-232)
[2031][2032]
步骤1:4-(4-环丙基哌嗪-1-基)苯甲醛(230)。
[2033]
向4-氟苯甲醛(1.00g,8.06mmol)在dmf(10ml)中的溶液添加1-环丙基哌嗪(1.22g,9.67mmol)、k2co3(1.67g,12.09mmol)。将反应混合物在130℃下搅拌16小时。将反应用h2o(40ml)淬灭并用乙酸乙酯萃取三次。将有机层合并,用饱和水性氯化钠洗涤,经na2so4干燥,过滤,并真空浓缩。将粗材料用石油醚(10ml)研磨,过滤,并将滤饼用另外的石油醚洗涤。收集滤饼,以提供呈黄色固体的4-(4-环丙基哌嗪-1-基)苯甲醛230(1.1g,4.73mmol,58.7%产率)。1hnmr(400mhz,cdcl3)δ=9.69(s,1h),7.70-7.61(m,2h),6.84(d,j=8.8hz,2h),3.35-3.26(m,4h),2.71-2.62(m,4h),1.62-1.54(m,1h),0.44-0.37(m,4h)。
[2034]
步骤2:(4-(4-环丙基哌嗪-1-基)苯基)甲醇(231):
[2035]
在0℃在n2气氛下,向4-(4-环丙基哌嗪-1-基)苯甲醛230(500mg,2.17mmol)在meoh(5ml)中的溶液缓慢添加nabh4(164mg,4.34mmol)。将反应放置于室温下并搅拌2小时。将反应过滤以除去不溶物质并真空浓缩,以提供呈白色固体的(4-(4-环丙基哌嗪-1-基)苯基)甲醇231(0.5g,2.15mmol,99%产率)。将粗产物直接用于下一步骤。lcms[m h]
:233.2。
[2036]
步骤3:1-(4-(氯甲基)苯基)-4-环丙基哌嗪(int-232):
[2037]
在25℃下,向(4-(4-环丙基哌嗪-1-基)苯基)甲醇231(400mg,1.72mmol)在dcm(4ml)中的溶液添加socl2(1.02ml,8.61mmol)。将反应在40℃下搅拌2小时。将反应在减压下浓缩,以提供呈黄色固体的1-(4-(氯甲基)苯基)-4-环丙基哌嗪int-232(0.4g,1.60mmol,93%产率)。将粗产物直接用于下一步骤。
[2038]
实例157:3-(5-(((r)-1-(4-(4-环丙基哌嗪-1-基)苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-233)
[2039][2040]
在室温下,向3-(1-氧代-5-(((r)-哌啶-2-基)甲氧基)异吲哚啉-2-基)哌啶-2,6-二酮i-47(200mg,0.55mmol)和1-(4-(氯甲基)苯基)-4-环丙基哌嗪int-232(280mg,1.12mmol)在acn(2ml)中的溶液添加nahco3(188mg,2.24mmol)。将反应在40℃下搅拌12小时。将反应真空浓缩。将粗材料通过反相hplc(柱:waters xbridge 150*25mm*5um;流动相:[水(10mm nh4hco3)-acn];b%:38%-68%,10min)纯化,并进一步通过反相hplc(柱:waters xbridge 150*25mm*5um;流动相:[水(10mm nh4hco3)-acn];b%:45%-75%,10min)纯化,以提供呈灰白色固体的3-(5-(((r)-1-(4-(4-环丙基哌嗪-1-基)苄基)哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-233s0-ee-sten(21.3mg,0.037mmol,6.65%产率)。lcms[m h]
:572.4。1h nmr(400mhz,dmso-d6)δ=8.28(s,1h),7.61(d,j=8.0hz,1h),7.21-7.12(m,3h),7.07(m,1h),6.85(d,j=8.0hz,2h),5.08(m,1h),4.41-4.26(m,4h),4.12(m,2h),3.90(m,2h),3.29(m,2h),3.07-3.02(m,4h),2.91(m,1h),2.66(m,4h),2.12-2.07(m,1h),2.02-1.96(m,1h),1.83-1.76(m,1h),1.67-1.62(m,2h),1.54-1.45(m,2h),1.42-1.32(m,2h),0.47-0.41(m,2h),0.34(m,2h)。
[2041]
实例158:甲基(2r,4r)-4-氟-1-((r)-1-苯基乙基)哌啶-2-甲酸酯(int-238)和甲基(2s,4s)-4-氟-1-((r)-1-苯基乙基)哌啶-2-甲酸酯(int-239)
[2042][2043]
步骤1:(r)-n-(1-苯基乙基)丁-3-烯-1-胺(234)。
[2044]
向(r)-1-苯基乙-1-胺(15g,123.8mmol)在dmf(123ml)中的溶液添加4-溴丁-1-烯(16.7g,45.4mmol)和k2co3(17.1g,123.8mmol)。将混合物在n2气氛下在室温搅拌16小时。将反应混合物用水(200ml)稀释,并用乙酸乙酯萃取三次。将有机层合并,用饱和水性氯化钠洗涤三次,经na2so4干燥,过滤并真空浓缩。将粗材料通过硅胶色谱法(在石油醚中的0-40%乙酸乙酯)纯化,以提供呈黄色油状物的(r)-n-(1-苯基乙基)丁-3-烯-1-胺234(14.4g,80.5mmol,65%产率)。lcms[m h]
:176.1。1h nmr(400mhz,dmso-d6)δ=7.34-7.26(m,4h),7.23-7.15(m,1h),5.82-5.72(m,1h),5.03-4.91(m,2h),3.70-3.65(m,1h),2.46-2.27(m,2h),2.17-2.09(m,2h),1.92-1.81(m,1h),1.23(d,j=6.4hz,3h)。
[2045]
步骤2:(1r,5s)-2-((r)-1-苯基乙基)-6-氧杂-2-氮杂双环[3.2.1]辛-7-酮(235)。
[2046]
向(r)-n-(1-苯基乙基)丁-3-烯-1-胺234(18.8g,107.3mmol)在acn(188ml)中的溶液添加2-氧代乙酸(25.4g,171.6mmol)和分子筛(10g)。将反应混合物在n2下在室温下搅拌16小时。将反应混合物过滤,用水(200ml)稀释,并用乙酸乙酯萃取三次。将有机层合并,经na2so4干燥,过滤并真空浓缩。将粗材料通过硅胶色谱法(在石油醚中的0-100%乙酸乙酯)纯化,以提供呈黄色油状物的(1r,5s)-2-((r)-1-苯基乙基)-6-氧杂-2-氮杂双环[3.2.1]辛-7-酮235(18.50g,72.0mmol,67.1%产率)。lcms[m h]
:232.3。
[2047]
步骤3:甲基(2r,4s)-4-羟基-1-((r)-1-苯基乙基)哌啶-2-甲酸酯(236)和甲基(2s,4r)-4-羟基-1-((r)-1-苯基乙基)哌啶-2-甲酸酯(237)。
[2048]
向(1r,5s)-2-((r)-1-苯基乙基)-6-氧杂-2-氮杂双环[3.2.1]辛-7-酮235(18.5g,80.0mmol)在meoh(185ml)中的溶液添加nh3·
h2o(4.62ml,120mmol)。将混合物在室温下搅拌16小时。将反应混合物真空浓缩,并通过硅胶色谱法(在石油醚中的0-100%乙酸乙酯)纯化,以提供呈黄色油状物的甲基(2r,4s)-4-羟基-1-((r)-1-苯基乙基)哌啶-2-甲酸酯236(8.20g,30.1mmol,37.7%产率)和呈黄色油状物的甲基(2s,4r)-4-羟基-1-((r)-1-苯基乙基)哌啶-2-甲酸酯237(9.90g,37.6mmol,46.2%产率)。
[2049]
甲基(2r,4s)-4-羟基-1-((r)-1-苯基乙基)哌啶-2-甲酸酯(236):lcms[m h]
:264.3,rt 1.073min。1h nmr(400mhz,cdcl3)δ=7.44-7.40(m,2h),7.35-7.30(m,2h),7.27-7.22(m,1h),4.01-3.94(m,1h),3.89-3.84(m,1h),3.77(s,3h),3.75-3.72(m,1h),2.91-2.84(m,1h),2.35-2.29(m,1h),2.16-2.08(m,2h),1.80-1.70(m,1h),1.56-1.48(m,1h),
1.31-1.28(m,3h)。旋光度:在25℃下,比旋光度= 87.207
°
,c=1g/100ml chcl3[2050]
甲基(2s,4r)-4-羟基-1-((r)-1-苯基乙基)哌啶-2-甲酸酯(237):参考分配立体化学:bioorganic&medicinal chemistry letters[生物有机和药物化学快报],第6卷,第8期,第963-966页,1996。lcms[m h]
:264.3,rt 1.009min。1h nmr(400mhz,cdcl3)δ=7.36-7.31(m,2h),7.30-7.26(m,1h),7.25-7.20(m,2h),3.98-3.93(m,1h),3.77(s,3h),3.70-3.64(m,1h),3.23-3.13(m,2h),2.33-2.27(m,1h),2.03-1.98(m,1h),1.93-1.81(m,2h),1.75-1.65(m,1h),1.46(d,j=6.8hz,3h)。旋光度:在25℃下,比旋光度= 13.951
°
,c=1g/100ml chcl3。
[2051]
步骤4:单一非对映异构体甲基4-氟-1-((r)-1-苯基乙基)哌啶-2-甲酸酯(int-238)和单一非对映异构体甲基4-氟-1-((r)-1-苯基乙基)哌啶-2-甲酸酯(int-239)
[2052]
在0℃下,向甲基(2s,4r)-4-羟基-1-((r)-1-苯基乙基)哌啶-2-甲酸酯237(5.0g,19.0mmol)在dcm(50ml)中的溶液添加dast(6.98ml,57.0mmol)。将混合物在室温下在n2下搅拌16小时。将反应混合物用水稀释,并用乙酸乙酯萃取三次。将有机层合并,经na2so4干燥,过滤并真空浓缩。将粗材料通过反相hplc(柱:waters xbridge beh c18 250*50mm*10um;流动相:[水(0.05%氢氧化氨v/v)-acn];b%:45%-75%,20min)纯化。将含有所希望的产物的级分浓缩以除去有机溶剂然后冻干,以提供呈黄色油状物的单一非对映异构体甲基(2s,4s)-4-氟-1-((r)-1-苯基乙基)哌啶-2-甲酸酯int-239(1.2g,4.50mmol,23.7%产率)和呈黄色油状物的单一非对映异构体甲基(2r,4r)-4-氟-1-((r)-1-苯基乙基)哌啶-2-甲酸酯int-238(0.62g,2.34mmol,12.3%产率)。
[2053]
单一非对映异构体甲基4-氟-1-((r)-1-苯基乙基)哌啶-2-甲酸酯(int-239):lcms[m h]
:266.3,rt 1.287min。1h nmr(400mhz,dmso-d6)δ=7.36-7.27(m,3h),7.25-7.21(m,2h),4.83-4.65(m,1h),3.89-3.81(m,1h),3.66(s,3h),2.94-2.88(m,1h),2.59-2.52(m,1h),2.48-2.21(m,1h),1.95-1.85(m,1h),1.84-1.63(m,2h),1.33(d,j=6.8hz,3h),1.30-1.21(m,1h)。
[2054]
单一非对映异构体甲基4-氟-1-((r)-1-苯基乙基)哌啶-2-甲酸酯(int-238):lcms[m h]
:266.3,rt 1.191min。1h nmr(400mhz,dmso-d6)δ=7.39-7.28(m,4h),7.26-7.19(m,1h),4.83-4.65(m,1h),3.94-3.92(m,1h),3.89-3.94(m,1h),3.68(s,3h),2.57-2.52(m,1h),2.47(s,1h),2.27-2.12(m,1h),1.98-1.86(m,1h),1.84-1.69(m,1h),1.63-1.47(m,1h),1.24(d,j=6.8hz,3h)。
[2055]
实例159;3-(5-(((2r,4r)-1-乙基-4-氟哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-244)
[2056][2057]
步骤1:(4-氟-1-((r)-1-苯基乙基)哌啶-2-基)甲醇(240)。
[2058]
在0℃下,向甲基4-氟-1-((r)-1-苯基乙基)哌啶-2-甲酸酯int-238(620mg,2.34mmol)在thf(12ml)中的溶液分批添加lah(133mg,3.51mmol)。将混合物在室温下搅拌1小时。将反应混合物用水性饱和nh4cl(10ml)淬灭,并用乙酸乙酯萃取两次。将有机层合并,经na2so4干燥,过滤并真空浓缩,以提供呈无色油状物的(4-氟-1-((r)-1-苯基乙基)哌啶-2-基)甲醇240。将物质无需纯化即可直接用于下个步骤。lcms[m h]
:238.2。
[2059]
步骤2:叔丁基4-氟-2-(羟基甲基)哌啶-1-甲酸酯(241)。
[2060]
向(4-氟-1-((r)-1-苯基乙基)哌啶-2-基)甲醇240(620mg,2.61mmol)在meoh(6ml)中的溶液添加boc2o(627mg,2.87mmol)和10%pd/c(150mg,0.141mmol)。将反应在40℃下在h2(15psi)下搅拌16小时。将悬浮液通过celite垫过滤,并用乙酸乙酯洗涤三次。将合并的滤液真空浓缩,以提供呈无色油状物的叔丁基4-氟-2-(羟基甲基)哌啶-1-甲酸酯241(550mg,2.35mmol,90%产率)。将物质无需任何其他纯化即可直接用于下个步骤。1h nmr(400mhz,cdcl3)δ4.98-4.66(m,1h),4.48-4.31(m,1h),4.04-4.01(m,1h),3.78-3.61(m,2h),3.08-3.01(m,1h),2.19-1.97(m,2h),1.84-1.59(m,2h),1.47(s,9h)。
[2061]
步骤3:叔丁基2-(((2-(2,6-二氧代-1-((2-(三甲基甲硅烷基)乙氧基)甲基)哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)-4-氟哌啶-1-甲酸酯(242)。
[2062]
在n2下,将叔丁基4-氟-2-(羟基甲基)哌啶-1-甲酸酯241(550mg,2.36mmol)、3-(5-溴-1-氧代异吲哚啉-2-基)-1-((2-(三甲基甲硅烷基)乙氧基)甲基)哌啶-2,6-二酮(356mg,0.79mmol)、ir[df(cf3)ppy]2(dtbpy)(pf6)(9mg,0.008mmol)和nicl2·
dtbbpy(15mg,0.039mmol)、奎宁环(9mg,0.079mmol)、tmp(217mg,1.58mmol)在mecn(10ml)中的混合物脱气三次。然后,将反应小瓶用封口膜密封,放置在距离一个蓝色led灯2cm远的地方,并在25℃下照射16小时。将反应混合物过滤,并将滤饼用acn洗涤三次。将合并的滤液浓缩,并通过硅胶色谱法(在石油醚中的0-100%乙酸乙酯)纯化。将含有所希望的产物的级分合
并并浓缩,以提供呈亮黄色油状物的叔丁基2-(((2-(2,6-二氧代-1-((2-(三甲基甲硅烷基)乙氧基)甲基)哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)-4-氟哌啶-1-甲酸酯242(320mg,0.528mmol,67.2%产率)。1h nmr(400mhz,dmso-d6)δ7.64(d,j=8.4hz,1h),7.20(s,1h),7.10-7.04(m,1h),5.24-5.14(m,1h),5.11-4.88(m,3h),4.73-4.59(m,1h),4.46-4.36(m,1h),4.29-4.13(m,3h),3.60-3.45(m,2h),3.13-2.91(m,2h),2.86-2.71(m,1h),2.46-2.30(m,2h),2.26-2.16(m,1h),2.10-2.00(m,2h),1.73-1.62(m,1h),1.52-1.42(m,1h),1.36(s,9h),0.89-0.77(m,2h),-0.02(s,9h)。
[2063]
步骤4:3-(5-((4-氟哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(243)。
[2064]
向叔丁基2-(((2-(2,6-二氧代-1-((2-(三甲基甲硅烷基)乙氧基)甲基)哌啶-3-基)-1-氧代异吲哚啉-5-基)氧基)甲基)-4-氟哌啶-1-甲酸酯242(320mg,0.53mmol)在acn(2ml)中的溶液添加msoh(0.34ml,5.28mmol)。将反应在40℃下搅拌3小时。在0℃下添加三乙胺(0.94ml,6.87mmol)和dmeda(0.23ml,2.11mmol)。将反应混合物在室温下搅拌16小时。将反应浓缩以给出粗材料。将粗产物用h2o(2ml)溶解,并通过反相hplc(柱:26.8*125mm,40g的xb-c18,20-40μm,流动相:a表示h2o(0.1%fa v/v)以及b表示乙腈;梯度:在15min内b 0%-40%;流速:25~40ml/min;柱温:室温,波长:220nm/254nm)纯化。将洗脱液浓缩以除去acn并冻干,以提供呈黄色固体的3-(5-((4-氟哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮243(120mg,0.32mmol,60.5%产率)。lcms[m h]
:376.2。
[2065]
步骤5:3-(5-((1-乙基-4-氟哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-244)。
[2066]
向3-(5-((4-氟哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮243(120mg,0.32mmol)和乙醛(176mg,1.6mmol)在thf(0.6ml)和etoh(0.6ml)中的溶液添加在thf(218mg,0.8ml,1.6mmol)中的2m zncl2。将反应混合物在室温下搅拌1小时,然后添加nabh3cn(58mg,0.96mmol)。将反应混合物在室温下搅拌15小时。将反应混合物过滤,浓缩,通过制备型hplc(柱:waters xbridge 150*25mm*5um;流动相:[水(10mm nh4hco3)-acn];b%:15%-45%,9min)纯化。将含有所希望的产物的级分合并,浓缩以除去有机溶剂,并将残余的水溶液冻干,以提供呈灰白色固体的3-(5-((1-乙基-4-氟哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-244的甲酸盐(42.1mg,0.104mmol,32.6%产率)。lcms[m h]
:404.4。1h nmr(400mhz,dmso-d6)δ=10.96(br s,1h),8.22(s,1h),7.62(d,j=8.4hz,1h),7.24-7.02(m,2h),5.11-5.03(m,1h),5.03-4.84(m,1h),4.43-4.22(m,2h),4.17-4.04(m,2h),2.99-2.85(m,2h),2.78-2.66(m,2h),2.63-2.52(m,3h),2.44-2.33(m,1h),2.06-1.90(m,2h),1.88-1.66(m,3h),0.98(t,j=7.2hz,3h),
[2067]
实例160:3-(5-(((2s,4s)-1-乙基-4-氟哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-249)
[2068]
除了使用单一非对映异构体int-239来代替int-238之外,与实例159类似地来制备实例160。
[2069]
将在步骤5获得的3-(5-((1-乙基-4-氟哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-249通过反相hplc(柱:waters xbridge 150*25mm*5um;流动相:[水(10mm nh4hco3)-acn];b%:15%-45%,9min)纯化。将含有所希望的产物的级分合并,浓缩
以除去有机溶剂,并将残余的水溶液冻干,以提供呈灰白色固体的3-(5-((1-乙基-4-氟哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-249的甲酸盐(80.9mg,0.20mmol,62.7%产率)。lcms[m h]
:404.3。1h nmr(400mhz,dmso-d6)δ10.95(br s,1h),8.22(s,1h),7.62(d,j=8.4hz,1h),7.22-7.02(m,2h),5.11-5.03(m,1h),5.02-4.85(m,1h),4.41-4.24(m,2h),4.16-4.07(m,2h),3.01-2.84(m,2h),2.80-2.66(m,2h),2.62-2.52(m,3h),2.43-2.32(m,1h),2.03-1.91(m,2h),1.87-1.69(m,3h),0.98(t,j=7.2hz,3h)。
[2070]
实例161:3-(5-((4,4-二氟哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-251)
[2071][2072]
使用通用方法vi进行的3-(5-溴-1-氧代异吲哚啉-2-基)-1-((2-(三甲基甲硅烷基)乙氧基)甲基)哌啶-2,6-二酮(907mg,2.00mmol)和叔丁基4,4-二氟-2-(羟基甲基)哌啶-1-甲酸酯250(如wo 2013/127913 a1中所述的制备)(553mg,2.19mmol)之间的光氧化还原催化、随后整体脱保护(通用方法vii)以及通过硅胶色谱法(在含1%tea作为改性剂的dcm中的15%-100%etoh)进行的纯化提供了呈白色固体的3-(5-((4,4-二氟哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-251(556mg,1.41mmol,70%产率)。lcms[m h]
:394.4。1h nmr(400mhz,cd2cl2)δ7.96(s,1h),7.64(d,j=8.4hz,1h),6.95(dd,j=8.4,2.2hz,1h),6.91(d,j=2.2hz,1h),5.04(dd,j=13.4,5.2hz,1h),4.29(d,j=16.1hz,1h),4.22(d,j=16.1hz,1h),4.01(dd,j=9.2,3.7hz,1h),3.91(dd,j=9.1,7.0hz,1h),3.20(td,j=7.7,7.2,3.6hz,1h),3.10(ddt,j=12.7,5.4,2.7hz,1h),2.86-2.66(m,3h),2.26(qd,j=12.8,5.6hz,1h),2.18-1.93(m,3h),1.93-1.61(m,2h)。
[2073]
实例162:非对映异构体3-(5-((1-乙基-4,4-二氟哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-252)
[2074][2075]
使用通用方法iii,使3-(5-((4,4-二氟哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-251(200mg,0.51mmol)和乙醛(0.09ml,1.53mmol)进行还原胺化。将粗材料通过硅胶色谱法(用et3n饱和的硅胶,在庚烷中的15%-80%3:1etoac:etoh)纯化,以提供呈白色固体的异构体3-(5-((1-乙基-4,4-二氟哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-252的混合物(130mg,0.31mmol,60%产率)。lcms[m h]
:422.4。将异构体的混合物通过手性sfc[柱chiralpak ic 21x250mm,co2助溶剂50%3:1acn:etoh;以
70g/min在100巴下]分离,以提供两个峰。将峰1进一步通过手性sfc[柱chiralpak ad-h 21x250mm,co2助溶剂45%1:1acn:etoh;以70g/min在100巴下]纯化,以提供两种异构体。呈白色固体的3-(5-((1-乙基-4,4-二氟哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮的异构体1(6.4mg,0.02mmol);手性sfc rt 1.8min[柱chiralpak ad-h 4.6x100mm,co2助溶剂40%1:1acn:etoh;以4ml/min在125巴下];1h nmr(400mhz,cd2cl2)δ7.97(s,1h),7.75(d,j=8.8hz,1h),7.04(d,j=6.6hz,2h),5.17-5.07(m,1h),4.39(d,j=16.1hz,1h),4.32(d,j=16.1hz,1h),4.15(s,2h),3.24-2.95(m,1h),2.94-2.72(m,4h),2.75-2.56(m,1h),2.35(qd,j=12.9,5.6hz,1h),2.20(dtd,j=13.0,5.0,2.8hz,2h),2.13-1.90(m,2h),1.74-1.42(m,2h),1.43-1.01(m,3h)。呈白色固体的3-(5-((1-乙基-4,4-二氟哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮的异构体2(6.0mg,0.01mmol);手性sfc rt 2.3min[柱chiralpak ad-h 4.6x100mm,co2助溶剂40%1:1acn:etoh;以4ml/min在125巴下];1h nmr(400mhz,cd2cl2)δ7.94(s,1h),7.76(d,j=8.8hz,1h),7.05(d,j=9.0hz,2h),5.16-5.03(m,1h),4.40(d,j=16.1hz,1h),4.32(d,j=16.1hz,1h),4.28-3.99(m,2h),3.05-2.92(m,1h),2.92-2.73(m,4h),2.71-2.56(m,1h)2.35(qd,j=12.9,5.5hz,2h),2.20(dtd,j=13.0,5.1,2.7hz,2h),1.99(d,j=29.1hz,1h),1.64-1.38(m,2h),1.31-0.98(m,3h)。将峰2进一步通过手性sfc[柱chiralpak ad-h 21x250mm,co2助溶剂35%异丙醇;以70g/min在100巴下]纯化,以提供两种异构体。呈白色固体的3-(5-((1-乙基-4,4-二氟哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮的异构体3(7.0mg,0.02mmol);手性sfc rt 2.1min[柱chiralpak ad-h 4.6x100mm,co2助溶剂35%异丙醇;以4ml/min在125巴下];1h nmr(400mhz,cd2cl2)δ7.97(s,1h),7.74(d,j=8.3hz,1h),7.21-6.81(m,2h),5.13(dd,j=13.3,5.2hz,1h),4.39(d,j=16.1hz,1h),4.31(d,j=16.1hz,1h),4.11(s,2h),2.99(s,1h),2.94-2.74(m,4h),2.66(s,1h),2.35(qd,j=12.9,5.6hz,1h),2.20(dtd,j=13.2,5.2,2.9hz,2h),2.06(s,2h),1.53(s,2h),1.09(s,3h)。呈白色固体的3-(5-((1-乙基-4,4-二氟哌啶-2-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮的异构体4(6.0mg,0.01mmol);手性sfc rt 3.1min[柱chiralpak ad-h 4.6x100mm,co2助溶剂35%异丙醇;以4ml/min在125巴下];1h nmr(400mhz,cd2cl2)δ7.99(s,1h),7.74(d,j=8.4hz,1h),7.16-6.89(m,2h),5.13(dd,j=13.3,5.1hz,1h),4.39(d,j=16.1hz,1h),4.31(d,j=16.1hz,1h),4.21-4.00(m,2h),3.11-2.93(m,1h),2.94-2.75(m,3h),2.75-2.50(m,2h),2.35(qd,j=12.8,5.5hz,1h),2.20(dtd,j=13.0,5.1,2.8hz,2h),2.04(s,2h),1.73-1.42(m,2h),1.08(s,3h)。
[2076]
实例163:非对映异构体3-(5-((内切-2-乙基-2-氮杂双环[2.2.1]庚烷-3-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-255)
[2077][2078]
步骤1:叔丁基(内切)-3-(羟基甲基)-2-氮杂双环[2.2.1]庚烷-2-甲酸酯(253)。
[2079]
将内切-2-(叔丁氧基羰基)-2-氮杂双环[2.2.1]庚烷-3-甲酸的外消旋体(0.30g,1.24mmol)溶解于thf(6ml)中并冷却至0℃。逐滴添加在thf中的1m硼烷thf复合物(2.6ml,2.60mmol)。将反应在室温下搅拌过夜。将反应冷却至0℃并用甲醇(1.0ml,24.7mmol)淬灭,并在室温下搅拌2小时。将反应浓缩至干燥,然后重新溶解于甲醇(5ml)中。将反应在室温下搅拌过夜。将反应浓缩,以提供呈澄清油状物的叔丁基(内切)-3-(羟基甲基)-2-氮杂双环[2.2.1]庚烷-2-甲酸酯253的外消旋混合物(256mg,1.13mmol,91%产率)。将物质无需纯化即可用于下一步骤。
[2080]
步骤2:3-(5-((内切-2-氮杂双环[2.2.1]庚烷-3-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(254)。
[2081]
使用通用方法vi进行的外消旋体叔丁基内切-3-(羟基甲基)-2-氮杂双环[2.2.1]庚烷-2-甲酸酯253(1.65g,7.28mmol)和3-(5-溴-1-氧代异吲哚啉-2-基)-1-((2-(三甲基甲硅烷基)乙氧基)甲基)哌啶-2,6-二酮(3.00g,6.62mmol)之间的光氧化还原催化、随后整体脱保护(通用方法vii)以及通过硅胶色谱法(在dcm中的15%-100%etoh,1%tea作为改性剂)进行的纯化提供了呈白色固体的3-(5-((内切-2-氮杂双环[2.2.1]庚烷-3-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮254(1.07g,2.90mmol,44%产率)。lcms[m h]
:370.4。
[2082]
步骤3:非对映异构体3-(5-((内切-2-乙基-2-氮杂双环[2.2.1]庚烷-3-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮(i-255)
[2083]
使用通用方法iii,使3-(5-((内切-2-氮杂双环[2.2.1]庚烷-3-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮254(200mg,0.54mmol)和乙醛(0.09ml,1.62mmol)进行还原胺化。将粗材料通过硅胶色谱法(用tea饱和的硅胶,在庚烷中的15%-80%3:1etoac:etoh)纯化,以提供呈白色固体的3-(5-((内切-2-乙基-2-氮杂双环[2.2.1]庚烷-3-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮i-255的异构体混合物(103mg,0.26mmol,48%产率)。lcms[m h]
:398.3。将异构体的混合物通过手性sfc[柱chiralpak ic 21x250mm,含0.25%tea的co2助溶剂50%3:1acn:etoh;以80g/min在100巴下]分离,以提供两个峰。将峰1进一步通过手性hplc[柱chiralpak id 30x250mm,含0.05%tea的3:1tbme:etoh,以20ml/min]纯化,以提供两种异构体。呈白色固体的3-(5-((内切-2-乙基-2-氮杂双环[2.2.1]庚烷-3-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮的异构体3(5.5mg,
0.01mmol);手性sfc rt 3.9min[柱chiralpak ia-3 3x100mm,含0.1%nh4oh的co2助溶剂30%meoh;以2.5ml/min在1800psi下];1h nmr(400mhz,cd2cl2)δ7.95(s,1h),7.74(d,j=8.4hz,1h),7.12(d,j=2.3hz,1h),7.07(dd,j=8.4,2.3hz,1h),5.12(dd,j=13.3,5.0hz,1h),4.79(s,1h),4.40(d,j=16.1hz,1h),4.33(d,j=16.1hz,1h),3.89(s,1h),3.45(s,1h),3.11(s,2h),2.94-2.72(m,3h),2.36(qd,j=12.9,5.6hz,1h),2.19(dtd,j=13.1,5.3,2.9hz,1h),2.05-1.93(m,1h),1.84-1.40(m,9h)。呈白色固体的3-(5-((内切-2-乙基-2-氮杂双环[2.2.1]庚烷-3-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮的异构体4(5.6mg,0.01mmol);手性sfc rt 4.5min[柱chiralpak ia-3 3x100mm,含0.1%nh4oh的co2助溶剂30%meoh;以2.5ml/min在1800psi下];1h nmr(400mhz,cd2cl2)δ7.95(s,1h),7.72(d,j=8.9hz,1h),7.08-7.01(m,2h),5.21-5.02(m,1h),4.38(d,j=16.0hz,1h),4.31(d,j=16.1hz,1h),4.21-3.79(m,1h),3.19(s,1h),3.04-2.74(m,3h),2.74-2.45(m,2h),2.35(qd,j=12.9,5.8hz,1h),2.19(dtd,j=13.1,5.1,2.8hz,1h),1.85-0.92(m,11h)。将峰2进一步通过手性sfc[柱chiralpak ad-h 21x250mm,含0.25%tea的co2助溶剂35%异丙醇;以70g/min在100巴下]分离,以提供两种异构体。呈白色固体的3-(5-((内切-2-乙基-2-氮杂双环[2.2.1]庚烷-3-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮的异构体1(13mg,0.03mmol);手性sfc rt 3.4min[柱chiralpak ia-3 3x100mm,含0.1%nh4oh的co2助溶剂30%meoh;以2.5ml/min在1800psi下];1h nmr(400mhz,cd2cl2)δ7.95(s,1h),7.74(d,j=8.4hz,1h),7.27-6.90(m,2h),5.19-5.02(m,1h),4.82(s,1h),4.40(d,j=16.3hz,1h),4.33(d,j=16.1hz,1h),3.92(s,1h),3.47(s,1h),3.13(s,2h),2.97-2.72(m,3h),2.36(qd,j=12.9,5.5hz,1h),2.26-2.12(m,1h),2.09-1.92(m,1h),1.87-1.36(m,9h)。呈白色固体的3-(5-((内切-2-乙基-2-氮杂双环[2.2.1]庚烷-3-基)甲氧基)-1-氧代异吲哚啉-2-基)哌啶-2,6-二酮的异构体2(3.0mg,0.01mmol);手性sfc rt 3.8min[柱chiralpak ia-3 3x100mm,含0.1%nh4oh的co2助溶剂30%meoh;以2.5ml/min在1800psi下];1h nmr(400mhz,cd2cl2)δ7.94(s,1h),7.73(d,j=8.4hz,1h),7.05(d,j=9.2hz,2h),5.18-5.02(m,1h),4.39(d,j=16.0hz,1h),4.32(d,j=16.3hz,1h),3.92(s,1h),3.11(s,1h),2.97-2.72(m,3h),2.63(s,2h),2.35(qd,j=12.9,5.6hz,1h),2.28-2.11(m,1h),1.90-0.97(m,11h)。
[2084]
生物学数据
[2085]
缩写
[2086]
amo
ꢀꢀꢀꢀꢀꢀꢀ
抗mirna寡核苷酸
[2087]
bsa
ꢀꢀꢀꢀꢀꢀꢀ
牛血清白蛋白
[2088]
cas9
ꢀꢀꢀꢀꢀꢀ
crispr相关蛋白9
[2089]
crispr
ꢀꢀꢀꢀ
成簇的规则间隔短回文重复序列
[2090]
crrna
ꢀꢀꢀꢀꢀ
crispr rna
[2091]
dmem
ꢀꢀꢀꢀꢀꢀ
杜尔贝科改良伊格尔培养基
[2092]
dmso
ꢀꢀꢀꢀꢀꢀ
二甲基亚砜
[2093]
dtt
ꢀꢀꢀꢀꢀꢀꢀ
二硫苏糖醇
[2094]
edta
ꢀꢀꢀꢀꢀꢀ
乙二胺四乙酸
[2095]
egfp
ꢀꢀꢀꢀꢀꢀ
增强的绿色荧光蛋白
[2096]
facs
ꢀꢀꢀꢀꢀꢀ
荧光激活细胞分选
[2097]
fbs
ꢀꢀꢀꢀꢀꢀꢀ
胎牛血清
[2098]
fitc
ꢀꢀꢀꢀꢀꢀ
荧光素
[2099]
flt3l
ꢀꢀꢀꢀꢀ
fms相关的酪氨酸激酶3配体,flt3l
[2100]
hbf
ꢀꢀꢀꢀꢀꢀꢀ
胎儿血红蛋白
[2101]
hepes
ꢀꢀꢀꢀꢀ
(4-(2-羟基乙基)-1-哌嗪乙磺酸)
[2102]
imdm
ꢀꢀꢀꢀꢀꢀ
伊斯科夫改良的杜尔贝科培养基(iscove’s modified dulbecco’s medium)
[2103]
kcl
ꢀꢀꢀꢀꢀꢀꢀ
氯化钾
[2104]
mpb
ꢀꢀꢀꢀꢀꢀꢀ
动员的外周血
[2105]
pbs
ꢀꢀꢀꢀꢀꢀꢀ
磷酸盐缓冲盐水
[2106]
rhepo
ꢀꢀꢀꢀꢀ
重组人红细胞生成素
[2107]
rhil-3
ꢀꢀꢀꢀ
重组人白介素-3
[2108]
rhil-6
ꢀꢀꢀꢀ
重组人白介素-6
[2109]
rhscf
ꢀꢀꢀꢀꢀ
重组人干细胞因子
[2110]
rhtpo
ꢀꢀꢀꢀꢀ
重组人促血小板生成素
[2111]
rnp
ꢀꢀꢀꢀꢀꢀꢀ
核糖核蛋白
[2112]
shrna
ꢀꢀꢀꢀꢀ
短发夹rna
[2113]
tracrrna
ꢀꢀ
反式激活crrna
[2114]
wiz
ꢀꢀꢀꢀꢀꢀꢀ
含有宽间隔的锌指的蛋白
[2115]
材料与方法
[2116]
实例55:hibit标签融合蛋白测定中wiz蛋白水平的定量
[2117]
将来自普洛麦格公司(promega)的hibit系统用于开发高通量和定量测定,以测量wiz蛋白水平对化合物的响应变化。hibit标签衍生自分裂的纳米荧光素酶,并且具有以下蛋白质序列:vsgwrlfkkis(seq id no:1)。将纳米荧光素酶(称为lgbit,来自普洛麦格公司)的互补片段添加到hibit标签中,以形成有活性的纳米荧光素酶,其活性可以精确测量。以这种方式,可以在细胞裂解物中定量具有hibit标签的融合蛋白的水平。
[2118]
构建慢病毒载体(基于invitrogen
tm
plenti6.2/v5 dest骨架),其将hibit标签置于wiz上游,并从hsvtk启动子表达融合蛋白。
[2119]
为了确保hibit-wiz融合蛋白在群体中的所有细胞中的适度和一致的表达,从具有单拷贝构建体的细胞构建稳定的细胞系。使用来自invitrogen
tm
的virapower
tm
试剂盒制备与构建体一起包装的慢病毒。在低感染复数下,将来自atcc的293t细胞(目录号:crl-3216)用病毒感染,并在培养基中通过5μg/ml杀稻瘟菌素选择2周。
[2120]
如下测量化合物处理的细胞系中hibit-wiz标记的融合蛋白的水平:
[2121]
第1天,将细胞在正常生长培养基中稀释至1.0x106个细胞/ml。将20μl的细胞悬液接种到固体白色384孔板的每个孔中。将板在37℃和5%co2湿润的组织培养箱中孵育过夜。
[2122]
第2天,在384孔板中制备连续稀释的化合物。在第1、2、23、24列给化合物板提供dmso,在第3-12列和第13-22列给化合物板提供10点化合物稀释系列。将10mm的化合物储备溶液放入第3列或第13列中,并进行1:5连续稀释,直至每种化合物有10点稀释系列。通过(labcyte公司)声转移将50nl稀释的化合物转移到铺板的细胞中。化合物的最高浓
度为25μm。将板在37℃和5%co2湿润的组织培养箱中孵育过夜(约18小时)。
[2123]
第3天,将板从培养箱中取出并允许其在室温下平衡60分钟。如制造商方案所述的,添加hibit底物(hibit lytic检测系统,普洛麦格公司目录号:n3050)。将板在室温下孵育30分钟,并使用en读数器读取发光。使用软件包对数据进行分析和可视化。
[2124]
化合物的wiz降解活性(表1)
[2125]
表1示出了本披露的化合物在293t细胞中的wiz hibit测定中的wiz降解活性。wiz amax反映了dmso归一化,wiz-hibit的曲线拟合百分比保持为25um。通过将dmso对照归一化为100%,对剂量响应数据进行参数曲线拟合(10点,5倍),然后使用拟合方程计算在25um的响应(nd=未确定)来计算。
[2126]
表1:
[2127]
[2128]
[2129]
[2130]
[2131]
[2132]
[2133][2134]
na=未测量
[2135]
实例56:小分子hbf诱导测定
[2136]
从澳赛尔斯公司(allcells,llc)获得冷冻保存的原代人cd34
造血干细胞和祖细胞。在通过施用粒细胞集落刺激因子进行动员后,从健康供体的外周血中分离cd34
细胞。使用2阶段培养法使细胞向红系谱系离体分化。在第一阶段,将细胞在37℃在5%co2下在补充有rhscf(50ng/ml,公司)、rhil-6(50ng/ml,公司)、rhil-3
(50ng/ml,公司)和rhflt3l(50ng/ml,公司)以及1x抗生素-抗真菌药(生命技术公司(life technologies),赛默飞世尔科技公司)的stemspan
tm
无血清扩增培养基(sfem)(干细胞技术公司(stemcell technologies inc.))中培养6天。在第二阶段期间,将细胞在37℃下在5%co2下、在化合物存在下、在红系分化培养基中以5,000个细胞/ml培养7天。红系分化培养基包括imdm(生命技术公司),补充有胰岛素(10μg/ml,西格玛奥德里奇公司)、肝素(2u/ml,西格玛奥德里奇公司)、全转铁蛋白(330μg/ml,西格玛奥德里奇公司)、人血清ab(5%,西格玛奥德里奇公司)、氢化可的松(1μm,干细胞技术公司)、rhscf(100ng/ml,公司)、rhil-3(5ng/ml,公司)、rhepo(3u/ml,公司)和1x抗生素-抗真菌剂。将所有化合物溶解并稀释到二甲基亚砜(dmso)中,然后将其添加到培养基中,使最终浓度为0.3%dmso,从而从30um开始以7点、1:3稀释系列进行测试。
[2137]
染色和流式细胞术
[2138]
为了进行活力分析,将样品洗涤并重悬于磷酸盐缓冲盐水(pbs)中,并用live/dead
tm
可固定紫色死细胞染色试剂盒(生命技术公司,l34963)染色20分钟。然后将细胞再次用pbs洗涤,并重悬于补充有2%胎牛血清(fbs)和2mm edta的pbs中,以准备进行细胞表面标志物分析。将细胞用别藻蓝素偶联的cd235a(1:100,bd生物科学公司,551336)抗体和brilliant violet偶联的cd71(1:100,bd生物科学公司,563767)抗体标记20分钟。为了分析细胞质胎儿血红蛋白(hbf),根据制造商的方案,使用固定缓冲液(420801)和透化洗涤缓冲液(421002)将细胞固定并透化。在透化步骤期间,将细胞用藻红蛋白偶联或fitc偶联的hbf特异性抗体(1:10-1:25,invitrogen
tm
,mhfh04-4)染色30分钟。在facscanto
tm
ii流式细胞仪或lsrfortessa
tm
(bd生物科学公司)上进行分析之前,将染色的细胞用磷酸盐缓冲盐水洗涤。使用flowjo
tm
软件(bd生物科学公司)进行数据分析。
[2139]
化合物的hbf诱导活性(表2)
[2140]
将mpb cd34 细胞扩增6天,然后在化合物存在下使其红系分化7天。将细胞固定,染色并通过流式细胞术分析。表2示出了化合物的hbf诱导活性。hbf amax=在拟合的剂量响应曲线中hbf阳性染色细胞的最高百分比(%hbf 细胞)。dmso处理的细胞的基线%hbf 细胞约为30%-40%。
[2141]
表2:
[2142][2143]
实例57:用于shrna和crispr测定的细胞培养
[2144]
将hek293t细胞维持在含有丙酮酸钠、非必需氨基酸、10%fbs、2mm l-谷氨酰胺、100u/ml pen/strep、25mm hepes的dmem高葡萄糖完全培养基中。除非另有说明,否则所有用于培养hek293t细胞的试剂均从invitrogen
tm
获得。
[2145]
在shrna转导或靶向wiz的靶向性核糖核蛋白(rnp)电穿孔之前,将动员的外周血(mpb)cd34 细胞(澳赛尔斯公司)维持在补充有各自50ng/ml的rhtpo、rhil-6、rhflt3l、rhscf的stemspan
tm
无血清扩增培养基(sfem)(干细胞技术公司)中2-3天。所有细胞因子均从公司获得。将细胞培养物保持在37℃和5%co2湿润的组织培养箱中。
[2146]
靶向wiz的shrna慢病毒克隆的产生
[2147]
针对wiz的各自的shrna的5
’‑
磷酸化有义和反义互补单链dna寡核苷酸由集成dna技术公司(integrated dna technologies,inc.,idt)合成。将每个dna寡核苷酸设计为分别在5
’‑
末端和3'-末端带有pmei/asci限制性突出端,以便随后相容性连接到慢病毒载体骨架中。通过在98℃在加热块上加热5分钟、随后在工作台上冷却至室温来将等摩尔的互补寡核苷酸在neb缓冲液2(new england公司)中退火。使用t4dna连接酶试剂盒(新
英格兰生物实验室),将退火的双链dna寡核苷酸连接到用pmei/asci消化的phage慢病毒主链中。根据制造商的方案,将连接反应转化为化学感受态的stbl3细胞(invitrogen
tm
)。使用测序引物(5
’‑
ctacattttacatgatagg-3’)验证阳性克隆,并将质粒通过阿尔塔生物技术公司(alta biotech llc)纯化。
[2148]
按照制造商的说明(invitrogen
tm
),使用lipofectamine 3000试剂以150mm组织培养皿形式,通过用表达pcmv-dr8.91和pcmv-vsv-g的包膜质粒共转染hek293t细胞来生成相应shrna构建体的慢病毒颗粒。共转染后48小时收获慢病毒上清液,通过0.45μm过滤器(密理博公司(millipore))过滤,并使用带有ultracel-100膜的amicon ultra 15(密理博公司)进行浓缩。连续稀释和感染hek293t细胞后,使用egfp表达作为转导标志物,通过流式细胞术确定每种慢病毒颗粒的感染单位。
[2149]
shrna序列如下:
[2150]
shwiz_#1 5'-agcccacaatgccacggaaat-3'(seq id no:2);
[2151]
shwiz_#2 5'-gcaacatctacaccctcaaat-3'(seq id no:3);
[2152]
shwiz_#4 5'-tgaccgagtggtacgtcaatg-3'(seq id no:4);
[2153]
shwiz_#5 5'-agcggcagaacatcaacaaat-3'(seq id no:5)。
[2154]
mpb cd34 细胞的慢病毒shrna转导和facs
[2155]
mpb cd34 转导在retronectin包被的非组织培养物处理的96孔平底板(康宁公司(corning,inc.))上进行。简而言之,将板用100μl的(1μg/ml)(宝生物公司(takarabio,inc.))包被,密封并在4℃孵育过夜。然后去除并将板与pbs中的bsa(牛血清白蛋白)(1%)在室温下孵育30分钟。随后,将bsa(牛血清白蛋白)吸出并用100μl慢病毒浓缩液代替,并在室温下以2000xg离心2小时。接下来,轻轻吸取残留的上清液,准备进行mpb cd34 细胞的转导。将一万个细胞接种于150μl补充有各自50ng/ml的rhtpo、rhil-6、rhflt3l和rhscf的stemspan
tm
无血清扩增培养基(sfem)中,以开始转导。将细胞培养72小时,然后使用egfp表达作为标志物评估转导效率。
[2156]
在facsaria
tm iii(bd生物科学公司)上分选egfp阳性细胞。简而言之,将转导的mpb cd34 细胞群洗涤,并用含1x hank缓冲盐水溶液、edta(1mm)和fbs(2%)的facs缓冲液重悬。分选的egfp阳性细胞用于红系分化测定。
[2157]
对wiz进行靶向性crispr敲除
[2158]
alt-r crispr-cas9 crrna和tracrrna(5'-agcauagcaaguuaaaauaaggcuaguccguuaucaacuugaaaaaguggcaccgagucggugcuuu-3';seq id no:6)购自集成dna技术公司。通过使用聚合酶链式反应(pcr)机(伯乐公司(bio-rad))在95℃下加热5分钟,随后在操作台上冷却至室温将等摩尔的tracrrna与靶向wiz的crrna(表3)在tris缓冲液(10mm,ph 7.5)中退火。随后,通过将退火的tracrrna:crrna与6ug cas9在37℃下在含hepes(100mm)、kcl(50mm)、mgcl2(2.5mm)、甘油(0.03%)、dtt(1mm)和tris ph 7.5(2mm)的1x缓冲液中混合5分钟来生成核糖核蛋白(rnp)复合物。
[2159]
根据制造商的建议,在4d-nucleofector
tm
(龙沙公司(lonza))上进行rnp复合物的电穿孔。简而言之,将重悬于含有补充剂(龙沙公司)的原代细胞p3缓冲液中的50,000个mpb cd34 细胞与核比色皿中每孔5μl rnp复合物预混合,并在室温下孵育5分钟。随后,使用cm-137程序使混合物进行电穿孔。rnp电穿孔后将细胞培养72小时,然后开始红系分化。下表3
中示出了crrna序列。
[2160]
表3.
[2161]
名称序列(5'至3')目标基因组区域链seq id norg_0111acggaggctaagcgtcgcaa随机导向,非靶向 7wiz_6aacatctttcgggccgtaggchr19:15427143-15427163( )8wiz_9gacatccgctgcgagttctgchr19:15427488-15427510(-)9wiz_12tgcagcgtcccgggcagagcchr19:15425751-15425773(-)10wiz_14caagccgtgcctcatcaagachr19:15425571-15425593(-)11wiz_15cgggcacacctgcggcagttchr19:15424942-15424964(-)12wiz_18agtgggtgcggcacttacagchr19:15423169-15423191(-)13
[2162]
shrna转导的或rnp电穿孔的mpb cd34 细胞的红系分化
[2163]
通过在96孔组织培养板中每孔接种8,000个rnp电穿孔的或facs分选的egfp mpb cd34 细胞来开始红系分化。基础分化培养基由imdm(伊斯科夫改良的杜尔贝科培养基)、人ab血清(5%)、转铁蛋白(330μg/ml)、胰岛素(10μg/ml)和肝素(2iu/ml)组成。分化培养基补充有rhscf(100ng/ml)、rhil-3(10ng/ml)、rhepo(2.5u/ml)和氢化可的松(1μm)。分化4天后,使细胞在新鲜培养基中分裂(1:4),以维持最佳生长密度。将细胞再培养3天,并用于评估胎儿血红蛋白(hbf)表达。
[2164]
通过rna-seq分析hbf基因表达
[2165]
在mpb cd34 hsc中,使用wiz_6和wiz_18grna或非靶向加扰grna阴性对照对wiz进行两次独立的靶向性crispr/cas9敲除(ko)。然后将来自ko和阴性对照的细胞培养7天以进行红系分化并用于总rna分离(zymo研究公司(zymo research),目录号r1053)。在测序前使用agilent rna 6000 pico试剂盒(安捷伦公司(agilent),目录号5067-1513)确定分离的rna的量。
[2166]
使用illumina truseq stranded mrna样品制备方案制备rna测序文库,并使用illumina novaseq6000平台(依诺米那公司(illumina))进行测序。样品被测序为具有2x76个碱基对的长度。对于每个样品,使用salmon版本0.8.2(patro等人,2017;doi:10.1038/nmeth.4197)来将测序片段映射到由ensembl数据库提供的人参考基因组hg38中的注释转录物。通过使用tximport(soneson等人,2015;doi:10.12688/f1000research.7563.1)将转录物水平计数的计数相加来获得每个基因的表达水平。使用deseq2来标准化文库大小和转录物长度差异,并测试用靶向wiz的grna处理的样品与用加扰grna对照处理的样品之间的差异表达(love等人,2014;doi:10.1186/s13059-014-0550-8)。使用ggplot2(wickham h(2016).ggplot2:elegant graphics for data analysis[用于数据分析的精致图形].springer-verlag new york[纽约施普林格出版社].isbn 978-3-319-24277-4;https://ggplot2.tidyverse.org)来可视化数据。
[2167]
hbf细胞内染色
[2168]
将十万个细胞等分到u型底96孔板中,并根据制造商的建议(英杰公司(invitrogen)),在黑暗中用稀释的live/dead可固定紫色活力染料染色20min。将细胞用facs染色缓冲液洗涤,随后在黑暗中用抗cd71-bv711(bd生物科学公司)和抗cd235a-apc(bd生物科学公司)染色20min。在用三倍体积的1x pbs洗涤两轮后,在室温在黑暗中,将细
胞用1x bd cytofix/cytoperm(bd生物科学公司)固定并透化30分钟。随后,将细胞用三倍体积的1x perm/wash缓冲液(bd生物科学公司)洗涤两次。将抗hbf-fitc(赛默科技公司(thermoscientific))在1x perm/wash缓冲液中稀释(1:25),添加到透化细胞中并在室温在黑暗中孵育30分钟。接下来,将细胞用三倍体积的1x perm/wash缓冲液洗涤两次,并使用lsr fortessa(bd生物科学公司)通过流式细胞术进行分析。使用flowjo软件分析数据。
[2169]
结果
[2170]
wiz ko在红系分化时上调hbg1/2表达
[2171]
使用两个独立的grna(wiz_6和wiz_18)对wiz进行靶向ko显示出胎儿血红蛋白基因(hbg1/2)上调,如图1a所示。
[2172]
wiz的缺失诱导胎儿血红蛋白在mpb cd34
衍生的红系细胞中表达
[2173]
为了验证wiz是否为hbf表达的负调节物,采用了shrna和crispr-cas9介导的敲低和敲除功能遗传学方法。将mpb cd34
细胞用shrna或crispr-cas9试剂处理并使其红系分化7天,然后进行流式细胞术分析。靶向敲低wiz转录物导致78%-91%的hbf
细胞,相比之下,阴性对照加扰的shrna导致40%的hbf
细胞。误差条代表两个生物学重复的标准误差,每个生物学重复具有三个技术重复(图1b)。crispr/cas9介导的wiz的靶向缺失导致62%-88%的hbf
细胞,相比之下,随机导向的crrna导致39%的hbf
细胞。误差条代表一种生物样品的标准误差,该生物样品具有四个技术重复(图1c)。总而言之,结果表明wiz的缺失在人原代红系细胞中诱导了hbf。因此,锌指转录因子宽间隔锌指基序(wiz)被确定为进行hbf诱导的新靶标。这些数据提供了遗传证据,即证明wiz是胎儿血红蛋白表达的调节剂,并且是治疗镰状细胞病和β-地中海贫血的新靶点。
[2174]
已经如此描述了若干实施例的若干方面,应理解,本领域技术人员将容易想到各种改变、修改和改进。这些改变、修改和改进旨在成为本披露的一部分,并且旨在落入本披露的精神和范围内。因此,前述的说明书和附图仅是举例来说。
[2175]
本领域技术人员应承认,或者能够使用不超出常规的实验法确定在此明确描述的具体发明实施例的等效物。此类等效物旨在涵盖在下列权利要求的范围中。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。