1.本发明属于医疗器械技术领域,尤其涉及采用介入性手术进行动脉瘤治疗的辅助医疗器械领域,具体涉及一种动脉瘤介入手术微导管塑形辅助模具及其制作方法。
背景技术:
2.现有动脉瘤常用治疗方式是包括外科手术治疗和血管内介入治疗。血管内介入治疗主要包括弹簧圈栓塞、血流导向装置等。
3.其中,弹簧圈栓塞是目前最常用的介入治疗方式。在栓塞过程中,最关键的步骤是将输送弹簧圈的微导管精准超选到目标动脉瘤中,而微导管塑形正式解决这一问题的关键。现有微导管放置技术存在的主要问题是在于手术前或者手术中耽误的时间长,且由于病灶处的血管通常比较曲迂,若微导管的自然形态与血管及动脉瘤的形态构造不一致,非常难将微导管内的栓塞填充物送到动脉瘤中进行填充堵塞;故而,因此原因手术往往会反复进行而影响病患治疗和手术的成功性。因此,多数情况下需要在术前进行微导管塑形。而微导管塑形的不准确,会引发手术中的微导管介入障碍,不能快速的将栓塞材料填充的动脉瘤中,从而不可避免的延长手术时间和对微导管反复塑形的诸多问题。
4.进行微导管栓塞介入手术治疗动脉瘤的过程中,通常需要通过ct血管造影成像(cta),或者等同的属于本领域技术人员常用的mra,dsa等方式将病灶处的血管分布,以及血管构造与动脉瘤的连接位置情况进行立体呈现,医生根据ct成像的血管造型选用以下几种可能的方式进行微导管塑型:
5.(1)人工弯折塑形针:人工通过将微导管缠绕在曲率弧度大致等于病灶血管曲率或凭借医生经验手工弯折而成的钢针上,并进行高温熏蒸,以达到微导管塑形定型的目的,否则,在进行微导管介入血管的过程中,由于病灶处的血管弯曲幅度大,构造复杂,若微导管的自然形态与血管及动脉瘤的形态构造不一致,非常难将微导管内的栓塞填充物送到动脉瘤中进行填充堵塞;故而,给予此原因手术往往会反复进行而影响病患治疗和手术的成功性。由于每一个患者的血管分布均不相同,现有技术中完全依赖于医生的经验的主观判断,存在极大的误差,从而对塑形的精度不能保证,导致后续手术的进行存在障碍的概率增大。
6.另外上述方法还存在其它缺点。例如塑形针长度制约导管塑形弯曲数量;误差叠加:手工仿照 导管回弹 弯曲数量少;容易损伤导管等等。
7.(2)基于算法模拟导管弯曲形状,基于该模型,比对图像或通过3d打印输出后的实体,对塑形针进行弯折,再重复(1)的操作(相关专利申请号:201710628619,2017106494831)
8.(3)通过辅助塑形模具塑形(相关专利申请号:2018105592329,2018102200994,2016102897044)。将微导管穿入模具固定后进行高温熏蒸塑形。
9.现有技术中,方法(1)非常依赖经验判断,不同医生操作效果差异很大;方法(2)若不进行打印,比对操作弯折塑形针难度和误差都较大,3d打印后误差减小,但仍存在误差,
与算法误差叠加后,手术效果难以保证,算法生成的形状与医生操作习惯不同也会导致手术难度增加;方法(3)避免了上述两种方式的误差,塑形结果直观,但现有模具制备方法,均难以放入并将微导管固定在理想的位置。因此,亟需研发出一种准确、稳定且简便的动脉瘤介入手术微导管塑形的制作方法。
技术实现要素:
10.为克服上述现有技术的缺陷,本发明提供一种动脉瘤介入手术微导管塑形辅助模具及其制作方法。
11.本发明的技术方案包括:
12.本发明第一方面提供一种动脉瘤介入手术微导管塑形辅助模具,其特征在于,包括透明的模具主体,在该模具主体内部设置有与沿动脉轴线延伸的载瘤动脉完全吻合的内部空间,所述载瘤动脉上的动脉瘤位于所述的内部空间内,该内部空间用于置入微导管,在接近动脉瘤处的模具主体上设置有用于穿过微导管的孔洞,所述孔洞的直径设置大于塑形的微导管直径0.05mm-0.2mm;在该模具主体上,设置有一与外界连通的开槽,所述开槽配置为允许微导管侧向置入所述内部空间。
13.在一些优选的实施例中,其特征在于,所述模具主体形成为沿动脉轴线延伸的管状,具有近端和远端,所述开槽从所述近端连续延伸到所述远端。
14.在一些优选的实施例中,其特征在于,所述开槽围绕所述动脉轴线形成为螺旋状。
15.在一些优选的实施例中,其特征在于,所述的模具主体的材质为光敏树脂,通过3d打印得到。
16.本发明另一方面提供一种动脉瘤介入手术微导管塑形辅助模具的制作方法,其特征在于,包括以下步骤:
17.s1、造影:通过造影获得病灶动脉瘤及载瘤动脉影像在内的血管影像原始数据包a01;
18.s2、3d重建:利用3d重建软件,对原始数据包进行建模,获得3d数学模型b01;
19.s3、模具加工:利用3d建模软件,对3d数学模型b01进行加工生成塑形模具文件c01;
20.s4、3d打印和处理:使用打印机,选用透明、可耐受100℃高温不形变且不释放有毒物质光敏树脂,使用打印机自带切片软件,对塑形模具文件c01的可打印模型g01进行增加支撑和切片处理,切片厚度0.05-0.1mm,并导入打印机列印;印制完成后,使用清洗剂进行清洗,并进行加温后固化,去除支撑并对尖锐部位进行打磨,得到模具主体e01;
21.s5、微导管置入并塑形:
22.5-1、对微导管进行消毒后,将微导管沿着开槽侧向放入模具主体内,远端从孔洞伸出,根据动脉瘤的顶颈距调节伸出长度,确保模具主体的远端固定在动脉瘤解剖学中心;
23.5-2、推拉微导管,使微导管走向贴合模具主体的弯曲处切线;将微导管和模具主体固定好进行加热塑形;
24.在所述的步骤5-2中,所述的模具主体的弯曲处不小于五处。
25.在一些优选的实施例中,其特征在于,所述的步骤s3具体为:
26.3-1、筛选动脉瘤及近端载瘤动脉,载瘤动脉长度大于等于3cm,对因扫描出现的毛
刺噪点进行平滑处理,生成模型d01,
27.3-2、按需将动脉瘤的瘤体直径的1/2-1/3或全部去除,暴露动脉瘤的解剖学中心或附近位置,得到模型e01,模型e01均匀生成具有一定厚度的外壳f01,最终输出可打印模型g01。
28.在一些优选的实施例中,在所述的步骤3-2中,结合模型e01,制备具有一定厚度的外壳f01,外壳厚度根据打印材料韧性和透明度确定,不小于0.5mm,不大于0.1mm;在外壳f01的动脉瘤或瘤颈处,根据微导管塑形需求开孔,孔直径设置大于塑形导管直径范围0.05mm~0.2mm。
29.在一些优选的实施例中,其特征在于,对于外壳f01,沿载瘤动脉的走向开槽,保持从近端到远端的连续开放,开槽呈螺旋状弯曲,并经过血管瘤对侧血管壁,便于微导管置入;开槽避免经过血管弯曲的突出部位,以防微导管弹出,在所述微导管的外围均匀开设有直径为0.5-1mm的透气孔,加速蒸汽或热水通过;当载瘤动脉长度过短时,在近端增加1-3cm长的手柄便于加热时的夹持固定;最终输出可打印模型g01。
30.本发明透气孔的设置,一是能够释放打印后辅助模具弯曲引起的部分应力,防止长时间模具内应力集中引起的模具的变形进而影响其寿命及塑形准确性;二是在后续加热塑形工序中使微导管与模具内壁部分挥发物通过透气孔及时排出,不影响塑形效果。
31.在一些优选的实施例中,其特征在于,所述的步骤s1采用数字减影血管造影。
32.在一些优选的实施例中,其特征在于,在所述的步骤s4中,所述的有机溶剂为无水酒精或异丙醇,固化温度为80-100℃,固化时间1分钟,或放置于阳光干燥处6-8小时。
33.在一些优选的实施例中,其特征在于,在所述的步骤s5中,加热塑性的具体步骤为:80度以上热水浴10-30秒后置于冷水降温定型;或水蒸气熏蒸10-30秒后置冷水降温定型。
34.相对现有技术(例如2018105592329,2018102200994,2016102897044),本发明的优点包括:
35.1、支持复杂形状塑形本发明可按需进行5个以上弯曲,显著增加导管放置的稳定性和准确性。
36.2、快速直观:本发明外观透明或半透明,可直接观察导管在模具内部的状态,可调整指导达到符合医生习惯的形状。
37.3、可操作:开槽让微导管放置变得非常容易,相比从近端插入经过若干迂曲,更快速到达动脉瘤内部。
38.4、准确复刻:透气孔的设置,能够释放打印后辅助模具弯曲引起的部分应力,防止长时间模具内应力集中引起的模具的变形进而影响其寿命及塑形准确性;同时在后续加热塑形工序中使微导管与模具内壁部分挥发物通过透气孔及时排出,不影响塑形效果。
附图说明
39.图1是本发明的3d数学模型构建的之一结构示意图。
40.图2是本发明的3d数学模型构建的另一结构示意图。
41.图3是本发明动脉瘤及近端载瘤动脉的结构示意图。
42.图4是本发明模型d01的其中一结构示意图。
43.图5是本发明模型e01的另一结构示意图。
44.图6是本发明模型外壳f01的结构示意图。
45.图7是本发明模型增加支撑和切片处理后的结构示意图。
46.图8是本发明模型开孔后的结构示意图。
47.图9是本发明模型开槽后的结构示意图。
48.图10是图9设置有透气孔后的结构示意图。
49.图11是本发明打印机列印的结构示意图。
50.图12是本发明微导管置于本发明模型塑形时的结构示意图。
具体实施方式
51.下面结合具体实施例来进一步描述本发明,本发明的优点和特点将会随着描述而更为清楚。但这些实施例仅是范例性的,并不对本发明的范围构成任何限制。本领域技术人员应该理解的是,在不偏离本发明的精神和范围下可以对本发明技术方案的细节和形式进行修改或替换,但这些修改和替换均落入本发明的保护范围内。
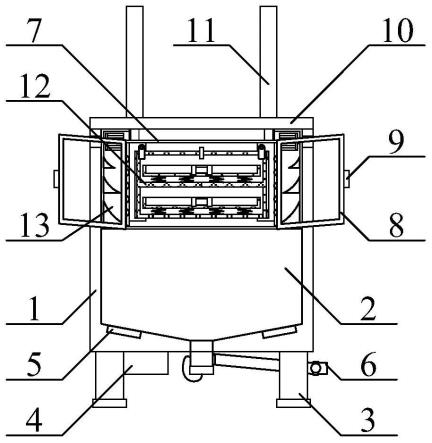
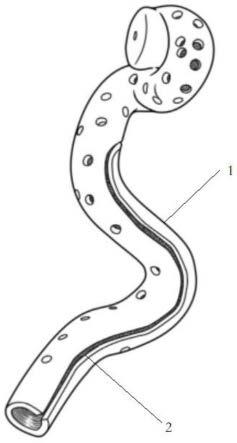
52.本发明动脉瘤介入手术微导管塑形辅助模具的3d数学模型的结构示意图,如图1所示。需要注意的是,图1仅是本发明众多动脉瘤介入手术微导管塑形辅助模具的模型之一,根据实际的具体需要,完全可以在制作过程设定具体的工艺及参数,满足需要,例如弯曲部的个数,开孔直径以及开槽的宽度等等。参见图1,动脉瘤介入手术微导管塑形辅助模具主体1,区别于现有技术结构不同的是,含有一个开槽2,开槽的目的是为了允许微导管侧向置入所述内部空间。在模具主体1内部设置有与沿动脉轴线延伸的载瘤动脉完全吻合的内部空间,所述载瘤动脉上的动脉瘤位于所述的内部空间内,该内部空间通过开槽2用于置入微导管;同时在接近动脉瘤处的模具主体1上设置有用于穿过微导管的孔洞,所述孔洞的直径比被塑形的微导管直径大,考虑到穿过微导管时方便以及放置后动脉与介入导管的相适相容性,优选孔洞直径比微导管直径大0.05mm-0.2mm。图2为本发明的3d数学模型另一结构示意图,该模型具有不同的弯曲部以及开槽位置。
53.本发明动脉瘤及近端载瘤动脉的结构示意图,如图3所示。明显看出,载瘤动脉的构造结构的复杂性,具有多处弯曲处以及表面突起的部位,同时在动脉的远端分布有瘤体肿块。本发明的动脉瘤介入手术微导管塑形辅助模具就是为了让微导管与动脉及瘤构造尽量一致,从而设计出的辅助塑形工具。
54.图4至图11,示意地表示了本发明涉及一种动脉瘤介入手术微导管塑形辅助模具制作各阶段的模型结构。
55.本发明模具主体的材质优选为光敏树脂,通过3d打印得到。模具加工:利用3d建模软件,对构建好的3d数学模型b01进行加工生成塑形模具文件c01,然后通过扫描筛选动脉瘤及近端载瘤动脉,生成模型d01,结构如图4所示。
56.根据按需瘤体的瘤体直径的1/2-1/3或全部去除,暴露动脉瘤的解剖学中心或附近位置,得到模型结构e01,结构如图5所示。
57.使用打印机自带切片软件,对塑形模具文件的可打印模型进行增加支撑和切片处理,切片厚度0.05-0.1mm,结构如图6所示。将图6的模型结构导入打印机列印。
58.在上述模型的基础上,生成具有一定厚度的外壳f01,结构如图7所示。外壳厚度根
据打印材料韧性和透明度确定,不小于0.5mm,不大于0.1mm。
59.在外壳f01的动脉瘤或瘤颈处,根据微导管塑形需求开孔,孔直径大于塑形导管的直径范围为0.05mm~0.2mm,结构示意图如图8所示。最终输出可打印模型g01。
60.对于外壳f01,沿载瘤动脉的走向开槽,结构示意图如图9所示。开槽经过血管瘤对侧血管壁,便于微导管置入;开槽避免经过血管弯曲的突出部位,以防微导管弹出。
61.在所述微导管塑形模具的外围均匀开设有直径为0.5-1mm的透气孔,结构示意如图10所示,以便加速蒸汽或热水通过;当载瘤动脉长度过短时,在近端增加1-3cm长的手柄便于加热时的夹持固定。
62.最终输出可打印模型,印制完成后,使用与树脂匹配的清洗剂进行清洗,并进行加温后固化,去除支撑并对尖锐部位进行打磨,得到的具体模具结构示意图为图11所示。
63.本发明微导管置于本发明模型塑形时的结构示意图如图12所示,可以看出微导管与本发明辅助模具相适性好:该模具主体上,沿载瘤动脉内的血流走向,设置有一与外界连通的开槽,还可以沿血管轴心盘旋开槽,避免微导管在制备过程中弹出。根据需要,塑形固定时进行加热、降温等操作。
64.以下是本发明实施例的具体操作工艺和参数的披露。
65.实施例1:
66.一种制备动脉瘤介入手术微导管塑形辅助模具的方法,其特征在于,包括以下步骤:
67.s1、造影:通过造影获得病灶动脉瘤及载瘤动脉影像在内的血管影像原始数据包a01;
68.s2、3d重建:利用3d重建软件,对原始数据包进行建模,获得3d数学模型b01;;
69.s3、模具加工:利用3d建模软件,对3d数学模型b01进行加工生成塑形模具文件c01;
70.s4、3d打印和处理:使用打印机,选用透明、可耐受100℃高温不形变且不释放有毒物质光敏树脂,使用打印机自带切片软件,对塑形模具文件c01的可打印模型g01进行增加支撑和切片处理,切片厚度0.05-0.1mm,并导入打印机列印;印制完成后,使用与树脂匹配的清洗剂进行清洗,并进行加温后固化,去除支撑并对尖锐部位进行打磨,得到模具e01。
71.s5、微导管置入并塑形:
72.5-1、对微导管进行消毒后,将微导管沿着开槽放入模具主体内,远端从孔洞伸出,根据动脉瘤顶颈距调节伸出长度,确保远端固定在动脉瘤解剖学中心;
73.5-2、推拉微导管,使微导管走向贴合模具主体的弯曲处切线;将微导管和模具主体固定好进行加热塑形。
74.所述的步骤s3具体为:
75.3-1、筛选动脉瘤及近端载瘤动脉,载瘤动脉长度大于等于3cm,对因扫描出现的毛刺噪点进行平滑处理,生成模型d01;
76.3-2、按需瘤体的瘤体直径的1/2-1/3或全部去除,暴露动脉瘤的解剖学中心或附近位置,得到模型e01,模型e01均匀生成具有一定厚度的外壳f01,最终输出可打印模型g01。
77.在所述的步骤3-2中,结合模型e01,制备具有一定厚度的外壳f01,外壳厚度根据
打印材料韧性和透明度确定,不小于0.5mm,不大于0.1mm;在外壳f01的动脉瘤或瘤颈处,根据微导管塑形需求开孔,孔直径设置大于塑形导管直径范围0.05mm~0.2mm。
78.对于外壳f01,沿载瘤动脉的走向开槽,开槽经过血管瘤对侧血管壁,便于微导管置入;开槽避免经过血管弯曲的突出部位,以防微导管弹出,在所述微导管的外围均匀开设有直径为0.5-1mm的透气孔,加速蒸汽或热水通过;当载瘤动脉长度过短时,在近端增加1-3cm长的手柄便于加热时的夹持固定;最终输出可打印模型g01。
79.所述的步骤s1采用数字减影血管造影。
80.在所述的步骤5-2中,所述的模具主体的弯曲处不小于五处。
81.在所述的步骤s4中,所述的有机溶剂为无水酒精或异丙醇,固化温度为80-100℃,固化时间1分钟。
82.在所述的步骤s5中,加热塑性的具体步骤为:80度以上热水浴10-30秒后置于冷水降温定型。
83.实施例2:
84.一种制备动脉瘤介入手术微导管塑形辅助模具的方法,其特征在于,包括以下步骤:
85.s1、造影:通过造影获得病灶动脉瘤及载瘤动脉影像在内的血管影像原始数据包a01;
86.s2、3d重建:利用3d重建软件,对原始数据包进行建模,获得3d数学模型b01;;
87.s3、模具加工:利用3d建模软件,对3d数学模型b01进行加工生成塑形模具文件c01;
88.s4、3d打印和处理:使用打印机,选用透明、可耐受100℃高温不形变且不释放有毒物质光敏树脂,使用打印机自带切片软件,对塑形模具文件c01的可打印模型g01进行增加支撑和切片处理,切片厚度0.05-0.1mm,并导入打印机列印;印制完成后,使用与树脂匹配的清洗剂进行清洗,并进行加温后固化,去除支撑并对尖锐部位进行打磨,得到模具e01。
89.s5、微导管置入并塑形:
90.5-1、对微导管进行消毒后,将微导管沿着开槽放入模具主体内,远端从孔洞伸出,根据动脉瘤顶颈距调节伸出长度,确保远端固定在动脉瘤解剖学中心;
91.5-2、推拉微导管,使微导管走向贴合模具主体的弯曲处切线;将微导管和模具主体固定好进行加热塑形。
92.所述的步骤s3具体为:
93.3-1、筛选动脉瘤及近端载瘤动脉,载瘤动脉长度大于等于3cm,对因扫描出现的毛刺噪点进行平滑处理,生成模型d01,
94.3-2、按需瘤体的瘤体直径的1/2-1/3或全部去除,暴露动脉瘤的解剖学中心或附近位置,得到模型e01,模型e01均匀生成具有一定厚度的外壳f01,最终输出可打印模型g01。
95.在所述的步骤3-2中,结合模型e01,制备具有一定厚度的外壳f01,外壳厚度根据打印材料韧性和透明度确定,不小于0.5mm,不大于0.1mm;在外壳f01的动脉瘤或瘤颈处,根据微导管塑形需求开孔,孔直径为大于微导管直径范围0.05mm~0.2mm。
96.对于外壳f01,沿载瘤动脉的走向开槽形成模型f03,开槽经过血管瘤对侧血管壁,
便于微导管置入;开槽从近端到远端连续开放,呈螺旋状或适度弯曲,避免经过血管弯曲的突出部位,以防微导管弹出;在所述微导管的外围均匀开设有直径为0.5-1mm的透气孔,加速蒸汽或热水通过;当载瘤动脉长度过短时,在近端增加1-3cm长的手柄便于加热时的夹持固定;最终输出可打印模型g01。
97.所述的步骤s1采用数字减影血管造影。
98.在所述的步骤5-2中,所述的模具主体的弯曲处不小于五处。
99.在所述的步骤s4中,所述的有机溶剂为无水酒精或异丙醇,固化时,放置于阳光(夏季)干燥处6-8小时。
100.在所述的步骤s5中,加热塑性的具体步骤为水蒸气熏蒸10-30秒后置冷水降温定型。
101.基于以上步骤,本发明支持复杂形状塑形本发明可按需进行5个以上弯曲,显著增加导管放置的稳定性和准确性。
102.本发明外观透明或半透明,可直接观察导管在模具内部的状态,可调整指导达到符合医生习惯的形状。
103.可操作:连续开放的开槽让微导管放置变得非常容易,相比从近端插入经过若干迂曲,更快速到达动脉瘤模具内部,盘旋状开槽避免微导管置入后弹出。
104.以上所述,仅为本发明较佳的具体实施方式,但本发明的保护范围并不局限于此,任何熟悉本技术领域的技术人员在本发明揭露的技术范围内,根据本发明的技术方案及其发明构思加以等同替换或改变,都应涵盖在本发明的保护范围之内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。