1.本发明涉及一种茶叶提取物组合物的制备方法以及相应的应用。
背景技术:
2.茶叶,作为中国历史传统的一部分,具有悠久的文化,作为一种保健饮品,茶叶已经应用到各个领域,比如饮料、保健品等。
3.茯茶是一种以黑毛茶为原料,通过筛分、汽蒸、渥堆、称茶、蒸茶、压制、包装、发花、干燥等工艺制得的一种黑茶,因其加工中独特的”发花”工艺(真菌固体发酵)及与之形成的金黄色颗粒真菌(俗称“金花”)而成为微生物发酵茶中独具特色的黑茶种类。近年来,大量临床前以及临床研究的结果表明,茯砖茶在降血脂、降血糖、抗氧化等方面表现出广泛的药理活性,因此也受到了广大消费者的推崇。本文对近年来茯茶在药理活性方面的研究进行综述,以期为进一步探索研究茯砖茶提供思路,寻找突破口。
4.21世纪以来,随着生活水平的不断提升,肥胖及相关疾病发病率在全球范围内急剧增长。茶作为我国的一项传统饮品,具有消饮食、消积滞、消宿食等作用。元代昊瑞《日用本草》中就有“除烦止渴、解腻清神”的记载。而茯茶、普洱这类黑茶,多为以肉类、奶类为主食的少数民族饮用,这说明茯茶是具有帮助消化与调节脂肪代谢的功效。茶叶提取的成分中,包括茶多酚、茶单宁等。其具有抗氧化的作用。茯砖茶是以黑毛茶作为原料,经过筛分、汽蒸、沤堆、压制、发花和干燥等工序加工而成的一种黑茶,其提取物的应用研究,在国内并不多见。尤其在食品、药品或保健品等功能性应用领域,目前还存在许多的空白,特别是对于降低体内嘌呤,缓解痛风等症状尚未有相关报道。痛风是多基因、多因素作用的疾病,仅使用单一治疗靶点的化药难以达到良好的治疗效果,中医药多成分、多靶点的特点使其在抗痛风领域具有独特优势,但其背后的相关药理机制尚不明确,限制了其临床应用和推广。
5.由于不良的饮食生活习惯导致近年来痛风患者逐年增长,临床对于抗痛风治疗手段多以化药为主,但仍存在盲区与不足,临床需求迫切。近年来,国内外对于痛风领域的研究越来越受到重视,在痛风的病理研究、药物的开发与选择以及治疗方案优化等方面,国外的研究较为全面,也更加重视以及与临床实践的结合。
6.痛风主要可以分为四个阶段:无症状高尿酸血症期(无msu沉积)、无症状msu晶体沉积期(无痛风性关节炎发作)、急性发作期和慢性痛风性关节炎期。
7.当痛风急性发作时,西药常规治疗的首选药物是非甾体类抗炎药物(nsaids),此类药物容易造成胃肠道的不良反应;对nsaids有禁忌的患者可以服用低剂量的秋水仙碱(英文名colchicine目前临床抗痛风的一线用药),有效且发生胃肠道不良反应的几率较低,但依然会导致一些不良副反应;对于前两者均不适用的患者则可以选择短期单独服用糖皮质激素。对常规治疗无效且症状严重的患者可以考虑使用白介素1(il-1)抑制剂的非常规疗法。
技术实现要素:
8.本发明的第一目的在于提供一种茶叶提取物组合物,用于制备降低人体对嘌呤含量、缓解或治疗痛风的食品、保健品或药品的应用,用于制备阻止、减少或降低人体对嘌呤摄入或吸收的食品、药品或保健品中的应用,以及用于制备缓解或者治疗痛风的食品、药品或保健品中的应用。
9.本发明公开的一种茶叶提取物组合物,含有至少以下两种成分:儿茶素、茶多酚、茶多糖、茶色素、没食子酸和/或其衍生物、氨基酸、生物碱、化合物a。
10.其中所述的组合物含有化合物a,所述的化合物a的分子工如下:
[0011][0012]
所述的化合物a的含量为0.0001-1%,优选为0.0001-0.1%,更优选为0.0001-0.01%,更优选为0.0001-0.001%。
[0013]
如上的组合物,其中所述的组合物中含有茶多酚,其含量为0.01%-80%,优选为30-80%,更优选为40-60%。
[0014]
如上所述的组合物,其中所述的组合物中含有茶多糖,其含量为20%以下或0.01%-30%,优选为0.1-20%。
[0015]
如上所述的组合物,其中所述的组合物中含有没食子酸,其含量为5%以下,优选为3%以下。
[0016]
如上所述的组合物,其中所述的组合物中含有氨基酸,其含量为10%以下,优选为6%以下。
[0017]
如上所述的组合物,其中所述的组合物中含有儿茶素,其含量为0.01%-60%,优选为30-50%。
[0018]
如上所述的组合物,其中所述的组合物中含有没食子酸,其含量为5%以下,优选为3%以下。
[0019]
如上所述的组合物,其中所述的组合物中含有茶色素,其含量为0.01%-40%,优选为0.1-30%。
[0020]
如上所述的组合物,其中所述的组合物含有其它辅料的提取物,所述的其它辅料包括紫苏、青蒿、薄荷叶、红花、玫瑰、丁香、小茴香、甘草、干姜、姜黄、甜菊叶、灵芝、陈皮其中之一或任何两种或两种以上的混合。
[0021]
如上所述的组合物,本发明公开了其在制备一种降嘌呤的食品、药品或保健品中的应用。
[0022]
如上所述的组合物,本发明公开其在制备一种阻止或减少人体对嘌呤吸收的食品、药品或保健品中的应用。
[0023]
如上所述的组合物,本发明公开了其在制备一种增强人体嘌呤排泄的食品中的应用。
[0024]
如上所述的茶叶提取物组合物,含有茯茶素a。
[0025]
所述的茶叶提取物组合物制备来源的茶叶或原料包括茯茶、茯砖茶、散茯茶,或者含有茯茶素/冠突散囊菌的茶叶。
[0026]
茶叶提取组合物添加常规的辅助成分后可以制备为提取物混合物,具体应用可以是药品、食品和/或保健品,其状态可以为液体、胶状物、乳化物或者膏状物、固状物。提取物混合物含有的茶叶提取物组合物,以干基质量计,至少为100mg/kg,优选为1500mg/kg、200mg/kg,最优选为300mg/kg。
附图说明
[0027]
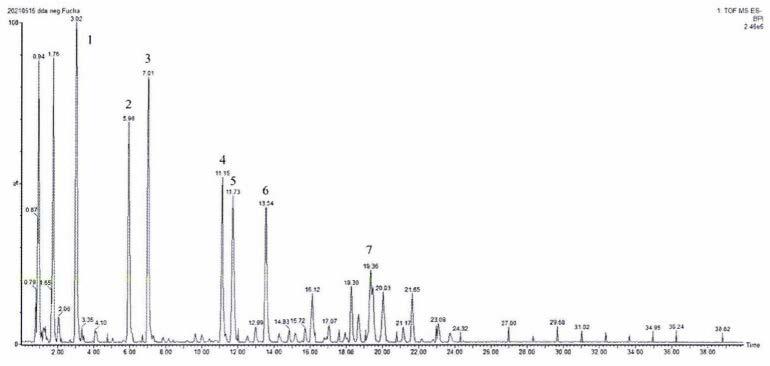
图1制备例1的分析检测图。
[0028]
图2三组溶液的色差对比图。
[0029]
图3三组溶液的吸收曲线图。
[0030]
图4各组大鼠右踝关节内侧注射msu前(0h)及注射后(4、8、24、48h)肿胀程度实拍图。
[0031]
图5大鼠右踝关节肿胀指数经时变化(0-8h)。
[0032]
图6大鼠右踝关节肿胀指数经时变化(0-48h)。
具体实施方式
[0033]
本发明中,术语“含有”或“包括”表示各种成分可一起应用于本发明的混合物或组合物中。因此,术语“主要由
…
组成”和“由
…
组成”包含在术语“含有”或“包括”中。
[0034]
如本文内容中的比例、百分含量等数值,如无说明,均指重量比或重量百分比。茶叶提取物组合物在计算百分含量时,以干基质量计算,另有说明除外。
[0035]
本发明的各方面的详细内容:
[0036]
茶叶
[0037]
所述的茶叶提取物组合物,其制备的茶叶来源,包括符合国家标准、行业标准或企业标准的各种的茶叶。所述的标准包括:gb/t30766-2014《茶叶分类》、gb/t32719.1-2016《黑茶第1部分:基本要求》、部分:基本要求》、gb/t32719.2-2016《黑茶第2部分:花卷茶》、gb/t32719.3-2016《黑茶第3部分:湘尖茶》、gb/t32719.4-2016《黑茶第4部分:六堡茶》、gb/t 32719.5-2018《黑茶第5部分:茯茶》、gh/t 1246-2019《茯茶加工技术规范》、gb/t9833.3-2013《紧压茶第3部分:茯砖茶》。
[0038]
在本发明的一个具体实施例中,所述的茶叶通过以下工艺制备得到:以黑毛茶为主要原料,经过毛茶筛分、半成品拼配、渥堆、汽蒸、发花、干燥、检验、成品包装等工艺生产的散状黑茶产品,或以黑毛茶为原料经过毛茶筛分、半成品拼配、渥堆、汽蒸、压制成型、发花、干燥、检验、成品包装等工艺制成的紧压黑茶产品。本发明的实施例中的茶叶仅为举例说明使用,并不作为本发明的具体限定。
[0039]
所述的茶叶提取物组合物的制备工艺,包括传统的水提和/或醇提步骤。优选的,采用去离子水进行浸泡和/和提取,或者电解水进行浸泡和/和提取;优选的,采用乙醇进行浸泡和/和提取。
[0040]
所述的茶叶提取物组合物的制备工艺,包括过滤步骤,优选的,所述的过滤步骤采用特殊粒径的过滤膜进行过滤,所述的过滤膜包括但不限于陶瓷膜、过滤布等。
80%,优选为30-70%,更优选为40-60%。
[0057]
在本发明的一个具体实施方式中,所述的组合物中含有茶多糖,其含量为0.01%-30%,优选为0.1-20%。
[0058]
在本发明的一个具体实施方式中,所述的组合物中含有没食子酸和/或其衍生物,其含量为5%以下,优选为3%以下。
[0059]
在本发明的一个具体实施方式中,所述的组合物中含有氨基酸,其含量为10%以下,优选为6%以下。
[0060]
在本发明的一个具体实施方式中,所述的组合物中含有茶色素,其含量为0.01%-40%,优选为0.1-30%,更优选为0.1-5%。
[0061]
在本发明的一个具体实施方式中,所述的组合物中含有儿茶素,其含量为0.01%-60%,优选为0.1-50%,更优选为20-50%。
[0062]
在本发明的一个具体实施方式中,所述的组合物中含有生物碱,其含量为20%以下,优选为0.1-10%。
[0063]
在本发明的一个具体实施方式中,所述的儿茶素的含量为20-60%,优选为25-60%。
[0064]
在本发明的一个具体实施方式中,所述的儿茶素的含量为20-60%,优选为25-60%。
[0065]
在本发明的一个具体实施方式中,所述的儿茶素选自egcg(表没食子儿茶素没食子酸酯,分子式为c22h18o11)。
[0066]
在本发明所述的儿茶素包括类儿茶素化合物。
[0067]
在本发明的一个具体实施方式中,所述的生物碱选自咖啡因、可可碱,优选为咖啡因。
[0068]
在本发明的一个具体实施方式中,所述组合物中,化合物a的含量为10-6
%以上但低于1%,优选10-6
%-0.1%所述的儿茶素与茶多糖的比例为:1~10∶1,优选为(2~8)∶1。
[0069]
在本发明的一个具体实施方式中,所述组合物中,儿茶素与茶多糖的所述的儿茶素与茶多糖的比例为:1~10∶1,优选为(2~8)∶1。
[0070]
在本发明的一个具体实施方式中,以干基质量计,儿茶素百分含量为20~60%,茶多糖的比例为5~30%,含有茶色素、化合物a及其衍生物的含量为30%以下。
[0071]
在本发明的一个具体实施方式中,以干基质量计,儿茶素百分含量为20~60%,茶多糖的比例为5~30%,含有茶色素、咖啡因、化合物a及及其衍生物的含量为20%以下。
[0072]
在本发明的一个具体实施方式中,所述的茶叶提取物组合物来源于茯砖茶、茯茶或其类似物,其中冠突散囊菌≥20
×
104(cfu/g)。
[0073]
提取物混合物
[0074]
提取物混合物是由茶叶提取物组合物加入其它成分制备而成,提取物混合物含有茶叶提取物组合物。
[0075]
在本发明的一个具体实施方式中,以干基成分质量计,提取物混合物中,茶叶提取物组合物含量不低于100mg/kg,优选为不低于150mg/kg,更优选不低于250mg/kg、300250mg/kg,例如约100mg/kg、110mg/kg、120mg/kg、130mg/kg、140mg/kg、150mg/kg、160mg/kg、170mg/kg、180mg/kg、190mg/kg、200mg/kg、210mg/kg、220mg/kg、230mg/kg、
240mg/kg、250mg/kg、260mg/kg、270mg/kg、280mg/kg、290mg/kg、300mg/kg、310mg/kg、320mg/kg、330mg/kg、340mg/kg、350mg/kg、360mg/kg、370mg/kg、380mg/kg、390mg/kg、400mg/kg。由于其中茶叶提取物组合物的含量决定了其是否具备特定的功效,因此,提取物混合物中的有效成分含量需要控制在特定的范围内。
[0076]
在本发明的一个具体实施方式中,以干基成分质量计,提取物混合物中,茶多酚的含量不低于50mg/kg,优选不低于60mg/kg,更优选不低于70mg/kg,例如约:80mg/kg、90mg/kg、100mg/kg、110mg/kg、120mg/kg、130mg/kg、140mg/kg、150mg/kg、160mg/kg、170mg/kg、180mg/kg、190mg/kg、200mg/kg、210mg/kg、220mg/kg、230mg/kg、240mg/kg、250mg/kg、260mg/kg、270mg/kg、280mg/kg、290mg/kg、300mg/kg。
[0077]
在本发明的一个具体实施方式中,以干基成分质量计,提取物混合物中,儿茶素的含量不低于20mg/kg,优选不低于50mg/kg,更优选不低于60mg/kg,例如约:80mg/kg、90mg/kg、100mg/kg、110mg/kg、120mg/kg、130mg/kg、140mg/kg、150mg/kg、160mg/kg、170mg/kg、180mg/kg、190mg/kg、200mg/kg、210mg/kg、220mg/kg、230mg/kg、240mg/kg、250mg/kg、260mg/kg、270mg/kg、280mg/kg、290mg/kg、300mg/kg。
[0078]
所述的提取物混合物可选自食品、药品、保健品。
[0079]
在本发明的一个具体实施方式中,所述的提取物混合物中含有的茶多酚、儿茶素、茶多糖和/或化合物a,可由所述成分在茶叶提取物组合物中相应的比例折算。在本发明的一个具体实施方式中,以干基成分质量计,提取物混合物中,化合物a的含量高于10-4
mg/kg,非限制性例子为2
×
10-4
mg/kg、3
×
10-4
mg/kg、4
×
10-4
mg/kg、5
×
10-4
mg/kg、、6
×
10-4
mg/kg、7
×
10-4
mg/kg。
[0080]
制备方法
[0081]
本发明还提供了一种茶叶提取物组合物的制备方法或制备工艺。
[0082]
在本发明的一个具体实施方式中,所述的茶叶提取物组合物通过下述制备工艺得到,所述的制备工艺包括水提和/或醇提步骤。优选的,采用去离子水进行浸泡和/和提取,或者电解水进行浸泡和/和提取;优选的,采用乙醇进行浸泡和/和提取。
[0083]
在本发明的一个具体实施方式中,所述的茶叶提取物组合物通过下述制备工艺得到,所述的制备工艺包括在沸腾条件下,将原料与水进行浸泡和/和提取。
[0084]
在本发明的一个具体实施方式中,所述的茶叶提取物组合物通过下述制备工艺得到,所述的制备工艺包括冻干步骤,优选的,将茶叶提取物组合物制备为冻干粉。
[0085]
在本发明的一个具体实施方式中,所述的茶叶提取物组合物通过下述制备工艺得到,所述的制备工艺包括在对原料进行破碎或粉碎。
[0086]
在本发明的一个具体实施方式中,所述的制备工艺,包括对原料的浸泡液的液体与固体进行分离。
[0087]
在本发明的一个具体实施方式中,所述的茶叶提取物组合物通过下述制备工艺得到,所述的制备工艺包括对原料的浸泡液与固体进行分离。
[0088]
在本发明的一个具体实施方式中,所述的茶叶提取物组合物通过下述制备工艺得到,所述的制备工艺包括过滤步骤,优选的,所述的过滤步骤采用特殊粒径的过滤膜进行过滤,所述的过滤膜包括但不限于陶瓷膜、过滤布等。
[0089]
在本发明的一个具体实施方式中,所述的制备方法/制备工艺包括以下几个步骤:
[0090]
原料的筛选,所选用的茯砖茶或茯茶,其中冠突散囊菌要求≥20
×
104(cfu/g);优选的,对茯砖茶进行破碎或粉碎;更优选的,煮沸下将原料与液体进行混合或浸泡,将过滤液与固体分离,分离后的固体继续在液体煮沸下制备。
[0091]
具体的,非限定性例子为:称取原料,加入水浸泡,加热或加热至沸腾,然后过滤,优先为精密过滤。优选的,滤渣继续加入水加热或加热至沸腾然后过滤。合并两次滤液,浓缩冻干。最后打粉。分装后避光、4℃保存。
[0092]
在本发明的一个具体实施方式中,原料与水的重量比例为1∶(5~20),优选为1∶(7~12),例如约1∶6、1∶7、1∶8、1∶9、1∶10、1∶11、1∶12、1∶13、1∶14、1∶15、1∶16、1∶17。在本发明的一个优选实施方式中,第一次蒸煮的原料与水的比例小于第二次的比例。
[0093]
在本发明的一个具体实施方式中,所述的制备方法中的沸腾下至少0.5小时,优选为1小时,更优选为1.5小时,例如约0.5、0.6、0.7、0.8、0.9、1.0、1.1、1.2、1.3、1.4、1.5、1.6、1.7、1.8、1.9、2.0等。在本发明的一个优选实施方式中,第一次蒸煮的时间大于第二次蒸煮的时间。
[0094]
茶叶提取物组合物在制备食品、药品或保健品中的应用
[0095]
本发明中所述的组合物添加常规的辅料或成分后,可以用于制备提取物混合物。
[0096]
所述的提取物混合物可以选自食品、药品、保健品,其形态为液体、膏装物、泥状物和/或乳状物。在本发明的一个具体的实施方式中,所述的食品为块状。在本发明的一个优选的实施方式中,所述的食品为10-30克每份,更优选为20克。在本发明的一个优选的实施方式中,所述的食品饮料。在本发明的一个优选的实施方式中,所述的调味料。其可以提升食品的色泽、口感和香味,并且具备特别的保健功能,所述的食品,包括调料(或调味料)、煲汤料、火锅底料添加物中任意一种或其它类似物。本发明的组合物,在制备得到的食品中,同时,可以实现汤味香味更浓(具有提香作用)、色光透亮、不发浑、色泽不发黑、口感不发苦、口感不发涩,并且具备多种保健功能。在制备得到的食品如带汤的食品中,能够抑制泡沫的生成,特别是在加入火锅作为火锅底料使用时,香味更持久,其具备很好的耐煮性。由于前述的食品中,会产生或引入大量的嘌呤化合物,因此加入本发明所述的茶叶提取物组合物可以降低或降解嘌呤,进而使得阻止、减少或降低人体对嘌呤摄入或吸收。
[0097]
本发明的茶叶提取物组合物,可应用于制备食品、药品或保健品。
[0098]
所述的食品的非限制性例子为饮料、调味品、增味剂、保健品等。
[0099]
在本发明的一个具体实施方式中,公开了所述的茶叶提取物组合物在制备一种降低体内尿酸的食品、药品或保健品中的应用。
[0100]
在本发明的一个具体实施方式中,公开了所述的茶叶提取物组合物作为制备一种降低人体内嘌呤含量的食品、药品或保健品中的应用。
[0101]
在本发明的一个具体实施方式中,公开了所述的茶叶提取物组合物作为制备一种降血脂的食品、药品或保健品中的应用。
[0102]
在本发明的一个具体实施方式中,公开了所述的茶叶提取物组合物作为制备一种增强人体免疫力的食品、药品或保健品中的应用。
[0103]
在本发明的一个具体实施方式中,公开了所述的茶叶提取物组合物作为制备一种阻止、减少或降低人体对嘌呤摄入或吸收的食品、药品或保健品中的应用。所述的嘌呤包括次黄嘌呤。非限制性的例子为,本发明的组合物制备的食品中,与食品中产生的嘌呤进行反
centrifuge,美国beckman公司。
[0124]
uplc-pda-esi-qtof-ms分析方法:
[0125]
液相分离采用waters acquity beh c18色谱柱,柱温设定为40℃。流动相由0.1%的甲酸水(a)和0.1%甲酸-乙腈(b)组成,梯度程序如下:0-12min,5%-15%(b);12-20min,15%-30%(b);20-25min,30%-80%(b);25-27min,80%-5%(b);27-30min,5%(b)。流速为0.4ml/min。进样体积为2μl。
[0126]
质谱采用正离子与负离子两种模式采集,电喷雾原离子参数设置如下:
[0127]
脱溶剂气的流速为800l/h,温度为400℃,锥孔气的流速为50l/h,源温度设定为120℃,毛细管电压和锥孔电压分别设定为2500v和20v。使用dda裂解方式获得样品的二级质谱碎片,扫描时间为0.2s,裂解能量为20-50v。数据采集范围为50-1200da。
[0128]
仪器使用甲酸钠校正,并使用亮氨酸-脑啡肽进行实时校正。
[0129]
通过与对照品的保留时间、分子离子峰、特征碎片进行比对进行鉴定。
[0130]
下述的检测结果中,检测例编号分别对应相同编号的制备例,其成分与常规的茶泡水完全不同:
[0131]
检测例1中,鉴定出的部分化合物:其中黄酮类成分12个(化合物1-8,1.rutin芦丁、2.catechin儿茶素、3.l-epicatechin表儿茶素、4.(-)-epigallocatechin表没食子儿茶素、5.(-)-gallocatechin右旋没食子儿茶素、6.(-)-gallocatechin gallate没食子儿茶素没食子酸酯、7.(-)-epigallocatechin gallate(-)-表没食子儿茶素没食子酸酯、8.(-)-epicatechin gallate表儿茶素没食子酸酯)、酚类成分2个(化合物9、10:9.gallic acid没食子酸、pyrogallol没食子酚)、香豆素类成分1个(化合物11:11.5,7-dihydroxycoumarin香豆素)、生物碱类成分1个(化合物12:caffeine咖啡因),以及化合物a,部分化合物的定性图形见图1。经估算,类儿茶素的含量为48.0%,茶多糖的含量为9.7%,提取物成分(茶色素、化合物a及其衍生物、没食子酸及其衍生物、香豆素、生物碱)质量计30%以下,化合物a的含量为0.1%以下。
[0132]
检测例2中,鉴定出黄酮类成分、酚类成分、香豆素类成分、生物碱类成分、茯茶素a等。
[0133]
检测例3中,鉴定出黄酮类成分、酚类成分、香豆素类成分、生物碱类成分、茯茶素a等。
[0134]
检测例4中,鉴定出黄酮类成分、酚类成分、香豆素类成分、生物碱类成分、茯茶素a等。
[0135]
检测例5中,鉴定出黄酮类成分、酚类成分、香豆素类成分、生物碱类成分、茯茶素a等。
[0136]
效果检测例:
[0137]
效果例1:精密称取制备例1的提取物冻干粉,加纯水配制成5mg/ml水提取物。
[0138]
对照品溶液制备
[0139]
精密称取次黄嘌呤对照品,加1m氢氧化钠溶液溶解后,加纯水配制成2mg/ml次黄嘌呤母液。
[0140]
吸附实验:
[0141]
分别设置吸附组、制备例1组与次黄嘌呤组,方法如下:
[0142]
吸附组:制备例1水提取物160μl 次黄嘌呤母液25μl 纯水4815μl;
[0143]
茯茶组:制备例1水提取物160μl 纯水4840μl;
[0144]
次黄嘌呤组:次黄嘌呤母液25μl 纯水4975μl;
[0145]
三组溶液平行制备三份,100℃煎煮1h,冷却2h,离心(2000rpm,5min),取上清稀释3倍后进行全波长扫描检测。
[0146]
见图2:由图可知,次黄嘌呤与茯茶水提物混合后液体颜色加深,提示两者并非简单物理混合,表明次黄嘌呤与茯茶水提物中的成分发生反应。
[0147]
见图3中:蓝色拟合线为茯茶水提物与次黄嘌呤溶液全波长图叠加后的理论全波长特征,与实际检测得到的绿色全波长扫描图比较可知,两者结合后全波长特征与拟合线不同,表明茯茶提取物可影响次黄嘌呤紫外光谱,提示两者之间发生相互作用。且肉眼可见的,从混合后的颜色角度,可以看出三组颜色有明显的不同。
[0148]
制备例2-5的结果与图2-图3的结论相同或实质相似。由前面的实验例可以证明,由于本发明的茶叶提取组合物能够降低次黄嘌呤的含量,也意味着可以降低体内的次黄嘌呤的含量,用于缓解或治疗痛风症状。
[0149]
体内药效实验例:尿酸钠(msu)制备大鼠痛风性关节炎模型
[0150]
【动物、试剂与材料】
[0151]
50只雄性sd大鼠,清洁级,150-180g。
[0152]
msu结晶购于sigma公司,保存于无菌条件下。实验前,用0.9%无菌生理盐水配制成msu混悬液(100mg/ml)。
[0153]
茯茶提取物为制备例制备,秋水仙碱购于sigma公司。
[0154]
茯茶提取物与秋水仙碱,用无菌生理盐水配制,给药剂量100mg/kg、300mg/kg。
[0155]
【造模及给药方法】
[0156]
实验大鼠分为五组,适应性喂养约3天后开始实验
[0157]
正常组10只:正常饲养
[0158]
模型组10只:生理盐水连续灌胃14天,于第12天在大鼠右后踝关节单次注射50μl msu混悬液。
[0159]
低剂量给药组10只:制备例1制备的茯茶提取物水溶液(100mg/kg)连续灌胃给药14天。于第12天在大鼠右后踝关节单次注射50μl msu混悬液。
[0160]
高剂量给药组10只:制备例1制备的茯茶提取物水溶液(300mg/kg)连续灌胃给药14天。于第12天在大鼠右后踝关节单次注射50μl msu混悬液。
[0161]
阳性药组10只:秋水仙碱0.6mg/kg连续灌胃给药14天。于第12天在大鼠右后踝关节单次注射50μl msu混悬液。
[0162]
关节肿胀外观及肿胀指数:
[0163]
用缚线法测量造模前和造模后第4,8,24,48小时大鼠右踝关节同一部位的周径,计算肿胀指数,考察关节肿胀程度的经时变化。并拍摄关节外观图片,见图4。
[0164]
图5:为大鼠右踝关节肿胀指数经时变化(0-8h)大鼠右脚踝注射msu(5mg)后,分别在2,4,6,8h四个时间点测量踝关节大小,得出肿胀指数,肿胀指数计算方式为(致炎后踝关节周径-致炎前踝关节周径)/致炎前踝关节周径。实验结果以平均值
±
标准误表示,每组n=6。采用graphpad prism 8.0软件进行统计学分析。采用two-way anova法(双因
素方差分析)。*p<0.05为具有统计学差异,**p<0.01为有显著性统计学差异,***p<0.001为有极其显著的统计学差异。
[0165]
图6:大鼠右踝关节肿胀指数经时变化(0-48h)大鼠右脚踝注射msu(5mg)后,分别在2,4,6,8,24,48h等时间点测量踝关节大小,得出肿胀指数,肿胀指数计算方式为(致炎后踝关节周径-致炎前踝关节周径)/致炎前踝关节周径。实验结果以平均值
±
标准误表示,每组n=6。采用graphpad prism 8.0软件进行统计学分析。采用two-way anova法(双因素方差分析)。*p<0.05为具有统计学差异,**p<0.01为有显著性统计学差异,***p<0.001为有极其显著的统计学差异。
[0166]
由图可以看出,当使用100mg/kg的茶叶提取物时,具有明显的缓解痛风症状的效果,当用量高于100mg/kg时,效果呈线性增长。当200mg/kg时,根据机理分析,具有较佳的效果。当300mg/kg时,可以实现更快速的治疗效果,与传统的秋水仙碱相比具有几乎相同的效果,且本发明采用的茶叶提取物,没有秋水仙碱带来的副效果或人体副反应。
[0167]
实验结论:由上述可以看出茯茶提取物可减轻大鼠等哺乳动物踝关节炎性肿胀,而制备例2-5基本成分一致,因此效果相同或相近。
[0168]
在本发明提及的所有文献都在本技术中引用作为参考,就如同每一篇文献被单独引用作为参考那样。此外应理解,在阅读了本发明的上述内容之后,本领域技术人员可以对本发明作各种改动或修改,这些等价形式同样落于本技术所附权利要求书所限定的范围。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。