药物涂层球囊
1.相关申请的交叉引用
2.本技术要求2020年5月22日提交的临时申请第pct/us2020/034279号的权益,该临时申请通过引用全文纳入本文用于所有目的。
技术领域
3.本公开一般涉及药物涂层球囊,更具体地涉及药物涂层球囊系统,其中药物涂层不包括赋形剂。
背景技术:
4.血管疾病,例如动脉粥样硬化、动脉闭塞和再狭窄,是人类死亡和发病的主要原因。血管疾病的起因很多,在一些情况下必须进行手术或血管内介入治疗。血管系统的创伤还可能需要外科手术干预来治疗受伤组织。通常优选在局部而非全身水平治疗血管疾病。与药物局部施用于靶组织以治疗血管疾病相比,全身施用药物可产生不希望的副作用。药物涂层血管内医疗装置的使用已成为治疗血管疾病的标准技术。特别地,血管疾病的常见治疗是组织与血管内医疗装置(例如球囊或支架)的短期或长期接触,所述血管内医疗装置涂覆有预防或减少接触部位处血管疾病的药物。包括基于导管的球囊的血管医疗装置的短期接触通常用于治疗血管疾病和血管创伤,而长期接触,例如血管内医疗装置的植入,包括血管移植物、支架移植物和支架的植入。在血管内医疗机械与患病的血管组织接触后,药物从血管内医疗装置洗脱到接触部位的周围组织,从而以局部而非全身的水平治疗血管疾病。
5.药物涂层球囊(dcb)是药物涂覆的血管内医疗机械的一个实例。该文献公开了dcb用于治疗血管疾病,包括冠状动脉疾病和外周动脉疾病的用途(参见例如dror等人的美国专利第5,102,402号)。dror等人公开了将dcb置于血管管腔中以治疗血管壁,使球囊膨胀,并使球囊表面与管腔壁接触以将药物递送到血管壁中。使用dcb将药物给药至治疗部位在植入或展开后可能立即变得高度可变且不可预测,并且血管组织中的局部药物水平可能在长时间内高度可变且不可预测。因此,需要具有改进的用于治疗血管疾病的dcb和技术,其在药物给药中是可靠且可重复的。
6.为了改进用于治疗血管疾病的常规dcb和技术,dcb可以由一层或多层材料构成,所述材料被选择以提供某些性质,从而根据应用以某种特定方式优化dcb的性能。在多层或复合球囊的情况下,复合材料内的多个层可以是不同的材料,以获得物理和/或化学性质的混合从而优化性能。cully等人的美国专利申请公开第2016/0106961号公开了复合或分层dcb。所述复合材料可包括粘附到可吹塑聚合物上的多孔层,例如包含膨胀含氟聚合物层的复合材料,所述膨胀含氟聚合物层通过拉伸吹塑工艺粘附到可吹塑聚合物上。另外,cleek等人的美国专利申请公开第2014/0271775号公开了包含具有高纵横比特性的取向药物晶体的基材的复合或分层dcb。所述复合材料可包括基材,该基材包括多孔微结构和一定量的结晶紫杉醇(ptx),该结晶紫杉醇包含与基材相关的空心晶体性质。
7.尽管cully等人和cleek等人描述的多层或复合球囊在药物给药的可靠性和可重复性方面取得了一些成功,但是许多常规的多层或复合球囊表现出低于最佳的药物施用和保留。这种现象是由于许多因素引起的,包括药物在基材上的不均一涂层,在dcb展开期间药物涂层的颗粒化或损失,和/或药物涂层的不均一或不完全地转移到血管腔的表面,最终导致低于最佳的药物施用和保留。因此,需要改进的用于针对药物施用和保留增加血管通透性的dcb和技术。
8.常规dcb的药物涂层包括赋形剂或其他添加剂,以促进药物在使用前保留在球囊表面上、在使用过程中从球囊表面释放药物以及将药物转运到组织中。
技术实现要素:
9.在过去人们认为赋形剂对于药物涂层球囊上的药物制剂是必需的,以在使用前将药物保留在球囊表面上,从而促进药物制剂在使用过程中从球囊释放到被治疗的组织,并在被治疗的组织中保留药物。使用本文进一步详述的各种方法研究了赋形剂对紫杉醇从药物涂层球囊释放、组织保留、手术过程中药物涂层损失和晚期管腔丢失的影响。测试包括对包括eptfe的复合球囊和市售球囊进行比较。还比较了使用不同量赋形剂的不同药物制剂。测试表明,赋形剂的存在对测试的任何参数都没有显著影响。
10.根据本公开的实例(“实例1”),公开了一种药物涂层球囊。该药物涂层球囊包括具有外表面的球囊和位于球囊外表面上的药物涂层,所述球囊的外表包含膨胀聚四氟乙烯。药物涂层包含至少一种治疗剂并且基本上不含赋形剂。
11.实例1的药物涂层球囊的球囊可以包含复合材料,该复合材料包含膨胀聚四氟乙烯和尼龙。至少一种治疗剂可以包括紫杉醇。在所述至少一种治疗剂包含紫杉醇的情况下,所述球囊可以被配置为将紫杉醇递送至组织以减少与再狭窄相关的细胞增殖反应。当所述至少一种治疗剂包含紫杉醇时,药物涂层可进一步包含选自以下的治疗剂:多西紫杉醇、前紫杉醇(protaxel)、三氧化二砷、沙利度胺、阿托伐他汀、西立伐他汀、氟伐他汀、二丙酸倍他米松、地塞米松21-棕榈酸酯、西罗莫司、依维莫司、佐他莫司、拜欧莫司(biolimus)或替西罗莫司(temsirolimus)。
12.实例1的药物涂层球囊的药物涂层可以包含0重量%至4.75重量%的赋形剂。实例1的药物涂层球囊的药物涂层可含有0重量%至4.75重量%的赋形剂,其中赋形剂选自脂肪酸及其衍生物和尿素。实例1的药物涂层球囊的球囊外表面还可以包含尼龙。药物涂层球囊的球囊外表面可以包含膨胀聚四氟乙烯。药物涂层可以以2μm至10μm的平均穿透深度穿透球囊的外表面。植入后约100分钟内,约80%的药物涂层可从球囊释放出来。
13.药物涂层可以包含干草堆状取向(haystack orientation)的微晶,其在球囊外表面上的放置是随机的并且基本上没有均一性。在药物涂层包含微晶的情况下,大多数微晶可各自具有比主尺寸宽度大至少10倍的主尺寸长度。大多数微晶的主尺寸长度可以比主尺寸宽度大至少13倍或至少15倍。大多数微晶的主尺寸宽度可以在0.5μm至2μm之间。微晶与外表面所成的角度可能随机且基本不均一,并且大多数微晶可以以50度至15度的角度从外表面突出。
14.在本公开的另一个实例(“实例2”)中,公开了一种药物涂层球囊。该药物涂层球囊包括具有外表面的球囊和位于球囊外表面上的药物涂层。药物涂层包含至少一种治疗剂并
且基本上不含赋形剂。药物涂层还可以包含干草堆状取向的微晶,其在球囊外表面上的放置是随机的并且基本上没有均一性。
15.实例2的药物涂层球囊的球囊外表面可以包含尼龙。球囊的外表面可以包含膨胀聚四氟乙烯。实例2的药物涂层球囊的药物涂层的大多数微晶可各自具有比主尺寸宽度大至少10倍的主尺寸长度。大多数微晶的主尺寸长度可以比主尺寸宽度大至少13倍或至少15倍。大多数微晶的主尺寸宽度可以在0.5μm至2μm之间。微晶与外表面所成的角度可能随机且基本不均一,并且大多数微晶以以50度至15度的角度从外表面突出。
16.在本公开的又一个实例(“实例3”)中,公开了一种制备用于药物应用的容器的方法。该方法包括以下步骤:将至少一种治疗剂溶解在溶剂中以产生溶液;用该溶液涂覆医用球囊的外表面;和蒸发溶剂,在球囊的外表面上留下包含至少一种治疗剂的药物涂层,使得药物涂层包含干草堆状取向的微晶,其在球囊外表面上的放置是随机的并且基本上没有均一性。该溶液基本上不含赋形剂。
17.实例3的方法的溶剂可以包含丙酮。在溶剂包含丙酮的情况下,溶剂还可以包含水。在溶剂包含丙酮和水两者的情况下,溶剂可包含约75%的丙酮和约25%的水。在溶剂包含丙酮和水两者的情况下,溶剂还可包含二噁烷。在溶剂包含丙酮、二噁烷和水三者的情况下,溶剂可包含约58%的丙酮、14%的二噁烷和28%的水。实例3的球囊可以包含复合材料,所述复合材料包含含氟聚合物和尼龙。实例3的至少一种治疗剂可以包括紫杉醇。
18.在本公开的另一个实例(“实例4”)中,公开了一种药物涂层球囊。该药物涂层球囊包括具有外表面的球囊和位于球囊外表面上的药物涂层,所述球囊的外表面包含膨胀聚四氟乙烯。药物涂层包含至少一种治疗剂和0重量%至4.75重量%的脂肪酸及其衍生物。实例4的脂肪酸及其衍生物可以选自单羧酸、聚山梨醇酯/盐和紫胶。
19.在本公开的另一个实例(“实例5”)中,公开了一种药物涂层球囊。该药物涂层球囊包括具有外表面的球囊和位于球囊外表面上的药物涂层,所述球囊的外表面包含膨胀聚四氟乙烯。药物涂层包含至少一种治疗剂和0重量%至4.75重量%的尿素。
20.前述实例仅是实例,不应被理解为限制或以其他方式缩小本公开提供的任何发明构思的范围。尽管公开了多个实例,但是根据以下详细描述,其他实施方式对于本领域技术人员来说也是明显的,该详细描述示出并描述了说明性实例。因此,附图和详细描述本质上应被认为是说明性的而不是限制性的。
21.附图简要说明
22.包括附图以提供对本公开的进一步理解,附图被并入本说明书中并构成本说明书的一部分,附图示出了实施方式,并且与说明书一起用于解释本公开的原理。
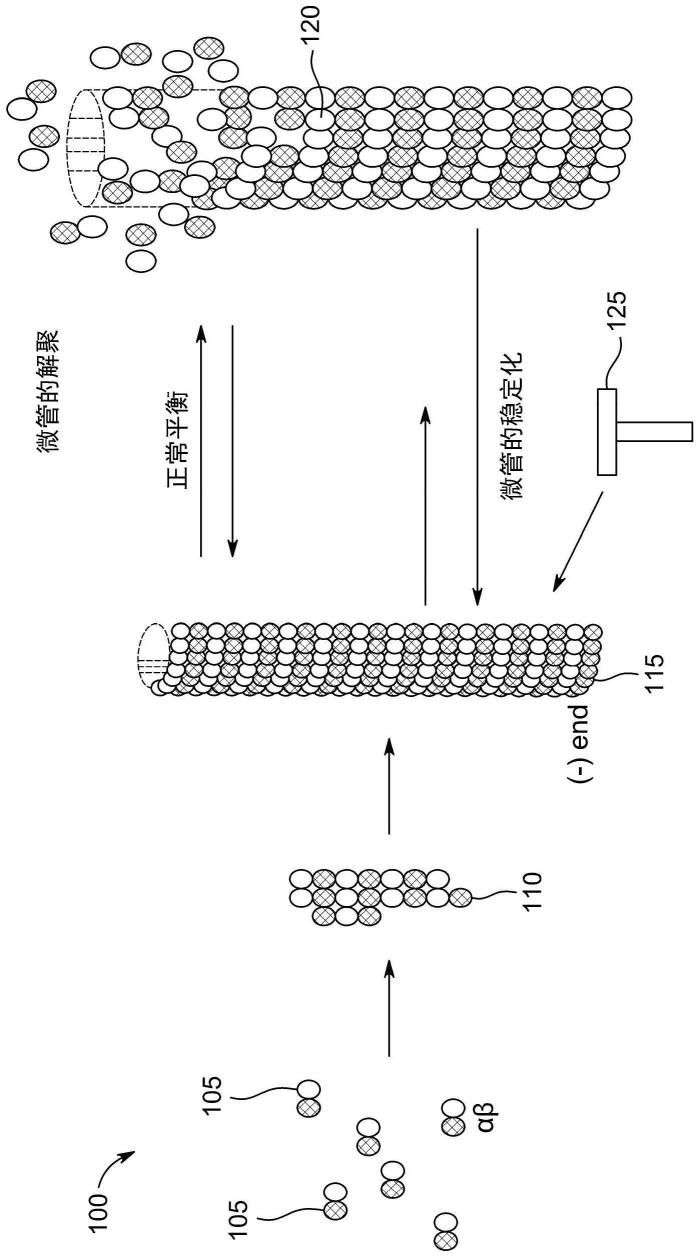
23.图1显示了根据本公开的一些方面通过聚合来组装微管;
24.图2a显示了根据本公开的一些方面的dcb;
25.图2b显示了形成图2a中所示的dcb实施方式的复合材料的横截面;
26.图2c显示了图2a所示的dcb实施方式的横截面;
27.图2d显示了根据本公开的一些方面,形成dcb的复合材料的厚度表征;
28.图3a和3b显示了根据本公开的一些方面,无孔和多孔球囊基材上的微晶形态;
29.图4显示了根据本公开的一些方面的球囊导管组件;
30.图5a是根据本公开的一些方面在比较例a中测试的不同dcb递送的药物的组织保
留进行比较的图;
31.图5b是根据本公开的一些方面在比较例a中测试的不同dcb递送的药物的组织保留进行比较的表;
32.图5c是根据本公开的一些方面在比较例a中测试的不同dcb递送的药物的组织保留进行比较的图;
33.图6是根据本公开的一些方面在比较例a中测试的不同dcb的药物释放进行比较的表;
34.图7是根据本公开的一些方面在比较例a中测试的不同dcb进行比较的图;
35.图8是根据本公开的一些方面在实施例b中测试的不同dcb的目标载量百分比的表;
36.图9是根据本公开的一些方面在实施例b中测试的不同dcb的累积体外ptx释放的图;
37.图10是根据本公开的一些方面在实施例b中测试的不同dcb在体内膨胀后在所述dcb上残留的ptx的图;
38.图11是根据本公开的一些方面,在用实施例b中测试的不同dcb对组织进行治疗一天后,在被治疗的组织中残留的ptx的图;
39.图12a是根据本公开的一些方面,在用实施例c中测试的不同dcb对组织进行治疗后不同时间段内被治疗的组织中ptx浓度的图;
40.图12b是根据本公开的一些方面在用实施例c中测试的不同dcb对动脉内的组织进行治疗后的不同时间段内留在动脉中的ptx总量的图;
41.图13是根据本公开的一些方面在实施例d中测试的不同dcb的累积体外ptx释放的图;
42.图14a是根据本公开的一些方面在实施例d中测试的不同dcb在通过引导器阀之后其上残留的ptx的图;
43.图14b是根据本公开的一些方面在实施例d中测试的不同dcb在通过引导器阀之后,相应的不同dcb的不同包装护套上残留的ptx的图;
44.图14c是根据本公开的一些方面在实施例d中测试的不同dcb在各自通过引导器阀之后,相应的不同dcb的不同引导器阀上残留的ptx的图;和
45.图15是根据本公开的一些方面由实施例e中测试的不同dcb治疗的被治疗的动脉的晚期管腔丢失的图。
具体实施方式
46.定义和术语
47.关于不精确性的术语,术语“约”和“大约”可以互换使用,指代包括所述测量值并且还包括合理接近所述测量值的任何测量值的测量值。如相关领域的普通技术人员所理解和容易确定的,与所述测量值相当接近的测量值与所述测量值偏离相当小的量。例如,这种偏差可能归因于测量误差、测量和/或制造设备校准的差异、读取和/或设置测量中的人为错误、鉴于与其他组件相关的测量差异而进行的调整以优化性能和/或结构参数、特定实施方案、人或机器对对象的不精确调整和/或操纵等。如果确定相关领域的普通技术人员不容
易确定这种合理小的差异的值,则术语“约”和“大约”可以理解为表示所述值的正负10%。
48.在此使用某些术语只是为了方便。例如,“顶”、“底”、“上”、“下”、“左”、“右”、“水平”、“垂直”、“向上”和“向下”等词仅描述图中所示的配置或零件在安装位置的取向。实际上,所提到的组件可以沿任何方向取向。类似地,在整个本公开中,在显示或描述过程或方法的情况下,可以以任何顺序或同时进行该方法,除非从上下文清楚该方法取决于首先进行的某些动作。
49.坐标系在图中呈现并在描述中被引用,其中“y”轴对应于垂直方向,“x”轴对应于水平或横向方向,“z”轴对应于内部/外部方向。
50.术语“主要”或“大多数”表示至少一半或50%。
51.术语“包含”(和任何形式的包含,例如“含有”和“含”),“具有”(以及任何形式的具有,例如“有”和“拥有”),“包括”(以及任何形式的包括,例如“囊括”和“括入”)和“含有”(以及任何形式的含有,例如“含入”和“包含”)都是开放式的连接动词。结果,“包含”、“具有”、“包括”或“含有”一个或多个要素的任何本发明装置、系统和方法拥有所述的一个或多个要素,但不限于仅拥有所述的这些一个或多个要素。同样,“包含”、“具有”、“包括”或“含有”一个或多个特征的装置、系统或方法的要素具有所述的一个或多个要素,但不限于仅具有所述的这些一个或多个要素。同样,“包含”、“具有”、“包括”或“含有”一个或多个特征的装置、系统或方法的要素具有所述的一个或多个特征,但不限于仅具有所述的这些一个或多个特征。
52.任何本发明的装置、系统和方法可以由或基本上由任何所描述的要素和/或特征和/或步骤组成,而不是包含/包括/含有/具有所描述的要素和/或特征和/或步骤。因此,在任何权利要求中,术语“由......组成”或“基本上由......组成”可以代替上述任何开放式连接动词,以便改变原本用开放式连接动词限定的给定权利要求的范围。
53.此外,能够以某种方式执行功能或进行配置的结构是至少能够以该方式执行功能或进行配置,但也能够以未列出的方式执行功能或进行配置。
54.如本文所用,“标称直径”是指球囊在标称膨胀压力下的近似直径。超过该状态,压力增加(例如,达到额定爆破压力)导致直径增加小于20%,直径增加小于15%,或直径增加小于10%。通常,标称直径是标记直径,如为最终用户(例如临床医生)提供的说明书中所示。
[0055]“微晶干草堆状”或短语“干草堆状取向的微晶”被定义为多个微晶,其中大多数微晶以与它们所在的表面成小于20
°
角取向。另外,多个微晶中的大多数各自的主要(整体)尺寸长度比微晶的主要(整体)尺寸宽度大至少五(5)倍。
[0056]
术语“角度”,“突出角度”,“突出的角度”等是突出物体相对于表面的最外部面的几何角度。
[0057]“放置(placement)”等是指物体相对于表面的最外部面的中心轴的旋转或偏移。
[0058]“均一分布”,“均一分布的”等措辞意味着基材表面上给定体积内存在的微晶的体积百分比在表面上保持在一定百分比内,其中一定百分比包括3%、10%和/或20%。在一个特定实例中,如果基材表面上的每个给定体积包含65体积%至68体积%的微晶(即,差异在3%以内)、65体积%至75体积%的微晶(即,差异在10%以内)、和/或65体积%至85体积%的微晶(即,差异在20%以内),则微晶在基材上可以是“均一分布的”。
[0059]“赋形剂”是药物涂层中的任何非活性成分。赋形剂是与治疗剂一起配制以稳定、增加或赋予治疗剂治疗增强作用的物质,例如促进药物吸收、降低粘度或提高溶解度。此类赋形剂包括饱和或不饱和脂肪酸及其衍生物,例如衍生自单羧酸(例如硬脂酸)和碱(例如三(羟甲基)氨基甲烷(“tris”))的单羧酸盐,衍生自山梨糖醇和脂肪酸(例如月桂酸、硬脂酸和油酸)的聚氧乙烯山梨聚糖脂肪酸酯(聚山梨醇酯),和紫胶(例如紫胶桐酸、茉莉酸和壳脑酸)。另一种赋形剂包括例如尿素。
[0060]
下文描述中的章节标题并不意味着以限制性意义来阅读,也不意味着将下文呈现的集体公开分开。该公开应作为一个整体来阅读。提供这些标题只是为了帮助审阅,并不意味着特定标题之外的讨论不适用于该标题下的披露部分。本公开内容并非旨在以限制性方式阅读。例如,申请中使用的术语应该在该领域的技术人员将这些术语所归属的含义的情形中宽泛地理解。
[0061]
各种实施方式的描述
[0062]
本领域的技术人员容易理解,可通过构造以实施所需作用的任何数量的方法和设备来实现本公开内容的各个方面。还应注意,本文参考的附图不一定是按比例绘制,而是有可能放大以说明本公开的各个方面,就此而言,附图不应视为限制性的。
[0063]
i.引言
[0064]
在各个实施方式中,提供一种球囊,该球囊包括外表面和在球囊外表面上的药物涂层。用于治疗血管疾病的常规方法包括使用药物涂层球囊(dcb)。然而,与传统dcb相关的问题是在dcb输送至治疗位置期间难以维持药物的组织保留并难以减少生物流体(例如血液)中的药物损失,特别是当存在一些因素使得药物与受体结合和/或解离(即,可逆结合和结合动力学)的速率增加时尤为明显。例如,药物与组织内受体的可逆结合是剂量和停留时间的函数。
[0065]
图1显示了药物如紫杉烷与微管内受体部位的可逆结合如何影响组织保留。通过αβ微管蛋白异二聚体105聚合而进行的微管组装100以两个阶段发生:成核110和伸长115。形成短聚合核,然后通过可逆的非共价加成微管蛋白亚基而在每个末端进行伸长或聚合物生长。对于净聚合物伸长,微管蛋白异二聚体105结合为生长的微管比微管解聚更快。然而,在稳定状态下,由于αβ-异二聚体加成引起的微管聚合物的生长被分解成αβ-微管蛋白亚基导致的收缩而抵消。因此,聚合的微管120在生长期和收缩期之间切换,这是一种称为动态不稳定性的特性(即,微管的正常平衡)。
[0066]
紫杉醇(ptx)之类的紫杉烷类125是微管结合药物,其靶向聚合微管120的管腔内的特定部位。紫杉烷类125通过与gdp结合β-微管蛋白分子结合并通过将它们的构象改变为更稳定的gtp结合β-微管蛋白结构来稳定它们而起作用。紫杉烷类细胞毒性作用归因于它们结合微管蛋白并稳定原丝的能力,导致微管过度聚合,并最终由于细胞凋亡而死亡。然而,不受理论束缚,紫杉烷类125与聚合微管120的管腔的可逆结合可能阻碍紫杉烷类125沿微管轴的扩散,并因此影响紫杉烷类125的组织保留。
[0067]
为了克服上述组织保留和药物损失的问题,us公开第2017/0367705号公开了一种涂层形态,该涂层形态包括以干草堆状取向的微晶,其在dcb输送、膨胀和缩小到治疗位置(例如,动脉壁)的过程中将药物保持在dcb的表面上,同时也增加从dcb转移的药物的组织保留。该涂层形态可以减少或消除对dcb上可移除覆盖物和/或dcb表面上多孔层的需要,这
些可移除覆盖物和/或多孔层是传统上常用于在dcb运输、膨胀和缩小期间将药物保持在dcb表面上的技术。
[0068]
不受理论束缚,已经证明包含干草堆状取向的微晶的微晶表面涂层形态可以决定药物在血管内表面上的分布,并且以某种方式可以最大程度提高药物的组织保留。此外,包含干草堆状取向的微晶的微晶表面涂层形态可以使得在运输期间和/或在膨胀和缩小期间的药物损失最小化,而不需要在药物涂层上额外的覆盖物/层,如以下比较例a中所示。因此,已经证明,利用具有微晶表面涂层形态的dcb并且该微晶表面涂层形态包含在含氟聚合物表面上以干草堆状取向的微晶,使得运输、膨胀和缩小期间的药物损失最小化,而不需要在药物涂层上额外的可移除覆盖物/层。这些结果表明,具有含氟聚合物表面且该含氟聚合物表面具有多孔微结构的dcb可以促进从多孔微结构的微晶生长,以及/或者克服在运输、膨胀和缩小期间药物涂层的颗粒化。
[0069]
而且,已经证明,当包含干草堆状取向的微晶的微晶表面涂层形态位于球囊的多孔或无孔聚合物层上时,该微晶表面涂层形态可以改善药学在血管内表面上的分布。
[0070]
此外,已经证明,dcb的组织保留受益于包含干草堆状取向的微晶的微晶表面涂层形态,而不是像之前推测的那样是由于增加的剂量暴露。尽管本领域技术人员预期提供比另一dcb更高的初始剂量暴露的dcb也将具有比另一dcb更高的在1小时的可保留剂量,具有含氟聚合物表面和包含干草堆状取向的微晶的微晶表面涂层形态的dcb的结果提供了组织保留的协同增加,如下面的比较例a所示。这表明具有含氟聚合物表面且该含氟聚合物表面具有多孔微结构的dcb上的微晶表面涂层形态可以制备动脉以增强吸收和/或克服药物释放不良的限制。
[0071]
除了上述组织保留问题外,以前认为药物涂层制剂中需要赋形剂以增强长期稳定性,增加含有强效活性成分的固体制剂(因此通常称为“填充剂”、“填料”或“稀释剂”),或赋予最终剂型中治疗剂的治疗增强作用,例如促进药物吸收、降低粘度或提高溶解度。
[0072]
不受理论的束缚,已经证明赋形剂在具有含氟聚合物表面的球囊上的存在,特别是作为包含干草堆状取向的微晶的微晶表面涂层形态的一部分,对治疗剂在被治疗的组织中的保留几乎没有影响。此外,已经证明,相对于具有带有赋形剂的药物涂层的装置,具有含氟聚合物表面和没有赋形剂的药物涂层的球囊可以通过引导阀而不会增加药物损失。此外,现在令人惊讶地发现,赋形剂可能对体内和体外治疗药物从球囊释放即使有影响,此种影响也很小。因此,本公开的药物涂层可以基本上不含赋形剂。
[0073]
ii.药物涂层球囊(dcb)
[0074]
在各个实施方式中,提供了一种医疗装置,其包括球囊,球囊具有外表面和在球囊外表面上的药物涂层。药物涂层可以包括均匀地施加在球囊外表面上的干草堆状取向的微晶。球囊可具有任何适合于临床应用的尺寸和大小。在一些实施方式中,球囊沿着工作长度基本上是圆柱形的。在一些实施方式中,球囊可以是卷绕的球囊,例如以20度至90度或40度至70度之间的角度或以其他合适的卷绕角度螺旋卷绕的球囊。在一些实施方式中,球囊可以是以大约90度角卷绕的卷绕球囊(即,烟卷球囊(cigarette wrapped balloon))。如图2a所示,示例性球囊700具有两个相反的腿部705,其一体化地连接到肩部/锥形部分710。为了本公开的目的,“工作长度”被定义为球囊700的直体部分715的长度,其包括相反的肩部/锥形部分710之间的大致长度。腿部705、肩部/锥形部分710和直体部分715限定了球囊700的“总长度”。球囊700的工作长度可以是约10mm至约150mm或更长。类似地,球囊700的标称直径可为约2mm至约30mm或更大。举例来说,球囊700可具有4mm直径和30mm工作长度,或者,可具有8mm直径和约60mm工作长度。当然,本公开的球囊700可以以适合于特定用途的任何尺寸构造。球囊700可以在腿部处附接或安装到导管915(如图4所示),用于通过球囊700在脉管系统中的膨胀来递送药物涂层。导管915可具有一个或多个管腔,其中一个管腔可与球囊700的室连通,用于供应膨胀流体以使球囊700膨胀。
[0075]
参考图2a、2b、2c和2d,球囊700还可包括球囊壁720,球囊壁720包括外表面725和内表面727。球囊壁720限定室730并且可由层状材料735构成。在一些实施方式中,层状材料735包含以彼此叠置的关系至少部分地附连到基材或聚合物层745的热塑性聚合物层740。在某些实施方式中,层状材料735可以通过拉伸吹塑法制备,如美国专利申请公开第2016/0106961号中所述。在其他实施方式中,层状材料735可以通过将一层围绕另一层卷绕(例如,螺旋卷绕)来形成,例如,聚合物层745可以围绕热塑性聚合物层740卷绕,如美国专利申请公开号2016/0143759a1中所述。层状材料735可以通过吹塑或卷绕来构造,使得热塑性聚合物层740的厚度为10μm至40μm,例如15μm至35μm或约30μm,并且聚合物层745的厚度为5μm至50μm,例如,10μm至30μm或约15μm。
[0076]
在一些实施方式中,热塑性聚合物层740限定了球囊壁720的内表面727,其用作保持膨胀流体的囊状物,因此包括不可渗透或不透流体的材料。根据这些方面,聚合物层745或其他材料层(例如,第二聚合物层)限定了球囊壁720的外表面725。在另一些实施方式中,聚合物层745限定了球囊壁720的内表面,其用作保持膨胀流体的囊状物,因此包括不可渗透或不透流体的材料。根据这些方面,热塑性聚合物层740或其他材料层(例如,第二聚合物层)可限定球囊壁720的外表面725。
[0077]
在各种实施方式中,涂层750(例如,药物涂层)均匀地分布在层状材料735的外表面725的至少一部分上。例如,如图2b、2c和2d所示,涂层750可以均匀地分布在聚合物层745的至少一部分外表面725上。在一些实施方式中,涂层750仅均匀地基本上分布在球囊700的工作长度上。在另一些实施方式中,涂层750均匀地基本上分布在球囊700的工作长度,以及腿部705和/或肩部/锥形部分710的至少一部分上。“均匀分布”、“均匀地分布”等是指在外表面725的部分上的涂层750的厚度保持为与特定厚度相差在一定百分比内,其中该百分比包括3%、10%和20%。在某些实施方式中,涂层750的厚度为5μm至50μm,例如10μm至35μm。
[0078]
如图2d所示,通过拉曼光谱和扫描电子显微镜技术研究层状材料735和涂层750的厚度,发现涂层750被具有多孔微结构的聚合物层745穿透的平均穿透深度可为2μm至10μm(例如,约5μm),因此可以渗透多孔微结构覆盖物(例如,膨胀聚四氟乙烯(eptfe))的最外层。相反,涂层750不会穿透到具有无孔微结构的聚合物层745中,因此将完全设置在无孔微结构覆盖物(例如,尼龙)的最外层(例如,外部两层)上。因此,不受理论束缚,具有多孔微结构的聚合物层745(例如eptfe)为涂层750(例如,ptx)提供海绵状支架,并且涂层穿透至约5μm的深度。
[0079]
在一些实施方式中,涂层750和聚合物层745的厚度为5μm至45μm,例如,10μm至35μm或约25μm。在一些实施方式中,涂层750、热塑性聚合物层740和聚合物层745的厚度为30μm至60μm,例如,40μm至55μm或约45μm。热塑性聚合物层740的厚度与聚合物层745的厚度之比可以为1.5:1至2.5:1,例如约2:1,或约30μm的热塑性聚合物层740相较于15μm的聚合物层
745。热塑性聚合物层740的厚度与(聚合物层745和涂层750)的厚度之比可为1:1至1.7:1,例如约1.2:1,或约30μm的热塑性聚合物层740相较于25μm的(聚合物层745和涂层750)。
[0080]
热塑性聚合物层740可以包括顺应性、半顺应性或非顺应性热塑性聚合物。合适的热塑性聚合物包括医用级且可吹塑的聚合物。合适的热塑性聚合物的实例可包括聚甲基丙烯酸甲酯(pmma或丙烯酸类)、聚苯乙烯(ps)、丙烯腈丁二烯苯乙烯(abs)、聚氯乙烯(pvc)、改性聚对苯二甲酸乙二醇酯(petg)、乙酸丁酸纤维素(cab);半结晶商品塑料,包括聚乙烯(pe)、高密度聚乙烯(hdpe)、低密度聚乙烯(ldpe或lldpe)、聚丙烯(pp)、聚甲基戊烯(pmp);聚碳酸酯(pc)、聚苯醚(ppo)、改性聚苯醚(mod ppo)、聚亚苯基醚(ppe)、改性聚亚苯基醚(mod ppe)、热塑性聚氨酯(tpu);聚甲醛(pom或缩醛)、聚对苯二甲酸乙二醇酯(pet,热塑性聚酯)、聚对苯二甲酸丁二醇酯(pbt,热塑性聚酯)、聚酰亚胺(pi,酰亚胺化塑料)、聚酰胺-酰亚胺(pai,酰亚胺化塑料)、聚苯并咪唑(pbi,酰亚胺化塑料);聚砜(psu)、聚醚酰亚胺(pei)、聚醚砜(pes)、聚芳基砜(pas);聚苯硫醚(pps)、聚醚醚酮(peek);含氟聚合物,包括氟化乙烯丙烯(fep)、乙烯-氯三氟乙烯(ectfe)、乙烯四氟乙烯(etfe)、聚氯三氟乙烯(pctfe)、聚偏二氟乙烯(pvdf)、全氟烷氧基(pfa),或其组合、共聚物或衍生物。其他通常已知的医用级材料包括弹性有机硅聚合物和聚醚嵌段酰胺(例如)。特别地,聚酰胺可包括尼龙12、尼龙11、尼龙9、尼龙6/9和尼龙6/6。在某些实施方式中,可以选择pet、尼龙和pe用于冠状动脉成形术或其他高压应用中使用的医用球囊。材料的具体选择可取决于球囊的所需特性/预期应用。
[0081]
聚合物层745可以包括顺应性、半顺应性或非顺应性聚合物。合适的聚合物包括多孔微结构或无孔微结构。在具有多孔微结构(在本文中称为“多孔层”)的实施方式中,合适的聚合物包括含氟聚合物,包括但不限于全氟弹性体等,聚四氟乙烯(ptfe)等以及膨胀含氟聚合物,包括eptfe。在具有无孔微结构(在本文中称为“无孔层”)的实施方式中,合适的聚合物包括聚酰胺,包括但不限于尼龙12、尼龙11、尼龙9、尼龙6/9和尼龙6/6。
[0082]
可以基于预期应用的需要来选择多孔微结构的结构。在一些实施方式中,多孔微结构可以基本上原纤化(例如,具有基本上只有原纤的微结构的非织造网,一些原纤在交叉点熔合或具有较小的节点尺寸)。在另一些实施方式中,多孔微结构可包括大的节点或大的致密区域,其可在吹塑过程中对材料的可压缩性/可收缩性的程度产生影响。在另一些实施方式中,多孔微结构可以是上述实施方式之间某处的节点和原纤微结构。在一些实施方式中,多孔微结构可具有“开放”微结构,使得外聚合物层745可具有更高蓬松度,并且/或者使得药物涂层750可具有更多空隙空间以占据外聚合物层745表面附近。多孔结构的其他实例可以是纤维结构(例如织造(梭织)或编织织物),纤维、微纤维或纳米纤维的非织造垫,闪纺膜、电纺膜和其他多孔膜。
[0083]
在一些实施方式中,多孔微结构可包括膨胀含氟聚合物或膨胀聚乙烯(参见例如sridharan等人的美国专利第6,743,388号)。膨胀含氟聚合物的非限制性实例包括但不限于eptfe,膨胀改性ptfe和膨胀ptfe共聚物。可膨胀的ptfe掺混物、可膨胀的改性ptfe和膨胀ptfe共聚物已申请了专利,诸如branca的美国专利第5,708,044号;baillie的美国专利第6,541,589号;sabol等的美国专利第7,531,611号;ford的美国专利第8,637,144号;和xu等的美国专利第8,937,105号。
[0084]
聚合物层745可以由具有多孔或无孔微结构的聚合物的管状构件形成。管状构件
可以形成为挤出管,或者可以是膜卷绕的。管状构件可具有微结构的周向、螺旋或轴向取向。在各种实施方式中,管状构件可以通过卷绕膜或带形成,并且取向可以通过卷绕的角度来控制。管状构件可以周向卷绕或螺旋卷绕。当多孔材料相对于周向或轴向螺旋卷绕时,给定方向上的顺应度可以变化并且可以影响复合材料的整体顺应性。(如本文所用,术语“轴向”可与术语“纵向”互换。如本文所用,“周向”是指基本垂直于纵向轴的角度。)
[0085]
涂层750可以包含至少一种天然、半合成或合成治疗剂(例如,至少一种药物)。涂层750的功能特征是允许在球囊膨胀期间将至少一种治疗剂释放到血管壁的组织(例如,在患有外周动脉阻塞性疾病的患者中通过经皮腔内血管成形术进行治疗)。在某些实施方式中,治疗剂是亲脂性的(正丁醇和水之间的分配系数》10)或显示非常差的水溶性(《10mg/ml,20℃)。措辞“至少一种治疗剂(或治疗剂制品)”是指包括单一治疗剂或不同治疗剂的混合物。因此,如果需要不同的药理作用或者要改善功效或耐受性,可以应用各种治疗剂或将各种治疗剂组合。
[0086]
适用于涂层750的治疗剂可包括再狭窄或细胞增殖的抑制剂(例如,抗有丝分裂药物或抗增殖药物),例如长春花生物碱,例如秋水仙碱、鬼臼毒素、灰黄霉素、抗有丝分裂生物碱剂和抗微管生物碱剂,以及紫杉烷类,例如ptx、多西紫杉醇和前紫杉醇(protaxel)。在某些实施方式中,治疗剂包括ptx或三氧化二砷。或者,适用于涂层750的治疗剂可包括特定的新血管形成抑制剂,例如沙利度胺,他汀类如阿托伐他汀、西立伐他汀、氟伐他汀,或抗炎药如皮质激素或者甚至皮质激素的亲脂性衍生物,例如倍他米松二丙酸酯或地塞米松21-棕榈酸酯,和利莫斯(limus)药物,尤其是免疫抑制剂和有丝分裂抑制剂,如mtor抑制剂,诸如西罗莫司、依维莫司、佐他莫司、拜欧莫司(biolimus)和替西罗莫司(temsirolimus)。即,对于一些实施方式,治疗剂包括ptx、紫杉烷、多西紫杉醇、长春花生物碱、秋水仙碱、鬼臼毒素、灰黄霉素、抗有丝分裂生物碱剂、抗微管生物碱剂、前紫杉醇(protaxel)、三氧化二砷、沙利度胺、阿托伐他汀、西立伐他汀、氟伐他汀、倍他米松二丙酸酯、地塞米松21-棕榈酸酯、西罗莫司、依维莫司、佐他莫司、拜欧莫司(biolimus)或替西罗莫司(temsirolimus)。应理解,至少一种治疗剂可包括任何上述药物的结构类似物、相关物质、降解物和衍生物。
[0087]
药物涂层750可以基本上不含赋形剂,这可以允许更薄的药物涂层750和更低的总涂层质量的递送。例如,药物涂层750可以基本上不含旨在以下作用的成分:增强长期稳定性,增加含有强效活性成分的固体制剂,或赋予最终剂型中治疗剂治疗增强作用,例如促进药物吸收、降低粘度或提高溶解度。此类赋形剂包括饱和或不饱和脂肪酸及其衍生物,例如衍生自单羧酸(例如硬脂酸)和碱(例如tris)的单羧酸盐,衍生自山梨糖醇和脂肪酸(例如月桂酸、硬脂酸和油酸)的聚氧乙烯山梨聚糖脂肪酸酯(聚山梨醇酯),和紫胶(例如紫胶桐酸、茉莉酸和壳脑酸)。另一种赋形剂包括例如尿素。因此,药物涂层750可以基本上不含脂肪酸及其衍生物(包括单羧酸、聚山梨醇酯/盐和紫胶)、尿素和/或其他赋形剂。换句话说,药物涂层750可以由至少一种治疗剂组成,而没有任何赋形剂(即,药物涂层750中赋形剂为0重量%),或者基本上由至少一种治疗剂组成,具有少量的赋形剂(即药物涂层750中赋形剂为4.75重量%或更少)。因此,在某些实施方式中,药物涂层750可包含0重量%至4.75重量%的赋形剂,例如约0.1重量%、约0.5重量%、约1.0重量%、约1.5重量%、约2.0重量%、约2.5重量%、约3.0重量%、约3.5重量%、约4.0重量%、4.5重量%或4.75重量%的赋形剂。
[0088]
在各种实施方式中,用于涂层750的制剂包含至少一种治疗剂和挥发性溶剂。溶剂的选择可用于干燥状态下涂层750的晶体形态以及治疗剂对医疗装置表面的粘附和从该表面的释放。因此,溶剂可包括丙酮、二噁烷、四氢呋喃(thf)、水及其混合物。
[0089]
因此,在一些实施方式中,溶剂包含丙酮、二噁烷、thf和水。在另一些实施方式中,溶剂基本上由丙酮、二噁烷、thf和水组成。在另一些实施方式中,溶剂包含丙酮、二噁烷和水。在另一些实施方式中,溶剂基本上由丙酮、二噁烷和水组成。在另一些实施方式中,溶剂包含丙酮和水。在另一些实施方式中,溶剂基本上由丙酮和水组成。在一些实施方式中,溶剂包含约35体积%至约85体积%的丙酮,例如,约75%或约0.75v/v,和约5体积%至约35体积%的水,例如约25%或约0.25v/v。在另一些实施方式中,溶剂包含约35体积%至约65体积%的丙酮,例如,约58%或约0.58v/v,和约5体积%至约35体积%的水,例如约28%或约0.27v/v,和约5体积%至约30体积%的二噁烷,例如,约14%或约0.14v/v。然而,本领域技术人员将理解,该制剂的改良可以是可接受的,条件是所述改良不改变主要成分,并且可包括但不限于涉及与这些主要成分类似的衍生物和类似物的改良。为了药物涂层750基本上不含赋形剂,用于形成药物涂层750的制剂可以仅包含至少一种治疗剂和溶剂,而基本上不含赋形剂。
[0090]
如本文所讨论的,各种实施方式涉及有利地具有涂层形态的dcb,所述涂层形态在dcb输送到治疗位置(例如,动脉壁)和在治疗位置膨胀和缩小期间将药物保持在dcb的表面上,同时也增加从dcb转移的药物的组织保留。如图3a和3b所示,根据本文所述的各种实施方式建立的涂层制剂在无孔基材(例如,尼龙)805(图3a)和多孔球囊基材(例如eptfe)810(图3b)上提供基本相似的微晶形态。微晶形态可包括干草堆状取向820的微晶815。例如,微晶815可以均一地分布在基材805、810上,并且表现为随机且基本上没有均一性地(非均一地)放置在基材805、810上,以及/或者随机且基本上没有均一性地(非均一地)以一定角度从基材805、810突出。在一些实施方式中,存在于基材805、810的表面上的给定体积内的微晶815的体积百分比为约50%至约100%,例如约65%至约85%。
[0091]
大多数微晶815可以以小于20
°
的角度从基材805、810的表面延伸(因此晶体在基材805、810上相对平坦地放置)。在另一些实施方式中,大多数微晶815以50
°
至17
°
、50
°
至15
°
、小于15
°
、小于10
°
或小于8
°
的角度从基材805、810表面延伸。另外,大多数微晶815各自的主尺寸长度比微晶815的主尺寸宽度大至少五(5)倍。在另一些实施方式中,大多数微晶815各自的主尺寸长度比微晶815的主尺寸宽度大至少十(10)倍。在另一些实施方式中,大多数微晶815各自的主尺寸长度为主尺寸宽度的至少13倍或至少15倍。另外,大多数微晶815任选地各自具有在12μm至22μm之间的主尺寸长度,例如在14μm至20μm之间或者约17μm,并且大多数微晶815各自具有在0.5μm至2.0μm之间的主尺寸宽度,例如在0.8μm至1.6μm之间或约1.3μm。
[0092]
再看图2d,涂层750以及相应的微晶(例如,微晶815)可以穿透到具有类似于图3b的多孔基材810的多孔微结构的聚合物层745的外表面中2-7μm(例如,约5μm),因此可以渗透到多孔微结构覆盖物(例如eptfe)的最外层(例如,外部两层)中。相反,涂层750以及相应的微晶815不会穿透到具有类似于图3a的无孔基材805的无孔微结构的聚合物层745中,因此将基本设置在无孔微结构覆盖物(例如,尼龙)的最外层(例如,外部两层)上。因此,具有多孔微结构的聚合物层745(例如eptfe)为涂层750(例如,ptx)提供海绵状支架,并且涂层
穿透至约5μm的深度,这可以有助于在跟踪和布置期间使得药物损失最小化以及提供更好的应用。
[0093]
有利地,涂层制剂和形态允许治疗剂足够牢固地粘附到基材(例如,多孔基材810和无孔基材805)以耐受生产和最终临床使用期间的机械应力,所述生产包括折叠球囊、包装、运送给顾客,所述最终临床使用涉及通过狭窄的止血阀、引导护套或引导导管,以及距离不定的可能曲折且狭窄的血管。此外,涂层形态在制造上是经济且有效的,因为它不需要增加成本或制造步骤来提供:粗糙的球囊表面以增强粘附性,保护性护套或膜,或其他物理或化学方法以增强治疗剂对球囊表面的粘附。
[0094]
如图4所示,球囊导管组件900可包括球囊905,例如关于2a、2b、2c和2d所述的球囊700,其安装在导管915的远端部分910上。球囊导管组件900还可包括定位在导管915的近端部分925上的毂组件920。毂组件920可包括膨胀端口930,其与导管915的膨胀管腔流体连通。导管915的膨胀管腔可以与球囊905的内部区域流体连通,使得膨胀介质可以插入膨胀端口930中,以使球囊905膨胀。毂组件920还可以包括与导管915的中心管腔连通的第二端口935。导管915的中心管腔可以从导管915的近端部分925延伸到导管915的远端部分910,并且可以接收导丝。在一些方面,导管915的中心管腔也可用于从球囊905流出膨胀介质。一个或多个辐射不透性标记物940,例如但不限于辐射不透性铂-铱标记物,可位于球囊905上,以指示球囊905的工作长度并且在递送和放置期间促进球囊905的荧光可视化。在一些实施方式中,辐射不透性标记物可位于导管915上以指示球囊905的工作长度。如上文关于图2b、2c和2d所述,球囊905包括在球囊905的外表面的至少一部分上的涂层945。
[0095]
iii.使用dcb的治疗方法
[0096]
根据各种实施方式,dcb(例如,作为球囊导管组件的一部分)可用于在体腔中的期望部位处提供一种或多种治疗。dcb可包括在球囊的外表面上具有涂层的球囊,如关于图2a、2b、2c和2d所述的。用于进行一种或多种治疗的技术可以包括将dcb定位在球囊导管组件的远端部分上(如关于图4所描述的),将dcb在体腔内推进到期望的部位。当dcb或导管在体腔内行进时,使用位于dcb或导管上的辐射不透性元素监测或跟踪dcb或导管的位置。一旦dcb行进到期望的部位,dcb可以提供单次治疗(或膨胀),或者在其他实施方式中,可以在期望的部位提供多次或重复的治疗(或膨胀)。在dcb在期望部位提供单次治疗的各种实施方式中,对于每次治疗(或膨胀),dcb可以膨胀20至200秒,例如约45秒、约60秒、约90秒、约180秒或其他合适的时间长度。在一次或多次治疗之后,dcb可以缩小并从体腔中取出。
[0097]
应当理解,多次或重复治疗可以通过在同一治疗部位使单个dcb膨胀多次(如上述过程中所述)或通过在同一治疗部位使多个dcb膨胀多次(重复执行以上过程多次)来进行。例如,本公开的其他方面涉及在顺序医疗过程中使用所描述的dcb的技术。这样的技术可以包括使其上安装有dcb的球囊导管装置通过解剖学导管或血管到达期望部位,并且使所述dcb一次或顺序地膨胀到标称直径。该方法可以进一步包括使球囊膨胀并在膨胀时将位于球囊外表面上的治疗剂递送到周围组织或血管内装置。该方法可以进一步包括从解剖学导管或血管顺序地缩回球囊导管装置,并使安装到球囊导管装置的另一个dcb通过解剖学导管或血管到达期望部位,并使后一个球囊一次或顺序地膨胀到标称直径。
[0098]
iv.测试方法
[0099]
应理解,虽然下文描述了某些方法和设备,但也可替代性地采用本领域普通技术
人员确定适用的其它方法或设备。
[0100]
v.实施例
[0101]
不意图限制本文所讨论的实施方式的范围,通过参考以下实施例可以更好地理解在各种实施方式中实施的系统和方法。
[0102]
对比例a
[0103]
评估dcb实施方式的临床前性能,其中将用赋形剂配制的ptx施加于复合eptfe/尼龙球囊的eptfe多孔表面。
[0104]
方法:剂量密度为3.5μg/mm2(标记量)或3.3μg/mm2(测量量)ptx的ptx/赋形剂涂层球囊(5mm x 40mm和6mm x 40mm的eptfe-w.l.戈尔公司,美国亚利桑那州弗拉格斯塔夫(w.l.gore,flagstaff ariz.))在约克郡猪的外周动脉中膨胀。剂量密度为3.5μg/mm2(标记量)或3.3μg/mm2(测量量)紫杉醇的ptx/赋形剂涂层球囊(市售,美敦力in.pact
tm
admiral
tm
紫杉醇涂层pta球囊导管)在约克郡猪的外周动脉中膨胀。动脉接受膨胀60秒的单次治疗的临床剂量。在治疗后1小时至30天对动物实施安乐死并进行全面的尸检。收集球囊用于分析紫杉醇释放,收集经治疗的动脉以及其他组织用于生物分析或处理用于组织学和扫描电子显微镜(sem)评估。
[0105]
另外,剂量密度为3.5μg/mm2的ptx/赋形剂涂层球囊(5mm x 40mm和6mm x 40mm的eptfe-w.l.戈尔公司,美国亚利桑那州弗拉格斯塔夫(w.l.gore,flagstaff ariz.))在台面上膨胀和缩小。在膨胀/缩小后收集来自每个球囊的涂层的颗粒用于分析。
[0106]
结果:如图5-7所示,根据本公开的实施方式的剂量密度为3.5μg/mm2的ptx/赋形剂涂层球囊(eptfe-w.l.戈尔公司,美国亚利桑那州弗拉格斯塔夫(w.l.gore,flagstaff ariz.))释放61.2%的加载剂量,例如1456
±
233μgptx,并且分别实现了在1小时1270μg/g的组织浓度或剂量,在1天48μg/g的组织浓度或剂量,在14天22μg/g的组织浓度或剂量和在28天6.4μg/g的组织浓度或剂量,并且清除斜率指数为0.73。类似剂量密度3.5μg/mm2的ptx/赋形剂涂层球囊(市售)释放85.1%的加载剂量,例如2445μg
±
343μg ptx,并且分别实现了在1小时330μg/g的组织浓度或剂量,在1天30μg/g的组织浓度或剂量,在14天6.4μg/g的组织浓度或剂量和在28天2.5μg/g的组织浓度或剂量,并且清除斜率指数为0.73。
[0107]
虽然与根据本公开实施方式的ptx涂层球囊(eptfe-w.l.戈尔公司,美国亚利桑那州弗拉格斯塔夫)相比,ptx/赋形剂涂层球囊(市售)递送更大的初始ptx剂量(eptfe/市售比为0.6),但是ptx/赋形剂涂层球囊(eptfe-w.l.戈尔公司,美国亚利桑那州弗拉格斯塔夫)能够实现与ptx/赋形剂涂层球囊(市售)相比,1小时最大可保留剂量增加3.8倍(eptfe/市售比为3.8),并且可实现与ptx/赋形剂涂层球囊(市售)相比,1天最大可保留剂量增加1.6倍(eptfe/市售比为1.6)。尽管本领域技术人员预期比ptx/赋形剂涂层球囊(eptfe-w.l.戈尔公司,美国亚利桑那州弗拉格斯塔夫)递送更高的初始剂量ptx的ptx/赋形剂涂层球囊(市售)也将比ptx/赋形剂涂层球囊(eptfe-w.l.戈尔公司,美国亚利桑那州弗拉格斯塔夫)具有更高的1小时或1天可保留剂量,但是具有含氟聚合物表面和微晶表面涂层形态的dcb的结果提供了组织保留的协同增加。
[0108]
令人惊讶的是,相比于ptx/赋形剂涂层球囊(市售),ptx/赋形剂涂层球囊(eptfe-w.l.戈尔公司,美国亚利桑那州弗拉格斯塔夫)的含氟聚合物表面和微晶表面涂层形态在1小时产生高3.8倍的可保留药物递送,并且在1天产生高1.6倍的可保留药物递送。此外,ptx
涂层球囊(eptfe-w.l.戈尔公司,美国亚利桑那州弗拉格斯塔夫)在台面上膨胀/缩小后没有显示出颗粒化的迹象,而ptx/赋形剂涂层球囊(市售)显示出颗粒化。
[0109]
结论:总体而言,在3.5μg/mm2的剂量密度下用本公开的dcb实施方式治疗外周动脉导致可接受的急性装置性能,无不良安全事件,类似于其他ptx/赋形剂涂层球囊的药代动力学。涂覆有相似ptx剂量(3.5μg/mm2)的球囊表面的成像显示出不同的形态。来自本公开的实施方式的组织保留受益于涂层球囊的含氟聚合物表面和微晶表面涂层形态,而不是由于增加的剂量暴露。以某种方式的微晶表面涂层形态可以减少颗粒化并增加药物的组织保留。相似的清除速率可归因于两种类型的dcb的相似组织清除机制,这证明了早期递送和保留药物的重要性。
[0110]
实施例b
[0111]
评估dcb实施方式的临床前性能,其中将ptx施加于于复合eptfe/尼龙球囊的eptfe多孔表面。其中六个测试组含有不同量的硬脂酸和tris赋形剂,而一个测试组不含赋形剂。
[0112]
方法:ptx涂层球囊(w.l.戈尔公司,美国亚利桑那州弗拉格斯塔夫)(5x40 mm)被构建并涂有七种不同的涂层配方,其中根据图8含有不同水平的硬脂酸和tris。涂层球囊上的ptx载量在所有组中都是恒定的(3.5μg/mm2)。配方为100-100-100的装置代表对照组,具有如公开号第2017/0367705中所述的ptx-硬脂酸-tris水平(ptx:3.5μg/mm2,硬脂酸:0.12μg/mm2,tris:0.05μg/mm2)。配方为100:0:0的装置仅含有ptx,不含赋形剂。所有装置都经过消毒,然后在体外和体内环境中都进行了部署。
[0113]
结果:如图9所示,无论赋形剂水平如何,所有装置都表现出相似的ptx体外释放曲线。
[0114]
如图10所示,赋形剂水平对体内部署期间从球囊释放的ptx量没有影响。在体内部署后,所有装置在球囊表面上残留大约35%的ptx。图11显示赋形剂加载对装置部署后1天的ptx组织水平没有影响。用仅ptx涂层球囊(100-0-0)处理的动脉导致1天ptx组织水平约为100μg ptx/g组织,ptx组织水平在涂层配方之间没有显著差异(p》0.05)。
[0115]
结论:这些结果表明,赋形剂水平对从eptfe球囊表面体外释放ptx即使有影响,这些影响可能也是很小的,因为似乎不含赋形剂的仅采用ptx的涂层与含赋形剂的对照涂层具有相似的药物水平。此外,对于部署后装置上残留的ptx百分比和一天时被处理的组织中ptx的保留率,治疗手段之间没有显著差异。
[0116]
实施例c
[0117]
评估dcb实施方式的临床前性能,其中将ptx施加于复合eptfe/尼龙球囊的eptfe多孔表面。一个测试组包括含有硬脂酸和tris赋形剂的药物涂层(图8中的配方100-100-100),而另一个测试组包括仅含药物的涂层(图8中的配方100-0-0,无赋形剂)。
[0118]
方法:构建、涂覆和消毒剂量密度为3.5μg/mm2(5x40mm和6x40mm)的ptx涂层球囊(w.l.戈尔公司,美国亚利桑那州弗拉格斯塔夫)。然后将这些装置部署在约克郡猪的外周动脉中,并在治疗后的1天、3天、7天和28天测量ptx组织浓度。
[0119]
结果:如图12a所示,使用仅药物涂层球囊的治疗部位处的ptx的平均动脉组织浓度在1天约为74.42ng/mg,在3天约为14.15ng/mg,在7天约为2.05ng/mg,并且在28天约为0.20ng/mg。使用包含赋形剂的球囊的治疗部位处的ptx的平均动脉组织浓度在1天约为
35.26ng/mg,在3天约为12.07ng/mg,在7天约为4.43ng/mg,并且在28天约为1.27ng/mg。如图12b所示,使用仅药物涂层球囊处理的动脉内的ptx平均总量在1天为12.12μg,在3天为1.75μg,在7天为0.33μg,并且在28天为0.03μg。使用包含赋形剂的球囊处理的动脉内的ptx平均总量在1天约为6.26μg,在3天约为1.63μg,在7天约为0.79μg,并且在28天约为0.17μg。
[0120]
结论:在1天和3天,对于没有赋形剂的配方,ptx组织水平呈上升趋势,但这种趋势后来在7天和28天逆转。
[0121]
实施例d
[0122]
评估dcb实施方式的临床前性能,其中将ptx施加于复合eptfe/尼龙球囊的eptfe多孔表面和尼龙球囊的无孔表面。每种球囊类型的一个测试组包括含有硬脂酸和tris赋形剂的药物涂层,而每种球囊类型的另一个测试组包括不含赋形剂的仅药物涂层。
[0123]
方法:构建、涂覆、包装和消毒具有ptx涂层的复合eptfe/尼龙球囊(w.l.戈尔公司,美国亚利桑那州弗拉格斯塔夫)(5x40mm)。一组ptx涂层球囊包括硬脂酸和tris赋形剂(图8中的配方100-100-100),而另一组ptx涂层球囊不包括赋形剂(图8中的配方100-0-0)。此外,将两组尼龙球囊用ptx涂覆,进行包装和灭菌,同样一组含有赋形剂(图8中的配方100-100-100),另一组不含赋形剂(图8中的配方100-0-0)。每个装置的目标ptx载量为2.6mg。每组均进行体外溶出试验。复合球囊组还另外经历了跨越引导器阀,ptx保留在装置上,包装护套和引导器的ptx损失计算为目标载量的百分比。
[0124]
结果:如图13所示,尼龙球囊和仅含ptx(无赋形剂)的复合球囊与涂有ptx和赋形剂的复合球囊具有相似的体外释放。这三个装置组表现出相似的突释和最终累积释放。涂有ptx和赋形剂的尼龙球囊显示出比其他3个装置组更高的突释。
[0125]
如图14a所示,在跨越引入器阀后,在涂有赋形剂或没有赋形剂的复合球囊上残留的ptx平均量没有显著差异(p》0.05)。同样,对于包装护套或引导器阀的ptx损失,配方之间没有显著差异(分别参见图14b和14c)。
[0126]
结论:ptx溶出曲线表明赋形剂对体外ptx溶出的影响很小,因为没有发现显著的结果差异。此外,复合球囊、包装护套和引导器上的ptx含量在测试组之间没有显著差异,这表明与涂有赋形剂的复合球囊相比,没有赋形剂的复合球囊可以通过引导器阀而不会增加药物损失。
[0127]
实施例e
[0128]
评估dcb实施方式的体内性能,其中将ptx施加于复合eptfe/尼龙球囊的eptfe多孔表面。将具有包含赋形剂的药物涂层的dcb(图8中的配方100-100-100)与具有不含赋形剂的药物涂层的dcb(图8中的配方100-0-0)进行全面比较。
[0129]
方法:含有赋形剂和不含赋形剂的ptx涂层球囊(5mm x 40mm和6mm x 40mm eptfe
–
w.l.戈尔公司,美国亚利桑那州弗拉格斯塔夫)在家族性高胆固醇血症猪支架内再狭窄模型的外周动脉中膨胀。两种市售球囊:一个是含有赋形剂的ptx涂层尼龙球囊(市售1,美敦力in.pact
tm
admiral
tm
紫杉醇涂层pta球囊导管),另一个是未涂覆的尼龙球囊(市售2,科迪斯(cordis)pro pta扩张导管),也将这两种市售球囊在家族性高胆固醇血症猪支架内再狭窄模型的外周动脉中膨胀。简而言之,该模型是通过在0天时损伤治疗部位而创建的。损伤是通过用标准血管成形术球囊导管过度拉伸动脉而造成的,目标是130%过度拉伸,在该部位进行3次膨胀,然后部署裸金属自膨胀支架。选择的支架以大约
20%的过度拉伸为目标。大约在15天,用血管造影和光学相干断层扫描(oct)对受伤的支架部位进行成像,然后用球囊进行治疗。受伤部位从每个球囊接受一次治疗并膨胀60秒。治疗后,重复血管造影。大约在45天,受伤并经过治疗的部位接受了血管造影和oct的重复成像。在0、15和45天收集的图像用于定量血管造影(qva)分析。收集治疗过的外周动脉以及其他组织,并准备用于光学显微镜分析和组织形态计量学。
[0130]
结果:如图15所示,用包含赋形剂的复合球囊治疗的动脉平均出现约0.18mm的晚期管腔丢失,而用不包括赋形剂的复合球囊治疗的动脉平均出现约0.58mm的晚期管腔丢失。用市售1涂层球囊治疗的动脉平均出现约0.22mm的晚期管腔丢失,而用市售2未涂覆球囊治疗的动脉平均出现约1.88mm的晚期管腔丢失。
[0131]
结论:结果表明赋形剂对晚期管腔丢失几乎没有影响,因为测试的药物涂层球囊之间的差异不显著。
[0132]
上文中已经概括性地并且结合具体实施方式描述了本技术的发明。对本领域的技术人员来说显而易见的是,可以在不偏离本公开的范围的情况下,对实施方式进行各种修改和变动。因此,实施方式旨在覆盖对本发明的这些修改和变动,只要这些修改和变动在所附权利要求及其等同方案的范围之内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。