1.本发明涉及中药药理领域,具体涉及的是玛咖在治疗非酒精性脂肪肝中的应用。
背景技术:
2.玛咖(lepidium meyenii walp)为十字花科独行菜属植物,在秘鲁安第斯山区已有几千年的栽培历史。不仅含有丰富的氨基酸,多糖,维生素,蛋白质等营养成分,而且具有黄酮、生物碱以及有机酸类等活性成分,在国外常用作营养补充剂或用以预防和治疗心血管、糖尿病等慢性疾病。随着玛咖被批准成为中国新资源药食同源的食品时,出现了玛咖研究的热潮。最重要的是,因其具有无毒安全的优点,越来越符合人民群众对多层次、多样化的健康养生的需求,是未来健康产业发展不可分割的重要部分。但由于我国对玛咖的研究多趋向于化学成分、保健食品类的开发,对于药效的研究较为单薄,因此将玛咖以新中药资源的开发利用为代表,赋予中药的内涵,加入中医药对玛咖的阐释,有利于推进中医药现代化,推动中医药走向世界,作为丰富中医药的治疗手段的重要途径之一,来缓解一些中药资源匮乏等问题。
技术实现要素:
3.本发明提供了玛咖在治疗非酒精性脂肪肝中的应用,实验证明玛咖水提物可以干预非酒精性脂肪肝病,可以显著降低alt、ast、tc等血清生化指标,可以改善肝脏脂肪变性和脂滴的减少。
4.本发明首先提供了玛咖在制备预防和/或治疗非酒精性脂肪肝药物中的应用。
5.本发明还提供了玛咖在制备下述1)-5)中任一种药物中的应用;
6.1)降低血清中谷丙转氨酶含量的药物;
7.2)降低血清中谷草转氨酶含量的药物;
8.3)降低血清中总胆固醇含量的药物;
9.4)减少肝脏中脂肪性空泡和炎性细胞的药物;
10.5)减少肝脏中脂滴的药物;
11.6)上调脂肪酸fa 22:5、fa 22:4、fa 18:3和fa 18:1中的至少一种的药物;
12.7)回调fa 18:2和fa 20:5的药物。
13.上述的应用中,所述玛咖指的是玛咖水提物。
14.具体的,所述玛咖水提物的制备方法,包括如下步骤:将玛咖药材加入水,提取,将滤液浓缩干燥,得到玛咖冻干粉,即所述玛咖水提物。
15.所述水的质量为玛咖药材质量的8~15倍;
16.所述提取的温度为50~80℃;
17.所述提取次数为1~3次;
18.每次提取的时间为0.5~1.5h;
19.所述浓缩干燥采用喷雾干燥,温度为160℃。
20.上述的应用中,所述非酒精性脂肪肝为非酒精性脂肪肝肝炎。
21.所述非酒精性脂肪肝由食用高脂食物引起。
22.本发明进一步提供了一种预防和/或治疗非酒精性脂肪肝的药物,所述药物的活性成分为玛咖。
23.上述的药物中,所述玛咖为玛咖水提物。
24.具体的,所述玛咖水提物的制备方法,包括如下步骤:将玛咖药材加入水,提取,将滤液浓缩干燥,得到玛咖冻干粉,即所述玛咖水提物。
25.所述水的质量为玛咖药材质量的8~15倍;
26.所述提取的温度为50~80℃;
27.所述提取次数为1~3次;
28.每次提取的时间为0.5~1.5h;
29.所述浓缩干燥采用喷雾干燥,温度为160℃。
30.所述玛咖均可以通过上调脂肪酸来改善非酒精性脂肪肝。
31.具体的,所述玛咖可以通过上调脂肪酸fa 22:5、fa 22:4、fa 18:3和fa 18:1以及回调fa 18:2和fa 20:5改善非酒精性脂肪肝。
32.本发明具有如下有益效果:
33.(1)本发明证明了玛咖水提物可以干预非酒精性脂肪肝病,可以显著降低alt、ast、tc等血清生化指标,可以改善肝脏脂肪变性和脂滴的减少;
34.(2)本发明为玛咖新的药效研究拓展了新的方向;
35.(3)本发明为非酒精性脂肪肝的治疗干预提出了新的研究药物,为外来药的本土化发展提供一种示例典范。
附图说明
36.图1为各组大鼠血清生化指标表达水平;与对照组比较,
#
p<0.05,
##
p<0.01;与模型组比较,*p<0.05,**p<0.01,***p<0.001,****p<0.0001。
37.图2为各组he染色结果。
38.图3为各组油红o染色结果。
39.图4为不同给药组对非酒精性脂肪肝大鼠的差异代谢物调节作用;
40.与对照组比较,
#
p<0.05;与模型组比较,*p<0.05,**p<0.01,***p<0.001,****p<0.0001。
具体实施方式
41.下面结合具体实施方式对本发明进行进一步的详细描述,给出的实施例仅为了阐明本发明,而不是为了限制本发明的范围。
42.下述实施例中的实验方法,如无特殊说明,均为常规方法。
43.下述实施例中所用的材料、试剂等,如无特殊说明,均可从商业途径得到。
44.实施例1、非酒精性脂肪肝大鼠模型的构建及验证评价
45.1、非酒精性脂肪肝肝炎大鼠模型的构建方法
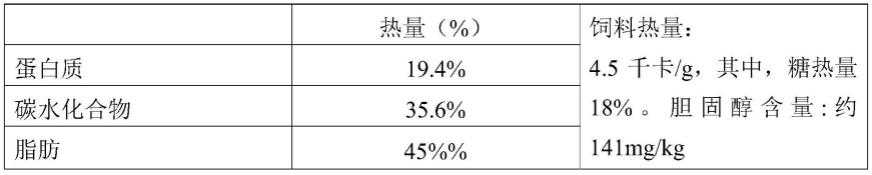
46.采用含玉米油高脂饲料(tp23000,45%高脂肥胖模型饲料。见表1,南通特洛菲饲
料科技有限公司(江苏,南通))建立非酒精性脂肪肝肝炎sd大鼠模型,以及使用对应的对照饲料(tp23302,10%低脂饲料)。造模前,对每批大鼠称体重并随机分为高脂饲料组(n=60)和空白对照组(n=18)两组。连续喂养对应饲料自由饮食8周。适应性喂养一周后,将高脂饲料喂养的sd老鼠随机分为模型组(n=12)、玛咖高剂量组(n=12,2g
·
kg-1
剂量灌胃给药(生药量/大鼠质量,以临床人用剂量20g/60kg/天计)、玛咖中剂量组(n=12,1g
·
kg-1
)、玛咖低剂量组(n=12,0.5g
·
kg-1
)以及盐酸吡格列酮阳性药组(n=12),空白对照组随机分为对照组(n=6)、对照给玛咖组(n=12,1g
·
kg-1
)。盐酸吡格列酮阳性药组依照说明书以临床人用剂量15mg/60kg/天计换算灌胃给药盐酸吡格列酮混悬液。对照组和模型组则以10ml
·
kg-1
给药体积灌胃相应体积的蒸馏水。
47.表1:tp23000饲料热量情况
[0048][0049]
末次给药后,大鼠禁食24h,于第二天进行取材相关操作。戊巴比妥钠麻醉大鼠后进行腹主动脉取血、不抗凝,于3500r
·
min-1
转速下离心15分钟,分离血清分为三份,一份用于血清生化指标检测,一份用于代谢组检测,其余置于-80℃低温冰箱中保存。然后立即处死大鼠,取肝脏组织,将大叶肝置于4%多聚甲醛(磷酸盐缓冲液pb,质量百分数,ph7.4,索莱宝)中固定,进行he染色和油红o染色,其余置于ep管-80℃低温冰箱中保存。
[0050]
上述玛咖以冻干粉末形式给药,冻干粉的制备方法如下:
[0051]
玛咖药材15kg,分别加入10倍质量的水提取3次,第一次提取1h,第二次提取1h,第三次提取45min,合并滤液,浓缩喷雾干燥,得到玛咖冻干粉。
[0052]
上述提取的温度均为55℃;
[0053]
滤液使用喷雾干燥机组在160℃喷干干燥;
[0054]
所用仪器为中药浸膏专用喷雾干燥机,型号:zlg-10,常州一步干燥设备有限公司;直筒提取罐,型号:300l,上海远跃制药机械有限公司;单效浓缩器,型号:80l/h,上海远跃制药机械有限公司。
[0055]
2、一般生理观察
[0056]
自大鼠适应期起,每日观察大鼠精神状态、体重、皮毛、饮食以及死亡等情况并作记录。每周记录体重,于最后取材记录肝脏指数。
[0057]
3、血清生化指标检测
[0058]
自造模起第2、4、5、6、7、8周进行大鼠眼眶取血1.5ml,于3500r
·
min-1
转速下离心15分钟,取血清,检测血清中alt、ast和tc各指标表达水平。
[0059]
4、病理组织学观察
[0060]
将肝脏组织置于4%多聚甲醛(磷酸盐缓冲液pb,质量百分数)中固定48h后,用石蜡包埋,进行常规病理切片,然后分别进行he和油红o染色。
[0061]
5、靶向代谢组研究
[0062]
(1)靶向代谢组分析:将血清放置4℃冰箱解冻,振荡混合均匀。取样10μl于离心管
中,加入150μl含有内标的甲醇溶液,充分震荡30秒。分别加入500μl甲基叔丁基醚溶液(mtbe),室温震荡20分钟。之后分别加入125μl水,震荡30秒,于4℃,13200rpm条件下离心10分钟,取上层溶液100μl,置记好标签的离心管中,放入真空离心浓缩仪中挥干。复溶再加入200μl复溶液(含乙腈:异丙醇:水(65:30:5,v/v/v)),涡旋30秒,于4℃,13200rpm条件下离心10分钟,取上清液于装有内衬管中的玻璃瓶中用于进样。
[0063]
(2)靶向条件
[0064]
a.液相条件
[0065]
超高效液相色谱acquity beh c8色谱柱(2.1mm
×
100mm,1.7μm),流动相a:含5mmol/l甲酸铵的乙腈-水(6:4,v/v),流动相b:含5mmol/l甲酸铵的异丙醇-乙腈(9:1,v/v)。柱温为55℃,流速为0.26ml
·
min-1
,正离子进样量为1μl,负离子进样量为2μl。
[0066]
表2脂溶性代谢物分析的液相色谱条件
[0067][0068]
b.质谱条件
[0069]
waters三重四级杆质谱(tq-s)仪:在正负离子模式采用多反应监测(multiple reaction monitoring,mrm)模式进行采集;毛细管电压为0.4kv;锥孔电压为20v。离子源温度为150℃;去溶剂气温度为400℃;去溶剂气流量为800l
·
h-1
;锥孔气流量为150l
·
h-1
。数据分析利用markerlynx v4.1对采集得到的谱图进行离子对的积分等操作。
[0070]
(3)采用marker lynx v4.1对采集得到的谱图进行离子对的提取、峰对齐、峰匹配、峰强度校正以及离子对积分等操作,将结果转化为包含化合物的保留时间和质荷比信息的csv格式文件。再导入多元统计分析软件simca进行包括主成分分析及偏最小二乘判别分析在内的多元统计分析。采用t-test检验筛选差异代谢物。通过在线工具metaboanalyst 5.0对差异代谢物进行生物通路分析。
[0071]
6、实验结果
[0072]
(1)玛咖对非酒精性脂肪肝大鼠日常状态的影响
[0073]
造模前,各组大鼠均毛色光泽、饮食正常、排便正常、状态活跃。自高脂肪饲料造模后,大鼠逐渐毛色暗淡杂乱、倦怠、发生应激等症状。
[0074]
(2)玛咖对非酒精性脂肪肝大鼠血清生化指标的影响
[0075]
利用2-8周动态血清生化指标来评价玛咖药效如图1。在第二周,模型组大鼠的alt、ast、tc表达水平高于对照组。玛咖高剂量组、玛咖中剂量组和玛咖低剂量组以及阳性药组的alt表达水平均显著低于模型组;而玛咖低剂量组、阳性药组的ast在2、4、8周均显著低于模型组,玛咖中剂量组ast在2周显著降低;但玛咖中剂量组的tc在4周有下降的趋势。
[0076]
(3)大鼠肝脏病理组织学结果分析
[0077]
a、he染色
[0078]
大鼠肝脏he染色后显微镜下病理切片照片显示(见图2),对照组大鼠的肝大叶结构清晰,肝细胞索排列整齐、边界清晰,肝内无脂肪变性、没有炎症。而模型组大鼠肝脏可见明显的脂肪变性,肝细胞普遍明显肿大,肝细胞排列无规律,产生脂肪性空泡。玛咖高剂量组、玛咖中剂量组和玛咖低剂量组相对于模型组,不同程度上减少了脂肪性空泡和炎性细胞浸润的现象。
[0079]
b、油红染色
[0080]
油红o染色显示,与对照组比较,模型组肝脏中脂滴显著增加。与模型组比较,玛咖高剂量组、玛咖中剂量组和玛咖低剂量组中肝脏中的脂滴显著减少,脂肪肝呈现好转趋势。且玛咖高剂量组、玛咖中剂量组和玛咖低剂量组对脂滴减少的作用优于盐酸吡格列酮阳性药组,见图3。
[0081]
c、差异代谢物解析
[0082]
在负离子模式下根据opls-da,p《0.05最终筛选出24个脂肪酸类差异代谢物。其中6个脂肪酸类代谢物不论在正常生理的大鼠上还是病理上均发生显著回调,如图4所示。与对照组相比,模型组的fa 22:5(eicosapentaenoic acid)、fa 22:4(docosatetraenoic acid)、fa 18:3(linolenic acid)、fa 18:2(linoleic acid)、fa 18:1(oleic acid)和fa 20:5(eicosapentaenoic acid)的脂肪酸类均显著上升。与模型组相比,玛咖高剂量显著升高了fa 18:2,fa 20:5;玛咖中剂量显著降低了fa 22:5以及显著升高了fa 20:5,玛咖低剂量显著降低了fa 18:3、fa 18:1。
[0083]
由此可以看出,玛咖可以通过上调脂肪酸fa 22:5、fa 22:4、fa 18:3、fa 18:1以及回调fa 18:2和fa 20:5来干预大鼠机体。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。