1.本发明涉及呋喃类化合物合成技术领域,具体涉及一种偕二溴烯基二氢呋喃类化合物的合成方法。
背景技术:
2.呋喃类化合物是一种常见的含氧五元杂环化合物,其可以表现出特殊的化学性质和生物活性,在新型药物、材料科学、香料、化学助剂等领域得到了广泛应用。而且,呋喃环上具有多个反应位点,常常被作为复杂杂环化合物的合成砌块。因此,合成和修饰这类杂环化合物在合成化学领域至关重要。
3.炔基是有机化学中一种重要的结构基元,是参与多类转化的优越反应前体。烯炔酮类化合物是一种独特的官能团化炔烃,其与普通炔烃相比具有更大的共轭体系和更大的电荷偏移,因此具有更丰富的反应位点和更强的反应活性。目前,利用烯炔酮类化合物作为原料来构建呋喃类化合物已经成为呋喃类化合物合成化学中重要的组成部分。通常情况下烯炔酮类化合物中的烯基、炔基和羰基碳均具有一定的亲电活性,在一定条件下三者都能够与亲核试剂反应。目前报道的关于用烯炔酮类化合物来构建呋喃骨架的方法中,大多数反应都是通过形成金属卡宾来实现,在该类反应中形成的金属卡宾中间体可以接受体系中亲核试剂的进攻,或者接受硅氢键、炔烃和异腈的插入,又或者通过后续串联环化来实现呋喃骨架的构筑(例如:j.huang,f.li and l.cui,chem.commun.,2020,56,4555;m.y.huang,j.m.yang and y.t.zhao,acs.catal.,2019,9,5353;l.chen,k.wang and y.shao,org.lett.,2019,21,3804;h.zhang,t.cao and h.luo,org.chem.front.,2019,6,1118;h.peng,y.wan and y.zhang,chem.commun.,2020,56,1417.)。然而,经由这些方法合成的呋喃骨架往往结构较为简单,而对于一些官能化程度较高的呋喃类化合物(特别是含多个溴原子的呋喃类化合物)的合成研究还十分缺乏。众所周知,碳-溴键通过易操作的交叉偶联反应极易转化为其它官能团,碳-溴键的引入对于呋喃骨架的后修饰具有重大意义。
4.因此,开发一种不同于金属卡宾催化的偕二溴烯基二氢呋喃类化合物合成方法具有十分重要的意义。
技术实现要素:
5.本发明的目的在于提供一种偕二溴烯基二氢呋喃类化合物的合成方法。
6.本发明所采取的技术方案是:
7.一种偕二溴烯基二氢呋喃类化合物的合成方法包括以下步骤:将5-三异丙基硅基烯炔酮类化合物和一元醇混合进行反应,即得偕二溴烯基二氢呋喃类化合物。
8.优选的,一种偕二溴烯基二氢呋喃类化合物的合成方法包括以下步骤:将钯催化剂、配体、n-溴代丁二酰亚胺(nbs)和添加剂分散在有机溶剂中,再加入5-三异丙基硅基烯炔酮类化合物和一元醇,保护气氛中进行反应,即得偕二溴烯基二氢呋喃类化合物。
9.优选的,所述5-三异丙基硅基烯炔酮类化合物的结构式为式中,r1选自甲基、丙基、环丙基、环丁基中的一种,r2选自乙酰基、乙氧酰基、丙氧酰基、丁氧酰基中的一种。注:tips代表三异丙基硅基
10.优选的,所述一元醇选自甲醇、乙醇、异戊醇、苯甲醇、4-氯苯甲醇、4-甲基苯甲醇、6-氯己醇、2-甲氧酰基乙醇、2-甲氧基乙醇中的一种。
11.优选的,所述5-三异丙基硅基烯炔酮类化合物、一元醇的摩尔比为1:3~6。
12.优选的,所述反应在常温下进行,反应时间为6h~8h。
13.优选的,所述钯催化剂选自二氯化钯、双三苯基膦二氯化钯、1,3-双二苯基膦丙烷二氯化钯中的至少一种。
14.优选的,所述5-三异丙基硅基烯炔酮类化合物、钯催化剂的摩尔比为1:0.05~0.20。
15.优选的,所述配体选自1,10-菲啰啉、2-甲基-1,10-菲啰啉、2,9-二甲基-4,7-二苯基-1,10-菲啰啉中的至少一种。
16.优选的,所述5-三异丙基硅基烯炔酮类化合物、配体的摩尔比为1:0.05~0.20。
17.优选的,所述5-三异丙基硅基烯炔酮类化合物、n-溴代丁二酰亚胺的摩尔比为1:1.5~2.0。
18.优选的,所述添加剂为三氟乙酸银、氟化钾和冠醚的混合物。
19.优选的,所述冠醚为18-冠醚-6。
20.优选的,所述5-三异丙基硅基烯炔酮类化合物、三氟乙酸银的摩尔比为1:0.05~0.50。
21.优选的,所述5-三异丙基硅基烯炔酮类化合物、氟化钾的摩尔比为1:1.0~1.5。
22.优选的,所述5-三异丙基硅基烯炔酮类化合物、冠醚的摩尔比为1:1.0~1.5。
23.优选的,所述有机溶剂选自乙腈、四氢呋喃中的至少一种。
24.优选的,所述保护气氛为氮气气氛。
25.优选的,所述反应结束后还进行了产物纯化操作,具体操作为:将反应液用乙酸乙酯萃取,合并有机相后用无水硫酸镁干燥,过滤,取滤液进行减压蒸馏,再进行柱层析提纯。
26.优选的,所述柱层析提纯采用的洗脱液由石油醚和乙酸乙酯按照体积比10~50:1组成。
27.进一步优选的,所述柱层析提纯采用的洗脱液由石油醚和乙酸乙酯按照体积比20~30:1组成。
28.本发明中的5-三异丙基硅基烯炔酮类化合物和一元醇进行反应的反应式如下:
29.式中,r1选自甲基、丙基、环丙基、环丁基中的一种,r2选自乙酰基、乙氧酰基、丙氧酰基、丁氧酰基中的一种,r3选自甲基、乙基、异戊基、苄基、4-氯苄基、4-甲基苄基、6-氯己基、2-甲氧酰基乙基、2-甲氧基乙基中的一种。
30.本发明的有益效果是:本发明利用5-三异丙基硅基烯炔酮类化合物与一元醇进行5-exo-dig环化反应构建了一系列具有独特性能的偕二溴烯基二氢呋喃类化合物,具有原料简单易得、操作安全、反应条件温和、底物适用性广等优点。
31.具体来说:
32.1)本发明中采用的基础原料5-三异丙基硅基烯炔酮类化合物可以由廉价的1,3-二酮类化合物和3-(三异丙硅基)丙炔醛合成,原料简单易得,生产成本低;
33.2)本发明的偕二溴烯基二氢呋喃类化合物合成方法具有原料简单易得、操作安全、反应条件温和、底物适用性广、对官能团的容忍性好、成本低等优点,适合进行工业生产和进一步的衍生化。
附图说明
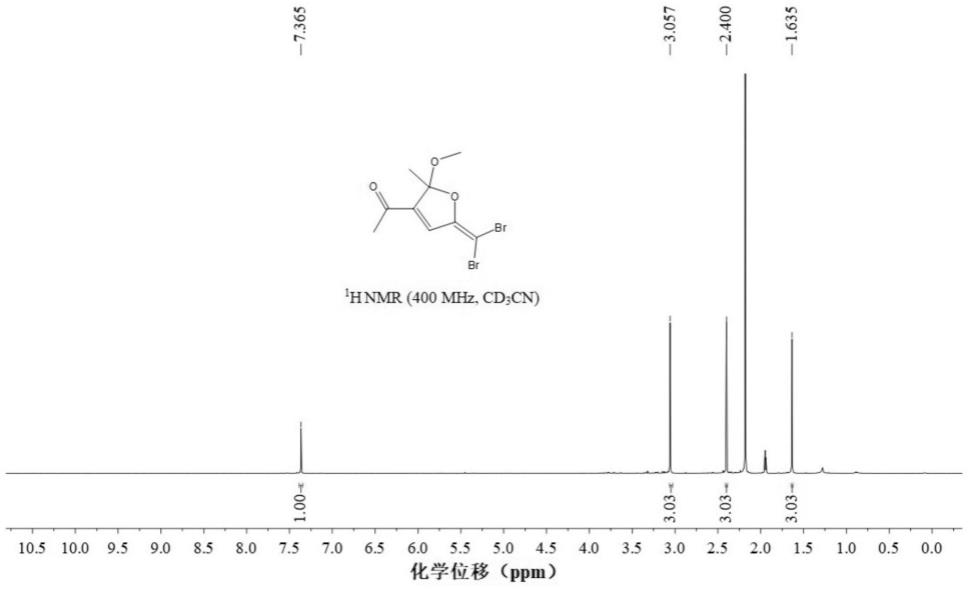
34.图1为实施例1的偕二溴烯基二氢呋喃类化合物的核磁共振氢谱图。
35.图2为实施例1的偕二溴烯基二氢呋喃类化合物的核磁共振碳谱图。
36.图3为实施例2的偕二溴烯基二氢呋喃类化合物的核磁共振氢谱图。
37.图4为实施例2的偕二溴烯基二氢呋喃类化合物的核磁共振碳谱图。
38.图5为实施例3的偕二溴烯基二氢呋喃类化合物的核磁共振氢谱图。
39.图6为实施例3的偕二溴烯基二氢呋喃类化合物的核磁共振碳谱图。
40.图7为实施例4的偕二溴烯基二氢呋喃类化合物的核磁共振氢谱图。
41.图8为实施例4的偕二溴烯基二氢呋喃类化合物的核磁共振碳谱图。
42.图9为实施例5的偕二溴烯基二氢呋喃类化合物的核磁共振氢谱图。
43.图10为实施例5的偕二溴烯基二氢呋喃类化合物的核磁共振碳谱图。
44.图11为实施例6的偕二溴烯基二氢呋喃类化合物的核磁共振氢谱图。
45.图12为实施例6的偕二溴烯基二氢呋喃类化合物的核磁共振碳谱图。
46.图13为实施例7的偕二溴烯基二氢呋喃类化合物的核磁共振氢谱图。
47.图14为实施例7的偕二溴烯基二氢呋喃类化合物的核磁共振碳谱图。
48.图15为实施例8的偕二溴烯基二氢呋喃类化合物的核磁共振氢谱图。
49.图16为实施例8的偕二溴烯基二氢呋喃类化合物的核磁共振碳谱图。
50.图17为实施例9的偕二溴烯基二氢呋喃类化合物的核磁共振氢谱图。
51.图18为实施例9的偕二溴烯基二氢呋喃类化合物的核磁共振碳谱图。
52.图19为实施例10的偕二溴烯基二氢呋喃类化合物的核磁共振氢谱图。
53.图20为实施例10的偕二溴烯基二氢呋喃类化合物的核磁共振碳谱图。
54.图21为实施例11的偕二溴烯基二氢呋喃类化合物的核磁共振氢谱图。
55.图22为实施例11的偕二溴烯基二氢呋喃类化合物的核磁共振碳谱图。
56.图23为实施例12的偕二溴烯基二氢呋喃类化合物的核磁共振氢谱图。
57.图24为实施例12的偕二溴烯基二氢呋喃类化合物的核磁共振碳谱图。
58.图25为实施例13的偕二溴烯基二氢呋喃类化合物的核磁共振氢谱图。
59.图26为实施例13的偕二溴烯基二氢呋喃类化合物的核磁共振碳谱图。
60.图27为实施例14的偕二溴烯基二氢呋喃类化合物的核磁共振氢谱图。
61.图28为实施例14的偕二溴烯基二氢呋喃类化合物的核磁共振碳谱图。
62.图29为实施例15的偕二溴烯基二氢呋喃类化合物的核磁共振氢谱图。
63.图30为实施例15的偕二溴烯基二氢呋喃类化合物的核磁共振碳谱图。
具体实施方式
64.下面结合具体实施例对本发明作进一步的解释和说明。
65.实施例1:
66.一种偕二溴烯基二氢呋喃类化合物,其合成方法包括以下步骤:
67.将0.02mmol的二氯化钯、0.02mmol的2,9-二甲基-4,7-二苯基-1,10-菲啰啉、0.2mmol的n-溴代丁二酰亚胺、0.05mmol的三氟乙酸银、0.12mmol的氟化钾和0.12mmol的18-冠醚-6加入1ml的干燥乙腈中,搅拌分散,再加入0.1mmol的1-甲基-2-乙酰基(5-三异丙基硅基)烯炔酮()和0.5mmol的甲醇,置于氮气气氛中常温搅拌6h,搅拌机的转速为700rpm,再停止搅拌后加入5ml的水,再将反应液用乙酸乙酯萃取3次,合并有机相后用0.5g的无水硫酸镁干燥,过滤,取滤液进行减压蒸馏,再进行柱层析提纯,柱层析提纯采用的洗脱液由石油醚和乙酸乙酯按照体积比20:1组成,即得偕二溴烯基二氢呋喃类化合物(产率:74%)。
68.本实施例合成的偕二溴烯基二氢呋喃类化合物的核磁共振氢谱图如图1所示,核磁共振碳谱图如图2所示,解谱分析(氢谱、碳谱、红外和质谱)如下:
[0069]1h nmr(400mhz,cd3cn):δ7.37(s,1h),3.06(s,3h),2.40(s,3h),1.63(s,3h);
[0070]
13
c nmr(100mhz,cd3cn):δ193.4,155.3,143.7,132.7,116.2,69.9,27.3,23.7;
[0071]
ir(kbr)ν
max
:3391,2927,1676,1234,789cm-1
;
[0072]
hrms(esi)calcd for c9h
10
br2nao3[m na]
:346.8894,found 346.8894;
[0073]
综上可知,本实施例合成的偕二溴烯基二氢呋喃类化合物的结构式如下:
[0074][0075]
实施例2:
[0076]
一种偕二溴烯基二氢呋喃类化合物,其在合成过程中除了将反应原料(一元醇)由甲醇替换成乙醇以外,其余和实施例1完全一样。
[0077]
本实施例中偕二溴烯基二氢呋喃类化合物的产率为83%。
[0078]
本实施例合成的偕二溴烯基二氢呋喃类化合物的核磁共振氢谱图如图3所示,核磁共振碳谱图如图4所示,解谱分析(氢谱、碳谱、红外和质谱)如下:
[0079]1h nmr(400mhz,cdcl3):δ7.19(s,1h),3.53-3.38(m,1h),3.32-3.12(m,1h),2.44(s,3h),1.77(s,3h),1.21(t,j=7.0hz,3h);
[0080]
13
c nmr(100mhz,cdcl3):δ192.2,154.3,144.1,131.6,115.5,71.0,59.1,27.5,24.3,14.8;
[0081]
ir(kbr)ν
max
:3595,3387,3114,1702,982,561cm-1
;
[0082]
hrms(esi)calcd for c
10h12
br2nao3[m na]
:360.9045,found 360.9043;
[0083]
综上可知,本实施例合成的偕二溴烯基二氢呋喃类化合物的结构式如下:
[0084][0085]
实施例3:
[0086]
一种偕二溴烯基二氢呋喃类化合物,其在合成过程中除了将反应原料(一元醇)由甲醇替换成异戊醇以外,其余和实施例1完全一样。
[0087]
本实施例中偕二溴烯基二氢呋喃类化合物的产率为85%。
[0088]
本实施例合成的偕二溴烯基二氢呋喃类化合物的核磁共振氢谱图如图5所示,核磁共振碳谱图如图6所示,解谱分析(氢谱、碳谱、红外和质谱)如下:
[0089]1h nmr(400mhz,cdcl3):δ7.26(s,1h),4.16-3.90(m,2h),3.50-3.40(m,1h),3.33-3.14(m,1h),1.99(m,1h),1.75(s,3h),1.17(t,j=7.0hz,3h),0.96(d,j=6.7hz,6h);
[0090]
13
c nmr(100mhz,cdcl3):δ161.7,154.6,138.9,132.8,115.4,71.4,70.6,59.4,27.8,24.7,19.1,15.1;
[0091]
ir(kbr)ν
max
:3447,1672,1413,1237,927,628cm-1
;
[0092]
hrms(esi)calcd for c
13h18
br2nao3[m na]
:402.9515,found 402.9517;
[0093]
综上可知,本实施例合成的偕二溴烯基二氢呋喃类化合物的结构式如下:
[0094][0095]
实施例4:
[0096]
一种偕二溴烯基二氢呋喃类化合物,其在合成过程中除了将反应原料(一元醇)由甲醇替换成苯甲醇、将洗脱液中石油醚和乙酸乙酯的体积比由20:1调整为30:1以外,其余和实施例1完全一样。
[0097]
本实施例中偕二溴烯基二氢呋喃类化合物的产率为84%。
[0098]
本实施例合成的偕二溴烯基二氢呋喃类化合物的核磁共振氢谱图如图7所示,核磁共振碳谱图如图8所示,解谱分析(氢谱、碳谱、红外和质谱)如下:
[0099]1h nmr(400mhz,cdcl3):δ7.28-7.26(m,5h),7.17(s,1h),4.46(d,j=8.8hz,1h),4.26(d,j=9.2hz,1h),)2.33(s,3h),1.82(s,3h);
[0100]
13
c nmr(100mhz,cdcl3):δ154.4,144.2,136.8,131.7,128.1,127.8,127.5,115.5,71.5,65.8,29.4,27.5,24.4;
[0101]
ir(kbr)ν
max
:2927,2044,1691,1390,1162,624cm-1
;
[0102]
hrms(esi)calcd for c
15h14
br2nao3[m na]
:422.9189,found 422.9207;
[0103]
综上可知,本实施例合成的偕二溴烯基二氢呋喃类化合物的结构式如下:
[0104][0105]
实施例5:
[0106]
一种偕二溴烯基二氢呋喃类化合物,其在合成过程中除了将反应原料(一元醇)由甲醇替换成4-氯苯甲醇以外,其余和实施例1完全一样。
[0107]
本实施例中偕二溴烯基二氢呋喃类化合物的产率为89%。
[0108]
本实施例合成的偕二溴烯基二氢呋喃类化合物的核磁共振氢谱图如图9所示,核磁共振碳谱图如图10所示,解谱分析(氢谱、碳谱、红外和质谱)如下:
[0109]1h nmr(400mhz,cdcl3):δ7.34-7.24(m,4h),7.22(s,1h),4.43(d,j=11.2hz,1h),4.24(d,j=11.2hz,1h),2.40(s,3h),1.83(s,3h);
[0110]
13
c nmr(100mhz,cdcl3):δ192.5,154.5,144.1,135.6,133.6,132.1,129.3,128.5,115.7,72.1,65.2,27.8,24.6;
[0111]
ir(kbr)ν
max
:3407,3094,1682,1575,1164,638cm-1
;
[0112]
hrms(esi)calcd for c
15h13
br2clnao3[m na]
:456.9089,found 456.8816;
[0113]
综上可知,本实施例合成的偕二溴烯基二氢呋喃类化合物的结构式如下:
[0114][0115]
实施例6:
[0116]
一种偕二溴烯基二氢呋喃类化合物,其在合成过程中除了将反应原料(一元醇)由甲醇替换成4-甲基苯甲醇以外,其余和实施例1完全一样。
[0117]
本实施例中偕二溴烯基二氢呋喃类化合物的产率为92%。
[0118]
本实施例合成的偕二溴烯基二氢呋喃类化合物的核磁共振氢谱图如图11所示,核磁共振碳谱图如图12所示,解谱分析(氢谱、碳谱、红外和质谱)如下:
[0119]1h nmr(400mhz,cdcl3):δ7.29-7.10(m,5h),4.46(d,j=10.8hz,1h),4.25(d,j=10.8hz,1h),2.32(s,6h),1.80(s,3h);
[0120]
13
c nmr(100mhz,cdcl3):δ192.4,154.8,144.6,137.4,134.8,131.8,130.4,128.3,125.8,115.7,71.6,64.5,27.8,24.6,19.0;
[0121]
ir(kbr)ν
max
:3597,1684,1560,1164,962,639cm-1
;
[0122]
hrms(esi)calcd for c
16h16
br2nao3[m na]
:436.8889,found 436.9365;
[0123]
综上可知,本实施例合成的偕二溴烯基二氢呋喃类化合物的结构式如下:
[0124][0125]
实施例7:
[0126]
一种偕二溴烯基二氢呋喃类化合物,其在合成过程中除了将反应原料(一元醇)由甲醇替换成6-氯己醇以外,其余和实施例1完全一样。
[0127]
本实施例中偕二溴烯基二氢呋喃类化合物的产率为86%。
[0128]
本实施例合成的偕二溴烯基二氢呋喃类化合物的核磁共振氢谱图如图13所示,核磁共振碳谱图如图14所示,解谱分析(氢谱、碳谱、红外和质谱)如下:
[0129]1h nmr(400mhz,cdcl3):δ7.16(s,1h),3.35(q,j=6.8hz,1h),3.13(q,j=7.0hz,1h),2.41(s,3h),1.74(s,2h),1.59(s,2h),1.32-1.25(m,6h),0.88(s,j=6.5hz,3h);
[0130]
13
c nmr(100mhz,cdcl3):δ192.5,154.7,144.6,131.8,115.9,71.2,63.9,31.5,29.5,27.8,25.6,24.6,22.5,14.0;
[0131]
ir(kbr)ν
max
:3413,2926,1679,1399,1239,693,627cm-1
;
[0132]
hrms(esi)calcd for c
14h19
br2clnao3[m na]
:450.8879,found 450.9291;
[0133]
综上可知,本实施例合成的偕二溴烯基二氢呋喃类化合物的结构式如下:
[0134][0135]
实施例8:
[0136]
一种偕二溴烯基二氢呋喃类化合物,其在合成过程中除了将反应原料(一元醇)由甲醇替换成2-甲氧酰基乙醇、将洗脱液中石油醚和乙酸乙酯的体积比由20:1调整为30:1以外,其余和实施例1完全一样。
[0137]
本实施例中偕二溴烯基二氢呋喃类化合物的产率为81%。
[0138]
本实施例合成的偕二溴烯基二氢呋喃类化合物的核磁共振氢谱图如图15所示,核磁共振碳谱图如图16所示,解谱分析(氢谱、碳谱、红外和质谱)如下:
[0139]1h nmr(400mhz,cdcl3):δ7.18(s,1h),3.67(s,3h),3.61(t,j=7.6hz,1h),3.49-3.41(m,1h),2.58(q,j=7.2,6.0hz,2h),2.42(s,3h),1.73(s,3h);
[0140]
13
c nmr(100mhz,cdcl3):δ192.45,171.6,154.5,143.9,132.0,115.6,71.8,59.2,51.8,34.5,27.9,24.5;
[0141]
ir(kbr)ν
max
:3405,2926,1680,1339,1236,625cm-1
;
[0142]
hrms(esi)calcd for c
12h14
br2nao5[m na]
:418.9089,found 418.9109;
[0143]
综上可知,本实施例合成的偕二溴烯基二氢呋喃类化合物的结构式如下:
[0144][0145]
实施例9:
[0146]
一种偕二溴烯基二氢呋喃类化合物,其在合成过程中除了将反应原料(一元醇)由甲醇替换成2-甲氧基乙醇、将洗脱液中石油醚和乙酸乙酯的体积比由20:1调整为10:1以外,其余和实施例1完全一样。
[0147]
本实施例中偕二溴烯基二氢呋喃类化合物的产率为69%。
[0148]
本实施例合成的偕二溴烯基二氢呋喃类化合物的核磁共振氢谱图如图17所示,核磁共振碳谱图如图18所示,解谱分析(氢谱、碳谱、红外和质谱)如下:
[0149]1h nmr(400mhz,cdcl3):δ7.17(s,1h),3.50(d,j=7.1hz,3h),3.33(m,4h),2.41(s,3h),1.76(s,3h);
[0150]
13
c nmr(100mhz,cdcl3):δ192.5,154.7,144.5,132.0,115.8,71.6,71.1,62.9,58.9,27.9,24.5;
[0151]
ir(kbr)ν
max
:3400,2925,2855,1678,1236,785,626cm-1
;
[0152]
hrms(esi)calcd for c
11h14
br2nao4[m na]
:390.9154,found 390.9156;
[0153]
综上可知,本实施例合成的偕二溴烯基二氢呋喃类化合物的结构式如下:
[0154][0155]
实施例10:
[0156]
一种偕二溴烯基二氢呋喃类化合物,其合成方法包括以下步骤:
[0157]
将0.02mmol的二氯化钯、0.02mmol的2,9-二甲基-4,7-二苯基-1,10-菲啰啉、0.2mmol的n-溴代丁二酰亚胺、0.05mmol的三氟乙酸银、0.12mmol的氟化钾和0.12mmol的18-冠醚-6加入1ml的干燥乙腈中,搅拌分散,再加入0.1mmol的1-丙基-2-乙氧酰基(5-三异丙基硅基)烯炔酮和0.5mmol的乙醇,置于氮气气氛中常温搅拌6h,搅拌机的转速为700rpm,再停止搅拌后加入5ml的水,再将反应液用乙酸乙酯萃取3次,合并有机相后用0.5g的无水硫酸镁干燥,过滤,取滤液进行减压蒸馏,再进行柱层析提纯,柱层析提纯采用的洗脱液由石油醚和乙酸乙酯按照体积比50:1组成,即得偕二溴烯基二氢呋喃类化合物(产率:74%)。
[0158]
本实施例合成的偕二溴烯基二氢呋喃类化合物的核磁共振氢谱图如图19所示,核磁共振碳谱图如图20所示,解谱分析(氢谱、碳谱、红外和质谱)如下:
[0159]1h nmr(400mhz,cdcl3):δ7.29(s,1h),4.28(q,j=7.1hz,2h),3.50-3.40(m,1h),
2-乙氧酰基(5-三异丙基硅基)烯炔酮将洗脱液中石油醚和乙酸乙酯的体积比由50:1调整为30:1以外,其余和实施例10完全一样。
[0177]
本实施例中偕二溴烯基二氢呋喃类化合物的产率为76%。
[0178]
本实施例合成的偕二溴烯基二氢呋喃类化合物的核磁共振氢谱图如图23所示,核磁共振碳谱图如图24所示,解谱分析(氢谱、碳谱、红外和质谱)如下:
[0179]1h nmr(400mhz,cdcl3):δ7.28(s,1h),4.26(q,j=7.1hz,2h),3.44(dq,j=9.1,7.1hz,2h),3.27(dq,j=9.1,7.0hz,2h),3.09(p,j=8.3hz,1h),2.38-2.26(m,1h),2.05(m,1h),1.83-1.76(m,2h),1.71-1.58(m,2h),1.32(t,j=7.1hz,3h),1.17(t,j=7.0hz,3h);
[0180]
13
c nmr(100mhz,cdcl3):δ161.6,155.2,137.2,133.3,117.8,70.0,61.3,59.5,40.4,22.45,22.2,17.8,15.2,14.2;
[0181]
ir(kbr)ν
max
:3394,2980,1721,1528,1236,773,682cm-1
;
[0182]
hrms(esi)calcd for c
14h18
br2nao4[m na]
:430.9472,found 430.9472;
[0183]
综上可知,本实施例合成的偕二溴烯基二氢呋喃类化合物的结构式如下:
[0184][0185]
实施例13:
[0186]
一种偕二溴烯基二氢呋喃类化合物,其在合成过程中除了将反应原料(5-三异丙基硅基烯炔酮类化合物)由1-丙基-2-乙氧酰基(5-三异丙基硅基)烯炔酮替换成1-甲基-2-乙氧酰基(5-三异丙基硅基)烯炔酮将洗脱液中石油醚和乙酸乙酯的体积比由50:1调整为40:1以外,其余和实施例10完全一样。
[0187]
本实施例中偕二溴烯基二氢呋喃类化合物的产率为79%。
[0188]
本实施例合成的偕二溴烯基二氢呋喃类化合物的核磁共振氢谱图如图25所示,核磁共振碳谱图如图26所示,解谱分析(氢谱、碳谱、红外和质谱)如下:
[0189]1h nmr(400mhz,cdcl3):δ7.30(s,1h),4.31(q,j=7.1hz,2h),3.56-3.42(m,1h),3.37-3.22(m,1h),1.79(s,3h),1.36(t,j=7.1hz,3h),1.22(t,j=7.0hz,3h);
[0190]
13
c nmr(100mhz,cdcl3):δ161.6,154.6,138.8,132.6,115.4,70.6,61.3,59.4,24.67,15.2,14.2;
[0191]
ir(kbr)ν
max
:3411,2928,1712,1387,1255,1088,955,741cm-1
;
[0192]
hrms(esi)calcd for c
11h14
br2nao4[m na]
:390.9154,found 390.9155;
[0193]
综上可知,本实施例合成的偕二溴烯基二氢呋喃类化合物的结构式如下:
[0194][0195]
实施例14:
[0196]
一种偕二溴烯基二氢呋喃类化合物,其在合成过程中除了将反应原料(5-三异丙基硅基烯炔酮类化合物)由1-丙基-2-乙氧酰基(5-三异丙基硅基)烯炔酮替换成1-甲基-2-丙氧酰基(5-三异丙基硅基)烯炔酮将洗脱液中石油醚和乙酸乙酯的体积比由50:1调整为20:1以外,其余和实施例10完全一样。
[0197]
本实施例中偕二溴烯基二氢呋喃类化合物的产率为79%。
[0198]
本实施例合成的偕二溴烯基二氢呋喃类化合物的核磁共振氢谱图如图27所示,核磁共振碳谱图如图28所示,解谱分析(氢谱、碳谱、红外和质谱)如下:
[0199]1h nmr(400mhz,cd3cn):δ7.35-7.27(m,1h),4.18(t,j=6.5hz,2h),3.41(dq,j=9.2,7.1hz,1h),3.29(dq,j=9.1,7.0hz,1h),1.75-1.70(m,5h),1.14(t,j=7.0hz,3h),0.99(t,j=7.4hz,3h);
[0200]
13
c nmr(100mhz,cd3cn):δ162.01,155.6,139.8,132.8,116.1,70.0,67.3,59.9,24.8,22.3,15.2,10.4;
[0201]
ir(kbr)ν
max
:3403,2926,1712,1387,1254,1161,955,740cm-1
;
[0202]
hrms(esi)calcd for c
12h16
br2nao4[m na]
:404.9309,found 404.9309;
[0203]
综上可知,本实施例合成的偕二溴烯基二氢呋喃类化合物的结构式如下:
[0204][0205]
实施例15:
[0206]
一种偕二溴烯基二氢呋喃类化合物,其在合成过程中除了将反应原料(5-三异丙基硅基烯炔酮类化合物)由1-丙基-2-乙氧酰基(5-三异丙基硅基)烯炔酮替换成1-甲基-2-丁氧酰基(5-三异丙基硅基)烯炔酮将洗脱液中石油醚和乙酸乙酯的体积比由50:1调整为30:1以外,其余和实施例10完全一样。
[0207]
本实施例中偕二溴烯基二氢呋喃类化合物的产率为82%。
[0208]
本实施例合成的偕二溴烯基二氢呋喃类化合物的核磁共振氢谱图如图29所示,核磁共振碳谱图如图30所示,解谱分析(氢谱、碳谱、红外和质谱)如下:
[0209]1h nmr(400mhz,cdcl3):δ7.29(s,1h),4.25(m,2h),3.54-3.42(m,1h),3.35-3.21(m,1h),1.78(s,3h),1.75-1.66(m,2h),1.52-1.40(m,2h),1.21(t,j=7.0hz,3h),0.98(t,j=7.4hz,3h);
[0210]
13
c nmr(100mhz,cdcl3):δ161.7,154.6,138.8,132.7,115.4,70.6,65.2,59.4,30.6,24.7,19.1,15.2,13.7;
[0211]
ir(kbr)ν
max
:3416,2927,2929,1712,1388,1254,1088,954cm-1
;
[0212]
hrms(esi)calcd for c
13h18
br2nao4[m na]
:418.9469,found 418.9465;
[0213]
综上可知,本实施例合成的偕二溴烯基二氢呋喃类化合物的结构式如下:
[0214][0215]
上述实施例为本发明较佳的实施方式,但本发明的实施方式并不受上述实施例的限制,其他的任何未背离本发明的精神实质与原理下所作的改变、修饰、替代、组合、简化,均应为等效的置换方式,都包含在本发明的保护范围之内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。
