1.本发明涉及球状且中空的钙镁磷酸盐颗粒、包括所述颗粒的组合物以及制备所述颗粒和组合物的方法。颗粒和包括所述颗粒的组合物可用于例如牙膏中,并通过增加矿化,尤其是增加深入牙本质小管的矿化来治疗过敏性牙齿(dentin tubules)。
背景技术:
2.牙本质过敏是一个普遍存在的临床相关问题,其表现为对外部热、机械、渗透或蒸发刺激的响应而出现的尖锐且突然的疼痛。如果由于牙釉质损失而导致牙本质保护层损失,或者如果由于牙龈回缩而导致牙骨质暴露,从而使牙本质小管向口腔环境开放,则可能发生过敏。牙釉质的损失可能是磨损、侵蚀或碎裂的结果。随着年龄的增长,牙龈回缩变得更加频繁,但由于例如过度刷牙、牙周袋缩小手术、过度使用牙线或对牙周病的继发反应,牙龈回缩也可能发生在较年轻的个体中。
3.非晶态钙磷酸盐(acp)为缺乏长程结晶有序的亚稳态相,因此比结晶态钙磷酸盐诸如羟基磷灰石(ha)和磷酸三钙(tcp)更易溶解。acp较高的溶解度使其更具生物活性,这是因为生物可利用的钙离子和磷酸根离子更容易释放到局部环境中。已经证明acp作为牙齿中磷灰石的前体,因此构成了自然矿化的重要部分。这使得开发用于生物医学应用的合成acp成为有趣的研究领域,但是由于其固有的亚稳定性以及后续在处理和产品制剂方面的限制,成功的方法少有报道。因此,许多商业上可获得的产品依赖于原位沉淀的acp,例如就在施用于牙齿表面之前通过双筒型递送来提供钙盐和磷酸盐。
4.为了在生物医学应用中使用合成acp,需要对其进行稳定化或进行配制以使得其不会过早结晶而丧失其部分生物活性。acp的稳定化可通过例如mg取代或使用乳衍生的酪蛋白磷酸肽(cpp)来实现。
5.wo2014/148997a1(wo’997)公开了用于治疗暴露的牙本质小管的基本不含锶的结晶态钙磷酸盐颗粒。然而,这些颗粒溶解性较差,因此不容易作为钙离子和磷酸根离子的来源。
6.cn107619031a公开了制备钙磷酸盐和磷酸镁球状颗粒的方法,包括使用湖水或海水作为钙离子和镁离子的来源。
7.需要在储存期间在其非晶体态下保持稳定的acp颗粒,以及包括该acp颗粒的组合物,其中颗粒是稳定的。此领域的另一个需求是具有受控形态且不含潜在过敏原的稳定的acp颗粒,该颗粒还能够大规模生产。
技术实现要素:
8.本发明旨在通过提供一种用于使acp颗粒稳定的组合物以及形成这种颗粒和组合物的可规模化且受控的连续制造方法来解决现有技术的问题。在制造过程中用成膏化合物直接使颗粒稳定增加了颗粒的稳定性和保质期,并有利于含有颗粒的产品制剂的配制。它还降低了颗粒聚集的风险,否则颗粒聚集会导致颗粒制剂不均匀,并降低颗粒渗入牙本质
小管的能力。此外,通过直接形成组合物而不是干燥、研磨和过筛以形成细粉,将与产品处理中的空气传播颗粒相关的任何安全问题降至最低。
9.牙本质小管的平均直径约为2μm,而本发明提供了更容易渗入牙本质小管,表现出与牙本质的适当亲和力的适当大小的颗粒,并且由于颗粒的非晶体态而允许更高的离子释放。这通过增加暴露的牙本质小管的矿化来促进对其更有效的治疗。此外,使用根据本发明的颗粒来矿化牙本质小管提供了更耐磨和更耐酸腐蚀的表面。通过形成含有颗粒的产品制剂,例如牙膏、脱敏凝胶、清漆或封闭剂,本发明可以容易地施用于治疗部位。根据本发明的用于制备颗粒的方法使得以受控的方式制备颗粒和组合物变得容易,在不同的生产规模下具有可重复的结果,并且该方法可以以连续的方式进行。
10.在第一方面,本发明涉及一种组合物,该组合物包括成膏化合物和xrd非晶态钙镁磷酸盐球状颗粒,颗粒具有中空芯和壳,其中颗粒为xrd非晶态,并且其中颗粒的壳包括15重量%~30重量%的钙、50重量%~70重量%的磷酸根、5重量%~11重量%的镁和1重量%至20重量%的结合水,并且其中ca/p摩尔比在0.70至1.20的范围内,并且其中(ca mg)/p摩尔比在1.00至1.70的范围内,并且其中颗粒具有在100nm至500nm的范围内的平均粒径,并且其中组合物中颗粒的量为25重量%~50重量%。
11.在第二方面,本发明涉及一种制备组合物的方法,包括以下步骤:
12.a.提供具有6至10的ph和第一温度的第一水性溶液,其中所述第一溶液含有磷酸二氢根离子和/或磷酸氢根离子以及优选选自钠和/或钾的一种或多种抗衡离子;
13.b.提供具有第二温度的第二水性溶液,其中所述第二溶液含有钙离子和镁离子以及优选选自氯、钠和/或钾的一种或多种抗衡离子;并且其中钙的量摩尔过量于镁;
14.c.将第一水性溶液、第二水性溶液或者第一水性溶液和第二水性溶液两者分别加热至第一高温和第二高温;
15.d.使第一水性溶液和第二水性溶液彼此接触,得到具有第三温度的第三水性溶液,其中第三水性溶液中磷酸根的量摩尔过量于钙和镁的总量;
16.e.使颗粒形成;
17.f.收集形成的颗粒;
18.g.可选地,使用合适的溶剂洗涤分离的颗粒;
19.h.可选地,在第五温度下使经洗涤的颗粒脱水,直到获得包括70重量%~95重量%,优选75重量%~85重量%游离水的浆料;
20.i.将球状颗粒与成膏化合物混合,其中组合物中的颗粒的量为25重量%~50重量%;
21.j.在第七温度下使球状颗粒和成膏化合物的混合物脱水;和
22.k.可选地,对球状颗粒和成膏化合物的混合物进行均质化以获得组合物。
23.在第三方面,本发明涉及根据本发明的组合物作为牙膏、脱敏凝胶(desensitizing gel)、漂白膏(bleaching paste)、牙科清漆(dental varnish)、洁牙膏(dental prophy paste)、窝沟封闭剂(pit and fissure sealant)、牙齿填充材料、盖髓材料(capping material)、漱口水(mouth wash)、齿间清洁工具、口香糖、植入物、骨移植材料、骨空隙填充材料中的成分的用途。
24.在第四方面,本发明涉及包括根据本发明组合物的牙膏、脱敏凝胶、漂白膏、封闭
剂、牙科清漆或洁牙膏,其中颗粒的量为0.5重量%至15重量%。
25.在第五方面,本发明涉及包括根据本发明组合物和过氧化脲的漂白膏,其中颗粒的量为3重量%~10重量%,过氧化脲的量为10重量%~20重量%。
26.这里公开的所有实施方式涉及本发明的所有方面,并且除非另有说明,所有实施方式可以组合。
附图说明
27.图1.钙镁磷酸盐颗粒的sem图像。
28.图2.钙镁磷酸盐颗粒的xrd图谱。这些颗粒为xrd非晶态的。
29.图3.钙镁磷酸盐颗粒的dls粒径分布。
30.图4.根据本发明方法的步骤1和2的示意图。
31.图5.根据本发明方法的步骤3和4的示意图。
32.图6.a)根据本发明方法的步骤5和6的示意图,以及b)根据本发明的方法的流程图。
33.图7.根据本发明的钙镁磷酸盐颗粒的ph缓冲能力。
34.图8.含有根据本发明钙镁磷酸盐颗粒的脱敏凝胶的ph缓冲能力。
35.图9.根据本发明的钙镁磷酸盐颗粒的ca、mg和p的离子释放曲线。a)最初6小时内的释放,b)持续释放,随后离子浓度降低,表明从溶液中沉淀。
36.图10.使用根据wo2014/148997a1的球状且中空的钙磷酸盐颗粒闭塞牙本质小管。
37.图11.用根据本发明的球状且中空的钙镁颗粒闭塞牙本质小管。
38.图12.每天用含有根据本发明的球状且中空的钙镁磷酸盐颗粒的脱敏凝胶治疗两周后,牙本质小管的闭塞和矿化。
39.图13.sem图像。每天用含氟牙膏和含有根据本发明的球状且中空的钙镁磷酸盐颗粒的脱敏凝胶治疗四次并持续四天后,牙本质小管的闭塞和矿化的牙本质表面和横截面。
40.图14.揭示根据本发明的钙镁磷酸盐颗粒在自来水中的降解和结晶的sem图像和xrd图谱。
41.图15.揭示根据本发明的钙镁磷酸盐颗粒在人工唾液中7、14和28天后的降解和结晶的sem图像和xrd图谱。
42.图16.根据本发明的含有40重量%钙镁磷酸盐颗粒、55重量%甘油和5重量%游离水的组合物储存18个月后的颗粒的sem图像和xrd图谱。
43.图17.根据本发明的含有40重量%钙镁磷酸盐颗粒、55重量%甘油和5重量%游离水的组合物加速储存12个月后的颗粒的sem图像和xrd图谱。
44.图18.在环境储存18个月后,根据本发明的脱敏剂凝胶中的钙镁磷酸盐颗粒的sem图像。
45.图19.在12个月加速储存后,根据本发明的脱敏剂凝胶中的钙镁磷酸盐颗粒的sem图像。
46.图20.根据本发明的钙镁磷酸盐颗粒在含有5%~50%过量游离水的组合物中储存20周后的sem图像。
47.图21.根据本发明的钙镁磷酸盐颗粒在含有5%~50%过量游离水的组合物中储
存长达20周后的xrd图谱。
48.图22.根据本发明的钙镁磷酸盐颗粒在环境条件下(20℃~25℃)以干细粉于封闭容器中储存11个月后的sem图像和xrd图谱。
具体实施方式
49.在本技术中,术语“平均粒径”对应于单个颗粒和形成小簇的融合颗粒的平均粒径。使用动态光散射(dls)测定平均粒径。
50.在本技术中,术语
‘
稳定的’是指在化学组成、和/或颗粒形态、和/或结晶度、和/或平均粒径、和/或颗粒表面积、和/或物理性能(对于组合物,诸如粘度)方面是稳定的。因此,稳定的颗粒或组合物可能意味着组合物或颗粒在长时间储存期间(例如12个月或相当更长的时间)保持基本相同。
51.在本技术中,术语“x射线衍射(xrd)非晶态”是指缺乏长程结晶有序的材料或颗粒。颗粒的结晶度或xrd非晶态使用cu-kα以大约0.02
°
的步长从7
°
到60
°
扫描2θ通过粉末x射线衍射来确定。晶体材料根据其晶面的排列反射x射线,并产生可识别的尖峰图谱,而xrd非晶态材料仅产生单个宽漫射峰。在本技术中,如果生成的图谱缺少可识别的尖峰,并且仅由宽漫射峰为特征,则颗粒将因此被分类为xrd非晶态。
52.在本技术中,术语“结合水”对应于与非晶态钙镁磷酸盐颗粒相关的水合水。结合水是颗粒化学式的一部分,即颗粒具有化学式cawmg
xhy
(po4)z·
nh2o。术语“游离水”表示不属于颗粒化学式的任何残留或过量的水。游离水可以例如为根据本发明组合物的一部分,或为在形成acp颗粒和/或组合物的过程中使用的水。
53.本发明的目的是提供促进牙本质小管快速且有效矿化的颗粒、组合物和含有颗粒的产品制剂。颗粒的目的不仅是机械地阻塞或填充牙本质小管的空隙,而且是矿化所述小管。不受理论的束缚,因此认为颗粒在递送到治疗部位时需要处于非晶态,以便快速且有效地释放钙离子和磷酸根离子,从而产生局部过饱和以及随后的羟基磷灰石样矿物质沉淀。因此,该目的包括提供在储存期间稳定(尤其是在结晶度方面)的颗粒。本发明人已经证明(实施例20),与根据wo2014/148997a1的更具结晶的钙磷酸盐颗粒相比,本发明使牙本质小管更快的闭塞。
54.参见图1,本发明的颗粒是具有中空核和壳的球状颗粒。壳优选是多孔的,以促进离子从颗粒本身更快地释放,或负载在颗粒中空芯内的物质的释放。孔的直径优选约为1nm~30nm。由于颗粒为xrd非晶态的,参见图2,它们更容易溶解并释放随后参与牙本质小管的再矿化的离子。在优选的实施方式中,颗粒的结晶度基本上为长程非晶态的,但是如果用例如高分辨率透射电子显微镜(hrtem)分辨,可以是短程(纳米)结晶的。不受理论束缚,平均粒径在100nm~500nm范围内的球状颗粒被认为比例如较大的球状颗粒或棒状或片状颗粒更容易深入渗入牙小管中。进一步认为,颗粒的x射线非晶态特征为镁取代、结合水和形成该颗粒的方法的结果。
55.钙、磷酸盐和镁为颗粒或颗粒的壳的主要组分,并且颗粒的壳包括15重量%~30重量%的钙、50重量%~70重量%的磷酸盐、5重量%~11重量%的镁和1重量%至20重量%的结合水,并且其中ca/p摩尔比在0.70至1.20的范围内,并且其中(ca mg)/p摩尔比在1.00至1.70的范围内。镁取代钙磷酸盐晶体结构中的钙。为了使颗粒形成良好的组合物或
制剂,并且为了使颗粒渗入直径约为2μm的牙本质小管中,颗粒的平均粒径在100nm至500nm的范围内。
56.优选的是,颗粒不要太小以至于表现出太大的正浮力而溶解太快,或太大以至于不能深入渗入到牙本质小管中,并且颗粒具有窄的尺寸分布,参见图3。本发明的优点在于组合物的颗粒不会团聚成较大的簇。在一个优选的实施方式中,平均粒径为150nm~450nm,更优选250nm~350nm。颗粒或颗粒的壳的含量或组成可以变化。例如,结合水的量或水合程度取决于制备颗粒或组合物时的干燥工艺。在优选的实施方式中,结合水的量为12重量%~16重量%。据认为,通过在颗粒中含有结合水,抑制了颗粒结晶的能力,取而代之的是颗粒保持非晶态。
57.颗粒中的钙含量优选18重量%或更高,或20重量%或更高,但优选25重量%或更低,或更优选23重量%或更低,更优选22重量%或更低。颗粒中的磷酸根(po4)含量优选55重量%或更高,或更优选58重量%或更高,但优选65重量%或更低,更优选62重量%或更低。颗粒中的镁含量优选6重量%或更高,或优选7重量%或更高,但优选9重量%或更低,更优选8重量%或更低。对于xrd非晶态颗粒,钙的镁取代度应该足够高,并且优选至少20mol%,更优选25mol%~50mol%,更优选30mol%~35mol%。
58.因为再矿化过程部分依赖于诸如钙、镁和磷酸根等离子的存在,所以这些离子在颗粒中的比例很重要。ca/p摩尔比优选0.8或更高,更优选0.9或更高,优选1.1或更低,更优选1.0或更低。(ca mg)/p摩尔比优选1.2或更高,更优选1.3或更高,优选1.5或更低,更优选1.4或更低。
59.在一个优选的实施方式中,颗粒的壳的含量包括21重量%~24重量%、优选22重量%~23重量%的钙,56重量%~60重量%、优选58重量%~59重量%的磷酸根,5重量%~8重量%、优选6重量%~7重量%的镁和12重量%~16重量%、优选13重量%~15重量%的结合水。ca/p比为0.8~1.1,优选0.9~1.0,并且(ca mg)/p比为1.2~1.5,优选1.3~1.4。
60.在另一优选的实施方式中,颗粒的壳的含量包括20重量%~26重量%的钙、52重量%~64重量%的磷酸根、5重量%~9重量%的镁和12重量%~16重量%的结合水,其中ca/p比为0.80~1.00且(ca mg)/p比为1.15~1.45。
61.本发明的颗粒可进一步含有其他离子,例如钠、钾、硅、锌和氟。所述离子的含量优选0.1重量%至3重量%,优选小于2重量%,更优选小于1重量%。在一个实施方式中,颗粒包括钠、钾和氟中的一种或多种。颗粒优选不含或基本不含锶。
62.使用氮气通过brunauer
–
emmett
–
teller(bet)法测定的平均表面积优选10m2/g~40m2/g,更优选15m2/g~35m2/g,更优选20m2/g~30m2/g。表面积越大使颗粒溶解越快,但颗粒在使用前和进入牙本质小管前不应溶解。
63.本发明人已经证明,本发明的颗粒在溶于水性介质时引起ph增加,这有利于羟基磷灰石矿物质在牙本质表面上和暴露的牙本质小管内成核和生长,参见实施例18。这是有利的,因为在使用过程中,颗粒会溶解在唾液或牙本质液中,因此可能促进羟基磷灰石矿物质的成核和生长。
64.为了使颗粒具有再矿化有效性,它们必须是稳定的,尤其在其xrd非晶态下是稳定的。优选地,颗粒在储存期间保持xrd非晶态至少24个月,即它们具有至少24个月的保质期。
通过这种方式,能够在一个地点制造颗粒,并将其运送到另一个地点用于产品配制而不会劣化再矿化性能。保持xrd非晶态颗粒的另一个优点是它们在使用前可以在货架上储存一段时间,因此不需要在制造时直接使用。
65.据认为,如果游离水的量减少,则颗粒保持在其xrd非晶态。这可以例如通过将颗粒与基本上不含水(诸如《10重量%)的成膏化合物一起配制以形成组合物来实现。本发明提供了形成这种包括均匀分散的颗粒、有限量的游离水且具有稳定性能的组合物的方法。形成所述组合物的这种方法在制备终产品(例如其中可加入组合物的牙膏)方面也是有利的。因此,有利的是,组合物具有良好的流动性和/或粘度,并且可以容易地与其它成分混合以制备例如牙膏。
66.本发明的颗粒优选用在或配制在组合物中,其中组合物优选为浆料或悬浮液的形式。除了颗粒之外,组合物还包括成膏化合物,该成膏化合物优选选自甘油、甘油三酯、聚乙二醇、丙二醇、聚丙二醇、聚乙烯醇、矿物油或液体石蜡,或它们的组合。在优选的实施方式中,成膏化合物为甘油。组合物还可以包括游离水,优选占组合物总含量的10重量%或更少的游离水,或更优选8重量%或更少的游离水,或甚至更优选5重量%或更少的游离水,但优选1重量%或更多,更优选2重量%或更多,甚至更优选3重量%或更多的游离水。
67.甘油因为广泛使用并被公认为药物、化妆品和个人护理产品中接受的成分,因此是优选的成膏化合物。甘油易溶于水,具有高沸点,并且在本发明所述的方法中,通过选择合适的干燥温度,可以选择性地保留在组合物中,同时蒸发掉过量的游离水。此外,甘油具有吸湿性,据认为这有助于提取在颗粒附近发现的游离水,从而提高颗粒的稳定性。水对甘油的亲和力进一步使一些游离水保留在组合物中,而不会显著损害保质期,进而有助于制备具有高颗粒含量的组合物,而其因为需要除去的游离水较少,仍然具有良好的粘度,并且使得制备工艺更容易且更经济。
68.非晶态钙磷酸盐为亚稳相,其倾向于结晶成更稳定形式的钙磷酸盐,诸如磷酸八钙或羟基磷灰石。根据本发明的非晶态钙磷酸盐颗粒通过镁取代而稳定,但是在环境条件下随时间推移仍可能会结晶,这取决于温度和湿度。根据本发明的具有颗粒和成膏化合物的组合物能够实现颗粒的长期稳定性。
69.本发明的组合物或含有颗粒的产品制剂优选具有非常有限量(诸如《10重量%)的游离水。一些与甘油结合的游离水甚至在干燥后仍可保留在组合物中。过量的游离水会降解颗粒,然后可形成具有更高结晶倾向的更小的颗粒。这种颗粒降解和结晶的过程对于颗粒的生物活性(引起牙本质小管的矿化和闭塞)是必不可少的,并且因此应该优选保存在到它们到达治疗部位或保存到它们与口腔中和牙本质表面的唾液和牙本质液接触。然而,完全不含水的组合物也是不理想的,因为它会太稠而不能在牙膏或类似物中正常起作用。通过使组合物或含有颗粒的产品制剂中保持少量,诸如《10重量%且》1重量%的游离水,组合物具有良好的流动性,同时仍保持颗粒的稳定性,即它们保持xrd非晶态达18个月或更长时间。在一个实施方式中,组合物中游离水的量为组合物或制剂总含量的10重量%或更少,或更优选含有8重量%或更少的游离水,或甚至更优选5重量%或更少的游离水,且优选1重量%或更多,更优选2重量%或更多,甚至更优选3重量%或更多的游离水。
70.该组合物或含有颗粒的产品制剂可以进一步优选含有添加剂,诸如氟化物、钾、过氧化氢或过氧化脲、木糖醇、黄原胶、香料(如薄荷醇)、聚合物增稠剂或防腐剂。因为氟化物
能强化牙齿,所以是优选的。钾为优选的神经去极化剂。过氧化氢和过氧化脲为优选的牙齿漂白剂。
71.在组合物中,颗粒优选以1重量%至50重量%的量或浓度存在。应该对该量进行调节,使得组合物的粘度、均匀性和处理性足以确保颗粒充分分散且不团聚。组合物中的颗粒浓度应该优选高到使每单位体积的值最大化,但是不能太高以至于粘度增加到妨碍正常处理或均质化的水平。在优选的实施方式中,组合物中颗粒的量为25重量%~50重量%。在另一优选的实施方式中,该量为35重量%~45重量%,更优选约40重量%。成膏化合物的量或浓度优选为至少50重量%,更优选至少55重量%。在一个优选的实施方式中,成膏化合物的浓度为55重量%~65重量%,优选约60重量%。在一个优选的实施方式中,组合物包括35重量%~45重量%、优选约40重量%的颗粒,50重量%~60重量%、优选约55重量%的甘油,和3重量%~8重量%、优选约5重量%的游离水。
72.成膏化合物、镁的存在,以及混合颗粒和成膏化合物并干燥以形成组合物的方法对于颗粒的长期稳定性和保质期是重要的。本发明人已经证明,本发明组合物中的颗粒在环境条件和加速条件下都是长期稳定的,参见实施例24和25。环境条件是指室温(20℃~25℃),加速条件是指40℃。
73.该组合物可用于制备含有颗粒的产品制剂,诸如牙齿或口腔护理产品。牙齿或口腔护理产品诸如牙膏、脱敏凝胶、漂白膏或凝胶、牙齿清漆、洁牙膏或封闭剂优选含有0.5重量%~15重量%的本发明颗粒,以及一些成膏化合物和添加剂。成膏化合物的浓度在不同的含有颗粒的产品制剂中有所不同,以为了不同应用的含有颗粒的产品制剂提供具有良好操作性质,诸如粘度、均匀性和可铺展性。在用于脱敏凝胶的优选的实施方式中,颗粒的浓度为5重量%~9重量%,更优选6重量%~8重量%,更优选约7.5重量%。成膏化合物的浓度优选为50重量%~90重量%,更优选60重量%~85重量%,更优选70~80重量%,以为产品提供具有良好操作性质,诸如粘度、均匀性和可铺展性。
74.含有颗粒的产品制剂的长期稳定性对于确保足够的产品保质期是重要的。例如,在储存期间,基本上保持颗粒外观和组合物稠度以及颗粒保持xrd非晶态是重要的。参见实施例26和27,本发明人已经证明了含有本发明颗粒和添加剂的脱敏凝胶在环境条件和加速条件下在延长的时间段中都是稳定的。脱敏凝胶优选含有5重量%~9重量%的颗粒。在优选的实施方式中,脱敏凝胶含有6重量%或更多,或7重量%或更多,且优选8重量%或更少或约7.5重量%的颗粒。
75.牙膏优选含有0.5重量%~6重量%的颗粒。在优选的实施方式中,牙膏含有0.5重量%或更多,或1重量%或更多的颗粒,但优选5重量%或更少,或4重量%或更少,或3重量%或更少。
76.清漆、洁牙膏或封闭剂优选含有5重量%~15重量%的颗粒。在优选的实施方式中,清漆、洁牙膏或封闭剂含有6重量%或更多、或8重量%或更多、或10重量%或更多的颗粒,但优选13重量%或更少、或11重量%或更少。
77.现在参见图4至图5,其中公开了制备本发明的球状且中空的颗粒的通用方法,其中步骤1示意性地表示了要求保护的方法中的a至b点,步骤2表示了c点,步骤3表示d至e点,步骤4表示f点。
78.在第一步骤中,提供ph为6至10,优选7至10,更优选7至8的第一水性溶液,并且其
中该溶液具有第一温度。第一水性溶液包括磷酸二氢根离子和/或磷酸氢根离子、抗衡离子和可选的额外离子。抗衡离子优选为钠离子和/或钾离子。额外离子可选自钠、钾、氯、硅、锌和氟,或它们的组合。第一水性溶液中h2po4:hpo4的摩尔比优选在0~100:75~600的范围内,更优选1~2:4~6。在优选的实施方式中,磷酸二氢根的浓度为0至100mm,或更优选20mm至80mm。磷酸氢根在第一水性溶液中的浓度优选为30mm至300mm,更优选为80mm至250mm。第一水性溶液中磷酸根的总浓度优选为60mm至800mm。
79.还提供了具有第二温度的第二水性溶液,其包括钙离子和镁离子、抗衡离子和可选的额外离子。抗衡离子优选为氯离子、钠离子和/或钾离子。额外离子可以选自钠、钾、氯、硅、锌和氟,或它们的组合。第二水性溶液中钙的浓度优选为10mm~200mm,镁的浓度优选为5mm至120mm。在优选的实施方式中,钙浓度为20mm~100mm,更优选30mm~70mm。在另一优选的实施方式中,镁含量为10mm~60mm,更优选12mm~40mm。在第二水性溶液中,钙优选摩尔过量于镁。钙与镁的摩尔比优选为4:1至1.05:1,更优选2:1至4:3,或更优选约5:3。
80.在一个优选的实施方式中,第一水性溶液中磷酸根的量摩尔过量于第二水性溶液中钙和镁的总量。在优选的实施方式中,磷酸根与钙离子和镁离子的摩尔比(po4:(ca mg))为1.5:1或更高,优选2:1或更高。在另一优选的实施方式中,摩尔比为2:1至6:1,或更优选2.2:1至5:1。
81.第一水性溶液和第二水性溶液分别具有第一温度和第二温度,第一温度和第二温度优选各自为10℃~35℃,更优选20℃~30℃,更优选20℃~25℃。第一水性溶液和第二水性溶液中的水可以是自来水或优选纯化水,更优选去离子水、蒸馏水、双蒸水或超纯水。尽管将本发明描述为使用两种水性溶液,即第一水性溶液和第二水性溶液,但是技术人员应当理解第一水性溶液和第二水性溶液实际上可以各自是两种或更多种水性溶液或子溶液。
82.然后,将两种水性溶液中的至少一种,即第一水性溶液和/或第二水性溶液分别加热至第一高温和第二高温。在一个实施方式中,将第一水性溶液和第二水性溶液分别加热至第一高温和第二高温。在图4(右手侧)中,两种溶液都使用热交换器加热,但是可以使用任何合适的加热装置。不受理论的束缚,认为加热步骤对于在电解质溶液中形成纳米气泡(持久的含气腔)是重要的,当两种溶液接触时,两种溶液的离子在纳米气泡上沉淀并形成本发明颗粒的中空结构。对两种溶液中的至少一种进行加热应当使各自温度升高优选至少40℃,更优选至少50℃。换句话说,第一温度/第二温度与第一高温/第二高温之间分别为第一温差和第二温差。在优选的实施方式中,第一温差为40℃~80℃,优选为50℃~70℃。在另一优选的实施方式中,第二温差为40~80℃,优选为50℃~70℃。第一高温和第二高温则各自优选为至少60℃,更优选70℃~90℃。
83.然后使其中至少一种已被加热的两种溶液彼此接触,产生具有第三温度的第三水性溶液(图5,步骤3)。这可以通过将溶液之一加入到另一种溶液中来完成,优选将第二溶液加入到第一溶液中来完成,但是优选以连续的方式,且优选以连续流动的方式使两种溶液接触。通过以连续流动的方式使它们接触,促进了更有效的生产,使得更容易按比例放大所形成颗粒的产量,并提供对该方法的更好控制。在一个实施方式中,使两种溶液(第一水性溶液和第二水性溶液)在歧管或三通歧管中接触,优选在y形歧管(y形截面)中接触,如图5(左手侧)示意性所示。当两种溶液彼此接触时,沉淀或多或少会立即发生(《10秒),并且使该沉淀持续合适的一段时间,该时间取决于实际限制以及对所需性质的针对性细微调整,
但通常为1秒~600秒。如果补充起始溶液,则可以继续其中混合两种溶液的连续流动过程,允许连续回收形成的颗粒。当第一溶液和第二溶液接触时,磷酸根的量摩尔过量于钙和镁的总量(po4》(ca mg))。不受理论的束缚,在第三水性溶液中,磷酸根过量于钙和镁的总量将增加缓冲能力,这进而限制了结晶钙磷酸盐相的形成,参见实施例12。在优选的实施方式中,在第三水性溶液中,磷酸根与钙和镁的摩尔比(po4:(ca mg))为1.5:1或更高,优选2:1或更高。在另一优选的实施方式中,该摩尔比为2:1至6:1,或更优选2.2:1至5:1。在优选的实施方式中,在第三水性溶液中,钙摩尔过量于镁。钙与镁的摩尔比优选为4:1至1.05:1,更优选2:1至4:3,或更优选约5:3。
84.在一个优选的实施方式中,第三温度为70℃~95℃,更优选80℃~85℃,这是因为反应的质量产率更高,并且当》100℃的温度时,结晶程度会增加,参见实施例16。当使第一水性溶液和第二水性溶液接触时,第一水性溶液和第二水性溶液之间的体积比优选为2:1至1:2,优选1.10:1至1:1.10,或优选1.05:1至1:1.05,或更优选1:1。
85.形成沉淀的颗粒和水性溶液的悬浮液,然后使用任何合适的技术分离和/或收集沉淀的颗粒。优选地,使用合适的过滤技术、离心和/或沉降和倾析来完成分离和/或收集。然后优选地,使用任何合适的溶剂,诸如水或醇来洗涤经分离和/或收集的颗粒。优选地,使用纯化水进行洗涤,更优选使用去离子水、蒸馏水、双蒸水或超纯水。洗涤可优选在50℃~90℃,更优选70~80℃的第四温度下进行。为了确保颗粒是干净的且没有不良的离子残留物,可重复洗涤步骤。然后可以优选通过离心或更优选在升高的温度和/或减压下使经分离和/或收集且经洗涤的颗粒脱水或部分脱水。在优选的实施方式中,脱水/部分脱水或干燥在至少50℃,优选50℃~150℃,更优选60℃~110℃,更优选60℃~80℃或约80℃的第五温度下进行。优选进行脱水或部分脱水直到获得含有70重量%~90重量%,更优选75重量%~85重量%游离水的浆料。在这个阶段,颗粒仍然很好地悬浮并均匀地分散在浆料中,并且该浆料可以容易地与成膏化合物混合以形成基本上没有任何团聚物的湿组合物。在这一阶段进一步使浆料脱水或彻底干燥颗粒会导致形成较大的颗粒团聚物,而这些团聚体越来越难以混合和均匀悬浮在成膏化合物中以获得光滑(smooth)且自由流动的组合物。本发明人发现,当将干燥或基本干燥的经分离的颗粒与成膏化合物混合时,即使使用精细研磨和过筛的粉末,也基本上不可能获得同样均匀、光滑且自由流动的组合物。避免干燥和研磨来形成用于分散在成膏化合物或产品制剂中的细粉也降低了与粉末处理相关的健康和安全风险。
86.在不存在成膏化合物的情况下干燥颗粒也可能无意中增加了结晶度,并促使形成可需要高能量来分散的较硬颗粒,进而危及颗粒的完整性。当在环境条件下以细粉的形式储存时,本发明颗粒的稳定性受到限制,参见实施例30,这进一步强调了在制造阶段就与成膏化合物形成组合物的重要性。
87.在一个实施方式中,尽管存在上述缺点,但如果需要的话,在优选50℃~150℃,更优选60℃~110℃的第六温度下,对形成的、经分离的和可选洗涤和/或脱水的颗粒进行进一步干燥以形成粉末。
88.现在转向图6a,其示意性地示出了本发明组合物的制备。通过制备本发明的颗粒并使该颗粒与成膏化合物混合来完成本发明组合物的制备。优选在使颗粒部分脱水后,即在颗粒仍处于悬浮且优选均匀分布在浆料中的状态下进行颗粒与成膏化合物的混合。在与
成膏化合物混合之前,浆料优选包括10重量%~30重量%的颗粒和70重量%~90重量%的水,更优选15重量%~25重量%的颗粒和75重量%~85重量%的水。成膏化合物优选选自甘油、甘油三酯、聚乙二醇、丙二醇、聚丙二醇、聚乙烯醇、矿物油或液体石蜡。在优选的实施方式中,成膏化合物为甘油。在优选的实施方式中,成膏化合物基本上不含水(诸如《10重量%的水)。
89.优选对颗粒、游离水和成膏化合物的所得组合物进行脱水,以尽可能多地除去游离水,并形成具有长期稳定性的稳定且均匀的组合物。在一个实施方式中,游离水的量小于10重量%,优选小于5重量%,更优选水小于3重量%。在组合物中保留少量的水可以有助于形成具有合适粘度的光滑且均匀的组合物。在一个优选的实施方式中,组合物中游离水的量为0.1重量%或更多,或0.5重量%或更多,或1重量%或更多,但优选8重量%或更少,或5重量%或更少。优选在第七温度和/或减压下,对球状且中空的颗粒和成膏化合物的所得混合物进行脱水,其中第七温度优选在50℃~150℃的范围内,更优选60℃~90℃。减压优选为500毫巴或更低。优选地,在脱水期间和/或之后,优选通过机械方法对混合物进行均质化,以形成光滑的组合物。所得的混合物可以例如使用机械均质化设备如转子-定子均化器来均质化1分钟至30分钟。组合物的制备示意性地总结在图6b中。如图所示,该方法包括至少三个步骤:
90.10:1:使如上所述制备的acp颗粒部分脱水,使颗粒脱水直到它们形成含有10重量%~30重量%颗粒和70重量%~90重量%水的浆料;
91.10:2:将含有颗粒的浆料与成膏化合物混合,直到形成均匀的混合物;和
92.10:3:在第七温度和/或减压下使步骤10:2中形成的组合物脱水,直到水的量为8重量%或更少,或5重量%或更少,或2重量%或更少。
93.甘油的吸湿性能够使其成为根据本发明的非晶态钙镁磷酸盐颗粒的有效防腐剂。有利的是,对于包含甘油的组合物,即使在包含过量游离水的情况下,acp颗粒也可以在储存期间保持xrd非晶态,参见实施例28。
94.牙齿漂白或美白为现代美容牙科中的常见实践,通常使用过氧化氢或过氧化脲来去除色斑并增强牙齿的外观和白度。不同的市场目前允许在美白产品中使用不同强度的过氧化物,但典型的外卖产品的制剂含有16%的过氧化脲,相当于5%~6%的过氧化氢。牙齿美白的常见副作用为牙齿敏感性增加,并且牙釉质可能由于处理而软化,导致牙齿强度降低。因此,令人感兴趣的提供有效的美白产品和治疗,它们还可降低牙齿敏感性并通过矿化增加牙釉质的硬度。因此,如实施例29所示,根据本发明的组合物不会对牙齿美白产品的漂白过程产生不利影响,这可能也是一个优点。
95.实施例
96.实施例1
97.按照图4中的步骤1,用浓缩物125mm nacl、160mm na2hpo4和30mm kh2po4制备第一水性溶液(ph 7.4),并且用浓缩物125mm nacl、25mm cacl2和15mm mgcl2制备第二水性溶液。按照图4中的步骤2,通过板式热交换器将两种溶液分别从室温加热到85℃,然后按照图5中的步骤3,以1:1的体积比进行流动混合,以在85℃下形成沉淀物。按照图5中的步骤4,使用细网滤布通过过滤收集沉淀物,然后在70℃下使用去离子水进行洗涤,随后利用真空进行部分脱水。按照图6中的步骤5,将含有约20重量%沉淀颗粒和80重量%水的浆料与甘油
混合,以形成颗粒和甘油干重比为2:3的均匀混合物。然后按照图6中的步骤6,在80℃下于强制对流烘箱中干燥混合物以除去水,并通过机械方法均质化以形成光滑、粘稠的组合物。组合物的干含量为98重量%。
98.形成的颗粒形状为球状,由多孔壳和中空内部结构组成。单个球体直径在100nm~300nm范围内,而融合球体的簇和组成物在200nm~500nm范围内。颗粒的代表性扫描电子显微镜(sem)图像如图1所示。
99.颗粒的xrd分析显示它们为非晶态的。不存在特征峰,仅在2θ=30
°
附近强度大幅增加,表明存在非晶态钙磷酸盐,参见图2。
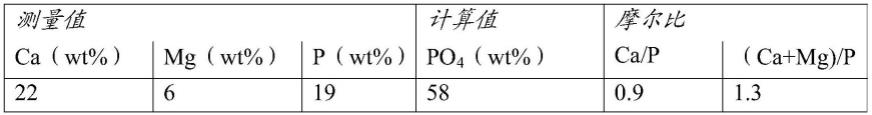
100.通过电感耦合等离子体发射光谱法(icp-oes)测定颗粒的元素分析,并且证实了表1中示出的含量。假设所有的p都以po4的形式存在,po4的计算含量以及ca/p和(ca mg)/p摩尔比也显示在表中。ca和mg的测量值结合po4的计算值总计为86重量%,使得大约14重量%的结合h2o。基于实施例中的数据,提出了颗粒的平衡化学式:
101.ca
2.7
mg
1.3
h(po4)3*4h2o
102.表1.形成的颗粒的icp-oes元素分析结果。
[0103][0104]
wt%表示重量%。
[0105]
将形成的颗粒悬浮在乙醇中并使用超声波分散聚集的颗粒后,通过dls测定粒径分布。z-平均粒径为370nm,其数量分布如图3所示。
[0106]
根据使用氮气的bet方法测定的材料的表面积为24m2/g。
[0107]
实施例2
[0108]
用浓缩物500mm nacl、640mm na2hpo4和119mm kh2po4制备第一水性溶液(ph7.4)。用浓缩物500mm nacl、100mm cacl2和60mm mgcl2制备第二水性溶液。将两种溶液分别加热至85℃,然后以1:1的体积比混合以形成沉淀物。通过过滤收集沉淀物,洗涤并用sem和xrd分析。形成的颗粒在形状、尺寸和外观上与图1所示的颗粒相似,并且为xrd非晶态,类似于图2所示的谱图。
[0109]
实施例3
[0110]
用100mm nacl、128mm na2hpo4和24mm kh2po4制备第一水性溶液(ph 7.4)。用100mm nacl、20mm cacl2和12mm mgcl2制备第二水性溶液。将两种溶液分别加热至70℃,然后以1:1的体积比混合以形成沉淀物。通过过滤收集沉淀物,洗涤并用sem和xrd分析。形成的颗粒在形状、尺寸和外观上与图1所示的颗粒相似,并且为xrd非晶态,类似于图2所示的谱图。
[0111]
实施例4
[0112]
用100mm nacl、128mm na2hpo4和24mm kh2po4制备第一水性溶液(ph 7.4)。用100mm nacl、20mm cacl2和12mm mgcl2制备第二水性溶液。将两种溶液分别加热至80℃,然后以1:1的体积比混合以形成沉淀物。通过过滤收集沉淀物,洗涤并用sem和xrd分析。形成的颗粒在形状、尺寸和外观上与图1所示的颗粒相似,并且为xrd非晶态,类似于图2所示的谱图。
[0113]
实施例5
[0114]
用100mm nacl、128mm na2hpo4和24mm kh2po4制备第一水性溶液(ph 7.4)。用100mm nacl、20mm cacl2和12mm mgcl2制备第二水性溶液。将两种溶液分别加热至90℃,然后以1:1的体积比混合以形成沉淀物。通过过滤收集沉淀物,洗涤并用sem和xrd分析。形成的颗粒在形状、尺寸和外观上与图1所示的颗粒相似,并且为xrd非晶态,类似于图2所示的谱图。
[0115]
实施例6
[0116]
用160mm na2hpo4和30mm kh2po4制备第一水性溶液(ph 7.4)。用50mm cacl2和30mm mgcl2制备第二水性溶液。将两种溶液分别加热至85℃,然后以1:1的体积比混合以形成沉淀物。通过过滤收集沉淀物,洗涤并用sem和xrd分析。形成的颗粒在形状、尺寸和外观上与图1所示的颗粒相似,并且为xrd非晶态,类似于图2所示的谱图。
[0117]
实施例7
[0118]
用100mm nacl和150mm kh2po4制备第一水性溶液(ph 4.7)。用100mm nacl、20mm cacl2和12mm mgcl2制备第二水性溶液。将两种溶液分别加热至85℃,然后以1:1的体积比混合以形成沉淀物。通过过滤收集沉淀物,洗涤并用sem和xrd分析。沉淀的颗粒是圆形的,但不是球状的。颗粒具有粗糙的表面特征,并且看起来不是中空的。xrd分析表明,颗粒为结晶白磷钙石,磷酸三钙(tcp)的镁离子取代形式。
[0119]
实施例8
[0120]
用100mm nacl、75mm na2hpo4和75mm kh2po4制备第一水性溶液(ph 6.4)。用100mm nacl、20mm cacl2和12mm mgcl2制备第二水性溶液。将两种溶液分别加热至85℃,然后以1:1的体积比混合以形成沉淀物。通过过滤收集沉淀物,洗涤并用sem和xrd分析。形成的颗粒在形状、尺寸和外观上与图1所示的颗粒相似,并且为xrd非晶态,类似于图2所示的谱图。
[0121]
实施例9
[0122]
用100mm nacl、145mm na2hpo4和4.8mm kh2po4制备第一水性溶液(ph 8.1)。用100mm nacl、20mm cacl2和12mm mgcl2制备第二水性溶液。将两种溶液分别加热至85℃,然后以1:1的体积比混合以形成沉淀物。通过过滤收集沉淀物,洗涤并用sem和xrd分析。形成的颗粒在形状、尺寸和外观上与图1所示的颗粒相似,并且为xrd非晶态,类似于图2所示的谱图。
[0123]
实施例10
[0124]
用75mm na2hpo4制备第一水性溶液(ph 9.3)。用20mm cacl2和12mm mgcl2制备第二水性溶液。将两种溶液分别加热至85℃,然后以1:1的体积比混合以形成沉淀物。通过过滤收集沉淀物,洗涤并用sem和xrd分析。形成的颗粒在形状、尺寸和外观上与图1所示的颗粒相似,并且为xrd非晶态,类似于图2所示的谱图。
[0125]
实施例11
[0126]
用190mm na2hpo4制备第一水性溶液(ph 9.4)。用50mm cacl2和30mm mgcl2制备第二水性溶液。将两种溶液分别加热至85℃,然后以1:1的体积比混合以形成沉淀物。通过过滤收集沉淀物,洗涤并用sem和xrd分析。形成的颗粒在形状、尺寸和外观上与图1所示的颗粒相似,并且为xrd非晶态,类似于图2所示的谱图。
[0127]
实施例12
[0128]
用60mm na2hpo4制备第一性水溶液(ph 9.3)。用50mm cacl2和30mm mgcl2制备第二水性溶液。将两种溶液分别加热至85℃,然后以1:1的体积比混合以形成沉淀物。通过过滤收集沉淀物,洗涤并用sem和xrd分析。收集的颗粒不是球状的,也不是中空的,而是由不规则且看似致密的表面粗糙的颗粒组成。该材料的xrd分析表明,结晶相是白磷钙石。该结果与实施例7中证实的在低ph下形成的颗粒类型一致。与该实施例的不同之处在于磷酸盐溶液的初始ph较高,且在于hpo
42-并未过量于ca
2
和mg
2
的含量,引起以下反应:
[0129]
3-xca
2
xmg
2
2hpo
42-→
ca
3-x
mg
x
(po4)2 2h
[0130]
没有过量的hpo
42-,体系将失去其缓冲能力,产物h
将降低ph并促使形成的tcp结晶颗粒,其具有的ca/p比高于实施例1中形成和表征的颗粒。
[0131]
实施例13
[0132]
用220mm na2hpo4制备第一水性溶液(ph 9.4)。用60mm cacl2和36mm mgcl2制备第二水性溶液。将两种溶液分别加热至85℃,然后以1:1的体积比混合以形成沉淀物。通过过滤收集沉淀物,洗涤并用sem和xrd分析。形成的颗粒在形状、尺寸和外观上与图1所示的颗粒相似,并且为xrd非晶态,类似于图2所示的谱图。滤液的ph为7.0,表明hpo
42-过量到足以维持中性ph。
[0133]
该实施例产生的颗粒质量为实施例1中颗粒质量的两倍。
[0134]
表2:实施例1~13中用于合成颗粒的工艺参数和组成的汇总表。
[0135][0136]
在结果列中:spher.part表示球状颗粒,amorph.表示非晶态。
[0137]
实施例14
[0138]
用0.5mm kcl、200mm nacl、16mm na2hpo4和3mm kh2po4制备第一水性溶液。用0.5mm kcl、200mm nacl、2.5mm cacl2和1.5mm mgcl2制备第二水性溶液。
[0139]
在第一个实验中,将两种溶液分别加热至45℃。然后将第一溶液(磷酸盐)与第二溶液(钙和镁)等体积混合以形成沉淀物,即以与图4和5中的步骤2和3相比的替代方式。通过过滤收集沉淀物,洗涤并用sem和xrd分析。形成的颗粒为球状颗粒和微晶的混合物,通过xrd鉴定为透钙磷石(cahpo4*2h2o)。
[0140]
在第二个实验中,将两种溶液分别加热至65℃。然后将第一溶液(磷酸盐)与第二溶液(钙和镁)等体积混合以形成沉淀物。通过过滤收集沉淀,洗涤并用sem和xrd分析。形成
的颗粒在形状、尺寸和外观上与图1所示的颗粒相似,并且为xrd非晶态,类似于图2所示的谱图。
[0141]
在第三个实验中,将两种溶液分别加热至85℃。然后将第一溶液(磷酸盐)与第二溶液(钙和镁)等体积混合以形成沉淀物。通过过滤收集沉淀物,洗涤并用sem和xrd分析。形成的颗粒在形状、尺寸和外观上与图1所示的颗粒相似,并且为xrd非晶态,类似于图2所示的谱图。与65℃下进行的实验相比,在85℃下进行的反应的质量产率增加。
[0142]
这一系列实验表明存在优选的温度窗口,在该温度窗口中,沉淀反应就形状、大小、外观和质量产量的一致性而言是稳定且有效的。
[0143]
实施例15
[0144]
用0.5mm kcl、200mm nacl、16mm na2hpo4和3mm kh2po4制备第一水性溶液(ph7.4)。用0.5mm kcl、200mm nacl、2.5mm cacl2和0.75mm mgcl2制备第二水性溶液。将两种溶液分别加热至85℃。然后将第一溶液(磷酸盐)与第二溶液(钙和镁)等体积混合以形成沉淀物。通过过滤收集沉淀物,洗涤并用sem和xrd分析。不存在球状颗粒,但是形成了在xrd中鉴定为白磷钙石的不良结晶相。
[0145]
在第二个实验中,用0.5mm kcl、200mm nacl、16mm na2hpo4和3mm kh2po4制备第一水性溶液。用0.5mm kcl、200mm nacl和2.5mm cacl2制备第二水性溶液。将两种溶液分别加热至85℃。然后将第一溶液(磷酸盐)与第二溶液(钙和镁)等体积混合以形成沉淀物。通过过滤收集沉淀物,洗涤并用sem和xrd分析。不存在球状颗粒,但是形成在xrd中鉴定为磷酸三钙(tcp)的片状晶体。
[0146]
这些实验表明,镁离子作为非晶相的稳定剂,并且需要足够程度的镁离子取代来保持非晶相。
[0147]
实施例16
[0148]
使用微波合成器来评估替代的加热方法和扩展的工艺温度范围。对于这些实验,用0.5mm kcl、200mm nacl、16mm na2hpo4、3mm kh2po4、2.5mm cacl2和1.5mm mgcl2制备单一溶液。在不同的实验中,将溶液置于密封的玻璃小瓶中,并利用微波辅助加热将其从室温(23℃)快速(《2分钟)加热至50℃、70℃、90℃、100℃、120℃或140℃。通过sem分析获得的沉淀物,结果显示在所有情况下都形成了球状且中空的颗粒,与图1所示的颗粒相当。在100℃或以上的温度下,颗粒具有稍微粗糙的表面特征,并显示出结晶的迹象。
[0149]
这些实验证明,可以使用替代的加热方式来合成颗粒,并且颗粒可以根据加热方式在较宽的温度窗口内来合成。
[0150]
实施例17
[0151]
将本发明的含有40重量%球状且中空的钙镁磷酸盐颗粒和60重量%甘油的组合物与去离子水混合,以评估ph缓冲能力。在实验中,将0.5g组合物加入到500ml水中,得到0.1重量%的浓度。监测组合物溶解前30分钟内溶液的ph,结果示出在图7中。通过加入组合物,溶液的ph在5分钟内从大约7.5急剧增加到9.5,之后保持稳定。
[0152]
这种离子的快速释放是某些牙科材料和产品的重要特征。因为ph的局部增加促进了羟基磷灰石的成核和生长,有益于牙釉质和牙本质的再矿化。
[0153]
实施例18
[0154]
将本发明的含有7.5重量%的球状且中空的钙镁磷酸盐颗粒的脱敏凝胶以0.1重
量%的浓度混合到ph 4和ph 7.9的水性溶液中。分别用0.1m hcl和0.1m naoh调节起始溶液的ph。监测凝胶溶解前30分钟内溶液的ph,结果示出在图8中。证实了,在两种情况下凝胶都使ph升高,分别从ph 4.0升高到8.6,和从ph 7.9升高到ph 9.3。以用惰性玻璃颗粒代替钙镁磷酸盐的相应凝胶进行类似的试验,其未产生ph变化,表明是颗粒引起了这种效果。
[0155]
脱敏凝胶旨在通过对暴露的牙本质小管进行再矿化而作为牙本质过敏的治疗选择。由颗粒引起的ph增加将促进羟基磷灰石矿物质在牙本质表面和暴露的牙本质小管内成核和生长。
[0156]
实施例19
[0157]
将本发明球状且中空的钙镁磷酸盐颗粒以10mg/ml的浓度分散在0.05m tris-hcl缓冲液(ph 7.4)中,并在37℃下储存长达8周。通过过滤颗粒和用icp-oes分析滤液来监测钙离子、镁离子和磷酸根离子从颗粒中的释放。在分析前稀释滤液。结果示出在图9中,并证实了释放的特征在于初始爆发,随后离子浓度降低,对于ca最为明显。离子的初始爆发释放将促进快速矿化过程,并且随后滤液中钙含量的降低表明钙磷酸盐从溶液中再沉淀,但是ca/p比高于比原始颗粒的ca/p比,即形成了ca/p比更接近羟基磷灰石的钙磷酸盐。
[0158]
实施例20
[0159]
制备含有5重量%的本发明球状且中空的钙镁磷酸盐颗粒的凝胶,用于评估牙本质闭塞和再矿化性能。还制备了含有5重量%根据先前发明(wo 2014/148997 a1)的中空钙磷酸盐颗粒的类似凝胶,并进行平行测试以比较结果。
[0160]
在这项研究中,从提取的人类来源的恒磨牙上切下1mm薄的牙本质样本,并在磷酸中腐蚀以暴露小管。通过用软毛牙刷刷拭,将凝胶施用于暴露的牙本质表面,每天两次,持续长达7天。牙本质样本在刷拭之间储存在37℃的人工唾液中。在最终的凝胶施用后,干燥样本并准备在sem中评估。用凝胶处理4天和7天后牙本质表面的外观示出在图10和图11中。与根据wo 2014/148997制备的颗粒相比,根据本发明的颗粒引起更快和更完全的小管闭塞。这归因于球状颗粒的较小平均直径,使得它们更容易渗入小管,以及本颗粒的非晶态特性,使得它们更快速地溶解和释放使表面矿化的生物活性离子。
[0161]
实施例21
[0162]
评估由7.5重量%的本发明球状且中空的钙镁磷酸盐颗粒配制的脱敏凝胶的牙本质闭塞和再矿化性能。在这项研究中,从提取的人类来源的恒磨牙上切下1mm薄的牙本质样本,并在磷酸中腐蚀以暴露小管。然后每天用凝胶刷拭牙本质样本两次,每侧一分钟,共持续14天。每次刷拭事件后,用去离子水冲洗样品,并储存在37℃的人工唾液中直到下一次刷拭事件。处理完成后,真空干燥样品并在sem中评估样品。
[0163]
处理结果示出在图12中,证实了暴露的牙本质小管完全闭塞。对横截面的评估表明,矿化发生在小管深(》60μm)处。通过处理实现的闭塞程度能够可靠地完全消除小管内的流体运动,从而为过敏性牙齿提供有效的疼痛缓解。
[0164]
实施例22
[0165]
评估由7.5重量%的本发明球状且中空的钙镁磷酸盐颗粒配制的脱敏凝胶在与含氟牙膏结合施用时的牙本质闭塞和再矿化性能。在这项研究中,从提取的人类来源的恒磨牙上切下1mm薄的牙本质样本,并在磷酸中腐蚀以暴露小管。首先用标准含氟牙膏刷拭牙本质样本,然后用脱敏凝胶刷拭。该事件在四天内每天重复四次。牙本质样本在两次刷拭之间
储存在37℃的人工唾液中。处理完成后,真空干燥样品并在sem中评估样品。
[0166]
处理结果示出在图13中,证实了暴露的小管被致密的矿化层完全闭塞。牙本质样品的横截面评估表明,小管内沉积的矿物质由高纵横比的微晶体组成,许多小管在距离牙本质表面超过20μm处完全闭塞。
[0167]
实施例23
[0168]
将本发明球状且中空的钙镁磷酸盐颗粒在37℃下储存在市政自来水和人工唾液中长达28天。目的是表征颗粒在这一时间段内于不同介质中的降解和结晶。
[0169]
在7、14和28天后取出颗粒样品来在sem中进行评估,并在28天后进行xrd评估。
[0170]
自来水的结果示出在图14中,证实了颗粒保持其特征形态长达两周。四周后,颗粒降解并部分结晶成羟基磷灰石。在人工唾液中,颗粒在一周内开始降解和重结晶,参见图15。两周后没有球状颗粒留下,四周后形成了较大的片状晶体。结晶相经鉴定羟基磷灰石和白磷钙石,均为人体硬组织中天然存在的矿物质。
[0171]
实施例24
[0172]
将根据本发明的含有40重量%球状且中空的钙镁磷酸盐颗粒、55重量%甘油和5重量%游离水的组合物在室温(20℃~23℃)下于密闭容器中储存长达18个月,之后评估组合物和颗粒的特征以确定颗粒的稳定性。
[0173]
发现,该组合物的特征得以保持,并且颗粒的关键性能诸如形态、结晶度、粒径和化学组成得以保留。sem和xrd数据参见图16。结果表明,根据本发明的含有颗粒和甘油的组合物是稳定的,并且该组合物的保质期为至少18个月。
[0174]
实施例25
[0175]
化学反应和相变,诸如非晶态钙磷酸的降解或结晶在高温下会加速。将根据本发明的含有40重量%球状且中空的钙镁磷酸盐颗粒、55重量%甘油和5重量%游离水的组合物在40℃下于密闭容器中储存长达12个月来评估加速条件下的稳定性。然后评估组合物和颗粒的特征以确定稳定性。
[0176]
发现,该组合物的特征得以保持,并且颗粒的关键性能诸如形态、结晶度、粒径和化学组成得以保留。sem和xrd数据参见图17。对40℃下的储存条件采用保守加速因子3,那么该结果表明根据本发明的具有颗粒和甘油的组合物是稳定的,并且具有36个月的预计保质期。
[0177]
实施例26
[0178]
将根据本发明的含有颗粒和添加剂的脱敏凝胶在环境条件(20℃~23℃)下在适合产品的ldpe管中储存长达18个月,在此期间评估产品性能,诸如含水量、稠度(consistency)和颗粒的外观。储存后凝胶中颗粒的外观参见图18。发现,被评估的产品性能得以保持,并得出脱敏凝胶的产品稳定性至少为18个月的结论。
[0179]
实施例27
[0180]
将根据本发明的含有颗粒和添加剂的脱敏凝胶在加速条件(40℃,》90%rh)下在适合产品的ldpe管中储存长达12个月,之后评估产品性能,诸如含水量、稠度和颗粒的外观。储存后的颗粒外观参见图19。发现,管重和凝胶的含水量由于相对高湿度的储存条件而有所增加,但是颗粒的外观和凝胶的稠度得以基本保持。对储存条件采用保守加速因子3,得到脱敏凝胶的暂定保质期(tentative shelf life)为36个月。
[0181]
实施例28
[0182]
为了证实根据本发明制造的含有颗粒和甘油的组合物,甚至在含有过量游离水(通常会促进acp结晶)的组合物中的稳定性,将根据本发明的含有40重量%球状且中空的钙镁磷酸盐颗粒、55重量%甘油和5重量%游离水的组合物与水混合以形成含有5重量%~50重量%过量游离水的混合物。将这些混合物在环境条件(20℃~23℃)下储存长达20周,然后通过sem和xrd分析颗粒,以记录外观和结晶度的任何显著变化,参见图20和图21中的结果。结果证实了,在研究期间(20周),颗粒在含有5重量%~10重量%过量水的混合物中保持球状和非晶态。在含有30重量%和50重量%过量游离水的混合物中,储存20周后,颗粒外观有轻微变化,但大多数颗粒仍保持其特征球状。在储存8周后,首先注意到50重量%过量游离水样品的结晶度增加。
[0183]
实施例29
[0184]
将根据本发明的含有16重量%过氧化脲和7.5重量%球状且中空的钙镁磷酸盐颗粒的原型美白凝胶施用于牙釉质样本,每天6小时,持续3天,间隔期间储存在37℃的人工唾液中。在来自相同牙齿的牙釉质样本上平行评估含有16重量%过氧化脲但没有颗粒的对照美白凝胶。
[0185]
用不同凝胶处理后的色度评估证实了美白效果相似,表明根据本发明的颗粒对美白过程没有不利影响。基于双尾配对t检验(显著性水平为0.05),处理前后牙釉质样本的维氏硬度评估(300gf,10s)证实了,用含有颗粒的美白凝胶处理的样本,硬度显著增加,而用对照凝胶处理的样本,硬度变化不显著,参见表3。对于用含有颗粒的美白凝胶处理的样本,观察到的硬度增加表明颗粒诱导了表面牙釉质的矿化,从而强化了牙齿。
[0186]
表3.用含有或不含本发明颗粒的凝胶进行三天美白处理之前和之后的牙釉质硬度评估结果。*显著性差异
[0187]
牙釉质样本处理处理前的维氏硬度(
±
sd)处理后的维氏硬度(
±
sd)p值1a颗粒凝胶313.5
±
11.6357.5
±
21.9《0.01*1b对照凝胶318.2
±
9.1334.9
±
17.50.192a颗粒凝胶294.3
±
10.4343.6
±
22.20.02*2b对照凝胶294.8
±
17.0296.6
±
12.30.732c无298.3
±
23.6298.2
±
8.50.99
[0188]
实施例30
[0189]
根据本发明的非晶态钙磷酸盐颗粒通过镁取代而稳定,但是在环境条件下随着时间的推移仍然会结晶。形成根据本发明的具有颗粒和成膏化合物的组合物,部分是为了实现颗粒的长期稳定性。
[0190]
将根据本发明的颗粒以干细粉的形式在环境条件下于密闭容器中储存11个月,以评估稳定性。发现,一些颗粒保持球状,但显示出降解和结晶的迹象。其他颗粒已经完全转化。xrd评估表明结晶度增加,参见图22。
[0191]
与含有甘油的组合物(实施例24和25)中的颗粒稳定性相比,粉末颗粒的降解/结晶度是显著的。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。