1.本发明属于检测分析技术领域,具体涉及将铁-黑色素作为过氧化物模拟酶应用在总抗氧化能力检测中。
背景技术:
2.辣根过氧化物酶(hrp)与同类过氧化物酶相比具有明显的优势,由于其灵敏度高、分析速度快、背景干扰小,已被广泛应用于生物传感器中用于检测h2o2、葡萄糖、乙酰胆碱和抗坏血酸。然而,在检测过程中,暴露的hrp活性中心容易受到温度、ph值、h2o2和反应副产物吸附的影响,给检测结果带来很大的不确定性。虽然目前已经开发了许多固定化策略来保护酶的活性和增加其稳定性,但由于固定化过程中酶负荷相对较低,酶的活性损失严重,导致材料的催化效果不足。
3.受天然酶的启发,人们开发了许多具有类似过氧化物酶催化活性的纳米材料作为模拟酶来构建新型生物传感器。然而,以往基于纳米材料的模拟酶大多存在成本高或制备工艺复杂的问题。例如,中国专利申请cn113617395a中公开了一种用于食品抗氧化活性检测的纳米酶及其制备方法,将六氰基铁酸钾和柠檬酸溶解于水中,然后依次加入四氯金酸钠(iii)和硫酸铜,反应得到金掺杂的纳米酶au@cu-hcf。该纳米酶既能用于检测氢原子转移类抗氧化物质,又能用于检测单电子转移类抗氧化物质。然而贵金属基纳米酶虽然具有较高的过氧化物酶活性,但其高昂的价格和稀缺性限制了其广泛应用。
4.因此,模拟酶的安全性和合成方法的简单性还需要进一步提高;迫切需要开发出具有活性高、制备方法简单、成本低和稳定性好的人工过氧化物酶模拟酶,以规避天然酶的缺点。
技术实现要素:
5.为了解决上述问题,本发明中使用铁-黑色素作为过氧化物模拟酶催化过氧化氢氧化显色底物,并利用抗氧化剂能将氧化后的显色底物还原的作用机理,来实现对总抗氧化能力的快速检测。
6.为了实现上述目的,本发明中将铁-黑色素作为过氧化物模拟酶用于检测总抗氧化能力的方法包括以下步骤:
7.s1、向醋酸钠-醋酸缓冲液中加入双氧水、显色底物、铁-黑色素,搅拌均匀得混合液a,所述混合液a中过氧化氢的浓度为1.0mmol/l,显色底物的浓度为1.0mmol/l,0<铁-黑色素的浓度≤50μg/ml;
8.s2、取n份所述混合液a,分别加入不同浓度的抗氧化剂水溶液混合均匀,静置孵育,得到n份抗氧化剂浓度各不相同的待测液b;所述待测液b中抗氧化剂的浓度为0~0.3mmol/l,将抗氧化剂浓度为0的所述待测液b作为对照组;
9.s3、测定步骤s2中n份所述待测液b在350~800nm范围内的紫外-可见吸收光谱,将对照组和其他所述待测液b在652nm处的吸光度值依次记录为y0、y1、y2……yn-1
;分别计算
y1、y2……yn-1
与y0的差值,对吸光度差值和抗氧化剂浓度进行数据分析,建立抗氧化剂浓度x与吸光度差值y之间的模型关系,得到检测抗氧化剂的标准曲线为y=0.00189x 0.03456;
10.s4、按照步骤s1和s2中的方法配制抗氧化剂浓度未知的样品溶液,测定所述样品溶液在652nm处的吸光度值,将得到的吸光度值与对照组的吸光度值y0的差值代入到步骤s3的标准曲线中,计算出抗氧化剂的浓度。
11.本发明中铁-黑色素在醋酸盐缓冲液提供的酸性条件下发挥类过氧化物酶活性作用,催化过氧化氢分解产生
·
oh氧化显色底物,再使用不同浓度的抗氧化剂将被氧化的显色底物还原并测定被还原后体系在652nm处的吸光度值,以未加入抗氧化剂的被氧化显色底物溶液作为对照组并测定其吸光度值,计算所述被还原后体系的吸光度值与所述对照组的吸光度值的差值,并分析所述差值与抗氧化剂浓度之间的关系,建立二者的线性方程得到检测抗氧化剂浓度的标准曲线。按照步骤s1的方法配制好被氧化的显色底物溶液,按照步骤s2的方法将浓度在检测范围内的待测样品加入到被氧化的显色底物溶液中,测定混合体系在652nm处的吸光度值,再计算该吸光度值与上述对照组吸光度值的差值,将差值代入到标准曲线中,即可计算出待测样品中抗氧化剂的浓度。在以抗坏血酸为主要抗氧化剂成分的待测样品中,检测出抗坏血酸的浓度,以抗坏血酸的抗氧化能力等效样品的总抗氧化能力,即可得出待测样品的总抗氧化能力。本发明中检测总抗氧化能力的方法适用于检测药品、保健品、食品、化妆品等各种以抗坏血酸为主要抗氧化剂成分的待测样品的总抗氧化能力。
12.优选的,所述醋酸钠-醋酸缓冲液的ph=2~6。
13.进一步优选的,所述醋酸钠-醋酸缓冲液的ph=2~5。
14.再进一步优选的,所述醋酸钠-醋酸缓冲液的ph=2~4。
15.更进一步优选的,所述醋酸钠-醋酸缓冲液的ph=3。
16.优选的,步骤s2中配制所述待测液b的温度为35~70℃。
17.进一步优选的,步骤s2中配制所述待测液b的温度为40~65℃。
18.更进一步优选的,步骤s2中配制所述待测液b的温度为50℃。
19.优选的,步骤s2中静置孵育的时间为5~25min。
20.进一步优选的,步骤s2中静置孵育的时间为15~25min。
21.优选的,所述显色底物为3,3',5,5'-四甲基联苯胺。
22.优选的,所述抗氧化剂为抗坏血酸。
23.优选的,所述铁-黑色素的制备方法包括如下步骤:
24.p1、将墨鱼汁加入到去离子水中,搅拌至墨鱼汁悬浮均匀,得到的混悬液用去离子水洗涤离心5~7次,冷冻干燥,得到黑色素纳米颗粒;
25.p2、将所述黑色素纳米颗粒重悬于去离子水中,加入含fe
3
的水溶液得到混合液c,用ph调节剂调节所述混合液c的ph至3,搅拌反应6h;所述混合液c中黑色素纳米颗粒的浓度为12.5mg/ml;所述混合液c中fe
3
的浓度为9.6mmol/ml;
26.p3、对步骤p2中反应结束后得到的聚集体溶液用去离子水进行离心清洗5~7次,得到铁-黑色素溶液,冷冻干燥,得到铁-黑色素粉末。
27.进一步优选的,步骤p1中所述混悬液中墨鱼汁的浓度为0.25g/ml。
28.进一步优选的,步骤p1中每次离心的速度为10000r/min,每次离心的时间为
10min。
29.进一步优选的,步骤p2中所述含fe
3
的水溶液为fecl3水溶液。
30.进一步优选的,步骤p2中的ph调节剂为氢氧化钠水溶液。
31.更进一步优选的,所述氢氧化钠水溶液的浓度为0.1mol/l。
32.进一步优选的,步骤p3中每次离心的速度为10000r/min,每次离心的时间为5min。
33.进一步优选的,步骤p1和步骤p3中冷冻干燥的条件为-60℃下干燥12h。
34.与现有技术相比,本发明的有益效果是:
35.(1)本发明中铁-黑色素作为过氧化物模拟酶使用时,在浓度仅为10μg/ml时,酶动力学米氏常数km为0.367,最大反应速率vmax可达10.1
×
10-8
m/s,其催化活性远大于天然辣根过氧化物酶的催化活性;并且本发明中的铁-黑色素过氧化物模拟酶的稳定性和可重复利用性非常优异,重复使用5次后,酶活性下降不超过10%;在实验室条件下(温度为20~30℃,湿度为45%~80%)储存20天,酶活性下降不超过10%。
36.(2)本发明中铁-黑色素过氧化物模拟酶检测以抗坏血酸为主要抗氧化剂成分的样品的总抗氧化能力时,最低检测限为12.61μmol/l,检测范围是5~250μmol/l。
37.(3)本发明中提供的铁-黑色素过氧化物模拟酶的合成方法简单,操作简便,合成时间快,原料来源广泛,成本低廉。
附图说明
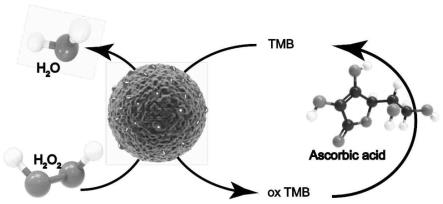
38.图1为本发明中检测总抗氧化能力的原理示意图;
39.图2为本发明制备的铁-黑色素的透射电镜图;
40.图3为不同温度下铁-黑色素过氧化物模拟酶活性的测定结果图;
41.图4为不同ph值下铁-黑色素过氧化物模拟酶活性的测定结果图;;
42.图5为不同浓度的铁-黑色素过氧化物模拟酶随反应时间变化的活性的测定结果图;
43.图6为不同tmb浓度下铁-黑色素过氧化物模拟酶的米氏动力学常数拟合曲线图;
44.图7为不同tmb浓度下铁-黑色素过氧化物模拟酶的反应速度图;
45.图8为不同过氧化氢浓度下铁-黑色素过氧化物模拟酶的米氏动力学常数拟合曲线图;
46.图9为不同过氧化氢浓度下铁-黑色素过氧化物模拟酶的反应速度图;
47.图10为铁-黑色素过氧化物模拟酶稳定性测定结果图;
48.图11为铁-黑色素过氧化物模拟酶可重复利用性测定结果图;
49.图12为总抗氧化能力检测的标准曲线图;
50.图13为采用本发明的方法检测两种维生素c片总抗氧化能力的结果与说明书含量对比图;
51.图14为采用本发明的方法检测三种饮料、橙子和柠檬的总抗氧化能力的检测结果图。
具体实施方式
52.以下结合实施例对本发明技术方案进行清楚、完整的描述,显然,所描述的实施例
仅仅是本发明的一部分实施例,而不是全部的实施例。基于本发明的实施例,本领域普通技术人员在没有做出创造性劳动的前提下所得到的所有其它实施例,都属于本发明所保护的范围。本领域技术人员依据以下实施方式所作的任何等效变换或替代,均属于本发明的保护范围之内。
53.实施例
54.1、制备铁-黑色素过氧化物模拟酶
55.本实施例中制备铁-黑色素的方法包括以下步骤:
56.p1、将25g墨鱼汁加入到100ml去离子水中,搅拌至墨鱼汁混悬均匀,得到的混悬液用去离子水在10000r/min的离心速度下清洗10min,重复清洗5~7次,然后在-60℃下冷冻干燥12h,得到干燥的黑色素纳米颗粒;
57.p2、将0.5g步骤p1中得到的黑色素纳米颗粒悬浮于35ml水中,再缓慢加入5ml0.077mol/l的fecl3水溶液,搅拌均匀,加入0.1mol/l的naoh溶液调节ph至3,磁力搅拌反应6h,得到含有fe
3
修饰的黑色素纳米颗粒聚集体溶液;
58.p3、将步骤p2中的聚集体溶液用去离子水在10000r/min的离心速度下清洗5min,重复清洗5~7次,得到具有类过氧化物酶活性的铁-黑色素溶液,在-60℃下冷冻干燥12h得到铁-黑色素(fe-nmps)过氧化物模拟酶粉末。
59.图2为步骤p3得到的铁-黑色素溶液的透射电镜图,从图2中可以看出,制备出的铁-黑色素的形状为球形,粒径为100nm。
60.2、铁-黑色素(fe-nmps)过氧化物模拟酶性能测定
61.(1)温度对铁-黑色素过氧化物模拟酶活性的影响
62.向430μl醋酸钠-醋酸缓冲液(ph=3)中加入20μl 0.25mg/ml的铁-黑色素溶液、25μl 20mmol/l的tmb溶液和25μl 20mmol/l的双氧水,得到的混合溶液中铁-黑色素的浓度为10μg/ml;共配制6份相同的溶液。将6份相同的溶液分别置于20℃、30℃、40℃、50℃、60℃和70℃下反应15分钟,从第15分钟开始用酶标仪测定每分钟每孔反应体系在652nm处的吸光度值,测定结果如图3所示。从图3中可知,在温度低于50℃时,铁-黑色素的催化活性随着温度升高而升高,在50℃时的活性达到最强,之后随着温度升高,铁-黑色素的催化活性逐渐下降;但是在70℃时其催化活性仍然有50%。
63.(2)ph值对铁-黑色素过氧化物模拟酶活性的影响
64.依次取ph值为2、3、4、5、6、7、8、9的醋酸钠-醋酸缓冲液各430μl,分别向每份缓冲液中加入20μl 0.25mg/ml的铁-黑色素溶液、25μl 20mmol/l的tmb溶液和25μl 20mmol/l的双氧水,得到的混合溶液中铁-黑色素的浓度为10μg/ml。将8份溶液静置孵育15min,从第15min开始用酶标仪测定每分钟每孔反应体系在652nm处的吸光度值,测定结果如图4所示。从图4中可以看出,在ph=2~9的范围内,铁-黑色素作为过氧化物模拟酶都具有活性;在ph=2~3的范围内,随着ph值升高模拟酶的活性逐渐增强;在ph=3~9的范围内,随着ph值升高模拟酶的活性逐渐降低;在ph=3~6的范围内活性下降较快,在ph=6~9的范围内活性下降较慢;当反应体系的ph=3时,铁-黑色素的催化活性最强。
65.(3)铁-黑色素浓度和反应时间对铁-黑色素过氧化物模拟酶活性的影响
66.取6份每份体积为170μl的醋酸钠-醋酸缓冲液(ph=3),向每份缓冲液中加入10μl浓度为20mmol/l的tmb溶液和10μl浓度为20mmol/l的双氧水,再分别加入10μl浓度各不相
同的铁-黑色素溶液,使铁-黑色素的终浓度依次为0、10μg/ml、20μg/ml、30μg/ml、40μg/ml、50μg/ml;其中,不加铁-黑色素的缓冲液体系作为空白对照;在25min内使用酶标仪测定每分钟每孔中反应体系在652nm处的吸光度,测定结果如图5所示。从图5中可以看出,无论缓冲液体系中铁-黑色素的浓度为多少,其催化活性都是随着反应时间延长而增强;在相同的反应时间内,铁-黑色素过氧化物模拟酶的活性随着其在缓冲液体系中浓度的增加而增强。
67.(4)铁-黑色素对显色底物的亲和力评价
68.向10份醋酸钠-醋酸缓冲液(ph=3)中分别加入10μl 0.2mg/ml的铁-黑色素溶液,再加入体积各不相同的浓度为20mmol/l的tmb溶液和10μl浓度为20mmol/l的双氧水,用醋酸钠-醋酸缓冲液(ph=3)定容至200μl,使10份缓冲液体系中的tmb终浓度依次为0.1mmol/l、0.5mmol/l、1mmol/l、1.5mmol/l、2mmol/l、2.5mmol/l、3mmol/l、3.5mmol/l、4mmol/l、4.5mmol/l;每隔7.5s测定每孔中反应体系在652nm处的吸光度;测定结果如图6和图7所示。图6为不同tmb浓度下,铁-黑色素的米氏动力学常数拟合曲线图,图7为不同tmb浓度下,铁-黑色素的反应速度图,从图6和图7中可以计算出,fe-nmps对tmb的米氏常数(km)和最大反应速度(vmax)分别为0.367mmol/l和10.1
×
10-8
mol/(l
·
s)。而天然辣根过氧化物酶(hrp)对tmb的米氏常数为0.434mmol/l,最大反应速度为10
×
10-8
mol/(l
·
s);fe-nmps在最大反应速度与hrp持平的情况下,却具有更小的km,说明与hrp相比fe-nmps对tmb具有更好的亲和力。
69.(5)铁-黑色素对过氧化氢的亲和力评价
70.向11份醋酸钠-醋酸缓冲液(ph=3)中分别加入10μl 0.2mg/ml的铁-黑色素溶液,再加入体积各不相同的浓度为20mmol/l的双氧水和10μl浓度为20mmol/l的tmb溶液,用醋酸钠-醋酸缓冲液(ph=3)定容至200μl,使11份缓冲液体系中过氧化氢的终浓度依次为0.1mmol/l、0.2mmol/l、0.4mmol/l、0.6mmol/l、0.8mmol/l、1.0mmol/l、1.2mmol/l、1.4mmol/l、1.6mmol/l、1.8mmol/l、2.0mmol/l;每隔7.5s测定每孔中反应体系在652nm处的吸光度;测定结果如图8和图9所示。图8为不同过氧化氢浓度下,铁-黑色素的米氏动力学常数拟合曲线图,图9为不同过氧化氢浓度下,铁-黑色素的反应速度图,从图9可以计算出,fe-nmps对过氧化氢的最大反应速为12
×
10-8
mol/(l
·
s),而hrp对h2o2的最大反应速度为8.71
×
10-8
mol/(l
·
s),可见fe-nmps作为过氧化物模拟酶比hrp具有更快的反应速度,说明fe-nmps与hrp相比具有更优异的过氧化物酶活性。
71.(6)铁-黑色素过氧化物模拟酶稳定性测定
72.向醋酸钠-醋酸缓冲液(ph=3)中加入10μl 0.2mg/ml的铁-黑色素溶液、10μl20mmol/l的tmb溶液和10μl 20mmol/l的双氧水,用醋酸钠-醋酸缓冲液(ph=3)定容至200μl,搅拌15min使缓冲液体系混合均匀,测定缓冲液体系在652nm处的吸光度。测定结束后,将缓冲体系置于实验环境(温度为20~30℃,湿度为45%~80%)下储存,每隔5天测定缓冲体系在652nm处的吸光度值,测定结果如图10所示。从图10中可以看出,缓冲液体系在不严格控制储存环境直接置于实验室中的情况下,在20天内,铁-黑色素过氧化物模拟酶的活性虽然在逐渐下降,但是下降幅度并不大,在第20天时仍然有90%的反应活性,说明本发明制备的铁-黑色素过氧化物模拟酶在一般的实验条件下具有优异的稳定性。
73.(7)铁-黑色素过氧化物模拟酶可重复利用性测定
74.向醋酸钠-醋酸缓冲液(ph=3)中加入10μl 0.2mg/ml的铁-黑色素溶液、10μ
l20mmol/l的tmb溶液和10μl 20mmol/l的双氧水,用醋酸钠-醋酸缓冲液(ph=3)定容至200μl,搅拌15min使缓冲液体系混合均匀,测定缓冲液体系在652nm处的吸光度。测定结束后,将缓冲液体系在10000r/min速度下离心5min,回收铁-黑色素,用去离子水清洗,再将得到的铁-黑色素按照前述方法重复使用并测定缓冲液体系在652nm处的吸光度值;一共循环使用5次;测定结果如图11所示。从图11中可以看出,本发明中制备的铁-黑色素在循环使用时催化活性下降幅度很小,在循环使用5次后,活性仍然有90%以上,说明本发明制备的铁-黑色素过氧化物模拟酶在一般的实验条件下具有良好的可重复利用性。
75.3、总抗氧化能力检测
76.如图1所示,本发明中铁-黑色素能催化过氧化氢氧化显色底物tmb,被氧化后的显色底物能被抗坏血酸还原成tmb,利用该原理可以测定样品的总抗氧化能力,本发明中测定样品的总抗氧化能力的方法包括如下步骤:
77.s1、向醋酸钠-醋酸缓冲液(ph=3)中加入10μl浓度为20mmol/l的tmb溶液、10μl浓度为20mmol/l的双氧水、10μl 0.2mg/ml的铁-黑色素溶液,搅拌均匀;
78.s2、将步骤s1中的缓冲液体系配制22份,每份中分别加入抗坏血酸溶液,用醋酸钠-醋酸缓冲液(ph=3)定容至200μl,使得最终的缓冲液体系中抗坏血酸的浓度依次为0、1mmol/l、2mmol/l、3mmol/l、4mmol/l、5mmol/l、10mmol/l、15mmol/l、20mmol/l、25mmol/l、30mmol/l、35mmol/l、40mmol/l、50mmol/l、60mmol/l、70mmol/l、80mmol/l、90mmol/l、100mmol/l、150mmol/l、200mmol/l、250mmol/l,其中不加抗坏血酸的缓冲液体系作为对照组;
79.s3、将步骤s2中22份缓冲液体系均在37℃孵育15min,测定在350~800nm范围内的紫外-可见吸收光谱,将吸光度值依次记录为y0、y1、y2……y21
;分别计算y1、y2……y21
与y0的差值,对吸光度差值和抗氧化剂浓度进行数据分析,建立抗坏血酸浓度x与吸光度差值y之间的模型关系,如图12所示,得到检测抗氧化剂的标准曲线为y=0.00189x 0.03456(r2=0.991);从图12中可以计算出,铁-黑色素作为过氧化物模拟酶用于检测抗坏血酸时的最低检测限为12.61μmol/l,检测范围为5μmol/l~250μmol/l;
80.s4、选取东北制药集团生产的维生素c片、康恩贝生产的维生素c片、超市购买的三种含维生素c的饮料、超市购买的橙子和柠檬,分别配制成浓度在步骤s3中检测范围内的样品溶液,按照步骤s1~s3的方法测定每份样品溶液在652nm处的吸光度值,将样品溶液的吸光度值与对照组吸光度的差值代入到步骤s3的标准曲线中,计算出样品溶液中抗坏血酸的浓度,结果如图13和图14所示;所有样品溶液的总抗氧化能力(tac)被转换成抗坏血酸(aa)的毫摩尔当量,样品中的tac含量以aa/l为单位表示。图13为两种维生素c片使用本发明的方法检测的结果与说明书含量对比图,从图中可以看出,按照本发明的方法测定的结果与说明书标示的含量相差很小,说明本发明中测定总抗氧化能力的方法准确有效。图14为三种饮料、橙子和柠檬的总抗氧化能力检测结果,三种饮料的检测结果与饮料瓶标签上的结果基本一致,橙汁饮料中的tac高于橙子,可能是由于饮料生产过程中添加了一些抗氧化剂;柠檬的tac比橙子的高,说明柠檬中抗坏血酸的含量比橙子中高。
81.以上所述仅为本发明的优选实施例而已,并不用于限制本发明的保护范围。对于任何熟悉本领域的技术人员来说,本发明可以有各种更改和变化。任何依据本发明申请保护范围及说明书内容所作的简单的等效变化和修饰,均应包含在本发明的保护范围之内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。