1.本发明涉及用于提高干细胞存活率的包含免疫抑制剂在内的组合物,以及使用所述组合物提高干细胞的治疗效果的方法。
背景技术:
2.干细胞是指具有分化成两种或更多种细胞的能力同时具有自我复制能力的细胞。此类干细胞可根据其分化能力分为全能干细胞、多能干细胞和专能干细胞,并且专能干细胞是指能够分化成对含有这些细胞的组织或器官具有特异性的细胞的干细胞。
3.间充质干细胞(msc)是存在于软骨、骨组织、脂肪组织、骨髓基质(基质)等中的干细胞,已知所述间充质干细胞(msc)能够通过将各种蛋白质分泌到外部(旁分泌效应)来改善微环境,并且所述间充质干细胞(msc)被认为是参与组织再生、治疗和免疫应答以及多潜能性的细胞,因此,利用这些特性从脐带血、骨髓等中分离和培养间充质干细胞,开发多种疾病的治疗剂的努力一直在稳步推进。
4.特别地,已经积极地进行了间充质干细胞几乎没有免疫排斥反应(与其它干细胞不同)的研究,但最近已经公布了对间充质干细胞的免疫原性的研究,因此需要能够改善治疗效果的方法,所述方法能够降低间充质干细胞的免疫应答并提高间充质干细胞的存活率。
5.尽管已经尝试了研究以显示组合使用间充质干细胞和免疫抑制剂的免疫抑制作用(transplant immunology 37(2016)1-9),但对于用于提高干细胞存活率的包含免疫抑制剂在内的组合物的研究并不充分。
6.公开内容
7.技术问题
8.由于对用于提高能够降低干细胞的免疫应答的治疗效果和干细胞存活率的方法的深入研究,本技术的发明人通过发现当用他克莫司或地塞米松(其在相关领域中被称为免疫抑制剂)处理干细胞时,干细胞的存活率提高,证实了干细胞的治疗效果显著改善,从而完成本发明。
9.因此,本发明的一个目的是提供用于提高干细胞存活率的包含免疫抑制剂在内的组合物。
10.此外,本发明的另一个目的是提供干细胞治疗佐剂,其包括用于提高干细胞存活率的组合物。
11.另外,本发明的另一个目的是提供用于提高干细胞的存活率和降低干细胞的免疫应答的方法,所述方法包括将免疫抑制剂施用至除人以外的哺乳动物。
12.然而,本发明要实现的技术问题不限于上述问题,并且本领域技术人员可以从以下描述中清楚地理解未提及的其他问题。
13.技术方案
14.为了实现本发明的上述目的,本发明提供了用于提高干细胞存活率的包含免疫抑制剂在内的组合物。
15.作为本发明的示例性实施方案,免疫抑制剂可以是他克莫司或地塞米松。
16.作为本发明的另一个示例性实施方案,他克莫司可以以1至10mg/kg的浓度腹腔内施用。
17.作为本发明的另一个示例性实施方案,地塞米松可以以0.5至3mg/kg的浓度口服施用。
18.作为本发明的另一个示例性实施方案,所述组合物可以降低由干细胞引起的免疫应答。
19.作为本发明的另一个示例性实施方案,所述干细胞可以是胚胎干细胞或成体干细胞。
20.作为本发明的另一个示例性实施方案,成体干细胞可以是间充质干细胞,其来源于选自以下的一种或多种组织:脐带、脐带血、骨髓、脂肪、肌肉、神经、皮肤、羊膜和胎盘。
21.此外,本发明提供了干细胞治疗佐剂,其包括用于提高干细胞存活率的组合物。
22.另外,本发明提供了用于提高干细胞的存活率和降低干细胞的免疫应答的方法,所述方法包括将免疫抑制剂施用至除人以外的哺乳动物。
23.作为本发明的示例性实施方案,所述免疫抑制剂可以是他克莫司或地塞米松。
24.作为本发明的另一个示例性实施方案,他克莫司可以以1至10mg/kg的浓度腹腔内施用。
25.作为本发明的另一个示例性实施方案,地塞米松可以以0.5至3mg/kg的浓度口服施用。
26.作为本发明的另一个示例性实施方案,可以经口服、腹腔内、静脉内、肌内或皮下施用所述免疫抑制剂。
27.此外,本发明提供了所述组合物用于提高干细胞存活率的用途。
28.有益效果
29.本技术的发明人证实了在施用人间充质干细胞(hmsc)的小鼠中发生免疫应答,并且通过实验证实了通过用免疫抑制剂处理小鼠,干细胞的治疗效果显著改善,如免疫应答的降低和干细胞存活率的提高。
30.因此,根据本发明,可以使用包括免疫抑制剂在内的组合物显著提高干细胞的存活率,并且可以在上述提高的基础上改善干细胞的治疗效果。所述组合物可以克服由施用异种细胞引起的免疫应答,从而准确地验证细胞的稳定性和功效,因此将能够用作使干细胞的治疗效果最大化的间充质干细胞治疗剂。
附图说明
31.图1说明了通过免疫组织化学染色(ihc)证实当将hmsc施用至正常小鼠脑实质时发生免疫细胞浸润的结果。
32.图2a说明了通过苏木精&伊红(h&e)组织染色证实了将小鼠msc和hmsc施用至正常小鼠脑实质的免疫应答的结果。
33.图2b说明了通过免疫组织化学染色证实了将小鼠msc和hmsc施用至正常小鼠脑实
质的免疫应答的结果。
34.图3说明了施用与hmsc移植组合使用的免疫抑制剂的实验条件。
35.图4a说明了通过免疫组织化学染色(ihc)证实了cd45白细胞表达差异的结果。
36.图4b说明了通过免疫组织化学染色(ihc)证实了占白细胞的大部分的嗜中性粒细胞表达差异的结果。
37.图5a说明了通过免疫组织化学染色(ihc)证实了iba-1小胶质细胞表达差异的结果。
38.图5b说明了通过免疫组织化学染色(ihc)证实了cd68巨噬细胞表达差异的结果。
39.图6通过免疫组织化学染色(ihc)证实了由于施用免疫抑制剂而导致的t细胞分布的变化,并且说明了证实了cd4和cd8αt细胞表达差异的结果。
40.图7说明了通过qpcr证实了通过免疫抑制剂的施用提高hmsc存活率的结果。
41.图8a说明了通过免疫组织化学染色(ihc)证实了当将hmsc施用至免疫缺陷裸鼠时cd45白细胞表达差异的结果。
42.图8b说明了通过免疫组织化学染色(ihc)证实了当将hmsc施用至免疫缺陷裸鼠时占白细胞的大部分的嗜中性粒细胞表达差异的结果。
43.图9a说明了通过免疫组织化学染色(ihc)证实了当将hmsc施用至免疫缺陷裸鼠时iba-1小胶质细胞表达差异的结果。
44.图9b说明了通过免疫组织化学染色(ihc)证实了当将hmsc施用至免疫缺陷裸鼠时cd68巨噬细胞表达差异的结果。
45.图10通过免疫组织化学染色(ihc)证实了当将hmsc施用至免疫缺陷裸鼠时t细胞分布的变化,并且说明了证实cd4和cd8αt细胞表达差异的结果。
46.图11说明了通过qpcr证实了当将hmsc施用至免疫缺陷裸鼠时提高hmsc存活率的结果。
47.发明模式
48.本技术的发明人证实了在施用人间充质干细胞(hmsc)的小鼠中发生免疫应答,并且通过实验证实了通过用免疫抑制剂处理小鼠,干细胞的治疗效果显著改善,如免疫应答的降低和干细胞存活率的提高,从而基于此完成本发明。
49.因此,本发明提供了用于提高干细胞存活率的包含免疫抑制剂在内的组合物。
50.如本文所用,术语“免疫抑制剂”是降低或抑制体内免疫系统活性的药物,并且统称为甾体药剂、细胞增殖抑制剂、抗体制剂、基于亲免素的药物、麦考酚酯、肿瘤坏死因子(tnf-α)抑制剂等。
51.在本发明中,免疫抑制剂的类型不受限制,具体地,钙调磷酸酶抑制剂或甾体免疫抑制剂是优选的,更具体地,他克莫司或地塞米松是更优选的。
52.在本发明中,他克莫司的剂量不受限制,但优选包括以1至10mg/kg的浓度腹腔内施用,并且更优选可以包括以3mg/kg的浓度腹腔内施用。
53.在本发明中,地塞米松的剂量不受限制,但优选包括以0.5至3mg/kg的浓度口服施用,并且更优选可以包括以1mg/kg的浓度口服施用。
54.在本发明中,用于提高干细胞存活率的组合物的特征在于降低由干细胞引起的免疫应答。
55.本技术的发明人通过具体的示例性实施方案证实了根据免疫抑制剂治疗降低干细胞的免疫应答和提高干细胞存活率的效果。
56.在本发明的示例性实施方案中,由于将干细胞和免疫抑制剂施用至正常小鼠,然后进行心脏灌注以提取脑并通过免疫组织化学染色分析脑,证实了与单独的干细胞施用组相比,施用免疫抑制剂的组中免疫应答降低,并且证实了在施用免疫抑制剂的组中。与单独施用hmsc的组相比,cd45免疫细胞的浸润减少(参见实施例3)。
57.在本发明的另一个示例性实施方案中,由于将干细胞和免疫抑制剂施用至正常小鼠,然后通过qpcr分析收获的脑,证实了在施用免疫抑制剂的组中,与单独的干细胞施用组相比,高度表现出干细胞的保留率(参见实施例4)。
58.以上结果显示通过施用免疫抑制剂,可以降低人间充质干细胞的有效免疫应答,并提高人间充质干细胞的存活率。
59.如本文所用,“干细胞”是指具有分化成两种或更多种不同细胞的能力同时具有自我复制能力的细胞。本发明的干细胞可以是自体或同种异体来源的干细胞,并且可以来源于任何类型的动物,包括人和非人哺乳动物,并且不限于来源于成体和来源于胚胎的那些。
60.在本发明中,干细胞可以是胚胎干细胞、诱导的多能干细胞(ipsc)或成体干细胞,并且可以优选是胚胎干细胞或成体干细胞,但不限于此。
61.在本发明中,间充质干细胞可以是来源于脐带、脐带血、骨髓、脂肪、肌肉、神经、皮肤、羊膜、胎盘等的间充质干细胞,但不限于此。
62.此外,本发明提供了干细胞治疗佐剂,其包括用于提高干细胞存活率的组合物。
63.如本文所用,“干细胞治疗佐剂”是指能够用作佐剂以提高本领域中通常使用的干细胞治疗剂的效果的制剂,并且通过使用根据本发明的佐剂,可以通过促进免疫应答的降低和干细胞存活率的提高来改善治疗剂的效果。
64.另外,本发明提供了用于提高干细胞的存活率和降低干细胞的免疫应答的方法,所述方法包括将免疫抑制剂施用至除人以外的哺乳动物。
65.在将免疫抑制剂施用至除人以外的哺乳动物时,免疫抑制剂可以经由任何一般途径施用,只要免疫抑制剂可以到达靶组织,免疫抑制剂可以经口服、腹腔内、静脉内、肌内和皮下施用,但途径不限于此。
66.此外,本发明提供了包含免疫抑制剂的组合物用于提高干细胞存活率的用途。
67.在下文中,将提出用于帮助理解本发明的优选实施例。然而,提供以下实施例仅是为了更容易地理解本发明,并且本发明的内容不受以下实施例的限制。
实施例
68.实施例1:在将异种hmsc施用至小鼠脑实质后免疫应答的证实
69.在将细胞培养基(mem)或hmsc施用至正常小鼠脑实质后,一周后处死小鼠。施用mem而不是细胞以指定对照,并将提取的小鼠脑固定在多聚甲醛(pfa)中,然后切片并进行组织学染色。
70.结果,如图1所示,证实了在mem施用组中发现了大部分非特异性染色,并且几乎没有发现白细胞(cd45抗体)免疫细胞的浸润,但在hmsc施用组中,免疫细胞的浸润在施用部位非常高(通过免疫组织化学染色(ihc))。虽然用线粒体标志物发现在hmsc施用部位处移
植的hmsc,但证实了移植的hmsc的数量明显少于免疫细胞的数量。
71.实施例2:在将同源的小鼠msc施用至小鼠脑实质后异种免疫应答的证实
72.为了证实免疫应答是否仅在将人来源的(即异种的)细胞施用至小鼠时显著发生,以与实施例1相同的方式将同源小鼠(c57bl/6)的干细胞施用至其它c57bl/6小鼠并证实。
73.结果,如图2a所示,通过苏木精&伊红(h&e)组织染色证实了在施用小鼠msc的组中,干细胞以msc特异性成纤维细胞的形式成功地移植,并且如图2b所示,由于在小鼠msc施用部位和hmsc施用部位进行组织学染色,证实了在施用小鼠msc的部位处发现非特异性染色,并且在施用hmsc的部位处表达cd45的免疫细胞的密度增加。
74.基于这些结果,证实了当施用异种msc而不是同源msc时,免疫应答增加,并且msc显示出免疫原性而不是免疫逃避。
75.实施例3:通过免疫抑制剂的组合施用降低间充质干细胞免疫应答的证实
76.通过将正常小鼠(c57b/l6)分成总共5组进行实验:单独的mem施用组、单独的hmsc施用组、地塞米松施用组、他克莫司施用组以及地塞米松和他克莫司组合施用组。如图3所示,将总共2
×
105个hmsc悬浮在5μl mem培养基中,并将所得溶液以1μl/min的施用速率以坐标a/p-0.5mm,m/l-1.7mm和d/v-3.3mm施用至正常小鼠脑实质。在细胞施用前一天和细胞施用当天以1mg/kg的剂量口服施用地塞米松,并且从细胞施用前一天至细胞施用后7天以3mg/kg的剂量每天腹腔内施用他克莫司。在mem或hmsc施用后的第7天,通过进行心脏灌注提取脑,然后在pfa中固定,并通过切片组织进行组织学染色。
77.结果,如图4a所示,通过ihc证实了在施用免疫抑制剂的所有组中,与单独施用hmsc的组相比,cd45免疫细胞的浸润减少。与hmsc组相比,差异在所有组中也是统计学上显著的。在几种类型的白细胞中,已知嗜中性粒细胞占最高比例(40-75%)。为了再次证实cd45结果,使用能够对嗜中性粒细胞进行染色的抗体进行ihc。结果,如图4b所示,通过ihc证实了在施用免疫抑制剂的所有组中,与单独施用hmsc的组相比,嗜中性粒细胞免疫细胞的浸润减少。观察到与cd45相同的表达模式。
78.另外,另外进行ihc以证实除免疫细胞(cd45,嗜中性粒细胞)以外的炎性细胞的表达差异。使用靶向小神经胶质细胞的iba-1抗体和靶向巨噬细胞的cd68抗体,它们是炎性细胞的代表性标志物。结果,如图5a所示,在所有组中,观察到iba-1在周围组织中比在施用细胞聚集的部位更强地表达,这与cd45不同。iba-1的表达高于hmsc组。然而,与hmsc组相比,在除单独的地塞米松施用组以外的单独的他克莫司施用组以及地塞米松和他克莫司组合施用组中,差异在统计学上不显著。证实了与cd45、嗜中性粒细胞和iba-1的表达相比,cd68的表达通常非常低。另外,如图5b所示,与hmsc组相比,在施用免疫抑制剂的所有组中cd68表达的差异在统计学上不显著。
79.此外,为了证实由于免疫抑制剂的施用而导致的t细胞表达的差异如何改变,使用能够靶向辅助t细胞(cd4)和细胞毒性t细胞(cd8α)的抗体进行ihc。结果,如图6所示,总的来说,cd4和cd8α的表达在所有组中非常低。证实了与hmsc组相比,在单独的地塞米松和单独的他克莫司施用组中cd4的表达降低。差异也是统计学上显著的。与hmsc组相比,在施用免疫抑制剂的所有组中未观察到cd8α表达的差异。
80.实施例4:通过免疫抑制剂的组合施用提高间充质干细胞存活率的证实
81.为了定量人来源的间充质干细胞(hmsc)的残留量,在与实施例3相同的条件下进
行实验,然后从提取的小鼠脑中分离基因组dna,制备能够结合人特异性alu dna序列的引物,并进行定量实时pcr(qpcr)。此外,在施用mem或hmsc后的第7天,为了进行另外的实验,通过进行心脏灌注提取脑,然后在pfa中固定,并通过切片组织进行组织学染色。还使用能够特异性染色人来源细胞的stem121抗体进行ihc。
82.结果,如图7所示,证实了与单独的hmsc施用组相比,当组合施用免疫抑制剂时干细胞的保留率是高的。证实了地塞米松和他克莫司组合施用组中干细胞的保留率最高,然后是单独的地塞米松施用组。通过ihc使用stem121标志物证实了相同的结果。
83.实施例5:(概念验证)免疫缺陷小鼠中降低间充质干细胞免疫应答的证实
84.使用免疫缺陷小鼠进行另外的实验以证明本研究的概念。在与实施例3相同的条件下将mem或hmsc施用至正常c57bl/6和免疫缺陷的balb/c裸鼠中。与实施例3不同,没有组合施用免疫抑制剂。
85.结果,如图8所示,证实了与正常小鼠(c57bl/6)相比,免疫缺陷的(balb/c裸鼠)小鼠中cd45(图8a)和嗜中性粒细胞(图8b)的表达在施用hmsc的部位处降低。证实了这与免疫抑制剂和hmsc共施用至正常小鼠后免疫细胞的分布的结果相同。
86.如图9所示,与正常小鼠相比,iba-1和cd68在裸鼠中的表达差异在统计学上不显著。
87.如图10所示,证实了与正常小鼠相比,裸鼠中cd4 t细胞的表达急剧降低。与正常小鼠相比,裸鼠中cd8αt细胞的表达看起来降低,但差异在统计学上不显著。
88.实施例6:(概念验证)免疫缺陷小鼠中间充质干细胞存活率提高的证实
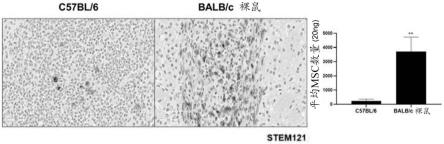
89.为了定量人来源的间充质干细胞(hmsc)的残留量,在与实施例3相同的条件下进行实验,然后从提取的小鼠脑中分离基因组dna,制备能够结合人特异性alu dna序列的引物,并进行定量实时pcr(qpcr)。还使用能够特异性染色人来源细胞的stem121抗体进行ihc。
90.结果,如图11所示,证实了干细胞在免疫缺陷小鼠中的保留率高于在正常小鼠中的保留率。对于ihc,还观察到stem121在免疫缺陷裸鼠中的表达高于在正常小鼠中的表达。
91.本发明的上述描述是为了说明的目的而提供的,并且本发明所属领域的技术人员将理解,在不改变本发明的技术精神或基本特征的情况下,可以容易地将本发明修改成其它特定形式。因此,应理解,上述实施方案在所有方面仅是示例性的,而不是限制性的。
92.工业实用性
93.根据本发明的包含免疫抑制剂的组合物可以显著提高干细胞的存活率,并且可以有效地用作间充质干细胞治疗剂,其通过克服由施用异种细胞引起的免疫应答而使干细胞的治疗效果最大化。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。