1.本发明属于中成药制备方法领域;具体涉及一种治疗动脉硬化的软胶囊的制备方法。
背景技术:
2.流行病学调查显示吸烟、糖尿病、高脂血症、高血压病、高同型半胱氨酸血症、高凝状态、血液粘着性增高及高龄等是下肢动脉硬化性闭塞症的危险因素。其中吸烟与糖尿病的危害最大,二者均可使周围动脉疾病的发生率增高3~4倍,合并存在危险性更高。其次是高脂血症,尤其是血低密度脂蛋白胆固醇升高,与全身多部位动脉粥样硬化的发生密切相关。
3.下肢动脉硬化性闭塞症一般见于中老年人,常伴有吸烟、糖尿病、高血压、高脂血症等危险因素。下肢动脉硬化性闭塞症症状的有无和严重程度,受病变进展的速度、侧支循环的多寡、个体的耐受力等多种因素影响。症状一般由轻至重逐渐发展,但在动脉硬化闭塞症基础上继发急性血栓形成时,可导致症状突然加重。
4.动脉硬化是一种全身性疾病,应整体看待和治疗,包括控制血压、血糖、血脂,严格戒烟等,并积极诊治可能伴发的心脑血管疾病。在医生指导下加强锻炼,促进侧支循环形成;并注意足部护理,避免皮肤破损、烫伤等。针对下肢动脉硬化性闭塞症的药物治疗,主要用于早、中期患者,或作为手术及介入治疗的辅助。常用药物包括:抗血小板药,如阿司匹林、氯吡格雷等;血管扩张及促进侧支循环形成的药物,如西洛他唑、安步乐克及前列腺素类药物等。
技术实现要素:
5.本发明目的是提供了一种治疗动脉硬化的软胶囊的制备方法。
6.本发明通过以下技术方案实现:
7.一种治疗动脉硬化的软胶囊的制备方法,包括如下步骤:
8.步骤1、称量中药生药蓬子菜180g、黄芪180g、金银花120g、赤芍90g~150g、泽泻90g、延胡索90g~120g、炙甘草90g、地龙90g~120g、全蝎90g、路路通90g~120g,待用;
9.步骤2、将步骤1称量好的中药生药加水浸没药材,并浸泡60~70min,然后加14~18倍质量的水煎煮2次,每次1~1.5h,合并煎液,滤过,待用;
10.步骤3、将步骤2得到的煎液浓缩至稠膏,稠膏相对密度为1.1~1.2g/cm3;
11.步骤4、将步骤3得到的稠膏中加入乙醇,含醇量为70~80%,静至使沉淀,取上清液,滤过,减压回收乙醇,浓缩成稠膏,真空干燥,粉碎成80~120目的粉末,待用;
12.步骤5、将步骤4得到的粉末按照质量比为1:1.35加入peg400或大豆油或玉米油,然后加入2wt%的peg6000或吐温80、4~12wt%的丙二醇,混匀,制成1000粒治疗动脉硬化的软胶囊。
13.本发明所述的一种治疗动脉硬化的软胶囊的制备方法,步骤1中药生药的成分为
蓬子菜180g、黄芪180g、金银花120g、赤芍90g、泽泻90g、延胡索90g、炙甘草90g、地龙90gg、全蝎90g、路路通90g。
14.本发明所述的一种治疗动脉硬化的软胶囊的制备方法,步骤1中中药生药的成分为蓬子菜180g、黄芪180g、金银花120g、赤芍150g、泽泻90g、延胡索120g、炙甘草90g、地龙120g、全蝎90g、路路通120g。
15.本发明所述的一种治疗动脉硬化的软胶囊的制备方法,步骤2中药生药加水浸没药材,并浸泡60min,然后加18倍质量的水煎煮2次,每次1.5h,合并煎液,滤过。
16.本发明所述的一种治疗动脉硬化的软胶囊的制备方法,步骤3煎液浓缩至稠膏的浓缩温度为85℃。
17.本发明所述的一种治疗动脉硬化的软胶囊的制备方法,步骤4稠膏中加入乙醇使含醇量为80%。
18.本发明所述的一种治疗动脉硬化的软胶囊的制备方法,步骤4真空干燥的温度为70℃下干燥12~60h。
19.本发明所述的一种治疗动脉硬化的软胶囊的制备方法,步骤4真空干燥的温度为70℃下干燥48h。
20.本发明所述的一种治疗动脉硬化的软胶囊的制备方法,步骤5中粉末按照质量比为1:1.35加入peg400,然后加入2wt%的peg6000、10wt%的丙二醇,混匀,制成1000粒治疗动脉硬化的软胶囊。
21.本发明所述的一种治疗动脉硬化的软胶囊的制备方法,优化了制备工艺,内容物为棕褐色的油状物;气微,味苦,具有最高的出膏率,分散性良好。
附图说明
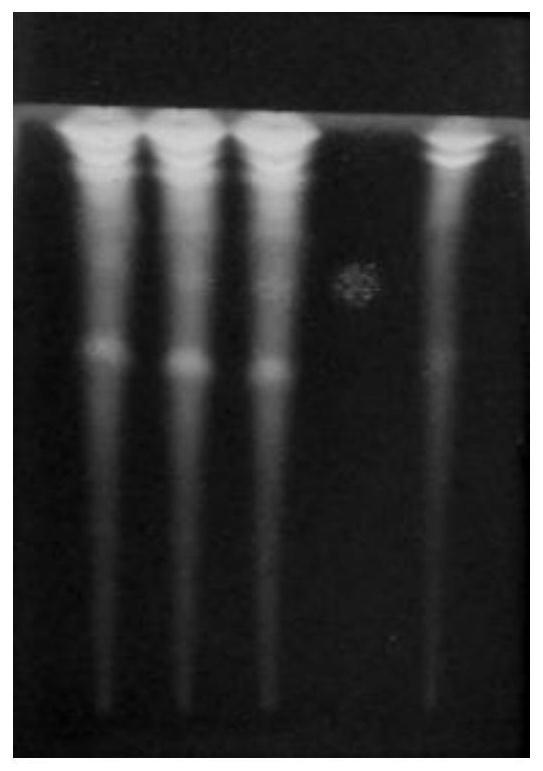
22.图1为具体实施方式二方法制备的成品中黄芪定性鉴别的tcl图谱;
23.图2为具体实施方式二方法制备的成品中金银花定性鉴别的tcl图谱;
24.图3为具体实施方式二方法制备的成品中赤芍定性鉴别的tcl图谱;
25.图4为具体实施方式二方法制备的成品中炙甘草定性鉴别的tcl图谱;
26.图5为具体实施方式二方法制备的成品中路路通定性鉴别的tcl图谱;
27.图6为具体实施方式二方法制备的成品中泽泻定性鉴别的tcl图谱;
28.图7为具体实施方式二方法制备的成品中延胡索定性鉴别的tcl图谱;
29.图8为具体实施方式二中黄芪甲苷对照品的高效液相色谱图谱;
30.图9为具体实施方式二方法制备的成品测试的高效液相色谱图谱;
31.图10为具体实施方式二方法除黄芪成分后制备的成品测试的高效液相色谱图谱。
具体实施方式
32.具体实施方式一:
33.一种治疗动脉硬化的软胶囊的制备方法,、包括如下步骤:
34.步骤1、称量中药生药蓬子菜180g、黄芪180g、金银花120g、赤芍90g~150g、泽泻90g、延胡索90g~120g、炙甘草90g、地龙90g~120g、全蝎90g、路路通90g~120g,待用;
35.步骤2、将步骤1称量好的中药生药加水浸没药材,并浸泡60~70min,然后加14~
18倍质量的水煎煮2次,每次1~1.5h,合并煎液,滤过,待用;
36.步骤3、将步骤2得到的煎液浓缩至稠膏,稠膏相对密度为1.1~1.2g/cm3;
37.步骤4、将步骤3得到的稠膏中加入乙醇,含醇量为70~80%,静至使沉淀,取上清液,滤过,减压回收乙醇,浓缩成稠膏,真空干燥,粉碎成80~120目的粉末,待用;
38.步骤5、将步骤4得到的粉末按照质量比为1:1.35加入peg400或大豆油或玉米油,然后加入2wt%的peg6000或吐温80、4~12wt%的丙二醇,混匀,制成1000粒治疗动脉硬化的软胶囊。
39.本实施方式所述的一种治疗动脉硬化的软胶囊的制备方法,步骤1中中药生药的成分为蓬子菜180g、黄芪180g、金银花120g、赤芍150g、泽泻90g、延胡索120g、炙甘草90g、地龙120g、全蝎90g、路路通120g。
40.本实施方式所述的一种治疗动脉硬化的软胶囊的制备方法,步骤2中药材吸水率实验效果如表1所示:实验表明复方药材在浸泡50分钟时,已达到最佳吸水率,基本处于饱和状态,考虑到误差因素,所以确定本处方药材最佳浸泡时间为1h,首次水提取时需多加出药材量的1倍。
41.表1药材吸水率实验
[0042][0043][0044]
本实施方式所述的一种治疗动脉硬化的软胶囊的制备方法,步骤4中选择用醇沉淀法进行除杂,实验效果如表2所示:从表2能够看出,乙醇浓度为80%时具有最好的提取效果。
[0045]
表2醇沉浓度实验
[0046][0047]
本实施方式所述的一种治疗动脉硬化的软胶囊的制备方法,步骤3中考察煎煮次数、加水量、煎煮时间四个因素,分别设定三个水平,以黄芪甲苷提取量和出膏率为评价指标,优化提取参数,取正交设计中9次试验所得干膏,按供试品溶液制备方法制得供试品溶液,进样10μl,记录黄芪甲苷峰面积,代入回归方程,计算干膏中黄芪甲苷的含量,最终得出结论:即将处方量1/2.5的药材,加18倍量水首剂量多加1倍量水,浸泡1小时后,煎煮2次,每次1小时,过滤,合并滤液,滤过,滤液浓缩,加乙醇使含醇量为80%,抽滤,回旋,干燥。平均出膏率为21.82%,黄芪甲苷含量为0.5225mg/g,结果证明该提取工艺稳定可靠。
[0048]
本实施方式所述的一种治疗动脉硬化的软胶囊的制备方法,考察步骤4中干燥时间如表3所示,以含水量为指标,见表3。从表3能够看出,干燥48小时为宜。
[0049]
表3干燥时间实验
[0050][0051]
本实施方式所述的一种治疗动脉硬化的软胶囊的制备方法,考察步骤4中粉碎粒度可知,80目时稳定性较差,100目和120目时稳定性良好。
[0052]
本实施方式所述的一种治疗动脉硬化的软胶囊的制备方法,考察步骤5中peg400、大豆油和玉米油,搅拌混合均匀,考察混合体系的均匀性及沉降体积比如表4所示:
[0053]
表4分散剂实验
[0054][0055]
本实施方式所述的一种治疗动脉硬化的软胶囊的制备方法,考察步骤5中peg用量效果,如表5所示:聚乙二醇400用量为药膏重量的1.35倍以上时,流动性较好,为减少用药剂量,节约成本,选用聚乙二醇400用量为药膏重量的1.35倍。
[0056]
表5 peg400用量实验
[0057][0058]
本实施方式所述的一种治疗动脉硬化的软胶囊的制备方法,考察步骤5单一采用peg400作为分散介质,混悬效果较差,所以考虑加入适量助悬剂。通常使用peg6000或吐温-80做助悬剂。取粉末10g(100目),以1∶1.35的比例加入peg400,2%的比例分别加入peg6000或吐温-80,搅拌混合均匀,从结果能够看出,加入peg6000的效果更好。考察peg6000的加入量效果如表6所示:peg 6000用量2%以上时,沉降体积比、流动性,再分散性较好。
[0059]
表6 peg6000实验效果
[0060][0061]
本实施方式所述的一种治疗动脉硬化的软胶囊的制备方法,为减少聚乙二醇类对囊壁的硬化,需加入丙二醇,丙二醇的加入量实验效果如表7所示:丙二醇的用量为10%以上时,沉降体积比、流动性,再分散性较好。
[0062]
表7丙二醇实验效果
[0063][0064]
具体实施方式二:
[0065]
一种治疗动脉硬化的软胶囊的制备方法,包括如下步骤:
[0066]
步骤1、称量中药生药蓬子菜180g、黄芪180g、金银花120g、赤芍90g~150g、泽泻90g、延胡索90g~120g、炙甘草90g、地龙90g~120g、全蝎90g、路路通90g~120g,待用;
[0067]
步骤2、将步骤1称量好的中药生药加水浸没药材,并浸泡60~70min,然后加14~
18倍质量的水煎煮2次,每次1~1.5h,合并煎液,滤过,待用;
[0068]
步骤3、将步骤2得到的煎液浓缩至稠膏,稠膏相对密度为1.1~1.2g/cm3;
[0069]
步骤4、将步骤3得到的稠膏中加入乙醇,含醇量为70~80%,静至使沉淀,取上清液,滤过,减压回收乙醇,浓缩成稠膏,真空干燥,粉碎成80~120目的粉末,待用;
[0070]
步骤5、将步骤4得到的粉末按照质量比为1:1.35加入peg400或大豆油或玉米油,然后加入2wt%的peg6000或吐温80、4~12wt%的丙二醇,混匀,制成1000粒治疗动脉硬化的软胶囊。
[0071]
本实施方式所述的一种治疗动脉硬化的软胶囊的制备方法,步骤1中中药生药的成分为蓬子菜180g、黄芪180g、金银花120g、赤芍150g、泽泻90g、延胡索120g、炙甘草90g、地龙120g、全蝎90g、路路通120g。
[0072]
本实施方式所述的一种治疗动脉硬化的软胶囊的制备方法,步骤2中药生药加水浸没药材,并浸泡60min,然后加18倍质量的水煎煮2次,每次1.5h,合并煎液,滤过。
[0073]
本实施方式所述的一种治疗动脉硬化的软胶囊的制备方法,步骤3煎液浓缩至稠膏的浓缩温度为85℃。
[0074]
本实施方式所述的一种治疗动脉硬化的软胶囊的制备方法,步骤4稠膏中加入乙醇使含醇量为80%。
[0075]
本实施方式所述的一种治疗动脉硬化的软胶囊的制备方法,步骤4真空干燥的温度为70℃下干燥48h。
[0076]
本实施方式所述的一种治疗动脉硬化的软胶囊的制备方法,步骤5中粉末按照质量比为1:1.35加入peg400,然后加入2wt%的peg6000、10wt%的丙二醇,混匀,制成1000粒治疗动脉硬化的软胶囊。
[0077]
本实施方式所述的一种治疗动脉硬化的软胶囊的制备方法,对制备好的治疗动脉硬化的软胶囊中的内容物进行鉴定:图1为本实施方式方法制备的成品中黄芪定性鉴别的tcl图谱;图2为本实施方式方法制备的成品中金银花定性鉴别的tcl图谱;图3为本实施方式方法制备的成品中赤芍定性鉴别的tcl图谱;图4为本实施方式方法制备的成品中炙甘草定性鉴别的tcl图谱;图5为本实施方式方法制备的成品中路路通定性鉴别的tcl图谱;图6为本实施方式方法制备的成品中泽泻定性鉴别的tcl图谱;图7为本实施方式方法制备的成品中延胡索定性鉴别的tcl图谱。从图中能够看出,相关中药成分能够清晰检测出来。
[0078]
本实施方式所述的一种治疗动脉硬化的软胶囊的制备方法,按照《中国药典》(2015版)四部(通则)微生物限度检查法操作,微生物分三批检测,检测结果如表8所示:
[0079]
表8微生物检测实验
[0080][0081]
本实施方式所述的一种治疗动脉硬化的软胶囊的制备方法,制备的治疗动脉硬化的软胶囊进行黄芪甲苷含量测试:如图8-图10所示,从图8-图10对比可知,精密吸取黄芪甲苷对照品溶液、供试品溶液及阴性对照溶液各20ul分别注入液相色谱仪。结果在黄芪甲苷对照品峰保留时间位置供试品溶液出现吸收峰,阴性对照溶液未出现吸收峰,表明其它组分对测定无干扰。测试结果为:按每粒0.5g计算,下限降幅20%,则每粒软胶囊中含黄芪甲
苷的量应不低于0.13mg。
[0082]
具体实施方式三:
[0083]
一种治疗动脉硬化的软胶囊的制备方法,包括如下步骤:
[0084]
步骤1、称量中药生药蓬子菜180g、黄芪180g、金银花120g、赤芍90g~150g、泽泻90g、延胡索90g~120g、炙甘草90g、地龙90g~120g、全蝎90g、路路通90g~120g,待用;
[0085]
步骤2、将步骤1称量好的中药生药加水浸没药材,并浸泡60~70min,然后加14~18倍质量的水煎煮2次,每次1~1.5h,合并煎液,滤过,待用;
[0086]
步骤3、将步骤2得到的煎液浓缩至稠膏,稠膏相对密度为1.1~1.2g/cm3;
[0087]
步骤4、将步骤3得到的稠膏中加入乙醇,含醇量为70~80%,静至使沉淀,取上清液,滤过,减压回收乙醇,浓缩成稠膏,真空干燥,粉碎成80~120目的粉末,待用;
[0088]
步骤5、将步骤4得到的粉末按照质量比为1:1.35加入peg400或大豆油或玉米油,然后加入2wt%的peg6000或吐温80、4~12wt%的丙二醇,混匀,制成1000粒治疗动脉硬化的软胶囊。
[0089]
本实施方式所述的一种治疗动脉硬化的软胶囊的制备方法,步骤1中中药生药的成分为蓬子菜180g、黄芪180g、金银花120g、赤芍90g、泽泻90g、延胡索90g、炙甘草90g、地龙90gg、全蝎90g、路路通90g。
[0090]
本实施方式所述的一种治疗动脉硬化的软胶囊的制备方法,步骤2中药生药加水浸没药材,并浸泡60min,然后加18倍质量的水煎煮2次,每次1.5h,合并煎液,滤过。
[0091]
本实施方式所述的一种治疗动脉硬化的软胶囊的制备方法,步骤3煎液浓缩至稠膏的浓缩温度为85℃。
[0092]
本实施方式所述的一种治疗动脉硬化的软胶囊的制备方法,步骤4稠膏中加入乙醇使含醇量为80%。
[0093]
本实施方式所述的一种治疗动脉硬化的软胶囊的制备方法,步骤4真空干燥的温度为70℃下干燥48h。
[0094]
本实施方式所述的一种治疗动脉硬化的软胶囊的制备方法,步骤5中粉末按照质量比为1:1.35加入peg400,然后加入2wt%的peg6000、10wt%的丙二醇,混匀,制成1000粒治疗动脉硬化的软胶囊。
[0095]
本实施方式所述的一种治疗动脉硬化的软胶囊的制备方法,制备的治疗动脉硬化的软胶囊的稳定性测试如表9所示:
[0096]
表9治疗动脉硬化的软胶囊的稳定性测试
[0097][0098][0099]
本实施方式所述的一种治疗动脉硬化的软胶囊的制备方法,治疗动脉硬化的软件囊治疗动脉硬化闭塞症的药效学试验研究如下:
[0100]
本实施方式所述的一种治疗动脉硬化的软胶囊的制备方法,通过观察治疗动脉硬化的软胶囊对动脉硬化闭塞症大鼠模型血脂、血液流变学及血管内皮细胞功能的影响,考
察治疗动脉硬化的软胶囊对动脉硬化闭塞症这一类疾病的治疗作用。为临床应用及药物开发提供参考依据,并完善药理方面实验内容。
[0101]
供试品配制,配制方法:根据临床用量,并参照人与实验动物体表面积折算系数,分别配制不同的浓度。配制频率:给药前一天配制。保存条件:4℃冷藏保存。给药时间:每天上午8:30点左右给药一次。
[0102]
实验动物:种系:sd大鼠;性别:
♀
30只、
♂
30只;要求购入数量:60只;要求购入时体重范围:230-270g;使用数量:60只;供给源:黑龙江中医药大学安全性评价中心;动物生产许可证号码:scxk(黑)2013-004。给药剂量如表10所示:给药频率:连续给药8周。
[0103]
表10治疗动脉硬化的软胶囊给药剂量
[0104][0105]
动脉硬化闭塞症(aso)模型复制:联合采用高脂饮食饲养及隐动脉内膜损伤的方法制作aso模型。实验前大鼠适应性喂养1周,排除饮食异常大鼠,高脂饮食喂养1周后用10%水合氯醛腹腔注射麻醉,每只大鼠均取左后肢消毒。从腹股沟中点向后肢内侧纵行切开皮肤,分离并暴露隐动脉,动脉夹阻断隐动脉远、近端共1.5-2.0cm,取胰岛素注射器一支,沿隐动脉血管长轴从远端向近端刺入血管腔,将0.2-0.3ml注射用无菌蒸馏水缓慢注入阻断部位血管,至血管充盈为止。5分钟后取下针头和动脉夹,压迫止血,缝合切口。内膜损伤完成后仍继续每日喂高脂饮食,并应用维生素d3(30万u/kg),右后肢肌肉注射,每4周注射1次。共制作aso模型50只。
[0106]
分组与给药:采用随机法分为模型组,高、中、低剂量组、阳性药对照组,每组10只。另取10只sd大鼠作为正常组。造模后次日,每组均予相应浓度的药物灌胃,模型及正常对照组给予等体积蒸馏水灌胃,每日1次,直至造模后8周。
[0107]
血脂检测:末次给药1小时后,眶静脉丛取血,离心,分离血清,按试剂盒方法检测血清中甘油三酯、胆固醇、高密度脂蛋白、低密度脂蛋白含量。
[0108]
血液流变学检测:末次给药1小时后,眶静脉丛取血,置于肝素钠抗凝管中用于,检测全血粘度、血浆粘度、聚集指数、刚性指数、变形指数。
[0109]
血管内皮细胞功能检测:末次给药1小时后,眶静脉丛取血,离心,分离血清,按试剂盒方法检测血清中no、内皮素-1(et-1)含量。
[0110]
隐动脉病理学检测:末次给药1小时后,取血后,将各组大鼠左侧隐动脉上段剪下约1cm,固定于4%多聚甲醛溶液,常规病理切片,he染色,进行病理学观察。
[0111]
实验结果如下:
[0112]
治疗动脉硬化的软胶囊对动脉硬化闭塞症大鼠血脂水平的影响
[0113]
与正常组相比,造模后各组大鼠的血清胆固醇、甘油三酯、低密度脂蛋白水平明显升高,高密度脂蛋白水平明显降低,差异均有显著意义(p<0.05);与模型组相比,治疗动脉硬化的软胶囊低、中、高浓度组的血清胆固醇、甘油三酯水平明显下降,差异均有显著意义
(p<0.05),但高、低密度脂蛋白的变化不明显。各给药组与阳性药对照组比较,无显著性差异(p》0.05)。结果见表11。
[0114]
表11各组大鼠血脂水平
[0115][0116]
注:与正常组比较,
△
p<0.05;与模型组比较,*p<0.05;
[0117]
治疗动脉硬化的软胶囊对动脉硬化闭塞症大鼠血流变学指标的影响
[0118]
与正常对照组相比,模型组的全血黏度、血浆黏度、红细胞聚集指数、刚性指数均明显升高(p<0.05),红细胞变形指数有下降趋势,但无统计差异。与模型对照组相比,中、高浓度治疗动脉硬化的软胶囊组的全血黏度、血浆黏度、红细胞聚集指数、刚性指数均有明显下降(p<0.05),高浓度组的作用更加显著。各给药组与阳性药对照组比较,无显著性差异(p》0.05),结果见表12。
[0119]
表12各组大鼠血液流变学的水平
[0120][0121][0122]
注:与正常组比较,
△
p<0.05;与模型组比较,*p<0.05。
[0123]
治疗动脉硬化的软胶囊对动脉硬化闭塞症大鼠血清中no、et-1含量的影响
[0124]
与正常组比较,模型组大鼠的血清et-1水平明显升高,差异有统学意义(p<0.05),血清中no水平无明显变化(p》0.05);与模型组比较,治疗动脉硬化的软胶囊低、中、高剂量组血清中的et-1水平有改善,以高剂量组的变化最为明显,差异有统计学意义(p<0.05),no水平无明显变化(p》0.05)。各给药组与阳性药对照组比较,无显著性差异(p》0.05)。结果见表13。
[0125]
表13血管内皮细胞中no及内皮素-1含量测定
[0126][0127]
注:与正常组比较,
△
p<0.05;与模型组比较,*p<0.05。
[0128]
病理形态观察:
[0129]
正常组大鼠隐动脉内皮细胞、内弹力板及平滑肌细胞均排列规整,血管腔未见狭窄;模型组大鼠隐动脉管腔不规则狭窄,动脉壁内皮细胞、内弹力板及平滑肌细胞均排列紊乱;治疗动脉硬化的软胶囊低、中剂量组大鼠隐动脉壁组织结构趋于改善,管腔逐渐扩大;高剂量组组和阳性药物对照组大鼠隐动脉管腔狭窄程度明显减轻。
[0130]
治疗动脉硬化的软胶囊各剂量组大鼠与动脉硬化闭塞症模型组大鼠相比,治疗动脉硬化的软胶囊中、高剂量组的血清胆固醇、甘油三酯水平,全血黏度、血浆黏度、红细胞聚集指数、刚性指数均明显降;低、中、高剂量组组血清中的et-1有改善,高剂量组的变化最为明显;隐动脉壁组织结构趋于改善,管腔逐渐扩大;高剂量组大鼠隐动脉管腔狭窄程度明显减轻。以上结果表明,治疗动脉硬化的软胶囊能够降低动脉硬化闭塞症模型组大鼠血清中的血脂水平、降低其血液粘稠度,使其动脉管腔狭窄程度明显减轻,对动脉硬化闭塞症具有良好的治疗作用。
[0131]
用spss11.6进行统计描述和分析,数据用表示,组间比较采用t检验,多组间比较采用单因素方差分析,p<0.05为差异有统计学意义。
[0132]
本实施方式所述的一种治疗动脉硬化的软胶囊的制备方法,治疗动脉硬化的软件囊治疗动脉硬化闭塞症的一般药理学试验研究如下:考察治疗动脉硬化的软胶囊对小鼠神经系统的影响、对大鼠心血管系统的影响、对大鼠呼吸系统的影响,观察确定治疗动脉硬化的软胶囊可能关系到人的安全性的非期望药理作用;评价药物在毒理学和/或临床研究中所观察到的药物不良反应和/或病理生理作用;研究所观察到的和/或推测的药物不良反应机制。为临床应用及药物开发提供参考依据,并完善安全性方面实验内容。
[0133]
本实施方式所述的一种治疗动脉硬化的软胶囊的制备方法,实验动物为:种系:昆明种小鼠、sd大鼠;性别:雌雄各半;购入数量:小鼠40只、sd大鼠40只;购入时体重范围:小鼠18-20g、大鼠200-210g;使用时体重范围:小鼠18-22g、大鼠220~240g;供给源:黑龙江中医药大学实验动物中心;动物合格证号::scxk(黑)2013-004。给药剂量如表14所示,给药频率,每日一次。
[0134]
表14治疗动脉硬化的软胶囊给药剂量
[0135][0136]
实验方法:对小鼠自发活动的影响:选取在实验室饲养3天的18~22g小鼠40只,雌
雄各半。按体重随机分成4组,即正常对照组、治疗动脉硬化的软胶囊高、中、低剂量组。各组按给药剂量每天灌胃给药1次,连续给药3天,正常对照组给等体积蒸馏水。末次给药1h后,观察小鼠异常步态、竖毛、活动减少、静卧、跳跃、震颤、异常分泌、异常排泄等变化,并分别把小鼠投入箱中适应5分钟后(每箱只放1只小鼠),记录小鼠5分钟内活动数值。结果以表示,用组间t检验检查其组间差异显著性。
[0137]
对戊巴比妥钠睡眠时间的影响
[0138]
按体重随机分成4组,即正常对照组、治疗动脉硬化的软胶囊高、中、低剂量组。各组按给药剂量每天灌胃给药1次,连续给药3天,正常对照组给等体积蒸馏水。末次给药1h后,腹腔注射阈剂量戊巴比妥钠(50mg/kg),以翻正反射消失为入睡时间,从翻正反射消失至恢复时间为睡眠持续时间。结果以表示,用组间t检验检查其组间差异显著性。
[0139]
对小鼠协调功能的影响
[0140]
取一直径1.77cm,长76.2cm光滑的玻璃棒(或金属棒)一根,与地面垂直放置,并固定底部,保持直立。使小鼠从玻璃棒顶端爬到底部(一步一步向下爬行),10s不能通过或掉棒者淘汰。取筛选合格的40只小鼠,适应喂养3天后,按体重随机分成4组,即正常对照组、治疗动脉硬化的软胶囊高、中、低剂量组。各组按给药剂量每天灌胃给药1次,连续给药3天,正常对照组给等体积蒸馏水。记录小鼠爬杆所用时间。
[0141]
实验结果:
[0142]
对小鼠一般行为表现的影响
[0143]
给药后,各给药组动物与空白组比较,活动正常、步态稳健、无流涎、肌颤等现象,未见产生不良反应。
[0144]
对小鼠自发活动的影响
[0145]
给药后各组动物与空白组比较,活动次数未出现显著性差异,结果见表15。
[0146]
表15药物对小鼠自主活动的影响
[0147][0148]
对戊巴比妥钠睡眠时间的影响
[0149]
给药后各组动物与空白组比较,睡眠时间未出现显著性差异。结果见表16。
[0150]
表16对戊巴比妥钠致小鼠睡眠时间的影响
[0151][0152][0153]
对小鼠协调运动的影响
[0154]
给药后各组动物与空白组比较,均稳步爬行,未有滑行及掉落现象,爬杆时间未出现显著性差异。结果见表17。
[0155]
表17对小鼠爬杆时间的影响
[0156][0157]
治疗动脉硬化的软胶囊对呼吸和心血管系统的影响:动物:sd品系健康成年大鼠,220~240g。雌雄各半,(购自黑龙江中医药大学实验动物中心)。
[0158]
取在实验室正常饲养7天的成年未孕sd大鼠40只,雌雄各半,体重220-240g。将大鼠按体重随机分为4组,即空白对照组(等体积蒸馏水)、治疗动脉硬化的软胶囊高、中、低剂量组,每组10只。大鼠以40mg/kg戊巴比妥钠腹腔麻醉,仰卧在手术台上,将充满肝素生理盐水的导管插入左颈总动脉,与压力换能器相连接,于大鼠胸部剑突下链接张力换能器,各换能器与生物机能系统相连接,以记录动物呼吸、血压、心率。动物各记录指标稳定后开始实验,分别记录给药前及给药后1h、2h的呼吸、血压、和心率情况。
[0159]
给药后各组动物与空白组比较,呼吸频率、血压、心率未出现显著性差异,结果见表18、表19、表20。
[0160]
表18对大鼠呼吸系统的影响
[0161][0162]
表19对大鼠心电的影响
[0163][0164]
表20对大鼠血压的影响
[0165][0166]
由实验结果可知,治疗动脉硬化的软胶囊在一般药理学各项指标检测中,各给药组与空白组比较,未见显著性差异。可推治疗动脉硬化的软胶囊对神经系统,心血管及呼吸系统无不良影响,可应用于临床。
[0167]
治疗动脉硬化的软胶囊灌胃给药小鼠急性毒性实验:观察治疗动脉硬化的软胶囊一日内灌胃给予受试动物(小鼠)后所产生的急性毒性反应及最大给药量,为多次重复给药毒性试验的剂量、可能的靶器官和毒性反应等指标的设计及临床剂量设计与观察提供参考依据,完善药理方面实验内容。
[0168]
实验动物:种系:昆明小鼠;等级:清洁级;性别:雌性;购入数量:50只;购入时体重范围:18-20g;使用数量:40只;使用时体重范围:19-21g;供给源:黑龙江中医药大学实验动物中心;动物生产许可证号:scxk(黑)2013-004;动物使用许可证号:syxk(黑)2013-012。
[0169]
依据国家食品药品监督管理局令《中药、天然药物急性毒性研究技术指导原则》。
[0170]
预实验
[0171]
目的:找出引起小鼠0%死亡的最大剂量和引起小鼠100%死亡的最小剂量,以便安排正式试验的组间间距。
[0172]
方法:选取健康雌性小鼠20只,体重20
±
1g,随机分5组,每组4只。各组小鼠禁食不禁水12小时后,以供试品浓度20.54%为最大浓度,组间浓度等比级数为k=1:0.75。各组按给药体积0.4ml/10g、3次/日,共给药1天,进行灌胃给药。给药后观察小鼠毒性反应情况及7日内行为活动、体征及死亡情况。
[0173]
结果:小鼠按上述剂量灌胃给药后,7日内各组无一只死亡,活动自如,饮食正常,毛发光泽,尿、粪便性状无异常,未能找出引起100%动物死亡的最小剂量。
[0174]
最大给药量的测定
[0175]
目的:测定供试品能达到人用量的多少倍,对其安全性进行评估。为临床用药提供参考,也为开展药效学的研究提供科学依据。
[0176]
方法:选取健康雌性小鼠20只,体重20
±
1g。禁食不禁水12小时后,24小时内灌胃给药3次,每次给予供试品浓度为20.54%,体积0.4ml/10g(40ml/kg),给药后观察小鼠毒性反应情况及14日内行为活动、体征及死亡情况。按公式计算小鼠的最大耐受量倍数。
[0177]
结果:小鼠按上述剂量灌胃给药后,14日内无一只死亡,活动自如,饮食正常,毛发光泽,尿、粪便性状无异常。
[0178]
经计算,小鼠的最大耐受量倍数为:
[0179][0180]
经计算,其最大给药量为临床用药剂量的675.66倍,并未表现出毒性反应,初步可以认为治疗动脉硬化的软胶囊临床用药是安全的。
[0181]
治疗动脉硬化的软胶囊大鼠灌胃给药长期毒性试验:
[0182]
观察重复经口给予治疗动脉硬化的软胶囊对大鼠所产生的毒性反应,出现的症状和严重程度,并提供毒副反应的靶器官及其损害的可逆程度,确定无毒反应剂量,以评价治疗动脉硬化的软胶囊长期用药的安全性,为拟定临床试验剂量及观察指标提供参考。
[0183]
供试品配制
[0184]
配制方法:称取一定重量的治疗动脉硬化的软胶囊,加入少量蒸馏水研磨,要尽量磨细、磨匀,最后加入一定量体积的蒸馏水,配制成一定百分浓度的混悬液。灌胃时要在磁力搅拌下抽取使用。给药剂量按动物每公斤体重治疗动脉硬化的软胶囊制剂重计算。
[0185]
保存条件:放在4℃保存。
[0186]
给药时间:每周一至周六的上午8:30左右给药1次,周日不给药。连续给药6个月。
[0187]
根据国家食品药品监督管理局2005年7月颁发的《中药、天然药物长期毒性研究技术指导原则》要求,选用wistar大鼠。因为该动物背景资料丰富,国内外多沿用这种实验系统,有利于与其它试验的结果进行比较。
[0188]
实验动物的种、系、数量、年龄、性别、体重范围、来源和等级:种系:wistar大鼠;等级:清洁级;性别:雌、雄各半;要求购入数量:120只;要求使用数量:120只;要求购入时体重范围:80-110g(6-9周龄);供给源:黑龙江中医药大学实验动物中心;动物生产许可证号:scxk(黑)2013-004;动物使用许可证号:syxk(黑)2013-012。
[0189]
实验结果为:对wistar大鼠作了长期毒性实验研究:
[0190]
治疗动脉硬化的软胶囊以10倍临床拟用剂量(0.3648g/kg)、30倍临床拟用剂量(1.0944g/kg)、60倍临床拟用剂量(2.1888g/kg),给大鼠连续灌胃180天,并进行实验中期(给药90天)和1个月恢复期实验观察。结果是:
[0191]
对大鼠血液学指标的影响:
[0192]
连续给药3个月,各给药组与空白对照组比较,血液学各指标无显著性变化,无统计学意义。
[0193]
连续给药6个月,各给药组与空白对照组比较,血液学各指标无显著性变化,无统计学意义。
[0194]
停药1月后所有血液学指标均为正常
[0195]
对大鼠血液生化指标的影响
[0196]
连续给药3个月,各给药剂量组的血液生化指标:alt、ast、alp、ck、bun、crea、glu、tp、alb、t-bil、tg、t-cho、k
与空白对照组比较,均无显著差异。
[0197]
连续给药6个月,各给药剂量组的血液生化指标:alt、ast、alp、ck、bun、crea、glu、tp、alb、t-bil、tg、t-cho、k
与空白对照组比较,均无显著差异。
[0198]
停药1个月后,所有生化学指标均为正常
[0199]
连续给药3个月及连续给药6各月,对大鼠脏器重量(心、肝、脾、肺、肾、肾上腺、胸腺、子宫、卵巢、睾丸、附睾、前列腺及脑共13个脏器)无明显影响,各组脏器系数基本相近。对脏器组织(除上述13个脏器外,还有胰腺、胃、回肠、结肠、脑垂体、脊髓、骨髓、淋巴结、膀胱、坐骨神经、甲状腺、主动脉、颌下腺等)病理组织学检查,未发现明显的与药物毒性有关的病理形态学改变。具体测试结果如以下表所示:
[0200]
表21用药3个月对大鼠体重的影响
[0201][0202][0203]
表22用药3个月对大鼠血常规的影响
[0204][0205]
表23用药3个月对大鼠血常规的影响
[0206][0207]
表24用药3个月对大鼠wbc分类计数(%)的影响
[0208][0209]
表25用药3个月对大鼠血液生化指标的影响
[0210][0211][0212]
注:与空白组比较,*p《0.05,**p《0.01,***p《0.001(以下同)
[0213]
表26用药3个月对大鼠脏器系数的影(x
±
s)
[0214][0215]
表27治疗动脉硬化的软胶囊给药3个月大鼠病理检验结果
[0216]
[0217][0218]
注:1、表中“ ”表示脏器有轻微病变
[0219]
2、表中“-”表示脏器没有明显的病理改变
[0220]
3、数字(1~10)表示动物的只数
[0221]
表28用药6个月对大鼠体重的影响
[0222]
[0223][0224]
表29用药6个月对大鼠血常规的影响
[0225][0226]
表30用药6个月对大鼠血常规的影响
[0227][0228]
表31对用药6个月大鼠wbc分类计数(%)的影响
[0229][0230]
表32用药6个月对大鼠血液生化指标的影响
[0231]
[0232][0233]
表33用药6个月对大鼠脏器系数的影响
[0234]
[0235][0236]
表34治疗动脉硬化的软胶囊给药6个月大鼠病理检查结果
[0237]
[0238][0239]
表35恢复期大鼠体重的变化
[0240][0241]
表36恢复期大鼠血常规的变化
[0242][0243]
[0244]
表37恢复期大鼠血常规的变化
[0245][0246]
表38恢复期大鼠wbc分类计数(%)的变化
[0247][0248]
表39恢复期大鼠生化指标的变化
[0249][0250]
表40恢复期大鼠脏器系数的变化
[0251]
[0252][0253]
表41恢复期大鼠病理检查结果
[0254]
[0255][0256][0257]
注:1、表中“ ”表示脏器有轻微病变
[0258]
2、表中“-”表示脏器没有明显的病理改变
[0259]
3、数字(1~10)表示动物的只数
[0260]
表42实验中期(用药3个月)大鼠进食量
[0261][0262]
表43用药3-6个月对大鼠进食量的影响
[0263]
[0264][0265]
表44恢复期大鼠进食量变化
[0266]
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。