1.本发明属于制剂学领域,具体涉及一种安立生坦雾化吸入溶液及制备方法。
背景技术:
2.肺动脉高压(pulmonary arterial hypertension,pah)是一种病变累计肺动脉血管内皮细胞、肌层以及外膜而使肺动脉血流受限,导致肺血管阻力增加,肺动脉压进行性升高,并最终引起右心衰竭甚至死亡的一种恶性心血管疾病,其主要特征为肺动脉阻塞引起肺血管阻力(pulmonary vascular resistance,pvr)及肺动脉压力(pulmonary arterial pressure,pap)渐进性升高,伴随不可逆的肺血管重构,患者症状严重可引起右心衰竭而死亡,预后较差,死亡率高。同时,随着我国人口老龄化的加剧,近年来pah患者总数逐年上升,严重危害患者的身心健康。
3.安立生坦又名安贝生坦,化学名称:( )-(2s)2-(4,6-二甲基嘧啶-2-基)氧基-3-甲氧基-3,3-二苯基丙酸;化学式:c
22h22
n2o4,分子量:378.42,结构式如下:
[0004][0005]
安立生坦作为一种口服的选择性内皮素受体拮抗剂,有减低内源性血管收缩、抗增生、抗纤维化和抗炎等作用,2007年被fda批准口服用于肺动脉高血压患者的治疗。
[0006]
肺血管内皮素(endothelin,et)系统成为治疗pah的新靶点,其中et受体拮抗药已成为口服治疗重度pah的一线药物。安立生坦作为et受体拮抗药,其与et受体结合后发挥作用,降低et与内皮素受体结合,降低内皮素的作用,改善病变组织的纤维化,提高血管的舒张能力。在临床实验中,可以提高患者运动能力,缓解症状的恶化,且只需每日一次给药,更加方便。
[0007]
目前国内外市场上所售安立生坦剂型均为片剂,但片剂对于幼儿及昏迷病人不宜吞服,且制备工艺复杂,技术要求高,用于治疗pah起效慢,不能直达病变部位。
[0008]
中国专利cn103860525a中公开了安立生坦的胶囊型吸入粉雾剂,其中记载了安立生坦胶囊型吸入粉雾剂包括胶囊壳和胶囊内容物,所述的胶囊内容物的重量为5~300mg;所述的安立生坦与赋形剂乳糖重量比为1:0.5~50;所述的安立生坦的平均粒径小于10μm,其中80%的粒径小于5μm;所述的赋形剂乳糖的粒径范围为30~200μm。但粉雾剂需要依赖于患者较大吸气流速以启动雾化,患者在正常呼吸条件下无法实现药物的递送,因而不适合儿童、老人和其他主动呼吸较为困难的患者使用。
[0009]
综上所述,现有技术中公开的安立生坦制剂,存在使用人群方面限制,因此开发一种适合无自主吸入能力的婴幼儿童和主动呼吸困难患者,可直接作用于病变部位,刺激性低,制备工艺简单且稳定性好的安立生坦制剂是本领域技术人员亟待解决的问题。
技术实现要素:
[0010]
为了解决上述技术问题,本发明提供了一种安立生坦雾化吸入溶液制剂和制备方法及其应用。
[0011]
本发明旨在一定程度上解决现有技术中的不足,提供如下技术方案:
[0012]
一方面,本发明提供一种安立生坦雾化吸入溶液,包含安立生坦、溶剂和辅料,
[0013]
所述单剂量规格的吸入溶液中包含安立生坦0.1~20mg,优选地,包含安立生坦2.5~15mg。
[0014]
所述吸入溶液单剂量规格为1~5ml,优选地,所述单剂量规格为2~5ml;
[0015]
所述溶剂为无菌注射用水;
[0016]
所述辅料包含缓冲剂、等渗调节剂;
[0017]
所述缓冲剂的用量为0.01%~1.0%(w/v);
[0018]
所述等渗调节剂的加入为使所述吸入溶液具有200~400mosmol/kg的重量克分子渗透浓度;
[0019]
所述缓冲剂可选自柠檬酸钠、磷酸氢二钠、磷酸二氢钠、磷酸氢二钾、磷酸二氢钾中的一种或几种;
[0020]
所述等渗调节剂可选自葡萄糖、氯化钠、甘油、丙二醇中的一种或几种,优选氯化钠;
[0021]
所述辅料还可以包括ph调节剂;
[0022]
所述ph调节剂的加入量为使所述吸入溶液的ph值为6.5~10.0,优选地,ph值为8.0~10.0;
[0023]
所述ph调节剂可选自药学上可接受的碳酸氢钠、碳酸钠、氢氧化钠中的一种或几种。
[0024]
另一方面,本发明提供一种安立生坦雾化吸入溶液的制备方法,包括以下步骤:
[0025]
(1)量取所需制备溶液总量60%~80%(v/v)的溶剂,得到第一溶液;
[0026]
(2)控制第一溶液温度为50~90℃条件下,逐量将等渗调节剂、缓冲剂依次加入所述第一溶液,搅拌均匀,得到第二溶液;
[0027]
(3)安立生坦加入所述第二溶液中,搅拌均匀,得到第三溶液;
[0028]
(4)待第三溶液降温至30℃以下,加入ph调节剂搅拌均匀,调节溶液ph至6.5~10.0,得到第四溶液;
[0029]
(5)向所述第四溶液中补加溶剂定容至所需制备溶液总量,搅拌均匀,得到第五溶液,用0.22μm滤膜或滤芯过滤;
[0030]
(6)灌装至1~5ml规格的安瓿瓶中,密封。
[0031]
再一方面:本发明提供一种安立生坦吸入溶液雾化给予人呼吸道的吸入系统,包括1ml-5ml安立生坦吸入溶液及液体雾化装置,所述安立生坦吸入溶液使用液体雾化装置雾化成气溶胶,
[0032]
所述液体雾化装置的气流压力为5bar,
[0033]
所述液体雾化装置的流速为(15
±
0.75)l/min,
[0034]
所述气溶胶中活性成分的递送速率》1.5mg/min,
[0035]
所述气溶胶递送率》60%,
[0036]
所述气溶胶ngi中微细粒子分数(fpf)》60%,
[0037]
所述气溶胶雾滴的粒径分布在1-6μm。
[0038]
本发明的有益效果是:
[0039]
1、本发明制备了一种稳定的安立生坦雾化吸入溶液,无需添加表面活性剂、稳定剂,通过加入适量缓冲剂和酌量加入ph调节剂,使安立生坦溶液中的溶解度及ph值均达到药学吸入溶液要求,且溶液的稳定性良好;通过加入等渗调节剂,减低了对呼吸道粘膜的刺激性,增加顺应性,使制剂更安全。
[0040]
2、本发明提供一种安立生坦雾化吸入溶液的制备工艺,控制合适的配液温度,使活性成分在溶媒中有适宜的溶解速度;采用过滤除菌工艺,在保障产品无菌水平的同时,进一步提高制剂的稳定性,质量可靠,工艺操作简单,易于控制,适合大规模生产。
[0041]
3、本发明为无自主吸入能力的婴幼儿童和主动呼吸困难患者提供了一种新型安全有效的安立生坦药物制剂。
[0042]
4、本发明提供一种安立生坦雾化吸入溶液雾化给药系统,通过控制液体雾化装置的气流压力、流速和雾化后气溶胶中活性成分的递送速率、递送总量、粒径分布,使药液得以精确控制形成气溶胶雾滴的粒径均匀分布在最适合肺部吸入的1-6μm,使得足够的药液在肺部被吸收,从而发挥相应的药效作用,使得安立生坦雾化吸入溶液可以精确的调节给药剂量。
具体实施方式
[0043]
为了更好的说明本发明,在下文的具体实施方式中给出了众多的具体细节。本领域技术人员应当理解,没有某些具体细节,本发明同样可以实施。下列实施例仅用于说明本发明,而不应视为限制本发明的范围。凡依照本发明内容进行的任何本领域的等同替换,均属于本发明的保护范围。
[0044]
以下,针对构成本发明所述的安立生坦雾化吸入溶液的各组分进行说明。
[0045]
试验例1不同辅料对安立生坦溶解情况影响考察
[0046]
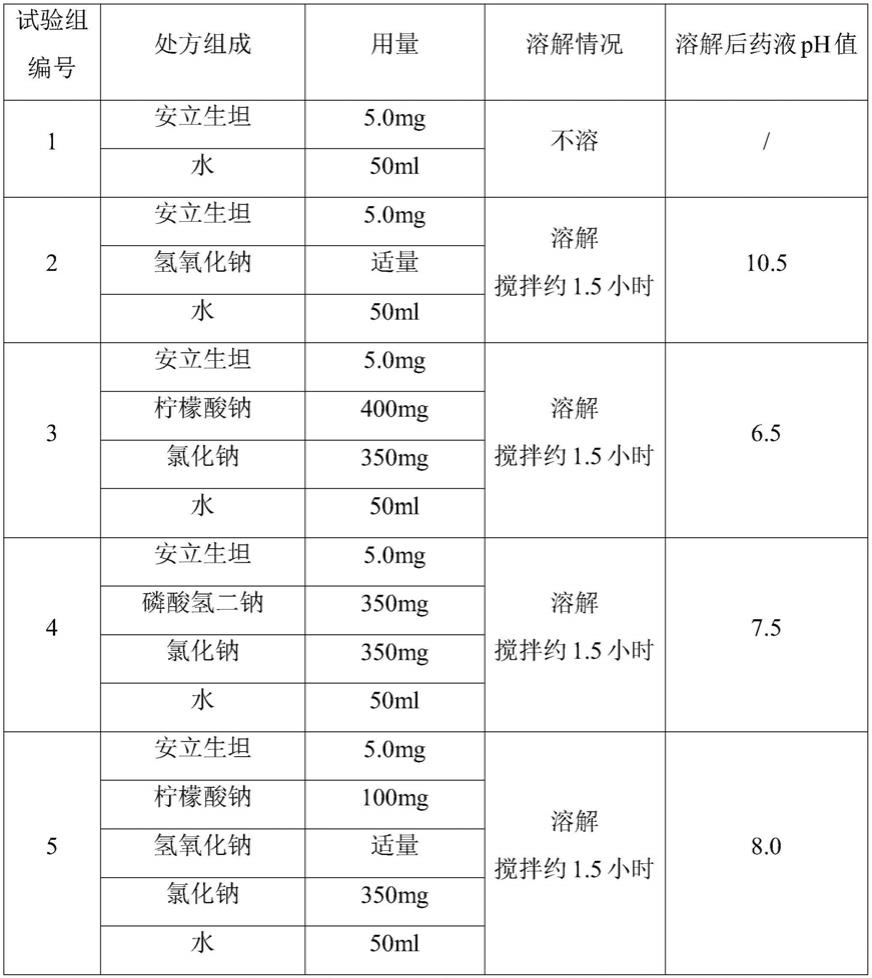
在溶剂(25℃)中加入不同辅料,观察对安立生坦溶解情况的影响:
[0047][0048]
由上表可知,试验组1中安立生坦的溶解度不能达到药学有效浓度;试验组2中安立生坦能溶解,但溶解后药液ph值超出吸入溶液剂要求的ph值范围(3~10),且药液ph过高对呼吸道的刺激性会增强;试验组3、试验组4和试验组5中安立生坦的溶解度均能达到药学有效浓度,且溶解后药液ph值又在吸入溶液剂要求的ph值范围(3~10)内,同时加入等渗调节剂,增加溶液的顺应性,减低对呼吸道粘膜的刺激性。综上,确定安立生坦吸入溶液制剂中的辅料组成:缓冲剂和等渗调节剂,还可以酌量加入ph调节剂。
[0049]
另外,以上实验结果表明,虽然药液ph值6.5以上时,加入适宜辅料可使安立生坦溶解度增加,但不同ph值和不同辅料均不能加快安立生坦的溶解速度。
[0050]
试验例2不同配液温度的考察
[0051]
对安立生坦溶液在不同配液温度下的溶解情况进行了考察:
[0052][0053]
由上表可知:随着配液温度的升高,安立生坦的溶解速率变快,配液温度为25℃时溶解时间过长,50℃~90℃时溶解速率较快,能满足生产需求。
[0054]
试验例3溶液不同ph值的考察
[0055]
在处方相同的情况下,考察不同溶液ph值体系对样品质量的影响:
[0056]
处方组成:
[0057]
名称组成安立生坦2.0g氯化钠7.5g柠檬酸钠3.0g氢氧化钠适量至ph值6.0、6.5、7.5、8.0、10.0加注射用水至1000ml
[0058]
制备方法:
[0059]
量取注射用水700ml(处方量的70%),加热升温至80℃并保温,依次投入处方量氯化钠、柠檬酸钠,搅拌溶解后投入安立生坦,继续搅拌,同时加入适量的氢氧化钠溶液,调节至药液ph值为6.0、6.5、7.5、8.0、10.0搅拌均匀后,用溶剂补至全量,用0.22μm滤膜或滤芯过滤后,灌装至2ml的安瓿瓶中、密封,即得。
[0060]
对调节至不同ph值样品的有关物质进行测定,采用hplc法,检测条件:色谱柱:waters symmctry shield rp18(3.9*150mm,5μm);流动相:流动相a:磷酸二氢钾缓冲液-乙腈(62:38),流动相b:乙腈,梯度洗脱;流速:1.2ml/min;柱温:30℃;检测波长:220nm;测定结果见下表:
[0061][0062]
由上表可看出:样品ph值为6.0(低于6.5)时,样品配置完放置第二天即有析出,样品ph值在6.5~10.0之间,室温放置2天及60℃放置10天后,均无析出,即可满足雾化吸入溶液要求;当样品ph值8.0~10.0之间时,有关物质总量更低,且60℃放置10天后增长更慢,即稳定性更优。
[0063]
综合考察试验例1和试验例3的结果可知:安立生坦吸入溶液制剂中的辅料包括缓冲剂和等渗调节剂时,安立生坦的溶解度能达到药学有效浓度,且溶解后药液ph值在6.5~7.5之间,即可满足吸入溶液剂要求的ph值范围(3~10)内;结合对溶液ph值的考察,溶液ph值在8.0~10.0之间时,有关物质总量更低,且60℃放置10天后增长更慢,即稳定性更优,因ph调节剂的加入可调节溶液的ph值在8.0~10.0之间,确定吸入溶液制剂中的辅料优选包括缓冲剂、等渗调节剂和ph调节剂。
[0064]
以下,参照实施例对本发明进行详述,但本发明的保护范围不限于此。
[0065]
实施例1
[0066]
处方组成
[0067]
名称组成安立生坦2.0g氯化钠7.5g柠檬酸钠3.0g氢氧化钠调节ph值至8.0加注射用水至1000ml
[0068]
制备方法:
[0069]
量取注射用水800ml(处方量的80%),加热升温至70℃并保温,依次投入处方量氯化钠、柠檬酸钠,搅拌溶解后投入安立生坦,继续搅拌使溶解,添加氢氧化钠溶液调节ph值至8.0,搅拌均匀后,用溶剂补至全量,用0.22μm滤膜或滤芯过滤后,灌装至5ml的安瓿瓶中、
密封,即得。
[0070]
实施例2
[0071]
处方组成
[0072][0073][0074]
制备方法:
[0075]
量取注射用水700ml(处方量的70%),加热升温至50℃并保温,依次投入处方量氯化钠、柠檬酸钠,搅拌溶解后投入安立生坦,继续搅拌使溶解,搅拌均匀后(ph值为6.5),溶剂补至全量,用0.22μm滤膜或滤芯过滤后,灌装至1ml的安瓿瓶中、密封,即得。
[0076]
实施例3
[0077]
处方组成
[0078]
名称组成安立生坦2.0g葡萄糖40g碳酸氢钠10g氢氧化钠调节ph值至10.0加注射用水至1000ml
[0079]
制备方法:
[0080]
量取注射用水600ml(处方量的60%),加热升温至60℃并保温,依次投入处方量葡萄糖、碳酸氢钠,搅拌溶解后投入安立生坦,继续搅拌使溶解,添加氢氧化钠溶液调节ph值至10.0,搅拌均匀后,用溶剂补至全量,用0.22μm滤膜或滤芯过滤后,灌装至2ml的安瓿瓶中、密封,即得。
[0081]
实施例4
[0082]
处方组成
[0083]
[0084][0085]
制备方法:
[0086]
量取注射用水800ml(处方量的80%),加热升温至90℃并保温,依次投入处方量甘油、磷酸氢二钾,搅拌溶解后投入安立生坦,添加氢氧化钠溶液调节ph值至9.0,搅拌均匀后,用溶剂补至全量,用0.22μm滤膜或滤芯过滤后,灌装至3ml的安瓿瓶中、密封,即得。
[0087]
实施例5
[0088]
处方组成
[0089]
名称组成安立生坦2.5g丙二醇15g磷酸氢二钠9.0g磷酸二氢钠1.25g加注射用水至1000ml
[0090]
制备方法:
[0091]
量取注射用水800ml(处方量的80%),加热升温至70℃并保温,依次投入处方量丙二醇、磷酸氢二钠、磷酸二氢钠,搅拌溶解后投入安立生坦,继续搅拌使溶解,搅拌均匀后(ph值为7.5),用溶剂补至全量,用0.22μm滤膜或滤芯过滤后,灌装至2ml的安瓿瓶中、密封,即得。
[0092]
实施例6空气动力学雾化粒径测定
[0093]
采用星帕泰克粒径测定仪,对各实施例1~5安立生坦雾化吸入溶液样品的雾化粒径进行测定,测定结果如下:
[0094][0095]
由上表可知:实施例的雾化粒径x
50
均在2~4μm之间,x
84
《6μm,符合雾化制剂的空气动力学参数。
[0096]
实施例7不同雾化装置比较
[0097]
取实施例1的样品,采用不同品牌雾化器进行雾化,其雾化情况见下表:
[0098]
雾化器品牌3min雾化率%5min雾化率%8min雾化率%百瑞40.25
±
1.0864.33
±
0.7978.20
±
1.66欧姆龙39.47
±
1.2265.35
±
0.9476.92
±
2.03
[0099]
注:每种品牌雾化器连续平行考察3组数据。
[0100]
由上表可知:采用百瑞和欧姆龙两种不同品牌的雾化器装置,累计8min雾化后,百瑞和欧姆龙雾化器对样品的雾化率无明显差异。
[0101]
实施例8雾化性能测定-递送速率和递送总量
[0102]
采用neu22型欧姆龙雾化器(压缩空气雾化),分别取上述实施例1~5的安立生坦雾化吸入溶液(雾化体积为样品规格),置己称重的雾化器中,精密称定后开始雾化至无雾释出,并再次精密称定,计算递送速率、递送总量、气雾损失、雾化杯残留、平衡回收率和输出药量。结果如下:
[0103][0104][0105]
注:每组实施例样品进行10次平行测定。
[0106]
由上表可知;1)固定雾化型号,采用本技术控制的雾化压力和流速,实施例样品雾化性能良好,耐用性高,且各实施例样品的递送速率和递送总量之间无明显差异;2)不同实施例之间样品灌装规格不同,除雾化完全所需时间不同外,在雾化性能上无差异;3)本技术中保护的雾化参数条件下安立生坦雾化吸入溶液递送总量高,雾化杯残留量低。
[0107]
实施例9雾化性能测定-微细粒子剂量
[0108]
采用neu22型欧姆龙雾化器(压缩空气雾化),分别取上述实施例1~5的安立生坦雾化吸入溶液(雾化体积为样品规格),置雾化器中,采用设定的气流压力(5bar)和设定的流速(15
±
0.75l/min),用ngi测定实施例的fpf%和mmad值,测定结果见下表:
[0109][0110]
注:每组实施例样品进行3次平行测定。
[0111]
由上表可知:所配制样品按照所设定参数雾化微细粒子剂量fpf%》60%,粒径分布在1-6μm之间。
[0112]
实施例10稳定性情况研究
[0113]
依据本技术实施例1~5配制安立生坦雾化吸入溶液样品,同时放样,进行稳定性影响因素测定其测定结果见下表:
[0114]
各实施例样品稳定性测定数据
[0115][0116]
由各个实施例稳定性及雾化输出药量(%)测定结果可看出,在本专利保护的处方组成和制备工艺条件下制备得到的安立生坦雾化吸入溶液质量稳定,各实施例样品在25℃放置6个月有关物质总量《0.3%,在4℃放置6个月有关物质总量《0.1%;采用本专利保护的雾化参数和特定设备安立生坦雾化吸入溶液的雾化输出药量》60%。
[0117]
以上对本发明进行了详细介绍,本文中应用了具体个例对本发明的原理及实施方式进行了阐述,以上实施例的说明只是用于帮助理解本发明的方法及其核心思想。应当指出对本领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以对本发明进行若干改进和修饰,这些改进和修饰也落入本发明权利要求的保护范围内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。