1.本发明涉及一种用于肺炎衣原体抗原检测的检测装置。
2.具体地说,是涉及一种肺炎衣原体抗原检测板、检测盒。
背景技术:
3.衣原体肺炎是由衣原体引起的肺炎,衣原体分为沙眼衣原体(ct)、肺炎衣原体(cp)鹦鹉热衣原体和家蓄衣原体,引起肺炎的多为肺炎衣原体。肺炎衣原体肺炎多见于学龄儿童,大部分为轻症,发病常隐匿。感染率没有性别差异,四季均可发生。
4.肺炎衣原体(chlamydiapneumoniae,cpn)是一种在细胞内寄生的革兰染色呈阴性的微生物,是常见社区感染的呼吸道病原体之一,在全世界范围内通过气溶胶在人群中传播,经呼吸道传染后可引起肺炎、咽炎、哮喘以及急性支气管炎等疾病。年老体弱、营养不良、免疫功能低者易被感染。肺炎衣原体不能体外培养,只能在细胞内寄生,肺炎衣原体能在呼吸道来源的细胞系如:hep-2和hl细胞系中稳定生长。肺炎衣原体侵入人体后,主要引起单核-巨噬细胞反应,肺泡巨噬细胞作为病原体贮存和传播的载体,造成其在宿主体内的持续感染。肺炎衣原体的致病首先通过黏附素黏附于上皮细胞,原体通过创面侵入机体后吸附于易感的柱状或杯状黏膜上皮细胞并在其中繁殖,促进肺炎衣原体吸附于宿主细胞表面,引起肺炎衣原体感染。
5.目前,肺炎衣原体主要检测方法是对其抗体的检测,对于肺炎衣原体抗原的检测目前市面上方法比较少,主要有荧光pcr法、双扩增法等,但操作繁琐,所需时间比较长,缺乏更为快速简易而又可靠的方法。荧光免疫层析技术作为一项新型免疫检测技术,既保留了传统胶体金试纸条的现场快速检测优点,又加入了荧光检测技术的高灵敏度特点,荧光免疫层析分析方法具有灵敏度高、稳定性好、受自然荧光干扰低等优点,成为提高免疫层析方法检测性能的主要途径之一。
技术实现要素:
6.本发明的目的在于克服上述传统技术的不足之处,提供一种肺炎衣原体抗原检测板、检测盒。
7.本发明的目的是通过以下技术措施来达到的:一种肺炎衣原体抗原检测板,包括密封扣合的上盖和下盖,所述上盖上设有加样孔和观察窗口,所述下盖上设有卡槽,所述卡槽内放置有试纸条,其特征在于:所述试纸条包括pvc板条,所述pvc板条上设有硝酸纤维素膜,所述硝酸纤维素膜的位置与所述观察窗口的位置相对应,所述硝酸纤维素膜远离所述加样孔的一端设有吸水纸,所述硝酸纤维素膜的另一端设有结合垫,且所述结合垫被所述上盖完全覆盖,所述结合垫的自由端设有加样垫,所述加样孔与所述加样垫的位置相对应。
8.作为一种改进,所述试纸条的制作方法如下:将所述pvc板条作为底板,在所述pvc板条的一端贴吸水纸,所述吸水纸的另一端粘贴有所述硝酸纤维素膜,所述硝酸纤维素膜与所述吸水纸重叠1mm,所述硝酸纤维素膜的另一端粘贴有所述结合垫,所述硝酸纤维素膜
与所述结合垫重叠1 mm,所述结合垫的另一端粘贴有所述加样垫,所述加样垫与所述所述结合垫重叠1 mm,将整体压平整后,用切条机切成3.8mm宽的所述试纸条。
9.作为进一步的改进,所述硝酸纤维素膜上包被有第一检测线t,第二检测线c;第一检测线 t与第二检测线c间隔40mm,且第一检测线t上喷涂有亲和素,所述第二检测线c上喷涂有羊抗鼠。
10.作为进一步的改进,所述结合垫的制备方法如下:结合垫处理液所选的缓冲系统为10mmol/l磷酸盐缓冲液;所述结合垫处理液主要包括表面活性剂s9质量分数为0.5%,聚乙烯吡咯烷酮pvp质量分数为0.5%,吐温体积分数为0.1%,将结合垫浸泡于结合垫处理液中,处理时间30min,烘箱烘干,存放备用。
11.作为进一步的改进,所述结合垫上将生物素肺炎衣原体抗体p1与荧光肺炎衣原体抗体p2固相与所述结合垫上,并将结合垫放于鱼线板上,放入37℃的恒温鼓风干燥箱中,干燥1-2h左右,等结合垫完全干燥后使用。
12.作为进一步的改进,所述结合垫上将生物素肺炎衣原体抗体p1与荧光肺炎衣原体抗体p2固相方法为:宽度为6mm的结合垫上每厘米固相生物素肺炎衣原体抗体0.02ul,荧光肺炎衣原体抗体0.25ul,并添加质量分数为2%的稳定剂(海藻糖及蔗糖),用划膜仪以5ul/cm的喷量划于结合垫中间。
13.作为进一步的改进,所述结合垫上生物素肺炎衣原体抗体p1,其制备方法如下:生物素肺炎衣原体抗体p1的最终浓度为2 mg/ml,用纯水配制nahco3, nahco3的终浓度为0.1mol/l,生物素最终浓度为0.000266 mmol/m l,将混匀后的生物素标记抗体,置于微量振荡器,避光、室温标记反应30min;生物素抗体的纯化:将标记结束的生物素抗体取出装入透析袋中,放入3000ml磷酸盐缓冲液pbs中,磁力搅拌器400 stir/min,4℃旋转透析24h,取出后存放备用 。
14.作为进一步的改进,所述结合垫上荧光标记肺炎衣原体抗体p2的制备如下:荧光标记肺炎衣原体抗体p2的最终浓度2.5 mg/ml,用纯水配制nahco3,nahco3的终浓度为0.1mol/l,荧光染料终浓度为1mmol/l,将混匀后的生物素标记抗体,置于微量振荡器,避光、室温标记反应60min;荧光抗体的纯化:将标记结束的荧光抗体取出装入透析袋中,放入3000ml 磷酸盐缓冲液pbs中,磁力搅拌器400 stir/min,4℃旋转透析24h。
15.本发明还公开了一种肺炎衣原体抗原检测盒,包括上面所述的检测板,还包括提取管、一次性采样拭子、样本检测液。
16.作为一种改进,所述样本检测液由20mmol/l,ph为8的tris-hcl缓冲液、质量分数为2.5%的s9,质量分数为0.9%的nacl,体积分数0.01%的吐温,质量分数为0.1%的酪蛋白。
17.由于采用了上述技术方案,与现有技术相比,本发明的优点是:第一:本发明采用抗原检测,抗原检测可以在潜伏期、急性期或病程初期检测到,而抗体检测要晚一些;第二:本发明采用生物素-亲和素放大系统,提高了灵敏度及特异性;第三:生物素标记抗体与荧光标记抗体固相与结合垫上,有利于信号的释放及提高稳定性;第四:优化后的放大系统结合垫及第一检测线t包被液中添加蔗糖海藻糖,有利于
工作液的均一性及稳定性,可提高重复性及本发明的储存;第五:本发明中的方法为免疫荧光法,利用免疫荧光定量分析仪,结果读取快速准确,只需15min即可获得结果,无需专业人士,普遍适用于门诊和急诊检测。
18.下面结合附图和具体实施方式对本发明作进一步说明。
附图说明
19.附图1是本发明所述上盖的结构示意图;附图2是本发明所述下盖的结构示意图;附图3是本发明所述试纸条结构示意图;附图4是本发明所述试纸条爆炸结构示意图。
具体实施方式
20.下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
21.在本发明的描述中,需要理解的是,术语“中心”、“纵向”、“横向”、“长度”、“宽度”、“厚度”、“上”、“下”、“前”、“后”、“左”、“右”、“竖直”、“水平”、“顶”、“底”、“内”、“外”、“顺时针”、“逆时针”等指示的方位或位置关系为基于附图所示的方位或位置关系,仅是为了便于描述本发明和简化描述,而不是指示或暗示所指的设备或元件必须具有特定的方位、以特定的方位构造和操作,因此不能理解为对本发明的限制。
22.在本发明中,除非另有明确的规定和限定,术语“安装”、“设置”、“连接”、“固定”、“旋接”等术语应做广义理解,例如,可以是固定连接,也可以是可拆卸连接,或成一体;可以是机械连接,也可以是电连接;可以是直接相连,也可以通过中间媒介间接相连,可以是两个元件内部的连通或两个元件的相互作用关系,除非另有明确的限定,对于本领域的普通技术人员而言,可以根据具体情况理解上述术语在本发明中的具体含义。
23.此外,术语“第一”、“第二”仅用于描述目的,而不能理解为指示或暗示相对重要性或者隐含指明所指示的技术特征的数量。由此,限定有“第一”、“第二”的特征可以明示或者隐含地包括一个或者更多个该特征。在本发明的描述中,“多个”的含义是两个或两个以上,除非另有明确具体的限定。
24.实施例一:如附图1-附图4所示,一种肺炎衣原体抗原检测板,包括密封扣合的上盖1和下盖2,所述上盖1上设有加样孔11和观察窗口12,所述下盖2上设有卡槽21,所述卡槽21内放置有试纸条3,所述试纸条3包括pvc板条31,所述pvc板条31上设有硝酸纤维素膜32,所述硝酸纤维素膜32的位置与所述观察窗口12的位置相对应,所述硝酸纤维素膜32远离所述加样孔11的一端设有吸水纸33,所述硝酸纤维素膜32的另一端设有结合垫34,且所述结合垫34被所述上盖1完全覆盖,所述结合垫34的自由端设有加样垫35,所述加样孔11与所述加样垫35的位置相对应。
25.所述试纸条3的制作方法如下:将所述pvc板条31作为底板,在所述pvc板条31的一端贴吸水纸33,所述吸水纸33的另一端粘贴有所述硝酸纤维素膜32,所述硝酸纤维素膜32
与所述吸水纸33重叠1mm,所述硝酸纤维素膜32的另一端粘贴有所述结合垫34,所述硝酸纤维素膜32与所述结合垫34重叠1 mm,所述结合垫34的另一端粘贴有所述加样垫35,所述加样垫35与所述所述结合垫34重叠1 mm,将整体压平整后,用切条机切成3.8mm宽的所述试纸条3。
26.所述硝酸纤维素膜32上包被有第一检测线t,第二检测线c;第一检测线 t与第二检测线c间隔40mm,且第一检测线t上喷涂有亲和素,所述第二检测线c上喷涂有羊抗鼠。
27.所述结合垫34的制备方法如下:结合垫处理液所选的缓冲系统为10mmol/l磷酸盐缓冲液;所述结合垫处理液主要包括表面活性剂s9质量分数为0.5%,聚乙烯吡咯烷酮pvp质量分数为0.5%,吐温体积分数为0.1%,将结合垫34浸泡于结合垫处理液中,处理时间30min,烘箱烘干,存放备用。
28.所述结合垫34上将生物素肺炎衣原体抗体p1与荧光肺炎衣原体抗体p2固相与所述结合垫34上,并将结合垫34放于鱼线板上,放入37℃的恒温鼓风干燥箱中,干燥1-2h左右,等结合垫34完全干燥后使用。
29.所述结合垫34上将生物素肺炎衣原体抗体p1与荧光肺炎衣原体抗体p2固相方法为:宽度为6mm的结合垫34上每厘米固相生物素肺炎衣原体抗体0.02ul,荧光肺炎衣原体抗体0.25ul,并添加质量分数为2%的稳定剂,稳定剂为海藻糖或蔗糖,用划膜仪以5ul/cm的喷量划于结合垫34中间。
30.所述结合垫34上生物素肺炎衣原体抗体p1,其制备方法如下:生物素肺炎衣原体抗体p1的最终浓度为2 mg/ml,用纯水配制nahco3, nahco3的终浓度为0.1mol/l,生物素最终浓度为0.000266 mmol/m l,将混匀后的生物素标记抗体,置于微量振荡器,避光、室温标记反应30min;生物素抗体的纯化:将标记结束的生物素抗体取出装入透析袋中,放入2000-3000ml磷酸盐缓冲液pbs中,磁力搅拌器200-400 stir/min,4℃旋转透析24h,取出后存放备用 。
31.所述结合垫34上荧光标记肺炎衣原体抗体p2的制备如下:荧光标记肺炎衣原体抗体p2的最终浓度2.5 mg/ml,用纯水配制nahco3,nahco3的终浓度为0.1mol/l,荧光染料终浓度为1mmol/l,将混匀后的生物素标记抗体,置于微量振荡器,避光、室温标记反应60min;荧光抗体的纯化:将标记结束的荧光抗体取出装入透析袋中,放入2000-3000ml 磷酸盐缓冲液pbs中,磁力搅拌器200-400 stir/min,4℃旋转透析24h。
32.实施例二:一种肺炎衣原体抗原检测盒,包括实施例一中所述的检测板,还包括提取管、一次性采样拭子、样本检测液。
33.所述样本检测液由20mmol/l,ph为8的tris-hcl缓冲液、质量分数为2.5%的s9,质量分数为0.9%的nacl,体积分数0.01%的吐温,质量分数为0.1%的酪蛋白。
34.本试剂盒检测采用免疫荧光双抗体夹心法并结合放大系统,其基本原理是免疫层析检测技术和放大系统标记技术的结合,产品采用抗原抗体相结合的基本原理,即结合垫34上包被生物素标记的肺炎衣原体抗体和荧光标记的肺炎衣原体抗体,硝酸纤维素膜32上包被亲和素和羊抗鼠质控线,当样本中含有肺炎衣原体抗原时,与结合垫34上的荧光标记的鼠抗肺炎衣原体单克隆抗体结合,在层析作用下沿膜向上移动,迁移至检测线处时生物素与亲和素结合形成复合物,荧光标记的鼠抗肺炎衣原体单克隆抗体继续迁移至质控线
时,与羊抗鼠igg多克隆抗体结合,形成复合物。
35.本实施例的检测方法如下:一、实验前的准备:1)样本采集:根据标准临床法收集拭子样本,从咽喉、扁桃体或咽喉其他发炎部位取样。
36.2)样本处理:预先在配置的提取管中加入0.5ml样本提取液,放在立架上,将采集样本后的拭子浸入样本提取液中搅拌。从提取管的外侧,用手指挤压棉棒数次,使提取液充分浸透棉棒,然后拔出棉棒,挤出的液体作为样品检测。
37.3)将id芯片插入仪器中,确保id芯片与试剂盒批号相匹配。
38.4)检测前将实施例一所述的检测板恢复至室温。
39.二、加样及检测1)在实施例一所述的检测板的加样孔11中滴加约2-3滴(约100μl)样本提取管中的液体;2)将实施例一所述的检测板插入分析仪的卡槽21中,确保实施例一所述的检测板方向正确并将其完全推入,开始检测,仪器将自动扫描实施例一所述的检测板,未在规定时间内的检测结果无效;3)从荧光免疫分析仪的显示屏幕上读取数据或直接打印结果。
40.三、阳性判断值或者参考区间阴性:结果﹤1.0阳性:结果≥1.0四、检验结果的解释荧光免疫分析仪器自动判定结果及实施例一所述的检测板是否有效。
41.阳性:表明检测出肺炎衣原体抗原;可疑:处于临界值(1.0
±
15%)附近的结果,建议使用其它适当的检测方法进行确认;阴性:表明未检测出肺炎衣原体抗原;无效:表明本次检测结果无效,应更换实施例一所述的检测板重新实验。
42.本发明所述性能指标主要包括以下几点:1 、外观1.1外包装应整洁无污染。检测试剂应无破损、完整、无毛刺,材料附着牢固。
43.1.2试剂盒组分应齐全。
44.2 、阴性符合率用阴性参考品n1-n10进行检测,结果均为阴性(阴性符合率:10/10)。
45.3、 阳性符合率用阳性参考品p1-p2进行检测,结果均为阳性(阳性符合率:2/2)。
46.4、 最低检出限用最低检出限参考品s1-s2进行检测,结果为阳性。
47.5 、精密度5.1 批内精密度
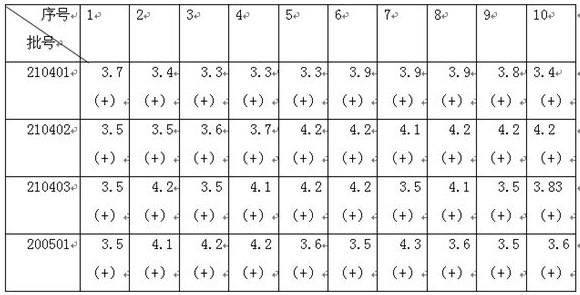
用精密度参考品r平行进行10人份检测,反应结果均为阳性,变异系数为7.2%,符合变异系数不大于15.0%表1肺炎衣原体抗原检测试剂盒批内精密度5.2批间精密度用精密度参考品r各平行进行10人份检测,反应结果均为阳性,变异系数为8.8%,结果符合变异系数不大于20.0%。
48.表2肺炎衣原体抗原检测试剂盒批间精密度6稳定性在2~30℃条件下保存至有效期结束或37℃条件下放置6个月,检测结果符合1-5所有性能指标,试剂盒稳定性考察结果如下:表1肺炎衣原体抗原检测板37℃加速破坏实验结果
注:阴性参考品浓度≤1ru/ml,阳性参考品浓度>1ru/ml。
49.根据阿伦尼乌斯公式对应的温度与老化天数关系, 37℃破坏6个月无问题,相当于常温下可保存2年,符合试剂盒效期要求。
50.以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,均应包含在本发明的保护范围之内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。