1.本发明涉及aav递送拆分型碱基编辑器领域中的用于碱基编辑的组合物及其应用。
背景技术:
2.单碱基编辑系统是基于crispr/cas9技术发展起来的一种新型的碱基替换技术,通过没有活性的或者具有单条链切割活性的cas蛋白与碱基脱氨酶融合,在特定grna的引导下可以引起碱基的定向突变但是不会造成双链的断裂,具有更高的编辑效率。目前常见的碱基编辑器有胞嘧啶碱基编辑器(cbe),其可以将碱基c突变为t,腺嘌呤碱基编辑器(abe)可以将碱基a突变为g,以及gbe碱基编辑器可以实现哺乳动物细胞中碱基c到g的转化。其中 cbe碱基编辑器可以在基因中引入提前终止密码子,从而达到基因敲除的目的。目前,引导编辑器(prime editor)可以实现特定位点任意碱基之间的变换,其主要由具有单条链切割活性的 cas9蛋白融合逆转录酶rt组成,并对grna进行改造,在其c端插入突变的模板和引物结合位点(primer binding site,pbs)得到prime editing guide rna(pegrna)。pe系统通过pegrna 靶向基因组内特定位点,被cas9n-h840a切口酶切断的非互补链与pegrna携带的pbs结合,在逆转录酶作用下,沿着逆转录模板(rt template)延伸,从而在靶位点实现特定碱基的转换、插入和缺失。
3.碱基突变引发的疾病在人类遗传病中占据绝大比例,由此,碱基编辑器的开发及应用将为这类疾病的治疗做出重大贡献。目前碱基编辑技术已经广泛应用于基因治疗、动物模型构建、精准动物育种和基因功能分析等领域,为基础和应用研究提供了强大的技术工具。基因治疗载体是将外源基因导入体内靶细胞并发挥作用的重要媒介,其承载量和导入效率严重影响治疗效果,其可分为病毒载体和非病毒载体。病毒载体是通过病毒将目的基因导入受体细胞从而实现疾病的治疗。目前已被广泛应用于细胞、动物模型和临床应用中。clinicaltrials.gov 上显示的正在进行的临床试验中,最常用的体内基因治疗载体是aav。aav是一种非致病性病毒,与其他病毒载体相比,aav已被证明具有较低的免疫原性,是相对安全的基因治疗载体。除此之外,基于aav的基因疗法也有望在单次给药后实现持久甚至终生的临床获益,也称为“一次性治疗”。aav较适用于直接向靶组织进行给药,即直接注射到相关病灶部位或理想的生物活性部位。
4.aav属于微小病毒科依赖病毒属,无自主复制能力,需要在辅助病毒如腺病毒或疱疹病毒的帮助下进行复制,是一种单链dna缺陷型病毒。aav直径在18-26nm之间,其整个基因组长度约为4.7kb,由两个反向重复序列(inverted terminal repeats,itrs)和两个基因,即rep基因和cap基因组成。itrs是位于aav基因组中的唯一顺式作用元件,是aav病毒包装所必须的自身结构,主要起指导基因复制和引导病毒组装的作用。重组aav病毒 (recombined aav,raav)是将天然存在的aav经过基因工程改造,由治疗性外源转基因代替rep和cap基因,仅保留两端的itr序列,所产生的一种可供人工转基因应用的载体。raav 中外源基因组的长度极限在4.7kb左右,如果超过其容量病毒的出毒率会显著降低,这也是影
响aav广泛应用的主要限制因素,因此如何将crispr/cas9系统或者碱基编辑器插入aav载体中实现高效的病毒组装及递送至靶点发挥其功能是目前基因治疗中面临的重要问题之一。目前常用的碱基编辑器主要有cbe、abe、gbe以及引导编辑pe系统。其中碱基编辑器cbe、abe、gbe的主要元件有脱氨酶、cas9核酸酶、尿嘧啶dna糖基化酶抑制剂(uracildnaglycosylaseinhibitor,ugi)等,pe系统则含有cas9蛋白和逆转录酶,长度均在5.5kb以上,再加上grna序列及其启动子区远远超出了aav病毒的容量。因此,本领域迫切需要开发及优化aav递送碱基编辑器的系统,从而实现高效的基因编辑。
技术实现要素:
5.本发明要解决的技术问题是如何提高腺相关病毒载体的包装效率、实现碱基编辑器递送并实现较高的基因编辑效率。
6.为解决上述技术问题,第一个方面,本发明提供用于构建重组腺相关病毒载体和/或用于碱基编辑的基因组合物,其特征在于:所述组合物为cbe-c、abe-c或pe-c,所述cbe-c为用于构建胞嘧啶碱基编辑器(cytidinebaseeditor,cbe)的组合物、所述abe-c为用于构建腺嘌呤碱基编辑器(adeninebaseeditor,abe)的组合物,所述pe-c为用于构建引导编辑器(primeeditor,pe)的组合物,
7.所述cbe-c包括cbe-c1、cbe-c2、cbe-c3、cbe-c4、cbe-c5或cbe-c6,
8.所述cbe-c1由cbe-c1-511编码基因和cbe-c512-1368编码基因组成,所述cbe-c1-511编码基因编码名称为cbe-c1-511的融合蛋白质,所述cbe-c1-511由名称为cas9n-1-511的cas9切口酶(cas9nickase,cas9n)的n端片段、胞嘧啶脱氨酶和内含肽的n端片段融合而成,所述cbe-c512-1368编码基因编码名称为cbe-c512-1368的融合蛋白质,所述cbe-c512-1368由内含肽的c端片段、名称为cas9n-512-1368的cas9切口酶(cas9nickase,cas9n)的c端片段和尿嘧啶糖基化酶抑制剂(ugi)融合而成,所述cas9n-1-511是由编码序列是seqidno.1第802-2331位核苷酸所示的编码基因编码的蛋白质,所述cas9n-512-1368是由编码序列是seqidno.1第2332-4902位核苷酸所示的编码基因编码的蛋白质,
9.所述cbe-c2由cbe-c1-507编码基因和cbe-c508-1368编码基因组成,所述cbe-c1-507编码基因编码名称为cbe-c1-507的融合蛋白质,所述cbe-c1-507由名称为cas9n-1-507的cas9切口酶的n端片段融合、所述胞嘧啶脱氨酶和所述内含肽的n端片段融合而成,所述cbe-c508-1368编码基因编码名称为cbe-c508-1368的融合蛋白质,所述cbe-c508-1368由所述内含肽的c端片段、名称为cas9n-508-1368的cas9切口酶的c端片段和所述尿嘧啶糖基化酶抑制剂(ugi)融合而成,所述cas9n-1-507是由编码序列是seqidno.1第802-2319位核苷酸所示的编码基因编码的蛋白质,所述cas9n-508-1368是由编码序列是seqidno.1第2320-4902位核苷酸所示的编码基因编码的蛋白质,
10.所述cbe-c3由cbe-c1-503编码基因和cbe-c504-1368编码基因组成,所述cbe-c1-503编码基因编码名称为cbe-c1-503的融合蛋白质,所述cbe-c1-503由名称为cas9n-1-503的cas9切口酶的n端片段、所述胞嘧啶脱氨酶和所述内含肽的n端片段融合而成,所述cbe-c504-1368编码基因编码名称为cbe-c504-1368的融合蛋白质,所述cbe-c504-1368由所述内含肽的c端片段、名称为cas9n-504-1368的cas9切口酶的c端片段和所述尿嘧啶糖基化酶抑制剂(ugi)融合而成,所述cas9n-1-503是由编码序列是seqidno.1第802-2307位
1368由所述内含肽的c端片段、名称为cas9n-1023-1368的cas9切口酶(cas9 nickase,cas9n)的c 端片段和逆转录酶融合而成,所述cas9n-1-1022是由编码序列是序列表中序列4第22-3084 位核苷酸所示的编码基因编码的蛋白质,所述cas9n-1023-1368是由编码序列是序列表中序列4第3085-4122位核苷酸所示的编码基因编码的蛋白质,
17.所述pe-c2由pe-c1-1026编码基因和pe-c1027-1368编码基因组成,所述pe-c1-1026 编码基因编码名称为pe-c1-1026的融合蛋白质,所述pe-c1-1026由名称为cas9n-1-1026的cas9切口酶(cas9 nickase,cas9n)的n端片段和所述内含肽的n端片段融合而成,所述 pe-c1027-1368编码基因编码名称为pe-c1027-1368的融合蛋白质,所述pe-c1027-1368由所述内含肽的c端片段、名称为cas9n-1027-1368的cas9切口酶(cas9 nickase,cas9n)的c 端片段和所述逆转录酶(rt)融合而成,所述cas9n-1-1026是由编码序列是序列表中序列1第 22-3096位核苷酸所示的编码基因编码的蛋白质,所述cas9n-1027-1368是由编码序列是序列表中序列1第3097-4122位核苷酸所示的编码基因编码的蛋白质,
18.所述pe-c3由pe-c1-1068编码基因和pe-c1069-1368编码基因组成,所述pe-c1-1068 编码基因编码名称为pe-c1-1068的融合蛋白质,所述pe-c1-1068由名称为cas9n-1-1068的 cas9切口酶(cas9 nickase,cas9n)的n端片段和所述内含肽的n端片段融合而成,所述 pe-c1069-1368编码基因编码名称为pe-c1069-1368的融合蛋白质,所述pe-c1069-1368由所述内含肽的c端片段、名称为cas9n-1069-1368的cas9切口酶(cas9 nickase,cas9n)的c 端片段和所述逆转录酶融合而成,所述cas9n-1-1068是由编码序列是序列表中序列1第 22-3222位核苷酸所示的编码基因编码的蛋白质,所述cas9n-1069-1368是由编码序列是序列表中序列1第3223-4122位核苷酸所示的编码基因编码的蛋白质。
19.本发明中,所述胞嘧啶碱基编辑器(cytidine base editor,cbe)、所述腺嘌呤碱基编辑器 (adenine base editor,abe)和引导编辑器(prime editor,pe)可为dna分子,如载体。
20.进一步地,上述的基因组合物中,所述胞嘧啶脱氨酶为a1)或a2)
21.a1)由seq id no.1第22-705位核苷酸所示的编码基因编码的蛋白质;
22.a2)由seq id no.2第85-678位核苷酸所示的编码基因编码的蛋白质;
23.所述腺嘌呤脱氨酶为由seq id no.3第22-1113位核苷酸所示的编码基因编码的蛋白质;
24.所述逆转录酶(rt)为由seq id no.4第4222-6318位核苷酸所示的编码基因编码的蛋白质;
25.所述尿嘧啶糖基化酶抑制剂(ugi)为由seq id no.1第5212-5460位核苷酸所示的编码基因编码的蛋白质。
26.所述内含肽的n端片段的氨基酸序列是seq id no.5,所述内含肽的c端片段的氨基酸序列是seq id no.6。
27.其中,a1)所述的胞嘧啶脱氨酶可用于be4max cbe碱基编辑器,a2)所述的胞嘧啶脱氨酶可用于ha3a-be3碱基编辑器。
28.所述cbe-c1-511编码基因由所述cas9n-1-511的编码基因、所述胞嘧啶脱氨酶的编码基因和所述内含肽的n端片段的编码基因融合而成,所述cbe-c512-1368编码基因由所述内含肽的c端片段的编码基因、所述cas9n-512-1368的编码基因和所述尿嘧啶糖基化抑
制酶的编码基因融合而成。
29.所述cbe-c1-507编码基因由所述cas9n-1-507的编码基因、所述胞嘧啶脱氨酶的编码基因和所述内含肽的n端片段的编码基因融合而成,所述cbe-c508-1368编码基因由所述内含肽的c端片段的编码基因、所述cas9n-508-1368的编码基因和所述尿嘧啶糖基化抑制酶的编码基因融合而成。
30.所述cbe-c1-503编码基因由所述cas9n-1-503的编码基因和所述胞嘧啶脱氨酶的编码基因和所述内含肽的n端片段的编码基因融合而成,所述cbe-c504-1368编码基因由所述内含肽的c端片段的编码基因、所述cas9n-504-1368的编码基因和所述尿嘧啶糖基化抑制酶的编码基因融合而成。
31.所述cbe-c1-502编码基因由所述cas9n-1-502的编码基因、所述胞嘧啶脱氨酶的编码基因和所述内含肽的n端片段的编码基因融合而成,所述cbe-c503-1368编码基因由所述内含肽的c端片段的编码基因、所述cas9n-503-1368的编码基因和所述尿嘧啶糖基化抑制酶的编码基因融合而成。
32.所述cbe-c1-501编码基因由所述cas9n-1-501的编码基因、所述胞嘧啶脱氨酶的编码基因和所述内含肽的n端片段的编码基因融合而成,所述cbe-c502-1368编码基因由所述内含肽的c端片段的编码基因、所述cas9n-502-1368的编码基因和所述尿嘧啶糖基化抑制酶的编码基因融合而成,
33.所述cbe-c1-498编码基因由所述cas9n-1-498的编码基因、所述胞嘧啶脱氨酶的编码基因和所述内含肽的n端片段的编码基因融合而成,所述cbe-c499-1368编码基因由所述内含肽的c端片段的编码基因、所述cas9n-499-1368的编码基因和所述尿嘧啶糖基化抑制酶的编码基因融合而成。
34.所述abe-c1-511编码基因由所述cas9n-1-511的编码基因、所述腺嘌呤脱氨酶的编码基因和所述内含肽的n端片段的编码基因融合而成,所述abe-c512-1368编码基因由所述内含肽的c端片段的编码基因和所述cas9n-512-1368的编码基因融合而成。
35.所述pe-c1-1022编码基因由所述cas9n-1-1022的编码基因和所述内含肽的n端片段的编码基因融合而成,所述pe-c1023-1368编码基因由所述内含肽的c端片段的编码基因、所述cas9n-1023-1368的编码基因和所述逆转录酶(rt)的编码基因融合而成。
36.所述pe-c1-1026编码基因由所述cas9n-1-1026的编码基因和所述内含肽的n端片段的编码基因融合而成,所述pe-c1027-1368编码基因由所述内含肽的c端片段的编码基因、所述cas9n-1027-1368的编码基因和所述逆转录酶(rt)的编码基因融合而成。
37.所述pe-c1-1068编码基因由所述cas9n-1-1068的编码基因和所述内含肽的n端片段的编码基因融合而成,所述pe-c1069-1368编码基因由所述内含肽的c端片段的编码基因、所述cas9n-1069-1368的编码基因和所述逆转录酶(rt)的编码基因融合而成。
38.本发明中,所述内含肽的n端片段的编码基因是核苷酸序列是seq id no.9的dna分子,所述内含肽的c端片段的编码基因是核苷酸序列是seq id no.10的dna分子。
39.所述胞嘧啶脱氨酶的编码基因是核苷酸序列是seq id no.1第22-705位的dna分子,或所述胞嘧啶脱氨酶的编码基因是核苷酸序列是seq id no.2第85-678位的dna分子。所述尿嘧啶糖基化抑制酶的编码基因是核苷酸序列是seq id no.1第4933-5181位的dna分子 (与seq id no.1第5212-5460位相同)。所述腺嘌呤脱氨酶的编码基因是核苷酸序列是
seqid no.3第22-519位和/或616-1113位的dna分子。所述逆转录酶(rt)的编码基因是核苷酸序列是seq id no.4第4222-6318位的dna分子。
40.所述cas9n-1-511的编码基因是核苷酸序列是seq id no.1第802-2331位的dna分子,所述cas9n-512-1368的编码基因是核苷酸序列是seq id no.1第2332-4902位的dna分子。
41.所述cas9n-1-507的编码基因是核苷酸序列是seq id no.1第802-2319位的dna分子,所述cas9n-508-1368的编码基因是核苷酸序列是seq id no.1第2320-4902位的dna分子。
42.所述cas9n-1-503的编码基因是核苷酸序列是seq id no.1第802-2307位的dna分子,所述cas9n-504-1368的编码基因是核苷酸序列是seq id no.1第2308-4902位的dna分子。
43.所述cas9n-1-502的编码基因是核苷酸序列是seq id no.1第802-2304位的dna分子,所述cas9n-503-1368的编码基因是核苷酸序列是seq id no.1第2305-4902位的dna分子。
44.所述cas9n-1-501的编码基因是核苷酸序列是seq id no.1第802-2301位的dna分子,所述cas9n-502-1368的编码基因是核苷酸序列是seq id no.1第2302-4902位的dna分子。
45.所述cas9n-1-498的编码基因的是核苷酸序列是seq id no.1第802-2292位的dna分子,所述cas9n-499-1368的编码基因是核苷酸序列是seq id no.1第2293-4902位的dna分子。
46.所述cas9n-1-511的编码基因是核苷酸序列是seq id no.3第1210-2739位的dna分子,所述cas9n-512-1368的编码基因是核苷酸序列是seq id no.3第2740-5310位的dna分子。
47.所述cas9n-1-1022的编码基因是核苷酸序列是seq id no.4第22-3084位的dna分子;所述cas9n-1023-1368的编码基因是核苷酸序列是seq id no.4第3085-4122位的dna分子,。
48.所述cas9n-1-1026的编码基因是核苷酸序列是seq id no.4第22-3096位的dna分子;所述cas9n-1027-1368的编码基因是核苷酸序列是seq id no.4第3097-4122位的dna分子。
49.所述cas9n-1-1068的编码基因是核苷酸序列是seq id no.4第22-3222位的dna分子;所述cas9n-1069-1368的编码基因是核苷酸序列是seq id no.4第3223-4122位的dna分子。
50.为解决上述技术问题,第二个方面,本发明提供与上述的基因组合物相关的表达盒组合物,所述表达盒组合物为下述任一种:
51.b1)含有上述的cbe-c1-511编码基因的表达盒和含有上述的cbe-c512-1368编码基因的表达盒;
52.b2)含有上述的cbe-c1-507编码基因的表达盒和含有上述的cbe-c508-1368编码基因的表达盒;
53.b3)含有上述的cbe-c1-503编码基因的表达盒和含有上述的cbe-c504-1368编码
基因的表达盒;
54.b4)含有上述的cbe-c1-502编码基因的表达盒和含有上述的cbe-c503-1368编码基因的表达盒;
55.b5)含有上述的cbe-c1-501编码基因的表达盒和含有上述的cbe-c502-1368编码基因的表达盒;
56.b6)含有上述的cbe-c1-498编码基因的表达盒和含有上述的cbe-c499-1368编码基因的表达盒;
57.b7)含有上述的abe-c1-511编码基因的表达盒和含有上述的abe-c512-1368编码基因的表达盒;
58.b8)含有上述的pe-c1-1022编码基因的表达盒和含有上述的pe-c1023-1368编码基因的表达盒;
59.b9)含有上述的pe-c1-1026编码基因的表达盒和含有上述的pe-c1027-1368编码基因的表达盒;
60.b10)含有上述的pe-c1-1068编码基因的表达盒和含有上述的pe-c1069-1368编码基因的表达盒。
61.为解决上述技术问题,第三个方面,本发明提供与上述的组合物相关的载体组合物,所述载体组合物为下述任一种:
62.v1)含有上述的cbe-c1-511编码基因的载体和含有上述的cbe-c512-1368编码基因的载体;
63.v2)含有上述的cbe-c1-507编码基因的载体和含有上述的cbe-c508-1368编码基因的载体;
64.v3)含有上述的cbe-c1-503编码基因的载体和含有上述的cbe-c504-1368编码基因的载体;
65.v4)含有上述的cbe-c1-502编码基因的载体和含有上述的cbe-c503-1368编码基因的载体;
66.v5)含有上述的cbe-c1-501编码基因的载体和含有上述的cbe-c502-1368编码基因的载体;
67.v6)含有上述的cbe-c1-498编码基因的载体和含有上述的cbe-c499-1368编码基因的载体;
68.v7)含有上述的abe-c1-511编码基因的载体和含有上述的abe-c512-1368编码基因的载体;
69.v8)含有上述的pe-c1-1022编码基因的载体和含有上述的pe-c1023-1368编码基因的载体;
70.v9)含有上述的pe-c1-1026编码基因的载体和含有上述的pe-c1027-1368编码基因的载体;
71.v10)含有上述的pe-c1-1068编码基因的载体和含有上述的pe-c1069-1368编码基因的载体。
72.进一步地,上述载体组合物中,v1)中所述的cbe-c1-511编码基因的载体、v2)中所述的cbe-c1-507编码基因的载体、v3)中所述的cbe-c1-503编码基因的载体、v4)中所述的
cbe-c1-502编码基因的载体、v5)中所述的cbe-c1-501编码基因的载体和v6)所述的cbe-c1-498编码基因的载体还含有sgrna基因;
73.v7)中所述abe-c512-1368编码基因的载体还含有sgrna基因;
74.v8)中所述的pe-c1023-1368编码基因的载体、v9)中所述的pe-c1027-1368编码基因的载体或v10)中所述的pe-c1069-1368编码基因的载体还含有pegrna基因。
75.本发明中,所述载体可为重组腺相关病毒载体。
76.为解决上述技术问题,第四个方面,本发明提供含有上述的基因组合物或含有上述的表达盒组合物或含有上述的载体组合物的重组微生物。
77.进一步地,上述的重组微生物中,所述重组微生物选自大肠杆菌或腺相关病毒。
78.为解决上述技术问题,第五个方面,本发明提供含有上述的基因组合物或含有上述的表达盒组合物或含有上述的载体组合物的重组细胞。
79.进一步地,上述的重组细胞中,所述细胞可为哺乳动物细胞。
80.本发明中,所述哺乳动物细胞可为非人哺乳动物细胞。
81.为解决上述技术问题,第六个方面,本发明提供上述的基因组合物或上述的表达盒组合物或上述的载体组合物在构建重组腺相关病毒载体和/或碱基编辑中的应用。
82.含有上述组合物的重组腺相关病毒(腺相关病毒颗粒)也是本发明的保护范围。
83.本发明针对不同的碱基编辑系统对cas9蛋白进行了不同位点的拆分,其中cbe系统将 cas9蛋白在511,507,503,502,501,498等6个位点进行拆分,分别在n端的末尾融合表达内含肽的n端,在c端的开头融合表达内含肽的c端,将u6及其grna序列反向放置在cas9n载体的c端位置。abe系统则在cas9蛋白的511位点进行拆分后具有良好的活性,同时将u6及其grna序列反向放置在cas9c载体的c端位置。由于pe系统与abe和cbe 的元件不太一样,因此拆分位点也有所不同。pe系统在cas9蛋白的1022,1026,1068位氨基酸进行拆分,然后分别在n端的末尾融合表达内含肽的n端,在c端的开头融合表达内含肽的c端。将u6及其pegrna放置在cas9c载体的c端,确保拆分后itr内部的序列在4.7kb 左右。在aav载体中,为了减少itr内部序列,我们对pe系统的启动子进行精简,选取较小的启动子ef-1α。
84.通过拆分的方法将上述碱基编辑器/引导编辑系统装载至aav病毒载体中,成功实现在靶细胞中碱基编辑器的递送,经过实验验证实现了对特定位点的编辑并获得较高的编辑效率。
附图说明
85.图1为拆分位点为cas9(d10a)511的拆分型be4max碱基编辑器的编辑效率。
86.图2为拆分位点为cas9(d10a)507的拆分型be4max碱基编辑器的编辑效率。
87.图3为拆分位点为cas9(d10a)503的拆分型be4max碱基编辑器的编辑效率。
88.图4为拆分位点为cas9(d10a)502的拆分型be4max碱基编辑器的编辑效率。
89.图5为拆分位点为cas9(d10a)501的拆分型be4max碱基编辑器的编辑效率。
90.图6为拆分位点为cas9(d10a)498的拆分型be4max碱基编辑器的编辑效率。
91.图7为对照组非拆分型be4max碱基编辑器的编辑效率。
92.图8为拆分位点为cas9(d10a)511的拆分型ha3a-be3碱基编辑器的编辑效率。
93.图9为拆分位点为cas9(d10a)507的拆分型ha3a-be3碱基编辑器的编辑效率。
94.图10为拆分位点为cas9(d10a)503的拆分型ha3a-be3碱基编辑器的编辑效率。
95.图11为拆分位点为cas9(d10a)502的拆分型ha3a-be3碱基编辑器的编辑效率。
96.图12为拆分位点为cas9(d10a)501的拆分型ha3a-be3碱基编辑器的编辑效率。
97.图13为拆分位点为cas9(d10a)498的拆分型ha3a-be3碱基编辑器的编辑效率。
98.图14为对照组非拆分ha3a-be3碱基编辑器的编辑效率。
99.图15为拆分位点为cas9(d10a)511的拆分型abe碱基编辑器的编辑效率。
100.图16为对照组非拆分型abe碱基编辑器的编辑效率。
101.图17为拆分位点为cas9(h840a)1022的拆分型pe碱基编辑器的编辑效率。
102.图18为拆分位点为cas9(h840a)1026的拆分型pe碱基编辑器的编辑效率。
103.图19为拆分位点为cas9(h840a)1068的拆分型pe碱基编辑器的编辑效率。
104.图20为对照组未拆分pe碱基编辑器的编辑效率。
105.图21为重组aav-n病毒载体aav-n-be4maxcas9c1-502的图谱。
106.图22为重组aav-c病毒载体aav-c-be4maxcas9c503-1368的图谱。
107.图23为重组aav-n病毒载体aav-n-ha3abe3cas9c1-502的图谱。
108.图24为重组aav-n病毒载体aav-n-spryabecas9c1-511的图谱。
109.图25为重组aav-c病毒载体aav-c-spryabecas9c512-1368的图谱。
110.图26为重组aav-n病毒载体aav-n-pe-cas9c1-1026-ef-1α的图谱。
111.图27为重组aav-c病毒载体aav-c-pe-cas9c1027-1368-pegrna-ef-1α的图谱。
具体实施方式
112.下面结合具体实施方式对本发明进行进一步的详细描述,给出的实施例仅为了阐明本发明,而不是为了限制本发明的范围。以下提供的实施例可作为本技术领域普通技术人员进行进一步改进的指南,并不以任何方式构成对本发明的限制。
113.下述实施例中的实验方法,如无特殊说明,均为常规方法,按照本领域内的文献所描述的技术或条件或者按照产品说明书进行。下述实施例中所用的材料、试剂等,如无特殊说明,均可从商业途径得到。以下实施例中的定量试验,均设置三次重复实验,结果取平均值。
114.本发明中的pcmv_be4max_p2a_gfp在addgene公司购买,货号为#112099。
115.本发明中的pcmv_ha3a-be3在addgene公司购买,货号为#113410。
116.本发明中的pcmv-t7-abemax(7.10)-spry-p2a-egfp(rtw5025)在addgene公司购买,货号为#140003。
117.本发明中的pcmv-pe2在addgene公司购买,货号为#132775。
118.hek293t细胞(实施例中用293t表示)为本实验室保存,在文献dongdong zhao,ju li, siwei li,xiuqing xin,muzi hu,marcus a price,susan j rosser,changhao bi,xueli zhang newbase editors change c to a in bacteria and c to g in mammalian cells.nature biotechnol 2020-07 中公开,公众可从申请人获得上述生物材料,所得上述生物材料只为重复本发明的实验所用,不可作为其它用途使用。
119.本发明中aav-n病毒载体和aav-c病毒载体由武汉淼灵生物科技有限公司购买,货号分别是p18828和p18882。
120.实施例1、cbe碱基编辑器拆分后aav载体的转染
121.1.1、be4max碱基编辑器拆分后aav载体的转染
122.为了验证新的拆分位点对cbe碱基编辑器活性的影响,本发明选取了 pcmv_be4max_p2a_gfp碱基编辑器(本发明中简称为be4max碱基编辑器)进行了拆分。其中,be4max碱基编辑器的全长质粒含有核苷酸序列如seq id no.1所示的dna分子,seqid no.1的第22-705位为胞嘧啶脱氨酶apobec-1的编码基因,第802-4902位为cas9(d10a) 的编码基因,第4933-5181位和第5212-5460位为尿嘧啶糖基化酶抑制剂(ugi)的编码基因。
123.分别在be4max的cas9蛋白的511,507,503,502,501,498共6个位点进行拆分,然后对编辑活性进行分析。在哺乳动物细胞中,将不同拆分位点的cas9蛋白n端载体和c 端载体共同转染,在znf410的特定grna靶标位点进行相关编辑活性分析,结果显示拆分后cas9蛋白共同转染后能够具有全长cas9蛋白的功能,可以对znf410 grna靶标位点进行高效编辑。
124.实验过程:将hek293t细胞按5
×
105个/孔铺24孔板,等每个孔细胞长至40%-60%时,按照上述cas9拆分位点将表达cas9n端载体的质粒和表达cas9c端载体的质粒共同转染,获得重组hek293t细胞。以be4max碱基编辑器的全长质粒为模板,按照上述切割位点设计引物进行pcr扩增获得含有目的片段的pcr产物,将上述pcr产物分别通过同源重组的方式连接到腺相关病毒载体中。具体如下:含有cas9(n)编码基因和胞嘧啶脱氨酶编码基因的上述pcr产物分别通过同源重组的方式连接到aav-n病毒载体上,得到重组aav-n病毒载体aav-n-be4maxcas9c1-511、aav-n-be4maxcas9c1-507、aav-n-be4maxcas9c1-503、 aav-n-be4maxcas9c1-502、aav-n-be4maxcas9c1-501、aav-n-be4maxcas9c1-498;含有 cas9(c)编码基因的上述pcr产物分别通过同源重组的方式连接到aav-c病毒载体上,得到重组aav-c病毒载体aav-c-be4maxcas9c512-1368、aav-c-be4maxcas9c508-1368、 aav-c-be4maxcas9c504-1368、aav-c-be4maxcas9c503-1368、aav-c-be4maxcas9c502-1368、 aav-c-be4maxcas9c499-1368。
125.靶向目标序列的grna的spacer n20通过goleden gate的方式构建至上述重组aav-n病毒载体,所用的限制性内切酶识别位点为bsmbi,由neb公司购买。其中grna的靶序列为: 5'-tagcctccgaaaacatctgg-3'(命名为znf410 grna),位于znf410基因组,znf410 基因组genbank编号为kj903016.1,共计1425bp。
126.将获得的重组aav病毒载体送测序,测序结果表明:重组aav-n病毒载体 aav-n-be4maxcas9c1-511是用seq id no.1第1-2331位核苷酸所示的dna分子替换 aav-n中的3915-6431之间的片段,znf410 grna序列替换aav-n中的7375-7395位核苷酸之间的小片段,保持aav-n的其它核苷酸不变,得到的表达sgrna、胞嘧啶脱氨酶 apobec-1、名称为cas9n-1-511的cas9切口酶的n端片段和内含肽的n端片段的重组表达载体。重组aav-c病毒载体aav-c-be4maxcas9c512-1368是用seq id no.1第2332-5523 位核苷酸所示的dna分子替换aav-c中的4041-6767位核苷酸之间的片段,并将aav-c中第7253-7611位核苷酸进行删除,保持aav-c的其它核苷酸不变,得到的表达内含肽的c端片段、名称为cas9n-512-1368的cas9切口酶的c端片段和尿嘧啶糖基化酶抑制剂(ugi)的重组表达载体。
127.重组aav-n病毒载体aav-n-be4maxcas9c1-507是用seq id no.1第1-2319位核苷酸所示的dna分子替换aav-n中的3915-6431之间的片段,znf410 grna序列替换aav-n 中的7375-7395位核苷酸之间的小片段,保持aav-n的其它核苷酸不变,得到的表达sgrna、胞嘧
啶脱氨酶apobec-1、名称为cas9n-1-507的cas9切口酶的n端片段和内含肽的n端片段的重组表达载体。重组aav-c病毒载体aav-c-be4maxcas9c508-1368是用seq id no.1 第2320-5523位核苷酸所示的dna分子替换aav-c中的4041-6767位核苷酸之间的片段,并将aav-c中第7253-7611位核苷酸进行删除,保持aav-c的其它核苷酸不变,得到的表达内含肽的c端片段、名称为cas9n-508-1368的cas9切口酶的c端片段和尿嘧啶糖基化酶抑制剂(ugi)的重组表达载体。
128.重组aav-n病毒载体aav-n-be4maxcas9c1-503是用seq id no.1第1-2307位核苷酸所示的dna分子替换aav-n中的第3915-6431之间的片段,znf410 grna序列替换aav-n 中的7375-7395位核苷酸之间的小片段,保持aav-n的其它核苷酸不变,得到的表达sgrna、胞嘧啶脱氨酶apobec-1、名称为cas9n-1-503的cas9切口酶的n端片段和内含肽的n端片段的重组表达载体。重组aav-c病毒载体aav-c-be4maxcas9c504-1368是用seq id no.1 第2308-5523位核苷酸所示的dna分子替换aav-c中的4041-6767位核苷酸之间的片段,并将aav-c中第7253-7611位核苷酸进行删除,保持aav-c的其它核苷酸不变,得到的表达内含肽的c端片段、名称为cas9n-504-1368的cas9切口酶的c端片段和尿嘧啶糖基化酶抑制剂(ugi)的重组表达载体。
129.重组aav-n病毒载体aav-n-be4maxcas9c1-502是用seq id no.1第1-2304位核苷酸所示的dna分子替换aav-n中的3915位到6431之间的片段,znf410 grna序列替换 aav-n中的7375-7395位核苷酸之间的小片段,保持aav-n的其它核苷酸不变,得到的表达 sgrna、胞嘧啶脱氨酶apobec-1、名称为cas9n-1-502的cas9切口酶的n端片段和内含肽的n端片段的重组表达载体。重组aav-c病毒载体aav-c-be4maxcas9c503-1368是用seqid no.1第2305-5523位核苷酸所示的dna分子替换aav-c中的4041-6767位核苷酸之间的片段,并将aav-c中第7253-7611位核苷酸进行删除,保持aav-c的其它核苷酸不变,得到的表达内含肽的c端片段、名称为cas9n-503-1368的cas9切口酶的c端片段和尿嘧啶糖基化酶抑制剂(ugi)的重组表达载体。
130.重组aav-n病毒载体aav-n-be4maxcas9c1-501是用seq id no.1第1-2301位核苷酸所示的dna分子替换aav-n中的3915-6431位核苷酸之间的片段,znf410 grna序列替换 aav-n中的7375-7395位核苷酸之间的小片段,保持aav-n的其它核苷酸不变,得到的表达 sgrna、胞嘧啶脱氨酶apobec-1、名称为cas9n-1-501的cas9切口酶的n端片段和内含肽的n端片段的重组表达载体。重组aav-c病毒载体aav-c-be4maxcas9c502-1368是用seqid no.1第2302-5523位核苷酸所示的dna分子替换aav-c中的4041-6767位核苷酸之间的片段,并将aav-c中第7253-7611位核苷酸进行删除,保持aav-c的其它核苷酸不变,得到的表达内含肽的c端片段、名称为cas9n-502-1368的cas9切口酶的c端片段和尿嘧啶糖基化酶抑制剂(ugi)的重组表达载体。
131.重组aav-n病毒载体aav-n-be4maxcas9c1-498是用seq id no.1第1-2292位核苷酸所示的dna分子替换aav-n中的3915-6431位核苷酸之间的片段,znf410 grna序列替换 aav-n中的7375-7395位核苷酸之间的小片段,保持aav-n的其它核苷酸不变,得到的表达 sgrna、胞嘧啶脱氨酶apobec-1、名称为cas9n-1-498的cas9切口酶的n端片段和内含肽的n端片段的重组表达载体。重组aav-c病毒载体aav-c-be4maxcas9c499-1368是用seqid no.1第2293-5523位核苷酸所示的dna分子替换aav-c中的4041-6767位核苷酸之间的片段,
并将aav-c中第7253-7611位核苷酸进行删除,保持aav-c的其它核苷酸不变,得到的表达内含肽的c端片段、名称为cas9n-499-1368的cas9切口酶的c端片段和尿嘧啶糖基化酶抑制剂(ugi)的重组表达载体。
132.内含肽的n端片段是氨基酸序列如seq id no.5所示的多肽,内含肽的c端片段是氨基酸序列如seq id no.6所示的多肽。胞嘧啶脱氨酶apobec-1是seq id no.1第22-705位编码基因编码的蛋白质,尿嘧啶糖基化酶抑制剂(ugi)是seq id no.1第4933-5181位编码基因编码的蛋白质或seq id no.1第5212-5460位编码基因编码的蛋白质。
133.名称为cas9n-1-511的cas9切口酶的n端片段为核苷酸序列是seq id no.1第802-2331 位的编码基因编码的蛋白质,名称为cas9n-512-1368的cas9切口酶的c端片段为核苷酸序列是seq id no.1第2332-4902位的编码基因编码的蛋白质;名称为cas9n-1-507的cas9切口酶的n端片段为核苷酸序列是seq id no.1第802-2319位的编码基因编码的蛋白质,名称为cas9n-508-1368的cas9切口酶的c端片段为核苷酸序列是seq id no.1第2320-4902位的编码基因编码的蛋白质;名称为cas9n-1-503的cas9切口酶的n端片段为核苷酸序列是seqid no.1第802-2307位的编码基因编码的蛋白质,名称为cas9n-504-1368的cas9切口酶的c 端片段为核苷酸序列是seq id no.1第2308-4902位的编码基因编码的蛋白质;名称为 cas9n-1-502的cas9切口酶的n端片段为核苷酸序列是seq id no.1第802-2304位的编码基因编码的蛋白质,名称为cas9n-503-1368的cas9切口酶的c端片段为核苷酸序列是seq idno.1第2305-4902位的编码基因编码的蛋白质;名称为cas9n-1-501的cas9切口酶的n端片段为核苷酸序列是seq id no.1第802-2301位的编码基因编码的蛋白质,名称为 cas9n-502-1368的cas9切口酶的c端片段为核苷酸序列是seq id no.1第2302-4902位的编码基因编码的蛋白质;名称为cas9n-1-498的cas9切口酶的n端片段为核苷酸序列是seq idno.1第802-2292位的编码基因编码的蛋白质,名称为cas9n-499-1368的cas9切口酶的c端片段为核苷酸序列是seq id no.1第2293-4902位的编码基因编码的蛋白质。
134.示例性给出了重组aav-n病毒载体aav-n-be4maxcas9c1-502的图谱(图21)和重组 aav-c病毒载体aav-c-be4maxcas9c503-1368的图谱(图22)。将同一拆分位点分别表达含有cas9n端和c端的上述重组载体转染至hek293t细胞。
135.转染剂量分别为0.5μg,pei转染的量为3μl。每种质粒组合转染设3个重复,以转染全长的pe质粒和grna作为对照。72小时后使用快速提取dna提取液(epicentre,usa)提取获得重组hek293t细胞的基因组dna,对被编辑位点附近200bp~300bp区域利用taq dna 聚合酶(康为世纪,中国)pcr,将pcr产物进行高通量测序计算编辑效率(金唯智,中国)。其中,含有cas9n端和c端的上述重组载体分别为表1的组号为1-6的任一种重组载体组合。
136.表1.重组表达载体分组转染hek293t细胞
137.组号拆分位点重组载体组合1511aav-n-be4maxcas9c1-511和aav-c-be4maxcas9c512-13682507aav-n-be4maxcas9c1-507和aav-c-be4maxcas9c508-13683503aav-n-be4maxcas9c1-503和aav-c-be4maxcas9c504-13684502aav-n-be4max cas9c1-502和aav-c-be4maxcas9c503-13685501aav-n-be4maxcas9c1-501和aav-c-be4maxcas9c502-13686498aav-n-be4maxcas9c1-498和aav-c-be4maxcas9c499-1368
138.1.2、ha3a-be3系统拆分后aav载体的转染
139.参照1.1中的拆分位点和实施步骤,选取pcmv_ha3a-be3(本发明中简称ha3a-be3) cbe碱基编辑器进行了拆分验证,其中,ha3a-be3 cbe碱基编辑器的全长质粒含有核苷酸序列如seq id no.2所示的dna分子,seq id no.2第55-648位为胞嘧啶脱氨酶apobec3a 的编码基因,第745-4845位cas9(d10a)的编码基因,第4876-5124位和第5155-5403位为尿嘧啶糖基化酶抑制剂(ugi)的编码基因。
140.分别在ha3a-be3的cas9蛋白的511,507,503,502,501,498等6个位点进行拆分,然后对编辑活性进行分析。在哺乳动物细胞中,将不同拆分位点的cas9蛋白n端载体和c 端载体共同转染,在znf410的特定grna靶标位点进行相关编辑活性分析,结果显示拆分后的cas9蛋白共同转染后能够具有全长cas9蛋白的功能,可以对znf410 grna靶标位点进行高效编辑。
141.实验过程同1.1,其区别仅在于将pcr扩增模板替换为ha3a-be3碱基编辑器的全长质粒,并针对该碱基编辑器设计合适的引物进行pcr扩增,获得含有目标序列的pcr产物。
142.将含有目标序列的pcr产物分别通过同源重组的方式连接到aav病毒载体中。具体如下:含有cas9(n)编码基因和胞嘧啶脱氨酶编码基因的上述pcr产物分别通过同源重组的方式连接到aav-n病毒载体上,得到重组aav-n病毒载体aav-n-ha3abe3cas9c1-511、 aav-n-ha3abe3cas9c1-507、aav-n-ha3abe3cas9c1-503、aav-n-ha3abe3cas9c1-502、 aav-n-ha3abe3cas9c1-501、aav-n-ha3abe3cas9c1-498。与上述重组aav-n病毒载体对应的相同拆分位点的重组aav-c病毒载体与1.1序列相同,不再重复构建。
143.将上述重组载体送测序,测序结果表明:重组aav-n病毒载体 aav-n-ha3abe3cas9c1-511是用seq id no.2第1-2274位核苷酸所示的dna分子替换aav 中的3915-6431之间的片段,znf410 grna序列替换aav-n中的7375-7395位核苷酸之间的小片段,保持aav-n的其它核苷酸不变,得到的表达sgrna、胞嘧啶脱氨酶apobec3a、名称为cas9n-1-511的cas9切口酶的n端片段和内含肽的n端片段的重组表达载体。
144.重组aav-n病毒载体aav-n-ha3abe3cas9c1-507是用seq id no.2第1-2262位核苷酸所示的dna分子替换aav-n中的3915-6431之间的片段,znf410 grna序列替换aav-n 中的7375-7395位核苷酸之间的小片段,保持aav-n的其它核苷酸不变,得到的表达sgrna、胞嘧啶脱氨酶apobec3a、名称为cas9n-1-507的cas9切口酶的n端片段和内含肽的n端片段的重组表达载体。
145.重组aav-n病毒载体aav-n-ha3abe3cas9c1-503是用seq id no.2第1-2250位核苷酸所示的dna分子替换aav-n中的3915-6431之间的片段,znf410 grna序列替换aav-n 中的7375-7395位核苷酸之间的小片段,保持aav-n的其它核苷酸不变,得到的表达sgrna、胞嘧啶脱氨酶apobec3a、名称为cas9n-1-503的cas9切口酶的n端片段和内含肽的n端片段的重组表达载体。
146.重组aav-n病毒载体aav-n-ha3abe3cas9c1-502是用seq id no.2第1-2247位核苷酸所示的dna分子替换aav-n中的3915-6431之间的片段,znf410 grna序列替换aav-n 中的7375-7395位核苷酸之间的小片段,保持aav-n的其它核苷酸不变,得到的表达sgrna、胞嘧啶脱氨酶apobec3a、名称为cas9n-1-502的cas9切口酶的n端片段和内含肽的n端片段的重组表达载体。
147.重组aav-n病毒载体aav-n-ha3abe3cas9c1-501是用seq id no.2第1-2244位核苷酸所示的dna分子替换aav-n中的3915-6431之间的片段,znf410 grna序列替换aav-n 中的7375-7395位核苷酸之间的小片段,保持aav-n的其它核苷酸不变,得到的表达sgrna、胞嘧啶脱氨酶apobec3a、名称为cas9n-1-502的cas9切口酶的n端片段和内含肽的n端片段的重组表达载体。
148.重组aav-n病毒载体aav-n-ha3abe3cas9c1-498是用seq id no.2第1-2235位核苷酸所示的dna分子替换aav-n中的3915-6431之间的片段,znf410 grna序列替换aav-n 中的7375-7395位核苷酸之间的小片段,保持aav-n的其它核苷酸不变,得到的表达sgrna、胞嘧啶脱氨酶apobec3a、名称为cas9n-1-502的cas9切口酶的n端片段和内含肽的n端片段的重组表达载体。
149.内含肽的n端片段是氨基酸序列如seq id no.5所示的多肽,内含肽的c端片段是氨基酸序列如seq id no.6所示的多肽。胞嘧啶脱氨酶apobec3a是seq id no.2第55-648位编码基因编码的蛋白质。
150.名称为cas9n-1-511的cas9切口酶的n端片段为核苷酸序列是seq id no.2第745-2274 位的编码基因编码的蛋白质;名称为cas9n-1-507的cas9切口酶的n端片段为核苷酸序列是 seq id no.2第745-2262位的编码基因编码的蛋白质;名称为cas9n-1-503的cas9切口酶的 n端片段为核苷酸序列是seq id no.2第745-2250位的编码基因编码的蛋白质;名称为 cas9n-1-502的cas9切口酶的n端片段为核苷酸序列是seq id no.2第745-2247位的编码基因编码的蛋白质;名称为cas9n-1-501的cas9切口酶的n端片段为核苷酸序列是seq id no.2 第745-2244位的编码基因编码的蛋白质;名称为cas9n-1-498的cas9切口酶的n端片段为核苷酸序列是seq id no.2第745-2235位的编码基因编码的蛋白质。
151.示例性给出了重组aav-n病毒载体aav-n-ha3abe3cas9c1-502的图谱(图23)。
152.1.3、编辑效率
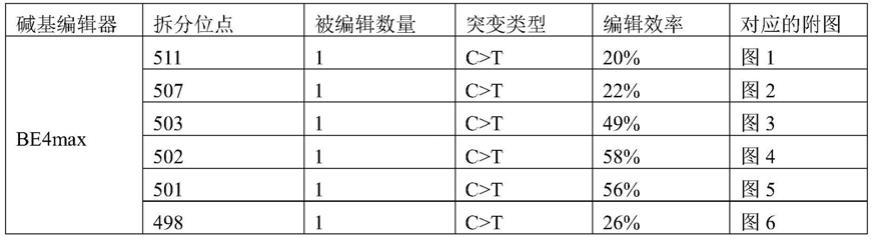
153.实验结果:选择znf410 grna位点作为结果分析的grna靶标位点,分析不同拆分位点的cbe对znf410的编辑效率,结果如表2所示。图1中特定编辑位点为左起第7位碱基 c,其突变为t的比例为20%;图2中特定编辑位点为左起第8位碱基c,其突变为t的比例为22%;图3中特定编辑位点为左起第7位碱基c,其突变为t的比例为49%;图4中特定编辑位点为左起第7位碱基c,其突变为t的比例为58%;图5中特定编辑位点为左起第 7位碱基c,其突变为t的比例为56%;图6中特定编辑位点为左起第7位碱基c,其突变为t的比例为26%;图7中特定编辑位点为左起第7位碱基c,其突变为t的比例为50%;图8中特定编辑位点为左起第8位碱基c,其突变为t的比例为29%;图9中特定编辑位点为左起第8位碱基c,其突变为t的比例为18%;图10中特定编辑位点为左起第8位碱基c,其突变为t的比例为62%;图11中特定编辑位点为左起第8位碱基c,其突变为t的比例为63%;图12中特定编辑位点为左起第8位碱基c,其突变为t的比例为63%;图13中特定编辑位点为左起第8位碱基c,其突变为t的比例为23%;图14中特定编辑位点为左起第 8位碱基c,其突变为t的比例为54%。
154.结果显示将cas9蛋白在511,507,503,502,501,498位点进行拆分后n端和c端共同转染仍然具有cas9蛋白的活性,可以对znf410位点进行有效的编辑,且以503,502和 501位点的编辑效率较高,编辑效率分别为49%,58%,56%。该结果表明拆分的cbe系统可以有效的进行基因特定位点的编辑。
spryabecas9c1-511是用seq id no.3第1-2739位核苷酸所示的dna分子替换 aav-n中的的3915-6431之间的片段,并将aav-n中第7286-7644位核苷酸进行删除,保持 aav-n的其它核苷酸不变,得到的表达腺嘌呤脱氨酶tada、名称为cas9n-1-511的cas9切口酶的n端片段和内含肽的n端片段的重组表达载体。重组载体 aav-c-spryabecas9c512-1368是用seq id no.3第2740-5373位核苷酸所示的dna分子替换aav-c中的4041-6767位核苷酸之间的片段,36h grna序列替换aav-c中的7342-7362 位核苷酸之间的片段,保持aav-c的其它核苷酸不变,得到的表达sgrna、内含肽的c端片段和名称为cas9n-512-1368的cas9切口酶的c端片段的重组表达载体。
164.内含肽的n端片段是氨基酸序列如seq id no.5所示的多肽,内含肽的c端片段是氨基酸序列如seq id no.6所示的多肽。腺嘌呤脱氨酶tada是seq id no.3第22-519位编码基因和seq id no.3第616-1113位编码基因编码的蛋白质。
165.名称为cas9n-1-511的cas9切口酶的n端片段为核苷酸序列是seq id no.3第1210-2739 位的编码基因编码的蛋白质;名称为cas9n-512-1368的cas9切口酶的n端片段为核苷酸序列是seq id no.3第2740-5310位的编码基因编码的蛋白质。
166.示例性给出了重组aav-n病毒载体aav-n-spryabecas9c1-511的图谱(图24)和重组aav-c病毒载体aav-c-spryabecas9c512-1368的图谱(图25)。
167.将上述重组表达载体转染hek293t,转染剂量分别为0.5μg,pei转染的量为3μl。每种质粒组合转染设3个重复,以转染全长的abe质粒和grna作为对照。72小时后使用快速提取dna提取液(epicentre,usa)提取重组hek293t细胞基因组dna,对被编辑位点附近200bp~300bp区域利用taq dna聚合酶(康为世纪,中国)pcr,将pcr产物进行高通量测序计算编辑效率(金唯智,中国)。
168.2.2、实验结果
169.选择36h grna位点作为结果分析的grna位点,分析该拆分位点的spry abemax对 36h grna的编辑效率。结果显示将cas9蛋白在511与512位氨基酸之间进行拆分后n端和 c端共同转染仍然具有cas9蛋白的活性,可以对36h位点进行有效的编辑,特定编辑位点为左起第五位碱基a,其突变为g的比例为42%,其编辑效率为42%(a>g,图15),非拆分对照组的编辑效率为54%(a>g,图16)。该结果表明拆分的spry abemax系统可以有效的进行基因特定位点的编辑。
170.实施例3、pe碱基编辑器拆分后aav载体的转染
171.3.1构建表达pegrna基因、cas9n基因和逆转录酶基因的表达载体
172.为了验证拆分位点对pe碱基编辑器活性的影响,本发明选取了pcmv-pe2碱基编辑器 (本发明中简称为pe)进行了拆分。pe碱基编辑器含有核苷酸序列如seq id no.4所示的 dna分子,seq id no.4第22-4122位为cas9(h840a)的编码基因,第4222-6318位为逆转录酶(rt)的编码基因。pe拆分位点分别是cas9蛋白的1015、1022、1026、1029、1040、1054 和1068共7个位点,在哺乳动物细胞中,将pe系统中不同拆分位点的cas9蛋白n端载体和c端载体共同转染,在vegfa位点进行相关编辑活性分析,结果显示拆分后cas9蛋白共同转染后能够具有全长cas9蛋白的功能,可以对vegfa位点进行高效编辑。
173.实验过程:将hek293t细胞按5
×
105个/孔铺24孔板,等每个孔细胞长至40%-60%时,按照上述cas9拆分位点将表达cas9n端载体的质粒和表达cas9c端载体的质粒共同转
染,获得重组hek293t细胞。其中,cas9n和cas9c质粒分别通过pcr的方法将目的片段扩增,以本实验室保存的pe编辑器的全长质粒为模板,按照上述拆分位点设计合适引物对作为扩增引物分别进行pcr扩增获得含有目的片段的pcr产物,
174.将上述pcr产物分别通过同源重组的方式连接到aav病毒载体中。具体如下:含有 cas9(n)编码基因的上述pcr产物分别通过同源重组的方式连接到aav-n病毒载体上,得到重组aav-n病毒载体aav-n-pecas9c1-1015、aav-n-pecas9c1-1022、aav-n-pecas9c1-1026、 aav-n-pecas9c1-1029、aav-n-pecas9c1-1040、aav-n-pecas9c1-1054、aav-n-pecas9c1-1068;含有cas9(c)编码基因的上述pcr产物通过同源重组的方式连接到aav-c病毒载体上,得到重组 aav-c病毒载体aav-c-pecas9c1016-1368、aav-c-pecas9c1023-1368、aav-c-pecas9c1027-1368、aav-c-pecas9c1030-1368、aav-c-pecas9c1041-1368、aav-c-pecas9c1055-1368、 aav-c-pecas9c1069-1368。
175.测序结果表明:重组aav-n病毒载体aav-n-pecas9c1-1015是用seq id no.4第22-3063 位核苷酸所示的dna分子替换aav-n中的3915-6431位核苷酸之间的片段,并将7299-7667 位核苷酸之间的片段删除,保持aav-n的其它核苷酸不变,得到的表达名称为cas9n-1-1015 的cas9切口酶的n端片段和内含肽的n端片段的重组表达载体。重组aav-c病毒载体 aav-c-pecas9c1016-1368是用seq id no.4第3064-6318位核苷酸所示的dna分子替换 aav-c中的第4041-6767位核苷酸之间的片段,保持aav-c的其它核苷酸不变,得到的表达内含肽的c端片段、名称为cas9n-1016-1368的cas9切口酶的c端片段和逆转录酶(rt) 的重组表达载体。
176.重组aav-n病毒载体aav-n-pecas9c1-1022是用seq id no.4第22-3084位核苷酸所示的dna分子替换aav-n中的3915-6431位核苷酸之间的片段,并将7299-7667位核苷酸之间的片段删除,保持aav-n的其它核苷酸不变,得到的表达名称为cas9n-1-1022的cas9 切口酶的n端片段和内含肽的n端片段的重组表达载体。重组aav-c病毒载体 aav-c-pecas9c1023-1368是用seq id no.4第3085-6318位核苷酸所示的dna分子替换 aav-c中的第4041-6767位核苷酸之间的片段,保持aav-c的其它核苷酸不变,得到的表达内含肽的c端片段、名称为cas9n-1023-1368的cas9切口酶的c端片段和逆转录酶(rt) 的重组表达载体。
177.重组aav-n病毒载体aav-n-pecas9c1-1026是用seq id no.4第22-3096位核苷酸所示的dna分子替换aav-n中的3915-6431位核苷酸之间的片段,并将7299-7667位核苷酸之间的片段删除,保持aav-n的其它核苷酸不变,得到的表达名称为cas9n-1-1026的cas9 切口酶的n端片段和内含肽的n端片段的重组表达载体。重组aav-c病毒载体 aav-c-pecas9c1027-1368是用seq id no.4第3097-6318位核苷酸所示的dna分子替换 aav-c中的第4041-6767位核苷酸之间的片段,保持aav-c的其它核苷酸不变,得到的表达内含肽的c端片段、名称为cas9n-1027-1368的cas9切口酶的c端片段和逆转录酶(rt) 的重组表达载体。
178.重组aav-n病毒载体aav-n-pecas9c1-1029是用seq id no.4第22-3105位核苷酸所示的dna分子替换aav-n中的3915-6431位核苷酸之间的片段,并将7299-7667位核苷酸之间的片段删除,保持aav-n的其它核苷酸不变,得到的表达名称为cas9n-1-1029的cas9 切口酶的n端片段和内含肽的n端片段的重组表达载体。重组aav-c病毒载体 aav-c-pecas9c1030-1368是用seq id no.4第3106-6318位核苷酸所示的dna分子替换 aav-c中的第4041-6767位核苷酸之间的小片段,保持aav-c的其它核苷酸不变,得到的表达内含肽的c
端片段、名称为cas9n-1030-1368的cas9切口酶的c端片段和逆转录酶(rt) 的重组表达载体。
179.重组aav-n病毒载体aav-n-pecas9c1-1040是用seq id no.4第22-3138位核苷酸所示的dna分子替换aav-n中的3915-6431位核苷酸之间的片段,并将7299-7667位核苷酸之间的片段删除,保持aav-n的其它核苷酸不变,得到的表达名称为cas9n-1-1040的cas9 切口酶的n端片段和内含肽的n端片段的重组表达载体。重组aav-c病毒载体 aav-c-pecas9c1041-1368是用seq id no.4第3139-6318位核苷酸所示的dna分子替换 aav-c中的第4041-6767位核苷酸之间的片段,保持aav-c的其它核苷酸不变,得到的表达内含肽的c端片段、名称为cas9n-1041-1368的cas9切口酶的c端片段和逆转录酶(rt) 的重组表达载体。
180.重组aav-n病毒载体aav-n-pecas9c1-1054是用seq id no.4第22-3180位核苷酸所示的dna分子替换aav-n中的3915-6431位核苷酸之间的片段,并将7299-7667位核苷酸之间的片段删除,保持aav-n的其它核苷酸不变,得到的表达名称为cas9n-1-1054的cas9 切口酶的n端片段和内含肽的n端片段的重组表达载体。重组aav-c病毒载体 aav-c-pecas9c1055-1368是用seq id no.4第3181-6318位核苷酸所示的dna分子替换 aav-c中的第4041-6767位核苷酸之间的片段,保持aav-c的其它核苷酸不变,得到的表达内含肽的c端片段、名称为cas9n-1055-1368的cas9切口酶的c端片段和逆转录酶(rt) 的重组表达载体。
181.重组aav-n病毒载体aav-n-pecas9c1-1068是用seq id no.4第22-3222位核苷酸所示的dna分子替换aav-n中的3915-6431位核苷酸之间的片段,并将7299-7667位核苷酸之间的片段删除,保持aav-n的其它核苷酸不变,得到的表达名称为cas9n-1-1068的cas9 切口酶的n端片段和内含肽的n端片段的重组表达载体。重组aav-c病毒载体 aav-c-pecas9c1069-1368是用seq id no.4第3223-6318位核苷酸所示的dna分子替换 aav-c中的第4041-6767位核苷酸之间的片段,保持aav-c的其它核苷酸不变,得到的内含肽的c端片段、名称为cas9n-1069-1368的cas9切口酶的c端片段和逆转录酶(rt)的重组表达载体。
182.由公司合成161bp的双链dna片段((pegrna基因),pegrna基因的一条链的序列为pegrna基因的一条链的序列为(s eq id no.7,波浪线示靶标序列(位于vegfa基因组,vegfa基因组genbank编号为 ac103801.2),单下划线示rt模板序列,双下划线示pbs(引物结合位点)序列,点式下划线示同源臂)。
183.a、以重组aav-c病毒载体aav-c-pecas9c1016-1368为模板,利用aav-c-f: ttcctgcccgaccttgcggc和aav-c-r:cggtgtttcgtcctttccacaagatata作为引物进行pcr扩增获得目的载体片段。将目的载体片段与上述161bp的双链dna片段进行同源重组,得到表达pegrna、内含肽的c端片段、名称为cas9n-1016-1368的cas9切口酶的c端片段和逆转录酶(rt) 的重组表达载体aav-c-pecas9c1016-1368-pegrna。
184.将a中的aav-c-pecas9c1016-1368替换为aav-c-pecas9c1023-1368,其它操作同a,得到表达pegrna、内含肽的c端片段、名称为cas9n-1023-1368的cas9切口酶的c端片段和逆转录酶(rt)的重组表达载体aav-c-pecas9c1023-1368-pegrna。
185.将a中的aav-c-pecas9c1016-1368替换为aav-c-pecas9c1027-1368,其它操作同a,得到表达pegrna内含肽的c端片段、名称为cas9n-1027-1368的cas9切口酶的c端片段和
逆转录酶(rt)的重组表达载体aav-c-pecas9c1027-1368-pegrna。
186.将a中的aav-c-pecas9c1016-1368替换为aav-c-pecas9c1030-1368,其它操作同a,得到表达pegrna、内含肽的c端片段、名称为cas9n-1030-1368的cas9切口酶的c端片段和逆转录酶(rt)的重组表达载体aav-c-pecas9c1030-1368-pegrna。
187.将a中的aav-c-pecas9c1016-1368替换为aav-c-pecas9c1041-1368,其它操作同a,得到表达pegrna、内含肽的c端片段、名称为cas9n-1041-1368的cas9切口酶的c端片段和逆转录酶(rt)的重组表达载体aav-c-pecas9c1041-1368-pegrna。
188.将a中的aav-c-pecas9c1016-1368替换为aav-c-pecas9c1055-1368,其它操作同a,得到表达pegrna、内含肽的c端片段、名称为cas9n-1055-1368的cas9切口酶的c端片段和逆转录酶(rt)的重组表达载体aav-c-pecas9c1055-1368-pegrna。
189.将a中的aav-c-pecas9c1016-1368替换为aav-c-pecas9c1069-1368,其它操作同a,得到表达pegrna、内含肽的c端片段、名称为cas9n-1069-1368的cas9切口酶的c端片段和逆转录酶(rt)的重组表达载体aav-c-pecas9c1069-1368-pegrna。
190.3.2替换3.1表达载体中的启动子
191.由于3.1表达载体中的原始启动子序列较长,因此在pe系统中替换成长度较小的启动子 ef-1α核心启动子。ef-1α核心启动子的序列为5'-ctagatcagggtaccgggcagagcgcacatcgccc acagtccccgagaagttggggggaggggtcggcaattgatccggtgcctagagaaggtggcgcggggtaaactgggaaagtgatgtcgtgt actggctccgcctttttcccgagggtgggggagaaccgtatataagtgcagtagtcgccgtgaacgttctttttcgcaacgggtttgccgccagaa cacagtggcaccggtccaac-3'(seq id no.8,下划线示15bp的同源臂)。
192.b、以重组表达载体aav-c-pecas9c1016-1368-pegrna为模板,利用aav-v-f: 5'-gttggaccggtgccaccatga-3';aav-v-r:5'-ggtaccctgatctagaggccgc-3'作为引物进行pcr扩增获得目的载体片段。将目的载体片段与核苷酸序列是seq id no.8的ef-1α核心启动子进行同源重组,得到表达pegrna、pe-cas9c1016-1368和逆转录酶的重组表达载体 aav-c-pecas9c1016-1368-pegrna-ef-1α。
193.将b中的aav-c-pecas9c1016-1368-pegrna替换为aav-c-pecas9c1023-1368-pegrna,其它操作同b,得到表达pegrna、pe-cas9c1023-1368和逆转录酶的重组表达载体 aav-c-pecas9c1023-1368-pegrna-ef-1α。
194.将b中的aav-c-pecas9c1016-1368-pegrna替换为aav-c-pecas9c1027-1368-pegrna,其它操作同b,得到表达pegrna、内含肽的c端片段、名称为cas9n-1027-1368的cas9切口酶的c端片段和逆转录酶(rt)的重组表达载体aav-c-pecas9c1027-1368-pegrna-ef-1α。
195.将b中的aav-c-pecas9c1016-1368-pegrna替换为aav-c-pecas9c1030-1368-pegrna,其它操作同b,得到表达pegrna、内含肽的c端片段、名称为cas9n-1030-1368的cas9切口酶的c端片段和逆转录酶(rt)的重组表达载体aav-c-pecas9c1030-1368-pegrna-ef-1α。
196.将b中的aav-c-pecas9c1016-1368-pegrna替换为aav-c-pecas9c1041-1368-pegrna,其它操作同b,得到表达pegrna、内含肽的c端片段、名称为cas9n-1041-1368的cas9切口酶的c端片段和逆转录酶(rt)的重组表达载体aav-c-pecas9c1041-1368-pegrna-ef-1
α。
197.将b中的aav-c-pecas9c1016-1368-pegrna替换为aav-c-pecas9c1055-1368-pegrna,其它操作同b,得到表达pegrna、内含肽的c端片段、名称为cas9n-1055-1368的cas9切口酶的c端片段和逆转录酶(rt)的重组表达载体aav-c-pecas9c1055-1368-pegrna-ef-1α。
198.将b中的aav-c-pecas9c1016-1368-pegrna替换为aav-c-pecas9c1069-1368-pegrna,其它操作同b,得到表达pegrna、内含肽的c端片段、名称为cas9n-1069-1368的cas9切口酶的c端片段和逆转录酶(rt)的重组表达载体aav-c-pecas9c1069-1368-pegrna-ef-1α。
199.将b中的aav-c-pecas9c1016-1368-pegrna替换为aav-n-pecas9c1-1015,其它操作同b,得到含有得到得到表达名称为cas9n-1-1015的cas9切口酶的n端片段和内含肽的n 端片段的重组表达载体aav-n-pecas9c1-1015-ef-1α。
200.将b中的aav-c-pecas9c1016-1368-pegrna替换为aav-n-pecas9c1-1022,其它操作同b,得到含有得到得到表达名称为cas9n-1-1022的cas9切口酶的n端片段和内含肽的n 端片段的重组表达载体aav-n-pecas9c1-1022-ef-1α。
201.将b中的aav-c-pecas9c1016-1368-pegrna替换为aav-n-pecas9c1-1026,其它操作同b,得到含有得到得到表达名称为cas9n-1-1026的cas9切口酶的n端片段和内含肽的n 端片段的重组表达载体aav-n-pecas9c1-1026-ef-1α。
202.将b中的aav-c-pecas9c1016-1368-pegrna替换为aav-n-pecas9c1-1029,其它操作同b,得到含有得到得到表达名称为cas9n-1-1029的cas9切口酶的n端片段和内含肽的n 端片段的重组表达载体aav-n-pecas9c1-1029-ef-1α。
203.将b中的aav-c-pecas9c1016-1368-pegrna替换为aav-n-pecas9c1-1040,其它操作同b,得到含有得到得到表达名称为cas9n-1-1040的cas9切口酶的n端片段和内含肽的n 端片段的重组表达载体aav-n-pecas9c1-1040-ef-1α。
204.将b中的aav-c-pecas9c1016-1368-pegrna替换为aav-n-pecas9c1-1054,其它操作同b,得到含有得到得到表达名称为cas9n-1-1054的cas9切口酶的n端片段和内含肽的n 端片段的重组表达载体aav-n-pe-cas9c1-1054-ef-1α。
205.将b中的aav-c-pecas9c1016-1368-pegrna替换为aav-n-pecas9c1-1068,其它操作同b,得到含有得到得到表达名称为cas9n-1-1068的cas9切口酶的n端片段和内含肽的n 端片段的重组表达载体aav-n-pecas9c1-1068-ef-1α。
206.内含肽的n端片段是氨基酸序列如seq id no.5所示的多肽,内含肽的c端片段是氨基酸序列如seq id no.6所示的多肽。逆转录酶(rt)是seq id no.4第4222-6318位编码基因编码的蛋白质。
207.名称为cas9n-1-1015的cas9切口酶的n端片段为核苷酸序列是seq id no.4第1210-3063位的编码基因编码的蛋白质;名称为cas9n-1016-1368的cas9切口酶的n端片段为核苷酸序列是seq id no.4第3063-4122位的编码基因编码的蛋白质;名称为cas9n-1-1022 的cas9切口酶的n端片段为核苷酸序列是seq id no.4第1210-3084位的编码基因编码的蛋白质;名称为cas9n-1023-1368的cas9切口酶的n端片段为核苷酸序列是seq id no.4第 3085-4122位的编码基因编码的蛋白质;名称为cas9n-1-1026的cas9切口酶的n端
片段为核苷酸序列是seq id no.4第1210-3096位的编码基因编码的蛋白质;名称为cas9n-1027-1368 的cas9切口酶的n端片段为核苷酸序列是seq id no.4第3097-4122位的编码基因编码的蛋白质;名称为cas9n-1-1029的cas9切口酶的n端片段为核苷酸序列是seq id no.4第 1210-3105位的编码基因编码的蛋白质;名称为cas9n-1030-1368的cas9切口酶的n端片段为核苷酸序列是seq id no.4第3106-4122位的编码基因编码的蛋白质;名称为cas9n-1-1040 的cas9切口酶的n端片段为核苷酸序列是seq id no.4第1210-3138位的编码基因编码的蛋白质;名称为cas9n-1041-1368的cas9切口酶的n端片段为核苷酸序列是seq id no.4第 3139-4122位的编码基因编码的蛋白质;名称为cas9n-1-1054的cas9切口酶的n端片段为核苷酸序列是seq id no.4第1210-3180位的编码基因编码的蛋白质;名称为cas9n-1055-1368 的cas9切口酶的n端片段为核苷酸序列是seq id no.4第3181-4122位的编码基因编码的蛋白质;名称为cas9n-1-1068的cas9切口酶的n端片段为核苷酸序列是seq id no.4第 1210-3222位的编码基因编码的蛋白质;名称为cas9n-1069-1368的cas9切口酶的n端片段为核苷酸序列是seq id no.4第3223-4122位的编码基因编码的蛋白质。
208.示例性给出了aav-n病毒载体aav-n-pe-cas9c1-1026-ef-1α的图谱(图26)和重组aav-c病毒载体aav-c-pe-cas9c1027-1368-pegrna-ef-1α的图谱(图27)
209.将同一拆分位点分别表达含有cas9n端和c端的上述重组载体转染至hek293t细胞。转染剂量分别为0.5μg,pei转染的量为3μl。每种质粒组合转染设3个重复,以转染全长的 pe质粒和grna作为对照。72小时后使用快速提取dna提取液(epicentre,usa)提取获得重组hek293t细胞的基因组dna,对被编辑位点附近200bp~300bp区域利用taq dna聚合酶(康为世纪,中国)pcr,将pcr产物进行高通量测序计算编辑效率(金唯智,中国)。其中,含有cas9n端和c端的上述重组载体分别为表3的组号为1-7的任一种重组载体组合。
210.表3.重组表达载体分组转染hek293t细胞
211.组号拆分位点重组载体组合11015aav-n-pe-cas9c1-1015-ef-1α和aav-c-pe-cas9c1016-1368-pegrna-ef-1α21022aav-n-pe-cas9c1-1022-ef-1α和aav-c-pe-cas9c1023-1368-pegrna-ef-1α31026aav-n-pe-cas9c1-1026-ef-1α和aav-c-pe-cas9c1027-1368-pegrna-ef-1α41029aav-n-pe-cas9c1-1029-ef-1α和aav-c-pe-cas9c1030-1368-pegrna-ef-1α51040aav-n-pe-cas9c1-1040-ef-1α和aav-c-pe-cas9c1041-1368-pegrna-ef-1α61054aav-n-pe-cas9c1-1054-ef-1α和aav-c-pe-cas9c1055-1368-pegrna-ef-1α71068aav-n-pe-cas9c1-1068-ef-1α和aav-c-pe-cas9c1069-1368-pegrna-ef-1α
212.实验结果:选择vegfa位点作为结果分析的grna位点,分析不同拆分位点的pe对 vegfa的编辑效率,实验结果如表4。图17中特定编辑位点为第一行左起第2-4位碱基cct,其突变为ggg的比例分别为6%、7%、10%;图18中特定编辑位点为第一行左起第2-4位碱基cct,其突变为ggg的比例分别为8%、10%、13%;图19中特定编辑位点为第一行左起第2-4位碱基cct,其突变为ggg的比例分别为5%、7%、11%;图20中特定编辑位点为第一行左起第2-4位碱基cct,其突变为ggg的比例分别为19%、18%、21%。
213.结果显示将cas9蛋白在1022,1026和1068位点进行拆分后n端和c端共同转染仍然具有cas9蛋白的活性,可以对vegfa位点进行有效的编辑。该结果表明拆分的pe系统可以有效的进行基因特定位点的编辑,而其它位点(1015、1029、1040和1054共4个位点)拆分的cas9编辑活性较低,认为该拆分位点不适合后续的应用。
214.表4.不同拆分位点的pe对vegfa的编辑效率
215.拆分位点被编辑数量突变类型编辑效率对应的附图10151cct》ggg7%无10221cct》ggg10%图1710261cct》ggg13%图1810291cct》ggg6%无10401cct》ggg6%无10541cct》ggg5%无10681cct》ggg11%图19未拆分对照1cct》ggg21%图20
216.以上对本发明进行了详述。对于本领域技术人员来说,在不脱离本发明的宗旨和范围,以及无需进行不必要的实验情况下,可在等同参数、浓度和条件下,在较宽范围内实施本发明。虽然本发明给出了特殊的实施例,应该理解为,可以对本发明作进一步的改进。总之,按本发明的原理,本技术欲包括任何变更、用途或对本发明的改进,包括脱离了本技术中已公开范围,而用本领域已知的常规技术进行的改变。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。
