放射治疗的多靶治疗计划和递送以及虚拟定位
1.相关申请的交叉引用
2.本技术要求2019年7月12日提交的美国临时专利申请第62/873,742号的优先权,其全部内容通过引用并入本文。
背景技术:
3.放射治疗涉及获取患者和一个或多个肿瘤区域的计划图像并设计向肿瘤区域提供规定剂量的放射的治疗计划。除了确定待照射的肿瘤区域外,放射治疗还试图限制对健康组织的照射。这可能包括识别放射敏感或放射回避区域(例如,危及器官或oar),并设计不会超出规定范围对这些放射回避区域进行照射的治疗计划。在大多数情况下,治疗计划假定一个或多个肿瘤区域、oar和健康组织区域在治疗时的绝对和/或相对位置匹配(或几乎匹配)它们在获取计划图像时的绝对和/或相对位置。一旦设计了满足肿瘤区域和oar剂量测定目标的治疗计划,患者就可以被放置在放疗系统的患者平台或床上,以便患者在床上感到相当舒适并且处于适合放射递送的位置。可以在床上(例如,扇形束ct扫描、锥形束ct扫描和/或pet扫描)获取患者的一个或多个定位图像。一个或多个肿瘤区域、oar和/或其他解剖结构中的每一个的位置可以使用定位图像来确定,并且它们相对于治疗放射源的绝对位置和/或它们彼此的相对位置可以与他们来自治疗计划图像中的位置相比。如果任何肿瘤区域和/或oar发生了移动,则放疗系统可以在治疗计划期间计算患者应该如何移动以匹配他们的位置,并且在可能的程度上,可以调整床以实施该移动。
4.然而,肿瘤区域和/或oar相对于放射治疗系统坐标的患者设置和定位可能是耗时的,特别是因为肿瘤区域和/或oar的大小、形状和/或/或计划图像的获取时间与治疗期之间的位置可能改变,并且在某些情况下,在治疗期期间可能继续改变。此外,患者设置和定位通常针对单个靶区域的治疗进行优化,并且可能不容易适应多个靶区域的治疗。例如,一个患者设置安排和定位可能适用于一个肿瘤区域,但可能不允许为另一个肿瘤区域递送规定剂量,和/或可能导致oar的不希望的照射。将患者准确登记到旨在同时治疗多个靶的计划中,涉及以某种方式将患者在递送时多个靶的新的实际位置映射到治疗计划中多个靶的原始位置。由于肿瘤一个可能相对于另一个移动,因此可能不会存在可以使所有肿瘤与计划对齐的患者的单个平移和取向移动。也就是说,将一个肿瘤与计划中的预期位置对齐的患者的调整、移动和旋转可能导致其他肿瘤失去对齐。
5.向多个患者靶区域递送放射的一种方法涉及执行一系列专利设置和定位。例如,对于第一患者靶区域,可以调整床以将患者定位到适合向第一靶区域递送放射的设置位置,可以获得定位图像以定位第一靶区域,然后将放射递送到该第一靶区域。然后对每个靶区域重复这些步骤,这可能是耗时的(尤其是如果患者设置涉及打开掩体门,以便临床医生或技术人员可以进入以调整床上的患者),并且因为每次迭代都是个体处理的,可能导致oar和/或健康组织的过量给药,和/或靶区域的给药不足(例如,努力不向oar过量给药时)。因此,需要改善的放射治疗计划、患者设置和配准以及定位方法,尤其是对于多个靶区域的照射。
技术实现要素:
6.本文公开了用于在单个治疗期或部分中照射多个患者靶区域的治疗计划、患者设置、定位和放射递送的方法。
7.用于照射多个靶区域的治疗计划方法可以包括为每个靶区域选择计划定位参考点,并基于所选择的计划定位参考点为每个靶区域计算平移不变发射滤波器。可以基于每个靶区域的平移不变发射滤波器和计划定位参考点来计算治疗计划注量图,该图指定递送至多个靶区域的放射注量以及至oar和健康组织的放射水平。
8.附加地或替代地,平移不变发射滤波器可以表示为基于每个靶区域的计划定位参考点递送到多个靶区域的放射注量的函数移位和定向算子。例如,函数移位算子可以包括用移位对二维或三维图进行插值的函数。例如,函数定向算子可以包括使用沿二维或三维空间中的轴的旋转来对二维或三维图进行插值的函数。例如,函数定向算子可用于基于治疗当天的定位参考点的位置来对用于递送的二维(或三维)注量图进行插值(例如,变换)。这可以包括计算注量图在(x,y)坐标中的平移,和/或在(x,y,z)中缩放注量图和/或沿中的轴旋转注量图。在一些变体中,治疗计划方法可以包括在包括低注量值区域的每个患者靶区域周围的治疗计划注量图中限定周界。多个靶区域的治疗计划方法可以包括计算包括每个靶区域的个体注量图的个体治疗计划,将个体注量图组合成累积治疗计划注量图,以及基于一个或多个约束(例如,剂量约束,如保持高注量区域彼此分开、满足oar注量限制、满足每个靶区域的剂量目标的剂量约束)迭代修改累积治疗计划注量图。在根据所需约束迭代修改累积治疗计划注量图之后,治疗计划方法可以包括在包括低注量值区域的每个患者靶区域周围的治疗计划注量图中限定周界,并且可以任选地包括将迭代修改的累积治疗计划注量图分离为沿限定周界的每个患者靶区域的个体注量图。在一些变体中,在治疗计划优化期间可以使用函数移位算子和定向算子中的一个或多个来计算基于每个靶区域的计划定位参考点的注量图。
9.任选地,在生物引导的放射治疗(bgrt)中,其中在治疗期期间获取正电子湮没发射路径数据并用于计算递送注量,治疗计划方法可以包括限定围绕第一患者靶区域的第一感兴趣区域(roi)或放射发射区和围绕第二患者靶区域的第二roi或放射发射区以用于第一和第二患者靶区域的预定位置移动范围。本文描述的治疗计划方法的输出可以包括治疗计划注量图,该注量图限定了要递送到每个患者靶区域的注量和oar和健康组织的放射暴露水平,以及一组与每个患者靶区域相关联的每个计划定位参考点的平移不变发射滤波器。替代地或附加地,在针对bgrt的治疗计划中,治疗计划方法可以输出与围绕每个患者靶区域限定的roi(例如,生物发射区(bfz))相关联的一组平移不变发射滤波器。附加地或替代地,一组平移不变发射滤波器可以包括函数移位算子和/或定向算子。任选地,治疗计划方法的输出可以包括一组放疗机器指令,以用于在患者设置和患者靶区域定位之后由放疗系统执行。
10.在一些变体中,用于虚拟靶区域定位和放射递送的方法可以包括获取处于治疗位置的患者的图像并且在所获取图像中识别患者靶区域,在所获取图像内选择定位参考点,其中定位参考点与计划定位参考点对应,根据定位参考点与计划定位参考点之间的移动计算空间偏移,根据空间偏移移动计划的感兴趣区域的界限,其中计划的感兴趣区域的界限围绕患者靶区域,获取已被移动的感兴趣区域空间过滤的成像数据,通过将一组发射滤波
器与所获取的成像数据卷积来计算在治疗放射源的每个发射位置处递送到患者靶区域的注量,和使用治疗放射源向患者靶区域发射计算注量。
11.在一些变体中,计划的感兴趣区域的界限可以包括空间滤波器。在一些变体中,移动计划的感兴趣区域的界限可以包括通过表示定位参考点相对于计划定位参考点的旋转平移的滚动校正因子对计划的感兴趣区域应用旋转和移动。计算递送注量可以包括将一组发射滤波器与滚动校正因子循环卷积。
12.在一些变体中,用于向多个患者靶区域的放射递送的治疗计划方法可以包括在患者计划图像中识别第一患者靶区域的第一位置和第二患者靶区域的第二位置,限定具有围绕第一患者靶区域的界限的第一感兴趣区域,限定具有围绕第二患者靶区域的界限的第二感兴趣区域。对于第一和第二患者靶区域的预定位置移动范围,可以选择第二感兴趣区域的界限以围绕第二患者靶区域。第一和第二感兴趣区域可以代表空间滤波器,该空间滤波器被配置为选择在治疗期期间获取的成像数据。该方法可以进一步包括计算用于第一患者靶区域和第二患者靶区域的治疗计划注量图,如果所选择的成像数据指示第一患者靶区域在第一感兴趣区域的界限内并且第二患者靶区域在第二感兴趣区域的界限内,则该治疗计划注量图指定待递送的注量。
13.在一些变体中,第一患者靶区域可以更靠近计划结构。在一些变体中,第一感兴趣区域可以小于第二发射区。在一些变体中,计划结构可以是危及器官(oar)。在一些变体中,第一患者靶区域可以比第二患者靶区域更靠近两个或更多个计划结构。在一些变体中,该方法可进一步包括将第一感兴趣区域内的治疗计划参考点指定为定位参考点以在治疗期开始时定位患者。在一些变体中,选定的成像数据可用于在治疗期期间引导放射递送。在一些变体中,治疗计划参考点可以是第一患者靶区域中的中心点。
14.在一些变体中,成像数据可以包括正电子湮没发射路径数据。在一些变体中,如果正电子湮没发射路径与第一和第二发射区中的至少一个相交,则选择该正电子湮没发射路径。在一些变体中,第二感兴趣区域的大小可以包括一系列第二患者靶区域的位置。在一些变体中,成像数据可以包括正电子发射断层扫描(pet)成像数据、计算机断层扫描(ct)成像数据和磁共振成像(mri)成像数据中的一种或多种。
15.本文还公开了用于对多个靶组织区域进行照射的患者设置和患者靶区域定位的方法。用于患者设置和靶配准/定位的方法可以包括将患者定位在放疗系统的患者平台或床上,获取患者的一个或多个定位图像,包括一个或多个靶区域和/或oar,以及选择一个或多个获取的定位图像内的定位参考点。选择的定位参考点可以与特定患者靶区域的计划定位参考点相对应,并且可以表示患者靶区域的更新位置。可通过基于所选择的定位参考点计算定位函数并用具有基于计划定位参考点导出的平移不变发射滤波器应用该定位函数来计算用于特定患者靶区域的递送的注量图。替代地或附加地,可以从其他计划参数中导出平移不变发射滤波器。例如,可通过基于所选择的定位参考点计算δ函数(例如,3-d离散δ函数)并将该δ函数与基于计划定位参考点和/或其他计划参数导出的平移不变发射滤波器卷积来计算用于递送至患者靶区域的注量图。在另一个实例中,用于递送到患者靶区域的注量图可以通过基于选择的定位参考点用移动或旋转对注量图进行插值来计算。以此类方式,递送注量图可以用患者靶区域的当前位置更新并且可能不需要使用床来调整患者的位
置。通过基于根据选定定位参考点的定位函数(例如,以选定定位参考点为中心的δ函数或高斯型函数)和一组平移不变发射滤波器计算注量图来定位患者靶区域可以被称为“虚拟定位”。在一些变体中,患者可以设置在床上一次,而定位图像的获取、定位参考点的选择以及递送注量图的计算可以针对每个患者靶区域(例如,一个物理定位/设置,多个定位图像扫描,对应多个患者靶区域的多个虚拟定位)进行。或者,可以一次获取定位图像(例如,在患者最初定位在放射治疗系统中时),并且可以为每个患者靶区域(例如,一个物理设置,一个定位图像扫描,对应于多个患者靶区域的多个虚拟定位)使用最初获得的定位图像进行定位参考点的选择和递送注量图的计算。
16.相比之下,常规治疗递送方法包括获取定位图像(例如,定位ct图像)以在患者平台上物理定位患者和患者靶区域以匹配在治疗计划时确定的患者靶区域的位置的步骤。为了在单一治疗期治疗多个患者靶区域,在照射每个患者靶区域之前可能需要物理重新定位患者,因为可能适合照射一个患者靶区域的患者的特定物理位置可能不适合照射另一个患者靶区域。对于每次重新定位,都会获取额外的定位图像。在一些变体中,患者的定位和重新定位可由患者平台提供。此外,一些治疗计划系统可以被配置为输出机器指令(例如,叶型),然后可以根据定位图像来移动机器指令。然而,本文描述的治疗计划系统和方法被配置为输出递送系统的注量图和/或发射滤波器以用于与定位参考点的图像和/或定位函数卷积以生成递送注量图。这可以允许治疗多个患者靶区域而无需针对每个靶区域重新定位患者。递送注量图可以恰好在剂量递送之前由递送系统分割成机器指令。因此,虚拟定位可以消除或减少获取定位图像以及为治疗多个患者靶区域而物理定位(和/或重新定位)患者的次数。
17.作为虚拟定位的替代或补充,用于患者设置的方法可以包括获取第一患者靶区域和第二患者靶区域的图像。第一组患者位置移动矢量可以基于所获取图像和第一患者靶区域的治疗计划图像来计算。可以基于所获取图像、第二患者靶区域的治疗计划图像和第一组患者位置移动矢量来计算第二组患者位置移动矢量。可以根据第一组患者位置移动矢量将患者定位到第一位置(location)和/或位置(position)。患者可以定位在第二位置并根据第二组患者位置移动矢量定位。根据第一组患者位置移动矢量定位患者可以包括根据第一组患者位置移动矢量移动放射治疗患者平台和/或治疗放射源。患者可以定位在第二位置并根据第二组患者位置移动矢量进行调整。根据第二组患者位置移动矢量定位患者可以包括根据第二组患者位置移动矢量移动放射治疗患者平台和/或治疗放射源。移动放射治疗患者平台可包括沿其x轴、和/或y轴、和/或z轴移动平台。移动放射治疗患者平台可以包括调整平台的偏航和/或俯仰和/或滚动,并且移动治疗放射源可以包括调整与治疗放射源耦合的机架的偏航/俯仰/滚动。第一治疗计划图像和第二治疗计划图像可以是相同的治疗计划图像。获取的图像可以是pet(正电子发射断层扫描)图像。获取的图像可以是ct(计算机断层扫描)图像。获取的图像可以是mri(磁共振成像)图像。在一些实施例中,计算第一组和第二组患者位置移动矢量可以在治疗放射源被激活之前发生。在一些实施例中,可以通过将获取的图像中的第一患者靶区域的位置与第一治疗计划图像中的第一患者靶区域的位置进行比较来计算第一位置差。可以通过将获取的图像中的第二患者靶区域的位置与第二治疗计划图像中的第二患者靶区域的位置进行比较来计算第二位置差。如果第一位置差或第二位置差超过位置差阈值,则可以生成通知。第一患者靶区域和第二患者靶区域可以
包括一个或多个肿瘤区域。第一患者靶区域可以包括肿瘤的第一部分并且第二患者靶区域可以包括肿瘤的第二部分。第一组和第二组位置移动矢量可以包括距离和方向平移。方向平移可以包括倾斜角。
18.用于向多个患者区域递送放射注量的方法可以包括将递送注量图变换(也称为分割)为放疗系统机器指令(例如,治疗放射源放射发射参数、围绕患者平台的每个发射位置的多叶准直器配置等),然后通过从治疗放射源向患者发射放射注量来执行机器指令。多个患者靶区域的递送注量图可以是在虚拟定位期间针对每个患者靶区域计算的个体注量图和用于递送至两个或更多个患者靶区域(例如,所有患者靶区域)的机器指令的组合,并且可以同时被分割。替代地或附加地,每个患者靶区域的个体注量图可以被分别(例如,依次地)分割。任选地,在bgrt中,在治疗期期间获取正电子湮没发射路径数据并用于计算递送注量,递送注量图可以实时分割成放疗系统机器指令,在例如,获取发射路径数据和递送治疗放射束之间的500ms或更短内分割。递送注量图可以是根据发射路径数据计算得到的注量图,并且可以通过移动或旋转roi来实现虚拟定位。
19.一种用于虚拟靶区域定位和放射递送的方法可以包括获取处于治疗位置的患者的图像并在所获取图像中识别患者靶区域,在所获取图像内选择定位参考点,其中所述定位参考点对应于计划定位参考点,通过基于定位参考点计算定位函数并将定位函数应用于基于计划定位参考点导出的平移不变发射滤波器来计算用于在治疗放射源的每个发射位置处递送至患者靶区域的注量,并使用治疗放射源将递送注量发射到患者靶区域。定位函数可以是δ函数,并且将定位函数应用于平移不变发射滤波器可以包括将δ函数与平移不变发射滤波器卷积。附加地或替代地,平移不变发射滤波器可以包括基于每个靶区域的计划定位参考点递送到多个靶区域的放射注量的一个或多个函数移位算子和定向算子。例如,如上所述,函数移位算子可以包括用移位对二维或三维图进行插值的函数。方向算子可以包括使用旋转来对二维或三维图进行插值的函数。例如,插值可以包括线性插值、最近邻插值、双三次插值、样条插值或傅立叶移位插值中的一种或多种。定位参考点可以是所获取图像内的用户选择位置和/或可以对应于在治疗计划期间相对于患者靶区域限定的治疗计划等中心。第一患者靶区域可以在治疗计划期间限定的患者的第一治疗区中并且第二靶区域可以在治疗计划期间限定的患者的第二治疗区中。第一治疗区可以包括第一组轴向平面并且可以具有大约8cm或更小的轴向长度,并且第二治疗区可以不与第一治疗区重叠并且可以具有大约8cm或更小的轴向长度并且可以包括第二组轴向平面。第一治疗区的中心和第二治疗区的中心可以是共线的,例如沿着iec-y轴和/或与iec-y轴共面。在一些变体中,第一治疗区可以与第二治疗区重叠。
20.治疗放射源的发射位置包括治疗放射源相对于患者平台位置的位置。治疗放射源可安装在可绕纵轴旋转的机架上,并且治疗放射源的位置可由绕纵轴的机架角度指定。患者平台可沿纵轴移动到不同位置。
21.在一些变体中,治疗放射源可以安装在机架上,使得放射可以以离散的连续弧(例如,非共面的vmat、4-pi vmat)递送到患者。在这些变体中的一些中,这些放射递送弧可能彼此不共面(例如,垂直于纵轴)。发射位置可以被指定为沿着每个弧的离散位置并且可以由弧索引。患者平台可以被配置为重新定位到每个弧之间的预定位置和取向。
22.在一些变体中,治疗放射源可以安装在机架上,使得放射可以在围绕4-pi或2-pi
半球外壳的固定点处递送。在这些变体中的一些中,可以基于二维注量图将一组发射位置指定为离散位置。患者平台可以被配置为将患者移动到每个固定点之间的一组预定位置和/或取向。
23.方法可以进一步包括在所获取图像中识别第二患者靶区域,为所获取图像内的第二患者靶区域选择第二定位参考点,其中第二定位参考点对应于第二计划定位参考点,通过基于第二定位参考点计算第二定位函数并基于第二计划定位参考点将第二定位函数应用于第二平移不变发射滤波器来计算在治疗放射源的每个发射位置处的第二递送注量,以及使用治疗放射源向第二患者靶区域发射第二递送注量。方法可以任选地包括在所获取图像中识别第二患者靶区域,为所获取图像内的第二患者靶区域选择第二定位参考点,其中第二定位参考点对应于第二计划定位参考点,通过基于第二定位参考点计算第二δ函数并将第二δ函数与基于第二计划定位参考点的第二平移不变发射滤波器卷积来计算在治疗放射源的每个发射位置处的第二递送注量,以及使用治疗放射源向第二患者靶区域发射第二递送注量。向第一患者靶区域发射第一递送注量和向第二患者靶区域发射第二递送注量可以同时发生,和/或可以依次发生。
24.在一些变体中,一种用于虚拟靶区域定位和放射递送的方法可以包括以下步骤:获取处于治疗位置的患者的图像并在所获取图像中识别患者靶区域,在所获取图像内选择定位参考点,其中定位参考点对应于计划定位参考点,通过基于定位参考点计算定位函数并将定位函数应用于基于计划定位参考点导出的平移不变发射滤波器来计算在治疗放射源的每个发射位置处用于递送至患者靶区域的注量,以及使用治疗放射源向患者靶区域发射递送注量。
25.在一些变体中,将定位函数应用于平移不变发射滤波器可以包括将定位函数与平移不变发射滤波器卷积。在一些变体中,定位函数可以是δ函数、高斯函数、圆函数和插值中的一种。在一些变体中,高斯函数可以是截断的高斯函数。在一些变体中,插值可以是线性、双三次、样条或傅立叶移位中的一种。在一些变体中,所获取图像可以包括正电子发射断层扫描(pet)图像、x射线投影图像、计算机断层扫描(ct)图像和磁共振成像(mri)图像中的一种或多种。
26.在一些变体中,该方法可以进一步包括在所获取图像中识别第二患者靶区域,并为所获取图像内的第二患者靶区域选择第二定位参考点。第二定位参考点可以对应于第二计划定位参考点。该方法可以进一步包括通过基于第二定位参考点计算第二定位函数并基于第二计划定位参考点将第二定位函数应用于第二平移不变发射滤波器来计算在治疗放射源的每个发射位置处的第二递送注量,以及使用治疗放射源向第二患者靶区域发射第二递送注量。
27.在一些变体中,该方法可以进一步包括在所获取图像中识别第二患者靶区域,并为所获取图像内的第二患者靶区域选择第二定位参考点。第二定位参考点可以对应于第二计划定位参考点。该方法可以进一步包括通过基于第二定位参考点计算第二δ函数并将第二δ函数与基于第二计划定位参考点的第二平移不变发射滤波器卷积来计算在治疗放射源的每个发射位置处的第二递送注量,以及使用治疗放射源向第二患者靶区域发射第二递送注量。在一些变体中,将第一递送注量发射到第一患者靶区域和将第二递送注量发射到第二患者靶区域同时发生。在一些变体中,向第一患者靶区域发射第一递送注量和向第二患
者靶区域发射第二递送注量依次发生。
28.在一些变体中,定位函数是第一定位函数(δ)。第一平移不变发射滤波器可以包括在治疗计划期间为治疗放射源的每个发射位置(i)计算的第一组注量图滤波器(p1,p2,...,pi)。该方法可以包括计算定位函数(δi)到每个发射位置(i)的第一组投影,δi=proji(δ).每个投影(δi)可能是2-d注量分布。计算第一递送注量可以包括通过将第一定位函数的第一组投影中的每个投影(δi)与对应的注量图滤波器(pi)卷积,fi=pi*δi来计算治疗放射源的每个发射位置(i)的第一递送注量图(fi),并且递送第一注量可以包括将治疗放射源移动到每个发射位置(i)并且根据第一递送注量图(fi)向第一患者靶区域发射放射。在某些变体中,每个投影(δi)可能是m
×
n矩阵,其中m是多叶准直器叶的数量,和n是在治疗计划期间选择的数量。在一些变体中,n是在治疗计划期间选择的光束站的数量。在一些变体中,第一定位函数可以是δ函数、高斯函数、圆函数和插值中的一个。在一些变体中,高斯函数可以是截断的高斯函数。在一些变体中,插值可以是线性、双三次、样条和傅立叶移位中的一种。
29.在一些变体中,第二平移不变发射滤波器可以包括在治疗计划期间为每个发射位置(i)计算的第二组注量图滤波器(p_21,p_22,...,p_2i)。该方法可以包括计算第二定位函数(δ_2i)到每个发射位置(i)的第二组投影,δ_2i=proji(δ_2),其中每个投影(δ_2i)是2-d注量分布。计算第二递送注量可以包括通过将第二定位函数的第二组投影中的每个投影(δ_2i)与对应的注量图滤波器(p_2i)卷积,f_2i=p_2i*δ_2i来计算每个发射位置(i)的第二递送注量图(f_2i)递送第二计算注量可以包括将治疗放射源移动到每个发射位置(i)并根据第二递送注量图(f_2i)向第二患者靶区域发射放射。在某些变体中,每个投影(δ_2i)可能是m
×
n矩阵。在一些变体中,m是多叶准直器叶的数量,并且n是在治疗计划期间选择的数量。在一些变体中,n是在治疗计划期间选择的光束站的数量。在一些变体中,第二定位函数可以是δ函数、高斯函数、圆函数和插值中的一种。在一些变体中,高斯函数可以是截断的高斯函数。在一些变体中,插值可以是线性、双三次、样条和傅立叶移位中的一种。在一些变体中,递送计算的注量可以包括将递送注量图(fi,f_2i)分割成用于每个发射位置的多个放射治疗系统机器指令。
30.在一些变体中,递送计算的注量可以包括将计算的注量分割成用于每个发射位置的多个放射治疗系统机器指令。在一些变体中,递送第二计算的注量可以包括将第二计算的注量分割成用于每个发射位置的多个放射治疗系统机器指令。
31.在一些变体中,多个放射治疗系统机器指令可以包括用于每个发射位置的一个或多个多叶准直器配置。发射放射注量可进一步包括将多叶准直器的叶移动到与治疗放射源的发射位置相对应的多叶准直器配置,并发射放射脉冲。
32.在一些变体中,多个放射治疗系统机器指令可进一步包括用于每个发射位置的治疗放射源发射(例如,脉冲)参数。发射放射脉冲可以包括发射具有对应于治疗放射源的发射位置的治疗放射源脉冲参数的放射。在一些变体中,计算传递注量图(fi,f_2i)可以进一步包括将第一组或第二组投影中的每个投影与对应的平移不变注量图滤波器卷积,并应用虚拟平坦滤波器校正因子(ff):
33.(fi)=ff
·
(pi*δi);(f_2i)=ff
·
(p_2i*δ_2i)。
34.在一些变体中,虚拟平坦滤波器校正因子(ff)是m
×
n矩阵并且是由治疗放射源发射的放射束的平坦概况的倒数。
35.在一些变体中,计算递送注量图(fi,f_2i)可以进一步包括将一组投影中的每个投影与平移不变注量图滤波器卷积,应用虚拟平坦滤波器校正因子(ff),以及距离补偿因子影与平移不变注量图滤波器卷积,应用虚拟平坦滤波器校正因子(ff),以及距离补偿因子
36.在一些变体中,di表示从发射位置i到治疗计划期间限定的患者靶区域中心的距离,并且d
′i表示从发射位置i到在放射递送时确定的患者靶区域中心的距离。
37.在一些变体中,定位参考点可以是所获取图像内的用户选择位置。在一些变体中,定位参考点可以对应于在治疗计划期间相对于患者靶区域限定的治疗计划等中心。在一些变体中,第一患者靶区域可以在治疗计划期间限定的患者的第一治疗区中并且第二靶区域可以在治疗计划期间限定的患者的第二治疗区中。在一些变体中,第一治疗区具有约8cm或更小的轴向长度并且包括第一组轴向平面,并且第二治疗区具有约8cm或更小的轴向长度并且不与第一治疗区重叠。第二治疗区可以包括第二组轴向平面。在一些变体中,第一治疗区的中心和第二治疗区的中心可以沿iec-y轴共线和/或与iec-y轴共面。在一些变体中,第一治疗区和第二治疗区可以重叠。在一些变体中,治疗放射源的发射位置可以包括治疗放射源相对于患者平台位置的位置。在一些变体中,治疗放射源可安装在可绕纵轴旋转的机架上,并且治疗放射源的位置可由绕纵轴的机架角度指定。在一些变体中,患者平台可沿纵轴移动到不同位置。
38.在一些变体中,计算递送注量图(fi,f_2i)可以进一步包括将一组投影中的每个投影与具有δ函数δi,δ_2i的平移不变注量图滤波器p
′
,p_2
′
卷积,所述δ函数已与具有角移动的δ函数循环卷积,其中患者靶区域位于位置δ
loc
和δ_2
loc
的等中心之外,
39.δi=proji(δ)*δ
i,roll
[0040][0041][0042]
(fi)=(pi′
*δi)
[0043]
δ_2i=proji(δ_2)*δ_2
i,roll
[0044][0045][0046]
(f_2i)=(p_2i′
*δ_2i)
[0047]
一种用于向多个患者靶区域递送放射的方法可以包括在治疗期开始时获取定位图像、在定位图像中识别第一靶区域和第二靶区域、移动治疗计划注量图的第一注量图子区域,使得第一注量图子区域的非零高注量区域与定位图像中的第一靶区域共同定位,移动治疗计划注量图的第二注量图子区域,使得第二注量图子区域的非零高注量区域与定位图像中的第二靶区域共同定位,将移动的第一注量图子区域递送到第一靶区域,以及将移动的第二注量图子区域递送到第二靶区域。
[0048]
可以通过沿着治疗计划注量图的非零低剂量区域限定每个子区域的界限,将治疗计划注量图划分为第一和第二注量图子区域。递送第一和第二移动的注量图子区域可以包
括将移动的第一和第二注量图子区域分割成用于治疗放射源的每个发射位置的多个放射治疗系统机器指令。放射治疗系统机器指令可以包括用于每个发射位置的一个或多个多叶准直器配置和治疗放射源控制参数。方法可以任选地包括在治疗期期间获取成像数据并且在向第一靶区域递送注量之前根据所获取的成像数据修改移动的第一注量图子区域。替代地或附加地,方法可以包括在治疗期期间获取成像数据并且在向第二靶区域递送注量之前根据所获取的成像数据修改移动的第二注量图子区域。
[0049]
递送移动的第一注量图子区域和递送移动的第二注量图子区域可以同时发生和/或可以依次发生。在一些变体中,递送移动的第一注量图子区域和递送移动的第二注量图子区域可以依次发生。定位图像可以包括ct图像和/或pet图像和/或mri图像。方法可以任选地包括将第一注量图子区域的高注量区域与第一靶区域的位置进行比较以限定第一定位校正,将第二注量图子区域的高注量区域与第二靶区域的位置进行比较以限定第二定位校正,以及在向第一靶区域递送注量之前根据第一定位校正调整患者平台。在向第一靶区域递送注量之后,方法可以包括在向第二靶区域递送注量之前根据第二定位校正调整患者平台。
[0050]
在一些变体中,将移动的第一注量图子区域递送到第一靶区域可以包括选择表示定位图像内的位置的定位参考点,将根据定位参考点计算的定位函数应用于在治疗计划期间对第一靶区域计算的第一平移不变发射滤波器以更新第一注量图子区域,将更新的第一注量图子区域分割成多个放射治疗系统指令,以及根据第一多个放射治疗系统指令向第一靶区域发射放射注量。
[0051]
应用定位函数可以包括将根据定位参考点计算的第一定位函数(例如,第一δ函数或第一高斯函数,例如截断的高斯函数)与第一平移不变发射滤波器进行卷积。将移动的第二注量图子区域递送到第二靶区域可以包括获取第二靶区域的成像数据,将成像数据与在治疗计划期间对第二靶区域计算的第二平移不变发射滤波器卷积以更新第二注量图子区域,将更新的第二注量图子区域分割成第二多个放射治疗系统指令,以及根据第二多个放射治疗系统指令向第二靶区域发射放射注量。
[0052]
在一些变体中,所获取的成像数据可以是pet成像数据。将移动的第二注量图子区域递送到第二靶区域可以包括选择位于第二靶区域内的第二定位参考点,通过将根据第二定位参考点计算的第二定位函数应用于第二平移不变发射滤波器来计算第二注量图子区域,将计算的第二注量图子区域分割成第二多个放射治疗系统指令,以及根据第二多个放射治疗系统指令向第一靶区域发射放射注量。替代地或附加地,将移动的第二注量图子区域递送到第二靶区域可以包括选择位于第二靶区域内的第二定位参考点,通过将根据第二定位参考点计算的第二定位函数(例如,第一δ函数或第一高斯函数,如截断的高斯函数)与第二平移不变发射滤波器卷积来计算第二注量图子区域,将计算的第二注量图子区域分割成第二多个放射治疗系统指令,以及根据第二多个放射治疗系统指令向第二靶区域发射放射注量。在一些变体中,该方法可以包括调整可递送的放射剂量以满足一个或多个剂量约束。在一些变体中,一个或多个剂量约束可以包括一个或多个成本函数。在一些变体中,一个或多个成本函数可以包括累积成本函数,每个成本函数的加权因子由下式给出:
[0053]
c=∑w
ici
(x) ∑w
kck
(ax) ∑w
mcm
(ax
cumulative
)
[0054]
∑w
ncn
(x
cumulative
)
[0055]
其中x是患者靶区域的注量,a是患者靶区域的剂量计算矩阵,ax
cumulative
是累积计划剂量并且x
cumulative
是累积计划注量。
[0056]
一种用于向多个患者靶区域放射递送的治疗计划方法可以包括在患者计划图像中识别第一患者靶区域的第一位置和第二患者靶区域的第二位置,限定具有围绕第一患者靶区域的界限的第一感兴趣区域(roi)(其可以是第一发射区),限定具有围绕第二患者靶区域的界限的第二roi(其可以是第二发射区),以及计算第一患者靶区域和第二患者靶区域的治疗计划注量图,如果选定的成像数据指示第一患者靶区域在第一感兴趣区域的界限内并且第二患者靶区域在第二感兴趣区域的界限内,则该治疗计划注量图指定待递送的注量。对于第一和第二患者靶区域的位置移动的预定范围,可以选择第二感兴趣区域的界限以围绕第二患者靶区域,并且第一和第二感兴趣区域可以表示被配置为选择在治疗期期间获得的成像数据的空间滤波器。第一患者靶区域可以更靠近计划结构。第一感兴趣区域可以小于第二感兴趣区域。在一些变体中,计划结构可以是危及器官(oar)。第一患者靶区域可以比第二患者靶区域更靠近两个或更多个计划结构。一些方法可进一步包括将第一感兴趣区域内的治疗计划参考点指定为定位参考点以在治疗期开始时定位患者。所选择的成像数据可用于在治疗期期间引导放射递送。治疗计划参考点可以是第一感兴趣区域中的中心点,并且在一些实例中可以是第一患者靶区域中的中心点。成像数据可以包括正电子湮没发射路径数据(例如,pet数据)、ct成像数据和/或mri成像数据。如果正电子湮没发射路径与第一和第二感兴趣区域中的至少一个相交,则可选择该正电子湮没发射路径。第二感兴趣区域的大小可以包括一系列第二患者靶区域的位置。
[0057]
在一些变体中,用于患者定位和放射递送的方法可以包括获取包括第一患者靶区域和第二患者靶区域的图像,和在治疗计划期间限定的第一感兴趣区域内对齐第一患者靶区域。如果第二患者靶区域位于治疗计划期间限定的第二感兴趣区域内,则该方法可以包括使用正电子发射检测器阵列获取包括多个响应线(lor)的正电子湮没发射数据。如果lor与第一感兴趣区域和第二感兴趣区域相交,则该方法可以包括通过将lor与在治疗计划期间针对对应感兴趣区域限定的平移不变发射滤波器卷积来计算递送注量。方法可以进一步包括使用治疗放射源发射递送注量,其中发射递送注量包括将递送注量分割成用于治疗放射源的每个发射位置的多个放射治疗系统机器指令。放射治疗系统机器指令可以包括用于每个发射位置的一个或多个多叶准直器配置和治疗放射源发射(例如,脉冲)参数。在一些变体中,图像可以包括正电子发射断层扫描(pet)图像、计算机断层扫描(ct)图像和磁共振成像(mri)图像中的一种或多种。
[0058]
一种用于为放射治疗治疗期定位和配准患者的方法可以包括将患者定位在放射治疗系统平台上,使得第一患者靶区域与治疗放射源的位置对齐并且位于第一预定感兴趣区域内,以及确定第二患者靶区域的位置是否在第二预定感兴趣区域内。如果第二患者靶区域的位置在第二预定感兴趣区域内,则该方法可包括继续将放射递送到第一患者靶区域。如果第二患者靶区域的位置不在第二预定感兴趣区域内,则该方法可以包括生成视觉和/或听觉通知。可以在治疗计划期间计算第一和第二预定感兴趣区域,并且相对于第一预定感兴趣区域的位置限定第二预定放射感兴趣区域的位置。
[0059]
任选地,一些方法可以包括在将放射递送至第二患者靶区域之前获取成像数据,其中第一和第二感兴趣区域是空间掩模,其被配置为抑制具有不与第一或第二感兴趣的放
射区域共同定位的空间特性的成像数据。在一些变体中,方法可以包括基于所获取的成像数据确定第二靶区域是否位于第二感兴趣区域内,并且如果第二靶区域位于第二感兴趣区域内,则继续将放射递送至第二靶区域。所获取的成像数据可以是正电子湮没发射路径数据(例如,pet成像数据)、ct成像数据和/或mri成像数据。递送放射可以包括将递送注量分割成用于治疗放射源的每个发射位置的多个放射治疗系统机器指令。放射治疗系统机器指令可以包括用于每个发射位置的一个或多个多叶准直器配置和治疗放射源发射(例如,脉冲)参数。
[0060]
在一些变体中,该方法可以进一步包括当第二患者靶区域的位置不在第二预定感兴趣区域内时调整患者的位置。在一些变体中,该方法可以进一步包括调整放疗系统平台以将第二患者靶区域的位置移动到第二预定感兴趣区域内。在一些变体中,该方法可以进一步包括根据第二患者靶区域的位置移动第二患者靶区域的计划注量。在一些变体中,该方法可以进一步包括递送放射,递送放射包括将递送注量分割成用于治疗放射源的每个发射位置的多个放射治疗系统机器指令。在一些变体中,该方法可以进一步包括放射治疗系统机器指令,该指令包括用于每个发射位置的一个或多个多叶准直器配置和治疗放射源脉冲参数。
[0061]
一种用于放射治疗的方法可以包括获取包括第一患者靶区域和第二患者靶区域的图像,将计划注量图划分为向第一患者靶区域递送第一规定剂量的第一注量子图,和向第二患者靶区域递送第二规定剂量的第二注量子图,移动第一注量子图以与所获取图像的第一患者靶区域对齐,移动第二注量子图以与获取图像的第二患者靶区域对齐,通过组合移动的第一注量子图和移动的第二注量子图来计算递送注量图,和如果移动的第一子注量图的高注量区域和移动的第二注量子图的高注量区域在递送注量图中彼此不共同定位,则将放射递送至第一患者靶区域。在一些变体中,计划注量图可以如下生成:在治疗计划图像中识别第一和第二患者靶区域,计算第一注量图以将第一规定剂量递送至第一患者靶区域、计算第二注量图以将第二规定剂量递送至第二患者靶区域,和通过组合第一和第二注量图并调整组合注量图以使得第一和第二注量图的高注量区域彼此不共同定位并且第一和第二患者靶区域各自接收对应的第一和第二规定剂量来计算计划注量图。在一些变体中,第一注量子图可以包括第一注量图并且第二注量子图可以包括第二注量图。在一些变体中,计算计划注量图可以包括基于一个或多个调整约束来调整组合注量图,使得第一注量图和第二注量图不超过预定剂量限制。在一些变体中,该方法可以包括在治疗计划图像中识别危及器官。计算计划注量图可以进一步包括调整组合注量图,使得对危及器官的注量不超过预定剂量限制。在一些变体中,递送放射可以包括将递送注量分割成用于治疗放射源的每个发射位置的多个放射治疗系统机器指令。在一些变体中,放射治疗系统机器指令可以包括用于每个发射位置的一个或多个多叶准直器配置和治疗放射源发射参数。在一些变体中,该方法可以包括确定递送注量图是否包括超过预定剂量限制的对危及器官的注量水平,并且如果对危及器官的注量不超过预定剂量限制,则向第一患者靶区域递送放射。在一些变体中,计划注量图可以如下生成:在治疗计划图像中识别第一和第二患者靶区域,计算第一注量图以将第一规定剂量递送至第一患者靶区域、计算第二注量图以将第二规定剂量递送至第二患者靶区域,和通过组合第一和第二注量图并迭代调整组合注量图以满足一组联合约束同时将第一和第二注量图保持为单独的注量图来计算计划注量图。在一些变
体中,所获取图像可以包括正电子发射断层扫描(pet)图像、计算机断层扫描(ct)图像和磁共振成像(mri)图像中的一种或多种。
[0062]
计划注量图可以如下生成:在治疗计划图像中识别第一和第二患者靶区域、计算第一注量图以将第一规定剂量递送至第一患者靶区域、计算第二注量图以将第二规定剂量递送至第二患者靶区域,和通过组合第一和第二注量图并调整组合注量图以使得第一和第二注量图的高注量区域彼此不共同定位,并且第一和第二患者靶区域各自接收对应的第一和第二规定剂量来计算计划注量图。第一注量子图可以包括第一注量图并且第二注量子图可以包括第二注量图。可以使用例如一组联合约束重新优化计划注量图,同时将第一子注量图和第二注量子图保持为单独的注量图。方法可以进一步包括在治疗计划图像中识别危及器官,并且计算计划注量图可以进一步包括调整组合的注量图,使得危及器官的注量不超过预定剂量限制。递送放射可以包括将递送注量分割成用于治疗放射源的每个发射位置的多个放射治疗系统机器指令。放射治疗系统机器指令可以包括用于每个发射位置的一个或多个多叶准直器配置和治疗放射源发射参数。任选地,方法可以包括确定递送注量图是否包括超过预定剂量限制的对危及器官的注量水平,并且如果对危及器官的注量不超过预定剂量限制,则向第一患者靶区域递送放射。
[0063]
在一些变体中,可以为每个患者靶区域生成单独的治疗计划。这些计划中的每一个都可以个体优化、汇总,然后基于一组联合约束重新优化,同时将治疗计划保持为单独的实体。可以基于每个治疗计划生成单独的注量图并将其汇总为组合注量图。在治疗期期间,每个单独的注量图可以独立移动,并且可以在剂量递送之前确认它们的总剂量体积直方图(dvh)。
[0064]
附加地或替代地,除了预定的一组约束之外,还可以应用一个或多个调整约束(例如,除了组织约束之外的人工约束,例如调整结构),以确保在给定地带(例如,区域)中剂量不超过预定阈值。例如,可以在治疗计划期间添加一个或多个预定剂量受限地带以将地带保持为“低剂量谷”,这可用于降低每个患者靶区域的注量图在治疗期期间独立移动时可能出现的剂量“热点”的可能性。在一些变体中,一个或多个调整约束可以帮助促进两个或更多个靶之间的放射递送的解耦。调整约束的一些变化可能会限制剂量递送角度。
[0065]
本文还公开了用于生成放射剂量的可视化图形表示的方法。用于生成可视化图形的方法的一种变体可以包括生成用于照射一个或多个患者靶区域的治疗计划,其中该治疗计划包括至少一个或多个治疗计划注量图、每个患者靶区域的一个或多个计划图像,以及对应的标称剂量图像,为每个患者靶区域计算多个表示治疗期不确定性的不确定性数据输入,在不确定性数据输入的存在下为每个不确定性数据输入计算待递送至每个患者靶区域的预期剂量以导出多个剂量图像,将多个剂量图像组合成包括复合体积的可视化图形,其中每个剂量图像代表复合体积中的帧,以及将可视化图形显示到显示设备。
[0066]
在一些变体中,治疗计划可进一步包括一个或多个平移不变发射滤波器。多个数据输入可以包括一个或多个标量值、矢量值和/或体积值。在一些变体中,复合体积可以是4-d体积。多个剂量图像可以包括一个或多个患者靶区域中的每一个的2-d剂量图像切片。复合体积可以包括每个患者靶区域的3-d剂量体积,并且每个3-d剂量体积可以包括每个患者靶区域的2-d剂量图像切片。在一些变体中,该方法可以包括在每个剂量图像中的每个点处迭代剂量值,将剂量值与最小剂量体积中的第一匹配点和最大剂量体积中的第二匹配点
进行比较以更新第一和第二匹配点,迭代最小剂量体积中的每个点,计算最小剂量体积和标称剂量体积的值之间的差值,将差值和差值的频率存储在δ剂量体积的两个帧中,迭代最大剂量体积中的每个点,计算最大剂量体积和标称剂量体积的值之间的差值,将差值和差值的频率存储在δ剂量体积的另外两个帧中,以及为δ剂量体积的每个四帧切片渲染表面图,其中最大值的频率从3-d平面沿 z挤出,最小值的频率从3-d平面沿
–
z挤出,并且表面图中点处的值由颜色表示。
[0067]
用于生成可视化图形的方法的一种变体可以包括生成用于照射一个或多个患者靶区域的治疗计划,其中该治疗计划可以包括至少一个或多个治疗计划注量图、每个患者靶区域的一个或多个计划图像和对应的标称剂量图像,为每个患者靶区域计算表示治疗期不确定性的多个不确定性数据输入,在不确定性数据输入的存在下为每个不确定性数据输入计算待递送至每个患者靶区域的预期剂量以导出多个剂量图像,将多个剂量图像组合成包括复合体积的可视化图形,其中每个剂量图像代表复合体积中的帧,并将可视化图形显示到显示设备。在一些变体中,治疗计划可进一步包括一个或多个平移不变发射滤波器。多个数据输入可以包括一个或多个标量值、矢量值和/或体积值。复合体积可以是4-d体积。多个剂量图像可以包括一个或多个患者靶区域中的每一个的2-d剂量图像切片。复合体积可以包括每个患者靶区域的3-d剂量体积,并且每个3-d剂量体积可以包括每个患者靶区域的2-d剂量图像切片。任选地,方法可以包括在每个剂量图像中的每个点处迭代剂量值,将剂量值与最小剂量体积中的第一匹配点和最大剂量体积中的第二匹配点进行比较以更新第一和第二匹配点,迭代最小剂量体积中的每个点,计算最小剂量体积和标称剂量体积的值之间的差值,将差值和差值的频率存储在δ剂量体积的两个帧中,迭代最大剂量体积中的每个点,计算最大剂量体积和标称剂量体积的值之间的差值,将差值和差值的频率存储在δ剂量体积的另外两个帧中,以及为δ剂量体积的每个四帧切片渲染表面图,其中最大值的频率从3-d平面沿 z轴挤出,最小值的频率从3-d平面沿
–
z轴挤出,并且表面图中点处的值由颜色表示。
[0068]
本文描述的是放射剂量的可视化图形表示。视觉图形表示的一种变体可以包括表示患者解剖结构的3-d体积,其中3-d体积包括一堆2-d患者解剖图像,以及对应于每个2-d患者解剖图像剂量分布的3-d剂量表面图。3-d剂量表面图的高度可以表示根据患者的治疗计划的剂量水平,并且跨表面图的颜色值可以表示治疗期的剂量水平的概率值。
[0069]
在一些变体中,用于多靶治疗计划的图形用户界面可以包括多个治疗区的第一图形表示,每个治疗区含一个或多个患者靶区域。每个治疗区可以跨越患者的不同区域并代表不同的患者定位,以及每个治疗区的剂量测定特性的第二图形表示。第一和第二图形表示可以被配置为同时输出到显示设备。
[0070]
在一些变体中,所有多个治疗区的剂量测定特性可以在显示设备上同时可视化。在一些变体中,每个治疗区的剂量测定特性可以个体可视化。在一些变体中,每个治疗区的剂量测定特性可以包括剂量测定目标、剂量体积直方图、剂量统计和目标性能中的一个或多个。在一些变体中,第三图形表示可以包括跨多个治疗区的所有患者靶区域的视图和表示一个或多个患者靶区域之间的相对空间关系的视觉标记。在一些变体中,图形用户界面可以进一步包括第三图形表示,其包括跨多个治疗区的多个危及器官(oar)的视图和表示每个oar与一个或多个治疗区的相对空间关系的视觉标记。在一些变体中,图形用户界面可
以进一步包括第三图形表示,其包括跨多个治疗区的所有患者靶区域的视图和表示一个或多个患者靶区域之间的相对空间关系的第一视觉标记,和第四图形表示,其包括跨多个治疗区的多个危及器官(oar)的视图和表示每个oar与一个或多个治疗区的相对空间关系的第二视觉标记。在一些变体中,图形用户界面可以包括表示患者解剖结构的3-d可视化。在一些变体中,第一图形表示可以分层到解剖3-d可视化上。在一些变体中,第一图形表示可以包括用于多个治疗区中的每一个的带。每个带可以具有表示其对应治疗区的维度的范围。在一些变体中,图形用户界面可以包括描绘多个治疗区的子组的第一查看模式和描绘所有多个治疗区的第二查看模式。在一些变体中,多个治疗区的子组可以包括用户选择的治疗区。
附图说明
[0071]
本技术可以通过结合附图参考以下描述来理解。
[0072]
图1a是用于sbrt虚拟定位的治疗计划方法的一种变体的流程图表示。
[0073]
图1b是用于bgrt的虚拟定位的治疗计划方法的一种变体的流程图表示。
[0074]
图2是用于马赛克多靶定位的治疗计划方法的一种变体的流程图表示。
[0075]
图3a-3b描绘了用于解耦多靶定位的治疗计划方法的一种变体的流程图表示。
[0076]
图4是用于基于bgrt的定位的治疗计划方法的一种变体的流程图表示。
[0077]
图5a是用于治疗计划的方法的一种变体的流程图表示。
[0078]
图5b是用于治疗计划的方法的一种变体的流程图表示。
[0079]
图5c是用于治疗计划的方法的一种变体的流程图表示。
[0080]
图6是用于治疗计划的方法的一种变体的流程图表示。
[0081]
图7a是用于虚拟定位的方法的一种变体的流程图表示。
[0082]
图7b是用于虚拟定位的方法的一种变体的流程图表示。
[0083]
图8a是用于马赛克多靶定位的方法的一种变体的流程图表示。
[0084]
图8b是用于马赛克多靶定位的方法的一种变体的流程图表示。
[0085]
图9是用于解耦多靶定位的方法的一种变体的流程图表示。
[0086]
图10是用于基于bgrt的定位的方法的一种变体的流程图表示。
[0087]
图11a是定位用于放射治疗的患者的方法的一种变体的流程图表示。
[0088]
图11b是方法的一种变体的流程图表示。
[0089]
图12a-12f示出了可以调整患者位置的过程的一种变体。
[0090]
图13a-13f示出了可以调整患者位置的过程的一种变体。
[0091]
图14a-14f示出了可以调整患者的位置以照射两个离散的患者靶区域的过程的一种变体。
[0092]
图15a描绘了代表剂量分布和/或概率的可视化图形的一种变体。
[0093]
图15b描绘了代表3-d剂量分布(标称、最小、最大剂量水平)的可视化图形的一种变体。
[0094]
图15c是生成可视化图形的方法的一种变体的流程图表示。
[0095]
图15d是生成可视化图形的方法的一种变体的框图。
[0096]
图15e是生成可视化图形的方法的一种变体的流程图表示。
[0097]
图16a是生成可视化图形的方法的一种变体的流程图表示。
[0098]
图16b是生成可视化图形的方法的一种变体的框图。
[0099]
图17a描绘了表示δ剂量分布的可视化图形的一种变体。
[0100]
图17b描绘了表示δ剂量分布的可视化图形的一种变体。
[0101]
图17c描绘了代表最大剂量水平的δ剂量分布的可视化图形的一种变体。
[0102]
图17d描绘了代表标称剂量水平的δ剂量分布的可视化图形的一种变体。
[0103]
图17e描绘了代表最小剂量水平的δ剂量分布的可视化图形的一种变体。
[0104]
图17f描绘了可视化图形(标称、最小、最大剂量水平)的一种变体。
[0105]
图18a是用于多靶放射递送的方法的一种变体的流程图表示。
[0106]
图18b是用于多靶放射递送的方法的一种变体的流程图表示。
[0107]
图18c是用于多靶放射递送的方法的一种变体的流程图表示。
[0108]
图18d是用于多靶放射递送的方法的一种变体的流程图表示。
[0109]
图19是用于多靶基于bgrt的放射递送的方法的一种变体的流程图表示。
[0110]
图20是用于多靶放射递送的方法的一种变体的流程图表示。
[0111]
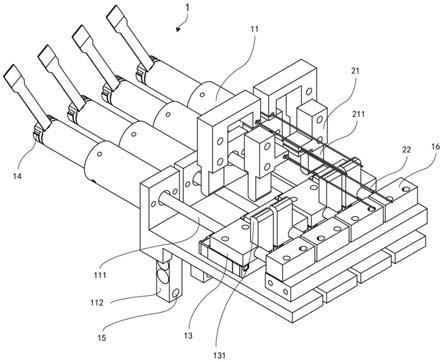
图21a描绘了可以与本文所述的任何方法一起使用的放射治疗系统的一个变体。
[0112]
图21b描绘了可以与本文所述的任何方法一起使用的放射治疗系统的另一变体的横截面图。
[0113]
图21c描绘了可以与本文所述的任何方法一起使用的放射治疗系统的另一变体的示意图。
[0114]
图22a是基于空间体素的δ函数的示意图。
[0115]
图22b是用于具有64个mlc叶和20个患者平台光束站的放射治疗系统的虚拟平坦滤波器校正因子(ff)的一个实例。
[0116]
图23a是描绘患者的移动定位图像的示意图。
[0117]
图23b描绘了具有对应于mlc叶的数量和发射位置的数量的行和列的正弦图。
[0118]
图23c描绘了注量移动之前和之后的剂量分布(沿着x-、y-和z-轴,从左到右)。
[0119]
图23d描绘了在注量移动之前和之后90度发射角/位置观察到的剂量分布(沿着x-、y-和z-轴,从左到右)。
[0120]
图24描绘了针对一组发射角的mlc叶指数上的δ函数的注量移动。
[0121]
图25描绘了针对一组发射角的mlc叶指数上的高斯函数的注量移动。
[0122]
图26描绘了针对一组发射角的mlc叶指数上的截断的高斯函数的注量移动。
[0123]
图27-29描绘了定位函数的模拟颜色强度图,该函数是截断的高斯函数,σ-值为2mm。
[0124]
图30-32描绘了定位函数的模拟图,该定位函数是截断的高斯函数,σ-值为4mm。
[0125]
图33是描绘具有滚动校正的虚拟定位的示意图。
[0126]
图34是描绘用于bgrt的具有滚动校正的虚拟定位的示意图。
[0127]
图35a-35c是描绘三种不同的患者治疗计划变体的图。
[0128]
图36a-36b是描绘治疗计划的实例的图。
[0129]
图37a-37n描绘了用于多靶混合定位的图形用户界面。
[0130]
图38a-38e描绘了用于多靶治疗区限定的图形用户界面。
具体实施方式
[0131]
本文公开了用于在单个治疗期或部分中照射多个患者靶区域的治疗计划、患者设置、定位和放射递送的方法。治疗计划方法可以包括为每个靶区域选择计划定位参考点,和基于选择的计划定位参考点为每个靶区域计算平移不变发射滤波器。对于多个靶区域的照射,执行本文描述的方法的治疗计划系统可以生成与每个患者靶区域的计划定位参考点相关联的一组平移不变发射滤波器。任选地,治疗计划系统可以生成表示跨一个或多个患者靶区域、一个或多个oar和/或健康组织的放射注量的计划注量图。在一些变体中,治疗计划系统在患者设置和患者靶区域定位之后不生成供放疗系统执行的一组放疗机器指令,而是可以“实时”发生递送注量图的分割,例如,在治疗期期间,在计算递送注量图的约2小时内、约1小时内、约30分钟内、约10分钟内、约5分钟内、约1分钟内、约30秒内、约1秒内、约0.5秒或更少内等。通过将机器指令分割推迟到治疗期,可以在计算机器指令之前用患者靶区域的最新位置数据(例如,计算递送注量图)更新计划注量图。可以容易地计算移动注量图(例如,线性移动、刚性移动),而“移动”机器指令可能导致影响递送剂量的非线性效应。此外,将机器指令分割至少推迟到患者靶区域定位之后允许“虚拟定位”,其中治疗计划系统生成的注量图根据最新的位置数据进行调整。在一些变体中,虚拟定位可以包括通过将平移不变发射滤波器与从最新位置数据(例如,计划定位参考点的当前位置)导出的定位函数卷积来更新计划注量图。通过在治疗期期间更新定位参考点并基于(例如)以定位参考点为中心的δ函数和该靶区域的一组平移不变发射滤波器计算递送注量图,计划注量图可以“跟随”患者靶区域而不是物理调整患者位置(例如,使用患者平台)以匹配计划注量图。与基于尚未更新以反映患者靶区域的实际位置的注量图递送放射相比,最好地反映患者靶区域的实际位置的分割注量图可以以更好的准确度促进放射递送。虚拟定位方法与bgrt方法(使用期间获取的成像数据,例如正电子湮没发射路径数据,进一步更新递送注量)相结合可能有助于提高向多个患者靶区域递送剂量的准确度。使用本文描述的虚拟定位方法,患者可以被物理地设置和定位一次(例如,对于一个患者靶区域),但是放射可以被施加到虚拟定位的多个患者靶区域。
[0132]
向多个患者靶区域和/或不规则形状的靶区域的放射递送对定位/配准和放射递送提出了挑战。例如,在获取治疗计划图像的时间和患者来到治疗的时间之间,多个肿瘤可能已经以不同的方式(例如,位置、形状和/或大小)发生了变化。一些肿瘤可能会生长,而另一些可能会缩小;一些肿瘤可能向右移动,而另一些则向左移动,等等。如果患者体重减轻或增加(例如,由于肿胀),肿瘤相对于健康组织或骨骼标志的位置可能会发生变化。此外,当在单个治疗期或部分中治疗多个靶区域时,在治疗期的较后部分治疗的靶区域可能已经从它们在治疗期的较早部分(例如,在患者设置和定位开始时,在患者设置和定位期间)的位置移动。运动可能是周期性的(例如由于呼吸)或静态的(例如在多个靶区域的连续治疗期间,待治疗的最后一个靶的定位不太可能有效,因为患者可能在递送期间的某个点移动了位置)。由于向患者递送剂量的高度耦合性质,解决在计划和治疗之间的患者和/或靶区域的变化,以及治疗期期间可能发生的变化具有额外层面的复杂性。施加到一个靶区域的放射可能会为其他靶区域产生散射剂量,并且在某些情况下,放射束可能会与两个靶区域(或一个靶区域和一个oar)相交,并将剂量直接递送到两个区域。如果这些靶区域相对于彼此移动,则治疗计划注量图可能不再递送规定剂量。因此,将与一个或多个肿瘤相关联的整
个靶区域或一批靶区域与用于预期(即未来)放射治疗期的放射治疗系统对齐,例如当护理提供者试图在治疗期开始时定位一个或多个靶时,可能具有挑战性,并可能导致剂量递送不准确。
[0133]
本文描述的治疗计划、定位和放射递送方法可以帮助减轻与在单个治疗期中对多个患者靶区域的治疗相关联的一些剂量递送不确定性。用于向多个患者靶区域进行放射递送的方法的一种变体可以包括个体地(例如,独立于其他患者靶区域)定位(例如,虚拟地定位和/或物理地定位)每个患者靶区域以导出用于每个患者靶区域的递送注量图,然后根据每个患者靶区域对应的递送注量图将放射递送到每个患者靶区域。定位每个患者靶区域可以包括(通过治疗计划期间的治疗计划系统或治疗期开始时的放疗系统)将计划注量图沿着低注量区划分为每个靶区域的注量图子区域,和通过移动注量图子区域,例如,通过使用移动计划注量图的虚拟定位方法来导出递送注量图。替代地或另外地,用于向多个患者靶区域进行放射递送的方法可以包括为每个患者靶区域个体生成计划注量图,个体地(例如,独立于其他患者靶区域)定位每个患者靶区域以导出每个患者靶区域的递送注量图,结合个体递送注量图和确认累积注量图满足规定的剂量目标,并且如果满足剂量目标(即规定的靶区域最小剂量,不超过oar的最大剂量等),则根据每个患者靶区域各自对应的递送注量图将放射递送至每个患者靶区域。用于向多个患者靶区域进行放射递送的bgrt方法可以包括将多个患者靶区域之一指定为配准靶区域,限定其他患者靶区域周围的大到足以包含那些患者靶区域的一系列位置移动的感兴趣区域(roi)(例如,生物发射区(bfz)),定位配准靶区域,和根据与每个患者靶区域的roi在空间上共同定位的成像数据将放射递送至每个患者靶区域。配准靶区域周围的roi可能小于其他患者靶区域周围的roi。
[0134]
任选地,在治疗计划和/或放射递送期间的一个或多个阶段,治疗计划系统和/或放疗系统的系统控制器可以生成并显示一个或多个可视化图形,其指示剂量在患者解剖结构上的沉积。如临床医生或技术人员所期望的,可以响应于可视化图形包括对放射递送的附加改变。提供描绘患者解剖结构上剂量分布的可视化图形,尤其是作为定位/配准程序的一部分或之后,可以帮助临床医生或技术人员评估为每个患者靶区域计算的注量的相互作用,并确定这些累积注量水平是否是可以接受的。例如,如果从一个靶区域到另一个靶区域的散射剂量相对低,或者在空间上是均匀的,则可以忽略计划注量图和递送注量图之间的空间变化的影响。可视化图形可以帮助临床医生或技术人员识别可能由向多个靶区域放射递送引起的热点和/或冷点和/或剂量耦合效应(例如,当放射束与两个或更多个靶区域和/或oar相交时)。在放射递送之前识别这些不需要的剂量相互作用并提供关于剂量分布的空间信息作为对治疗计划和优化过程的反馈可能有助于进一步改善计划注量图和/或发射滤波器。
[0135]
替代地或附加地,患者设置和靶区域定位/配准方法可以包括在图像引导定位程序期间获取一个或多个肿瘤的图像,其在施加放射之前反映关于肿瘤位置、大小和形状的当前信息。用户可以将获取的图像与在程序之前获取和/或准备的治疗计划图像进行比较。用户和/或放射治疗系统然后可以基于所获取图像对放射治疗期进行调整(即,对患者的定位和取向执行设置校正),使得所施加的放射可以更有效地靶向一个或多个肿瘤的当前形状、大小和位置。例如,用户可以在一个或多个肿瘤的图像中限定一个或多个治疗区(本文也称为“地带”和/或“治疗域”)以用于图像引导定位。然后可以为每个感兴趣的治疗区或区
域限定图像匹配或位置校正。在放射治疗系统在对靶区域(例如,肿瘤或肿瘤的一部分)或多个靶区域的照射方面取得进展时,放射治疗系统可以使每个位置校正的应用自动化。放射治疗系统可以向用户提供指示与用户要执行的位置校正动作(例如,移动患者的手臂或腿,或倾斜和/或旋转患者所在的表面)相对应的位置校正或调整指令的指令。在进行位置校正之后,放射治疗系统可以将放射应用于每个感兴趣区域中的肿瘤或肿瘤的一部分的实时或更新位置。此外,通过针对每个感兴趣区域使用患者相对于治疗放射源的最有效定位,而不是以其他肿瘤区域的较低质量适形剂量递送为代价将患者保持在允许某些肿瘤区域的更高质量适形剂量递送的位置,可以更准确地靶向每个感兴趣区域中的肿瘤或肿瘤部分。这可能具有提供更好的治疗结果和治疗计划的整体一致性的益处。此外,由于可以在单个放射治疗期期间治疗多个靶,因此可以减少放射治疗期的持续时间。缩短的时间可以允许护理机构在一天内治疗更多的患者。此外,治疗多个肿瘤或多个肿瘤部分所需的持续时间减少也改善了患者体验。
[0136]
一种用于设置用于放射治疗的患者的方法可以包括获取第一患者靶区域和第二患者靶区域的图像。第一组患者位置移动矢量可以基于所获取图像和第一患者靶区域的治疗计划图像来计算。第二组患者位置移动矢量可以基于获取的图像、第二患者靶区域的治疗计划图像和第一组患者位置移动矢量来计算。可以根据第一组患者位置移动矢量将患者定位到第一位置。可以将患者移动到第二位置并根据第二组患者位置移动矢量定位。
[0137]
应当注意,在本文描述的用于在单个治疗期中照射多个患者靶区域的患者设置、患者靶区域定位/配准和放射递送的方法可以单独或组合用于强度调制放射治疗(imrt)和/或立体定向体部放射治疗(sbrt)和/或bgrt。例如,临床医生可以确定所有患者靶区域都使用imrt/sbrt进行治疗,或者所有患者靶区域都使用bgrt进行治疗,或者某些患者靶区域使用sbrt/imrt进行治疗和其他使用bgrt进行治疗。一些治疗计划系统和/或放疗系统可能具有两种操作模式,其中第一种模式是sbrt/imrt计划和放射递送,和第二种模式是bgrt计划和放射递送。根据需要,单个治疗期可以包括针对某些患者靶区域使用sbrt/imrt方法的放射递送和针对其他患者靶区域使用bgrt方法的放射递送。
[0138]
方法概述
[0139]
虚拟定位
[0140]
患者靶区域的虚拟定位包括修改(例如,移动)特定患者靶区域的计划注量图以反映该患者靶区域的当前/实时位置。计划注量图包括一组放射子束和待施加到患者的子束强度,由治疗计划系统基于一个或多个计划图像计算。在概念上,这可以被认为是调整注量图,就好像定位图像是计划图像一样。与物理患者设置相比,其中患者的位置由患者平台进行物理调整,以使得治疗时的患者靶区域位置与治疗计划期间患者靶区域的位置相匹配,虚拟定位可能需要极少(如果有的话)的患者平台调整。物理患者设置通常包括获取定位图像(例如,定位ct图像、mri图像)、将定位图像与计划图像进行比较以计算表示患者靶区域位置变化的偏移,以及执行患者平台调整和/或以其他方式基于计算的偏移移动患者,使得患者靶区域的当前位置与其在计划图像中的位置对齐。在虚拟定位中,不是调整患者平台,而是通过计算的偏移来调整(例如,移动或滚动)计划注量图,即概念上类似于移动计划图像以与定位图像对齐。还可以包括其他注量修改,以帮助确保患者接收到的所得剂量分布转移到定位图像中的适当位置,而不会出现明显失真,例如,由于放射束的扇形束性质和增
加放射注量更接近放射源所导致的失真。
[0141]
虚拟定位方法旨在通过修改由放疗系统的治疗放射源在定位之后且在患者治疗之前或期间递送的注量图来改变患者接受的剂量。这是通过在治疗计划期间计算治疗计划的平移不变表示(例如,平移不变发射滤波器)并选择适当的定位参考点来完成的。平移不变治疗计划(例如,平移不变发射滤波器)可以应用于从定位图像导出的实际参考点位置以改变患者接受的剂量(并导出可以将放射引导至患者靶区域的当前位置的递送注量图)。平移不变治疗计划表示的一个实例可以包括对于每个患者靶区域的每个发射位置i的一组发射滤波器pi,其中每个发射滤波器是放射源光束-眼睛-视图坐标系中的2d注量图图像(即,对于具有三个患者靶区域和一百个发射位置的情况,治疗计划将计算三组发射滤波器,每组指定100个发射滤波器,每个发射位置一个)。发射滤波器pi可以基于与患者靶区域相关联的计划定位参考点来计算并且在一些变体中可以由用户选择。发射滤波器pi可以通过求解与以每个发射位置的2-d光束-眼睛-视图患者坐标系中的计划定位参考点为中心的离散3-dδ函数δ的2-d投影卷积时的一组滤波器来计算,导致产生每个发射位置i的注量fi[0142]fi
=pi*δi[0143]
其中
[0144]
δi=proji(δ)
[0145]
投影δi可能是2-d离散δ函数(即全零图像,除了值为1的单个像素),因此运算pi*δi可能是发射滤波器pi的2-d移动,可以将其视为与位置无关的注量图。注量fi可以基于由临床医生为每个患者靶区域指定的剂量约束和目标使用标准放疗剂量优化技术来确定,例如,使用梯度下降方法最小化患者剂量的成本函数的技术。任何此类fi可以通过选择所需的计划定位参考点(例如,靶区域中心的点,包括靶区域的治疗区中的点),创建表示向该参考点的移动的δi,和将反向移动应用于fi以获得来分解为卷积pi*δi。计划定位参考点可以位于患者靶区域的肿瘤中(例如,肿瘤的质心或中心部分)或可以处于位于肿瘤外部的解剖结构(例如,附近的骨结构)中。
[0146]
以定位参考点为中心的δ函数δ可表示患者靶区域的位置,并且因此可用于计算将放射引导至患者靶区域的当前位置的移动注量图。在概念上,δ函数δ可以被认为是对在3-d坐标中指定的患者靶区域的位置进行编码。δ函数δ可能包括全零3-d图像,其中无限窄尺寸的单一统一体素以计划定位参考点为中心,但它在发射位置上(例如,治疗放射源的“光束-眼睛-视图”,或多叶准直器空间)的投影δi可由每个多叶准直器(mlc)叶的宽度和/或光束站间距(即,在治疗放射递送期间平台停止的离散患者平台位置之间的间距)限定,并且可以含一个或多个非零体素。投影δi可以是矩阵(或图像),其维度与放疗系统的mlc中的mlc叶的数量和患者平台光束站的数量相匹配。图22a中描绘了基于空间体素及其到发射位置的投影的δ函数的示意图。或者,δ函数δ可能具有在治疗计划期间设置的有限大小。
[0147]
在一些变体中,虚拟定位可以包括将一组滤波器与定位函数进行卷积,定位函数可以包括以定位参考点为中心的δ函数、高斯函数和截断高斯函数。图24-26描绘了可以在本文描述的任何虚拟定位治疗计划和递送方法中使用的定位函数的实例以及它们跨多个发射角或位置的一组mlc叶指数的对应值。图24描绘了δ函数和剂量分布的值。图25描绘了高斯函数和剂量分布的值,并且图26描绘了截断的高斯函数和剂量分布的值。在图24-26中,x轴对应于mlc叶指数并且y轴是一维插值移位(例如,interp1移位,左侧的一组图)和傅
立叶移位(右侧的一组图)的定位函数投影的值或幅度。每条线代表不同发射角和/或位置的定位函数值。对于每个剂量图,x轴对应于以毫米为单位的距离,和y轴对应于注量(例如剂量)。峰间剂量变异是从曲线族中的最高峰到曲线族中的最低峰测量的。
[0148]
图24描绘了四个发射角和/或位置上的定位δ函数投影的值或幅度及其对应的剂量(或注量)分布。一维插值移位的峰间剂量变异约为40%,并且傅立叶移位的峰间剂量变异约为7.5%。图25描绘了在四个发射角和/或位置上的定位高斯函数投影的值或幅度及其对应的剂量(或注量)分布,而图26描绘了四个发射角和/或位置上的定位截断高斯函数投影的值或幅度及其对应的剂量(或注量)分布。如图25和26所示,高斯函数和截断的高斯函数相对于图24中所示的δ函数可以具有更好的峰间特性。高斯函数的峰间剂量变异为11%和1.5%,和截断高斯函数的峰间剂量变异为14%和2.1%(对应地针对线性插值和傅立叶移位)。然而,高斯函数和截断高斯函数具有比δ函数曲线更宽的曲线。更宽的曲线对应于更多的mlc叶,该mlc叶必须打开才能递送注量。也就是说,对于特定的发射角或位置,与δ函数相比,对于高斯函数或截断高斯函数,定位函数的值跨越更多的mlc叶。图26的截断高斯函数提供了优于δ函数的改善的峰间特性,曲线比高斯函数更窄。需要低峰间变异,使得移动注量不会导致显著的剂量差异。结合虚拟定位的治疗计划方法可以包括选择特定定位函数,该函数提供满足每个患者靶区域和/或oar的规定目标的剂量分布。
[0149]
除了在治疗计划期间选择特定的定位函数之外,治疗计划方法的一些变体还可以包括选择定位函数的参数(例如,特性、常数等)。例如,治疗计划方法可以包括选择截断的高斯函数作为定位函数并选择截断的高斯函数的σ-值(例如,宽度)。截断的高斯函数的μ-值(例如,平均值或中心)可以是计划定位参考点。具有不同σ-值的定位函数可能会导致具有不同适形性和/或失真特性的递送注量。例如,选择具有较低的σ-值的定位截断高斯函数可能导致与具有更高的σ-值的类似函数相比具有更好适形性的偏移剂量或注量。图27-29描绘了定位函数的模拟颜色强度图,该函数是截断的高斯函数,σ-值为2mm。图30-32描绘了定位函数的模拟图,该函数是截断的高斯函数,σ-值为4mm。图27-32的图的x轴是发射位置/角度,而y轴是mlc叶指数。图27和30分别描绘了定位函数到2mm和4mm截断高斯函数的每个发射位置的投影。图28和31分别描绘了2mm和4mm截断高斯函数的每个发射位置的发射滤波器值。图29和32分别描绘了2mm和4mm截断高斯函数的每个发射位置的注量值。图30中定位函数(σ-值为4mm)的投影比图27中的定位函数(σ-值为2mm)的投影更宽一些。这可能会导致4mmσ-值定位函数的注量分布(图32)比2mmσ-值定位函数的注量分布(图29)更模糊。然而,对于4mmσ-值定位函数比2mmσ-值定位函数(更失真),跨多个发射位置的注量峰值可能更均匀(失真更少)。。这些不同的注量特性可以在治疗计划期间基于每个患者靶区域和/或oar的临床和/或规定目标进行调整。例如,如图27-32所描绘的,治疗计划系统可以通过迭代和评估不同的定位函数的σ-值来平衡注量适形性和均匀性或失真之间的权衡。
[0150]
在一些变体中,三维图像或二维图像与定位函数(例如,δ函数、高斯函数、截断高斯函数)的卷积可以等效地表示为对三维图像或二维图像的运算,然后由插值算子移动。可以将具有δ函数的移动实现为2-d或3-d图像的线性、傅立叶、双三次插值。对三维图像或二维图像的运算可以通过高斯滤波器或截断高斯滤波器来过滤。
[0151]
应当理解,虽然本文描述的方法的实例和变体可以指δ函数的使用,但是可以替代地使用上述函数中的任何一个,例如高斯函数、截断高斯函数。
[0152]
虽然上述δ函数可以通过定位参考点对患者靶区域的位置进行编码(即,δ函数是定位参考点的3-d坐标的函数),但任选地,虚拟定位方法可以包括对患者靶区域的取向进行编码的第二旋转变换函数。例如,旋转函数r可以是患者平台的俯仰、偏航和滚动的定位函数,其可以表示患者体内患者靶区域的取向。即,虚拟定位方法可以包括两个定位函数:表示患者靶区域的参考位置的第一δ函数和表示患者靶区域的取向的第二旋转变换函数。也就是说,
[0153][0154][0155]
正如可以将移动投影到每个发射角一样,注量图旋转运算也可以投影到每个发射角。3-d旋转运算可能变成注量图的2-d仿射变换(即在3-d中旋转注量图,然后投影到相同的2-d光束-眼睛-视图空间)。实现俯仰和偏航校正的3-d旋转运算可以表示为以下。放疗系统使用的实时递送注量图可以是:
[0156]fi
=ri(δi*pi)
[0157]
对于环形机架放疗系统,可以通过向机架编码器位置添加单个偏移以将计划滚动到患者来实施滚动校正的一个实例。对于多个靶,可能不存在可以实现的可个体滚动每个个体的发射滤波器的单个滚动偏移。可以为具有一组发射滤波器pi的环形机架系统实现的虚拟滚动校正的一个实例,其中i是表示机架周围发射位置的指数,是通过跨发射角度对滤波器进行插值来实现的。具有n
fp
发射位置和旋转角度的放疗系统的一个实例相对于z轴为负且则每个患者靶区域的新的发射滤波器p
′i可能是:
[0158][0159][0160]
其中模函数mod返回环形机架周围的发射位置。如果旋转角度相对于z轴为正,并且则
[0161][0162]
据了解,如果可以使用其他插值算法将滤波器旋转到它们的新位置。在一些变体中,插值算法可包括一种或多种基于傅立叶、双三次和样条的插值算法。上述方法是在投影空间中实现发射滤波器旋转的方法的一个实例,其中发射位置角度θ上的p
′
组可以使用带有δ函数角滚动的圆形卷积来描述,其中:
[0163][0164]
按角度旋转后,新的发射滤波器p
′
可以用来代替以前的滤波器p。这可以赋予与将偏移应用于机架位置编码器以实现滚动校正相匹配的运算顺序。以这种方式计算一组新滤波器的优点是可以将计算出的任何注量加在一起。可以对所有患者靶区域的注量进
行求和,因为它们位于相同的旋转网格上。
[0165]
在一些环形机架放疗系统中,不在等中心的患者靶区域可能经历患者靶区域的虚拟旋转、参考系的旋转和注量的虚拟偏移。图33描绘了imrt/sbrt治疗递送系统的虚拟滚动校正。让δ位于患者靶区域的虚拟旋转中心。
[0166][0167][0168]
对应于自等中心的靶偏移的滚动量。在一些变体中,虚拟滚动校正可以包括通过将整个参考系旋转,使得患者靶区域可以基于患者靶区域的位置旋转和移动,如图33所描绘的。δxandδy可能对应靶的原始位置xy与旋转角度后参考系旋转后的新位置之间的差异。
[0169][0170][0171]
δr
θ
对应于每个治疗放射源(例如直线加速器)位置处的叶偏移量,以将注量移动到新位置的中心。对于扇形束治疗放射源,δw可能对应于靶处叶之间的间距,并且基于到靶的距离d
t
除以直线加速器源与系统等中心之间的距离d
iso
的比率,其中θ对应于环形机架周围发射位置之间的角度。
[0172]
δr
θ
≈(δx cosθ δy sinθ)/δw
[0173][0174]
在一些变体中,叶偏移可以与患者靶区域在放疗系统的旋转平面上的δx和δy的移动量近似相关。远离源的患者靶区域可能具有更大的叶移动。在某些变体中,δr
θ
的更准确的解决方案可以使用卷积运算计算叶偏移来获得。
[0175][0176]
在这个式中,患者靶区域的位置可以被投影到扇形束投影空间中。患者靶区域的位置δ
loc
在其旋转角度后可以在给定的发射位置i投影到扇形束投影空间。通过反演δ函数的投影并将其与患者靶区域的位置进行卷积,该运算可以移动注量。投影的δ函数的反演可以实现为转置δ函数的离散表示。或者,δ函数的反演可以表示δ函数的移位的否定。这种随着旋转的移动实现了围绕任意患者靶区域位置的计划注量的虚拟旋转。
[0177]
其中在具有3-d坐标(x,y,z)的治疗期选择定位参考点,并且俯仰、偏航、滚动和x-、y-、z-位置反映了患者设置的患者平台/床的取向(这可能与治疗计划期间患者平台的预定方向相对应)。在位置和取向上定位患者靶区域可能会相应地移动发射位置i的递送注量:
[0178]fdelivery,i
=δ
delivery,i
*p
′i[0179]
其中δ
delivery,i
是δ
delivery
在发射位置i上的投影,和p
′i是发射滤波器p
′
在发射位置i上的投影。
[0180]
图34描绘了用于bgrt治疗递送系统的虚拟滚动校正的示意图。对于患者靶区域的虚拟滚动,每个发射位置i处的注量可以是滚动与递送注量移动的组合。
[0181][0182]
δ
′
delivery,i
=δ
delivery,i
*δi(δr)
[0183]fdelivery,i
=δ
′
delivery,i
*p
′i[0184]
平移不变发射滤波器pi由治疗计划系统基于计划定位参考点针对特定患者靶区域计算,治疗时该患者靶区域的虚拟定位可以包括获取处于治疗位置(例如,定位或设置在患者平台上)的患者的定位图像,在图像中识别患者靶区域,选择与计划定位参考点对应的定位参考点,以及通过基于定位参考点计算δ函数δ
local
来计算在每个射击位置的递送注量f_deliveryi,并将δ函数与平移不变发射滤波器pi卷积:
[0185]
f_deliveryi=pi*δ_locali[0186]
其中
[0187]
δ_locali=proji(δ
local
)
[0188]
将发射滤波器与以定位参考点为中心的δ函数卷积具有移动(例如,移位)计划注量图以反映患者靶区域的当前位置的效果。在计算递送注量之后,放疗系统控制器然后可以将递送注量分割成机器指令(例如,mlc配置、治疗放射源参数等),然后可以执行以递送规定的注量。虚拟定位和机器指令分割可以在治疗期期间发生,并且优选地实时发生。这与其他治疗计划和放疗系统形成对比,在其他治疗计划和放疗系统中,机器指令是在治疗计划阶段期间而不是在治疗期期间计算的,这导致一组机器指令将放射递送到计划图像中患者靶区域的位置,而不是患者靶区域的当前位置。在sbrt/imrt放射递送的情况下,在虚拟定位和分割之后,放疗系统然后可以通过按照新分割的机器指令继续向患者靶区域递送规定的注量。在bgrt放射递送的情况下,感兴趣的区域或roi(例如,生物发射区或bfz)可以使用虚拟定位来调整(例如,移动),并且递送注量图可能不会被分割成机器指令,直到递送注量图已使用在治疗期期间获得的成像数据(例如,正电子湮没发射路径数据)进一步更新之后。例如,在治疗放射束的递送之前大约500ms,放疗系统可以用在500ms窗口中获取的成像数据更新递送注量,然后就在递送之前分割递送注量。在多个患者靶区域将在单期中被照射的情况下,每个患者靶区域的虚拟定位可以在治疗期开始时以单批执行和/或在整个治疗期依次执行(例如,定位第一患者靶区域,将递送注量分割成机器指令,并照射第一患者靶区域,定位第二患者靶区域,将递送注量分割成机器指令,并照射第二患者靶区域,等等)。
[0189]
当移动注量图以反映患者靶区域的当前位置时,一些定位方法可能会考虑并补偿移动注量图的一个或多个物理效应。实例包括mlc叶舌槽(t&g)效应、非平坦治疗光束效应,以及作为距治疗放射源距离的平方反比的治疗光束强度衰减效应。任选地,为了计算说明一个或多个这些效应的递送注量图,定位函数(例如,δ函数、高斯型函数)与发射滤波器的卷积可以与附加因子进行卷积。为补偿非平坦治疗光束(即,光束强度在iec-x和iec-y方向上跨照射场变化,其中场的中心部分比场的边缘具有更大的光束强度),虚拟平坦滤波器校正因子(ff)可以应用于每个投影,其中虚拟平坦滤波器校正因子是矩阵,它是治疗放射源光束沿mlc叶尺寸的光束强度平坦度分布的倒数:
[0190]
(fi)=ff
·
(pi*δi)
[0191]
虚拟平坦滤波器校正因子(ff)矩阵可以是二维矩阵,行数与mlc叶数相匹配,并且列数与患者平台光束站数相匹配。图22b描绘了用于具有64个mlc叶和20个患者平台光束站
的放疗系统的虚拟平坦滤波器校正因子(ff)的一个实例。
[0192]
计算递送注量图以补偿距治疗放射源的距离的平方反比光束强度降低可以包括在递送注量计算中应用距离补偿比例因子
[0193][0194]
其中di表示在治疗计划期间确定的从发射位置i到患者靶区域的中心(例如,靶区域质心)的距离,并且d
′i表示从发射位置i到基于定位图像在放射递送时确定的患者靶区域的中心(例如,靶区域质心)的距离。
[0195]
考虑非平坦治疗光束和平方反比光束强度降低的递送注量图可以如下计算:
[0196][0197]
本文所述的虚拟定位方法可用于在单个治疗期或部分中对多个患者靶区域进行照射。用于在单个治疗期中照射多个患者靶区域的方法可以包括为每个患者靶区域限定患者区域或治疗区(例如,由治疗计划系统限定,有或没有用户输入),根据本文描述的步骤为每个患者治疗区选择用于虚拟定位的定位参考点,然后根据通过虚拟定位为每个患者治疗区计算的递送注量图发射治疗放射束。患者治疗区可以包括针对单个物理设置和定位而被照射的患者区域。例如,治疗区可以是针对平台上的特定患者位置(例如,沿平台的位置、诸如手臂位置的患者位置等)和iec-y中的一组平台位置而被照射的患者区域。物理设置和定位可以包括患者的独特激光对齐和/或获取定位图像(例如ct或mri或pet图像)、患者位置(例如,手臂抬起、手臂放下、腹部按压、屏气等),和/或一个或多个患者平台调整中的一种或多种,以便患者位置与治疗计划期间的位置相匹配。患者治疗区可以跨越针对特定物理设置和定位而被照射的患者区域。每个治疗区可能有自己的物理设置和定位。在一些变体中,患者治疗区可以由iec-y中跨越患者的受照射区域的一组患者平台位置表示。例如,可以将获取的图像和/或治疗计划图像分为第一治疗区和第二治疗区。每个治疗区可以包括一个或多个患者靶区域,使得可以将获取的图像中的一个或多个患者靶区域与治疗计划图像中的一个或多个对应的患者靶区域进行比较。每个治疗区可以对应于患者的一部分,一个或多个患者靶区域位于该部分内,当在放射治疗期的特定部分期间根据特定设置定位患者时,该部分将被照射。治疗区可映射到一系列患者平台位置或阶段(例如,光束站)和/或一系列患者平台沿其纵轴的运动,其中该治疗区中的一个或多个靶区域与治疗放射源的放射束相交。治疗区可以对应于特定的患者位置和/或平台取向。例如,第一治疗区可以与用于照射第一治疗区内的第一患者靶区域的第一患者位置和取向相关联,并且第二治疗区可以与用于照射第二治疗区内的第二患者靶区域的第二患者位置和取向相关联。因此,在一些实施例中,第一治疗区可以与放射治疗期的第一部分(例如,通过第一组光束站移动患者平台),第一患者靶区域和患者的第一位置相关联,并且第二治疗区可以与放射治疗期的第二部分(例如,通过第二组光束站移动患者平台),第二患者靶区域和患者的第二位置相关联。
[0198]
任选地,所限定的患者治疗区的中心区域可以彼此对齐(例如,沿着“等值线”),使得在针对每个患者治疗区发射治疗放射之间,无需调整患者位置(除了纵向iec-y向每个患者平台光束站运动,使得iec-x和iec-z是固定的)。这可以帮助减少用户在治疗期期间进入治疗掩体的发生率,这会显著增加总治疗时间。例如,第一治疗区的中心和第二治疗区的中心可以沿着iec-y轴共线和/或与iec-y轴共面。在一些变体中,第一治疗区和第二治疗区可以重叠,而在其他变体中,治疗区可以不重叠。质心可以在同一平面中沿着iec-x(例如,沿着“等值线”)。治疗区的中心不一定是靶的中心。
[0199]
每个患者靶区域(或患者靶区域组)的定位参考点可以不同于治疗区的中心区域或点。在一些变体中,可以基于某些临床标准来选择在治疗计划期间限定的治疗区(例如,计划的患者治疗区)。例如,不同轴向平面中的靶区域可以被分成不同的计划患者治疗区,和/或与另一个靶区域分开超过约5-10cm的靶区域可以被分成不同的计划患者治疗区。在治疗计划期间,可以使用本文描述的方法计算共享定位参考点的每个患者靶区域和/或患者靶区域组的一组平移不变发射滤波器,使得如果需要的话,患者靶区域的虚拟定位可以在治疗期期间单独进行。根据每个计划的患者靶区域的递送注量图的治疗放射束的发射可以依次执行,并且在一些变体中,在将放射递送到下一个患者治疗区中的患者靶区域之前可以包括单独的、物理的患者设置(例如,通过调整患者平台的取向)。替代地或附加地,每个患者靶区域的递送注量图可以并行递送,例如,在一起分割并且在靶区域之间没有任何物理患者设置的情况下递送(除了使患者平台沿着纵轴即iec-y通过离散光束站位置步进)。对于其中一个或多个患者靶区域将接受bgrt放射递送并且这些bgrt患者靶区域已使用虚拟定位进行定位的治疗期,将虚拟移动应用于roi。结合了一个或多个bgrt靶的虚拟定位的治疗计划方法可以包括为bgrt患者靶区域选择计划定位参考点,限定患者靶区域周围感兴趣的区域(roi)(例如,生物发射区(bfz)),和基于roi和包括患者靶区域的计划引导图像(例如,计划pet图像、mri图像等)计算平移不变发射滤波器(例如,放射激发矩阵(rfm)或放射发射滤波器)pi。roi可以是限定患者区或区域的空间掩模或滤波器,该患者区或区域可以包括患者靶区域和患者靶区域周围的边缘。例如,roi可以包括肿瘤区域(或任何患者靶区域),并且肿瘤区域周围的边缘可以考虑肿瘤区域的位置估计误差、和/或肿瘤区域的移动、和/或发射递送期间肿瘤区域的可能位置,和/或肿瘤区域的几何变化。在治疗期期间,放疗系统可以获取与该bgrt靶区域的roi相交和/或共同定位的成像数据(例如,正电子湮没发射路径数据或lor数据(在患者已注射pet示踪剂的情况下)、spect数据(在患者已注射spect示踪剂的情况下)、γ放射数据、mri数据、ct数据和/或x射线数据)。不与roi相交或含有与位于roi之外的结构有关的数据的成像数据不包括在递送注量图的计算中。以此类方式,roi用作空间掩模或滤波器,其可以应用于在治疗期期间获取的成像数据。
[0200]
结合虚拟定位和bgrt递送的放射递送方法可以包括在包括bgrt患者靶区域和roi的治疗位置获取患者的图像,在所获取图像内选择定位参考点,通过基于定位参考点计算δ函数并将δ函数与roi进行卷积来调整roi,通过将成像数据与发射滤波器进行卷积来计算在治疗放射源的每个发射位置处用于递送至患者靶区域的注量,和继续发射递送注量:
[0201]
(fi)=(pi*proji(x
·
(roi*δ
i,delivery
)))
[0202]
其中x是获取的附加成像数据(例如,部分成像数据、限时获取的成像数据、正电子湮没发射路径数据、mri数据、spect数据、γ数据、ct数据和/或x射线数据),和pi是发射滤
波器(也称为bgrt发射滤波器或放射激发矩阵),与虚拟定位使用的滤波器相反。在这种情况下,虚拟定位将roi移动δ
delivery
。额外获取的成像数据可以由roi在空间上过滤(或掩蔽),使得只有与调整的roi共同定位的成像数据可以用于计算递送注量。
[0203]
对于bgrt,当任选地随时应用滚动校正时,滤波器pi旋转,roi可以旋转相同的度数。一个实例是实现2-d旋转函数,其沿z为每个平面在适当位置旋转roi掩模。在植入滚动校正时,运算顺序可能是重要的,并且在这个实例中,首先应用滚动校正,然后通过虚拟偏移平移:
[0204][0205][0206][0207]
现在旋转发射滤波器以匹配新的参考系:
[0208][0209]
给定发射位置的注量fi现在是成像数据的投影,被旋转和移动的roi掩盖,被虚拟偏移δ
delivery
移动,投影到给定的发射角i并且与一组旋转滤波器p
′i卷积:
[0210]
(fi)=(p
′i*proji(x
·
(roi
′
*δ
delivery
)))
[0211]
roi
′
=δ(δx,δy)*rot(roi,θ
roll
)
[0212]
(fi)=(pi*proji(x
·
(roi
′
*δ
delivery
)))
[0213]
任选地,考虑非平坦治疗束和bgrt靶区域的平方反比光束强度降低的递送注量图可以如下计算:
[0214][0215]
根据需要,可以在单期中依次地和/或并行地将治疗性放射递送至bgrt靶和/或sbrt/imrt靶。
[0216]
任选地,在已计算平移不变发射滤波器之后的治疗计划期间,可以计算显示患者靶区域体积上的最小和最大剂量值的有界剂量体积直方图曲线(bdvh),其中考虑到由于患者靶区域移动引起的可能剂量变化。在治疗计划期间和/或在患者设置和/或靶区域定位期间输出可视化图形,例如bdvh或本文所述的任何可视化图形可以帮助用户评估治疗计划是否适合患者(例如,在治疗当天)。
[0217]
在多靶虚拟定位之后,每个患者靶区域可以具有耦合在不同患者治疗区之间的剂量分量。这种剂量耦合可能是额外的注量束与多个患者靶区域相互作用的可能性的结果。一旦知道一组虚拟定位,就可以计算患者靶区域、oar和/或治疗区的剂量。一组归一化系数可以应用于每个患者靶区域和/或治疗区,以确保满足某些剂量测定目标,或者替代地,某些oar剂量受到约束。为来自一组n个定位中的每个imrt/sbrt虚拟多定位j实现这些系数的一个实例,可以求解每个定位的系数βj以归一化所有虚拟定位的联合效应(例如,整个治疗计划中的所有虚拟定位,每个治疗区中的所有虚拟定位)。联合求解的一个此类实例是最小化与每个患者靶区域和/或治疗区相关联的剂量测定标量的均方和dj。是在计划靶区域j时计算的剂量测定标量。
[0218]
对于imrt/sbrt:
[0219][0220]
对于bgrt:
[0221][0222][0223]
剂量测定标量dj可以是以下任何一项:ptv的平均剂量、ptv的百分位剂量、ptv的最大值。替代地,这个剂量测定标量dj可以基于与靶区域相关的oar剂量的函数。可以使用其他凸最小化算法来代替均方误差,例如加权最小二乘法。
[0224]
虽然上文和本文描述的一些虚拟定位方法使用从定位参考点导出的δ函数并将该δ函数与平移不变发射滤波器进行卷积,但应当理解,虚拟定位方法包括基于患者平台或床的俯仰、偏航和滚动的患者靶区域对患者靶区域的取向进行编码的其他定位函数。例如,本文描述的虚拟定位方法可以包括在可以在治疗期期间选择的定位参考点上使一组滤波器与定位函数卷积,该定位函数包括δ函数、高斯函数和截断的高斯函数。
[0225]
马赛克多靶定位
[0226]
如上所简单描述的,在单个治疗期中治疗多个患者靶区域的挑战之一是适用于一个患者靶区域的定位/配准可能不适合其他患者靶区域。用于多个患者靶区域的定位/配准的方法可以包括分别定位/配准每一个(例如,使用其中计划注量图移动的虚拟定位方法和/或使用利用平台移动患者的物理定位方法)。例如,治疗期可以包括针对患者靶区域的一个物理定位/配准以及针对其他患者靶区域的一个或多个虚拟定位。通过虚拟定位,可以照射多个患者靶区域,而无需物理移动和/或改变患者位置来定位每个靶区域。在可以针对所有患者靶区域计算和优化治疗计划的变体中,即指定每个患者靶区域的3-d注量的单个治疗计划,“全局”治疗计划(例如,“全局”注量图)可以划分为离散的子区域。基于单个定位图像,可以在多靶治疗计划中独立定位或配准每个子区域中的靶。通常,治疗计划注量图可以包括位于靶区域上(例如,与靶区域共同定位)的高注量区域和几乎其他任何地方的低注量区域。这些低注量区域可以被称为低注量带或界限区域。一种用于治疗计划的方法可包括生成具有与由低注量区域或低注量带包围或界定的靶区域共同定位的高注量区域的全局治疗计划或全局注量图,并且可进一步包括将全局治疗计划或注量图划分为由低注量区域包围或界定的子区域。在概念上,全局治疗计划可以沿着这些低注量带的中心“切割”,并分成在每个靶区域周围的离散区域。这些治疗计划注量图子区域或“马赛克”可以在治疗期开始时使用定位图像独立地移动和定向在每个目标周围。而计划注量图子区域移动可能会导致相邻子区域的低注量界限区域的注量重叠(即界限区域可能在照射两个或更多个相邻子区域的靶区域期间接收注量),这些界限区域中的低注量水平可以在治疗计划期间指定为足够低以使得该注量重叠不是临床关注的。在治疗计划期间,可以将低注量界限区域限
定为足够宽以使得可以容纳的重叠量足够大,从而可以解决所有定位/配准误差源。在一些变体中,可以在治疗计划期间添加调整结构和/或约束以获得期望的低注量界限区域。在独立注量图子区域中定位个体患者靶区域之后,可以将每个子区域的递送注量图分割成机器指令以供放疗系统执行。放射可以连续地和/或同时地递送到多个局部患者靶区域或注量图子区域。例如,一些患者靶区域或注量图子区域可以依次照射,而其他患者靶区域或注量图子区域可以与其他患者靶区域或注量图子区域同时照射。包括所有患者靶区域的单个定位图像可用于定位/配准每个患者靶区域或多个定位图像(例如,每个患者靶区域或注量图子区域一个定位图像)。例如,在治疗期期间,每个治疗区可能存在一个物理定位(如计划期间所限定),以及治疗区内一个或多个患者靶区域可能存在一个或多个虚拟定位。马赛克定位方法可用于sbrt/imrt递送和/或bgrt递送,并任选地与其他定位方法和患者设置方法结合使用(例如,结合移动患者平台、虚拟定位方法、刚体多定位方法,其中基于定位图像通过平台将“最佳拟合”移动应用于患者)。
[0227]
混合马赛克多靶定位
[0228]
任选地,当全局计划注量图被划分为计划注量图子区域时,在马赛克定位的治疗计划期间,该方法可以包括指定使用sbrt/imrt方法(例如,指定为sbrt/imrt靶区域)还是使用bgrt方法(例如,指定为bgrt靶区域)治疗每个注量图子区域中的患者靶区域。可以基于为所有靶区域选择的计划定位参考点来计算平移不变发射滤波器,如本文针对虚拟定位所描述的。任选地,可以为每个患者靶区域计算bdvh曲线,这可以包括生成bgrt靶区域和/或sbrt/imrt靶区域的所有潜在移动的一系列模拟。bdvh曲线可以在计划时由临床医生审查和批准。一种用于混合马赛克多靶定位的方法可以包括获取多个sbrt和bgrt靶区域的大体积ct(例如,单个大体积ct),基于ct定位图像为每个患者靶区域描绘一组患者平台调整(例如,6dof校正),和为每个患者靶区域选择定位参考点。为了定位/配准特定的患者靶区域,可以首先根据描绘的患者平台调整组移动患者平台,并且可以使用应用于该患者靶区域的选定定位参考点的虚拟定位技术来计算递送注量图。对于bgrt递送,可以结合获取定位图像来获取pet预扫描。基于pet预扫描,可以恰好在激活治疗放射源以照射bgrt靶区域之前计算bgrt靶的预测剂量,这可能有助于确保实际定位和pet预扫描图像在预先批准的剂量界限内。bgrt和sbrt/imrt靶区域的实时递送注量图可以平滑地组合在一起,并在运行中(即递送前的几分钟或几秒)分割成机器指令。在光束站递送中,其中患者平台在纵向位置保持静止,而治疗放射源在患者周围移动以递送计算的注量,特定光束站处的bgrt和sbrt/imrt靶区域的递送注量图可以添加在一起,并且当平台停在光束站时,一起分割成机器指令。以此方式,可同时递送多个bgrt和sbrt/imrt靶区域的递送注量。
[0229]
解耦多靶定位
[0230]
用于在单个治疗期中治疗多个患者靶区域的方法可以包括为每个患者靶区域计算个体治疗计划(即,指定个体患者靶区域的3-d注量的个体计划注量图),而不是计算全局治疗计划(即,指定每个患者靶区域的3-d注量的全局注量图)。在一些变体中,用于解耦定位的治疗计划的方法可包括计算每个靶区域的个体治疗计划而不考虑其他靶区域的存在,但考虑oar和/或其他关键结构的存在和位置,将个体治疗计划组合在一起形成组合治疗计划,同时仍将个体计划保持为单独的实体,限制组合计划不允许个体计划中的高注量区域与其他高注量区域重叠,并且还满足剂量覆盖、oar的剂量限制等的原始目标。约束组合治
疗计划可以创建计划的全局注量图,该图具有围绕每个患者靶区域的低注量区域或带,使得治疗计划可以容纳一些独立的靶区域运动。在一些变体中,可以在治疗计划期间添加调整结构和/或约束以获得期望的低注量界限区域。组合治疗计划(即,计划的全局注量图)可以在治疗之前由临床医生审查和批准。
[0231]
用于解耦多靶定位的治疗计划方法的一个实例可以包括生成用于照射第一治疗区中的第一患者靶和第二治疗区中的第二患者靶区域的治疗计划,将治疗计划划分为用于以第一规定剂量照射第一治疗区中的第一患者靶区域同时将oar的照射限制在低于第一剂量量的第一治疗计划和用于以第二规定剂量照射第二治疗区中的第二患者靶区域同时将oar的照射限制在低于第二剂量量的第二治疗计划,组合第一和第二治疗计划以生成联合治疗计划,和迭代修改组合治疗计划以满足所需的剂量目标和约束。剂量目标和约束的实例可以包括防止组合治疗计划中的热点或冷点。第一治疗计划可以包括向第一患者靶区域递送第一规定剂量的优化放射束,并且第二治疗计划可以包括向第二患者靶区域递送第二规定剂量的优化放射束。作为个体(例如,第一和第二)治疗计划的结果的对oar的剂量量或水平可以被设置为最大剂量量的某个比例。例如,来自第一治疗计划的对oar(例如,位于第一和第二治疗区之间或跨越这两者的oar)的第一剂量量可以是最大剂量水平的35%,并且来自第二治疗计划的对oar的第二剂量量可以是最大剂量水平的65%。第一和第二治疗计划对oar剂量的具体贡献值可以基于组合治疗计划中的目标评估基于联合优化内的迭代计算或通过不同贡献水平的一系列单独优化来动态设置直到达成可接受的计划。在修改组合治疗计划以满足所需剂量目标和约束之后,可以将其划分为第一和第二治疗计划,但具有用于递送的优化光束和/或注量。在一些实例中,组合治疗计划可以包括计划注量图,并且第一治疗计划可以包括第一注量子图并且第二治疗计划可以包括第二注量子图,其中第一注量子图和第二注量子图结合形成计划注量图。
[0232]
任选地,在一些变体中,用户可以选择一个患者靶区域作为比另一个更高的优先级。例如,如果用户将第一患者靶区域的照射限定为比第二患者靶区域的照射更高的优先级,则治疗计划方法可以包括将治疗计划划分为用于以第一规定剂量照射第一治疗区中的第一患者靶区域的第一治疗计划和用于以第二规定剂量照射第二治疗区中的第二患者靶区域的第二治疗计划,同时将oar的照射限制在低于选定剂量量,组合第一和第二治疗计划生成组合治疗计划,以及迭代修改组合治疗计划以满足所需的剂量目标和约束。在该方法中,第一治疗计划可以具有比第二治疗计划更少的剂量约束(例如,没有oar剂量约束),使得第一治疗计划包括被优化用于向第一患者靶区域递送规定剂量的光束,很少或根本不考虑oar的剂量。第二治疗计划然后可以将第一治疗计划递送的剂量考虑为“先前剂量”,其约束其光束优化以将剂量递送至第二患者靶区域。
[0233]
在治疗期期间,可以使用一个或多个定位图像(例如,通过调整患者平台或改变放疗机器指令使用典型的定位方法,和/或使用本文描述的虚拟定位方法)来个体地定位个体患者靶区域。在定位所有患者靶区域之后,可以将每个患者的递送注量图组合在一起以确认任何“重叠”剂量区域是否超过任何约束。如果满足所需剂量约束,则放疗系统可以将递送注量图分割成机器指令并继续向患者靶区域递送治疗放射。延迟将递送能量图的分割或翻译成放疗系统指令,以便分割发生尽可能接近递送,允许放疗系统更新递送注量以反映患者靶区域的实际位置(和/或位置的任何变化),从而导致更准确地递送总规定剂量。
[0234]
生物引导放疗(bgrt)定位
[0235]
正如简要描述的那样,bgrt是一种放射递送方法,它使用在治疗期期间获取的成像数据更新递送注量,并在获取成像数据的几分钟或几秒钟内发射治疗性放射。由于bgrt的低延时特性,用于更新递送注量的成像数据可能相对稀疏(例如,在短或有限的时间窗口内收集的“部分图像数据”不足以进行完整的图像重建)和/或有噪声(例如,具有不允许可靠确定患者靶区域质心的信噪比)。例如,在bgrt中,用于更新或计算递送注量图的成像数据可以包括包含一个或多个响应线(lor)的部分pet图像、包含k空间中的子采样的部分mri图像,和/或一个或多个x射线投影图像。虽然本文中的实例是在pet成像模式的上下文中描述的,但应当理解,可以单独或与pet成像模式结合使用任何其他成像模式。成像数据可在有限时间窗口内获取,该时间窗口可为例如约3秒或更少、约2秒或更少、约1秒或更少、约500ms或更少、约300ms或更少、约200ms或更少,等等。由于图像获取和放射递送之间的低延时(例如,约10秒或更少、约5秒或更少、约3秒或更少、约1秒或更少、约500ms或少),放射可以在靶区域移动之前递送到靶区域。可以在每个bgrt靶区域周围限定roi(例如,生物发射区或生物靶区),其代表用于确定使用什么lor来引导靶处的注量的体积。也就是说,roi可以是可以应用于lor的空间滤波器或掩模;如果检测到的lor与roi相交,则在bgrt递送算法中使用它来更新递送注量,否则它将被忽略。较小的roi可能是优选的,因为它可以减少在roi中包括不是靶的渴求pet组织的机会(roi中的任何渴求pet组织将被治疗,如同它是靶一样)。
[0236]
用于基于bgrt的多靶定位的方法可以包括将bgrt靶区域之一指定为配准靶区域,并在另一个周围限定足够大的roi,以包含那些患者靶区域的位置移动范围。在一些变体中,配准靶区域的roi可能小于其他bgrt靶区域的roi。在一些变体中,配准靶区域可以是最接近关键结构或oar(例如,诸如心脏的渴求petoar)的bgrt靶区域。在治疗期期间,只要配准靶区域的roi被定位/配准,并且其他bgrt靶区域在其roi内(可能更大或扩大以考虑相对于配准靶区域的空间定位的预期变化),放疗系统可以使用bgrt方法进行递送放射(即,通过将获取的空间滤波成像数据与平移不变的放射激发矩阵或发射滤波器进行卷积计算递送注量,然后分割成机器指令立即执行)。较大roi对剂量适形性的影响可以在治疗计划时计算和审查,并且可能被塑造或设计成帮助减少包括额外渴求pet组织的可能性,同时帮助增加计划和递送之间空间差异可被容纳的可能性。基于bgrt的定位可以任选地与其他定位方法和患者设置方法结合使用(例如,结合移动患者平台、虚拟定位方法、刚体多定位方法,其中基于定位图像通过平台将“最佳拟合”移动应用于患者)。
[0237]
本文所述的任何多靶定位和放射递送方法可以单独使用或与通常用于单个患者靶照射和/或在多个治疗期照射多个靶区域的定位和递送方法组合使用。例如,本文描述的任何计划、定位和递送方法可以与物理患者设置(例如,以连续方式,每个患者靶区域或治疗区一个物理患者设置)、刚体多定位、治疗计划变形、稳健的治疗计划(在优化过程期间考虑位置不确定性并创建不随位置变化而发生强烈变化的计划的治疗计划),和/或在线治疗计划适应(基于定位图像生成新的治疗计划)组合使用。在连续配准和治疗中,每个患者靶区域都被独立定位和治疗,一个接一个。定位后的立即治疗可能有助于降低治疗期间静态患者移动的可能性,然而,可能需要针对每个定位实例获取多个定位图像(例如,多个kvct图像)。用于连续配准和治疗的治疗计划可以包括联合优化跨多个患者靶区域的注量图和/
或可以被优化以在单独定位时对每个肿瘤的个体移动具有稳健性。刚体多定位可以包括获取定位图像,然后计算定位图像相对于最小化跨所有靶区域和/或oar的总配准误差的函数的计划图像的单次移动(即,执行“刚体”配准)。原始治疗计划中每个靶区域周围的边缘可能会被扩大以考虑这些预期的配准误差。治疗计划中的靶和oar可以作为刚体移动和定向,以找到到定位图像中靶和oar实际位置的“最佳”映射。用户可以选择考虑同等权重的所有配准误差,并最小化总配准“误差量”,或者替代地,他们可以选择将某些靶区域或oar加权为比其他更重要,并寻求更好地对齐那些靶,代价是更大的配准误差或其他地方增加的肿瘤边缘。
[0238]
例如,马赛克多靶定位和基于bgrt的定位可以与上述一种或多种方法相结合。预期多靶治疗计划中的一些靶可能会像刚体(例如与同一骨骼相关联的靶区域)一样移动更多,因此可以组合在一起并使用刚体方法进行配准,而可以使用马赛克多靶或基于bgrt的定位来配准其他患者靶区域。在治疗计划期间可以使用稳健性算法以帮助确保对每个治疗计划或注量图子区域进行的空间调整引入最小量的剂量变异。稳健计划还可与基于bgrt的虚拟定位结合使用,以优化每个患者靶区域的roi的形状和位置。也可能需要使用马赛克多靶或基于bgrt的定位技术配准患者靶区域,然后将软组织变形方法应用于每个子区域或靶区域。这可能有助于减少必须考虑的组织变形量,从而有助于减少软组织方法引入的剂量变异。替代地或附加地,可以使用马赛克多靶定位方法来减少在线治疗计划适应的计算负担。例如,可以使用马赛克多靶定位方法基于计划注量图配准患者靶区域,然后可以个体调整每个患者靶区域的注量图。在又一个实例中,bgrt治疗计划可以结合来自马赛克多靶定位方法的治疗计划步骤,这可以帮助减小每个靶区域的roi的大小。
[0239]
在另一个变体中,针对多个患者靶区域的治疗计划可以包括多个治疗区,其中可以针对每个治疗区对患者进行物理设置/定位。每个治疗区可具有一个或多个肿瘤或患者靶区域(例如,roi)。在治疗期期间,可以针对第一治疗区物理地设置/定位患者,并且放射治疗系统可以虚拟地定位第一治疗区内的每个患者靶区域。例如,物理定位可以为第一治疗区中的第一患者靶区域提供适当的定位,然后放射治疗系统使用本文描述的虚拟定位方法调整治疗区中的其他患者靶区域的注量。可以根据在治疗期期间从定位图像中选择的定位参考点来计算或调整递送注量。对第一治疗区中的患者靶区域的照射可以连续和/或并行执行。在第一治疗区已被照射之后,然后可以针对第二治疗区对患者进行物理设置/定位(例如,沿着iec-y移动患者平台),并且放射治疗系统可以虚拟地定位在第二治疗区内的每个患者靶区域。可以如上文针对第一治疗区所述的那样照射第二治疗区中的患者靶区域。第一和第二治疗区在一些变体中可以重叠并且在其他变体中可以不重叠。
[0240]
用于多靶治疗计划、定位和放射递送的方法可以任选地包括生成一个或多个可视化图形,其可以输出到显示设备(例如,监视器)。可视化图形可以包括多个患者靶区域中的每一个的剂量体积直方图(dvh)或有界剂量体积直方图(bdvh),使得用户可以被告知可以将剂量递送到患者靶区域。然而,dvh和bdvh曲线不提供有关不同靶区域的注量图之间的空间相互作用的信息。例如,当在定位期间移动和/或更新注量图时,先前在治疗计划期间未重叠的注量区可能在治疗期期间重叠。在马赛克定位中,注量图子区域可以单独定位和移动,并且在解耦定位中,不同患者靶区域的个体注量图也可以单独定位和移动。一些重叠区可能包括两个或更多个个体注量图或注量图子区域的低注量区,因此重叠区中的累积注量
可能不会超过非靶组织的剂量安全阈值,但是,在某些情况下,此类注量重叠可能会超过剂量安全阈值和/或可能共同定位在oar上。可视化图形可以基于定位数据(例如,移动的注量图或注量图子区域、定位参考点、定位图像等)生成并输出到显示设备以帮助用户评估多个患者靶区域的单独定位的剂量影响,和/或帮助识别由于这些定位注量图移动而导致的任何不需要的剂量测定效应。可视化图形可以帮助用户更好地理解靶间相互作用并编码空间信息以评估剂量递送的不确定性。
[0241]
一些可视化图形可基于bdvh曲线和计算来计算,并且可参考bdvh曲线的界限:标称剂量(dn),可能最小剂量(d
pmin
)和可能最大剂量(d
pmax
)。可视化图形可以描绘2-d切片和/或3-d渲染中某些解剖结构上某些剂量分布和水平的概率的表示。电影或短动画也可以描绘最小、标称和最大剂量水平,以便可以在这些水平之间进行视觉比较。与标称剂量(例如,δ剂量)的差异或波动可以向用户提供视觉工具以识别热点和冷点。
[0242]
多靶治疗计划方法
[0243]
需要时,用于在单个治疗期中治疗多个患者靶区域的治疗计划方法可以包括计算各种注量图(例如,所有患者靶区域和/或oar的全局注量图、包括靶区域和/或oar的子组的注量图子区域)、发射滤波器(例如,平移不变发射滤波器)、空间滤波器(例如,用于成像数据、感兴趣区域或roi、生物发射区或bfz、生物靶区的空间过滤)。用于在单个治疗期中治疗多个患者靶区域的治疗计划方法可以包括计算每个患者靶区域的一个或多个平移不变发射滤波器以进行虚拟定位,和/或计算由马赛克多靶定位的低注量带划分的注量图子区域,和/或为每个患者靶区域生成单独的治疗计划或注量图,和约束用于解耦多靶定位的累积注量图。用于治疗一个或多个bgrt患者靶区域(单独或与一个或多个sbrt/imrt患者靶区域组合)的bgrt治疗计划方法可以包括将一个bgrt患者靶区域指定为配准靶区域并限定另一个bgrt患者靶区域的roi以适应配准靶区域的运动和其他靶区域运动。用于治疗sbrt/imrt和bgrt患者靶区域的治疗计划方法(例如,混合马赛克多靶定位)可以进一步包括指定患者靶区域是bgrt靶区域还是sbrt/imrt靶区域。
[0244]
本文描述的治疗计划方法可以单独使用或组合使用以制定适合特定患者的多靶治疗计划。一些临床医生或诊所可以配置他们的治疗计划系统来计算治疗计划参数,该参数可以适应具有向患者靶区域的连续或并行放射递送的多个患者靶区域的虚拟定位和马赛克多靶定位。替代地或附加地,治疗计划系统可以被配置为计算治疗计划参数,该参数可以适应具有向患者靶区域的连续或并行放射递送的多个患者靶区域的虚拟定位和解耦的多靶定位。例如,一些治疗计划系统可以被配置为计算所有患者靶区域的平移不变发射滤波器,计算任何bgrt患者靶区域的发射滤波器,和/或基于患者靶区域和/或oar和/或计划注量图的低注量区的相对位置划分治疗计划或计划注量图。。bgrt患者靶区域可以在第一治疗期期间进行照射,并且sbrt/imrt患者靶区域可以在第二治疗期期间进行照射(即,在与第一治疗期不同的日子,其中第一和第二治疗期在时间上不重叠,在同一天的不同时间间隔发生,等等)。替代地,bgrt患者靶区域和sbrt/imrt患者靶区域可在同一治疗期期间依次照射。例如,可以在第一穿梭通过期间照射bgrt患者靶区域,并且可以在第二穿梭通过期间照射sbrt/imrt患者靶区域。
[0245]
图1a和1b是治疗计划方法的相应sbrt和bgrt变体的流程图表示,该方法使用虚拟定位来定位治疗期中的单个患者靶区域或多个患者靶区域。图1a描绘了结合了sbrt/imrt
患者靶区域的虚拟定位的治疗计划方法的一种变体。方法(120)可以包括获取(122)一个或多个患者靶区域的一个或多个治疗计划图像,限定(124)一个或多个患者靶区域和/或危及器官(oar)的轮廓和对应的剂量约束,为一个或多个患者靶区域和/或治疗区中的每一个选择(126)计划定位参考点,计算(128)每个定位参考点的对应定位函数,确定(129)一组治疗放射源发射位置并计算定位函数到每个发射位置的投影,以及基于每个患者靶区域的计划定位参考点和定位函数投影计算(130)每个发射位置的一组平移不变发射滤波器。限定(124)一个或多个患者靶区域的轮廓可以包括限定一组患者靶区域,该区域可以连接或关联(例如,附接到相同的骨骼结构)使得它们的位置和/或运动可能相关。方法(120)可以包括选择(128)整个患者靶区域组的计划定位参考点,和基于患者靶区域组的计划定位参考点计算(130)一组平移不变发射滤波器。可以将计算出的一组平移不变发射滤波器和每个患者靶区域、患者靶区域组和/或治疗区的计划定位参考点(连同其他治疗计划参数一起)传输到放疗系统以用于在治疗时定位。在一些变体中,计算出的平移不变发射滤波器可以表示基于(例如,集中于)计划定位参考点的计划递送注量。例如,对于特定患者靶区域(或患者靶区域组),定位函数可以是以该患者靶区域(例如,肿瘤质心)的计划定位参考点为中心的δ函数。用于特定患者靶区域的平移不变发射滤波器可以表示以计划定位参考点为中心的注量图(例如,计划注量图)。
[0246]
图1b描绘了治疗计划方法的一种变体,其结合了bgrt患者靶区域(即,其中基于获取的成像和/或生物数据,例如pet发射数据,计算递送到那些靶区域的注量的患者靶区域)的虚拟定位。图1b中描述的方法(140)可以包括获取(142)一个或多个患者靶区域的一个或多个治疗计划图像,限定(144)一个或多个患者靶区域和/或危及器官(oar)的轮廓和对应的剂量约束,为每个患者靶区域限定(146)包括围绕患者靶区域轮廓的边缘的感兴趣区域,为每个患者靶区域选择(148)计划定位参考点,获取(150)被感兴趣区域在空间上掩蔽的成像数据,确定(152)一组治疗放射源发射位置并计算所获取的成像数据到每个发射位置的投影,以及基于计划定位参考点和成像数据投影为每个患者靶区域计算(154)一组平移不变发射滤波器。在一些变体中,计划的感兴趣区域的界限可以包括空间滤波器。限定(146)一个或多个患者靶区域的轮廓可以包括限定可以连接或关联(例如,附接到相同的骨骼结构)的患者靶区域组,使得它们的位置和/或运动可能是相关的。方法(140)可以包括选择(148)整个患者靶区域组的计划定位参考点和基于患者靶区域组的计划定位参考点计算(154)一组平移不变发射滤波器.
[0247]
任选地,一些治疗计划方法可以包括将一些患者靶区域指定为sbrt/imrt靶区域并且将其他患者靶区域指定为bgrt靶区域。为sbrt/imrt靶区域和bgrt靶区域二者生成治疗计划还可以包括获取pet图像。对于每个bgrt患者靶区域,一种方法可以包括基于roi、bgrt患者靶区域的一个或多个计划图像和规定的bgrt患者靶区域的剂量计算平移不变发射滤波器(例如,放射激发矩阵(rfm))。任选地,一些治疗计划方法可以包括确定一组治疗放射源发射位置,计算诸如δ函数、高斯函数、截断高斯函数等的定位函数到每个发射位置的投影。任选地,一些治疗计划方法可以包括根据每个患者靶区域的定位参考点计算成本函数。
[0248]
放射激发矩阵(rfm)或发射滤波器可以是指定从部分图像到注量图的转换的矩阵,注量图可以包括在治疗期期间施加到患者的子束图案和/或子束强度。发射滤波器或
rfm可以表示用于向患者区域递送放射的注量图f与该患者区域的图像x之间的关系。也就是说,放射激发矩阵或发射滤波器p可以是任何矩阵,使得f=p
·
x。可以在针对每个患者靶区域的治疗计划期期间,结合计算基于放射剂量约束和目标形成的最小化一个或多个成本函数的注量图,例如所得剂量分布d和注量f的成本函数c(d,f),以及对f的任选限制来计算发射滤波器或rfm。成本函数的实例可包括但不限于靶区域的最小剂量、oar上的平均或最大剂量,和/或注量平滑度、总放射输出、总组织剂量、治疗时间等。在一些变体中,生成放射激发矩阵p可以包括设置优化问题以最小化成本函数c(d,f),并迭代不同组的p,使得成本函数c(d,f)在满足以下条件时最小化:
[0249]
f=p
·
x和
[0250]
d=a
•
f=a
·
p
·
x;
[0251]
其中d是预测的剂量分布,a是预先计算的剂量计算矩阵,f是预测的总递送放射注量,和x是已知的完整图像(例如,在诊断成像期和/或先前治疗期期间获取的图像)。预测的剂量分布d和预测的放射注量f可以使用剂量约束、患者靶体积和/或oar数据以及患者计划ct图像来计算。剂量计算矩阵a的一个实例可以是(kxn)矩阵,其中n可以是候选子束{bi}的数量并且k可以是用于roi的预选体素的数量。剂量计算矩阵a的第i列(其具有k个元素)表示从单位加权子束bi到k个体素中的每一个的剂量贡献。
[0252]
剂量计算矩阵a可以逐列计算,例如,通过沿着通过roi或患者体积的路径对每个子束的孔径进行光线跟踪并计算单位加权子束对k个体素中的每一个的贡献来逐列计算。子束孔径可以是由单个mlc叶开口(即,二元mlc或2-dmlc)限定的mlc孔径。可以在本文描述的任何方法中使用的剂量计算算法的实例可以包括蒙特卡洛模拟、筒串卷积叠加、笔形束卷积等。
[0253]
放射激发矩阵p(也称为rfm或发射滤波器)可以以下矩阵:当乘以完整图像x时,得到使成本函数最小化的预测的或期望的递送放射注量f。成本函数可以是凸的,允许使用众所周知的凸优化算法,例如梯度下降、加速近端梯度方法或内点方法。所计算出的放射激发矩阵p可以表示将注量f与完整的图像x联系在一起的乘数因子。可以在治疗期期间使用此关系在特定时间点基于在该同一时间点获取的部分图像xi通过将部分图像与放射激发矩阵p相乘(例如,fi=p
·
xi)来更新注量fi。关于bgrt治疗计划和递送方法的其他详细信息可以在于2018年5月30日提交的美国专利申请第15/993,325号中找到,其全部内容通过引用并入本文。
[0254]
任选地,一些方法(120)可以包括确定(132)一组治疗放射源发射位置并计算发射滤波器到每个发射位置的投影。例如,具有可旋转机架的放疗系统可具有围绕可推进患者平台的孔的100个周向分布的发射位置或角度。方法(120)可以包括计算每个发射滤波器到100个发射位置中的每个的投影。对于与高斯函数或截断高斯函数卷积的发射滤波器,高斯函数的宽度(σ)可以在治疗计划期间选择,其中平均值(μ)以计划定位参考点为中心。例如,高斯函数或截断的高斯函数的宽度(σ)可以基于mlc叶的宽度。
[0255]
图2描绘了治疗计划方法的一种变体的流程图表示,该方法使用马赛克多靶定位来配准治疗期中的多个患者靶区域。方法(220)可以包括获取(222)一个或多个患者靶区域的一个或多个治疗计划图像,限定(224)一个或多个患者靶区域和/或oar的轮廓以及对应的剂量约束,选择(228)一个或多个患者靶区域和/或oar中的每一个的计划定位参考点,和
基于每个患者靶区域和/或oar的计划定位参考点计算(230)一组平移不变发射滤波器。方法(220)可以包括基于发射滤波器和一个或多个计划图像生成(234)治疗计划注量图,和限定(236)围绕每个患者靶区域的周界,该患者靶区域包括治疗计划注量图中的低注量值区域。计算出的一组平移不变发射滤波器、每个患者靶区域和/或oar的计划定位参考点以及具有限定周界的治疗计划注量图可以(连同其他治疗计划参数一起)传输到放疗系统以用于治疗时的定位。
[0256]
任选地,一些治疗计划方法(220)可以包括将每个患者靶区域指定(226)为sbrt/imrt靶区域或bgrt靶区域。如果患者靶区域已被指定为bgrt靶区域,则方法(220)可包括计算该患者靶区域的roi。对于每个bgrt患者靶区域,方法(220)还可以包括计算平移不变发射滤波器(例如,rfm),如上所述。
[0257]
任选地,一些方法(220)可以包括确定(232)一组治疗放射源发射位置并且计算发射滤波器到发射位置中的每一个的投影。例如,具有可旋转机架的放疗系统可具有围绕可推进患者平台的孔的100个周向分布的发射位置或角度。方法(220)可以包括计算每个发射滤波器到100个发射位置中的每个的投影。
[0258]
任选地,一些治疗计划方法(220)可以包括计算(238)每个患者靶区域和/或oar的有界剂量体积直方图(bdvh)曲线,以及将每个患者靶区域和/或oar的bdvh曲线和/或剂量计算数据显示(240)到显示设备。患者靶区域的bdvh曲线可以通过计算运动包络中(或在bgrt靶的情况下,在roi中)患者靶区域的每个可能位置的每单位体积剂量来计算,和/或基于在计划期之前或期间获取的生物活性和/或生理和/或解剖数据来计算,以生成剂量体积曲线族。例如,可以通过在roi内执行患者靶区域的pet图像的刚性移动,并计算oar、roi和/或患者靶区域的对应剂量来计算针对该特定移动的靶区域位置的每个oar、roi和/或患者靶区域基于发射滤波器的有界dvh曲线族。例如,对于在roi内具有患者靶区域和一个oar的患者,可以针对患者靶区域在roi内的每个移动位置计算患者靶区域的dvh曲线族。bdvh曲线的阈值上界限可以包括剂量体积曲线族的最右边的点并且bdvh曲线的阈值下界限可以包括剂量体积曲线族的最左边的点。用于计算有界dvh曲线的方法的附加细节和变体在于2018年6月22日提交的美国专利申请第16/016,272号中提供,其全部内容通过引用并入本文。
[0259]
图3a和3b描绘了治疗计划方法的一种变体的流程图表示,该方法使用解耦多靶定位来在治疗期中配准多个患者靶区域。方法(350)可以包括获取(352)一个或多个患者靶区域的一个或多个治疗计划图像,限定(354)一个或多个患者靶区域和/或oar的轮廓以及对应的剂量约束,选择(358)一个或多个患者靶区域中的每一个的计划定位参考点,以及基于每个患者靶区域的计划定位参考点计算(360)一组平移不变发射滤波器。方法(350)可以包括基于发射滤波器和一个或多个计划图像为每个患者靶区域生成(362)注量图,并且将所有患者靶区域注量图组合(364)为累积治疗计划注量图。当患者靶区域彼此物理分离(例如,不重叠)时,每个患者靶区域可具有单独的计划定位参考点。这允许独立移动每个患者靶区域。每个患者靶区域的对应患者靶区域注量图可以被加在一起(因为剂量递送是线性的)以计算总剂量。例如,如果第一和第二计划定位参考点的位置从计划期改变到治疗期,则新的定位参考点位置可用于重新计算累积治疗计划注量图。多个患者靶区域的单独治疗计划注量图可以允许多个计划定位参考点彼此独立地移动,从而允许多个(例如,两个或更
多个)注量图相对于另一个移动以获得更优化的剂量覆盖。附加地或替代地,每个患者靶区域的相应患者靶区域注量图可以被个体约束。
[0260]
方法(350)然后可以包括基于一个或多个剂量约束迭代地修改(366)累积治疗计划注量图,所述剂量约束是例如以下中的一个或多个:(a)使高注量区保持彼此分离,(b)满足oar约束,(c)满足原始剂量约束/目标。
[0261]
在一些变体中,累积治疗计划注量图上的每个约束可以由限定或近似其相对重要性的线性因子加权。在一些变体中,靶区域的注量图可以被描述为变量x。对组合的注量求和可以描述为x
cumulative
。患者的剂量计算矩阵可以定义为a。特定靶区域的剂量可以定义为ax。此外,整个患者的剂量可以定义为ax
cumulative
。例如,剂量约束可以包括一个或多个成本函数,并且任选地,每个成本函数可以由个体的比例因子加权。规定剂量要求或约束(c)可包括一个或多个成本函数,并且可以包括,例如,放射注量(x)的成本函数c(x),和/或治疗区剂量的成本函数c(ax)和/或总剂量的成本函数c(ax
cumulative
),和/或总注量的成本函数c(x
cumulative
)中的一个或多个。这些可以各自任选地通过个体的比例因子(wi,wk,wm,wn)加权。例如,累积注量图的成本函数可用于在联合递送的情况下优化治疗时间。例如,可以优化每个治疗区剂量的成本函数,确保递送最小剂量。这确保了来自不同治疗区的注量不会将大部分剂量递送到给定的靶。这显著降低了治疗区之间的耦合,因此增加了治疗计划对治疗区之间相对移动的稳健性。例如,d
cumulative
的成本函数可用于限制从所有治疗区组合的对心脏的平均组合剂量。
[0262]
c=∑w
ici
(x) ∑w
kck
(ax) ∑w
mcm
(ax
cumulative
)
[0263]
∑w
ncn
(x
cumulative
)
[0264]
关于成本函数和其他约束的其他细节可以在2020年1月28日提交的美国临时专利申请第62/966,997号中找到,其全部内容通过引用并入本文。
[0265]
附加地或替代地,除了预定的一组剂量约束之外,还可以应用一个或多个调整约束(例如,除了组织约束之外的人工约束,调整结构)以确保剂量在给定地带(例如,区域)中不超过预定阈值。在一些变体中,一个或多个调整约束可以实现两个或更多个靶区域之间的放射递送的去耦。
[0266]
在累积治疗计划注量图已经被修改之后,方法(350)可以包括限定(368)每个患者靶区域周围的周界,该患者靶区域包括累积治疗计划注量图中的低注量值区域(例如,调整约束、成本函数),沿该周界将累积治疗计划注量图分离(370)为每个患者靶区域的个体注量图,并且针对每个患者靶区域,基于计划定位参考点和该患者靶区域的注量图计算(372)第二组平移不变发射滤波器。可以将第二组平移不变发射滤波器、每个患者靶区域和/或oar的计划定位参考点以及每个患者靶区域的个体治疗计划注量图(连同其他治疗计划参数一起)传输到放疗系统以在治疗时进行定位。
[0267]
在一些变体中,例如对于sbrt/imrt递送,治疗计划方法可以包括计算患者靶区域和/或治疗区的递送注量(例如,基于规定剂量、剂量约束和/或剂量计算矩阵),其中递送注量连接到(例如,锚定)计划定位参考点。然后可以将计算的递送注量分割成机器指令(通过治疗计划系统和/或放射治疗系统)以用于递送。在治疗期期间,可以基于定位参考点的更新位置(例如,由用户从治疗期期间获取的定位图像中选择)来更新计算的递送注量。在这种变体中,治疗计划系统可能不需要计算发射滤波器。
[0268]
任选地,一些治疗计划方法(350)可以包括将每个患者靶区域指定(356)为sbrt/imrt靶区域或bgrt靶区域。如果患者靶区域已被指定为bgrt靶区域,则方法(350)可包括计算该患者靶区域的roi。当患者靶区域彼此物理分离以允许每个患者靶区域独立移动时,每个患者靶区域可具有单独的计划定位参考点,从而允许注量图相对于另一个移动以优化剂量覆盖。对于每个bgrt患者靶区域,方法(350)还可以包括计算平移不变发射滤波器,如上所述。
[0269]
任选地,方法(350)可以包括将累积治疗计划注量图的可视化图形显示(374)到显示设备。任选地,一些治疗计划方法(350)可以包括计算(376)每个患者靶区域和/或oar的bdvh曲线,以及将每个患者靶区域和/或oar的bdvh曲线和/或剂量计算数据显示(378)到显示设备。可以如前所述计算患者靶区域的bdvh曲线。
[0270]
图4描绘了使用基于bgrt的多靶定位来配准治疗期中的多个患者靶区域的治疗计划方法的一种变体的流程图表示。方法(450)可以包括获取(452)一个或多个患者靶区域的一个或多个治疗计划图像,限定(454)一个或多个患者靶区域和/或oar的轮廓以及对应的剂量约束,指定(456)多个患者靶区域之一作为配准靶区域,以及为其他患者靶区域(即,不是配准靶区域)中的每一个限定(458)空间掩模或滤波器(例如,roi、发射区)的轮廓,以使其大小和形状适应配准靶区域的运动和其他患者靶区域的运动。方法(450)可以包括基于为每个患者靶区域和/或配准靶区域的roi选择的计划定位参考点计算(462)一组平移不变发射滤波器,基于发射滤波器和一个或多个计划图像生成(466)治疗计划注量图,以及计算(468)所有患者靶区域的配准靶区域和其他患者靶区域的剂量。方法(450)还可以包括计算平移不变发射滤波器,例如每个患者靶区域的每个roi的发射滤波器,其可以如前所述地计算,并且可以基于所计算的发射滤波器以及一个或多个计划图像来生成(466)治疗计划注量图。用于roi虚拟定位的平移不变发射滤波器和/或用于bgrt递送的平移不变发射滤波器(例如rfm),每个患者靶区域和/或oar的计划定位参考点和/或任何治疗计划注量图和/或剂量计算可以(连同其他治疗计划参数)传输到放疗系统以进行定位和放射递送。
[0271]
任选地,一些治疗计划方法(450)可以包括限定(460)配准靶区域的空间掩模或滤波器(例如,发射区、roi)的轮廓以小于其他患者靶区域的空间掩模或滤波器。例如,配准靶区域的roi可能小于其他患者靶区域的roi。在一些变体中,被选为配准靶区域的患者靶区域可以是最接近关键结构的患者靶区域,例如高放射敏感器官和/或渴求pet关键结构和/或骨骼结构。在一些变体中,被选为配准靶区域的患者靶区域可以是最接近计划结构(例如,计算的或用户选择的)的靶区域,例如两个患者靶区域之间的潜在剂量交界区。在一些变体中,被选为配准靶区域的患者靶区域可能对不确定性最敏感,例如具有高剂量梯度、关键剂量测定目标或约束、不一致的pet活动(例如,缺氧或灌注区域),或靠近roi边缘的可变运动轨迹的区域。
[0272]
任选地,一些方法(450)可以包括确定(464)一组治疗放射源发射位置并计算发射滤波器到每个发射位置的投影。例如,具有可旋转机架的放疗系统可具有围绕可推进患者平台的孔的100个周向分布的发射位置或角度。方法(450)可以包括计算每个发射滤波器到100个发射位置中的每个的投影。任选地,方法(450)可以包括计算(470)每个患者靶区域和/或oar的bdvh曲线,并将每个患者靶区域和/或oar的bdvh曲线和/或剂量计算数据显示(472)到显示器设备。可以如前所述计算患者靶区域的bdvh曲线。
[0273]
如前所述,用于多靶照射的任何治疗计划方法可以任选地包括计算每个患者靶区域和/或oar的bdvh曲线,并向临床医生显示dvh和其他剂量数据以供审查和/或批准。在一些变体中,此类剂量数据可用作反馈(即,作为附加约束)以进一步改善可帮助改善对剂量测定目标和处方的依从性的治疗计划注量图和/或发射滤波器。图5a-5c描绘了基于用户选择的对患者靶区域的bdvh的置信区间的修改和/或移动剂量分布来修改计划注量图和/或发射滤波器的治疗计划方法的变体的流程图表示。
[0274]
bdvh置信区间编辑
[0275]
bdvh置信区间编辑可以提供一种机制,通过该机制可以减少或消除空间不确定性。bdvh计算通常可以用95%的置信区间计算,目的是在治疗当天,患者将在那些界限内表示。减少bdvh中的界限宽度是为了使潜在最小剂量d
pmin
和潜在最大剂量d
pmax
更接近标称剂量dn。减少与标称剂量的差异的方法可以包括减少置信区间。例如,80%的置信区间可能会导致更窄的bdvh曲线,其中d
pmax
和d
pmin
可能更接近dn。权衡是,例如,不是预期二十分之一的患者在治疗时未通过bdvh安全性检查,而是五分之一的患者可能未通过bdvh安全性检查并被拒绝用非确定性治疗方法(即bgrt)治疗。类似地,如果靶区域的bdvh在初始95%ci计算时返回相当紧密,则可以使用更高的置信区间(例如99%ci)重新计算bdvh,这将扩大bdvh,导致d
pmin
和d
pmax
进一步移动远离dn(即加宽/扩展bdvh曲线)。使用此功能,临床医生可能能够减少或消除现有界限内的热点和冷点。
[0276]
图5a描绘了包括bdvh置信区间编辑的治疗计划方法。方法(550)可以包括开发(551)具有一个或多个指定不确定性矢量(例如,生物活性、设置位置误差等)的治疗计划和选择(552)不确定性矢量的置信区间(ci),其可以根据不确定性的类型确定。方法(550)可以包括用不确定性优化(553)治疗计划注量图,使用描述治疗日剂量拟合在bdvh界限内的可能性的ci计算bdvh和评估(554)bdvh并确定界限是否可以接受。例如,bdvh可以被输出到显示设备并且被用户观看。如果认为界限是可接受的,则方法(550)可以包括计算(556)治疗计划的最终剂量和批准(557)治疗计划的界限。如果界限不可接受,则方法(550)可以包括确定(558)如何调整界限。在一些变体中,方法(550)可以包括加宽界限和增加(559)可接受的不确定性以及设置大于原始ci的新ci。在一些变体中,方法(550)可以包括收紧界限并降低(560)可接受的不确定性以及设置小于原始ci的新ci。在ci被调整后,方法(550)可以包括优化(561)具有不确定性的治疗计划,使用描述治疗日剂量拟合在bdvh界限内的可能性的新的ci计算新的bdvh,然后评估(554)新的bdvh并确定界限是否可接受。bdvh的评估和计算(554-561)可以迭代,直到计算出具有可接受界限的bdvh。
[0277]
在一些变体中,置信区间编辑可以包括确定在ci已经被调整之后是否需要重新优化治疗计划注量图。图5b描绘了包括关于在bdvh置信区间编辑之后是否重新优化的确定的治疗计划方法。方法(570)可以包括开发(571)具有一个或多个指定不确定性矢量(例如,生物活性、设置位置误差等)的治疗计划和选择(572)不确定性矢量的置信区间(ci),其可以根据不确定性的类型确定。方法(570)可以包括优化(573)具有不确定性的治疗计划注量图,使用描述治疗日剂量拟合在bdvh界限内的可能性的ci计算bdvh和评估(574)bdvh并确定界限是否可以接受。例如,bdvh可以被输出到显示设备并且被用户观看。如果认为界限是可接受的,则方法(570)可以包括计算(576)治疗计划的最终剂量和批准(577)治疗计划的界限。如果界限不可接受,则方法(570)可以包括确定(578)如何调整界限。在一些变体中,
方法(570)可以包括加宽界限和增加(579)可接受的不确定性以及设置大于原始ci的新ci。在一些变体中,方法(570)可以包括收紧界限并降低(580)可接受的不确定性以及设置小于原始ci的新ci。在ci已经被调整之后,方法(570)可以包括确定是否需要新的优化。如果是,则方法(570)可以包括优化(581)具有不确定性的治疗计划,使用描述治疗日剂量拟合在bdvh界限内的可能性的新ci计算新的bdvh,然后评估(574)新的bdvh并确定界限是否可接受。如果确定不需要优化,则方法(570)可以从ci调整直接进行到评估(574)新的bdvh。bdvh的评估和计算(574-581)可以迭代,直到计算出具有可接受界限的bdvh。在一些变体中,可以任选地包括可视化图形以表示由于ci的变化而对bdvh的影响。
[0278]
一些治疗计划方法可以包括显示叠加在患者解剖图像上的治疗计划剂量分布(例如,从治疗计划注量图计算),该患者解剖图像还包括治疗期中待治疗的每个患者靶区域,接收与剂量移动有关的临床医生输入,以及根据临床医生输入的剂量移动重新计算治疗计划注量图和/或发射滤波器。在一些变体中,剂量移动可以是剂量沿任何方向刚性移动约0.1mm至约1mm。这些微小的剂量移动可以帮助避免不必要的注量递送到脊柱和/或减少由两个平面内靶区域之间的两个相互作用的注量图引起的热点。例如,当注量图子区域在马赛克多靶定位中单独定位时,和/或当不同患者靶区域的个体注量图在解耦多靶定位中单独定位时,累积递送注量图(即,所有递送注量图子区域的总和和/或每个患者靶区域的所有个体注量图的总和)可能具有有不需要的注量的区,例如oar或健康组织区域处的注量水平升高的区。这些不需要的注量区可能不存在于计划注量图中,但是,随着在定位期间实施的注量图变化(例如,移动),在递送注量图中可能出现不利的注量图伪影。放疗系统可以生成与患者的解剖图像重叠的反映这些注量图变化(和/或剂量变化)的可视化图形,使得用户可以决定是否可以移动任何递送注量图以减轻任何不需要的剂量或注量。替代地或附加地,在一些变体中,可以在治疗计划期间的注量图优化之后执行剂量移动,这可以帮助促进满足剂量测定目标的治疗计划和/或计划注量图的生成。在剂量移动之后,额外的注量图优化步骤可能是任选的(即,重新优化可能不是必要的)。更新的注量图和/或发射滤波器可以被传输到放射治疗系统以进行定位和治疗。
[0279]
图5c是治疗计划方法(590)的一种变体的流程图描绘,包括计算(591)所有患者靶区域的治疗计划注量图(和/或发射滤波器,例如本文所述的任何发射滤波器),计算(592)基于治疗计划注量图的剂量分布图,生成(593)包括叠加在包括一个或多个患者靶区域的患者解剖图像上的剂量分布图的合成图像,接收(594)与在剂量分布图上移动剂量有关的用户(例如,临床医生、放射剂量测试员)输入,以及根据用户输入的剂量移动计算(595)更新的治疗计划注量图。剂量移动后的注量图优化可能是任选的。
[0280]
在一些治疗计划方法中,剂量方差(也称为δ剂量)可用作优化治疗计划注量图的约束。可以选择最小或最大允许剂量方差作为约束。例如,将最大剂量方差设置为治疗计划注量图优化约束可能有助于减小bdvh的宽度,同时保持默认置信区间(例如,ci=95%)。图6描绘了包括设置剂量方差作为用于生成治疗计划注量图的约束的治疗计划方法。方法(670)可以包括开发(671)具有一个或多个指定不确定性矢量(例如,生物活性、设置位置误差等)的治疗计划和选择(672)不确定性矢量的最大允许剂量方差d
plan
,其可根据不确定性的类型确定。方法(670)可以包括优化(673)具有最大允许剂量方差d
plan
的治疗计划注量图,使用描述治疗日剂量拟合在bdvh界限内的可能性的ci计算bdvh,以及评估(674)用户合
成剂量方差d
actual
并确定d
actual
是否可接受。如果认为d
actual
是可接受的,则方法(670)可以包括计算(676)治疗计划的最终剂量和批准(677)治疗计划的剂量方差。如果d
actual
是不可接受的,则方法(670)可以包括确定(678)如何调整剂量方差。在一些变体中,方法(670)可以包括增加(559)可接受的剂量方差和设置大于原始d
plan
的新剂量方差d
plan
'。在一些变体中,方法(670)可以包括减小(580)可接受的剂量方差和设置小于原始d
plan
的新剂量方差d
plan
'。在调整了d
plan
之后,方法(670)可以包括用更新的剂量方差d
plan
'约束优化(681)治疗计划,基于d
plan
'约束值选择或多或少易受剂量方差影响的几何结构,以及然后评估(674)新的d
actual
并确定剂量方差是否可接受。剂量方差的评估和计算(674-681)可以迭代,直到计算出可接受的剂量方差。
[0281]
多靶定位方法
[0282]
虚拟定位方法移动患者靶区域的计划注量图,以反映治疗时该患者靶区域的当前/实时位置。在治疗计划期间,可以计算基于计划定位参考点和期望的剂量测定目标计算的一组平移不变发射滤波器,并且在治疗期时,平变不变发射滤波器可以用于计算在将剂量递送到该患者治疗区域时产生的递送注量。一种用于虚拟定位的方法可以包括选择与计划定位参考点对应的定位参考点。例如,如果计划定位参考点是患者靶区域的中心,则在定位期间,还应选择定位参考点作为定位图像中反映的患者靶区域的中心。然后,可以计算基于选择的定位参考点的定位函数(例如δ函数、高斯函数、截断高斯函数等)。例如,定位函数可以是δ函数,它可以是以定位参考点为中心的脉冲函数,或者定位函数可以是具有在治疗计划期间选择的宽度(σ)的高斯函数,其中平均值(μ)以定位参考点为中心。可以通过将δ函数在该发射位置上的投影与平移不变发射滤波器在该发射位置上的投影进行卷积来计算治疗放射源的每个发射位置的递送注量(这可以由治疗计划预先确定)。然后可以将用于该患者靶区域的每个发射位置的递送注量分割成用于放射递送的放疗系统机器指令。
[0283]
图7a描绘了用于sbrt/imrt递送的虚拟定位的方法的一种变体的流程图表示。该方法可以用于单个患者靶区域或多个患者靶区域的虚拟定位,并且可以在治疗期开始时或在整个治疗期中多次使用。在一些变体中,治疗计划可包括多个治疗区,每个治疗区具有一个或多个患者靶区域。可以针对治疗区对患者进行一次物理设置/定位,并且可以虚拟定位治疗区内的每个患者靶区域。在已在治疗计划期间限定了患者靶区域组的一些变体中,每个组可以共享单个定位参考点并且虚拟地一起定位。方法(700)可以包括获取(702)一个或多个患者靶区域的一个或多个定位图像,为每个患者靶区域选择(704)所获取图像内的定位参考点,其中定位参考点对应于在治疗计划期间选择的计划定位参考点,从每个患者靶区域的定位参考点计算(706)定位函数(例如,δ、高斯、截断高斯等)并计算定位函数到每个治疗放射源发射位置的投影,以及通过将对应的定位函数投影与基于计划定位参考点导出的平移不变发射滤波器卷积来计算(708)用于每个发射位置的用于递送到每个患者靶区域的注量。如上所述,在一些变体中,可以通过将定位函数和发射滤波器在每个发射位置上的投影进行卷积来计算用于治疗放射源的每个发射位置的递送注量。任选地,方法(700)可以包括进行(710)放射递送(即,使用治疗放射源将递送注量发射到每个患者靶区域)。可以在治疗计划期间基于(例如,集中于)计划定位参考点来计算平移不变发射滤波器。在一些变体中,定位函数可以是δ函数,并且在治疗计划期间计算的平移不变发射滤波器可以表示以计划定位参考点为中心的注量图(例如,计划注量图)。在该实例中,计算(708)递送注量可
以包括将计算的δ函数(其以选定的定位参考点为中心)与平移不变发射滤波器卷积,这可以导致产生作为计划注量图移动的递送注量图。在一些变体中,放疗系统可以实时地,即在放射递送之前的几分钟或几秒,将递送注量图分割成机器指令。待定位的患者靶区域可以包括在单个定位图像中,或者可以包括在治疗期开始时和/或整个治疗期获取的多个定位图像中。例如,可以在第一图像中识别第一患者靶区域并且可以在第二图像中识别第二患者靶区域。这些图像可以是在单独时间或同时获取的单独图像,或者可以是单个图像的子区域。计划定位参考点可以是治疗等中心,然而,在一些变体中,计划定位参考点可以不是治疗等中心并且可以是用户选择的任何点。定位参考点可以由坐标指定。用于定位患者靶区域的定位函数可以是脉冲函数或以所选择的定位参考点为中心的峰值或像素,如前所述。方法(700)可以与图1-4的中的任何治疗计划方法如图1a、1b的方法一起使用。
[0284]
图7b描绘了用于将bgrt递送到一个或多个患者靶区域的虚拟定位的方法的一种变体的流程图表示。bgrt患者靶区域的虚拟定位包括基于计划定位参考点与在治疗期期间选择的定位参考点之间的偏移来调整位置roi。方法(720)可以包括获取(722)一个或多个患者靶区域的一个或多个定位图像,为每个患者靶区域选择(724)所获取图像内的定位参考点,其中定位参考点对应于在治疗计划期间选择的计划定位参考点,基于所选择的定位参考和计划定位参考指向之间的移动计算(726)空间偏移,以及基于计算的空间偏移移动(728)计划的感兴趣区域(roi)的界限。在一些变体中,移动(728)计划的感兴趣区域的界限包括通过滚动校正因子对计划的感兴趣区域应用旋转和移动,该滚动校正因子表示定位参考点相对于计划定位参考点的旋转平移。方法(720)进一步可以包括以下步骤:获取(730)成像数据并使用移动的感兴趣区域对成像数据进行空间掩蔽(例如,过滤),通过将所获取的成像数据的投影与对应的平移不变发射滤波器卷积来计算(732)在治疗放射源的每个发射位置用于递送到每个患者靶区域的注量,以及进行(734)放射递送(即,使用治疗放射源将递送注量发射到每个患者靶区域)。所获取的成像数据(730)可以包括pet成像数据(例如,正电子湮没发射路径,lor)、x射线成像数据、mri成像数据、超声成像数据、光学成像数据(例如,来自照相机)等。计算(732)特定发射位置的递送注量可以包括将获取的、空间掩蔽的成像数据投影到该发射位置,以及将成像数据投影与用于该发射位置和靶区域的发射滤波器卷积。发射滤波器可以是在治疗计划期间计算的发射滤波器之一(例如,使用图1b的方法计算)。在已经将滚动校正因子应用于计划的感兴趣区域的变体中,计算(732)递送注量可以包括将一组发射滤波器与滚动校正因子循环卷积,并且在一些变体中,可以包括如上所述移动roi(例如,如图34中所描述和描绘的)。方法(720)可以与图1-4中的任何治疗计划方法如图1a、1b的方法一起使用。
[0285]
图8a描绘了用于马赛克多靶定位的方法的一种变体的流程图表示。该方法可以在治疗期开始时使用(例如,配准/定位所有患者靶区域)或在整个治疗期中多次使用(例如,依次配准/定位患者靶区域)。方法(800)可以包括获取(802)一个或多个患者靶区域的一个或多个定位图像,根据在治疗计划期间限定的每个患者靶区域周围的周界将治疗计划注量图划分(804)为一个或多个注量图子区域,以及移动(806)每个注量图子区域,使得高注量区域与其对应的患者靶区域共同定位。移动(806)注量图子区域可以使用本文描述的虚拟定位方法(例如,为每个患者靶区域选择定位参考点,基于定位参考点计算δ函数,和将δ函数与平移不变发射滤波器卷积)执行。替代地或附加地,可以通过移动放疗系统机器指令
(例如,mlc、机架、直线加速器、钳口等)来执行移动(806)注量图子区域。
[0286]
任选地,方法(800)的一些变体可以包括基于移动的注量图子区域计算(808)每个患者靶区域的剂量,将计算的剂量与在治疗计划期间计算的有界剂量体积直方图曲线进行比较,和/或将每个患者靶区域和/或oar的有界剂量体积直方图曲线和/或剂量计算数据显示到显示设备。任选地,方法(800)可以包括进行(810)放射递送(即,使用治疗放射源将递送注量发射到每个患者靶区域)。在一些变体中,放疗系统可以实时地,即在放射递送之前的几分钟或几秒,将递送注量图分割成机器指令。待定位的患者靶区域可以包括在单个定位图像中,或者可以包括在治疗期开始时和/或整个治疗期获取的多个定位图像中,如上所述。方法(800)可以与图1-4中的任何治疗计划方法如图2的方法一起使用。
[0287]
图8b描绘了包括患者平台移动或调整的用于马赛克多靶定位的方法的一种变体的流程图表示。在一些方法中,患者设置可以包括基于定位图像和治疗计划图像调整患者平台的取向(例如,滚动、俯仰、偏航、x-y-z平移等)。该方法可以在治疗期开始时使用(例如,配准/定位所有患者靶区域)或在整个治疗期中多次使用(例如,依次配准/定位患者靶区域)。方法(820)可以包括获取(822)一个或多个患者靶区域的一个或多个定位图像,根据在治疗计划期间限定的每个患者靶区域周围的周界将治疗计划注量图划分(824)为一个或多个注量图子区域,基于定位图像和治疗计划图像计算(826)每个注量图子区域的患者平台位置移动矢量,对于每个患者平台位置移动(828)注量图子区域,使得高注量区域与其对应的患者靶区域共同定位,以及计算(830)在每个患者平台位置移动矢量处对每个患者靶区域的注量。可以使用本文描述的虚拟定位方法(例如,为每个患者靶区域选择定位参考点,基于定位参考点计算δ函数,并且将δ函数与平移不变发射滤波器进行卷积)来执行移动(828)注量图子区域。替代地或附加地,可以通过移动放疗系统机器指令(例如,mlc、机架、直线加速器、钳口等)来移动(828)注量图子区域。
[0288]
任选地,方法(820)的一些变体可以包括基于移动的注量图子区域计算(832)每个患者靶区域的剂量,将计算的剂量与在治疗计划期间计算的有界剂量体积直方图曲线进行比较,和/或将每个患者靶区域和/或oar的有界剂量体积直方图曲线和/或剂量计算数据显示到显示设备。任选地,方法(820)可以包括进行(834)放射递送(即,使用治疗放射源将递送注量发射到每个患者靶区域)。在一些变体中,放疗系统可以实时地,即在放射递送之前的几分钟或几秒,将递送注量图分割成机器指令。待定位的患者靶区域可以包括在单个定位图像中,或者可以包括在治疗期开始和/或整个治疗期获取的多个定位图像中,如上所述。方法(820)可以与图1-4中的任何治疗计划方法如图2的方法一起使用。
[0289]
图9描绘了用于解耦多靶定位的方法的一种变体的流程图表示。方法(900)可以包括获取(902)一个或多个患者靶区域的一个或多个定位图像,其中每个患者靶区域具有包括一组治疗计划参数(包括一组平移不变发射滤波器)的单独的个体治疗计划,为每个患者靶区域选择(904)定位参考点并使用虚拟定位方法(例如,基于定位参考点计算δ函数,并将δ函数与平移不变发射滤波器卷积以获得每个患者靶区域的递送注量图)计算每个靶区域的递送注量图,以及通过组合所有患者靶区域的递送注量图来计算(906)累积注量图,并计算每个患者靶区域的剂量。方法(900)可以包括评估(908)是否满足所有患者靶区域的剂量目标和/或个体递送注量图的高注量区是否彼此充分分离(即,不与其他高注量区共同定位)。如果满足所有患者靶区域的剂量目标和/或个体递送注量图的高注量区彼此充分分
离,则方法(900)可以包括进行(912)放射递送,其可以包括将以下一项或多项分割(914)为放疗系统指令:(a)每个患者靶区域的个体注量图;和/或(b)累积注量图。如果未满足所有患者靶区域的剂量目标,和/或个体递送注量图的高注量区彼此未充分分离,则方法(900)可包括生成(916)视觉和/或听觉通知。可以任选地将剂量计算数据和/或dvh曲线呈现给用户,以便他们可以评估接下来的行动方案。在一些变体中,放疗系统可以实时地,即在放射递送之前的几分钟或几秒,将递送注量图分割成机器指令。待定位的患者靶区域可以包括在单个定位图像中,或者可以包括在治疗期开始时和/或整个治疗期获取的多个定位图像中,如上所述。方法(900)可以与图1-4中的任何治疗计划方法如图3a-3b的方法一起使用。
[0290]
图10描绘了用于解耦多靶定位的方法的一种变体的流程图表示。方法(1000)可以包括获取(1002)一个或多个患者靶区域的一个或多个定位图像,将在治疗计划期间指定为配准靶区域的患者靶区域与治疗等中心(例如,治疗放射束的中心部位)一起定位(1004),以及确定(1006)其他患者靶区域是否位于治疗计划期间指定的空间发射滤波器(例如,激发区,roi)的界限内。如果其他患者靶区域位于空间掩模或滤波器的界限内(例如,位于roi内),则方法(1000)可以包括进行(1002)放射递送。如果其他患者靶区域不位于空间掩模或滤波器的界限内(例如,不位于roi内),则方法(1000)可以包括生成(1010)视觉和/或听觉通知。可以任选地向用户呈现患者靶区域相对于他们相关联的roi的位置数据,以便他们可以评估接下来的行动方案。任选地,可以使用本文描述的虚拟定位方法来定位这些非配准靶区域中的一个或多个的roi。定位(1004)配准靶区域可以使用一种或多种设置和/或定位方法。例如,定位(1004)配准靶区域可以包括以下一项或多项:(a)移动放疗系统机器指令(例如,mlc、机架、直线加速器),(b)选择用于配准靶区域的roi的定位参考点,基于定位参考点计算δ函数,并将函数(例如,δ、高斯、截断高斯)与roi进行卷积,和/或(c)计算患者平台位置移动矢量并据此调整患者平台。在一些变体中,放射递送可包括将以下一项或多项分割成放疗系统指令:(a)每个患者靶区域的个体注量图;和/或(b)累积注量图。在一些变体中,放疗系统可以实时地,即在放射递送之前的几分钟或几秒,将递送注量图分割成机器指令。待定位的患者靶区域可以包括在单个定位图像中,或者可以包括在治疗期开始时和/或整个治疗期获取的多个定位图像中,如上所述。方法(1000)可以与图1-4中的任何治疗计划方法如图4的方法一起使用。例如,多个患者靶区域中的每一个都可以具有单独的计划定位参考点和一组发射滤波器。在治疗期期间,多个患者靶区域中的每一个的定位参考点的位置可基于所获取的定位图像而更新(例如,定位参考点可由用户选择)。基于更新的定位参考点的每个患者靶区域的单独和/或独立虚拟定位有效地将递送注量图移动到多个患者靶区域的实时位置。以此类方式,多个患者靶区域中的每一个的注量图可以相对于彼此移动。例如,在具有两个或更多个患者靶区域的治疗期中,放射递送方法可以包括执行一个或多个(例如,两个或更多个)虚拟定位,移动两个或更多个患者靶区域中的每一个的计划注量图。
[0291]
图11a是说明方法(100)的流程图。方法(100)可用于定位患者以进行放射治疗。如图11a所示,方法(100)包括获取(102)第一患者治疗区和第二患者治疗区的图像。在一些实施例中,第一患者治疗区和第二患者治疗区可以包括一个或多个肿瘤区域(例如,患者靶区域)。例如,在一些实施例中,第一患者治疗区可以包括肿瘤的第一部分,并且第二患者治疗区可以包括肿瘤的第二部分。在一些实施例中,第一患者治疗区和第二患者治疗区可各自
包括位于患者身体不同区域的一个或多个离散肿瘤。所获取图像可以是例如经由pet、ct、mri、超声、光学成像模式、其组合(例如,表面跟踪/地图、光学和ct以基于外表面数据预测内部位置)和/或任何其他合适的方法中的一种或多种获取的图像。在一些实施例中,例如,ct系统可用于在治疗期之前或开始时获取一个或多个图像。在一些实施例中,ct系统可以附接到与旨在在治疗期期间递送放射治疗的放射源相同的机架。在一些实施例中,ct系统可以附接到与支撑放射源的机架不同的机架。在一些实施例中,在离散的患者平台位置或地点(即,光束站)递送放射的情况下,第一患者治疗区的位置可以对应于治疗放射源的第一光束站的位置和第二患者治疗区的位置可以对应于第二光束站的位置。在一些变体中,第一和第二治疗区可以重叠,而在其他变体中,第一和第二治疗区不重叠。
[0292]
可以基于第一患者靶区域的所获取图像和治疗计划图像(本文也称为“第一治疗计划图像”)来计算(104)第一组患者位置移动矢量。第一治疗区和/或患者靶区域在所获取图像中的位置可以以2d和/或3d与第一治疗区和/或患者靶区域在治疗计划图像中的位置进行比较。例如,在一些实施例中,可以将患者靶区域划分为可以由体素表示的子区域(例如,子体积),并且可以将获取的图像的每个体素的坐标与治疗计划图像中患者靶区域的对应体素的坐标相比。第一组患者位置移动矢量中的每一个矢量可以表示所获取图像的体素的坐标与治疗计划图像的对应体素的坐标之间的距离和方向差。在一些实施例中,方向差可以包括倾斜角。在一些实施例中,可以通过相对于治疗计划图像移动所获取图像以将治疗计划图像的第一患者靶区域与所获取图像的第一患者靶区域对齐或配准来计算第一组患者位置移动矢量。例如,所获取图像的每个体素可以沿着或围绕x、y和/或z轴平移,在所获取图像的移动期间保持所获取图像的每个体素彼此的相对位置,直到所获取图像和治疗计划图像相对于第一患者靶区域近似对齐(例如,在预定的可接受容差或差数内对齐,使得图像中的第一患者靶区域之间存在可接受的区域或重叠比例)。第一组患者位置移动矢量然后可以基于在被移动到与治疗计划图像对齐增加之前和之后所获取图像之间的位置和/或地点差异来计算。第一组患者位置移动矢量可以反映所获取图像的每个体素将被平移以用于所获取图像的第一患者靶区域和治疗计划图像的第一患者靶区域之间的可接受对齐的距离和/或方向。此外,第一组患者位置移动矢量可以包括或对应于与患者的第一位置和/或第一取向(例如,患者在其上被布置的表面的第一位置和/或第一取向)相关的指令,使得患者的第一患者靶区域位于大约在获取治疗计划图像时第一患者靶区域所处的位置。这可以促进更接近治疗计划的治疗放射递送到患者靶区域。此外,第一组患者位置移动矢量可以包括关于任何倾斜、俯仰、偏航和/或滚动校正的信息,该校正需要通过患者平台的定位和/或通过调整与放射源(例如,治疗放射源)耦合(例如,以用于校正机架发射位置)的机架的滚动来实现,使得第一患者靶区域的位置接近第一治疗计划图像中第一患者靶区域的位置。
[0293]
在一些实施例中,第一治疗区和/或患者靶区域的获取图像和第一患者靶区域的治疗计划图像可以各自是二维图像。可以将二维获取图像与二维治疗计划图像进行比较以计算第一组患者位置移动矢量。在一些实施例中,可以沿着不同的取向或平面(例如,三个或更多个取向或平面)获取第一治疗区和/或患者靶区域的多个二维图像,并且可以将该图像与沿相同取向或平面获取的第一患者靶区域的对应治疗计划图像进行比较。可以使用在每个取向沿每个图像平面的第一患者靶区域的位置的变化来计算第一组患者位置移动矢
量。例如,获取的图像可以包括患者的第一患者靶区域的获取的轴向图像、获取的矢状图像和获取的冠状图像。当患者以仰卧位躺在诸如患者平台或治疗床的表面上且患者定向为使得患者将首先遇到治疗放射源头部时,所获取的轴向图像可沿患者的轴向平面(例如,将身体分为上部和下部的平面)拍摄,所获取的矢状图像可沿患者的矢状平面(例如,将患者分为左部和右部的平面)拍摄,并且所获取的冠状图像可沿患者的冠状平面(例如,将患者分成腹部和背部的平面)拍摄。轴向平面与矢状平面垂直设置,并且冠状平面与轴向平面和矢状平面均垂直设置。治疗计划图像可以包括患者的第一患者靶区域的治疗计划轴向图像、治疗计划矢状图像和治疗计划冠状图像。因此,获取的轴向图像对应于治疗计划轴向图像,获取的矢状图像对应于治疗计划矢状图像,并且获取的冠状图像对应于治疗计划冠状图像。
[0294]
应该沿着或围绕x轴、y轴和z轴中的每一个(例如,通过移动患者表面和/或旋转放射源)调整患者位置和/或取向以用于治疗第一患者靶区域的量可以基于治疗计划图像和在患者的轴向、矢状和冠状平面中的每一个内拍摄的相应获取图像之间的差异由第一组患者位置移动矢量反映。在一些实施例中,患者表面的x轴可以平行于患者的矢状平面和冠状平面的交点并且可以设置在矢状平面中。患者表面的y轴可以平行于患者的轴向平面和冠状平面的交点并且可以设置在轴向平面中。患者表面的z轴可以平行于患者的矢状平面和轴向平面的交点并且可以设置在患者的矢状平面或轴向平面中。为了确定第一组患者位置移动矢量,可以将第一患者靶区域的每个获取图像与在同一平面内拍摄的第一患者靶区域的相应治疗计划图像进行比较以确定患者在同一平面内的距离校正和/或旋转校正(例如,通过患者表面的移动和/或放射源的旋转)。第一组患者位置移动矢量中的一个或多个矢量可以表示患者表面将被移动(例如,移位和/或旋转)的幅度和方向,使得第一患者靶区域接近治疗计划图像中第一患者靶区域的位置。第一组患者位置移动矢量中的一个或多个矢量还可以表示放射源可以移动(例如,在机架上旋转)的幅度和方向,使得第一患者靶区域的位置接近治疗计划图像中第一患者靶区域的位置。在一些实施例中,第一组患者位置移动矢量可以反映多达六个校正(即,沿着或围绕患者平台的x轴、y轴和z轴中的每一个的调整量)。在一些实施例中,dicom空间配准对象(sro)可用于确定与第一组患者位置移动矢量相关的六个校正中的每一个(即,沿着或围绕患者平台的x轴、y轴和z轴中的每一个的调整量)。
[0295]
在一些实施例中,第一组患者位置移动矢量可以通过相对于其各自的治疗计划图像移动(例如,通过移位和/或旋转)每个获取的图像以将治疗计划图像的第一治疗区和/或患者靶区域与获取图像的第一患者靶区域对齐或配准来计算。每个获取的图像可以移动特定距离和/或旋转特定量以改善治疗计划图像的第一患者靶区域与获取的图像的第一患者靶区域的配准。例如,可以将治疗时沿轴向平面获取的图像与沿患者轴向平面获取的治疗计划图像进行比较,以确定沿轴向平面内患者表面(例如,平台或床)的横轴(即y轴)和竖轴(即,z轴)所需的校正量和绕机架滚动轴(例如,绕x轴)所需的校正量。可以将治疗时沿矢状平面获取的图像与沿患者矢状平面获取的治疗计划图像进行比较,以确定沿纵轴(即x轴)和竖轴所需的校正量,和矢状平面内患者表面(例如,平台或床)的俯仰校正量(例如,绕y轴旋转)。可以将治疗时沿冠状平面获取的图像与沿患者冠状平面获取的治疗计划图像进行比较,以确定沿横轴和纵轴所需的校正量和冠状平面内患者表面(例如,平台或床)的偏航
校正量(即,绕z轴)。
[0296]
第一组患者位置移动矢量可以反映沿着或围绕x轴、y轴和z轴中的每一个所需的患者表面校正量,以改善在获取治疗计划图像时第一患者靶区域和第一患者靶区域的位置之间的对齐。因此,在一些实施例中,第一组患者位置移动矢量可以包括至少一个患者位置移动矢量,该矢量基于从获取的矢状图像与治疗计划矢状图像的比较和/或获取的冠状图像与治疗计划冠状图像的比较确定的纵向差异反映沿患者表面的x轴的调整。第一组患者位置移动矢量可以包括至少一个患者位置移动矢量,其基于从获取的轴向图像与治疗计划轴向图像的比较和/或获取的冠状图像与治疗计划冠状图像的比较确定的横向差异反映沿患者表面的y轴的调整。第一组患者位置移动矢量可以包括至少一个患者位置移动矢量,其基于从获取的轴向图像与治疗计划轴向图像的比较和/或获取的矢状图像与治疗计划矢状图像的比较确定的垂直差异反映沿患者表面的z轴的调整。在一些实施例中,包括在第一组患者位置移动矢量中的沿患者表面的z轴的调整可以是从获取的轴向图像与治疗计划轴向图像的比较确定的横向差异以及从获取的矢状图像与治疗计划矢状图像的比较确定的横向差异的平均值。
[0297]
关于患者表面绕患者表面轴的旋转和/或放射源绕放射源轴的旋转,第一组患者位置移动矢量可包括基于获取的矢状图像与治疗计划矢状图像的比较的患者表面绕患者表面y轴的旋转校正,和/或基于获取的冠状图像与治疗计划冠状图像的比较的患者表面绕患者表面z轴的旋转校正,和/或基于获取的轴向图像与治疗计划轴向图像的比较的放射源绕放射源x轴(例如,与患者表面的x轴共同延伸的机架的x轴)的旋转校正。例如,移动或摇动获取的矢状或冠状图像以与治疗计划矢状或冠状图像相匹配可以转化为一组患者位置移动矢量,该矢量表示x轴、y轴和z轴的移动。倾斜获取的矢状或冠状图像以与治疗计划矢状或冠状图像相匹配可以转化为表示俯仰和/或滚动位置校正的一组患者位置移动矢量。因此,患者位置或取向应该沿着或围绕x轴、y轴和z轴中的每一个进行调整的量可以基于治疗计划图像和在患者的每个轴向、矢状和冠状平面内拍摄的相应获取图像之间的差异由第一组患者位置移动矢量反映。
[0298]
可以基于获取的图像、第二治疗区和/或患者靶区域的治疗计划图像(本文也称为“第二治疗计划图像”),以及第一组患者位置移动矢量来计算(106)第二组患者位置移动矢量。在一些实施例中,第二组位置移动矢量可以包括距离和/或方向平移。在一些实施例中,方向平移可以包括倾斜角。在一些实施例中,类似于上文关于第一组患者位置移动矢量所描述的,第二组患者位置移动矢量可通过相对于治疗计划图像移动获取的图像以将治疗计划图像的第二患者靶区域与获取图像的第二患者靶区域对齐或配准来计算。例如,所获取图像的每个体素可以沿着或围绕x、y和/或z轴平移,在所获取图像的移动期间保持所获取图像的每个体素彼此的相对位置,直到所获取图像和治疗计划图像相对于第二患者靶区域具有改善的对齐(例如,图像中第二患者靶区域之间的重叠被增加或优化)。然后可以基于所获取图像在被移动到与治疗计划图像的对齐增加之前和之后之间的位置和/或地点差异来计算第二组患者位置移动矢量。第二组患者位置移动矢量可以反映获取图像的每个体素必须平移以改善获取图像的第二患者靶区域与治疗计划图像的第二患者靶区域之间的对齐的距离和/或方向。在一些实施例中,可以基于第一组患者位置移动矢量计算第二组位置移动矢量,使得第二组位置移动矢量中包括的距离和/或方向信息相对于第一组位置移动
矢量,而不是所获取图像的体素的初始坐标。因此,基于第二组患者位置移动矢量的位置和/或取向指令可以包括或对应于记载基于第一组患者位置移动矢量要对患者的位置和/或取向相对于患者的第一位置和/或第一取向进行的修改的指令,使得患者将处于第二位置和/或取向以照射第二治疗区和/或患者靶区域。
[0299]
可以根据第二组患者位置移动矢量定位患者,使得患者从第一位置过渡到第二位置。例如,可以解除治疗放射源,使得第一患者靶区域不被治疗放射源照射,然后可以根据第二组患者位置移动矢量定位患者。根据第二组患者位置移动矢量定位患者可以包括相对于治疗放射源移动患者设置于其上的放射治疗患者平台和/或根据第二组患者位置移动矢量调整放射源的旋转位置。然后可以激活治疗放射源,使得照射第二患者靶区域。在一些实施例中,对于基于光束站的递送,在照射周期期间,可以根据与第一光束站相关联的第一位置处的第一组患者位置移动矢量来定位患者,并且可以根据在患者平台在与第一光束站相关联的第一位置和与第二光束站(例如,与第一光束站相邻的第二光束站)相关联的第二位置之间过渡期间的第二组患者位置移动矢量来定位患者。
[0300]
在一些实施例中,不仅限定第一患者靶区域和第二患者靶区域,该方法还可以包括限定任何合适数量的靶区域,获取每个靶区域的图像,以及基于如上所述的基于第一患者靶区域和第二患者靶区域的患者移动矢量定位患者。例如,对于基于光束站的递送,该方法可以包括限定多个患者靶区域,其中每个患者靶区域可以跨越多个光束站。在一些变体中,可能存在与光束站一样多的患者靶区域。可以获取每个患者靶区域的图像,并且可以如上所述生成与每个限定的患者靶区域相关联的一组位置移动矢量。每个患者靶区域和相关联的一组位置移动矢量可以与特定光束站相关联。在患者和/或患者平台过渡到与每个相应光束站相关联的位置期间,可以基于与该光束站相关联的一组位置移动矢量来定位患者。在一些实施例中,所限定的靶区域(以及相关的患者位置移动矢量组)可以与多于一个的光束站相关联,使得患者可以基于一组位置移动矢量定位而不是在患者平台前进通过一系列两个或更多个光束站时重新定位。因此,限定的靶区域的数量(以及相关联的患者位置移动矢量的相应组)可以等于或小于光束站的数量。
[0301]
附加地,第二组患者位置移动矢量可以包括关于需要通过移动患者平台和/或通过调整放射源耦合(例如,校正机架发射位置)的机架的滚动来实施的任何倾斜、俯仰、偏航和滚动校正的信息,使得第二患者靶区域与第二治疗计划图像中的第二患者靶区域的位置的对齐得到改善。
[0302]
在一些实施例中,类似于上文关于第一组患者位置移动矢量所描述的,第二治疗区和/或患者靶区域的多个二维图像可以沿着不同的取向或平面(例如,三个或更多个取向或平面)获取,并且可以将图像与沿相同取向或平面获取的第二患者靶的对应治疗计划图像进行比较。在一些实施例中,第二患者靶区域的多个二维图像可以与第一患者靶区域获取的用于计算第一组患者位置移动矢量的二维图像相同。可以使用相对于在每个取向沿每个图像平面的第二患者靶区域的位置的变化来计算第二组患者位置移动矢量。例如,获取的图像可以包括患者的第二患者靶区域的获取的轴向图像、获取的矢状图像和获取的冠状图像。当患者以仰卧位躺在诸如患者平台或治疗床的表面上且患者定向为使得患者将首先遇到治疗放射源头部时,所获取的轴向图像可沿患者的轴向平面(例如,将身体分为上部和下部的平面)拍摄,所获取的矢状图像可沿患者的矢状平面(例如,将患者分为左部和右部
的平面)拍摄,以及所获取的冠状图像可沿患者的冠状平面(例如,将患者分成腹部和背部的平面)拍摄。轴向平面与矢状平面垂直设置,并且冠状平面与轴向平面和矢状平面均垂直设置。治疗计划图像可以包括患者的第二患者靶区域的治疗计划轴向图像、治疗计划矢状图像和治疗计划冠状图像。因此,获取的轴向图像对应于治疗计划轴向图像,获取的矢状图像对应于治疗计划矢状图像,获取的冠状图像对应于治疗计划冠状图像。
[0303]
应沿着或围绕x轴、y轴和z轴中的每一个(例如,通过移动患者表面和/或旋转放射源)调整患者位置和/或取向以用于治疗第二患者靶区域的量可以基于第二患者靶区域的治疗计划图像和在患者的轴向、矢状和冠状平面中的每一个内拍摄的第二患者靶区域的相应获取图像之间的差异由第二组患者位置移动矢量反映。在一些实施例中,患者表面的x轴可以平行于患者的矢状平面和冠状平面的交点并且可以设置在矢状平面中。患者表面的y轴可以平行于患者的轴向平面和冠状平面的交点并且可以设置在轴向平面中。患者表面的z轴可以平行于患者的矢状平面和轴向平面的交点并且可以设置在患者的矢状平面或轴向平面中。为了确定第二组患者位置移动矢量,可以将第二患者靶区域的每个获取图像与在同一平面内拍摄的第二患者靶区域的相应治疗计划图像进行比较以确定患者在同一平面内的距离校正和/或旋转校正(例如,通过患者表面的移动和/或放射源的旋转)。第二组患者位置移动矢量中的一个或多个矢量可以表示患者表面将被移动(例如,移位和/或旋转)的幅度和方向,使得第二患者靶区域接近治疗计划图像中第二患者靶区域的位置。第二组患者位置移动矢量中的一个或多个矢量还可以表示放射源可以移动(例如,在机架上旋转)的幅度和方向,使得第二患者靶区域的位置接近治疗计划图像中第二患者靶区域的位置。在一些实施例中,第二组患者位置移动矢量可以反映多达六个校正(即,沿着或围绕患者平台的x轴、y轴和z轴中的每一个的调整量)。在一些实施例中,dicom空间配准对象(sro)可用于确定与第二组患者位置移动矢量相关的六个校正中的每一个(即,沿着或围绕患者平台的x轴、y轴和z轴中的每一个的调整量)。
[0304]
在一些实施例中,可以通过相对于其各自的治疗计划图像移动(例如,通过移位和/或旋转)每个获取的图像以将治疗计划图像的第二患者靶区域与所获取图像的第二患者靶区域对齐或配准来计算第二组患者位置移动矢量。每个获取的图像可以移动特定距离和/或旋转特定量以改善治疗计划图像的第二患者靶区域与获取的图像的第二患者靶区域的配准。例如,可以将治疗时沿轴向平面获取的图像与沿患者轴向平面获取的治疗计划图像进行比较,以确定沿轴向平面内患者表面(例如,平台或床)的横轴(即y轴)和竖轴(即,z轴)所需的校正量,和绕机架滚动轴(例如,绕x轴)所需的校正量。可以将治疗时沿矢状平面获取的图像与沿患者矢状平面获取的治疗计划图像进行比较,以确定沿纵轴(即x轴)和竖轴所需的校正量和矢状平面内患者表面(例如,平台或床)的俯仰校正量(例如,绕y轴旋转)。可以将治疗时沿冠状平面获取的图像与沿患者冠状平面获取的治疗计划图像进行比较,以确定沿横轴和纵轴所需的校正量和冠状平面内患者表面(例如,平台或床)的偏航校正量(即,绕z轴)。
[0305]
第二组患者位置移动矢量可以反映沿着或围绕x轴、y轴和z轴中的每一个所需的患者表面校正量,以改善在获取治疗计划图像时第二患者靶区域和第二患者靶区域的位置之间的对齐。因此,在一些实施例中,第二组患者位置移动矢量可以包括至少一个患者位置移动矢量,该矢量基于从获取的矢状图像与治疗计划矢状图像的比较和/或获取的冠状图
像与治疗计划冠状图像的比较确定的纵向差异反映沿患者表面的x轴的调整。第二组患者位置移动矢量可以包括至少一个患者位置移动矢量,该矢量基于从获取的轴向图像与治疗计划轴向图像的比较和/或获取的冠状图像与治疗计划冠状图像的比较确定的横向差异反映沿患者表面的y轴的调整。第二组患者位置移动矢量可以包括至少一个患者位置移动矢量,该矢量基于从获取的轴向图像与治疗计划轴向图像的比较和/或获取的矢状图像与治疗计划矢状图像的比较确定的垂直差异反映沿患者表面的z轴的调整。
[0306]
关于患者表面绕患者表面轴的旋转和/或放射源绕放射源轴的旋转,第二组患者位置移动矢量可包括基于获取的矢状图像与治疗计划矢状图像的比较的患者表面绕患者表面y轴的旋转校正,基于获取的冠状图像与治疗计划冠状图像的比较的患者表面绕患者表面z轴的旋转校正,和/或者基于获取的轴向图像与治疗计划轴向图像的比较的放射源绕放射源的x轴(例如,与患者表面的x轴共同延伸的机架的x轴)的旋转校正。例如,移动或摇动获取的矢状或冠状图像以与治疗计划矢状或冠状图像相匹配可以转化为一组患者位置移动矢量,该矢量表示x轴、y轴和z轴的移动。倾斜获取的矢状或冠状图像以与治疗计划矢状或冠状图像相匹配可以转化为一组表示俯仰和/或滚动位置校正的患者位置移动矢量。因此,患者位置或取向应该沿着或围绕x轴、y轴和z轴中的每一个进行调整的量可以基于治疗计划图像和在患者的每个轴向、矢状和冠状平面内拍摄的相应获取图像之间的差异由第二组患者位置移动矢量反映。
[0307]
在一些实施例中,第二组患者位置移动矢量可以反映相对于在根据第一组患者位置移动矢量移动之后的患者表面的位置和/或取向沿着或围绕x轴、y轴和z轴中的每一个所需的患者表面的校正量,以改善在获取治疗计划图像时第二患者靶区域与第二患者靶区域的位置之间的对齐。因此,在一些实施例中,可以通过首先确定第二患者靶区域的治疗计划图像和在患者的轴向、矢状和冠状轴中的每一个内拍摄的第二患者靶区域的相应获取图像之间的差异,然后考虑第一组患者位置移动矢量(例如,从所确定的治疗计划图像和获取图像之间的差异减去第一组患者位置移动矢量)使得第二组位置移动矢量相对于第一组患者位置移动矢量,来计算应该沿着或围绕x轴、y轴和z轴中的每一个调整患者位置或取向的量。因此,患者所在的表面可以从与第一组患者位置移动矢量对应的位置和/或取向过渡到与第二组患者位置移动矢量对应的位置和/或取向,而无需在最初获取治疗计划图像时首先返回到表面的位置和/或取向。
[0308]
在一些实施例中,不是将获取的图像的特定体素的坐标位置与治疗计划图像进行比较或将三个二维获取的图像与三个相应的二维治疗计划图像进行比较,而是可以通过将获取的第一患者靶区域的三维图像与第一患者靶区域的三维治疗计划图像进行比较来计算第一组患者位置移动矢量。可以通过将获取的第二患者靶区域的三维图像(与获取的第一患者靶区域的三维图像可以是相同的图像或不同的图像)与第二患者靶区域的三维治疗计划图像相比并考虑第一组患者位置移动矢量(例如,从通过将获取的第二患者靶区域的图像与第二患者靶区域的治疗计划图像进行比较来计算的中间组患者位置移动矢量中减去第一组患者位置移动矢量)来计算第二组患者位置移动矢量。
[0309]
在一些实施例中,可以在激活治疗放射源之前计算第一组和第二组患者位置移动矢量。在一些实施例中,第一治疗计划图像和第二治疗计划图像是相同的治疗计划图像。在一些实施例中,第一治疗计划图像和第二治疗计划图像是不同的治疗计划图像。
[0310]
在一些实施例中,第一位置差和/或第二位置差可被计算并用于确定患者的对应肿瘤或肿瘤部分是否已将形状、大小或位置改变到患者可能无法被定位或定向以使用现有治疗计划有效或准确地接受放射的程度。例如,可以通过将获取的图像中的第一患者靶区域中的特定体素的坐标位置与治疗计划图像中的第一患者靶区域的对应体素的坐标位置进行比较来计算第一位置差。获取的图像中第一患者靶区域的特定体素的位置与治疗计划图像中第一患者靶区域的对应体素的位置之间的距离可以是第一位置差。类似地,可以通过将获取的图像中的第二患者靶区域的特定体素的坐标位置与治疗计划图像中的第二靶区域中的对应体素的坐标位置进行比较来计算第二位置差。获取的图像中第二患者靶区域的特定体素的位置与治疗计划图像中第二患者靶区域的对应体素的位置之间的距离可以是第二位置差。在一些实施例中,第一位置差可以通过将获取的图像中的第一患者靶区域中的患者的横截面的二维图像内的坐标位置与治疗计划图像中第一患者靶区域中患者的横截面的二维图像内的坐标位置进行比较来计算。可以通过将获取的图像中的第二患者靶区域中的患者的横截面的二维图像内的坐标位置与治疗计划图像中第二患者靶区域中患者的横截面的二维图像内的坐标位置进行比较来计算第二位置差。第一位置差和第二位置差可以基于分别包括在如上所述的第一组患者位置移动矢量和第二组患者位置移动矢量中的方向和/或距离信息。在一些实施例中,可以基于包括在第一组患者位置移动矢量和第二组患者位置移动矢量中的方向和/或距离信息来计算第二位置差。在一些实施例中,如果第一位置差和/或第二位置差超过位置差阈值,则可以生成通知和/或可以自动暂停放射治疗期。例如,用于横向、纵向和垂直矫正的患者平台的最大矫正运动约为3cm,并且旋转、俯仰和滚动矫正的最大矫正运动不超过3
°
。在一些实施例中,临床医生或诊所可以选择用于横向、纵向和垂直校正的患者平台的最大校正运动以及用于旋转、俯仰和滚动校正的最大校正运动。例如,用于横向、纵向和垂直矫正的患者平台的最大矫正运动可以从大约1.5cm到大约10cm,和/或用于旋转、俯仰和滚动矫正的最大矫正运动可以从大约2
°
到大约20
°
。因此,位置差阈值将是导致矫正运动在任何方面超过患者平台的最大矫正运动的任何位置差。
[0311]
可以根据第一组患者位置移动矢量将患者定位在第一位置,在(108)。在一些实施例中,可以通过根据第一组患者位置移动矢量相对于治疗放射源移动放置患者的放射治疗患者平台来定位患者。例如,平台可以在照射之前在任何方向上倾斜,这可以包括平台在倾斜取向上相对于治疗放射源的平移。在一些实施例中,放置患者的放射治疗患者平台可以沿着或围绕放射治疗患者平台的x轴、y轴和/或z轴(例如,围绕偏航、俯仰和/或滚动轴)。此外,在一些实施例中,可以调整放射治疗患者平台的偏航和/或俯仰。在一些实施例中,放置患者的放射治疗患者平台可以沿着放射治疗患者平台的x轴、y轴和/或z轴并围绕偏航轴和/或俯仰轴移动,而放射源可以围绕滚动轴(例如,通过机架的移动)移动。作为另一个实例,将患者从第一位置过渡到第二位置可以包括在平台上移动和/或弯曲患者的一部分,例如头部、膝盖或肘部。然后可以激活治疗放射源,使得照射第一患者靶区域。
[0312]
在一些实施例中,可以通过沿计算的滚动校正的相反方向旋转放射源(例如,通过旋转机架)来实现对患者位置的滚动校正(例如,如由第一组患者位置移动矢量限定的)。例如,如果对患者位置的滚动校正是顺时针3
°
,则可以调整放射源的位置以提供来自相对于每个请求放射源递送位置逆时针-3
°
的机架位置(例如,机架发射位置)的放射。因此,如果
治疗计划包括基于治疗计划图像以0
°
的机架从放射源递送放射,并且基于治疗计划图像和获取的图像之间的差异滚动校正为3
°
,则放射源可以逆时针方向3
°
调整并从357
°
而不是0
°
递送放射(例如,放射)。
[0313]
然后可以根据第二组患者位置移动矢量定位患者,使得患者从第一位置过渡到第二位置,在110。与上述类似,根据第二组患者位置移动矢量定位患者可以包括相对于治疗放射源移动放置患者的放射治疗患者平台和/或根据第二组患者位置移动矢量调整放射源的旋转位置。然后可以激活治疗放射源,使得照射第二患者靶区域。
[0314]
在一些实施例中,不仅限定第一患者靶区域和第二患者靶区域,该方法还可以包括限定任何合适数量的靶区域,获取每个靶区域的图像,以及基于如上所述的基于第一患者靶区域和第二患者靶区域的位置移动矢量定位患者。
[0315]
图11b是用于患者设置的方法(200)的一种变体的流程图表示。方法(200)包括在放射治疗期开始时获取(202)一个或多个患者靶区域的图像。在一些实施例中,例如,ct系统可用于在治疗期之前或开始时获取一个或多个图像。在一些实施例中,ct系统可以附接到与旨在在治疗期期间递送放射治疗的放射源相同的机架。在一些实施例中,ct系统可以附接到与支撑放射源的机架不同的机架。可以基于一个或多个患者靶区域在所获取图像中的位置和/或地点以及一个或多个患者靶区域在治疗计划图像中的位置和/或地点来限定(204)一个或多个治疗区。例如,可以将获取的图像和/或治疗计划图像划分为第一治疗区和第二治疗区。每个治疗区可以包括一个或多个患者靶区域,使得可以将获取的图像中的一个或多个患者靶区域与治疗计划图像中的一个或多个对应的患者靶区域进行比较。每个治疗区可以对应于患者的一部分,一个或多个患者靶区域位于该部分内,当在放射治疗期的特定部分期间根据特定设置定位患者时,该部分将被照射。治疗区可映射到一系列患者平台位置或阶段(例如,光束站)和/或一系列患者平台沿其纵轴的运动,其中该治疗区中的一个或多个靶区域与治疗放射源的放射束相交。治疗区可以对应于特定的患者位置和/或平台取向。例如,第一治疗区可以与用于照射第一治疗区内的第一患者靶区域的第一患者位置和取向相关联,并且第二治疗区可以与用于照射第二治疗区内的第二患者靶区域的第二患者位置和取向相关联。因此,在一些实施例中,第一治疗区可以与放射治疗期的第一部分(例如,患者平台通过第一组光束站的移动)、第一患者靶区域和患者的第一位置相关联,并且第二治疗区可以与放射治疗期的第二部分(例如,患者平台通过第二组光束站的移动)、第二患者靶区域和患者的第二位置相关联。
[0316]
可以基于所获取图像中的患者靶区域与治疗计划图像中的患者靶区域之间的位置和/或地点差异为每个治疗区计算(206)一组患者位置移动矢量。可以2d和/或3d将获取的图像中患者靶区域的位置与治疗计划图像中的患者靶区域的位置进行比较。在已经限定了两个治疗区的实施例中,可以为第一治疗区计算第一组患者位置移动矢量并且可以为第二治疗区计算第二组患者位置移动矢量。每组位置移动矢量可以包括距离和/或方向平移。在一些实施例中,方向平移可以包括倾斜角。在一些实施例中,可以通过相对于治疗计划图像移动所获取图像以将治疗计划图像的第一患者靶区域与所获取图像的第一患者靶区域对齐或配准来计算第一组患者位置移动矢量。例如,在一些实施例中,第一患者靶区域可以被划分为可以由体素表示的子区域(例如,子体积),并且所获取图像的第一患者靶区域的每个体素的坐标可以与治疗计划图像中第一患者靶区域的对应体素的坐标进行比较。例
如,所获取图像的每个体素可以沿着或绕x、y和/或z轴平移,在所获取图像的移动期间保持所获取图像的每个体素的每个坐标彼此的相对位置,直到获取的图像和治疗计划图像相对于第一患者靶区域具有改善的对齐(例如,图像中第一患者靶区域之间的重叠增加或优化)。第一组患者位置移动矢量然后可以基于在被移动到与治疗计划图像的对齐增加之前和之后所获取图像之间的位置和/或地点差异来计算。第一组患者位置移动矢量可以反映获取的图像的每个体素必须平移已改善获取的图像的第一患者靶区域与治疗计划图像的第一患者靶区域之间的对齐的距离和/或方向。此外,第一组患者位置移动矢量可以包括或对应于与患者的第一位置和/或第一取向(例如,放置患者的表面的第一位置和/或第一取向)相关的指令,使得患者的第一患者靶区域位于接近在获取治疗计划图像时第一患者靶区域所处的位置。这可以促进更接近治疗计划的治疗放射递送到患者靶区域。此外,第一组患者位置移动矢量可以包括关于需要通过患者平台的定位实现的任何倾斜、俯仰、偏航和/或滚动校正的信息,使得第一患者靶区域的位置接近第一治疗计划图像中的第一患者靶区域的位置。
[0317]
在一些实施例中,第一患者靶区域的获取图像和第一患者靶区域的治疗计划图像各自可以是二维图像。可以将二维获取图像与二维治疗计划图像进行比较以计算第一组患者位置移动矢量。在一些实施例中,第一患者靶区域的多个二维图像可以沿着不同的取向或平面(例如,三个或更多个取向或平面)获取,并且图像可以与沿相同取向或平面获取的第一患者靶区域的对应治疗计划图像进行比较。可以使用在每个取向沿每个图像平面相对于第一患者靶区域的位置的变化来计算第一组患者位置移动矢量。例如,获取的图像可以包括患者的第一患者靶区域的获取的轴向图像、获取的矢状图像和获取的冠状图像。当患者以仰卧位躺在诸如患者平台或治疗床的表面上且患者定向为使得患者将首先遇到治疗放射源头部时,所获取的轴向图像可沿患者的轴向平面(例如,将身体分为上部和下部的平面)拍摄,所获取的矢状图像可沿患者的矢状平面(例如,将患者分为左部和右部的平面)拍摄,并且所获取的冠状图像可沿患者的冠状平面(例如,将患者分成腹部和背部的平面)拍摄。轴向平面与矢状平面垂直设置,并且冠状平面与轴向平面和矢状平面均垂直设置。治疗计划图像可以包括患者的第一患者靶区域的治疗计划轴向图像、治疗计划矢状图像和治疗计划冠状图像。因此,获取的轴向图像对应于治疗计划轴向图像,获取的矢状图像对应于治疗计划矢状图像,并且获取的冠状图像对应于治疗计划冠状图像。
[0318]
应该沿着或围绕x轴、y轴和z轴中的每一个(例如,通过移动患者表面和/或旋转放射源)调整患者位置和/或取向以用于治疗第一患者靶区域的量可以基于治疗计划图像和在患者的轴向、矢状和冠状平面中的每一个内拍摄的相应获取图像之间的差异由第一组患者位置移动矢量反映。在一些实施例中,患者表面的x轴可以平行于患者的矢状平面和冠状平面的交点并且可以设置在矢状平面中。患者表面的y轴可以平行于患者的轴向平面和冠状平面的交点并且可以设置在轴向平面中。患者表面的z轴可以平行于患者的矢状平面和轴向平面的交点并且可以设置在患者的矢状平面或轴向平面中。为了确定第一组患者位置移动矢量,可以将第一患者靶区域的每个获取图像与在同一平面内拍摄的第一患者靶区域的相应治疗计划图像进行比较以确定患者在同一平面内的距离校正和/或旋转校正(例如,通过患者表面的移动和/或放射源的旋转)。第一组患者位置移动矢量中的一个或多个矢量可以表示患者表面将被移动(例如,移位和/或旋转)的幅度和方向,使得第一患者靶区域接
近治疗计划图像中第一患者靶区域的位置。第一组患者位置移动矢量中的一个或多个矢量还可以表示放射源可以移动(例如,在机架上旋转)的幅度和方向,使得第一患者靶区域的位置接近治疗计划图像中第一患者靶区域的位置。在一些实施例中,第一组患者位置移动矢量可以反映多达六个校正(即,沿着或围绕患者平台的x轴、y轴和z轴中的每一个的调整量)。在一些实施例中,dicom空间配准对象(sro)可用于确定与第一组患者位置移动矢量相关的六个校正中的每一个(即,沿着或围绕患者平台的x轴、y轴和z轴中的每一个的调整量)。
[0319]
在一些实施例中,第一组患者位置移动矢量可以通过相对于其各自的治疗计划图像移动(例如,通过移位和/或旋转)每个获取的图像以将治疗计划图像的第一患者靶区域与获取图像的第一患者靶区域对齐或配准来计算。每个获取的图像可以移动特定距离和/或旋转特定量以改善治疗计划图像的第一患者靶区域与获取的图像的第一患者靶区域的配准。例如,可以将治疗时沿轴向平面获取的图像与沿患者轴向平面获取的治疗计划图像进行比较,以确定沿轴向平面内患者表面(例如,平台或床)的横轴(即y轴)和竖轴(即,z轴)所需的校正量和绕机架滚动轴(例如,绕x轴)所需的校正量。可以将治疗时沿矢状平面获取的图像与沿患者矢状平面获取的治疗计划图像进行比较,以确定沿纵轴(即x轴)和竖轴所需的校正量,和矢状平面内患者表面(例如,平台或床)的俯仰校正量(例如,绕y轴旋转)。可以将治疗时沿冠状平面获取的图像与沿患者冠状平面获取的治疗计划图像进行比较,以确定沿横轴和纵轴所需的校正量和冠状平面内患者表面(例如,平台或床)的偏航校正量(即,绕z轴)。
[0320]
第一组患者位置移动矢量可以反映沿着或围绕x轴、y轴和z轴中的每一个所需的患者表面校正量,以改善在获取治疗计划图像时第一患者靶区域和第一患者靶区域的位置之间的对齐。因此,在一些实施例中,第一组患者位置移动矢量可以包括至少一个患者位置移动矢量,该矢量基于从获取的矢状图像与治疗计划矢状图像的比较和/或获取的冠状图像与治疗计划冠状图像的比较确定的纵向差异反映沿患者表面的x轴的调整。第一组患者位置移动矢量可以包括至少一个患者位置移动矢量,其基于从获取的轴向图像与治疗计划轴向图像的比较和/或获取的冠状图像与治疗计划冠状图像的比较确定的横向差异反映沿患者表面的y轴的调整。第一组患者位置移动矢量可以包括至少一个患者位置移动矢量,其基于从获取的轴向图像与治疗计划轴向图像的比较和/或获取的矢状图像与治疗计划矢状图像的比较确定的垂直差异反映沿患者表面的z轴的调整。
[0321]
关于患者表面绕患者表面轴的旋转和/或放射源绕放射源轴的旋转,第一组患者位置移动矢量可包括基于获取的矢状图像与治疗计划矢状图像的比较的患者表面绕患者表面y轴的旋转校正,基于获取的冠状图像与治疗计划冠状图像的比较的患者表面绕患者表面z轴的旋转校正,和/或基于获取的轴向图像与治疗计划轴向图像的比较的放射源绕放射源x轴(例如,与患者表面的x轴共同延伸的机架的x轴)的旋转校正。例如,移动或摇动获取的矢状或冠状图像以与治疗计划矢状或冠状图像相匹配可以转化为一组患者位置移动矢量,该矢量表示x轴、y轴和z轴的移动。倾斜获取的矢状或冠状图像以与治疗计划矢状或冠状图像相匹配可以转化为表示俯仰和/或滚动位置校正的一组患者位置移动矢量。因此,患者位置或取向应该沿着或围绕x轴、y轴和z轴中的每一个进行调整的量可以基于治疗计划图像和在患者的每个轴向、矢状和冠状平面内拍摄的相应获取图像之间的差异由第一组
患者位置移动矢量反映。
[0322]
在一些实施例中,类似于上文关于第一组患者位置移动矢量所描述的,第二组患者位置移动矢量可通过相对于治疗计划图像移动获取的图像以将治疗计划图像的第二患者靶区域与获取图像的第二患者靶区域对齐来计算。例如,在一些实施例中,第二患者靶区域可以被划分为可以由体素表示的子区域(例如,子体积),并且所获取图像的第二患者靶区域的每个体素的坐标可以与治疗计划图像中第二患者靶区域的对应体素的坐标进行比较。例如,所获取图像的每个体素可以沿着或围绕x、y和/或z轴平移,在所获取图像的移动期间保持所获取图像的每个体素彼此的相对位置,直到所获取图像和治疗计划图像相对于第二患者靶区域具有改善的对齐(例如,图像中第二患者靶区域之间的重叠被增加或优化)。然后可以基于所获取图像在被移动到与治疗计划图像的对齐增加之前和之后之间的位置和/或地点差异来计算第二组患者位置移动矢量。第二组患者位置移动矢量可以反映必须平移获取的图像的每个体素以改善获取的图像的第二患者靶区域与治疗计划图像的第二患者靶区域之间的对齐的距离和/或方向。在一些实施例中,可以基于第一组患者位置移动矢量计算第二组位置移动矢量,使得第二组位置移动矢量中包括的距离和/或方向信息相对于第一组患者位置移动矢量,而不是所获取图像的体素的初始坐标。因此,基于第二组患者位置移动矢量的位置和/或取向指令可以包括或对应于记载基于第一组患者位置移动矢量要对患者的位置和/或取向相对于患者的第一位置和/或第一取向进行的修改的指令,使得患者将处于第二位置和/或取向以照射第二患者靶区域。附加地,第二组患者位置移动矢量可以包括关于需要通过移动患者平台和/或通过调整放射源耦合(例如,校正机架发射位置)的机架的滚动来实施的任何倾斜、俯仰、偏航和滚动校正的信息,使得第二患者靶区域与第一治疗计划图像中的第一患者靶区域的位置的对齐得到改善。
[0323]
在一些实施例中,与上文关于第一组患者位置移动矢量所描述的类似,可以沿着不同的取向或平面(例如,三个或更多个取向或平面)获取第二患者靶区域的多个二维图像,并且可以将图像与沿相同取向或平面获取的第二患者靶的对应治疗计划图像进行比较。在一些实施例中,第二患者靶区域的多个二维图像可以与第一患者靶区域获取的用于计算第一组患者位置移动矢量的二维图像相同。可以使用相对于在每个取向沿每个图像平面的第二患者靶区域的位置的变化来计算第二组患者位置移动矢量。例如,获取的图像可以包括患者的第二患者靶区域的获取的轴向图像、获取的矢状图像和获取的冠状图像。当患者以仰卧位躺在诸如患者平台或治疗床的表面上且患者定向为使得患者将首先遇到治疗放射源头部时,所获取的轴向图像可沿患者的轴向平面(例如,将身体分为上部和下部的平面)拍摄,所获取的矢状图像可沿患者的矢状平面(例如,将患者分为左部和右部的平面)拍摄,并且所获取的冠状图像可沿患者的冠状平面(例如,将患者分成腹部和背部的平面)拍摄。轴向平面与矢状平面垂直设置,并且冠状平面与轴向平面和矢状平面均垂直设置。治疗计划图像可以包括患者的第二患者靶区域的治疗计划轴向图像、治疗计划矢状图像和治疗计划冠状图像。因此,获取的轴向图像对应于治疗计划轴向图像,获取的矢状图像对应于治疗计划矢状图像,并且获取的冠状图像对应于治疗计划冠状图像。
[0324]
应沿着或围绕x轴、y轴和z轴中的每一个(例如,通过移动患者表面和/或旋转放射源)调整患者位置和/或取向以用于治疗第二患者靶区域的量可以基于第二患者靶区域的治疗计划图像和在患者的轴向、矢状和冠状平面中的每一个内拍摄的第二患者靶区域的相
应获取图像之间的差异由第二组患者位置移动矢量反映。在一些实施例中,患者表面的x轴可以平行于患者的矢状平面和冠状平面的交点并且可以设置在矢状平面中。患者表面的y轴可以平行于患者的轴向平面和冠状平面的交点并且可以设置在轴向平面中。患者表面的z轴可以平行于患者的矢状平面和轴向平面的交点并且可以设置在患者的矢状平面或轴向平面中。为了确定第二组患者位置移动矢量,可以将第二患者靶区域的每个获取图像与在同一平面内拍摄的第二患者靶区域的相应治疗计划图像进行比较以确定患者在同一平面内的距离校正和/或旋转校正(例如,通过患者表面的移动和/或放射源的旋转)。第二组患者位置移动矢量中的一个或多个矢量可以表示患者表面将被移动(例如,移位和/或旋转)的幅度和方向,使得第二患者靶区域接近治疗计划图像中第二患者靶区域的位置。第二组患者位置移动矢量中的一个或多个矢量还可以表示放射源可以移动(例如,在机架上旋转)的幅度和方向,使得第二患者靶区域的位置接近治疗计划图像中第二患者靶区域的位置。在一些实施例中,第二组患者位置移动矢量可以反映多达六个校正(即,沿着或围绕患者平台的x轴、y轴和z轴中的每一个的调整量)。在一些实施例中,dicom空间配准对象(sro)可用于确定与第二组患者位置移动矢量相关的六个校正中的每一个(即,沿着或围绕患者平台的x轴、y轴和z轴中的每一个的调整量)。
[0325]
在一些实施例中,可以通过相对于其各自的治疗计划图像移动(例如,通过移位和/或旋转)每个获取的图像以将治疗计划图像的第二患者靶区域与所获取图像的第二患者靶区域对齐或配准来计算。每个获取的图像可以移动特定距离和/或旋转特定量以改善治疗计划图像的第二患者靶区域与获取的图像的第二患者靶区域的配准。例如,可以将治疗时沿轴向平面获取的图像与沿患者轴向平面获取的治疗计划图像进行比较,以确定沿轴向平面内患者表面(例如,平台或床)的横轴(即y轴)和竖轴(即,z轴)所需的校正量和绕机架滚动轴(例如,绕x轴)所需的校正量。可以将治疗时沿矢状平面获取的图像与沿患者矢状平面获取的治疗计划图像进行比较,以确定沿纵轴(即x轴)和竖轴所需的校正量,和矢状平面内患者表面(例如,平台或床)的俯仰校正量(例如,绕y轴旋转)。可以将治疗时沿冠状平面获取的图像与沿患者冠状平面获取的治疗计划图像进行比较,以确定沿横轴和纵轴所需的校正量和冠状平面内患者表面(例如,平台或床)的偏航校正量(即,绕z轴)。
[0326]
第二组患者位置移动矢量可以反映沿着或围绕x轴、y轴和z轴中的每一个所需的患者表面校正量,以改善获取治疗计划图像时第二患者靶区域和第二患者靶区域的位置之间的对齐。因此,在一些实施例中,第二组患者位置移动矢量可以包括至少一个患者位置移动矢量,该矢量基于从获取的矢状图像与治疗计划矢状图像的比较和/或获取的冠状图像与治疗计划冠状图像的比较确定的纵向差异反映沿患者表面的x轴的调整。第二组患者位置移动矢量可以包括至少一个患者位置移动矢量,该矢量基于从获取的轴向图像与治疗计划轴向图像的比较和/或获取的冠状图像与治疗计划冠状图像的比较确定的横向差异反映沿患者表面的y轴的调整。第二组患者位置移动矢量可以包括至少一个患者位置移动矢量,该矢量基于从获取的轴向图像与治疗计划轴向图像的比较和/或获取的矢状图像与治疗计划矢状图像的比较确定的垂直差异反映沿患者表面的z轴的调整。
[0327]
关于患者表面绕患者表面轴的旋转和/或放射源绕放射源轴的旋转,第二组患者位置移动矢量可包括基于获取的矢状图像与治疗计划矢状图像的比较的患者表面绕患者表面y轴的旋转校正,基于获取的冠状图像与治疗计划冠状图像的比较的患者表面绕患者
表面z轴的旋转校正,和/或者基于获取的轴向图像与治疗计划轴向图像的比较的放射源绕放射源的x轴(例如,与患者表面的x轴共同延伸的机架的x轴)的旋转校正。例如,移动或摇动获取的矢状或冠状图像以与治疗计划矢状或冠状图像相匹配可以转化为一组患者位置移动矢量,该矢量表示x轴、y轴和z轴的移动。倾斜获取的矢状或冠状图像以与治疗计划矢状或冠状图像相匹配可以转化为表示俯仰和/或滚动位置校正的一组患者位置移动矢量。因此,患者位置或取向应该沿着或围绕x轴、y轴和z轴中的每一个进行调整的量可以基于治疗计划图像和在患者的每个轴向、矢状和冠状平面内拍摄的相应获取图像之间的差异由第二组患者位置移动矢量反映。
[0328]
在一些实施例中,第二组患者位置移动矢量可以反映相对于在根据第一组患者位置移动矢量移动之后的患者表面的位置和/或取向沿着或围绕x轴、y轴和z轴中的每一个所需的患者表面的校正量,以改善在获取治疗计划图像时第二患者靶区域与第二患者靶区域的位置之间的对齐。因此,在一些实施例中,可以通过首先确定第二患者靶区域的治疗计划图像和在患者的轴向、矢状和冠状轴中的每一个内拍摄的第二患者靶区域的相应获取图像之间的差异,然后考虑第一组患者位置移动矢量(例如,从所确定的治疗计划图像和获取图像之间的差异减去第一组患者位置移动矢量)使得第二组位置移动矢量相对于第一组患者位置移动矢量,来计算应该沿着或围绕x轴、y轴和z轴中的每一个调整患者位置或取向的量。因此,患者所在的表面可以从与第一组患者位置移动矢量对应的位置和/或取向过渡到与第二组患者位置移动矢量对应的位置和/或取向,而无需在最初获取治疗计划图像时首先返回到表面的位置和/或取向。
[0329]
在一些实施例中,不是将获取的图像的特定体素的坐标位置与治疗计划图像进行比较或将三个二维获取的图像与三个相应的二维治疗计划图像进行比较,而是可以通过将获取的第一患者靶区域的三维图像与第一患者靶区域的三维治疗计划图像进行比较来计算第一组患者位置移动矢量。可以通过将获取的第二患者靶区域的三维图像(与获取的第一患者靶区域的三维图像可以是相同的图像或不同的图像)与第二患者靶区域的三维治疗计划图像相比并考虑第一组患者位置移动矢量(例如,从通过将获取的第二患者靶区域的图像与第二患者靶区域的治疗计划图像进行比较来计算的中间组患者位置移动矢量中减去第一组患者位置移动矢量)来计算第二组患者位置移动矢量。
[0330]
可以根据第一组患者位置移动矢量将患者定位(208)到第一取向。定位可以包括,例如,将患者以特定姿势布置在患者平台上和/或根据第一组患者位置移动矢量在任何合适的方向上定向或倾斜患者平台。如下文进一步描述的,当患者处于第一取向时,治疗放射可被递送(210)到患者的第一靶区域。在一些实施例中,不是患者的第一取向与第一组患者平台移动相关联,而是第一取向可以仅与一个患者平台阶段或位置(例如,光束站)相关联。
[0331]
可以根据第二组患者位置移动矢量将患者定位(212)到第二取向。定位可以包括,例如,将患者以特定姿势布置在患者平台上和/或根据第二组患者位置移动矢量在任何合适的方向上定向或倾斜患者平台。然后可以在患者处于第二取向时将治疗放射递送(214)到患者的第二靶区域。在一些实施例中,不是患者的第二取向与第二组患者平台移动相关联,而是第二取向可以仅与一个患者平台阶段或位置相关联(例如,与和第一取向相关联的光束台相邻的光束台)。
[0332]
在一些实施例中,在将治疗放射递送给患者的同时,患者可以相对于治疗放射源
连续移动。例如,可以通过旋转和/或倾斜患者平台和/或旋转在其上设置有治疗放射源的机架而将患者定位在第一取向。患者平台然后可以相对于(例如,通过)治疗放射源的放射束路径或束平面连续移动,使得放射被递送到患者的第一靶区域。在将放射递送到患者的第一靶区域之后,可以通过旋转和/或倾斜患者平台和/或旋转其上设置有治疗放射源的机架来将患者定位在第二取向。患者平台然后可以相对于(例如,通过)治疗放射源的放射束路径或束平面连续移动,使得放射被递送到患者的第二靶区域。
[0333]
在一些实施例中,患者可以相对于治疗放射源移动通过一系列离散的、预限定的位置,并且可以在患者相对于治疗放射源静止时递送放射。例如,患者可以相对于治疗放射源移动到第一取向并且定位,使得患者相对于治疗放射源固定不动。放射束然后可以在特定的时间长度和/或在患者平台相对于治疗放射源的第一系列步进运动期间被施加到患者的第一患者靶区域。在治疗放射源安装在围绕患者旋转的可旋转机架上的变体中,可以在围绕患者的一个或多个旋转或循环内施加放射。例如,在圆形、连续旋转的机架中,可以在治疗放射源围绕患者旋转数次内施加放射。在根据治疗计划照射患者靶区域之后,可以关闭放射束并且可以将患者平台移动到下一个预定位置,并且可以如上所述对患者施加放射(并且根据需要重复)。因此,在根据治疗计划将放射束施加到第一靶区域之后,可以调整平台和/或患者以使得患者过渡到第二取向和位置。当处于第二取向和位置时,患者可以相对于治疗放射源固定不动。然后,可以在特定的时间长度内,在患者平台相对于治疗放射源的第二系列步进运动期间,将放射束施加到患者的第二靶区域,和/或在可旋转机架的一个或多个旋转或循环内将放射施加到第二靶区域(与上述类似)。在根据治疗计划照射第二患者靶区域之后,可以关闭放射束。如果有额外的患者靶区域要被照射,则可以将患者和/或患者平台调整到下一个预定位置。在2017年9月22日提交的美国临时申请第62/562,212号中描述了包括放射递送方法的放射治疗系统的附加细节和变体,其全部内容通过引用并入本文。
[0334]
在一些实施例中,用户可以指定限制设置校正的自动应用的标准以避免临床上不准确的位置校正和/或不可行的位置校正。例如,用户可以设置从图像获取到照射时间的阈值持续时间。阈值持续时间可以基于所获取图像仍然可能是准确的时间段。如果时间阈值过去了,则可以提醒用户并且停止放射治疗期。类似地,用户可以基于经过的治疗时间限制设置校正的自动应用。因此,如果计算出的一个或多个靶的位置可能仅在某个持续时间内一致,则用户可以在必须中断放射治疗期之前对治疗持续时间设置限制,和/或对新的/更新的获取的一个或多个靶区域的图像设置限制。可以包括的另一个标准是可以限制靶区域或靶肿瘤之间的距离,使得如果靶区域或靶肿瘤之间的距离超过距离阈值,则可以在放射治疗期开始之前通知用户。该距离可以基于靶区域中的一个或两个的位置的准确度可能不准确的距离。在一些实施例中,距离阈值可以基于临床协议。例如,距离阈值可以是大约30cm。此外,递送的监控单元(mu)的数量可用于确定系统是否可能提供临床上不准确的位置校正。例如,可以基于计划递送的总mu在放射治疗期开始之前向用户提供通知。
[0335]
此外,在一些实施例中,如果生成一组患者移位矢量并且对应的患者位置不可行,则可以生成对用户的通知和/或可以进行调整。例如,如果这组患者移位矢量表明斜面的倾斜角度太陡而不能安全实施,则可以通知用户和/或进行调整。此外,如果该组患者移位矢量表明将导致与患者治疗系统的另一部分碰撞的患者和/或平台的定位,则可以通知用户
和/或进行调整。在一些实施例中,系统可以被配置为基于预先确定的阈值和/或界限条件通知用户和/或进行调整,例如预先确定的平台斜面阈值或代表其他系统部件的位置的界限。在一些实施例中,可以生成替代定位指令,代表例如替代倾斜角。在一些实施例中,可以生成表示替代定位指令的效果的通知(例如,表示倾斜角不同的特定度数以特定量改变与患者靶区域的对齐)以供用户考虑。
[0336]
图12a-12f示出了可以调整患者位置的过程。例如,图12a表示在放射治疗期之前获取的治疗计划图像(322)。治疗计划图像(322)可用于准备在放射治疗期期间照射患者肿瘤的治疗计划。如所示的,治疗计划图像(322)可以包括分别代表肿瘤的第一部分和第二部分的第一患者靶区域(324)和第二患者靶区域(326)。图12b表示在放射治疗期之前或开始时通过成像获取的获取图像(332)。获取图像(332)可以包括分别代表肿瘤的第一部分和第二部分的第一患者靶区域(334)和第二患者靶区域(336)。治疗计划图像(322)和获取的图像(332)可以通过任何合适的成像方法获取,例如通过pet或ct扫描。治疗计划图像(322)和获取图像(332)可以是二维图像。
[0337]
图12c是与治疗计划图像(322)重叠的获取图像(332)的表示,使得治疗计划图像(322)的第一患者靶区域(324)和第二患者靶区域(326)的形状、大小和位置可以与获取图像(332)的第一患者靶区域(334)和第二患者靶区域(336)的形状、大小和位置进行比较。如图12c所示,治疗计划图像(322)的第一患者靶区域(324)和第二患者靶区域(326)以及获取图像(332)的第一患者靶区域(334)和第二患者靶区域(336)未对齐或完全重合。特别地,治疗计划图像(322)的第一患者靶区域(324)和获取的图像(332)的第一患者靶区域(334)是共同定位的并且看起来对齐,但是治疗计划图像(322)的第二患者靶区域(326)和获取图像(332)的第二患者靶区域(336)没有共同定位。可如图12c所示,获取图像(332)的第二患者靶区域(336)相对于治疗计划图像(322)的第二患者靶区域(326)以一定角度设置。可以通过定位和定向患者以使得患者的第二患者靶区域与治疗计划图像(322)的第二患者靶区域(326)的位置共同定位或更接近共同定位来提高治疗计划的准确性以用于将放射递送到第二患者靶区域。
[0338]
一个或多个治疗区可以基于获取图像(332)的每一部分的位置和地点以及治疗计划图像(322)的每一部分的位置和地点来限定。如图12d所示,用户可以指定第一治疗区r1(例如,经由与放射治疗系统相关联的图形用户界面)。由于治疗计划图像(322)的第一患者靶区域(324)和获取图像(332)的第一患者靶区域(324)在图12c所示的初始比较中被示出为共同定位并且共同扩展,所以第一治疗区r1内的治疗计划图像(322)和获取图像(332)之间不存在位置和/或地点差异。因此,在向第一治疗区r1内的患者递送治疗放射之前不需要位置移动。在一些实施例中,可以针对第一治疗区r1计算第一组患者位置移动矢量,该矢量反映沿着或围绕x、y和z轴(例如,围绕偏航、俯仰和/或滚动轴)的平移在开始将治疗放射递送到第一患者靶区域之前的患者设置期间不是必要的。例如,在一些实施例中,第一患者靶区域可以被划分为可以由体素表示的子区域(例如,子体积),并且获取图像(332)的第一患者靶区域(334)的每个体素的坐标可以与治疗计划图像(322)中的第一患者靶区域(324)的对应体素的坐标进行比较。如果第一组患者位置移动矢量通过包括获取图像(332)的每个体素的位置变化矢量反映与获取图像(332)和治疗计划图像(322)之间的差异相对应的获取图像(332)的每个体素的新坐标位置,则对应于第一治疗区r1的位置移动矢量可以反映
为零。在一些实施例中,不是将第一患者靶区域划分为多个子区域以将获取图像(332)中的子区域的位置与治疗计划图像(322)进行比较,而是第一组患者位置移动矢量可以反映获取图像(332)可以在同一平面中相对于治疗计划图像(322)移动(例如,平移和/或旋转)以改善第一患者靶区域(324)和第二患者靶区域(326)之间的对齐(例如,重叠)的距离和/或方向。如果获取图像(332)相对于治疗计划图像(322)不移动将改善第一患者靶区域(324)和第二患者靶区域(326)之间的对齐,则对应于第一治疗区r1的第一组位置变化矢量可以反映为零。
[0339]
如图12e所示,用户可以指定第二治疗区r2。获取图像(332)可以相对于治疗计划图像(322)移动以在第二治疗区r2内将治疗计划图像(322)与获取图像(332)对齐。在一些实施例中,第二患者靶区域可以被划分为可以由体素表示的子区域(例如,子体积),以及获取图像(332)的第二患者靶区域(336)的每个体素的坐标可以与治疗计划图像(322)中的第二患者靶区域(326)的对应体素的坐标进行比较。例如,获取图像(332)的每个体素可以沿着或围绕x、y和/或z轴平移,直到治疗计划图像(322)的第二患者靶区域(326)和获取图像(332)的第二患者靶区域(336)对齐和/或共同定位。例如,如图12e所示,获取图像(332)可以相对于治疗计划图像(322)逆时针旋转,直到治疗计划图像(322)和获取图像(332)对齐和/或第二患者靶区域(336)和第二患者靶区域(326)之间的重叠在第二治疗区r2内增加。可以基于第二治疗区r2中获取图像(332)移动之前治疗计划图像(322)和获取图像(332)之间的位置和/或地点差异计算对应于第二治疗区r2的第二组患者位置移动矢量以改善与治疗计划图像(322)的重叠。在一些实施例中,第二组患者位置移动矢量可以反映获取图像(332)的每个体素被平移以改善第二患者靶区域(336)和第二患者靶区域(326)之间的对齐的距离和/或方向。在一些实施例中,第二组患者位置移动矢量可以反映获取图像(332)可以在同一平面中相对于治疗计划图像(322)平移和/或旋转以改善第二患者靶区域(336)和第二患者靶区域(326)之间的对齐(例如,重叠)的距离和/或方向。此外,第二组患者位置移动矢量可以包括和/或对应于关于应该如何定位和定向患者以递送治疗放射(例如,通过其上设置有患者的平台的定位和/或定向)的指令,使得患者的第二靶区域可以比如果患者被布置在他们在获取治疗计划图像期间所处的位置更准确地被照射(例如,如果其上设置有患者的平台处于与获取治疗计划图像期间相同的位置和/或取向)。
[0340]
如图12f所示,然后可以相对于放射治疗系统的治疗放射源定位患者,使得可以将放射有效地施加到患者的靶区域。例如,患者可以在患者设置期间根据第一组患者位置移动矢量定位在第一取向。在这种情况下,第一组患者位置移动矢量表示从治疗计划图像(322)中的第一患者靶区域(324)到获取图像(332)中的第一患者靶区域(334)之间没有位置或地点差异。因此,可以根据治疗计划图像(322)中表示的治疗计划来定位患者。接下来,当患者处于第一取向时(例如,在相对于治疗放射源平移患者通过放射治疗系统时),治疗放射可以被递送到第一患者靶区域,如箭头tx1所示。
[0341]
在患者处于第一取向时向第一患者靶区域递送治疗放射之后,患者可以根据第二组患者位置移动矢量定位在第二取向。接着,当患者处于第二方位时(例如,当相对于治疗放射源平移患者通过放射治疗系统时),治疗放射可以被递送到第二患者靶区域,如箭头tx2所示。
[0342]
图13a-13f示出了可以调整患者位置的过程。例如,图13a表示在放射治疗期之前
获取的治疗计划图像(422)。治疗计划图像(422)可用于生成用于在放射治疗期期间照射患者的肿瘤的治疗计划。如所示的,治疗计划图像(422)可以包括分别代表肿瘤的第一部分和第二部分的第一患者靶区域(424)和第二患者靶区域(426)。图13b表示在放射治疗期之前或开始时通过成像获取的获取图像(432)。获取图像(432)可以包括分别代表肿瘤的第一部分和第二部分的第一患者靶区域(434)和第二患者靶区域(436)。治疗计划图像(422)和获取图像(432)可以通过任何合适的成像方法获取,例如,通过pet或ct扫描。治疗计划图像(422)和获取图像(432)可以是二维图像。
[0343]
图13c是与治疗计划图像(422)重叠的获取图像(432)的表示,使得治疗计划图像(422)的第一患者靶区域(424)和第二患者靶区域(426)的形状、大小和位置可以与获取图像(432)的第一患者靶区域(434)和第二患者靶区域(424)的形状、大小和位置进行比较。如图13c所示,治疗计划图像(422)的第一患者靶区域(424)和第二患者靶区域(426)未分别与获取图像(432)的第一患者靶区域(434)和第二患者靶区域(436)对齐或完全重合。可如图13c所示,获取图像(432)的第一患者靶区域(434)和第二患者靶区域(436)各自分别相对于治疗计划图像(422)的第一患者靶区域(424)和第二患者靶区域(426)成一定角度设置。因此,治疗计划的准确性可以如下改善:定位和/或定向患者,使得第一患者靶区域与治疗计划图像(422)的第一患者靶区域(424)的位置共同定位或更接近共同定位以用于将放射递送到第一患者靶区域,并重新定位和/或重新定向患者,使得患者的第二患者靶区域与治疗计划图像(422)的第二患者靶区域(426)的位置共同定位或更接近共同定位以用于将放射递送到第二患者靶区域。
[0344]
一个或多个治疗区可以基于获取图像(432)的每个部分的位置和地点以及治疗计划图像(422)的每个部分的位置和地点来限定。如图13d所示,用户可以指定第一治疗区r1(例如,经由与放射治疗系统相关联的图形用户界面)。获取图像(432)可以相对于治疗计划图像(422)移动以将第一治疗区r1内的治疗计划图像(422)与获取图像(432)对齐。在一些实施例中,第一患者靶区域可以被划分为可以由体素表示的子区域(例如,子体积),并且获取图像(432)的第一患者靶区域(434)的每个体素的坐标可以与治疗计划图像(422)中的第一患者靶区域(424)的对应体素的坐标进行比较。例如,获取图像(432)的每个体素可以沿着或围绕x、y和/或z轴平移,直到获取图像(432)和治疗计划图像(422)对齐和/或共同定位。例如,如图13d所示,获取图像(432)可以相对于治疗计划图像(422)顺时针旋转,直到治疗计划图像(422)和获取图像(432)对齐和/或第一患者靶区域(422)和第一患者靶区域(426)之间的重叠(424)在第一治疗区r1内增加。可以基于第一治疗区r1中在获取图像(432)移动之前治疗计划图像(422)和获取图像(432)之间的位置和/或地点差异来计算对应于第一治疗区r1的第一组患者位置移动矢量以改善与治疗计划图像(422)的重叠。第一组患者位置移动矢量可以反映获取图像(432)的每个体素被平移以改善获取图像(432)的第一患者靶区域(434)和治疗计划图像(422)的第一患者靶区域(424)之间的对齐的距离和/或方向。在一些实施例中,不是将第一患者靶区域划分为多个子区域以将获取图像(432)中的子区域的位置与治疗计划图像(422)进行比较,而是第一组患者位置移动矢量可以反映获取图像(432)可以在同一平面中相对于治疗计划图像(422)移动(例如,平移和/或旋转)以改善第一患者靶区域(424)和第一患者靶区域(426)之间的对齐(例如,重叠)的距离和/或方向。此外,第一组患者位置移动矢量可以包括和/或对应于关于用于递送治疗放
射的患者的第一位置和/或取向的指令(例如,经由其上设置有患者的平台的定位和/或定向)使得患者的第一患者靶区域可以比如果患者被安排在他们在获取治疗计划图像期间所处的位置更准确地被照射(例如,如果其上设置有患者的平台处于与治疗计划图像获取期间相同的位置和/或取向)。
[0345]
如图13e所示,用户可以指定第二治疗区r2。与上面参考图13d描述的类似,获取图像(432)可以相对于治疗计划图像(422)移动以在第二治疗区r2内将治疗计划图像(422)与获取图像(432)对齐和/或共同定位。在一些实施例中,第二患者靶区域可以被划分为可以由体素表示的子区域(例如,子体积),并且获取图像(432)的第二患者靶区域(436)的每个体素的坐标可以与治疗计划图像(422)中的第二患者靶区域(426)的对应体素的坐标进行比较。如图13e所示,获取图像(432)可以相对于治疗计划图像(422)逆时针旋转,直到治疗计划图像(422)和获取图像(432)对齐和/或第二患者靶区域(422)和第二患者靶区域(436)之间的重叠(426)在第二治疗区r2内增加。可基于第二治疗区r2中的治疗计划图像(422)、获取图像(432)之间的位置和/或地点差异和第一组患者位置移动矢量来计算对应于第二治疗区r2的第二组患者位置移动矢量。例如,第二组患者位置移动矢量可以基于获取图像(432)移动之前治疗计划图像(422)和获取图像(432)之间的差异来计算,以改善与治疗计划图像(422)的重叠。在一些实施例中,第二组患者位置移动矢量可以反映所获取图像(432)的每个体素被平移以改善获取图像(432)的第二患者靶区域(436)和治疗计划图像(422)的第二患者靶区域(426)之间的对齐的距离和/或方向。在一些实施例中,第二组患者位置移动矢量可以反映获取图像(432)可以在同一平面中相对于治疗计划图像(422)平移和/或旋转以改善第二患者靶区域(436)和第二患者靶区域(426)之间的对齐(例如,重叠)的距离和/或方向。可以基于第一组患者位置移动矢量计算第二组患者位置移动矢量,因为在确定反映治疗计划图像(422)和获取图像(432)之间的差异的一组初步位置移动矢量之后,可以基于在患者的第一患者靶区域的照射期间患者的第一位置和/或取向来计算第二组患者位置移动矢量。此外,第二组患者位置移动矢量可以包括用于重新定位和/或重新定向患者的指令(例如,通过定位和/或定向其上设置有患者的平台)以基于患者的第一位置/取向递送治疗放射。
[0346]
如图13f所示,然后可以相对于放射治疗系统的治疗放射源定位患者,使得可以将放射有效地施加到患者的靶区域。例如,在患者设置期间,患者可以根据第一组患者位置移动矢量以第一取向定位在患者平台上。然后,治疗放射可以被递送到第一患者靶区域,同时患者处于第一取向并且移动通过一系列患者平台位置进入治疗放射源的放射束,如箭头tx1所示。例如,患者平台移动的第一范围或组可以对应于第一患者靶区域的照射,并且患者平台移动的第二范围或组可以对应于第二患者靶区域的照射。因此,平台可以在第一取向上相对于治疗放射源移动通过第一范围组患者平台运动(例如,第一组患者平台阶段或位置)并且患者被布置在患者平台上的第一位置,同时递送治疗放射。在一些实施例中,不是患者的第一取向与第一组患者平台移动相关联,而是第一取向可以与第一组一个或多个患者平台阶段或位置(例如,一个或多个光束站)相关联。例如,第一取向可以与单个第一光束站相关联。在一些实施例中,患者平台可以在患者处于第一取向时在将治疗放射递送到第一患者区域期间相对于(例如,通过)治疗放射源的放射束路径或束平面连续移动(例如,沿着患者表面的y轴)。替代地或附加地,在治疗放射的递送期间患者平台可以步进通过多
个光束站并且停在光束站处。
[0347]
在患者处于第一取向时向第一患者靶区域递送治疗放射之后,可以停止递送治疗放射并且可以根据第二组患者位置移动矢量将患者定位在第二取向。例如,患者平台可以停止通过系统前进并且可以通知用户调整设置位置。接下来,治疗放射可以在患者处于第二取向时被递送到第二患者靶区域并且移动通过一系列患者平台位置进入治疗放射源的放射束,如箭头tx2所示。例如,平台可以在第二取向上相对于治疗放射源移动通过第二范围或组的患者平台移动(例如,第二范围或组的患者平台阶段或位置,或光束站),并且在递送治疗放射时患者布置在患者平台上的第二位置取向。在一些实施例中,不是患者的第二取向与第二组患者平台移动相关联,而是第二取向可以与第二组一个或多个患者平台阶段或位置(例如,一个或多个光束站,与和第一取向相关联的光束站相邻的光束站)相关联。例如,第二取向可以与单个第二光束站相关联。在一些实施例中,患者平台可以在患者处于第二取向时在将治疗放射递送到第二患者区域期间相对于(例如,通过)治疗放射源的放射束路径或束平面连续(例如,沿着患者表面的y轴)移动。替代地或附加地,在治疗放射的递送期间患者平台可以步进通过多个光束站并且在光束站处停止。
[0348]
图14a-14f示出了可以调整患者位置的过程。例如,图14a表示在放射治疗期之前获取的治疗计划图像(522)。在放射治疗期期间,治疗计划图像(522)可用于准备用于照射患者的两个或更多个肿瘤,例如位于患者不同身体区域的肿瘤的治疗计划。例如,肿瘤可能位于患者的头部和胸部或患者的颈部和肺部。如所示的,治疗计划图像(522)可以包括分别代表第一肿瘤和第二肿瘤的第一患者靶区域(524)和第二患者靶区域(526)。图14b表示在放射治疗期之前或开始时通过成像获取的获取图像(532)。获取图像(532)可以包括分别代表第一肿瘤和第二肿瘤的第一患者靶区域(534)和第二患者靶区域(536)。如可以分别在图14a和14b的代表性治疗计划图像(522)和获取图像(532)中看到的,第一肿瘤和第二肿瘤具有不同的形状,第一肿瘤具有圆形边缘并且第二肿瘤具有锐利边缘。治疗计划图像(522)和获取图像(532)可以通过任何合适的成像方法获取,如例如通过pet或ct扫描。治疗计划图像(522)和获取图像(532)可以是二维图像。
[0349]
图14c是与治疗计划图像(522)重叠的获取图像(532)的表示,使得治疗计划图像(522)的第一患者靶区域(524)和第二患者靶区域(526)的形状、大小和位置可以与获取图像(532)的第一患者靶区域(534)和第二患者靶区域(536)的形状、大小和位置进行比较。如图14c所示,治疗计划图像(522)的第一患者靶区域(524)和第二患者靶区域(526)未分别与获取图像(532)的第一患者靶区域(534)和第二患者靶区域(536)对齐或完全重合。如图14c中可以看到的,获取图像(532)的第一患者靶区域(534)和第二患者靶区域(536)各自相对于治疗计划图像(522)的第一患者靶区域(524)和第二患者靶区域(526)成一定角度设置。因此,治疗计划的准确性可以如下改善:定位和/或定向患者,使得第一患者靶区域与治疗计划图像(522)的第一患者靶区域(524)的位置共同定位或更接近共同定位以用于将放射递送到第一患者靶区域,并重新定位和/或重新定向患者,使得患者的第二患者靶区域与治疗计划图像(522)的第二患者靶区域(526)的位置共同定位或更接近共同定位以用于将放射递送到第二患者靶区域。
[0350]
一个或多个治疗区可以基于获取图像(532)的每个部分的位置和地点以及治疗计划图像(522)的每个部分的位置和地点来限定。如图14d所示,用户可以指定第一治疗区r1
(例如,经由与放射治疗系统相关联的图形用户界面)。获取图像(532)可以相对于治疗计划图像(522)移动以在第一治疗区r1内将治疗计划图像(522)与获取图像(532)对齐。在一些实施例中,第一患者靶区域可以被划分为可以由体素表示的子区域(例如,子体积),并且获取图像(532)的第一患者靶区域(534)的每个体素的坐标可以与治疗计划图像(522)中的第一患者靶区域(524)的对应体素的坐标进行比较。例如,获取图像(532)的每个体素可以沿着或围绕x、y和/或z轴平移,直到获取图像(532)和治疗计划图像(522)对齐和/或共同定位。例如,如图14d所示,获取图像(532)可以相对于治疗计划图像(522)顺时针旋转,直到治疗计划图像(522)和获取图像(532)对齐和/或第一患者靶区域(524)和第一患者靶区域(534)之间的重叠在第一治疗区r1内增大。可以在获取图像(532)的移动之前基于第一治疗区r1中治疗计划图像(522)和获取图像(532)之间的位置和/或地点差异来计算对应于第一治疗区r1的第一组患者位置移动矢量以改善与治疗计划图像(522)的重叠。第一组患者位置移动矢量可以反映获取图像(532)的每个体素被平移以改善获取图像(532)的第一患者靶区域(534)和治疗计划图像(522)的第一患者靶区域(524)之间的对齐的距离和/或方向。在一些实施例中,不是将第一患者靶区域划分为多个子区域以将获取图像(532)中的子区域的位置与治疗计划图像(522)进行比较,而是第一组患者位置移动矢量可以反映获取图像(532)可以在同一平面中相对于治疗计划图像(522)移动(例如,平移和/或旋转)以改善第一患者靶区域(524)和第一患者靶区域(526)之间的对齐(例如,重叠)的距离和/或方向。此外,第一组患者位置移动矢量可以包括和/或对应于关于用于递送治疗放射的患者的第一位置和/或取向的指令(例如,经由其上设置有患者的平台的定位和/或定向)使得患者的第一患者靶区域可以比如果患者被安排在他们在获取治疗计划图像期间所处的位置更准确地被照射(例如,如果其上设置有患者的平台处于与治疗计划图像获取期间相同的位置和/或取向)。
[0351]
如图14e所示,用户可以指定第二治疗区r2。与上面参考图14d描述的类似,获取图像(532)可以相对于治疗计划图像(522)移动以在第二治疗区r2内将治疗计划图像(522)与获取图像(532)对齐和/或共同定位。在一些实施例中,第二患者靶区域可以被划分为可以由体素表示的子区域(例如,子体积),并且获取图像(532)的第二患者靶区域(536)的每个体素的坐标可以与治疗计划图像(522)中的第二患者靶区域(526)的对应体素的坐标进行比较。如图14e所示,获取图像(532)可以相对于治疗计划图像(522)逆时针旋转,直到治疗计划图像(522)和获取图像(532)对齐和/或第二患者靶区域(522)和第二患者靶区域(536)之间的重叠(526)在第二治疗区r2内增加。可基于在第二治疗区r2中的治疗计划图像(522)、获取图像(532)之间的位置和/或地点差异和第一组患者位置移动矢量计算对应于第二治疗区r2的第二组患者位置移动矢量。例如,第二组患者位置移动矢量可以基于在获取图像(532)移动之前治疗计划图像(522)和获取图像(532)之间的差异来计算以改善与治疗计划图像(522)的重叠。在一些实施例中,第二组患者位置移动矢量可以反映获取图像(532)的每个体素被平移以改善获取图像(532)的第二患者靶区域(536)和治疗计划图像(522)的第二患者靶区域(526)之间的对齐的距离和/或方向。在一些实施例中,第二组患者位置移动矢量可以反映获取图像(532)可以在同一平面中相对于治疗计划图像(522)平移和/或旋转以改善第二患者靶区域(536)和第二患者靶区域526之间的对齐(例如,重叠)的距离和/或方向。可以基于第一组患者位置移动矢量计算第二组患者位置移动矢量,因为在
确定反映治疗计划图像(522)和获取图像(532)之间的差异的一组初步位置移动矢量之后,可以基于在患者的第一患者靶区域的照射期间患者的第一位置和/或取向来计算第二组患者位置移动矢量。此外,第二组患者位置移动矢量可以包括用于重新定位和/或重新定向患者的指令(例如,通过定位和/或定向其上设置有患者的平台)以基于患者的第一位置/取向递送治疗放射。
[0352]
如图14f所示,然后可以相对于放射治疗系统的治疗放射源定位患者,使得可以将放射有效地施加到患者的靶区域。例如,患者可以在患者设置期间根据第一组患者位置移动矢量定位在第一取向。然后,当患者处于第一取向时(例如,在相对于治疗放射源平移患者通过放射治疗系统时),治疗放射可以被递送到第一患者靶区域,如箭头tx1所示。例如,第一组患者平台移动可以对应于第一患者靶区域的照射,并且第二组患者平台移动可以对应于第二患者靶区域的照射。因此,平台可以在第一取向上相对于治疗放射源移动通过第一组患者平台移动(例如,第一组患者平台阶段或位置)并且在递送治疗放射时患者被布置在患者平台上的第一位置。
[0353]
在患者处于第一取向时向第一患者靶区域递送治疗放射之后,患者可以根据第二组患者位置移动矢量定位在第二取向。例如,患者平台可以停止通过系统前进并且可以通知用户调整设置位置。接下来,治疗放射可以在患者处于第二取向时(例如,在相对于治疗放射源平移患者通过放射治疗系统时)递送到第二患者靶区域,如箭头tx2所示,以照射第二肿瘤。例如,平台可以在第二取向上相对于治疗放射源移动经过第二组患者平台移动(例如,第二组患者平台阶段或位置),并且在递送治疗放射时患者布置在患者平台上的第二位置取向。
[0354]
可视化图形
[0355]
图15a描绘了表示剂量值在患者解剖结构上的叠加和那些剂量值的概率值的可视化图形的一种变体。这可以帮助用户识别和/或评估患者治疗计划内的热点和冷点,这对于评估多个患者靶区域的治疗计划可能是有用的。对于患者治疗计划内的每个切片(例如,对于3-d渲染、dcm-x、-y和-z),可以生成剂量强度的两个参数化剂量图。在一个变体中,用于计算这些剂量图的方法包括获取针对靶区域的bdvh计算的剂量变化,并将跨越变化的每个体素的最大值分配给一个3-d剂量图像,并将每个体素的最小值分配给另一个3-d剂量图像。或者,用于计算这些剂量图的方法可以包括基于其他函数计算最小和最大剂量的统计可能值。在一种变体中,用户可以为患者内的给定体积区域指定剂量的相对上限和相对下限的容差水平(例如,d
max
和d
min
容差值,以标称剂量的百分比计)。然后将通过将指定体积区域内每个体素的标称剂量值乘以用户限定的容差值来计算参数剂量图(例如,分别产生d
max
和d
min
容差值的d
pmax
和d
pmin
剂量图)。无论选择何种方法,这都会产生两个3-d剂量分布,分别代表最大强度投影和最小强度投影。这些强度中的每一个,在可视化时,都可以应用颜色lut以在视觉上区分高值和低值。当与标称剂量图像组合成单个分箱图像时,4-d剂量图像可以通过多种方式进行可视化。例如,用户可以选择他们希望在使用标准3-d图像查看器时可视化的箱(例如,最小、最大或标称)。可替代地或另外地,这些箱可以通过将现有箱作为电影播放、迭代它们来表示为动图,即,在逐帧的基础上循环通过每个箱的短动画。替代地或附加地,可视化图形可以包括用插值函数(例如,d
pmin-dn和d
n-d
pmax
之间的插值)描绘这些箱,允许用户在不同的箱之间进行插值(通常使用滑块,但也能够使用文本输入指定两个箱
之间的百分比)。替代地或附加地,还可以通过在箱之间的任意数量的步长上将插值箱作为电影播放来将插值函数呈现为动图。
[0356]
可视化图形可以通过在4-d剂量图像的每个体素处应用概率矩阵并将这些可视化为从平面(例如表示标称概率的平面)延伸出的矢量来任选地合并剂量概率。这种可视化图形的一个实例在图15b中描绘。用户可以选择可以用彩色剂量图像可视化的2-d切片。可以使图像的每个体素通过概率分布函数,以确定跨为bdvh计算的变化发生该值的可能性。该概率值可以在3-d图像的z轴中表示,如图15b中最右边的图像所描绘的。此实例显示在单个ct图像切片顶部的单向3-d挤出。当前3-d剂量图像切片中每个像素的挤出水平是该体素的变化概率。从该可视化中,用户可能能够看到患者剂量分布中最热的区域也是存在最大变异性的区域。类似地,冷点之一具有生高的变异性水平。图15b的顶行、中行和底行描绘了标称、最小和最大3-d剂量图。左列描绘了所选切片的视图,中列和右列描绘了所选幻灯片相对于其他患者解剖结构的位置。
[0357]
图15c-15e描绘了可用于生成可视化图形的方法,例如图15a-15b中所示的图形。方法(1500)可以包括生成(1502)治疗计划,该治疗计划含有一个或多个平移不变发射滤波器、治疗计划注量图、每个患者靶区域的一个或多个计划图像以及对应的标称剂量图像,为每个患者靶区域计算(1504)对应于治疗当天可能经历的不确定性表示的多个输入(标量、矢量或体积),为每个输入集计算(1506)在存在输入集的情况下待递送到患者靶区域的预期剂量,这可能导致多个潜在剂量图像,并且将多个剂量图像组合(1508)为复合4-d体积,每个剂量图像代表该体积中的一帧。
[0358]
图15d是表示图像切片的组合以形成一堆2-d图像切片,从而生成4-d可视化图形的框图。所得的4-d可视化图形表示多个剂量图像体积,体积中的第四维是不确定性(与时间相反,如在4d成像中所考虑的那样)。
[0359]
图15e描绘了用于生成可视化图形的方法的另一变体,例如图15a-15b的可视化图形。方法(1520)可以包括生成(1522)治疗计划,该治疗计划含有一个或多个平移不变发射滤波器、治疗计划注量图、每个患者靶区域的一个或多个计划图像以及对应的标称剂量图像,为每个患者靶区域计算(1524)对应于治疗当天可能经历的不确定性表示的多个输入(标量、矢量或体积),为每个输入集计算(1526)在存在输入集的情况下待递送到患者靶区域的预期剂量,这可能导致多个潜在剂量图像,并且为每个潜在剂量图像迭代(1528)剂量图像中每个点处的剂量值。如果剂量值低于最小剂量体积中的匹配点,则方法(1520)可以包括将最小剂量体积中的匹配点设置(1530)为新值。如果剂量值高于最大剂量体积中的匹配点,则方法(1520)可以包括将最小剂量体积中的匹配点设置(1532)为新值。一旦评估了所有点,方法(1520)就可以包括将最小剂量体积、标称剂量体积和最大剂量体积组合(1534)到计算机4d体积中,每个体积代表该体积中的帧之一。
[0360]
图16a-16b描绘了可用于生成图17a-17f的可视化图形的方法的变体。图17a描绘了来自标称平面的δ剂量的冠状2-d切片(左)和轴向切片(右)。图17b描绘了δ剂量可视化图形的2-d切片(左)、冠状2-d幻灯片(中)和2-d幻灯片的测试图(右)。图17c-17d分别描绘了最大剂量、标称剂量和最小剂量2-d切片,具有与图17b相同的视图。图17f分别描绘了最小剂量、标称剂量和最大剂量2-d切片。一种用于生成图17a-17b的δ剂量可视化图形的方法可以包括拍摄dn、d
pmin
和d
pmax
的3-d剂量图像,并如下创建3-dδ剂量投影:(a)最小δ剂量投影
(d
ddmin
):每个体素的dn减去d
pmin
;(b)最大δ剂量投影(d
ddmax
):每个体素的d
pmax
减去dn,然后组合d
ddmin
、dn和d
ddmax
投影并将它们叠加在4-d剂量图像/电影上。任选地,可以创建称为总δ剂量投影的第三δ剂量投影,其可以表示bdvh中的界限宽度(即每个体素的d
pmax
减去d
pmin)。
一些可视化图形可能将变异性概率表示为决定网格挤出的因素,用于挤出的因素将是δ剂量(即与标称的差异)。这可以帮助用户快速地将d
pmin
和d
pmax
剂量图像与dn剂量图像进行比较以识别热点和冷点。热点将出现在向3-d可视化顶部的挤出,而冷点将出现在向3-d可视化底部的向下挤出,而没有挤出将代表标称和d
pmin
或d
pmax
匹配的值。这可用于可视化bdvh曲线的不同扰动(除了d
pmin
或d
pmax
)。
[0361]
现在转向图16a,方法(1600)可以包括生成(1600)含有一个或多个平移不变发射滤波器、治疗计划注量图、每个患者靶区域的一个或多个计划图像以及对应的标称剂量图像的治疗计划,为每个患者靶区域计算(1604)对应于治疗当天可能经历的不确定性表示的多个输入(标量、矢量或体积),为每个输入集计算(1606)在输入集存在的情况下待被递送到患者靶区域的预期剂量,这可能导致多个潜在剂量图像,并且为每个潜在剂量图像迭代(1608)剂量图像中每个点处的剂量值。如果剂量值低于最小剂量体积中的匹配点,则方法(1600)可以包括将最小剂量体积中的匹配点设置(1610)为新值。如果剂量值高于最大剂量体积中的匹配点,则方法(1600)可以包括将最小剂量体积中的匹配点设置(1612)为新值。一旦评估了所有点,方法(1600)就可以包括迭代(1614)最小剂量体积中的每个点,计算最小剂量体积和标称剂量体积的值之间的差,将值和频率存储在δ剂量体积的两个帧(帧1=标称-最小值,帧2=所有潜在剂量体积中最小值的频率)。方法(1600)然后可以包括迭代(1616)最大剂量体积中的每个点,计算最大剂量体积和标称剂量体积的值之间的差,将值和频率存储在δ剂量体积的两个帧中(帧3=最大值-标称值,帧4=所有潜在剂量体积中最大值的频率)。方法(1600)然后可以包括渲染(1618)每个切片(每个切片由4帧表示)的表面图,最大值的频率从3-d平面的 z挤出,最小值的频率从3-d平面的-z挤出,并且由表面中该点处的值表示表面颜色。
[0362]
图16b是表示图像幻灯片的组合以形成一堆2-d图像幻灯片,从而生成包括δ剂量信息的3-d可视化图形的框图。
[0363]
定位图形用户界面
[0364]
图37a-37n描绘了用于多靶定位的图形用户界面。在一些变体中,图37a-37n中描绘的用于虚拟定位的用户界面可以包括患者靶区域和/或oar的混合定位和单独定位之间的转换(例如,切换)。图37a描绘了患者靶区域和/或oar的参考图像(例如,计划图像)。左图和右图是两个患者靶区域的图像,并且中间图是oar的图像。图37b描绘了在进行两个患者靶区域和oar的定位图像扫描之后的递送工作空间定位用户界面。在一些变体中,参考图像和定位图像中的靶区域和/或oar的解剖结构可以通过几何形状来近似。用户(例如,临床医生和/或技术员)可以为靶区域和/或oar中的每一个指定配准质心,其可以是例如体积质心。替代地或附加地,靶区域和/或oar的体积质心可以由放疗系统计算。用于定位的图形用户界面可以包括参考图像和定位图像中的患者靶区域和/或oar的示意性近似或几何表示。这可以促进参考图像和定位图像之间的相对对齐的视觉检查,和/或降低计算参考图像和定位图像中的靶区域和/或oar的移动和/或偏差的计算复杂度。示意图可能与靶区域和/或oar的实际解剖结构有些相似,或者可以任意选择。图37c描绘了配准前的递送工作空间定
位的实例,其中第一靶区域由左图中的大圆圈表示,第二靶区域由右图中的小圆圈表示,并且oar由中间图中的垂直条或矩形表示。几何形状的位置差异(例如,未对齐)可用于调整患者的位置并定位患者靶区域。图37d-37f描绘了定位和配准期间的递送工作空间定位用户界面。当用户和/或放疗系统评估各种位置移动(虚拟移动和/或实际物理移动)时,图形用户界面可以更新各种患者结构的对齐。例如,当对齐患者结构时,可以在对齐的患者结构上方呈现视觉指示物(例如,三角形),其对于每个患者结构可以具有不同的颜色。用户和/或放疗系统然后可以评估其他患者结构的对齐以确定此类对齐是否可接受。图37d描绘了当第一靶区域被移动以使得其在定位图像中的位置与其在参考图像中的位置匹配时两个患者靶区域和oar的相对位置。图37e描绘了当移动第二靶区域使得其在定位图像中的位置与其在参考图像中的位置匹配时两个患者靶区域和oar的相对位置。图37f描绘了当oar被移动以使其在定位图像中的位置与其在参考图像中的位置匹配时两个患者靶区域和oar的相对位置。
[0365]
图37d-37f中各靶区域和/或oar的单独移动和/或对齐可以例如通过在计算对另一个患者结构的对齐之前呈现每个患者结构对齐的视觉表示以供用户检查和/或批准来依次地执行。替代地或附加地,可以通过自动计算方法(例如,可以通过选择按钮激活)来自动计算移动和/或对齐,并且可以在图形用户界面中单独地或组合地描绘。例如,图形用户界面可以包括将每个患者结构的单独对齐配置叠加在单个图形表示上。图37g描绘了图形用户界面,其包括图37d-37f中描绘的对齐/配准中的每一个的两个患者靶区域和oar的相对位置的表示,其各自由在对齐的患者结构上描绘的其自己的视觉指示物表示(例如,分别以第一靶区域、第二靶区域和oar为中心的三角形1、三角形2和三角形3)。对于每个患者结构,视觉指示物可以具有独特的颜色或形状。图37g中的图形用户界面可以任选地包括表示混合对齐/配准的视觉指示物(例如,三角形4),其中放疗系统可以计算满足指定标准的对齐。例如,混合配准可以将与oar的对齐优先于与任一靶区域的对齐。图形用户界面的一些变体可以包括允许用户调整相对对齐优先级的滑动条,并且图形表示可以实时更新以反映不同患者结构之间调整后的位置对齐。在一些变体中,混合配准可以用作物理定位,并且可以使用本文描述的任何方法虚拟定位患者靶区域。在一些变体中,图形用户界面可以包括允许用户在解剖视图和各种对齐的示意图之间转换的切换。这可以允许用户未来调整患者结构之间的相对权重(例如,对齐优先级)。例如,图37h描绘了可能已经基于图37g的示意性表示计算的混合配准的解剖图像。在该视图中,用户可以确定与周围解剖结构的对齐是否可接受。可以使用图形用户界面中提供的滑动条来调整混合配准。图37i描绘了用建议的混合配准叠加个体患者结构的配准的图形用户界面。每个患者结构的轮廓以及它们在不同配准中相对于彼此的移动可以帮助用户确定是否需要进一步调整。图形用户界面可以包括用于每个患者结构的一个滑动条,从而可以调整相对配准。例如,图37j描绘了定位图形用户界面,其中第一和第二患者靶区域的滑动条已经被调整,使得第一患者靶区域(左靶区域)的对齐权重为25并且第二患者靶区域(右靶区域)的权重为50。中心的三角形4表示基于滑动条指定的对齐权重的定位参考点的物理位置。图37k描绘了定位图形用户界面,其中第一和第二患者靶区域以及oar的滑动条已经被调整,使得第一患者靶区域(左靶区域)的对齐权重为50,第二患者靶区域的权重为50患者靶区域(右侧靶区域)为100,oar(中心结构)的权重为50。图37l描绘了定位图形用户界面,其描绘了当第一患者靶区域(左靶区域)的对齐权重为
50、第二患者靶区域(右靶区域)的权重为25,并且oar(中心结构)的权重为50时这些患者结构中的每一个的相对对齐。图37m描绘了定位图形用户界面,其描绘了当第一患者靶区域(左靶区域)的对齐权重为50、第二患者靶区域(右靶区域)的权重为50,并且oar(中心结构)的权重为零时这些患者结构中的每一个的相对对齐。图37n描绘了定位图形用户界面,其描绘了当第一患者靶区域(左靶区域)的对齐权重为50、第二患者靶区域(右靶区域)的权重为100,并且oar(中心结构)的权重为零时这些患者结构中的每一个的相对对齐。图37n描绘了用于具有100比50的比率的配准混合的递送工作空间本地化用户界面。在查看各种对齐之后,用户可以为患者设置选择所需的对齐。在一些变体中,混合配准可用于计算用于物理定位的位置坐标和/或矢量,其中患者可在平台上移动,并且平台位置和/或取向也可被调整。然后可以使用本文描述的方法虚拟定位患者靶区域,并且任选地,可以在定位图形用户界面中的同一图中描绘物理定位和虚拟定位。以这种方式,可以减少或避免额外的定位扫描,这可以帮助加快治疗期。
[0366]
治疗计划图形用户界面
[0367]
治疗计划图形用户界面的一些变体可以包括单个视图中多个治疗区的图形表示。在单个视图中描绘多个治疗区可以促进含有多个治疗区的治疗计划的几何限定、剂量测定限定和剂量测定评估。治疗计划图形用户界面可以包括控制特征,以供用户在几何限定、剂量测定限定和剂量测定评估的每个步骤期间独立地或总和地可视化每个治疗区。如前所述,治疗区是为了独特的物理定位而被照射的患者区域。治疗区可以相互重叠或不重叠。该计划图形用户界面可以允许用户(例如,临床医生、放射剂量测试员、技术员等)查看一个治疗区的变化对其他治疗区和/或oar的影响。例如,计划图形用户界面可以包括描绘叠加在解剖图像上的治疗区界限和对应的剂量测定数据。例如,为一个治疗区中的患者靶区域调整剂量分布可能会影响到另一个治疗区中的另一个患者靶区域的剂量分布。图38a-38e描绘了用于多靶治疗区限定的治疗计划图形用户界面,其可用于在单个治疗区内生成每个靶的独立等中心(例如,每个患者目标区的计划定位参考点),从而实现虚拟定位。图形用户界面可以包括各自含有一个或多个患者靶区域的一个或多个治疗区的第一图形表示(即,图形元素),以及每个治疗区的剂量测定特性的第二图形表示。例如,第一图形表示可以包括代表每个治疗区的带。第三图形表示可以包括多个患者靶区域中的一个。在一些变体中,第一图形表示可以叠加到第三图形表示上,使得用户可以通过视觉检查识别在治疗区的界限内的患者靶区域。在一些变体中,计划图形用户界面还可包括第四图形表示,其包括跨多个治疗区的多个危及器官(oar)的视图和表示每个oar与一个或多个治疗区的相对空间关系的视觉标记。在一些变体中,治疗计划图形用户界面还可包括图形表示,该图形表示包括跨多个治疗区的所有患者靶区域的视图和表示一个或多个患者靶区域之间的相对空间关系的视觉标记。计划图形用户界面还可包括具有跨多个治疗区的多个oar的视图的图形表示和表示每个oar与一个或多个治疗区的相对空间关系的视觉标记。任选地,第一、第二和/或第三图形表示(例如,图形元素、本文所述的任何图形表示)中的一个或多个可以叠加到患者解剖结构的2-d或3-d渲染(例如,ct图像、pet图像、mri图像、超声图像等)上。在一些变体中,所有多个治疗区的剂量测定特性可以在治疗计划图形用户界面上同时可视化。在一些变体中,每个治疗区的剂量测定特性可以个体可视化。在一些变体中,每个治疗区的剂量测定特性可以包括剂量测定目标、剂量体积直方图、剂量统计和目标性能中的一个或多个。
[0368]
图38a描绘了描绘具有叠加在解剖ct-pet扫描上的两个治疗区的治疗计划的治疗计划图形用户界面。在该实例中,两个独立的治疗区由同时向用户显示的叠加在解剖图像上的两个半透明水平带表示。治疗计划图形用户界面可以具有允许用户依次在两个治疗区的视图和一个治疗区的视图之间切换的按钮。图38b描绘了治疗计划图形用户界面的实例,其具有叠加在单个ct-pet图像上的多个(例如,两个)治疗区的图形表示和呈现不同查看选项(例如查看所有治疗区或治疗区的子组的ct-pet图像),并允许用户选择可用于包括每个治疗区的ct-pet图像的计划/参考图像的菜单。治疗计划图形用户界面可以包括便于选择用户希望查看的治疗区和/或患者结构的查看选项卡。例如,图38c描绘了允许用户选择用于查看的治疗区(例如,区1)的第一视图选择选项卡,以及允许用户选择用于查看的选定治疗区内的患者靶区域和/或oar(例如,区1中的靶1或靶2)的第二视图选择选项卡。治疗计划图形用户界面还可以包括便于选择用于查看的oar的查看选项卡,并且可以任选地包括指示oar参与和/或与每个治疗区的共同定位的数据字段。图38d描绘了包括允许选择查看oar的查看选项卡的治疗计划图形用户界面的一种变体,并且在oar查看选项卡内,该界面包括指示oar是否跨越一个或多个治疗区的一个或多个字段。例如,界面可以包括列出每个oar和关于每个oar是否与区1或区2(或两者)共同定位(例如,重叠)的标记的表格。治疗计划图形用户界面还可包括多个治疗区、患者靶区域和/或oar的剂量测定特性的视图。上述一项或多项的剂量测定特性可以同时或单独显示。剂量测定特性可以包括一个或多个剂量测定目标、剂量体积直方图、剂量统计和目标性能。图38e描绘了治疗计划图形用户界面,其包括列出用户有兴趣查看的体积的第一图和描绘第一图中列出的体积的剂量体积直方图(dvh)的图形表示的第二图。第一图可以包括将被描绘在第二图中的允许用户选择剂量测定信息的类型以及治疗区、患者靶区域和/或oar的选项卡或按钮。在图38e中描绘的查看模式中,“总体计划”(例如,所有患者靶区域和跨所有治疗区的oar)的dvh曲线/概况描绘在第二图中。在其他查看模式中,用户可以选择查看仅区1、仅区2、仅oar及其任意组合的dvh曲线/概况。dvh曲线可以是有界dvh曲线,其表示基于位置、运动和/或其他参数的变化而递送至该体积的剂量范围(例如,上限和下限)。在一些变体中,有界dvh曲线可以代表由临床医生和/或诊所设置的可接受的剂量差异容差。任选地,图形用户界面可以包括描绘患者的解剖图像(例如,ct-pet、mri-pet等)的第三图,其具有治疗区、患者靶区域和/或oar的视觉标记(例如,轮廓或阴影)。剂量特性可以叠加或重叠在它们对应的解剖区域上。
[0369]
多靶放射递送方法
[0370]
在使用一种或多种上述方法定位多个患者靶区域中的至少一个之后,可以将放射递送递送至已经定位的患者靶区域。治疗性放射可以依次地或同时地递送到患者靶区域。在一个变体中,在单个治疗期中向多个患者靶区域的放射递送可包括基于第一定位图像定位第一患者靶区域,将治疗放射递送至第一患者靶区域,然后定位第二患者靶区域,将治疗放射递送至第二患者靶区域,等等,直到所有患者靶区域都已被规定剂量照射。可以使用相同的定位图像完成连续定位,或者每个连续定位可以基于新获取或更新的定位图像。替代地或附加地,一些放射递送方法可以包括同时定位所有患者靶区域(例如,使用在治疗期开始时获取的相同定位图像组),然后在患者移动通过治疗放射束平面时和/或治疗放射源在患者周围移动时照射所有患者靶区域。在使用虚拟定位来定位患者靶区域的变体中,每个患者靶区域的递送注量图可以在虚拟定位之后被分割成放疗系统机器指令,然后放疗系统
可以步进通过分割的机器指令和相应地递送放射。在至少一些患者靶区域是bgrt靶区域的变体中,那些靶区域的递送注量图(例如,在虚拟定位期间计算)可能不会被分割成放疗机器指令,直到进一步用治疗期间获得的成像数据更新递送注量图。例如,从在下一个发射位置将放射发射到患者靶区域时起大约一分钟或更短或一秒或更短(例如,大约500ms或更短),可以使用在有限时间窗口中获取的成像数据计算即将到来的发射位置的递送注量(例如,通过将发射滤波器在该发射位置的投影与部分成像数据进行卷积)。在治疗放射到达下一个发射位置之前的时刻(例如,之前少于大约1秒、之前少于大约0.5秒、之前少于大约0.25秒,等等),放疗系统可以将该发射位置的递送注量分割成放疗系统指令,并且可以根据那些指令发射递送注量。在一些变体中,患者平台可以被配置为移动患者,使得所有患者靶区域在每个治疗期通过治疗放射束平面不止一次。每个此类患者“扫过”光束平面可以称为穿梭通过。例如,将患者从第一位置移动到第二位置可以限定第一穿梭通过,并且将患者从第二位置移动到第一位置可以限定第二穿梭通过。患者平台可以随着放射的递送而连续移动,或者可以沿着纵轴(沿iec-y)步进到一系列床位置,以便仅当床停在这些预定位置(或光束站)时递送放射。治疗区可以由一组光束站或iec-y中预先确定的患者平台位置来限定。在一些变体中,一个或多个患者靶区域在第一穿梭期间被照射,而一个或多个其他患者靶区域在第二穿梭期间被照射。在一些变体中,bgrt患者靶区域可以在第一穿梭期间被照射并且sbrt/imrt靶区域可以在第二穿梭期间被照射。替代地或附加地,所有患者靶区域可以在相同的穿梭通过期间被照射。任选地,在每次完整的bgrt通过之后,可以基于前一次bgrt通过计算所有靶区域的一组归一化系数。关于计算和应用归一化系数和穿梭模式放射传递的方法的附加细节在于2018年9月21日提交的美国专利申请系列第16/138,631号中提供,其全部内容通过引用并入本文。
[0371]
在一些变体中,用于患者的多靶放射递送可包括将待治疗的患者区域分割(例如,区分、划分等)为多个治疗区,每个治疗区具有一个或多个患者靶区域,执行治疗区的物理定位(例如,床移动和/或患者位置调整),然后对治疗区中的一个或多个患者靶区域执行虚拟定位。在一些变体中,患者治疗计划可以包括一组治疗区,该治疗区代表对于单个患者固定要向其递送放射的患者区域。例如,治疗区(ta)可以包括将被一组通过单个kvct定位和任选的激光设置递送的光束照射的患者区域。在一些变体中,治疗区(ta)可以对应于相应的pet预扫描和评估以及分数计数器。例如,每个治疗区(ta)可以包括相应的激光设置和物理定位和/或虚拟定位。注量图可以由跨越一个或多个光束站的一组照射正弦图表示。在一些变体中,注量图可以被配置为在单个治疗期内不间断地递送。图35a-35c是描绘三种不同的患者治疗计划变体的图。图35a是具有含三个靶区域组(由暗虚线包围)的跨越两个患者设置(由灰色虚线包围的区域)的三个治疗区(由实线包围的区域)的治疗计划的实例,每个靶区域组具有对应的注量图。在治疗期期间,这将导致总共获得三个定位ct,其中最多三个物理定位和三个虚拟定位。在此实例中,治疗计划具有三个靶区域组(trg1、trg2和trg3),其中trg1包含两个患者靶区域的两个注量图,并且trg2和trg3各自包含一个患者靶区域的一个计划注量图。图35b是具有单个患者设置(由灰色虚线包围)和具有四个靶区域组(由暗虚线包围)的单个治疗区(由实线包围)的治疗计划的实例,每个靶区域组具有对应的注量图。在治疗期期间,这将导致获得单个定位ct,其中最多一个物理定位和四个虚拟定位。图35c是具有四个治疗区(由实线包围)的治疗计划的实例,每个治疗区具有它们自己的定位
ct、物理定位和/或虚拟定位。图35b和36c中的每个靶区域组各自具有一个计划注量图(因为每个靶区域组只有一个靶区域)。
[0372]
图36a和图36b是描绘包括患者的两个不同靶区域组配置的治疗计划的实例的图。虽然图35a-35c描绘了具有不同治疗区的治疗计划的实例,但是图36a和36b描绘了具有在图36a和36b中描绘的不同靶区域组的治疗计划的实例。在这个实例中,存在四个将被治疗计划照射的患者靶区域(由圆圈表示)。在治疗计划期间,用户可以限定治疗区和靶区域组配置,其中每个治疗区和靶区域组可以包含不同的患者靶区域。每个靶区域组(由暗虚线包围)可以包括与四个患者靶区域中的每一个相关联的一个或多个注量图。如前所述,每个治疗区可以包括其自己的基于kvct的定位、任选的激光设置和/或任选的患者位置。每个靶区域组可以包括其自己的虚拟定位。在治疗区被照射时,靶区域组内的每个患者靶区域的注量图可以依次地或并行地递送。在一些变体中,可以对一个或多个靶区域组执行虚拟定位。例如,治疗计划的虚拟定位可以减少或消除患者平台移动(例如,床移动)并提供与常规床移动相同或相似的安全概况,除了虚拟定位代替床移动之外。可以为每个治疗区和/或靶区域组设置定位参考点,并且可以增加患者靶区域和/或危及器官(oar)的安全裕度。在一些变体中,治疗区可由治疗计划限定,该治疗计划可由临床医生批准使得治疗区在治疗递送时不改变。附加地或替代地,可以选择靶区域组中的一个用于床移动,而其余的靶区域组可以进行虚拟定位。
[0373]
图35a所描绘的治疗计划可以包括三个治疗区,其中第一治疗区包括第一患者靶区域组(trg1,具有对应的注量图),第二治疗区包括第二患者靶区域组(具有对应的注量图),并且第三治疗区包括第三患者靶区域组(具有对应的注量图)。在治疗期期间,可以针对第一治疗区对患者进行物理设置/定位以将放射递送到前两个患者靶区域。然后,可以针对第二治疗区对患者进行物理设置/定位(第二次)以将放射递送到第三患者靶区域。最后,可以针对第三治疗区对患者进行物理设置/定位(第三次)以将放射递送到第四患者靶区域。任选地,可以针对三个治疗区和/或靶区域组中的至少一个虚拟地设置/定位患者,使得不会第二次或第三次物理地设置/定位患者。
[0374]
图35b中描绘的治疗计划可以包括含四个靶区域组的单个治疗区。在治疗期期间,患者可能仅针对限定的治疗区进行一次物理设置/定位。然后,可以针对四个靶区域组中的每一个虚拟地定位患者以将放射递送到所有四个患者靶区域。
[0375]
图35c中描绘的治疗计划可以包括四个治疗区,其中每个靶区域组包含在单独的治疗区内。在治疗期期间,可以针对每个治疗区物理地设置/定位患者一次和/或针对每个靶区域组虚拟定位一次以将放射递送至包含在其中的相应患者靶区域。
[0376]
图36a中描绘的治疗计划可以包括两个治疗区,一个包括前三个患者靶区域(具有对应的注量图),第二个包括第四患者靶区域。在治疗期期间,可以为两个限定的治疗区中的每一个物理地设置/定位患者一次和/或为两个限定的靶区域组中的每一个虚拟定位一次。
[0377]
图36b中描绘的治疗计划可以包括两个治疗区,其中第一治疗区包括第一和第二患者靶区域组(具有前三个患者靶区域的对应注量图)并且第二治疗区包括第三患者靶区域组(具有第四患者靶区域的对应注量图)。在治疗期期间,可以针对第一治疗区物理地设置/定位患者并且针对第一和第二患者靶区域组中的一个或两个虚拟定位患者以将放射递
送至包含在其中的患者靶区域。然后,可以针对第二治疗区对患者进行物理设置/定位(第二次)以将放射递送到第四患者靶区域。任选地,可以针对两个治疗区和/或靶区域组中的一个来虚拟地设置/定位患者,使得患者不会第二次物理地设置/定位。
[0378]
图18a描绘了用于在治疗期中治疗多个患者靶区域(例如,sbrt/imrt患者靶区域)的方法的流程图表示,其中在治疗期期间将注量图分割成放疗机器指令。方法(1800)可以包括在指定的光束站定位(1802)患者平台,加载(1804)光束站的注量图,其中注量图已经在治疗期的定位阶段期间更新,将注量图分割(1806)为放疗系统机器指令,指令包括针对患者平台周围每个发射位置的多叶准直器和治疗放射源的命令,从治疗源发射(1808)放射以根据光束站的注量图递送放射,从而同时或依次照射一个或多个患者靶区域,和将患者平台推进(1810)到下一光束站,直到所有指定光束站都已被访问至少一次。可以使用物理定位、虚拟定位和/或任何其他移动计划注量图以反映对应患者靶区域的实际位置的方法来执行定位。可以加载(1804)的注量图可以包括以下一项或多项:(a)多个患者靶区域的累积递送注量图,和/或(b)多个患者靶区域的个体注量图。例如,可能已经使用本文描述的虚拟定位方法更新了所递送的注量图。方法(1800)可以包括重复(1804)-(1810)直到所有光束站都被访问了一次或多次(例如,一次或多次穿梭通过)。
[0379]
图18b描绘了用于在治疗期中治疗多个患者靶区域(例如,sbrt/imrt患者靶区域)的方法的流程图表示,其中在治疗期期间将注量图分割成放疗机器指令并且多个患者靶区域可以同时被照射。方法(1820)可以包括计算(1821)每个患者靶区域的定位/配准注量图,例如,使用虚拟定位方法计算,将所有患者靶区域的注量图组合(1822)为累积递送注量图,将累积递送注量图分段(1824)为每个患者平台光束站的光束站递送注量图,为每个光束站将光束站递送注量图分割(1825)为放疗系统机器指令,该指令包括对围绕患者平台的每个发射位置的多叶准直器和治疗放射源的命令,并且根据每个患者平台光束站处的放疗系统机器指令从治疗源发射(1826)放射以递送放射。任选地,方法(1820)可以包括在将累积递送注量图分割(1823)成光束站递送注量图之前根据期望的约束(例如治疗和/或剂量约束)优化(1823)累积递送注量图。任选地,可以通过计算解决最小均方误差剂量测定目标的一组标量归一化系数来优化累积递送注量图。
[0380]
图18c描绘了用于在治疗期中治疗多个患者靶区域(例如,sbrt/imrt患者靶区域)的方法的流程图表示,其中在治疗期期间将注量图分割成放疗机器指令并且多个患者靶区域可以依次被照射。方法(1830)可以包括计算(1831)每个患者靶区域的定位/配准注量图,例如,使用虚拟定位方法和/或物理设置/定位方法计算,将每个患者靶区域的每个定位注量图分段(1832)为每个患者平台光束站的光束站递送注量图,对于每个光束站,将每个患者靶区域的光束站递送注量图分割(1833)为放疗系统机器指令,该指令包括对用于围绕患者平台的每个发射位置的多叶准直器和治疗放射源的命令,将患者平台定位(1834)在指定的光束站,并根据放疗系统机器指令从治疗源发射(1835)放射以依次将放射递送到每个患者靶区域。方法(1830)可以包括将患者平台推进(1836)到下一个光束站,直到所有指定的光束站都被访问了至少一次。
[0381]
图18d描绘了用于在治疗期中治疗多个患者靶区域(例如,sbrt/imrt患者靶区域)的方法的流程图表示,其中在治疗期期间将注量图分割成放疗机器指令并且多个患者靶区域可以经多次穿梭通过依次照射。方法(1840)可以包括计算(1841)每个患者靶区域的定
位/配准注量图,例如,使用虚拟定位方法和/或物理设置/定位方法计算,和将(1842)患者靶区域分配给多次患者平台穿梭通过中的一次。方法(1840)然后可以包括对于每次穿梭通过将分配给穿梭通过的每个患者靶区域的定位注量图分段(1843)为每个患者平台光束站的光束站递送注量图,并且为穿梭通过中的每个光束站,将每个患者靶区域的光束站递送注量图分段(1844)为放疗系统机器指令,该指令包括针对患者平台周围每个发射位置的多叶准直器和治疗放射源的命令。方法(1840)然后可以包括开始(1845)穿梭通过,根据放疗系统机器指令在穿梭通过中的每个光束站从治疗源发射(1846)放射以将放射递送到分配给穿梭通过的每个患者靶区域,结束(1847)穿梭通过,并重复(1848)每次穿梭通过照射一个患者靶区域,直到所有患者靶区域都已被照射。
[0382]
图19描绘了用于在治疗期中治疗多个bgrt患者靶区域的方法的流程图表示。如前所述,可以使用虚拟定位方法来配准bgrt患者靶区域。在bgrt放疗的一些变体中,患者被注射pet示踪剂,该示踪剂在可能指定在患者靶区域的肿瘤区域处积聚。放疗系统可以包括用于检测正电子湮没发射路径数据(lor)的pet检测器阵列和诸如直线加速器的治疗放射源,其被配置为基于检测到的lor数据来递送放射。方法(1900)可以包括将患者平台定位(1902)在指定的光束站,在整个治疗期的治疗放射递送阶段连续获取(1904)成像数据,通过将每个患者靶区域的平移不变发射滤波器与连续获取的成像数据进行卷积来计算(1906)治疗放射源每个发射位置的递送注量图,将注量图分割(1908)为放疗系统机器指令,该指令包括对围绕患者平台的每个发射位置的多叶准直器和治疗放射源的命令,根据光束站的注量图从治疗源发射(1910)放射以递送放射,从而同时或依次照射一个或多个患者靶区域,和推进(1912)患者平台到下一个光束站。如先前在bgrt递送中所述,可在有限时间窗口(例如,约1秒或更短、约500ms或更短、约250ms或更短)内获取成像数据,并且所获取的成像数据可用于计算将在未来发射位置递送的注量,并在治疗放射源位于该发射位置之前的时刻分割成放疗系统指令。在一些直线加速器安装在快速旋转的机架(例如,约40rpm、约50rpm、约60rpm、约70rpm)上的系统中,成像数据获取和治疗放射发射之间的延迟可能是约2秒或更短、约1秒或更短、约500ms或更短等)。递送注量和实时分割的此类频繁计算和/或更新可以允许将规定的放射剂量更精确地递送到预期的患者靶区域。递送注量的计算(1906)可以使用一种或多种上述方法,包括但不限于从虚拟定位导出的注量图、将平移不变发射滤波器或放射发射矩阵(rfm)与部分图像数据(例如,已被roi空间过滤并反投影到发射位置的lor数据)卷积、与虚拟平坦滤波器卷积、距离补偿缩放因子等。任选地,可以通过计算解决每个靶区域的最小均方误差剂量测定目标的一组标量归一化系数来优化累积递送注量图。
[0383]
图20描绘了用于在治疗期中治疗多个患者靶区域的方法的流程图表示,其中一些患者靶区域可以是bgrt靶并且其他可以是sbrt/imrt靶。如前所述,可以使用虚拟定位方法来配准患者靶区域。在bgrt放疗的一些变体中,患者被注射pet示踪剂,该示踪剂在可能指定在患者靶区域的肿瘤区域处积聚。放疗系统可以包括用于检测正电子湮没发射路径数据(lor)的pet检测器阵列和诸如直线加速器的治疗放射源,其被配置为基于检测到的lor数据来递送放射。方法(2000)可以包括将患者平台定位(2002)在指定的光束站,在整个治疗期的治疗放射递送阶段连续获取(2004)成像数据,通过合并通过将第一患者靶区域的平移不变发射滤波器与连续获取的成像数据进行卷积计算的第一注量和在治疗期的定位阶段
更新的第二患者靶区域的第二注量来计算(2006)治疗放射源每个发射位置的递送注量图,将递送注量图分割(2008)成放疗系统机器指令,该指令包括对患者平台周围每个发射位置的多叶准直器和治疗放射源的命令,根据光束站的注量图从治疗源发射(2010)放射以递送放射,从而同时或依次照射一个或多个患者靶区域,和推进(2012)患者平台到下一个光束站并重复直到所有光束站都被访问了至少一次。任选地,在所有光束站已经被访问至少一次之后,方法(2000)可以包括计算一组归一化系数以确定是否已经满足剂量目标。如先前在bgrt递送中所述,可在有限时间窗口(例如,约1秒或更短、约500ms或更短、约250ms或更短)内获取成像数据,并且所获取的成像数据可用于计算将在未来发射位置递送的注量,并在治疗放射源位于该发射位置之前的时刻分割成放疗系统指令。在一些直线加速器安装在快速旋转机架(例如,约50rpm或更高、约60rpm、约70rpm)上的系统中,成像数据获取和治疗性放射发射之间的延迟可能是约2秒或更短,约1秒或更短、约500ms或更短等。递送注量和实时分割的此类频繁计算和/或更新可以允许将规定的放射剂量更精确地递送到预期的患者靶区域。递送注量的计算(1906)可以使用上述方法中的一种或多种,包括但不限于从虚拟定位导出的注量图、将平移不变发射滤波器或放射发射矩阵(rfm)与部分图像数据(例如,已被roi空间过滤并反投影到发射位置的lor数据)卷积、与虚拟平坦滤波器卷积、距离补偿缩放因子等。任选地,计算递送注量图(2006)可以包括通过计算解决每个靶区域的最小均方误差剂量测定目标的一组标量归一化系数来优化累积递送注量图(即,将迄今为止在治疗期递送的所有放射注量相加)。
[0384]
系统
[0385]
如上所述,放疗系统,例如本文所述的任何放疗系统,可用于提供包括上述任何方法的图像引导放射治疗(igrt)。放疗系统可以包括成像系统,该成像系统包括任何合适的成像模式,例如pet、ct、mri、超声等。在一些变体中,放疗系统可以包括运动系统,该成像系统可以安装到该运动系统。任选地,放疗系统的治疗放射源和一个或多个光束成形部件可以安装在同一机架上。在一些变体中,成像系统可以安装在圆形机架上,该圆形机架被配置为以大约30rpm或更高(例如,大约60rpm、大约65rpm、大约70rpm)的速度围绕患者区旋转。替代地或附加地,成像系统能够在没有任何旋转的情况下获取断层摄影成像数据,例如mri成像系统。
[0386]
可用于提供如上所述的igrt的放疗系统可包括被配置为实时递送治疗放射束的治疗放射源。即,治疗放射源可以安装在运动系统上,该运动系统将放射源快速移动到患者区周围的每个发射位置,并且光束成形部件被配置为在发射位置之间的时间间隔内改变光束成形配置,使得放射束可以在靶区域显著移动之前施加到靶区域。图像获取和放射递送之间的延迟越大,靶区域在放射递送时移动的可能性就越大。因此,运动系统(例如,机架、底盘、臂等)和光束成形部件(例如,钳口、准直器等)可以被配置为在大约10ms或更短内移动(例如,将放射源移动到新的发射位置的运动系统)并改变配置(例如,移动/改变不透射线元件的定位的准直器或钳口)。例如,放疗系统可以包括成像系统(例如pet、ct、mri)、可旋转机架、安装在可旋转机架上的直线加速器、以及安装在机架上并设置在直线加速器的光束路径中的动态多叶准直器。动态多叶准直器可以是例如二元多叶准直器,其中每个叶在位于发射位置时处于打开或关闭配置,并且可以在于发射位置之间移动时在打开和关闭配置之间过渡。放疗系统的一个实例可以具有以大约30rpm或更多(例如,大约40rpm、大约
50rpm、大约60rpm、大约70rpm)旋转的机架,动态多叶二元准直器可以在10ms内改变配置,并且同步治疗放射源可在10ms内发射多个脉冲。同步治疗放射源脉冲放射,而二元多叶准直器的叶在于配置之间移动的短时段内是静止的。用于移动二元多叶准直器的指令可以在图像获取后以低至10ms的延迟生成。放疗系统的另一个实例可能具有以5rpm旋转的机架、不断改变配置的动态2d多叶准直器,其中当位于发射位置时,每个叶可处于其完全关闭和完全打开位置之间的任何中间位置,以及以大约100hz或更高的速率脉冲或连续发射的异步治疗放射源。在一些变体中,2d动态多叶准直器的叶能够以可以跟踪两倍于肿瘤速度的速度移动。速度可以基于使用治疗放射源相对于2d多叶准直器和靶两者的位置的几何计算。所需的2d多叶准直器叶位置和对应的靶位置之间的延迟可以低至从图像获取开始的10ms。
[0387]
本文描述的方法和系统可以包括任何合适的患者平台,例如如上所述的可移动桌子或床。例如,患者平台可以包括于2017年11月15日提交的美国专利申请。第15/814,276号中描述的任何患者平台,其全部内容通过引用并入本文。
[0388]
快速机架系统
[0389]
运动系统的一种变体可以包括可旋转的机架。例如,可旋转机架可以是连续旋转机架,配置为围绕患者区旋转360度。图5a描绘了此类机架的实例,其可以被配置为以大约30rpm或更高(例如,大约40rpm、大约50rpm、大约60rpm、大约70rpm)的速率旋转。
[0390]
在一些变体中,放疗系统可以围绕轴旋转治疗放射源和准直器,并且可以任选地停止在各种发射角。当机架围绕患者区旋转时,用于放疗系统的控制器可以跟踪机架的速度。机架可以以低的或固定的角速度相对缓慢地旋转,或者可以以较高的角速度相对快地旋转,使得它以近似成像系统的帧速率完成一圈。
[0391]
在于2017年11月15日提交美国专利申请。第15/814,222号中描述了包括高速机架的放疗系统的附加细节和变体,其全部内容通过引用并入本文。
[0392]
动态mlc
[0393]
放疗系统可以包括光束成形部件,例如mlc,其被配置为在选定的时间间隔内改变叶的配置。例如,选定的时间间隔可以是运动系统将直线加速器从第一发射位置移动到第二发射位置所花费的时间。作为时间函数的叶的位置可以至少部分地由每个mlc叶的时间带宽和/或配置过渡速度来确定。一些放疗系统可包括高速二元mlc,其可包括叶片致动机构,所述叶片致动机构在每个发射位置或机架角度上将每个叶片移动到新的mlc配置或模式。这种架构可以促进广义靶跟踪,甚至是多个同时发生的靶。于2016年6月10日提交的美国专利申请系列第15/179,823号中提供了可用于放疗系统的动态二元多叶准直器的更多细节,其全部内容通过引用并入本文。
[0394]
图21a描绘了放疗系统的一种变体,其可用于实施本文所述的任何方法的图像引导放射治疗。放疗系统(600)可包括可围绕患者区(604)旋转的机架(602)、安装在机架上的一个或多个pet检测器(606)、安装在机架上的治疗放射源(608)以及设置在治疗放射源的光束路径中的动态多叶准直器(610)。在一些变体中,放疗系统可以包括第一阵列的pet检测器(606a)和设置在第一阵列对面的第二阵列的pet检测器(606b)、直线性加速器(608)或直线加速器,以及动态二元多叶准直器(610)。该系统可进一步包括与机架、pet检测器、直线加速器和mlc通信的控制器,其中控制器具有一个或多个存储器,可以存储治疗计划、放
射发射矩阵、注量图、系统指令/命令,以及被配置为执行本文描述的计算和方法的处理器。设置在患者区内的患者可能已被注射发射正电子的pet示踪剂,并且pet示踪剂可能积聚在患者的特定区域(例如,诸如肿瘤区域的放射靶区域)。正电子与附近电子的湮没可能导致两个光子的发射以相反的方向行进以限定线。一个或多个获取的部分图像或检测到的部分图像数据可以包括一个或多个正电子湮没发射路径(即,响应线或lor,发射路径)。在一些变体中,pet检测器可以是飞行时间pet检测器,其可以帮助识别正电子湮没事件的位置。任选地,放疗系统(600)可以包括安装在与治疗放射源相同的机架上或安装在单独的机架上的ct成像系统。在于2017年11月15日提交美国专利申请第15/814,222号中描述了基于pet的放疗系统的其他细节和实例,其全部内容通过引用并入本文。
[0395]
图21b描绘了放疗系统的另一个变体,其可用于实施本文所述的任何方法的图像引导放射治疗。放疗系统(620)可以包括可围绕患者区(624)旋转的机架(622)、具有kvx射线源(628)的kv成像系统(626)和安装在机架上的kv检测器(630)以及安装在机架(622)上的治疗放射源(632)(例如,mvx射线源)和mv检测器(634)。kv检测器(630)可以跨过kvx射线源(628)定位并且mv检测器(634)可以跨过mvx射线源(632)定位。任选地,kv成像系统可以包括在kvx射线源(628)上的动态mlc(627)。该系统可以包括设置在mvx射线源(632)上方的动态mlc(631)。部分图像或成像数据可以包括在每个kvx射线源脉冲之后由kv检测器获取的图像数据。部分kvx射线图像的实例可以包括x射线投影图像数据,例如2d投影数据。在2018年3月29日提交的pct/us18/25252中描述了基于pet的放疗系统的其他细节和实例,其全部内容通过引用并入本文。
[0396]
图21c描绘了放疗系统(650)的另一个变体,其可用于实施本文所述的任何方法的图像引导放射治疗。放疗系统(650)可以包括机架(651),该机架包括可围绕患者区旋转的第一对臂(652)和可围绕患者区旋转的第二对臂(654),成像系统,该成像系统包括安装在第一对臂(652)的第一臂(652a)上的kv放射源(656)和安装在第一对臂(652)的第二臂(652b)上的kv检测器(658),以及治疗放射系统,该治疗放射系统包括安装在第二对臂(654)的第一臂(654a)上的mv放射源(660)和安装在第二对臂(654)的第二臂(654b)上的mv检测器(662)。第一对臂(652)的第一臂和第二臂可以彼此相对地定位(例如,在患者区的相对侧、彼此相对和/或彼此成大约180度),使得kv放射源(656)和kv检测器(658)彼此相对定位(例如,kv检测器位于kv放射源的光束路径中)。第二对臂(654)的第一臂和第二臂可以彼此相对地定位(例如,在患者区的相对侧、彼此相对和/或彼此成大约180度),使得mv放射源(660)和mv检测器(662)彼此相对定位(例如,mv检测器位于mv放射源的光束路径中)。部分图像或成像数据可以包括在每个kvx射线源脉冲之后由kv检测器获取的图像数据。部分kvx射线图像的实例可以包括x射线投影图像数据,例如2d投影数据。在2018年3月29日提交的pct/us18/25252中描述了基于pet的放疗系统的其他细节和实例,其全部内容通过引用并入本文。
[0397]
控制器
[0398]
可以被配置为基于更新的患者图像提供患者定位和/或取向指令的系统(例如,治疗计划系统、放疗系统)可以包括与放疗系统的成像系统和/或治疗放射源和/或多叶准直器和/或机架通信的控制器。控制器可以包括一个或多个处理器以及与一个或多个处理器通信的一个或多个机器可读存储器。控制器可以通过有线或无线通信信道连接到放疗系统
和/或其他系统。在一些变体中,治疗计划系统的控制器可以位于与患者相同或不同的房间中。例如,控制器可以与患者平台偶联或者设置在与患者和/或操作者相邻的手推车或医疗车上。
[0399]
控制器可以与许多通用或专用计算系统或配置一致地实现。可适用于与本文公开的系统和设备一起使用的各种示例性计算系统、环境和/或配置可包括,但不限于,在个人计算设备,网络设备,服务器或服务器计算设备(例如路由/连接组件)、便携式(例如,手持式)或膝上型设备、多处理器系统、基于微处理器的系统和分布式计算网络内或体现在其上的软件或其他组件。
[0400]
便携式计算设备的实例包括智能手机、个人数字助理(pda)、手机、平板电脑、平板手机(比智能手机大但比平板电脑小的个人计算设备)、采用智能手表形式的可穿戴计算机、便携式音乐设备等。
[0401]
处理器
[0402]
在一些实施例中,处理器可以是被配置为运行和/或执行一组指令或代码的任何合适的处理设备,并且可以包括一个或多个数据处理器、图像处理器、图形处理单元、物理处理单元、数字信号处理器和/或中央处理单元。处理器可以是例如通用处理器、现场可编程门阵列(fpga)、专用集成电路(asic)等。处理器可以被配置成运行和/或执行应用程序进程和/或与和其相关联的系统和/或网络相关联的其它模块、过程和/或功能。可以提供各种组件类型的底层设备技术,例如,金属氧化物半导体场效应晶体管(mosfet)技术(如互补金属氧化物半导体(cmos))、双极技术(如发射极耦合逻辑(ecl))、聚合物技术(例如,硅共轭聚合物和金属共轭聚合物-金属结构)、混合模拟和数字等。
[0403]
存储器
[0404]
在一些实施例中,存储器可以包括数据库,并且可以是,例如,随机存取存储器(ram)、存储缓冲器、硬盘驱动器、可擦除可编程只读存储器(eprom)、电可擦除只读存储器(eeprom)、只读存储器(rom)、闪存等。存储器可以存储指令以使处理器执行与系统相关联的模块、过程和/或功能,例如一个或多个治疗计划、完整或高snr图像、部分或低snr图像,基于治疗计划和/或临床目标计算注量图,将注量图分成放疗系统指令(例如,可指导机架、患者桌、治疗放射源、多叶准直器和/或放疗系统和/或诊断或治疗计划系统的任何其他组件),以及与治疗计划和/或递送相关联的图像和/或数据处理。
[0405]
本文描述的一些实施例涉及具有非暂时性计算机可读介质(也可以称为非暂时性处理器可读介质)的计算机存储产品,其上具有用于执行各种计算机实现的操作的指令或计算机代码。计算机可读介质(或处理器可读介质)从其本身不包括暂时传播信号的意义来说是非暂时性的(例如,在诸如空间或电缆的传输介质上承载信息的传播电磁波)。介质和计算机代码(也可以称为代码或算法)可以是为特定的一种或多种目的而设计和构造的那些。非暂时性计算机可读介质的实例包括,但不限于,磁存储介质,诸如硬盘、软盘以及磁带;光存储介质,诸如光盘/数字视频光盘(cd/dvd);光盘只读存储器(cd-rom)和全息设备;磁光存储介质,诸如光碟;固态存储设备,诸如固态驱动器(ssd)和固态混合驱动器(sshd);载波信号处理模块;以及被专门配置用于存储和执行程序代码的硬件设备,诸如专用集成电路(asic)、可编程逻辑器件(pld)、只读存储器(rom)和随机存取存储器(ram)设备。本文描述的其他实施例涉及计算机程序产品,其可以包括,例如,本文公开的指令和/或计算机
代码。
[0406]
用户界面可以用作操作者或临床医生与治疗计划系统之间的通信接口。用户界面可以包括输入设备和输出设备(例如,触摸屏和显示器)并且被配置为从支撑臂、外部磁体、传感器、递送设备、输入设备、输出设备、网络、数据库以及服务器中的一个或多个接收输入数据和输出数据。来自一个或多个传感器的传感器数据可以由用户界面接收并且由一个或多个输出设备在视觉上、听觉上和/或通过触觉反馈输出。作为另一个实例,输入设备(例如,操纵杆、键盘、触摸屏)的操作者控制可以由用户接收,然后由用户界面的处理器和存储器处理,以将控制信号输出到一个或多个支撑臂、外部磁体、腔内设备以及递送设备。在一些变体中,输出设备可以包括显示设备,所述显示设备包含发光二极管(led)、液晶显示器(lcd)、电致发光显示器(eld)、等离子体显示板(pdp)、薄膜晶体管(tft)、有机发光二极管(oled)、电子纸/电子墨水显示器、激光显示器和/或全息显示器中的至少一个。
[0407]
通信
[0408]
在一些实施例中,治疗计划系统和/或放疗细胞可以经由,例如,一个或多个网络与其他计算设备通信,每个网络可以是任何类型的网络(例如,有线网络、无线网络)。无线网络可以指未通过任何类型的电缆连接的任何类型的数字网络。无线网络中的无线通信的实例包含但不限于,蜂窝、无线电、卫星以及微波通信。然而,无线网络可以连接到有线网络,以便与互联网、其他运营商语音和数据网络、商业网络以及个人网络连接。有线网络通常通过铜双绞线、同轴电缆和/或光纤电缆承载。存在许多不同类型的有线网络,包含广域网(wan)、城域网(man)、局域网(lan)、互联网(ian)、校园网(can)、全球区域网(gan)(如互联网),以及虚拟专用网(vpn)。在下文中,网络是指通常通过互联网互连的无线、有线、公共以及私有数据网络的任何组合,以提供统一的联网和信息存取系统。
[0409]
蜂窝通信可以包括诸如gsm、pcs、cdma或gprs、w-cdma、edge或cdma2000、lte、wimax以及5g网络标准的技术。一些无线网络部署组合来自多个蜂窝网络的网络或使用蜂窝、wi-fi以及卫星通信的混合。在一些实施例中,本文描述的系统、装置以及方法可以包括射频接收器、发射器和/或光学(例如,红外)接收器和发射器,以与一个或多个设备和/或网络通信。
[0410]
实例
[0411]
图23a-23d描绘了模拟结果,其展示了虚拟定位的原理并展示了移动注量导致剂量的对应移动。模拟是使用bgrt工作流程实现的,其中图像被前向投影和过滤以创建注量。出于这些模拟的目的,放疗系统包括患者平台或床、可围绕床移动(例如,从0度到360度或更多)的可旋转(例如,圆形)机架,以及安装在机架上的治疗放射源(例如,直线加速器),该治疗放射源可以从各种机架角度(发射位置或发射角度)向在床上的患者发射放射。多叶准直器(mlc)可以位于治疗放射源的放射束路径中。图23a是描绘与计划图像相比向左移动6cm(例如,沿iec-x-6cm)的患者(2300)和靶区域(2302)的定位图像的示意图。对于图23b-23d中描绘的结果,计划ct图像沿iec-x移动6cm。由于移动,当靶远离(或接近)治疗放射源时,放大倍数会发生变化。图23b描绘了具有对应于mlc叶的数量和发射位置的数量的行和列的正弦图,其中顶行显示定位函数的投影,中行显示来自位于90度发射角/位置的直线加速器的患者靶区域的光束的眼睛视图,并且底行显示来自位于270度发射角/位置的直线加速器的患者靶区域的光束眼睛视图。左列的正弦图是根据计划图像计算的,并且右列的正
弦图是根据6cm注量移动计算的,以反映治疗时患者靶区域的6cm移动。
[0412]
图23c显示了6cm注量移动之前和之后的剂量(沿x-、y-和z-轴)。还显示了6cm注量移动(使用本文所述的虚拟定位方法应用)之前和之后的剂量概况。如图23c所示,计划注量和移动注量几乎重合。通过将注量图准确分割成机器指令,可以密切保持递送剂量和计划剂量之间的剂量等效性。
[0413]
图23d显示了在6cm注量移动之前和之后从90度发射角/位置观察的剂量(沿x-、y-和z-轴)。如图23d所示,计划注量和移动注量几乎重合;最大剂量值d
max
紧密匹配。下面的这些概况显示,本文描述的虚拟定位方法适应和/或补偿可能由注量移动引起的放大倍数变化,因此,适当地按比例调节剂量以便无论深度(即与直线加速器的距离)如何变化,都能递送计划的剂量。
[0414]
虽然上面已经描述了各种实施例,但是应当理解,它们仅通过实例而非限制的方式呈现。在上述方法指示以特定顺序发生的特定事件的情况下,可以修改特定事件的排序。此外,某些事件可以在可能的情况下在并行过程中同时执行,以及如上所述依次执行。
[0415]
在上述示意图和/或实施例指示以某些取向或位置布置的某些部件的情况下,可以修改部件的布置。虽然已经具体地示出和描述了实施例,但是应当理解,可以在形式和细节上进行各种改变。除了相互排斥的组合之外,本文描述的装置和/或方法的任何部分可以以任何组合进行组合。本文描述的实施例可以包括所描述的不同实施例的功能、组分和/或特征的各种组合和/或子组合。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。