辅酶q10在制备脊柱老化性疾病治疗药物中的应用
技术领域
1.本发明涉及医学领域,具体涉及辅酶q10在制备脊柱老化性疾病治疗药物中的应用,尤其涉及其在椎间盘退变突出治疗药物中的应用。
背景技术:
2.目前,脊柱老化性疾病,尤其椎间盘退变性疾病在临床上多见,患者一般需要卧床休息,康复理疗及药物治疗,但其中仍有相当一部分患者效果不佳,并需要进行手术治疗[1]。然而手术本身存在相关风险及并发症,有其自身的限制因素。随着人口老龄化及发病患者年轻化,脊柱老化性疾病,尤其椎间盘退变突出已经对社会及家庭造成巨大负担。
[0003]
目前临床使用的治疗药物多针对具体症状,而对退变椎间盘本身进行保护及改善的相关药物种类少,患者选择余地小。同时,目前使用相关药物疗效有限,且长期应用有一定副作用,所以在一定程度上限制了使用。
[0004]
近期研究提示,保护性小分子在椎间盘退变中存在潜在应用价值[2]。我们通过前期实验,对fda批准的药物辅酶q10进行磷脂微球的构建并予以应用研究,发现其对椎间盘退变过程具有改善功能,可为长期使用从而减少椎间盘退变突出发病提供潜在方法。
[0005]
[1]m.yao,b.p.xu,z.j.li,s.zhu,z.r.tian,d.h.li,j.cen,s.d.cheng,y.j.wang,y.m.guo,x.j.cui,a comparison between the low back pain scales for patients with lumbar disc herniation:validity,reliability,and responsiveness,health and quality of life outcomes 18(1)(2020)175.
[0006]
[2]a.kamali,r.ziadlou,g.lang,j.pfannkuche,s.cui,z.li,r.g.richards,m.alini,s.grad,small molecule-based treatment approaches for intervertebral disc degeneration:current options and future directions,theranostics 11(1)(2021)27-47.
技术实现要素:
[0007]
本发明的目的是提供一种具有抗氧化特性的辅酶q10,尤其其缓释形式,特别的针对其磷脂微球缓释形式在制备脊柱老化性疾病治疗药物中的应用。
[0008]
辅酶q10,又名泛醌10,是一种存在于自然界的脂溶性醌类化合物,其结构与维生素k、维生素e与质体醌相似。在人类身体细胞内参与能量制造及活化,是预防多种疾病过程的最有效的抗氧化成份之一。
[0009]
其中,缓释辅酶q10的磷脂微球作为一种抗炎抗氧化新型材料,具有改善椎间盘细胞代谢,改善椎间盘退变性疾病病情的作用,且体外实验未显示缓释辅酶q10的磷脂微球有细胞毒性作用,药物长期使用更加安全。因此本发明选择缓释辅酶q10的磷脂微球进行具体的研究。
[0010]
具体的,本发明的技术方案是:
[0011]
辅酶q10(coenzyme q10),cas:303-98-0,其分子量:863.344。
[0012]
辅酶q10大量表达于多种食物之中,作为临床常用药物成分,合成提纯工艺简单,价格低廉,这也是其相较于其他椎间盘退变保护性分子的优势所在。同时,目前对于其纯度,已经达到98%以上,纯度符合药物制备要求。
[0013]
然而,辅酶q10作为脂溶性分子,其给药方式及药物吸收利用方式在一定程度上影响其药物递送效率。
[0014]
本发明制备磷脂胶束微球提供抗炎抗氧化药物缓释辅酶q10的高效递送,并在椎间盘退变性疾病模型中进行应用,尤其的,在应用机理上,其作为氧化应激反应拮抗分子,阻断氧化应激及改善局部细胞活性的功能实现。
[0015]
具体的,尤其是在制备椎间盘突出保护性药物中的应用,首选局部注射使用。
[0016]
本发明所述药物,还包括药学上可接受的载体、助剂或稀释剂。
[0017]
所述药物的形式选自如下之一:喷雾、气溶胶、溶液、洗液、凝胶、片剂、胶囊、软膏、糊剂、乳剂和悬浮液。
[0018]
优选的,所述药物的形式优选局部注射使用。
[0019]
通过体外细胞实验及体内动物模型实验结果表明,缓释辅酶q10的磷脂微球可拮抗h2o2诱导的氧化应激反应,并在脊柱老化性疾病,尤其椎间盘退变性疾病中发挥保护性作用。
[0020]
辅酶q10属于细胞氧化应激拮抗分子,可通过现有技术直接合成纯化,从而降低成本。另外,动物模型中,缓释辅酶q10的磷脂微球的长期应用未见明显毒副作用,可用于椎间盘退变性疾病等领域。
[0021]
因此其在制备脊柱老化性疾病,尤其椎间盘退变性疾病治疗药物中具有可预期的应用,具有广阔的市场前景。
附图说明
[0022]
图1是缓释辅酶q10的磷脂微球在大鼠椎间盘退变模型中的mri治疗效果图像
[0023]
图2是缓释辅酶q10的磷脂微球在大鼠椎间盘退变模型中的基于mri信号的统计学分析
[0024]
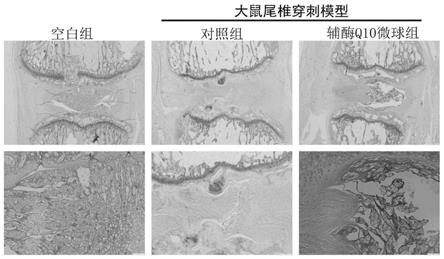
图3是缓释辅酶q10的磷脂微球在大鼠椎间盘退变模型中的he染色图像
[0025]
图4是缓释辅酶q10的磷脂微球在大鼠椎间盘退变模型中基于he组织学染色图像的统计学分析
[0026]
图5是缓释辅酶q10的磷脂微球对于h2o2诱导的髓核细胞氧化应激反应ros的减轻作用
具体实施方式
[0027]
以下实施例中涉及的实验动物、试剂、培养基和缓冲液的来源:
[0028]
辅酶q10(coenzyme q10),cas:303-98-0。其分子量:863.344(北京百奥莱博医学化工有限公司)
[0029]
磷脂微球,cas:474922-84-4,其分子量:5676(上海艾伟拓医药科技有限公司)
[0030]
sd雄性大鼠,(山东大学动物中心)
[0031]
pbs缓冲液,(碧云天生物试剂公司)
[0032]
ripa细胞蛋白质提取裂解液(thermo fisher,pierce)
[0033]
蛋白酶抑制剂(北京索莱宝科技有限公司)
[0034]
bca蛋白定量试剂盒(上海炎熙生物科技有限公司)
[0035]
complete edta-free(罗氏生物医药)
[0036]
二甲苯(国药集团化学试剂有限公司)
[0037]
中性树胶(上海泰坦科技股份有限公司)
[0038]
浓盐酸(国药集团化学试剂有限公司)
[0039]
伊红(上海泰坦科技股份有限公司)
[0040]
苏木素(上海泰坦科技股份有限公司)
[0041]
甲醇(国药集团化学试剂有限公司)
[0042]
柠檬酸盐缓冲液(0.01m,ph=6.0)(生工生物工程上海股份有限公司)
[0043]
10%ngs(生工生物工程上海股份有限公司)
[0044]
过氧化氢(h2o2)(国药集团化学试剂有限公司)
[0045]
bsa(生工生物工程上海股份有限公司)
[0046]
无水乙醇(国药集团化学试剂有限公司)
[0047]
细胞计数仪购自美国thermo fisher公司
[0048]
显微镜购自上海蔡康光学仪器有限公司
[0049]
离心机购自济南欧莱博医疗器械有限公司
[0050]
电子天平购自济南欧莱博医疗器械有限公司
[0051]
酶联免疫检测仪(酶标仪)购自北京美华仪科技有限公司
[0052]
制冰机购自济南欧莱博医疗器械有限公司
[0053]
超纯水系统购自济南欧莱博医疗器械有限公司
[0054]
涡旋混合器购自济南欧莱博医疗器械有限公司
[0055]
1.尾椎间盘穿刺大鼠模型构建
[0056]
在12周龄野生型sd雄性大鼠中建立尾椎间盘穿刺模型(共21只)。首先,用剃刀和脱毛膏清理所有大鼠的尾部皮肤。空白组的sd大鼠(7只)不做任何处理。阳性对照组的sd大鼠(7只)在第8/9尾椎间盘上进行20g针头穿刺5mm,并在间盘内旋转180度。试验组的sd大鼠(7只)在第8/9尾椎间盘上进行20g针头穿刺5mm,并在间盘内旋转180度。模型建立后,使用无菌pbs(阳性对照)或缓释辅酶q10的磷脂微球,局部注射。
[0057]
4周后,将所有组的小鼠用过量的10%水合氯醛(山东大学齐鲁医院)安乐死,收集尾椎标本用于mri检测,分析信号改变的程度。
[0058]
图1-2为本部分实验的结果,图1为磁共振图像,图2为基于mri的信号评分,均显示大鼠的尾椎间盘退变在缓释辅酶q10的磷脂微球治疗下有明显缓解。
[0059]
2.组织切片制备
[0060]
将来自所有组的大鼠椎间盘组织固定在10%福尔马林中,至少在室温下固定72小时。50%乙醇(60分钟)、70%乙醇(60分钟)、85%乙醇(60分钟)、95%乙醇(60分钟)、100%乙醇(30分钟)、100%乙醇(30分钟)依次进行组织脱水;经过乙醇和二甲苯(60分钟)、二甲苯(60分钟)依次处理;然后用二甲苯和石蜡(60分钟),石蜡(80分钟)透明;将组织放入盒中,用石蜡填充,然后将其放在石蜡包埋机的冷台上。将嵌入的组织石蜡块置于切片机上并
切片,组织厚度约4μm;将含有组织的石蜡片轻轻涂抹在42℃的水中。完全展平后,用干净的玻璃片轻轻拨起切片;将切片放在载玻片上,编号,并在68℃的烤箱中烘烤至少6小时。
[0061]
3.苏木精/伊红染色
[0062]
切片常规脂溶性溶剂脱蜡至水(二甲苯两次,15分钟/每次;100%酒精5分钟;95%酒精5分钟;75%酒精5分钟;50%酒精5分钟),然后使用苏木精染色液染色5分钟,用清水冲洗干净后,继续使用伊红染色液染色5分钟,清水冲洗干净后脱水(50%酒精5分钟;75%酒精5分钟;95%酒精5分钟;100%酒精5分钟;二甲苯两次,15分钟/每次),后等切片晾干后使用中性树胶封片,放在光学显微镜下观察,并使用image j进行组织学评分分析。
[0063]
图3-4为本部分实验的结果图,图3为he组织学染色,图4为基于he染色的组织学评分,表明缓释辅酶q10的磷脂微球的使用减轻了尾椎穿刺模型中大鼠椎间盘组织的损伤退变。
[0064]
4.人原代髓核细胞培养
[0065]
行后路腰椎减压椎间融合术患者术中髓核取出(样本的收集经山东大学齐鲁医院伦理委员会审核通过),用无菌pbs冲洗3次后,清除终板软骨和纤维环。将剩余髓核组织切成大约1立方毫米组织块。然后用0.25%胰蛋白酶(hyclone,logan,usa)消化30分钟,再用0.2%ii型胶原(sigma-aldrich,st.louis,usa)消化4小时。在dmem/f-12培养基(hyclone,thermo co)中加入10%的牛血清(fbs,gibco,usa)、1%100u/ml青霉素和100mg/ml链霉素(hyclone,usa),于ph7.2同步培养髓核细胞(95%空气,5%co2,37℃)。培养基每3天更换一次,细胞达到80-90%汇合时传代。第二代或第三代细胞用于指定的实验。
[0066]
5.细胞氧化应激反应ros测定
[0067]
在本实验中,我们使用ros检测试剂盒(s0033;beyotime生物科技)进行细胞内的ros检测。所有的步骤都按照生产商的产品说明进行。首先使用无菌pbs清洗髓核细胞两遍,然后用10μm dcfda进行暗箱孵育,条件为37℃,持续20分钟,且每4分钟进行一次混匀。随后,使用无血清培养基清洗髓核细胞3遍以排除多余dcfda干扰。最后,dcfda荧光信号强度由lsm780激光扫描共聚焦显微镜(蔡司公司,德国)进行观察及检测。
[0068]
图5为本实验结果图,通过使用ros检测试剂盒,观察h2o2刺激所导致的氧化应激反应水平异常,而缓释辅酶q10的磷脂微球则减轻了髓核细胞在氧化应激刺激下的这一退变现象。
[0069]
6.统计学分析
[0070]
所有数据均以至少三次独立实验的平均数士标准差表示。对于两组数据的统计学分析采用配对t检验多于两组数据的统计学分析采用单因素方差分析。
[0071]
通过上述实验,证实缓释辅酶q10的磷脂微球能够直接拮抗氧化应激反应介导的椎间盘退变过程,并且对于针刺损伤诱导的椎间盘退变动物模型有确切疗效,并有效促使椎间盘内环境稳态。同时,辅酶q10是一种临床常用小分子药物,使用磷脂微球给药体系便于髓核细胞吸收利用,填补目前国内椎间盘退变防治药物的空白。
[0072]
另外,细胞实验显示,缓释辅酶q10的磷脂微球可以减轻炎性刺激所造成的线粒体结构功能紊乱及氧化应激过程,在髓核细胞退变过程中发挥保护作用。
[0073]
更为重要的是,辅酶q10提纯工艺简单,磷脂微球制备方法纯熟,可明显降低成本,从而降低患者经济负担。
[0074]
以上对本发明的一个实施例进行了详细说明,但所述内容仅为本发明的较佳实施例,不能被认为用于限定本发明的实施范围。凡依本发明申请范围所作的均等变化与改进等,均应仍归属于本发明的专利涵盖范围之内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。