普氏菌属制剂以及治疗慢性阻塞性肺部疾病(copd)和其他肺部疾病
1.有关联邦资助的研究的声明
2.本发明得到国家卫生研究院(national institutes of health)授予的第ar060077号政府资助。政府对本发明拥有一定的权利。
3.相关申请的交叉引用
4.本技术要求于2019年6月17日提交的美国临时申请序列号62/862,186的优先权,该申请通过引用整体并入本文。
技术领域
5.本发明涉及普氏菌属(例如组织普氏菌(p.histicola))制剂以及使用普氏菌属(例如组织普氏菌(p.histicola))制剂治疗慢性阻塞性肺部疾病(copd)和其他肺部疾病。本发明还涉及(a)产黑色素普氏菌(p.melaninogenica)的制剂和(b)普氏菌属菌种(例如组织普氏菌和/或产黑色素普氏菌)的囊泡以及此类制剂和/或此类囊泡用于治疗诸如copd等肺部疾病的用途。
背景技术:
[0006][0007]
动物的消化道中存在大量微生物,通常被称为肠道菌群或微生物菌群。细菌构成了结肠中的大部分菌群和大约60%的粪便干物质。事实上,肠道中可能生活着300到1000种不同的菌种。
技术实现要素:
[0008]
本发明提供了与使用含有活的和/或灭活的普氏菌属(例如,组织普氏菌)的组合物治疗copd相关的方法和材料。本发明还提供了含有活的和/或灭活的普氏菌属(例如,组织普氏菌)的组合物以及用于制备此类组合物的方法和材料。例如,本发明以口服药物或膳食补充剂(例如,丸剂、片剂、胶囊)的形式提供了包含活的和/或灭活的普氏菌属(例如,组织普氏菌)的组合物。在一些情况下,本发明提供的包含活的和/或灭活的普氏菌属(例如,组织普氏菌)的组合物可用作口服copd药物或膳食补充剂以治疗copd。在一些情况下,本发明提供的包含活的和/或灭活的普氏菌属(例如,组织普氏菌)的组合物可以用作呼吸系统(例如,鼻)copd药物来治疗copd。
[0009]
本文提供的包含活的和/或灭活的普氏菌属(例如,组织普氏菌)的组合物以及使用如本文所述的此类组合物的方法可以允许医学专业人员有效地治疗患有copd的对象(例如,哺乳动物(例如,人)患者)。在一些情况下,本文提供的方法和材料可以允许人们用能够降低copd严重程度或减缓其发展的细菌生物体补充他们的饮食。
[0010]
一般而言,本发明的一个方面提供了一种治疗哺乳动物慢性阻塞性肺部疾病(copd)的方法。该方法包括(或基本上由以下组成或由以下组成)向哺乳动物施用包含活的
或灭活的普氏菌属的组合物。该组合物可包含活的普氏菌属。该组合物可包含灭活的普氏菌属和不含活的普氏菌属。哺乳动物可以是人。哺乳动物可以是啮齿动物。施用可以包括口服施用。该组合物可以是丸剂、片剂或胶囊。该组合物可以是被配制为将普氏菌属递送至哺乳动物肠道的丸剂、片剂或胶囊。施用可以包括对呼吸系统的施用。该组合物可以使用鼻喷雾剂、吸入剂或雾化剂施用。施用后可以降低copd症状的严重程度。施用后,copd症状的严重程度可降低约25%以上。施用后,copd症状的严重程度可降低约50%以上。施用后,copd症状的严重程度可降低约75%以上。在施用步骤之后,哺乳动物的肺顺应性会降低。与施用前相比,施用后的肺顺应性降低了至少约5%。与施用前相比,施用后的肺顺应性可降低至少约10%。与施用前相比,施用后的肺顺应性可降低至少约15%。该方法还可包括在施用前测量一种或多种肺功能参数,并在施用后测量相同的一种或多种肺功能参数。与施用前相比,施用后测量的一种或多种肺功能参数中的至少一种可以得到改善。一种或多种肺功能参数可包括肺顺应性、肺容积、气道阻力、弹性或其组合。该方法可以包括在施用步骤之前将哺乳动物鉴定为患有copd。该方法可以包括在施用步骤之前将哺乳动物鉴定为患有肺气肿。组织普氏菌的代表性细胞可以是那些以nrrl登录号b-50329保藏的细胞。该组合物可以包含约1x103至约1x10
14
cfu的普氏菌属。该组合物可以包含约1x105至约1x10
12
cfu的普氏菌属。该组合物可以包含约1x108至约1x10
10
cfu的普氏菌属。该组合物可以每天施用一次。该组合物可以每天施用两次。该组合物可以每天施用三次。该组合物可以施用至少约4周的时间。该组合物可以施用至少约8周的时间。普氏菌属可以包含组织普氏菌(或基本上由其组成或由其组成)。
[0011]
在另一方面,本发明提供了慢性阻塞性肺部疾病(copd)的非人哺乳动物模型。非人哺乳动物模型的体细胞包含编码一种或多种人hla血清型的核酸,其中,所述非人哺乳动物模型的体细胞缺乏内源性mhc ii类分子和内源性il-17多肽的表达,并且其中,当暴露于香烟烟雾约2-6周时,与未暴露于香烟烟雾的对照模型相比,该模型的肺功能下降。人hla血清型可以是dq8。该模型可以是il-17-/-敲除哺乳动物。哺乳动物可以是啮齿动物。哺乳动物可以是小鼠。哺乳动物可具有约45至约185ng/ml的血液烟碱水平。哺乳动物可具有约50至约150ng/ml的血液烟碱水平。与不是copd的非人动物模型的对照哺乳动物相比,哺乳动物的cxcr3、cxcl10或两者的表达水平可以提高。与不是copd的非人动物模型的对照哺乳动物相比,哺乳动物的一种或多种纤维化相关基因的表达水平可以降低。至少一种纤维化相关基因可以选自:胶原a1、纤连蛋白和转化生长因子β。可以使用一种或多种肺功能参数来测量肺功能的降低。一种或多种肺功能参数可包括肺顺应性、肺容积、气道阻力、弹性或其组合。
[0012]
在另一方面,本发明提供了一种产生慢性阻塞性肺部疾病(copd)的非人哺乳动物模型的方法。所述方法包括(a)提供非人哺乳动物,其中所述非人哺乳动物的体细胞包含编码一种或多种人hla血清型的核酸,并且其中所述非人哺乳动物模型的体细胞缺乏内源性mhc ii类分子和内源性il-17多肽的表达;(b)将哺乳动物暴露于香烟烟雾约3-6周,从而产生copd的非人动物模型。人hla血清型可以是dq8。哺乳动物可以是il-17-/-。哺乳动物可以是啮齿动物。哺乳动物可以是小鼠。暴露可包括将哺乳动物暴露于约2支香烟约10分钟,每天约3小时,每周约5天。暴露可包括充分暴露于香烟烟雾以产生约45至约185ng/ml的血液烟碱水平。暴露可包括充分暴露于香烟烟雾以产生约50至约150ng/ml的血液烟碱水平。与
暴露于空气而不是香烟烟雾的类似哺乳动物相比,暴露后,哺乳动物的cxcr3、cxcl10或两者的表达水平会提高。与暴露于空气而不是香烟烟雾的类似哺乳动物相比,暴露后,哺乳动物的一种或多种纤维化相关基因的表达水平会降低。至少一种纤维化相关基因可以选自:胶原a1、纤连蛋白和转化生长因子β。与暴露于空气而不是香烟烟雾的类似哺乳动物相比,暴露后,哺乳动物的肺功能可能会下降。可以使用一种或多种肺功能参数来测量肺功能的降低。一种或多种肺功能参数可包括肺顺应性、肺容积、气道阻力、弹性或其组合。
[0013]
另一方面,本发明提供了通过以下方法产生的copd的非人哺乳动物模型,所述方法包括(a)提供非人哺乳动物,其中非人哺乳动物的体细胞包含编码一种或多种人类hla血清型的核酸,并且其中非人哺乳动物模型的体细胞缺乏内源性mhc ii类分子和内源性il-17多肽的表达;(b)将哺乳动物暴露于香烟烟雾约3-6周,从而产生copd的非人动物模型。人hla血清型可以是dq8。哺乳动物可以是il-17-/-。哺乳动物可以是啮齿动物。哺乳动物可以是小鼠。暴露可包括将哺乳动物暴露于约2支香烟约10分钟,每天约3小时,每周约5天。暴露可包括充分暴露于香烟烟雾以产生约45至约185ng/ml的血液烟碱水平。暴露可包括充分暴露于香烟烟雾以产生约50至约150ng/ml的血液烟碱水平。与暴露于空气而不是香烟烟雾的类似哺乳动物相比,暴露后,哺乳动物的cxcr3、cxcl10或两者的表达水平会提高。与暴露于空气而不是香烟烟雾的类似哺乳动物相比,暴露后,哺乳动物的一种或多种纤维化相关基因的表达水平会降低。至少一种纤维化相关基因可以选自:胶原a1、纤连蛋白和转化生长因子β。与暴露于空气而不是香烟烟雾的类似哺乳动物相比,暴露后,哺乳动物的肺功能可能会下降。可以使用一种或多种肺功能参数来测量肺功能的降低。一种或多种肺功能参数可包括肺顺应性、肺容积、气道阻力、弹性或其组合。
[0014]
另一个方面,本发明提供了一种治疗哺乳动物肺部疾病的方法。该方法包括(或基本上由以下组成或由以下组成)向哺乳动物施用包含活的或灭活的普氏菌属的组合物。该组合物可包含活的普氏菌属。该组合物可包含灭活的普氏菌属和不含活的普氏菌属。哺乳动物可以是人。哺乳动物可以是啮齿动物。施用可以包括口服施用。该组合物可以是丸剂、片剂或胶囊剂。该组合物可以是被配制为将普氏菌属递送至哺乳动物肠道的丸剂、片剂或胶囊。施用可以包括对呼吸系统的施用。该组合物可以使用鼻喷雾剂、吸入剂或雾化剂施用。施用后可以降低肺部疾病症状的严重程度。施用后,肺部疾病症状的严重程度可降低约25%以上。施用后,肺部疾病症状的严重程度可降低约50%以上。施用后,肺部疾病症状的严重程度可降低约75%以上。在施用步骤之后,哺乳动物的肺顺应性会降低。与施用前相比,施用后的肺顺应性可降低至少约5%。与施用前相比,施用后的肺顺应性可降低至少约10%。与施用前相比,施用后的肺顺应性可降低至少约15%。该方法还可包括在施用前测量一种或多种肺功能参数,并在施用后测量相同的一种或多种肺功能参数。与施用前相比,施用后测量的一种或多种肺功能参数中的至少一种可以得到改善。一种或多种肺功能参数可包括肺顺应性、肺容积、气道阻力、弹性或其组合。该方法可以包括在施用步骤之前将哺乳动物鉴定为患有肺部疾病。该方法可以包括在施用步骤之前将哺乳动物鉴定为患有肺炎。普氏菌属的代表性细胞可以是以nrrl登录号b-50329保藏的细胞。该组合物可以包含约1x103至约1x10
14
cfu的普氏菌属。该组合物可以包含约1x105至约1x10
12
cfu的普氏菌属。该组合物可以包含约1x108至约1x10
10
cfu的普氏菌属。该组合物可以每天施用一次。该组合物可以每天施用两次。该组合物可以每天施用三次。该组合物可以施用至少约4周的时间。该
组合物可以施用至少约8周的时间。普氏菌属(prevotella)可包括组织普氏菌(prevotella histicola)。肺部疾病可以选自:慢性阻塞性肺部疾病(copd)、哮喘、肺纤维化、结节病、感染引起的疾病以及它们的组合。感染引起的疾病可以选自:病毒感染、细菌感染、真菌感染、寄生虫感染及其组合。病毒感染可选自:病毒性肺炎、病毒性支气管炎、流感、冠状病毒感染、腺病毒感染、合胞病毒感染、鼻病毒感染及其组合。细菌感染可选自:链球菌感染、葡萄球菌感染、衣原体感染、支原体感染、嗜血杆菌感染、棒状杆菌感染、分枝杆菌感染、军团菌感染及其组合。肺部疾病可以包括肺炎。
[0015]
另一个方面,本发明提供了一种治疗哺乳动物肺部疾病的方法。该方法包括(或基本上由以下组成或由以下组成)向哺乳动物施用包含活的或灭活的产黑色素普氏菌(prevotella melaninogenica)的组合物。该组合物可包含活的产黑色素普氏菌。该组合物可包含灭活的产黑色素普氏菌和不含活的产黑色素普氏菌。哺乳动物可以是人。哺乳动物可以是啮齿动物。施用可以包括口服施用。该组合物可以是丸剂、片剂或胶囊剂。该组合物可以是被配制为将产黑色素普氏菌递送至哺乳动物肠道的丸剂、片剂或胶囊。施用可以包括对呼吸系统的施用。该组合物可以使用鼻喷雾剂、吸入剂或雾化剂施用。施用后可以降低肺部疾病症状的严重程度。施用后,肺部疾病症状的严重程度可降低约25%以上。施用后,肺部疾病症状的严重程度可降低约50%以上。施用后,肺部疾病症状的严重程度可降低约75%以上。在施用步骤之后,哺乳动物的肺顺应性会降低。与施用前相比,施用后的肺顺应性可降低至少约5%。与施用前相比,施用后的肺顺应性可降低至少约10%。与施用前相比,施用后的肺顺应性可降低至少约15%。该方法还可包括在施用前测量一种或多种肺功能参数,并在施用后测量相同的一种或多种肺功能参数。与施用前相比,施用后测量的一种或多种肺功能参数中的至少一种可以得到改善。一种或多种肺功能参数可包括肺顺应性、肺容积、气道阻力、弹性或其组合。该方法可以包括在施用步骤之前将哺乳动物鉴定为患有肺部疾病。该方法可以包括在施用步骤之前将哺乳动物鉴定为患有肺炎。该方法可以包括在施用步骤之前将哺乳动物鉴定为患有copd。该组合物可以包含约1x103至约1x10
14
cfu的产黑色素普氏菌。该组合物可以包含约1x105至约1x10
12
cfu的产黑色素普氏菌。该组合物可以包含约1x108至约1x10
10
cfu的产黑色素普氏菌。该组合物可以每天施用一次。该组合物可以每天施用两次。该组合物可以每天施用三次。该组合物可以施用至少约4周的时间。该组合物可以施用至少约6周的时间。该组合物可以施用至少约8周的时间。肺部疾病可以选自:慢性阻塞性肺部疾病(copd)、哮喘、肺纤维化、结节病、感染引起的疾病以及它们的组合。感染引起的疾病可以选自:病毒感染、细菌感染、真菌感染、寄生虫感染及其组合。病毒感染可选自:病毒性肺炎、病毒性支气管炎、流感、冠状病毒感染、腺病毒感染、合胞病毒感染、鼻病毒感染及其组合。细菌感染可选自:链球菌感染、葡萄球菌感染、衣原体感染、支原体感染、嗜血杆菌感染、棒状杆菌感染、分枝杆菌感染、军团菌感染及其组合。肺部疾病可以包括肺炎。
[0016]
另一个方面,本发明提供了一种治疗哺乳动物肺部疾病的方法。该方法包括(或基本上由以下组成或由以下组成)向哺乳动物施用包含普氏菌属菌种的囊泡的组合物。哺乳动物可以是人。哺乳动物可以是啮齿动物。施用可以包括口服施用。该组合物可以是丸剂、片剂或胶囊剂。该组合物可以是被配制为将普氏菌属菌种的囊泡递送至哺乳动物肠道的丸剂、片剂或胶囊。施用可以包括对呼吸系统的施用。该组合物可以使用鼻喷雾剂、吸入剂或雾化剂施用。施用后可以降低肺部疾病症状的严重程度。施用后,肺部疾病症状的严重程度
可降低约25%以上。施用后,肺部疾病症状的严重程度可降低约50%以上。施用后,肺部疾病症状的严重程度可降低约75%以上。在施用步骤之后,哺乳动物的肺顺应性会降低。与施用前相比,施用后的肺顺应性可降低至少约5%。与施用前相比,施用后的肺顺应性可降低至少约10%。与施用前相比,施用后的肺顺应性可降低至少约15%。该方法还可包括在施用前测量一种或多种肺功能参数,并在施用后测量相同的一种或多种肺功能参数。与施用前相比,施用后测量的一种或多种肺功能参数中的至少一种可以得到改善。一种或多种肺功能参数可包括肺顺应性、肺容积、气道阻力、弹性或其组合。该方法可以包括在施用步骤之前将哺乳动物鉴定为患有肺部疾病。该方法可以包括在施用步骤之前将哺乳动物鉴定为患有肺炎。普氏菌属菌种的代表性细胞可以是以nrrl登录号b-50329保藏的细胞。该组合物可以每天施用一次。该组合物可以每天施用两次。该组合物可以每天施用三次。该组合物可以施用至少约4周的时间。该组合物可以施用至少约8周的时间。普氏菌属(prevotella)菌种可包括组织普氏菌(prevotella histicola)。普氏菌属(prevotella)菌种可包括产黑色素普氏菌(prevotella melaninogenica)。肺部疾病可以选自:慢性阻塞性肺部疾病(copd)、哮喘、肺纤维化、结节病、感染引起的疾病以及它们的组合。感染引起的疾病可以选自:病毒感染、细菌感染、真菌感染、寄生虫感染及其组合。病毒感染可选自:病毒性肺炎、病毒性支气管炎、流感、冠状病毒感染、腺病毒感染、合胞病毒感染、鼻病毒感染及其组合。细菌感染可选自:链球菌感染、葡萄球菌感染、衣原体感染、支原体感染、嗜血杆菌感染、棒状杆菌感染、分枝杆菌感染、军团菌感染及其组合。肺部疾病可以包括肺炎。
[0017]
除非另外定义,本文使用的所有技术和科学术语的意义与本发明所属领域普通技术人员通常所理解的相同。虽然在本发明的实施可以采用类似于或等同于本文所述的那些方法和材料,但下文描述了合适的方法和材料。本文中述及的所有出版物、专利申请、专利和其它参考文献都通过引用全文纳入本文。若有抵触,以本包括定义在内的本技术说明书为准。此外,材料、方法和实施例都仅是说明性的,并不意在构成限制。
[0018]
附图和以下说明进一步详细说明了本发明的一种或多种实施方式。本发明的其他特征、目的和优点将从说明书、附图以及权利要求中显而易见。
附图说明
[0019]
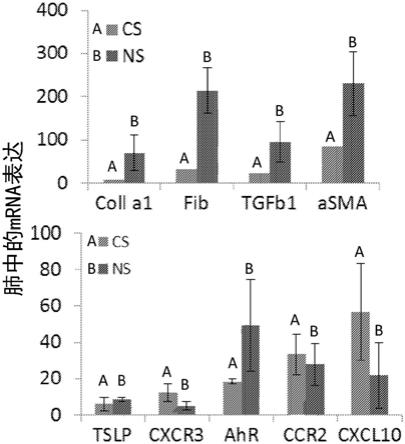
图1的柱状图显示了暴露于香烟烟雾(cs)或空气(ns)5周的dq8小鼠中通过rtpcr测量的各种蛋白质在肺中的表达。(n=3只小鼠/组)
[0020]
图2a是显示dq8小鼠暴露于空气(ns)4周后肺顺应性(cst)(作为pv曲线)的图。n=7。
[0021]
图2b是显示dq8小鼠暴露于cs 4周后肺顺应性(cst)(作为pv曲线)的图。n=7。
[0022]
图2c是显示dq8.il-17-/-小鼠暴露于cs 4周后肺顺应性(cst)(作为pv曲线)的图。n=4。
[0023]
图3的柱状图显示图2a-2c中各个组的汇编数据。
[0024]
图4显示示例性组织普氏菌(p.histicola)16s rrna序列(seq id no:1和seq id no:2)。
[0025]
图5a显示了cs暴露的dq8小鼠肺顺应性的代表性pv曲线。
[0026]
图5b显示了用组织普氏菌处理的cs暴露的dq8小鼠肺顺应性的代表性pv曲线。
[0027]
图5c显示了用产黑色素普氏菌处理的cs暴露的dq8小鼠肺顺应性的代表性pv曲线。
[0028]
图5d是幼稚dq8小鼠以及图5a-5c的小鼠的肺顺应性的图。
[0029]
图6是幼稚dq8.il17-/-小鼠(n)、用香烟烟雾(cs)处理、用香烟烟雾和组织普氏菌(cs/ph)处理、或用香烟烟雾和产黑色素普氏菌(cs/pm)处理的相同类型小鼠的肺顺应性的图。
[0030]
图7是用cs(cs)处理、用组织普氏菌的外膜囊泡(omv)(cs/ph/omv)处理、或用产黑色素普氏菌的omv(cs/pm/omv)处理的相同类型的dq8小鼠的肺顺应性的图。
[0031]
图8a是用cs(dq8 cs幼稚)处理、或用cs和组织普氏菌(dq8幼稚cs组织普氏菌)处理的dq8小鼠中il-1b转录的图。
[0032]
图8b是用cs(dq8 cs幼稚)处理、或用cs和组织普氏菌(dq8幼稚cs组织普氏菌)处理的dq8小鼠中tnf转录的图。
[0033]
图8c是用cs(dq8 cs幼稚)处理、或用cs和组织普氏菌(dq8幼稚cs组织普氏菌)处理的dq8小鼠中il-23a转录的图。
[0034]
图8d是用cs(dq8 cs幼稚)处理、或用cs和组织普氏菌(dq8幼稚cs组织普氏菌)处理的dq8小鼠中t ctla-4转录的图。
[0035]
图8e是用cs(dq8 cs幼稚)处理、或用cs和组织普氏菌(dq8幼稚cs组织普氏菌)处理的dq8小鼠中il-13转录的图。
[0036]
图9a是dq8小鼠中的il-1b转录的图:幼稚小鼠(幼稚)、cs处理的小鼠(dq8 cs幼稚)、以及用cs和组织普氏菌处理的小鼠(dq8幼稚cs组织普氏菌)。
[0037]
图9b是dq8小鼠中的ctla-4转录的图:幼稚小鼠(幼稚)、cs处理的小鼠(dq8 cs幼稚)、以及用cs和组织普氏菌处理的小鼠(dq8幼稚cs组织普氏菌)。
[0038]
图10a是用cs(dq8 cs幼稚)处理、或用cs和组织普氏菌(dq8幼稚cs组织普氏菌)处理的dq8小鼠中il-17r转录的图。
[0039]
图10b是用cs(dq8 cs幼稚)处理、或用cs和组织普氏菌(dq8幼稚cs组织普氏菌)处理的dq8小鼠中il-6转录的图。
[0040]
图11是暴露于cs 2周并用ii型胶原(cii)免疫的小鼠的肺顺应性的柱状图,其中一半用牙龈卟啉单胞菌(porphorymonas gingivalis)处理。
具体实施方式
[0041]
慢性阻塞性肺部疾病copd是第五大死亡原因。据信吸烟是导致肺气肿/copd发展的重要病因。香烟烟雾(cs)被认为是肺气肿/copd发病机制中的一个促成因素。copd有时表征为气道炎症和发展为不可逆气流受限的肺气肿。戒烟并不总能影响疾病进展,这表明除了吸烟外,其他内源性因素也参与了疾病的进展。鉴于目前阻止copd进展的疗法的局限性,确定与发病机制有关的因素作为治疗靶点是有帮助的。
[0042]
吸烟是加剧自身免疫和炎症性疾病的主要环境因素。cs引起炎症的机制已被广泛研究。人们认为cs通过诱导嗜中性粒细胞和其他分泌il-17的促炎细胞的流入而促使免疫失调。粘膜相关共生体对th17细胞的分化有助于保护免受感染。肺部不是无菌的,肺部微生物群可能是cs引起的肺部炎症的一个因素。这一概念得到了肠道微生物群在调节适应性和
先天免疫反应中的作用的支持。关于肺微生物组在copd中的作用的信息有限。与健康肺相比,吸烟者的肺和copd肺的微生物组组成发生变化(参见例如yadava,k.等人,am j respir crit care med 193:975-987,2016;wang,z.等人,thorax 73:331-338(2018);larsen,j.immunology 151.4:363-374(2017);scher,j.等人,microbiome 4.1:60(2016))。在某些情况下,已观察到肺和口腔微生物群之间的关系比肺和鼻微生物群之间的关系更密切(参见例如bassis,c.m.等人,mbio 6:e00037(2015))。copd微生物组可能含有丰富的假单胞菌属(pseudomonas)和嗜血杆菌属(haemophilus),但可能缺乏普遍存在的属于普氏菌属(prevotella)的口腔和肠道微生物(参见例如wang,z.等人,thorax 73:331-338(2018))。
[0043]
普氏菌属的任何适当菌种或菌种组合可用于本文所述的任何方法。在一些实施方式中,可以使用组织普氏菌。在一些实施方式中,可以使用产黑色素普氏菌。在一些实施方式中,可以使用组织普氏菌和产黑色素普氏菌。在一些情况下,普氏菌属菌种的组合可以平衡免疫反应并改善肺部疾病中的肺功能(例如本文所述的任何肺部疾病,例如copd)。
[0044]
本发明提供了治疗哺乳动物肺部疾病的方法。所述方法可以包括向哺乳动物施用包含(a)普氏菌属菌种(例如,组织普氏菌和/或产黑色素普氏菌),和/或(b)普氏菌属菌种(例如,组织普氏菌和/或产黑色素普氏菌)的囊泡的组合物。可以如本文所述治疗的肺部疾病的例子包括但不限于:copd、哮喘、肺纤维化、结节病和影响肺或影响肺功能的感染(例如病毒、细菌、寄生虫或真菌感染)。在一些实施方式中,这种感染可以是病毒感染(例如病毒性肺炎、病毒性支气管炎、流感、冠状病毒感染、腺病毒感染、合胞病毒感染、鼻病毒感染或其组合)、细菌感染(例如,链球菌感染、葡萄球菌感染、衣原体感染、支原体感染、嗜血杆菌感染、棒状杆菌感染、分枝杆菌感染、军团菌感染或其组合)、真菌感染(例如曲霉感染、隐球菌感染、肺孢子虫感染或其组合)、寄生虫感染(例如疟原虫感染、弓形虫感染、内阿米巴感染、蛔虫感染、血吸虫感染或其组合)或它们的组合。在一些实施方式中,肺部疾病可以是肺炎。
[0045]
本发明还提供了治疗哺乳动物copd的方法。所述方法可以包括向哺乳动物施用包含(a)普氏菌属菌种(例如,组织普氏菌和/或产黑色素普氏菌)和/或(b)普氏菌属菌种(例如,组织普氏菌和/或产黑色素普氏菌)的囊泡的组合物。
[0046]
如本文所用,普氏菌属菌种的“囊泡”可以指由普氏菌属菌种产生的任何膜囊泡。在一些实施方式中,普氏菌属菌种的囊泡可以是外膜囊泡。由革兰氏阴性菌产生的细胞外囊泡通常称为外膜囊泡(omv)。不受任何特定理论的束缚,据信由于整个微生物可以参与其他功能,与完整的活的细菌相比,使用来自普氏菌属菌种的囊泡(例如,omv)可以减少或消除任何潜在的致病作用。
[0047]
在一些实施方式中,施用包含普氏菌属(例如,组织普氏菌)的组合物可以包括施用包含活的普氏菌属(例如,组织普氏菌)、死的(或灭活的)普氏菌属(例如,组织普氏菌)、普氏菌属(例如,组织普氏菌)的组分、或它们的组合的组合物。在一些情况下,施用包含普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的组合物可以包括施用包含活的普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、死的(或被灭活的)普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的组分、或它们的组合的组合物。
[0048]
如本文所用,细菌的“组分”可以是不属于囊泡的细菌的一部分或一块。在一些实
施方式中,细菌的组分可以是细胞壁和/或细胞膜的片段。在一些实施方式中,细菌的组分可以是蛋白质。
[0049]
在一些实施方式中,在施用包含(a)活的和/或灭活的普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)和/或(b)普氏菌属菌种(例如,组织普氏菌和/或产黑色素普氏菌)的囊泡的组合物之前,哺乳动物可以被鉴定为具有一种或多种肺部疾病(例如copd)的症状。肺部病症的症状的例子可以根据病症而变化,但可以包括但不限于呼吸急促、喘息、胸闷和/或疼痛、咳嗽、发烧和声音嘶哑。在某些情况下,哺乳动物可能有吸烟史或接触过香烟烟雾。在一些实施方式中,在施用包含(a)活的和/或灭活的普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)和/或(b)普氏菌属菌种(例如,组织普氏菌和/或产黑色素普氏菌)的囊泡的组合物之前,哺乳动物可以被鉴定或诊断为具有肺部疾病。
[0050]
在一些实施方式中,在施用包含活的和/或灭活的普氏菌属(例如,组织普氏菌)的组合物之前,哺乳动物可以被鉴定为具有一种或多种copd症状。在一些实施方式中,在施用包含活的普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、死的(或灭活的)普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的组分、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的囊泡(例如,omv)、或它们的组合之前,哺乳动物可以被鉴定为具有一种或多种copd症状。
[0051]
copd症状的例子包括但不限于:呼吸急促、喘息、胸闷、慢性咳嗽和发绀。在某些情况下,哺乳动物可能有吸烟史或接触过香烟烟雾。在一些实施方式中,在施用包含活的和/或灭活的普氏菌属(例如,组织普氏菌)的组合物之前,哺乳动物可以被鉴定或诊断为患有copd。在一些实施方式中,在使用包含活的普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、死的(或灭活的)普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的组分、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的囊泡(例如,omv)、或它们的组合之前,哺乳动物可以被鉴定或诊断为患有copd。
[0052]
在一些实施方式中,在施用包含活的和/或灭活的普氏菌属(例如,组织普氏菌)的组合物之前,哺乳动物可以被鉴定或诊断为患有肺气肿。
[0053]
在一些实施方式中,在使用包含活的普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、死的(或灭活的)普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的组分、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的囊泡(例如,omv)、或它们的组合之前,哺乳动物可以被鉴定或诊断为患有肺气肿。在一些实施方式中,患有copd和肺气肿的哺乳动物可以使用一种方法进行治疗,该方法包括向哺乳动物施用包含活的和/或灭活的普氏菌属(例如,组织普氏菌)的组合物。在一些实施方式中,患有copd和肺气肿的哺乳动物可以使用一种方法进行治疗,该方法包括向哺乳动物施用包含活的普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、死的(或灭活的)普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的组分、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的囊泡(例如,omv)、或它们的组合的组合物。
[0054]
在一些实施方式中,普氏菌属可以包括组织普氏菌。在一些实施方式中,普氏菌属可以主要是组织普氏菌。在一些实施方式中,普氏菌属可以几乎都是组织普氏菌。在一些实施方式中,普氏菌属可以全都是组织普氏菌。在一些情况下,如本文所述施用于哺乳动物的
组合物中的大于80%(例如大于85%、90%、95%或99%)的普氏菌属可以是组织普氏菌。
[0055]
在一些实施方式中,普氏菌属可以包括产黑色素普氏菌。在一些实施方式中,普氏菌属可以主要是产黑色素普氏菌。在一些实施方式中,普氏菌属可以几乎都是产黑色素普氏菌。在一些实施方式中,普氏菌属可以全都是产黑色素普氏菌。在一些情况下,如本文所述施用于哺乳动物的组合物中的大于80%(例如大于85%、90%、95%或99%)的普氏菌属可以是产黑色素普氏菌。在一些实施方式中,普氏菌属菌种的囊泡可以包括组织普氏菌的囊泡。在一些实施方式中,普氏菌属菌种的囊泡可以主要是组织普氏菌的囊泡。在一些实施方式中,普氏菌属菌种的囊泡可以几乎都是组织普氏菌的囊泡。在一些实施方式中,普氏菌属菌种的囊泡可以全都是组织普氏菌的囊泡。在一些情况下,如本文所述施用于哺乳动物的组合物中的大于80%(例如大于85%、90%、95%或99%)的普氏菌属的囊泡可以是组织普氏菌的囊泡。
[0056]
在一些实施方式中,普氏菌属菌种的囊泡可以包括产黑色素普氏菌的囊泡。在一些实施方式中,普氏菌属菌种的囊泡可以主要是产黑色素普氏菌的囊泡。在一些实施方式中,普氏菌属菌种的囊泡可以几乎都是产黑色素普氏菌的囊泡。在一些实施方式中,普氏菌属菌种的囊泡可以全都是产黑色素普氏菌的囊泡。在一些情况下,如本文所述施用于哺乳动物的组合物中的大于80%(例如大于85%、90%、95%或99%)的普氏菌属的囊泡可以是产黑色素普氏菌的囊泡。
[0057]
在一些实施方式中,普氏菌属菌种的囊泡可以任何合适的比例(例如,70:30、60:40、50:50、40:60或30:70)包括组织普氏菌的囊泡和产黑色素普氏菌的囊泡。
[0058]
一些普氏菌属细菌是人类微生物组的一部分,但在某些情况下,一些普氏菌属细菌可能是致病性或机会性病原体;例如,参见de steenhuijsen piters等人,“老年肺炎患者的上呼吸道微生物群失调”(dysbiosis of upper respiratory tract microbiota in elderly pneumonia patients),isme j.,10:97
–
108(2016),doi:10.1038/ismej.2015.99。
[0059]
本文提供的方法可以在任何合适的哺乳动物上进行。例如,在一些实施方式中,哺乳动物可以是人。可以如本文所述治疗的患有肺部疾病的哺乳动物的实例包括但不限于:人、猴、马、牛、猪、狗、猫、山羊、绵羊、兔、豚鼠、大鼠和小鼠。可以如本文所述治疗的患有copd和/或肺气肿的哺乳动物的实例包括但不限于:人、猴、马、牛、猪、狗、猫、山羊、绵羊、兔、豚鼠、大鼠和小鼠。
[0060]
可以以任何适当的方式施用含有活的和/或灭活的普氏菌属(例如,组织普氏菌)的组合物。例如,本文提供的包含普氏菌属(例如,组织普氏菌)(例如,活的普氏菌属(例如,组织普氏菌)微生物)的组合物可以如其他地方针对益生菌所描述的那样施用(参见,例如,美国专利申请公开号2008/0241226的第[0049]-[0108]段;和美国专利号8,617,536的第5栏第53行至第8栏第8行,两者均通过引用整体并入本文)。
[0061]
在一些实施方式中,可以口服施用本文所述的含有普氏菌属(例如,组织普氏菌)的组合物。在一些实施方式中,本文所述的含有普氏菌属(例如,组织普氏菌)的组合物可以丸剂、片剂或胶囊剂的形式施用。在一些实施方式中,丸剂、片剂或胶囊可以被配制为将普氏菌属(例如,组织普氏菌)递送至哺乳动物的肠道。
[0062]
在一些情况下,可以将本文所述的含有普氏菌属(例如,组织普氏菌)的组合物施
用于哺乳动物的呼吸系统。在一些实施方式中,可以经鼻施用本文所述的含有普氏菌属(例如,组织普氏菌)的组合物。可以使用任何合适的装置或方法将如本文所述的含有普氏菌属(例如,组织普氏菌)的组合物施用于哺乳动物的呼吸系统。例如,可以使用鼻喷雾剂、吸入剂(例如,定量吸入剂或干粉吸入剂)或雾化剂(例如,喷射雾化剂、超声雾化剂或振动网状雾化剂)将本文所述的含有普氏菌属(例如,组织普氏菌)的组合物施用于哺乳动物的呼吸系统。在一些实施方式中,可以鼻内施用本文所述的含有普氏菌属(例如,组织普氏菌)的组合物。
[0063]
施用包含活的普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、死的(或灭活的)普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的组分、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的囊泡(例如,omv)、或它们的组合的组合物可以以任何合适的方式进行。例如,本文提供的包含活的普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、死的(或灭活的)普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的组分、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的囊泡(例如,omv)、或它们的组合的组合物可以如其他地方针对益生菌所描述的那样施用(参见,例如,美国专利申请公开号2008/0241226的第[0049]-[0108]段;和美国专利号8,617,536的第5栏第53行至第8栏第8行,两者均通过引用整体并入本文)。
[0064]
在一些实施方式中,本文所述的包含活的普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、死的(或灭活的)普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的组分、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的囊泡(例如,omv)、或它们的组合的组合物可以口服施用。在一些实施方式中,本文所述的包含活的普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、死的(或灭活的)普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的组分、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的囊泡(例如,omv)、或它们的组合的组合物可以丸剂、片剂或胶囊剂的形式施用。在一些实施方式中,丸剂、片剂或胶囊可以被配制为将活的普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、死的(或灭活的)普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的组分、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的囊泡(例如,omv)、或它们的组合递送至哺乳动物的肠道。在一些实施方式中,本文所述的包含活的普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、死的(或灭活的)普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的组分、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的囊泡(例如,omv)、或它们的组合的组合物可以经鼻施用。
[0065]
在一些情况下,本文所述的包含活的普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、死的(或灭活的)普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的组分、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的囊泡(例如,omv)、或它们的组合的组合物可以施用于哺乳动物的呼吸系统。在一些实施方式中,本文所述的包含活的普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、死的(或灭活的)普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、普氏菌属(例如,
组织普氏菌和/或产黑色素普氏菌)的组分、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的囊泡(例如,omv)、或它们的组合的组合物可以经鼻施用。本文所述的包含活的普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、死的(或灭活的)普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的组分、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的囊泡(例如,omv)、或它们的组合的组合物可以采用任何合适的装置或方法施用于哺乳动物的呼吸系统。例如,本文所述的包含活的普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、死的(或灭活的)普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的组分、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的囊泡(例如,omv)、或它们的组合的组合物可以使用鼻喷雾剂、吸入剂(例如,定量吸入剂或干粉吸入剂)、或喷雾器(例如,喷射喷雾器、超声波雾化剂或振动网状雾化剂)施用于哺乳动物的呼吸系统。
[0066]
如本文所述,可以使用任何合适的给药方案来治疗肺部疾病。如本文所述,可以使用任何合适的给药方案来治疗copd和/或肺气肿。例如,本文提供的组合物可以一天一次、一天两次、一天三次或一天四次施用,有或没有进食。
[0067]
本文所述的组合物的施用可以进行任何适当的时间段。例如,本文提供的组合物可以施用1周至约10周(例如,约1周至约8周、约1周至约4周、约1周至约2周、约2周约4周、约2周至约8周、约2周至约10周、约4周至约10周、约8周至约10周、约2周至约8周、或约3周至约5周)。作为另一个实例,本文所述的组合物可以施用至少约2周(例如,至少约4周、至少约8周、至少约12周、至少约18周或至少约24周)。在一些情况下,只要哺乳动物还活着,就可以施用本文所述的组合物。
[0068]
在一些情况下,可以监测接受本文所述组合物的哺乳动物以确定组合物对肺功能的影响(例如,确认肺部疾病例如copd的一种或多种症状的减轻)。在施用之前、施用期间(例如,给药之间)或施用停止之后,可以使用任何合适的方法评估肺功能。例如,可以通过测量肺顺应性(cst)、肺容量、气道阻力或弹性来评估肺功能。可以使用任何适当的方法来测量肺功能。在一些情况下,可以在两个时间点之间比较肺功能的测量值(例如,在施用本文所述的组合物之前和施用一周或多周之后;在一个剂量和随后的剂量之间;或在施用之前和施用停止之后)以确定肺功能的测量是否有变化。在本文提供的方法的一些实施方式中,所述方法可以包括在施用本文所述的组合物之前、期间或之后(例如,在施用本文所述的组合物至少1周(例如,至少2、4、8、12、18或24周)之后)测量肺功能的一个或多个参数。在一些实施方式中,与施用本文所述的组合物之前相同的一种或多种肺功能参数相比,在施用本文所述的组合物之后(例如,在施用本文所述的组合物至少1周(例如,至少2、4、8、12、18或24周)之后)一种或多种肺功能参数得到改善。在一些实施方式中,与施用本文所述的组合物之前相比,哺乳动物(例如人)的肺顺应性在施用本文所述的组合物之后(例如,在施用本文所述的组合物至少1周(例如,至少2、4、8、12、18或24周)之后)可降低至少约5%(例如,至少约6%、8%、10%或15%)。在本文提供的方法的一些实施方式中,在施用本文所述的组合物之后,肺部疾病例如copd的严重程度可以降低。例如,在一些实施方式中,在施用本文所述的组合物之后,肺气肿的严重程度可以降低大于25%、大于50%或大于75%。可以通过任何合适的方法确定肺气肿严重程度的降低。例如,肺气肿严重程度的降低可以通过测量肺顺应性来确定。
[0069]
如本文所述,可以使用任何合适的含有普氏菌属(例如,组织普氏菌)的组合物。如本文所述,可以使用任何合适的含有活的普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、死的(或灭活的)普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的组分、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的囊泡(例如,omv)、或它们的组合的组合物。
[0070]
如本文所述可用于治疗copd和/或肺气肿的含有普氏菌属(例如,组织普氏菌)的组合物的实例包括但不限于从美国专利号8,617,536第5栏第53行延伸至第8栏第8行的部分中所描述的那些,该专利通过引用整体并入本文。如本文所述可用于治疗copd和/或肺气肿的含有活的普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、死的(或灭活的)普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的组分、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的囊泡(例如,omv)、或它们的组合的组合物的实例包括但不限于从美国专利号8,617,536第5栏第53行延伸至第8栏第8行的部分中所描述的那些,该专利通过引用整体并入本文。
[0071]
如本文所述可用于治疗肺部疾病的含有普氏菌属(例如,组织普氏菌)的组合物的实例包括但不限于从美国专利号8,617,536从第5栏第53行延伸至第8栏第8行的部分中所描述的那些,该专利通过引用整体并入本文。如本文所述可用于治疗肺部疾病的含有活的普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、死的(或灭活的)普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的组分、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的囊泡(例如,omv)、或它们的组合的组合物的实例包括但不限于从美国专利号8,617,536第5栏第53行延伸至第8栏第8行的部分中所描述的那些,该专利通过引用整体并入本文。
[0072]
简言之,含有普氏菌属的组合物可以包含活的普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、灭活的(也称为死的)普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的组分、裂解的普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的囊泡(例如,omv)、或它们的组合。这样的组合物可以包含任何合适量的普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的组分,或它们的组合。在一些情况下,本文提供的组合物可以包含活的普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、死的(或灭活的)普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的组分、或它们的组合,其中,以干重计,0.001%至100%(例如,1%至95%、10%至95%、25%至95%、50%至95%、20%至80%、50%至95%、60%至95%、70%至95%、80%至95%、90%至95%、95%至99%、50%至100%、60%至100%、70%至100%、80%至100%、90%至100%、或95%至100%)的组合物可以是活的普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、死的(或灭活的)普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的组分、或它们的组合。在一些情况下,本文提供的组合物可包含约10至约10
14
个活的普氏菌属(例如,组织普氏菌)微生物。在一些情况下,本文提供的组合物可以包含任何合适量的普氏菌属菌种(例如,组织普氏菌和/或产黑色素普氏菌)的囊泡。
[0073]
在一些情况下,本文提供的组合物可以包含活的普氏菌属(例如,组织普氏菌)、产
黑色素普氏菌、或其组合(例如,活的普氏菌属(例如,组织普氏菌)、或产黑色素普氏菌、微生物、死的普氏菌属(例如,组织普氏菌)、或产黑色素普氏菌、微生物、或其组合),用量和剂量如其他地方针对益生菌所述的那样(美国专利申请公开号2008/0241226,通过引用整体并入本文;参见,例如,第[0049-0103]段)。在一些情况下,本文提供的组合物可以包含活的普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、死的(或灭活的)普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的组分、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的囊泡(例如,omv)、或它们的组合,用量和剂量如其他地方针对益生菌所述的那样(美国专利申请公开号2008/0241226,通过引用整体并入本文;参见,例如,第[0049-0103]段)。可以使用任何合适的剂量。例如,活的普氏菌属(例如,组织普氏菌)的剂量可以为约1x103至约1x10
14
菌落形成单位(cfu)(例如,约1x103至约1x10
12
、约1x103至约1x10
10
、约1x103至约1x103、约1x103至约1x105、约1x105至约1x10
14
、约106至约109、约107至约108、约1x108至约1x10
14
、约1x10
10
至约1x10
14
、约1x10
12
至约1x10
14
、约1x105至约1x10
12
、或约1x108至约1x10
10
cfu)。在一些情况下,活的普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的剂量可以为约1x103至约1x10
14
cfu(例如,约1x103至约1x10
12
、约1x103至约1x10
10
、约1x103至约1x103、约1x103至约1x105、约1x105至约1x10
14
、约106至约109、约107至约108、约1x108至约1x10
14
、约1x10
10
至约1x10
14
、约1x10
12
至约1x10
14
、约1x105至约1x10
12
、或约1x108至约1x10
10
cfu)。应当理解,死的普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的剂量可以与活的普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的剂量相当,虽然死的普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)不能形成菌落。
[0074]
普氏菌属菌种(例如,组织普氏菌和/或产黑色素普氏菌)的囊泡的剂量可以是任何合适的剂量。例如,普氏菌属菌种的囊泡的剂量可以为约10mg omv lps(脂多糖)至约1000mg omv lps(例如,约10mg omv lps至约50mg omv lps、约10mg omv lps至约100mg omv lps、约10mg omv lps至约500mg omv lps、约50mg omv lps至约1000mg omv lps、约100mg omv lps至约1000mg omv lps、约500mg omv lps至约1000mg omv lps、约50mg omv lps至约500mg omv lps、或约50mg omv lps至约250mg omv lps)。
[0075]
在一些情况下,剂量可以在治疗过程中变化(例如,可以使用一种或多种高负荷剂量,然后使用一种或多种较低的剂量)。应当理解,合适的剂量会受到若干因素的影响,包括待治疗哺乳动物的年龄、体重或症状的严重程度。
[0076]
活的普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)微生物可以从任何合适的哺乳动物(例如,人)的消化系统中获得。例如,普氏菌属(例如,组织普氏菌)微生物可以从人(例如,被诊断患有乳糜泻的人类患者)的小肠粘膜(例如,小肠活检或抽吸样品)中分离。普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)菌种可以通过任何适当的方法来鉴定,例如,通过使用标准16s rrna引物的16s rrna pcr。用于鉴定普氏菌属(例如,组织普氏菌)的16s rrna序列可以如图4所示(例如,seq id no:1和/或seq id no:2)。在某些情况下,可以从ars培养物保藏中心(nrrl登录号nrrl b-50329,2009年10月28日保藏)获得普氏菌属(例如,组织普氏菌)微生物。可以使用任何适当的方法来获得普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)微生物的培养物。例如,可以使用标准微生物培养技术获得普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)或普氏菌属(例如,组织普氏菌和/或产黑
色素普氏菌)的组分。一般而言,普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)微生物可以在含有牛奶(例如,脱脂奶)的肉汤中培养以获得每ml肉汤含有大于1x108个普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的培养物。普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)微生物可以通过离心与肉汤分离。一旦获得,可以将活的普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)微生物配制成药物或营养补充剂组合物以施用于哺乳动物(例如,人),可以添加到食品中用于消耗,或者可以冷冻以备后用。在一些情况下,可以对获得的普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)微生物进行处理(例如,化学处理、重复冻融循环、抗生素处理、固定处理如福尔马林处理、辐射、热灭活和/或冻干)以获得死的或裂解的普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)微生物的组合物,或者可以被加工(例如,裂解然后分级分离)以获得普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)组分的组合物。
[0077]
在某些情况下,可以将可在2x脱脂牛奶中冷冻储存的普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)制剂解冻并在配备有anaeropack system(产品编号10-01,纽约州纽约的三菱瓦斯化学株式会社(mitsubishi gas chemical america,inc.))的厌氧罐中在含有卡那霉素和万古霉素(kv)的cdc厌氧湖羊血琼脂上生长(美国马里兰州sparks的bd公司(becton,dickson and company,sparks),产品编号221846)。培养物可以在35-37℃下培养至少48小时。
[0078]
可以通过任何合适的方法获得普氏菌属菌种(例如,组织普氏菌和/或产黑色素普氏菌)的囊泡(例如,omv)。例如,在一些情况下,普氏菌属菌种(例如,组织普氏菌和/或产黑色素普氏菌)的囊泡可以通过以下过程获得:过滤(例如,去除细菌)普氏菌属菌种的培养物上清液(例如,由较低力离心,例如10k x g),通过离心分离囊泡(例如,使用较高力离心,例如400k x g),和任选地洗涤囊泡。
[0079]
在一些情况下,含有普氏菌属(例如,组织普氏菌)或普氏菌属(例如,组织普氏菌)组分的组合物可以是口服药物或营养补充剂的形式。例如,含有普氏菌属(例如,组织普氏菌)或普氏菌属(例如,组织普氏菌)组分的组合物可以是丸剂、片剂、粉末、液体或胶囊的形式。片剂或胶囊剂可以通过任何合适的方法与药学上可接受的赋形剂例如粘合剂、填充剂、润滑剂、崩解剂或润湿剂一起制备。片剂可以通过本领域已知的方法进行包衣。在一些情况下,包含活的普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、死的(或灭活的)普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的组分、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的囊泡(例如,omv)、或它们的组合的组合物可以是口服药物或营养补充剂的形式。例如,包含活的普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、死的(或灭活的)普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的组分、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的囊泡(例如,omv)、或它们的组合的组合物可以是丸剂、片剂、粉末、液体或胶囊剂的形式。
[0080]
在一些情况下,可以配制含有普氏菌属(例如,组织普氏菌)或普氏菌属(例如,组织普氏菌)组分的组合物,以使活的或死的普氏菌属(例如,组织普氏菌)或普氏菌属(例如,组织普氏菌)组分经包封用于在哺乳动物的肠内释放。在一些情况下,可以配制含有活的普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、死的(或灭活的)普氏菌属(例如,组织普
氏菌和/或产黑色素普氏菌)、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的组分、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的囊泡(例如,omv)、或它们的组合的组合物,使得活的普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、死的(或灭活的)普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的组分、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的囊泡(例如,omv)、或它们的组合经包封以在哺乳动物的肠内释放。
[0081]
用于口服施用的液体制剂可以采取例如溶液、糖浆或悬浮液的形式,或者它们可以作为干燥产品存在,用于在使用之前用盐水或其他合适的液体载剂构建。在一些情况下,本文提供的含有普氏菌属(例如,组织普氏菌)(例如,活的普氏菌属(例如,组织普氏菌)微生物、死的普氏菌属(例如,组织普氏菌)微生物、或其组合)的组合物可以是其他地方描述的剂型(美国专利申请公开号2008/0241226;参见例如第[0129-0135]段)。例如,本文提供的组合物可以是配制为含有普氏菌属(例如,组织普氏菌)(例如,活的普氏菌属(例如,组织普氏菌)微生物)或普氏菌属(例如,组织普氏菌)的组分的食品形式。在一些情况下,本文提供的包含活的普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、死的(或灭活的)普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的组分、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的囊泡(例如,omv)、或它们的组合的组合物可以是如其他地方所述的剂型(美国专利申请公开号2008/0241226;参见,例如,第[0129-0135]段)。例如,本文所述的组合物可以是配制成包含活的普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、死的(或灭活的)普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的组分、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的囊泡(例如,omv)、或它们的组合的食品形式。此类食品的实例包括但不限于:牛奶(例如酸化牛奶)、酸奶、奶粉、茶、果汁、饮料、糖果、巧克力、咀嚼棒、饼干、威化饼、薄脆饼干、谷类食品、零食及其组合。
[0082]
在一些情况下,含有普氏菌属(例如,组织普氏菌)或普氏菌属(例如,组织普氏菌)的组分的组合物在一些情况下可以是施用于呼吸系统的药物形式,例如,用于经鼻施用或用于肺部施用。在一些情况下,含有普氏菌属(例如,组织普氏菌)或普氏菌属(例如,组织普氏菌)的组分的组合物可以是鼻喷雾剂、吸入剂(例如计量吸入剂或干粉吸入剂)、或用于雾化的制剂(例如,用于喷射雾化剂、超声雾化剂或振动网状雾化剂)的形式。在一些情况下,含有活的普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、死的(或灭活的)普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的组分、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的囊泡(例如,omv)、或它们的组合的组合物在一些情况下可以是施用于呼吸系统的药物形式,例如,用于经鼻施用或用于肺部施用。在一些情况下,含有活的普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、死的(或灭活的)普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的组分、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的囊泡(例如,omv)、或它们的组合的组合物可以是鼻喷雾剂、吸入剂(例如计量吸入剂或干粉吸入剂)、或用于雾化的制剂(例如,用于喷射雾化剂、超声雾化剂或振动网状雾化剂)的形式。这些制剂可以通过任何合适的方法使用药学上可接受的赋形剂形成。在一些此类制剂中,普氏菌属(例如,组织普氏菌)或普氏菌属(例如,组织普氏菌)的组分可以任何合
适的剂量存在。在一些这样的制剂中,活的普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、死的(或灭活的)普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的组分、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的囊泡(例如,omv)、或它们的组合可以任何合适的剂量存在。
[0083]
含有普氏菌属(例如,组织普氏菌)或普氏菌属(例如,组织普氏菌)的组分的组合物可以包含其他成分,例如缓冲剂、自由基清除剂、抗氧化剂、还原剂或它们的混合物。例如,可以将含有活的普氏菌属(例如,组织普氏菌)的组合物配制成含有植物素(botanicals)、维生素、矿物质或它们的组合。在一些情况下,本文提供的含有普氏菌属(例如,组织普氏菌)(例如,活的普氏菌属(例如,组织普氏菌)微生物、死的普氏菌属(例如,组织普氏菌)微生物、或其组合)的组合物可以含有如其他地方描述的成分(美国专利申请公开号2008/0241226;参见例如第[0104-0128]段)。
[0084]
包含活的普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、死的(或灭活的)普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的组分、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的囊泡(例如,omv)、或它们的组合的组合物可以包含其他成分,例如缓冲剂、自由基清除剂、抗氧化剂、还原剂或其混合物。例如,包含活的普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、死的(或灭活的)普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的组分、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的囊泡(例如,omv)、或它们的组合的组合物可以配制成含有植物素、维生素、矿物质或其组合。在一些实施方式中,包含活的普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、死的(或灭活的)普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的组分、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的囊泡(例如,omv)、或它们的组合的组合物可以包含如其他地方所述的其他成分(美国专利申请公开第2008/0241226号;参见例如第[0104-0128]段)。
[0085]
在一些情况下,含有普氏菌属(例如,组织普氏菌)或普氏菌属(例如,组织普氏菌)的组分的组合物可以包含施用于哺乳动物的药学上可接受的载体,包括但不限于无菌水性溶液或非水性溶液、悬浮液和乳液。在一些情况下,包含活的普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、死的(或灭活的)普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的组分、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的囊泡(例如,omv)、或它们的组合的组合物可以包含施用于哺乳动物的药学上可接受的载体,包括不限于无菌水性或非水性溶液、悬浮液和乳液。非水性溶剂的实例包括但不限于:丙二醇、聚乙二醇、植物油和有机酯。水性载体包括但不限于:水、醇、盐水和缓冲溶液。药学上可接受的载体还可以包括生理学上可接受的水性载剂(例如生理盐水)或其他已知的用于口服施用的载体。
[0086]
本发明还提供了使用组合物的方法和材料,该组合物含有活的普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、死的(或灭活的)普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的组分、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的囊泡(例如,omv)、或它们的组合作为治疗肺部疾病的药物。在一些情况下,包含活的普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、死的
(或灭活的)普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的组分、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的囊泡(例如,omv)、或它们的组合的组合物可以用作营养补充剂,以用能够降低肺部疾病严重程度或减缓其发展的细菌有机体来补充哺乳动物的膳食。可以如本文所述进行治疗的哺乳动物的实例包括但不限于人、猴、狗、猫、牛、马、猪和羊。
[0087]
本发明还提供了使用包含普氏菌属(例如,组织普氏菌)或普氏菌属(例如,组织普氏菌)的组分的组合物作为copd药物的方法和材料。在一些情况下,含有普氏菌属(例如,组织普氏菌)或普氏菌属(例如,组织普氏菌)的组分的组合物可以用作营养补充剂,以用能够降低copd严重程度或减缓其发展的细菌有机体来补充哺乳动物的膳食。可以如本文所述进行治疗的哺乳动物的实例包括但不限于人、猴、狗、猫、牛、马、猪和羊。
[0088]
本发明还提供了使用组合物的方法和材料,该组合物含有活的普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、死的(或灭活的)普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的组分、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的囊泡(例如,omv)、或它们的组合作为治疗copd的药物。在一些情况下,包含活的普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、死的(或灭活的)普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的组分、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的囊泡(例如,omv)、或它们的组合的组合物可以用作营养补充剂,以用能够降低copd严重程度或减缓其发展的细菌有机体来补充哺乳动物的膳食。可以如本文所述进行治疗的哺乳动物的实例包括但不限于人、猴、狗、猫、牛、马、猪和羊。
[0089]
可以将任何量的含有普氏菌属(例如,组织普氏菌)或普氏菌属(例如,组织普氏菌)的组分的组合物施用于哺乳动物。普氏菌属(例如,组织普氏菌)(例如,活的或死的普氏菌属(例如,组织普氏菌))或普氏菌属(例如,组织普氏菌)的组分的剂量可以取决于许多因素,包括所需的结果。通常,单剂量中包含的普氏菌属(例如,组织普氏菌)(例如,活的或死的普氏菌属(例如,组织普氏菌))或普氏菌属(例如,组织普氏菌)的组分的量可以是在哺乳动物体内有效表现出抗炎活性的量。例如,可以将含有活的普氏菌属(例如,组织普氏菌)的组合物配制成一定剂量,使得哺乳动物接受约10至10
14
个活的普氏菌属(例如,组织普氏菌)微生物。
[0090]
任何量的含有活的普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、死的(或灭活的)普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的组分、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的囊泡(例如,omv)、或它们的组合的组合物可以施用于哺乳动物。活的普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、死的(或灭活的)普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的组分、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的囊泡(例如,omv)、或它们的组合的剂量可以取决于许多因素,包括所需的结果。通常,单剂量中包含的活的普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、死的(或灭活的)普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的组分、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的囊泡(例如,omv)、或它们的组合的量可以是在哺乳动物体内有效表现出抗
炎活性的量。例如,可以将含有活的普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的组合物配制成一定剂量,使得哺乳动物接受约10至10
14
个活的普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)微生物。
[0091]
含有普氏菌属(例如,组织普氏菌)(例如,活的或死的普氏菌属(例如,组织普氏菌))或普氏菌属(例如,组织普氏菌)的组分的组合物的最终ph可以在约3.5和约9.5之间(例如,约4.0至约9.0;约4.5至约9.0;约4.5至约8.5;约5.0至约8.5;或约6.5至约8.0)。含有活的普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、死的(或灭活的)普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的组分、普氏菌属(例如,组织普氏菌和/或产黑色素普氏菌)的囊泡(例如,omv)、或它们的组合的组合物的ph可以在约3.5和约9.5之间(例如在约4.0至约9.0;约4.5至约9.0;约4.5至约8.5;约5.0至约8.5;或约6.5至约8.0)。为了获得这样的ph,例如可以使用ph调节剂来调节组合物的ph。应当理解,如果组合物具有太高的ph(例如,在调节前大于10.0),可以用多种酸中的任一种来完成ph调节。同样,如果组合物的ph值过低(例如,在调节前低于3.0),可以使用多种碱中的任何一种来完成ph调节。
[0092]
在某些情况下,cs诱导的肺气肿的非人动物模型可以阐明机制;然而,关于肺微生物组的作用的信息有限。非人动物模型可能需要4-6个月暴露于cs,这是一项艰巨的任务(参见例如wright,jl.和a.churg.,expert rev respir med 4:723-734,2010),并且有时动物模型中的免疫反应不能重现人类效应反应。
[0093]
本发明还提供了copd的非人动物模型。这种非人动物模型可以是任何合适的动物物种。在一些实施方式中,非人动物模型可以是非人哺乳动物。可用于制作本文所述模型的非人动物的实例包括但不限于:啮齿动物、兔子、狗、猫、牛、猪、绵羊、山羊和非人灵长类动物。例如,在一些情况下,非人动物可以是啮齿动物(例如,小鼠、大鼠或豚鼠)。在另一个例子中,非人动物可以是兔子。在又一个例子中,非人动物可以是非人灵长类动物。
[0094]
copd的非人动物模型可以被基因工程改造以改变非人动物基因组的一个或多个方面,例如,复制人类效应反应(参见例如,taneja,v.和cs david.,immunological reviews 233:62-78.(2010))。在某些情况下,可以设计非人动物模型以表达一种或多种人类白细胞抗原(hla)(例如血清型dq8)。在一些情况下,本文所述的非人动物模型可以设计为缺乏表达功能性内源性主要组织相容性复合物(mhc)ii类分子的能力。在一些情况下,本文所述的非人动物可被设计为缺乏表达内源性功能性白细胞介素17(il-17)多肽的能力。例如,本文所述的copd非人动物模型可以设计为(a)表达一种或多种人hla(例如,dq8),(b)缺乏表达功能性内源性ii类mhc分子的能力,和(c)缺乏表达功能性内源性il-17多肽的能力。如本文所用,本文提供的表达dq8且缺乏内源性mhc ii类分子的copd非人动物模型可记为“aeo.dq8”或“dq8”;本文提供的缺乏功能性il-17的copd非人动物模型可记为“il-17-/
‑”;以及表达dq8、缺乏功能性内源性mhc ii类分子表达、并且缺乏功能性内源性il-17表达的copd非人动物模型可记为“dq8.il-17-/
‑”。
[0095]
在一些实施方式中,本文提供的copd的非人动物模型可以是暴露于香烟烟雾(cs)一段时间的动物,例如小于约6周的时间(例如,小于约5周,小于约4周)。在一些实施方式中,本文提供的copd的非人动物模型可以是暴露于香烟烟雾(cs)约3至约6周的动物(例如,约3至约5周、约3至约4周、约4至约5周、约4至约6周、或约5至约6周、约4周、或约5周)。在一
些实施方式中,本文提供的copd的非人动物模型可以表现出肺功能的丧失(例如,与暴露于空气而不是香烟烟雾的类似动物(例如,具有相同基因型)相比)。肺功能丧失可以基于任何合适的测量来确定,例如肺顺应性(cst)、肺容量、气道阻力和弹性,如通过任何合适的方法确定的那样。在一些实施方式中,本文提供的暴露于cs的copd非人动物模型(例如,dq8.il-17-/-小鼠)与暴露于空气而不是cs的类似非人动物相比可以具有改变的一种或多种基因的表达水平(参见例如barnes,j.allergy clin.immunol.,138:16-27(2016))。在一些实施方式中,与暴露于空气而不是cs的类似非人动物相比,本文提供的暴露于cs的copd非人动物模型(例如,dq8.il-17-/-小鼠)可以具有cxc基序趋化因子受体3(cxcr3)、cxc基序趋化因子配体10(cxcl10)或两者的表达增加(例如,通过mrna水平测量)。在一些实施方式中,与暴露于空气而不是cs的类似非人动物相比,本文提供的暴露于cs的肺气肿非人动物模型(例如,dq8.il-17-/-小鼠)可具有纤维化相关基因,例如胶原蛋白a1(coll a1)、纤连蛋白(fib)和转化生长因子β(tgfβ)的表达降低(例如,使用任何合适的方法通过mrna水平测量)。
[0096]
当暴露于cs约3周至约6周(例如,约3至约5周、约3至约4周、约4至约5周、约4至约6周、或约5至约6周、约4周、或约5周)时,与暴露于空气的比较动物(例如,空气暴露的aeo.dq8小鼠)相比,表达人hla-dq8并且缺乏内源性ii类分子表达的非人动物(例如,小鼠)(例如,aeo.dq8小鼠)可发展为轻度至中度肺功能丧失,copd的一个病理特征,而当暴露于cs约3周至约6周(例如,约3至约5周、约3至约4周、约4至约5周、约4至约6周、或约5至约6周、约4周、或约5周)时,与暴露于空气的比较动物(例如,空气暴露的dq8.il-17-/-小鼠)相比,表达人hla-dq8、缺乏内源性ii类分子表达并且缺乏内源性il-17多肽表达的非人动物(例如,小鼠)(例如,dq8.il-17-/-小鼠)会发展为更明显的肺功能丧失。在某些情况下,当暴露于cs约3周至约6周(例如,约3至约5周、约3至约4周、约4至约5周、约4至约6周、或约5至约6周、约4周、或约5周)时,与表达内源性il-17的类似小鼠(例如,暴露于cs的aeo.dq8小鼠)相比,表达人hla-dq8、缺乏内源性ii类分子表达并且缺乏内源性il-17多肽表达的非人动物(例如,小鼠)(例如,dq8.il-17-/-小鼠)会发展为更明显的肺功能丧失。
[0097]
本文件还提供了用于产生copd的非人动物模型的方法。为了形成本文所述的非人动物模型,可以对非人动物进行遗传修饰以缺乏内源性mhc ii类分子。在一些情况下,可以进一步对非人动物进行工程改造以表达一种或多种人白细胞抗原(hla)。在一些情况下,非人动物可以被工程改造以表达hla血清型dq8,如其他地方所述(参见,例如,vassallo,r.等人,clin immunol 152:25-35,2014,也参见美国专利号5,965,787,例如,第10栏,第25-44行,其全部内容以引用的方式并入本文)。可以使用任何适当的遗传修饰技术。例如,可以使用转基因技术,使得非人动物的所有体细胞都表达人dq8(参见,例如,vassallo,r.等人clin immunol 152:25-35,2014)。此外,可以使用任何适当的技术敲除另外的基因。例如,可以使用任何合适的方法使编码il-17多肽的核酸失去功能(例如,“敲除”或突变)。例如,可以使用设计用于破坏内源核酸序列的敲除构建体。破坏可以位于内源核酸序列中的任何适当位点。破坏的实例包括但不限于内源序列中的缺失和异源核酸序列插入内源序列中。插入的例子可以包括但不限于与终止密码子偶联的人工剪接受体或与诸如gfp之类的融合配偶体偶联的剪接供体。敲除构建体可以包含与内源核酸序列或与内源核酸序列相邻的序列同源的序列。在一些情况下,敲除构建体可以包含可操作地连接至调节序列(例如,启动子)的编码选择标记(例如,抗生素抗性、荧光报告基因(例如,gfp或yfp)、或酶(例如,β-半
乳糖苷酶))的核酸序列。敲除构建体可以包括其他核酸序列,例如重组序列(例如,loxp序列)、剪接受体序列、剪接供体序列、转录起始序列和转录终止序列。内源核酸序列的破坏可导致基因表达降低或编码多肽的非功能性截短或融合。
[0098]
在一些实施方式中,产生copd的非人动物模型的方法可以包括提供aeo.dq8非人动物(例如,aeo.dq8小鼠)并使非人动物经受香烟烟雾约3周至约6周(例如,约3至约5周、约3至约4周、约4至约5周、约4至约6周、或约5至约6周、约4周或约5周)。在一些实施方式中,产生copd的非人动物模型的方法可以包括提供dq8.il-17-/-非人动物(例如,dq8.il-17-/-小鼠)并且使非人动物模型(例如,dq8.il-17-/-小鼠)经受香烟烟雾约3周至约6周(例如,约3至约5周、约3至约4周、约4至约5周、约4至约6周、或约5至约6周、约4周或约5周)。使动物经受香烟烟雾约3周至约6周(例如,约3至约5周、约3至约4周、约4至约5周、约4至约6周、或约5至约6周、约4周或约5周)可以通过任何合适的方法实现。在一些实施方式中,使动物经受香烟烟雾约3周至约6周可包括将小鼠暴露于香烟烟雾中,大约每10分钟约2支香烟,每天持续约3小时,每周约5天。在一些实施方式中,使动物经受香烟烟雾约3周至约6周可包括充分暴露于香烟烟雾以导致在暴露期结束时血液烟碱水平为约45至约185ng/ml(例如,约50至约185ng/ml,约100至约185ng/ml,约150至约185ng/ml,约45至约75ng/ml,约45至约100ng/ml,约45至约150ng/ml,约50约150ng/ml,或约75至约125ng/ml)。
[0099]
在一些实施方式中,产生copd的非人动物模型的方法可以包括提供aeo.dq8非人动物(例如,aeo.dq8小鼠)并使该非人动物经受香烟烟雾小于约6周(例如,小于约5周,小于约4周)。在一些实施方式中,产生copd的非人动物模型的方法可以包括提供dq8.il-17-/-非人动物(例如,dq8.il-17-/-小鼠)并使该非人动物模型(例如,dq8.il-17-/-小鼠)经受香烟烟雾小于约6周(例如小于约5周,小于约4周)。使动物经受香烟烟雾小于约6周(例如小于约5周、小于约4周)可以通过任何合适的方法实现。在一些实施方式中,使动物经受香烟烟雾小于约6周可包括使小鼠暴露于香烟烟雾中,大约每10分钟约2支香烟,每天持续约3小时,每周约5天。在一些实施方式中,使动物经受香烟烟雾小于约6周可包括充分暴露于香烟烟雾以导致在暴露期结束时血液烟碱水平为约45至约185ng/ml(例如,约50至约185ng/ml,约100至约185ng/ml、约150至约185ng/ml、约45至约75ng/ml、约45至约100ng/ml、约45至约150ng/ml、约50至约150ng/ml,或约75至约125ng/ml)。
[0100]
本发明将在以下实施例中进一步描述,其不限制权利要求中描述的本发明的范围。
[0101]
示例性实施方式
[0102]
实施方式1是治疗哺乳动物慢性阻塞性肺病(copd)的方法,其中所述方法包括向哺乳动物施用包含活的或灭活的普氏菌属(prevotella)的组合物。
[0103]
实施方式2是实施方式1所述的方法,其中所述组合物包含活的普氏菌属。
[0104]
实施方式3是实施方式1所述的方法,其中所述组合物包含灭活的普氏菌属和无活性的普氏菌属。
[0105]
实施方式4是实施方式1-3中任一项所述的方法,其中所述哺乳动物是人。
[0106]
实施方式5是实施方式1-3中任一项所述的方法,其中所述哺乳动物是啮齿动物。
[0107]
实施方式6是实施方式1-5中任一项所述的方法,其中所述施用包括口服施用。
[0108]
实施方式7是实施方式1-6中任一项所述的方法,其中所述组合物是丸剂、片剂或
胶囊。
[0109]
实施方式8是实施方式1-7中任一项所述的方法,其中所述组合物是被配制为将普氏菌属递送至哺乳动物的肠道的丸剂、片剂或胶囊。
[0110]
实施方式9是实施方式1-5中任一项所述的方法,其中所述施用包括施用至呼吸系统。
[0111]
实施方式10是实施方式1-5或9中任一项所述的方法,其中所述组合物使用鼻喷雾剂、吸入剂或喷雾剂施用。
[0112]
实施方式11是实施方式1-10中任一项所述的方法,其中所述copd的症状的严重程度在施用后降低。
[0113]
实施方式12是实施方式11所述的方法,其中所述copd的症状的严重程度在施用后降低大于约25%。
[0114]
实施方式13是实施方式11所述的方法,其中所述copd的症状的严重程度在施用后降低大于约50%。
[0115]
实施方式14是实施方式11所述的方法,其中所述copd的症状的严重程度在施用后降低大于约75%。
[0116]
实施方式15是实施方式11-14中任一项所述的方法,其中所述哺乳动物的肺顺应性在所述施用步骤之后降低。
[0117]
实施方式16是实施方式15所述的方法,其中与施用前相比,施用后肺顺应性降低至少约5%。
[0118]
实施方式17是实施方式15所述的方法,其中与施用前相比,施用后肺顺应性降低至少约10%。
[0119]
实施方式18是实施方式15所述的方法,其中与施用前相比,施用后肺顺应性降低至少约15%。
[0120]
实施方式19是实施方式1-18中任一项所述的方法,所述方法还包括在施用前测量一种或多种肺功能参数,并在施用后测量相同的一种或多种肺功能参数。
[0121]
实施方式20是实施方式19所述的方法,其中在施用后测量的一种或多种肺功能参数中的至少一种与施用前相比得到改善。
[0122]
实施方式21是实施方式19-20中任一项所述的方法,其中所述一种或多种肺功能参数包括肺顺应性、肺容量、气道阻力、弹性或其组合。
[0123]
实施方式22是实施方式1-21中任一项所述的方法,其中所述方法包括在所述施用步骤之前鉴定所述哺乳动物患有copd。
[0124]
实施方式23是实施方式1-22中任一项所述的方法,其中所述方法包括在所述施用步骤之前鉴定所述哺乳动物患有肺气肿。
[0125]
实施方式24是实施方式1-23中任一项所述的方法,其中普氏菌属的代表性细胞以nrrl登录号b-50329保藏。
[0126]
实施方式25是实施方式1-24中任一项所述的方法,其中所述组合物包含约1
×
103至约1
×
10
14
cfu的普氏菌属。
[0127]
实施方式26是实施方式1-24中任一项所述的方法,其中所述组合物包含约1
×
105至约1
×
10
12
cfu的普氏菌属。
[0128]
实施方式27是实施方式1-24中任一项所述的方法,其中所述组合物包含约1
×
108至约1
×
10
10
cfu的普氏菌属。
[0129]
实施方式28是实施方式1-27中任一项所述的方法,其中所述组合物每天施用一次。
[0130]
实施方式29是实施方式1-27中任一项所述的方法,其中所述组合物每天施用两次。
[0131]
实施方式30是实施方式1-27中任一项所述的方法,其中所述组合物每天施用三次。
[0132]
实施方式31是实施方式1-30中任一项所述的方法,其中所述组合物被施用至少约4周的持续时间。
[0133]
实施方式32是实施方式1-30中任一项所述的方法,其中所述组合物被施用至少约8周的持续时间。
[0134]
实施方式33是实施方式1-32中任一项所述的方法,其中所述普氏菌属包括组织普氏菌。
[0135]
实施方式34是慢性阻塞性肺病(copd)的非人哺乳动物模型,其中所述非人哺乳动物模型的体细胞包含编码一种或多种人hla血清型的核酸,并且其中所述非人哺乳动物模型的体细胞缺乏内源性mhc ii类分子和内源性il-17多肽的表达,并且其中当暴露于香烟烟雾约2至约6周时,与未暴露于香烟烟雾的对照模型相比,该模型的肺功能下降。
[0136]
实施方式35是实施方式34所述的非人哺乳动物模型,其中人hla血清型是dq8。
[0137]
实施方式36是实施方式34或35所述的非人哺乳动物模型,其中所述模型是il-17-/-敲除的哺乳动物。
[0138]
实施方案37是实施方案34-36中任一项所述的非人哺乳动物模型,其中所述哺乳动物是啮齿动物。
[0139]
实施方案38是实施方案34-37中任一项所述的非人哺乳动物模型,其中所述哺乳动物是小鼠。
[0140]
实施方式39是实施方式34-38中任一项所述的非人哺乳动物模型,其中所述哺乳动物具有约45至约185ng/ml的血液烟碱水平。
[0141]
实施方式40是实施方式34-39中任一项所述的非人哺乳动物模型,其中所述哺乳动物具有约50至约150ng/ml的血液烟碱水平。
[0142]
实施方式41是实施方式34-40中任一项所述的非人哺乳动物模型,其中与不是copd的非人动物模型的比较哺乳动物相比,所述哺乳动物的cxcr3、cxcl10或两者的表达水平增加。
[0143]
实施方式42是实施方式34-41中任一项所述的非人哺乳动物模型,其中与不是copd的非人动物模型的比较哺乳动物相比,所述哺乳动物的一种或多种纤维化相关基因的表达水平降低。
[0144]
实施方式43是实施方式42所述的非人哺乳动物模型,其中纤维化相关基因中的至少一种选自胶原a1、纤连蛋白和转化生长因子β。
[0145]
实施方式44是实施方式34-43中任一项所述的非人哺乳动物模型,其中所述肺功能降低是使用一种或多种肺功能参数测量的。
[0146]
实施方式45是实施方式44所述的非人哺乳动物模型,其中所述一种或多种肺功能参数包括肺顺应性、肺容量、气道阻力、弹性或其组合。
[0147]
实施方式46是一种产生慢性阻塞性肺病(copd)的非人哺乳动物模型的方法,所述方法包括:
[0148]
提供非人哺乳动物,其中所述非人哺乳动物的体细胞包含编码一种或多种人hla血清型的核酸,并且其中所述非人哺乳动物模型的体细胞缺乏内源性mhc ii类分子和内源性il-17多肽的表达;和
[0149]
使哺乳动物暴露于香烟烟雾中约3至约6周,
[0150]
从而产生copd的非人动物模型。
[0151]
实施方式47是实施方式46所述的方法,其中人hla血清型是dq8。
[0152]
实施方式48是实施方式46或实施方式47所述的方法,其中所述哺乳动物是il-17-/-。
[0153]
实施方案49是实施方案46-48中任一项所述的方法,其中所述哺乳动物是啮齿动物。
[0154]
实施方案50是实施方案46-49中任一项所述的方法,其中所述哺乳动物是小鼠。
[0155]
实施方式51是实施方式46-50中任一项所述的方法,其中所述暴露包括将哺乳动物暴露于约2支香烟约10分钟,每天约3小时,每周约5天。
[0156]
实施方式52是实施方式46-51中任一项所述的方法,其中所述暴露包括充分暴露于香烟烟雾以导致约45至约185ng/ml的血液烟碱水平。
[0157]
实施方式53是实施方式46-51中任一项所述的方法,其中所述暴露包括充分暴露于香烟烟雾以导致约50至约150ng/ml的血液烟碱水平。
[0158]
实施方式54是实施方式46-53中任一项所述的方法,其中在暴露之后,与暴露于空气而不是香烟烟雾的类似哺乳动物相比,哺乳动物的cxcr3、cxcl10或两者的表达水平增加。
[0159]
实施方式55是实施方式46-54中任一项所述的方法,其中在暴露之后,与暴露于空气而不是香烟烟雾的类似哺乳动物相比,哺乳动物的一种或多种纤维化相关基因的表达水平降低。
[0160]
实施方式56是实施方式55所述的方法,其中纤维化相关基因中的至少一种选自胶原a1、纤连蛋白和转化生长因子β。
[0161]
实施方式57是实施方式46-55中任一项所述的方法,其中在暴露之后,与暴露于空气而不是香烟烟雾的类似哺乳动物相比,哺乳动物的肺功能降低。
[0162]
实施方式58是实施方式57所述的方法,其中所述肺功能降低是使用一种或多种肺功能参数测量的。
[0163]
实施方式59是实施方式58所述的方法,其中所述一种或多种肺功能参数包括肺顺应性、肺容量、气道阻力、弹性或其组合。
[0164]
实施方式60是通过实施方式46-59中任一项所述的方法产生的copd的非人哺乳动物模型。
[0165]
实施方案61是治疗哺乳动物肺部疾病的方法,其中所述方法包括向哺乳动物施用包含活的或灭活的普氏菌属(prevotella)的组合物。
[0166]
实施方案62是实施方案61的方法,其中所述组合物包含活的普氏菌属。
[0167]
实施方案63是实施方案61的方法,其中所述组合物包含灭活的普氏菌属和无活性的普氏菌属。
[0168]
实施方案64是实施方案61-63中任一项所述的方法,其中所述哺乳动物是人。
[0169]
实施方案65是实施方案61-63中任一项所述的方法,其中所述哺乳动物是啮齿动物。
[0170]
实施方式66是实施方式61-65中任一项所述的方法,其中所述施用包括口服施用。
[0171]
实施方式67是实施方式61-66中任一项所述的方法,其中所述组合物是丸剂、片剂或胶囊。
[0172]
实施方式68是实施方式61-67中任一项所述的方法,其中所述组合物是被配制为将普氏菌属递送至哺乳动物的肠道的丸剂、片剂或胶囊。
[0173]
实施方式69是实施方式61-65中任一项所述的方法,其中所述施用包括施用至呼吸系统。
[0174]
实施方式70是实施方式61-65或69中任一项所述的方法,其中所述组合物使用鼻喷雾剂、吸入剂或喷雾剂施用。
[0175]
实施方式71是实施方式61-70中任一项所述的方法,其中所述肺部疾病的症状的严重程度在施用后降低。
[0176]
实施方式72是实施方式71所述的方法,其中所述肺部疾病的症状的严重程度在施用后降低大于约25%。
[0177]
实施方式73是实施方式71所述的方法,其中所述肺部疾病的症状的严重程度在施用后降低大于约50%。
[0178]
实施方式74是实施方式71所述的方法,其中所述肺部疾病的症状的严重程度在施用后降低大于约75%。
[0179]
实施方式75是实施方式71-74中任一项所述的方法,其中所述哺乳动物的肺顺应性在所述施用步骤之后降低。
[0180]
实施方式76是实施方式75所述的方法,其中与施用前相比,施用后肺顺应性降低至少约5%。
[0181]
实施方式77是实施方式75所述的方法,其中与施用前相比,施用后肺顺应性降低至少约10%。
[0182]
实施方式78是实施方式75所述的方法,其中与施用前相比,施用后肺顺应性降低至少约15%。
[0183]
实施方式79是实施方式61-78中任一项所述的方法,所述方法还包括在施用前测量一种或多种肺功能参数,并在施用后测量相同的一种或多种肺功能参数。
[0184]
实施方式80是实施方式79所述的方法,其中在施用后测量的一种或多种肺功能参数中的至少一种与施用前相比得到改善。
[0185]
实施方式81是实施方式79-80中任一项所述的方法,其中所述一种或多种肺功能参数包括肺顺应性、肺容量、气道阻力、弹性或其组合。
[0186]
实施方式82是实施方式61-81中任一项所述的方法,其中所述方法包括在所述施用步骤之前鉴定所述哺乳动物患有肺部疾病。
[0187]
实施方式83是实施方式61-82中任一项所述的方法,其中所述方法包括在所述施用步骤之前鉴定所述哺乳动物患有肺炎。
[0188]
实施方式84是实施方式61-83中任一项所述的方法,其中普氏菌属的代表性细胞以nrrl登录号b-50329保藏。
[0189]
实施方式85是实施方式61-84中任一项所述的方法,其中所述组合物包含约1
×
103至约1
×
10
14
cfu的普氏菌属。
[0190]
实施方式86是实施方式61-84中任一项所述的方法,其中所述组合物包含约1
×
105至约1
×
10
12
cfu的普氏菌属。
[0191]
实施方式87是实施方式61-84中任一项所述的方法,其中所述组合物包含约1
×
108至约1
×
10
10
cfu的普氏菌属。
[0192]
实施方式88是实施方式61-87中任一项所述的方法,其中所述组合物每天施用一次。
[0193]
实施方式89是实施方式61-87中任一项所述的方法,其中所述组合物每天施用两次。
[0194]
实施方式90是实施方式61-87中任一项所述的方法,其中所述组合物每天施用三次。
[0195]
实施方式91是实施方式61-90中任一项所述的方法,其中所述组合物被施用至少约4周的持续时间。
[0196]
实施方式92是实施方式61-90中任一项所述的方法,其中所述组合物被施用至少约8周的持续时间。
[0197]
实施方式93是实施方式61-92中任一项所述的方法,其中所述普氏菌属包括组织普氏菌。
[0198]
实施方式94是实施方式61-93中任一项所述的方法,其中所述肺部疾病选自:慢性阻塞性肺病(copd)、哮喘、肺纤维化、结节病、感染引起的疾病及其组合。
[0199]
实施方式95是实施方式94所述的方法,其中所述感染引起的疾病选自:病毒感染、细菌感染、真菌感染、寄生虫感染及其组合。
[0200]
实施方式96是实施方式95所述的方法,其中所述病毒感染选自:病毒性肺炎、病毒性支气管炎、流感、冠状病毒感染、腺病毒感染、合胞病毒感染、鼻病毒感染及其组合。
[0201]
实施方式96是实施方式95所述的方法,其中所述细菌感染选自:链球菌感染、葡萄球菌感染、衣原体感染、支原体感染、嗜血杆菌感染、棒状杆菌感染、分枝杆菌感染、军团菌感染及其组合。
[0202]
实施方式98是实施方式61-93中任一项所述的方法,其中所述肺部疾病包括肺炎。
[0203]
实施方案99是治疗哺乳动物肺部疾病的方法,其中所述方法包括向哺乳动物施用包含活的或灭活的产黑色素普氏菌的组合物。
[0204]
实施方案100是实施方案99所述的方法,其中所述组合物包含活的产黑色素普氏菌。
[0205]
实施方案101是实施方案99所述的方法,其中所述组合物包含灭活的产黑色素普氏菌和无活性的产黑色素普氏菌。
[0206]
实施方案102是实施方案99-101中任一项所述的方法,其中所述哺乳动物是人。
[0207]
实施方案103是实施方案99-101中任一项所述的方法,其中所述哺乳动物是啮齿动物。
[0208]
实施方式104是实施方式99-103中任一项所述的方法,其中所述施用包括口服施用。
[0209]
实施方式105是实施方式99-104中任一项所述的方法,其中所述组合物是丸剂、片剂或胶囊。
[0210]
实施方式106是实施方式99-105中任一项所述的方法,其中所述组合物是被配制为将产黑色素普氏菌递送至哺乳动物的肠道的丸剂、片剂或胶囊。
[0211]
实施方式107是实施方式99-103中任一项所述的方法,其中所述施用包括施用至呼吸系统。
[0212]
实施方式108是实施方式99-103或107中任一项所述的方法,其中所述组合物使用鼻喷雾剂、吸入剂或喷雾剂施用。
[0213]
实施方式109是实施方式99-108中任一项所述的方法,其中所述肺部疾病的症状的严重程度在施用后降低。
[0214]
实施方式110是实施方式109所述的方法,其中所述肺部疾病的症状的严重程度在施用后降低大于约25%。
[0215]
实施方式111是实施方式109所述的方法,其中所述肺部疾病的症状的严重程度在施用后降低大于约50%。
[0216]
实施方式112是实施方式109所述的方法,其中所述肺部疾病的症状的严重程度在施用后降低大于约75%。
[0217]
实施方式113是实施方式109-112中任一项所述的方法,其中所述哺乳动物的肺顺应性在所述施用步骤之后降低。
[0218]
实施方式114是实施方式113所述的方法,其中与施用前相比,施用后肺顺应性降低至少约5%。
[0219]
实施方式115是实施方式113所述的方法,其中与施用前相比,施用后肺顺应性降低至少约10%。
[0220]
实施方式116是实施方式113所述的方法,其中与施用前相比,施用后肺顺应性降低至少约15%。
[0221]
实施方式117是实施方式99-116中任一项所述的方法,所述方法还可包括在施用前测量一种或多种肺功能参数,并在施用后测量相同的一种或多种肺功能参数。
[0222]
实施方式118是实施方式117所述的方法,其中在施用后测量的一种或多种肺功能参数中的至少一种与施用前相比得到改善。
[0223]
实施方式119是实施方式117-118中任一项所述的方法,其中所述一种或多种肺功能参数包括肺顺应性、肺容量、气道阻力、弹性或其组合。
[0224]
实施方式120是实施方式99-119中任一项所述的方法,其中所述方法包括在所述施用步骤之前鉴定所述哺乳动物患有肺部疾病。
[0225]
实施方式121是实施方式99-120中任一项所述的方法,其中所述方法包括在所述施用步骤之前鉴定所述哺乳动物患有肺炎。
[0226]
实施方式122是实施方式99-121中任一项所述的方法,其中所述方法包括在所述
施用步骤之前鉴定所述哺乳动物患有copd。
[0227]
实施方式123是实施方式99-122中任一项所述的方法,其中所述组合物包含约1
×
103至约1
×
10
14
cfu的产黑色素普氏菌。
[0228]
实施方式124是实施方式99-122中任一项所述的方法,其中所述组合物包含约1
×
105至约1
×
10
12
cfu的产黑色素普氏菌。
[0229]
实施方式125是实施方式99-122中任一项所述的方法,其中所述组合物包含约1
×
108至约1
×
10
10
cfu的产黑色素普氏菌。
[0230]
实施方式126是实施方式99-125中任一项所述的方法,其中所述组合物每天施用一次。
[0231]
实施方式127是实施方式99-125中任一项所述的方法,其中所述组合物每天施用两次。
[0232]
实施方式128是实施方式99-125中任一项所述的方法,其中所述组合物每天施用三次。
[0233]
实施方式129是实施方式99-128中任一项所述的方法,其中所述组合物被施用至少约4周的持续时间。
[0234]
实施方式130是实施方式99-128中任一项所述的方法,其中所述组合物被施用至少约6周的持续时间。
[0235]
实施方式131是实施方式99-128中任一项所述的方法,其中所述组合物被施用至少约8周的持续时间。
[0236]
实施方式132是实施方式99-131中任一项所述的方法,其中所述肺部疾病选自:慢性阻塞性肺病(copd)、哮喘、肺纤维化、结节病、感染引起的疾病及其组合。
[0237]
实施方式133是实施方式132所述的方法,其中所述感染引起的疾病选自:病毒感染、细菌感染、真菌感染、寄生虫感染及其组合。
[0238]
实施方式134是实施方式133所述的方法,其中所述病毒感染选自:病毒性肺炎、病毒性支气管炎、流感、冠状病毒感染、腺病毒感染、合胞病毒感染、鼻病毒感染及其组合。
[0239]
实施方式135是实施方式133所述的方法,其中所述细菌感染选自:链球菌感染、葡萄球菌感染、衣原体感染、支原体感染、嗜血杆菌感染、棒状杆菌感染、分枝杆菌感染、军团菌感染及其组合。
[0240]
实施方式136是实施方式99-131中任一项所述的方法,其中所述肺部疾病包括肺炎。
[0241]
实施方案137是治疗哺乳动物肺部疾病的方法,其中所述方法包括向哺乳动物施用包含普氏菌属菌种的囊泡的组合物。
[0242]
实施方式138是实施方式137所述的方法,其中所述哺乳动物是人。
[0243]
实施方式139是实施方式137所述的方法,其中所述哺乳动物是啮齿动物。
[0244]
实施方式140是实施方式137所述的方法,其中所述施用包括口服施用。
[0245]
实施方式141是实施方式137-140中任一项所述的方法,其中所述组合物是丸剂、片剂或胶囊。
[0246]
实施方式142是实施方式137-141中任一项所述的方法,其中所述组合物是被配制为将普氏菌属菌种的囊泡递送至哺乳动物的肠道的丸剂、片剂或胶囊。
[0247]
实施方式143是实施方式137-139中任一项所述的方法,其中所述施用包括施用至呼吸系统。
[0248]
实施方式144是实施方式137-139或143中任一项所述的方法,其中所述组合物使用鼻喷雾剂、吸入剂或喷雾剂施用。
[0249]
实施方式145是实施方式137-144中任一项所述的方法,其中所述肺部疾病的症状的严重程度在施用后降低。
[0250]
实施方式146是实施方式145所述的方法,其中所述肺部疾病的症状的严重程度在施用后降低大于约25%。
[0251]
实施方式147是实施方式145所述的方法,其中所述肺部疾病的症状的严重程度在施用后降低大于约50%。
[0252]
实施方式148是实施方式145所述的方法,其中所述肺部疾病的症状的严重程度在施用后降低大于约75%。
[0253]
实施方式149是实施方式145-148中任一项所述的方法,其中所述哺乳动物的肺顺应性在所述施用步骤之后降低。
[0254]
实施方式150是实施方式149所述的方法,其中与施用前相比,施用后肺顺应性降低至少约5%。
[0255]
实施方式151是实施方式149所述的方法,其中与施用前相比,施用后肺顺应性降低至少约10%。
[0256]
实施方式152是实施方式149所述的方法,其中与施用前相比,施用后肺顺应性降低至少约15%。
[0257]
实施方式153是实施方式137-152中任一项所述的方法,所述方法还可包括在施用前测量一种或多种肺功能参数,并在施用后测量相同的一种或多种肺功能参数。
[0258]
实施方式154是实施方式153所述的方法,其中在施用后测量的一种或多种肺功能参数中的至少一种与施用前相比得到改善。
[0259]
实施方式155是实施方式153-154中任一项所述的方法,其中所述一种或多种肺功能参数包括肺顺应性、肺容量、气道阻力、弹性或其组合。
[0260]
实施方式156是实施方式137-155中任一项所述的方法,其中所述方法包括在所述施用步骤之前鉴定所述哺乳动物患有肺部疾病。
[0261]
实施方式157是实施方式137-156中任一项所述的方法,其中所述方法包括在所述施用步骤之前鉴定所述哺乳动物患有肺炎。
[0262]
实施方式158是实施方式137-157中任一项所述的方法,其中普氏菌属菌种的代表性细胞以nrrl登录号b-50329保藏。
[0263]
实施方式159是实施方式137-158中任一项所述的方法,其中所述组合物每天施用一次。
[0264]
实施方式160是实施方式137-158中任一项所述的方法,其中所述组合物每天施用两次。
[0265]
实施方式161是实施方式137-158中任一项所述的方法,其中所述组合物每天施用三次。
[0266]
实施方式162是实施方式137-161中任一项所述的方法,其中所述组合物被施用至
少约4周的持续时间。
[0267]
实施方式163是实施方式137-161中任一项所述的方法,其中所述组合物被施用至少约8周的持续时间。
[0268]
实施方式164是实施方式137-163中任一项所述的方法,其中所述普氏菌属菌种包括组织普氏菌。
[0269]
实施方式165是实施方式137-164中任一项所述的方法,其中所述普氏菌属菌种包括产黑色素普氏菌。
[0270]
实施方式166是实施方式137-165中任一项所述的方法,其中所述普氏菌属菌种包括组织普氏菌和产黑色素普氏菌。
[0271]
实施方式167是实施方式137-165中任一项所述的方法,其中所述肺部疾病选自:慢性阻塞性肺病(copd)、哮喘、肺纤维化、结节病、感染引起的疾病及其组合。
[0272]
实施方式168是实施方式166所述的方法,其中所述感染引起的疾病选自:病毒感染、细菌感染、真菌感染、寄生虫感染及其组合。
[0273]
实施方式169是实施方式167所述的方法,其中所述病毒感染选自:病毒性肺炎、病毒性支气管炎、流感、冠状病毒感染、腺病毒感染、合胞病毒感染、鼻病毒感染及其组合。
[0274]
实施方式170是实施方式167所述的方法,其中所述细菌感染选自:链球菌感染、葡萄球菌感染、衣原体感染、支原体感染、嗜血杆菌感染、棒状杆菌感染、分枝杆菌感染、军团菌感染及其组合。
[0275]
实施方式171是实施方式137-165中任一项所述的方法,其中所述肺部疾病包括肺炎。
[0276]
实施例
[0277]
实施例1
[0278]
用含有活的组织普氏菌的组合物治疗被诊断患有copd或表现出其一种或多种症状(例如肺气肿)的人。以约1
×
103至约1
×
10
14
cfu的剂量将含有活的组织普氏菌的组合物每天一次口服施用于人,持续8周。监测人以确认copd的一种或多种症状的减轻。
[0279]
实施例2
[0280]
用含有活的组织普氏菌的组合物治疗被诊断患有copd或表现出其一种或多种症状(例如肺气肿)的人。以约1
×
103至约1
×
10
14
cfu的剂量将含有活的组织普氏菌的组合物每天一次经鼻施用于人,持续8周。监测人以确认copd的一种或多种症状的减轻。
[0281]
实施例3
[0282]
使用dq8小鼠生成了香烟烟雾(cs)诱导的肺气肿模型。暴露于cs 4-5周通过增强促炎细胞因子(如il-17)改变肺免疫并诱导轻度肺气肿。使用dq8.il-17-/-小鼠研究了il-17在cs诱导的肺气肿中的作用。暴露于cs 4周导致这些小鼠出现严重的肺气肿,表明il-17具有保护作用。copd肺部的微生物群可能发生了改变,在某些情况下会选择性地删除普氏菌属菌种。这些结果表明,气道微生物群可能参与指导促炎细胞因子的分化,进而促进炎症细胞的流入和copd。
[0283]
实施例4
[0284]
为了研究细胞因子在肺部病理学中的作用,将dq8小鼠暴露于cs或空气中5周,并通过逆转录酶聚合酶链反应(rtpcr)确定肺部的免疫反应(图1)。图1是暴露于cs(红色条)
或空气(蓝色条)的小鼠肺部mrna表达的柱状图。暴露于cs的小鼠表现出cxcr3和cxcl10的增加,与吸烟者中已知的相似(参见,例如,saetta,等人,am.j.respir.crit.care med.,165:1404-1409(2002)),伴有纤维化相关基因coll a1、纤连蛋白和tgfβ的表达降低。
[0285]
实施例5
[0286]
通过产生缺乏il-17的aeo.dq8小鼠(dq8.il-17-/-)来研究il-17在肺气肿中的作用。dq8和dq8.il-17-/-小鼠暴露于cs 4周。暴露于空气(ns)的dq8小鼠用作对照(图2a、2b和2c)。通过在活体动物中进行肺力学扫描,通过确定肺顺应性(cst)来测量小鼠的肺功能。在三组小鼠中研究了压力-体积(pv)曲线,并且数据按照所描述的方式编译(ns dq8小鼠(图2a)和cs dq8小鼠(图2b),各自n=7,以及dq8.il-17-/-,cs小鼠(图2c),n=4)。这些结果表明,暴露于cs的人源化小鼠出现肺气肿,这是copd的一个关键特征。这些结果还证明了il-17在copd中的保护作用,因为在没有il-17的情况下,肺顺应性增加。如图3所示,相对于对照“非吸烟者”(ns)dq8小鼠,在暴露于cs的dq8以及dq8.il-17-/-小鼠中观察到肺顺应性显著增加。
[0287]
不受任何特定理论的束缚,据信il-17在copd中的作用可能是1)一种补偿机制或2)生态失调导致il-17增加。
[0288]
dq8.il-17-/-模型与其他模型的不同之处在于,与其他模型(参见,例如,wright,jl和a.churg.expert.rev.respir.med.4:723-734.(2010))报告的16-24周相比,copd是在短期cs暴露后(例如,大约4周后)发生的。此外,dq8.il-17-/-模型表现出受人dq8分子限制的免疫反应效应臂,并模拟人对各种抗原和自身免疫病理的免疫反应。
[0289]
实施例6
[0290]
如实施例5所示,在吸烟者dq8.il-17-/-小鼠中出现肺气肿,在该模型中暴露于cs 3-4周导致慢性肺部炎症伴随肺泡破坏和肺气肿。用组织普氏菌进行口服治疗以确认通过产生生态平衡和减少肺部炎症来调节暴露于cs的dq8.il-17-/-小鼠中的肺气肿。简言之,在dq8.il-17-/-小鼠中用组织普氏菌或产黑色素普氏菌处理cs诱导的肺气肿用于确定肺功能的变化。暴露于空气而不是cd的dq8.il-17-/-小鼠用作对照。使用静态肺顺应性测量处理小鼠肺功能的改善。
[0291]
实施例7
[0292]
copd患者存在普氏菌属低丰度,而普氏菌属是口腔、肺和肠道黏膜中最丰富的菌属之一。确定cs诱导的肺气肿是否可以通过口腔粘膜占优势的人类共生体来治疗。
[0293]
dq8.il-17-/-小鼠每天暴露于cs 2周,队列被随机分配到4组:
[0294]
组1
–
介质处理(对照),
[0295]
组2
–
假对照,
[0296]
组3
–
用组织普氏菌进行口服处理,和
[0297]
组4
–
用产黑色素普氏菌进行口服处理。
[0298]
如实施例5、图2a-2c和图3所示,在暴露于cs的4周内,小鼠表现出明显的肺功能丧失。暴露2周后,结构变化似乎开始了。
[0299]
选择该暴露持续时间是因为4周是在dq8.il-17-/-小鼠中可重复且有效地诱导肺气肿生理异常所需的时间,如实施例5所示。肺功能力学是终末事件,因此在cs暴露2周后,实验组用细菌培养物中的活细菌(10^9cfu/100μl)隔日口服处理2周。小鼠继续暴露于cs,
总暴露时间为4周。对照年龄匹配的小鼠进行假烟熏:将它们放在靠近香烟烟雾室的笼子里。每组包括约7-10只小鼠用于肺功能。
[0300]
慢性cs暴露在烟雾室(teague enterprises,ca)中进行,使小鼠暴露于由3r4f肯塔基研究香烟产生的调节浓度的cs吸入(每10分钟2支香烟,每天3小时/天,持续5天/周,如其他地方所述(参见,例如,kroening等人,journal of immunology,181:1536-1547(2008))。在该系统中,小鼠暴露于主流和侧流香烟烟雾的混合物中,这使得足够的暴露导致小鼠血液中烟碱水平与重度吸烟者达到的水平相似(范围约为45-181ng/ml)(参见,例如,kroening等人,journal of immunology,181:1536-1547(2008);和jarvik等人,pharmacol.biochem.behav.,66:553-558(2000))。
[0301]
每天监测小鼠并在隔天称重以确定它们的状况。
[0302]
在实验结束时进行肺功能分析。使用系统执行cs暴露和对照小鼠的肺功能。这允许确定肺顺应性、容量和气道阻力。呼吸系统阻力、顺应性和弹性的基线测量是使用单室模型在2秒屏气期间以2.5hz正弦振荡进行的(参见,例如,ewart,s.等人j appl physiol(1985)79:560-566)。使用所有4组小鼠确定暴露于香烟烟雾4周的影响。在暴露期结束时,在自主通气下进行静态肺顺应性、气道和组织阻力。
[0303]
进行测量以确认组织普氏菌和产黑色素普氏菌抑制肺气肿。
[0304]
实施例8
[0305]
cs会导致肺微生物群的生态失调,从而改变局部免疫反应,导致促炎细胞因子积聚。通过执行许多补充策略来分析暴露于cs的肺的结构和分子变化。
[0306]
为了确定形态气道和远端肺变化,如实施例7所述处理小鼠。在第4周实验结束时,处死小鼠。用0.5ml的10%中性缓冲福尔马林使肺膨胀,并固定过夜。将固定的肺组织包埋在石蜡中,切片并用苏木精和伊红染色(h&e染色)确定是否存在肺气肿的形态学特征(例如,肺泡间壁的扩张和平均线性截距的测定(参见,例如hasleton,p.s.pathol eur 11:211-218,(1976)))。每只小鼠评估四到五条血管。简言之,对于每条血管,评估血管周围浸润的两个特征。周长分数表示被细胞包围的血管周长的百分比。1分代表5-20%的血管周长被细胞包围;2分代表25-45%的血管被细胞包围;3分表示50
–
75%的血管被细胞包围;4分代表75-100%的血管被细胞包围。
[0307]
在另一组小鼠中,一个肺在-80℃下冷冻,随后用于使用rtpcr确定细胞因子和趋化因子。
[0308]
在处死时收集上一段和实施例7中每只小鼠的一个肺并进行16s测序(参见例如chen,j.等人genome med 8:43(2016))。样品被冷冻,所有样品一起进行16s rrna测序。使用16s核糖体rna(rrna)基因的高变v4区域的深度rdna测序生成微生物群的系统型谱(参见,例如,人类微生物组研究的基于16s rdna的社区分析评估(evaluation of 16s rdna-based community profiling for human microbiome research),plos one 7:e39315(2012))。微生物dna是使用mobio powersoil试剂盒和珠击步骤提取的。使用50ng cdna和0.3μm条形码引物和kapa hifi hotstart ready mix进行聚合酶链式反应(pcr)。如实施例7分析数据以确认处理如何改变微生物组成。
[0309]
实施例9
[0310]
数据解读计划
[0311]
肺顺应性的差异通过使用anova分析确定,每组7只小鼠。
[0312]
微生物组分析:使用miseq reagent kit v2(500循环)(illumina inc.)在mayo genomics facility的一条miseq泳道上对样本进行测序,产生20m 2x250读数。预处理的序列文件由im-tornado(jeraldo,p.等人,plos one 9:e114804,2014)处理,去除质量差和不完整的序列。然后通过核糖体数据库项目输入序列,以获得用于以后相关性分析的分类群调用。生物信息学管道允许操作分类单元(otu)分配,然后是微生物群落分析,包括序列比对、系统发育树、基于系统发育和分类的多样性分析和网络分析,以及用于聚类成otu、生成稀疏曲线和计算物种丰富度估计ace(基于丰度的覆盖率估计器)和chao1(chao 1估计器)值的unifrac分析。坐标分析基于门级的bray-curtis距离,允许测试样本的聚类。用于这些分析的bray-curtis距离矩阵是在各种系统发育水平上计算的,包括dna序列水平、门水平、科水平、属水平的分箱或属和种水平组合的选择性分组。bray-curtis相异指数用于使用phylip包计算聚类分析的距离矩阵。用于聚类微生物谱的bray-curtis距离分析、坐标和统计分析如所述进行(参见例如chen,j.等人genome med 8:43,2016.)。预测分析和其他统计分析在r-3.0.2(r开发核心团队)中进行,如其他地方所述(参见,例如,chen,j.等人genome med 8:43,2016)。
[0313]
统计功效:15只小鼠/株用于定义微生物谱的变化(参见,例如,chen,j.等人genome med 8:43,2016)。聚类的统计功效分析通过两组manova方法进行评估(参见,例如,cohen,j.1988.第10章,行为科学的统计功效分析(statistical power analysis for the behavioral sciences),第2版,lawrence erlbaum assoc inc.567)。每组15只小鼠提供了与样本聚类相关的显著结果,并允许检验处理和未处理小鼠的微生物谱存在特征性变化的假设。通过非参数学生t检验分析细胞因子反应。两侧p值《0.05被认为具有统计学意义。
[0314]
实施例10
[0315]
在口腔中补充共生体,并测量处理和未处理小鼠肺微生物组的变化。共生体的口服补充导致肠道中存在共生体。如果观察到cs诱导的处理没有差异,则用抗生素万古霉素(仅影响肠道)处理小鼠,以确认肠道微生物群对cs诱导的肺气肿的影响。
[0316]
对于肠道微生物组测试,在处理开始前和处理停止后收集粪便样本。即使口服补充剂仅改变肠道微生物群,考虑到存在的肠-肺轴,也可以确认处理后肺部免疫反应的差异。
[0317]
实施例11
[0318]
微生物的经鼻应用对肺特异性作用的确认与微生物口服应用的描述相同。
[0319]
实施例12
[0320]
幼稚dq8小鼠暴露于香烟烟雾(cs)或不暴露于香烟烟雾(n)4周。暴露于cs 2周的两组小鼠隔天鼻内使用组织普氏菌(ph)或产黑色素普氏菌(pm)进行处理。数据显示,未用ph或pm处理的小鼠肺功能显著丧失,顺应性增加,表明肺气肿或copd(图5a和5d)。n相对于cs,p《.008。在用组织普氏菌或产黑色素普氏菌处理后,小鼠表现出与仅暴露于空气(n)的幼稚dq8小鼠相似的顺从性(图5b-d)。cs/ph相对于cs,p《0.004,cs/pm相对于cs,p《0.006。使用prism软件和非配对t检验进行分析。
[0321]
使用flexivent系统将肺功能测量为静态肺顺应性(cst)。确定静态肺顺应性、容量和气道阻力的定量评估。在自主通气下测量静态肺顺应性、气道和组织阻力。呼吸系统阻
力、顺应性和弹性的基线测量是使用单室模型在2秒屏气期间以2.5赫兹正弦振荡进行的。在暴露于cs的4周内,小鼠的肺功能显著丧失。肺功能力学是终末事件,因此在cs暴露2周后,小鼠接受悬浮在100微升tsb(厌氧)细菌培养物中的活细菌(10^9cfu/100μl)组织普氏菌或产黑色素普氏菌的为期2周的鼻内处理。
[0322]
香烟烟雾暴露:慢性cs暴露在吸烟室(teague enterprises,ca)中进行,使小鼠暴露于由3r4f肯塔基研究香烟(3r4f kentucky research cigarettes)产生的调节浓度的cs吸入(每10分钟2支香烟,每天3小时,以5天/周为基础。在该系统中,小鼠暴露于主流和侧流香烟烟雾的混合物中,并能够充分暴露,从而产生与重度吸烟者的血液烟碱水平相似的小鼠血液烟碱水平(范围为45-181ng/ml)。
[0323]
实施例13
[0324]
幼稚dq8.il-17-/-小鼠暴露于香烟烟雾(cs)或不暴露于香烟烟雾(n)4周。暴露于cs 2周的两组小鼠隔天鼻内使用组织普氏菌(ph)或产黑色素普氏菌(pm)进行处理。图6中的数据显示,与幼稚dq8小鼠相比,未暴露于cs的dq8.il-17-/-幼稚小鼠肺功能显著丧失(如图5a所示),p《0.048。暴露于cs后,在dq8.il-17-/-小鼠中观察到肺功能丧失,尽管与幼稚小鼠相比并不显著,这表明il-17对于维持肺功能至关重要。暴露于cs的dq8.il-17-/-小鼠如实施例12一样用组织普氏菌或产黑色素普氏菌处理。处理后,小鼠表现出与仅暴露于空气的幼稚dq8.il-17-/-小鼠(n)相似的顺应性。cs/ph相对于cs,p《0.03,cs/pm相对于cs,p《0.02。处理的dq8.il-17-/-小鼠表现出与处理的dq8小鼠相似的功能,这表明普氏菌属菌种能够恢复由于il-17缺乏而丧失的功能。
[0325]
实施例14
[0326]
来自组织普氏菌和产黑色素普氏菌的omv用于确定这些囊泡是否可以改善copd小鼠的肺功能。源自产黑色素普氏菌的omv显示出显著改善,cs相对于cs/pm omv,p《0.02,而那些用源自组织普氏菌的omv处理的小鼠表现出不同的反应,一些小鼠表现出肺功能恢复,而另一些则没有(图7)。这些数据表明,普氏菌属的omv中的某些蛋白质可能能够恢复copd的肺功能。
[0327]
使用超速离心法从组织普氏菌和产黑色素普氏菌的体外肉汤培养物中纯化omv(yang d.等人,immunity.2019;50(3):692-706.e7.doi:10.1016/j.immuni.2019.02.001)。简言之,将使用胰蛋白酶大豆肉汤(tsb)在厌氧条件下生长的细菌在10,000g下离心15分钟(4℃)以收集无菌上清液。将收集的上清液以400,000g超速离心1.5小时(在4℃)。超速离心后,去除上清液以获得沉淀的omv。将omv沉淀悬浮在磷酸盐缓冲液(pbs)中。将制备的omv悬浮液的一部分铺在tsb-血琼脂板上以检查细菌污染。
[0328]
纯化的omv通过量化总蛋白(pierce bca蛋白检测试剂盒
–
thermo fisher scientific)进行生化表征,以阐明omv和总lps的纯度。暴露于cs的dq8小鼠用100mg(omv脂多糖(lps))/小鼠鼻内处理。
[0329]
实施例15
[0330]
幼稚dq8小鼠暴露于香烟烟雾中2周。将小鼠分为2组,一组用组织普氏菌(ph)鼻内应用处理2周并暴露于香烟烟雾中,而另一组是对照组并且仅暴露于cs。*表示cs相对于cs/ph的p值。每组n=6。
[0331]
使用市售试剂盒通过rtpcr测量mrna转录物(图8a-e)。用组织普氏菌处理的小鼠
表现出较低的促炎细胞因子表达。此外,t细胞上的共刺激ctla-4减少。已知il-13可诱导b细胞的活化和增殖以及抗体的产生。il-23是一种th17细胞因子,已知参与维持th17反应。copd患者肺部的il-1b和il-23均升高并引起炎症。tnf-a是一种多效性细胞因子,参与细胞毒性、血管生成、生长抑制、炎症和免疫调节。tnf-a抑制剂已显示出对严重copd的疗效,可减少住院治疗。这些数据表明,接受组织普氏菌处理的copd小鼠的炎症比未处理的小鼠少。
[0332]
实施例16
[0333]
暴露于cs并用组织普氏菌处理的dq8幼稚小鼠显示某些细胞因子转录物的水平达到幼稚小鼠的水平。il-1b在幼稚和组织普氏菌处理的小鼠之间没有表现出任何差异(图9a)。同样,经过处理的小鼠表现出恢复了与幼稚小鼠相似的ctla表达水平(图9b)。
[0334]
所测试的所有细胞因子的表达表明,组织普氏菌处理小鼠和幼稚小鼠之间没有差异,这表明组织普氏菌处理使暴露于cs的小鼠肺部的免疫状态正常化。
[0335]
实施例17
[0336]
与cs幼稚dq8小鼠相比,用组织普氏菌处理降低了暴露于cs的幼稚dq8小鼠的促炎细胞因子水平(图10a和10b)。然而,差异并不显著,表明它可以减少炎症而不引起免疫抑制。因此,这种处理不会导致无法抵抗感染。
[0337]
实施例18
[0338]
dq8小鼠暴露于cs 2周并用ii型胶原(cii)(n=4)免疫4周。两只小鼠隔日用牙龈卟啉单胞菌鼻内处理2周,而2只小鼠未接受任何处理。4周后分析肺顺应性。没有观察到显著差异(图11)。
[0339]
实施例19
[0340]
使用另外一组重复实施例7的实验:组5
–
用牙龈卟啉单胞菌处理。进行肺功能测量以确认组织普氏菌和产黑色素普氏菌抑制肺气肿,而牙龈卟啉单胞菌没有效果。
[0341]
实施例20
[0342]
用含有活的组织普氏菌的组合物治疗被诊断患有肺炎或表现出其一种或多种症状(例如肺气肿)的人。以约1
×
103至约1
×
10
14
cfu的剂量将含有活的组织普氏菌的组合物每天一次口服施用于人,持续8周。监测人以确认肺炎的一种或多种症状的减轻。
[0343]
实施例21
[0344]
用含有活的组织普氏菌的组合物治疗被诊断患有肺炎或表现出其一种或多种症状(例如肺气肿)的人。以约1
×
103至约1
×
10
14
cfu的剂量将含有活的组织普氏菌的组合物每天一次经鼻施用于人,持续8周。监测人以确认肺炎的一种或多种症状的减轻。
[0345]
其他实施方式
[0346]
应理解,虽然本发明已经结合具体实施方式进行了描述,但前述描述旨在说明而不是限制由所附权利要求书的范围所限定的本发明的范围。其它方面、优点和改进均在权利要求书的范围内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。