1.本发明属于医药领域,具体涉及褐藻糖胶在制备治疗前列腺炎药物中的应用。
背景技术:
2.慢性非细菌性前列腺炎(chronic nonbacterial prostatitis,cnp)是青壮年男性中的常见病,约有50%的男性一生中会出现不同程度的前列腺炎症状,其主要症状通常表现为不伴尿路感染的尿频、尿急、尿痛、夜尿增多等排尿症状和骨盆会阴区的疼痛症状。但是由于对cnp的病因和发病机制了解不清,目前针对cnp的治疗常常是经验性的,治疗效果有限,并且常常容易复发,造成患者强烈的痛苦感和巨大的经济负担。
3.褐藻糖胶是一种多糖类物质,但是与一般的多糖类物质不同,褐藻糖胶的部分羟基被硫酸酯化,因此,也被称为“褐藻多糖硫酸酯”。褐藻糖胶在我们的生活场景中,最常见于藻类表面的那一层黏滑的成分,是保护藻类的重要成分,能防止细菌等不利成分的侵入,也能防止藻类的水分流失,保护内部的细胞。近年,关于褐藻糖胶的研究发现,褐藻糖胶是中性粒细胞迁移所必须的选择素(selectin)的竞争性抑制剂,因此,褐藻糖胶能够抑制中性粒细胞迁移至炎症部分,从而在牙龈炎、放射性肺炎等炎症性动物模型中起有效的治疗作用,但是已发表的研究成果中,尚未有关于褐藻糖胶应用于前列腺炎的研究。
技术实现要素:
4.有鉴于此,本发明的目的在于提供褐藻糖胶在制备治疗前列腺炎药物中的应用,褐藻糖胶能减轻前列腺炎症和痛觉过敏反应,可用于制备治疗慢性非细菌性前列腺炎的药物。
5.为了实现上述发明目的,本发明提供了以下技术方案:
6.本发明提供了褐藻糖胶在制备治疗前列腺炎药物中的应用。
7.优选的,所述前列腺炎包括慢性非细菌性前列腺炎。
8.优选的,所述前列腺炎包括小鼠实验性自身免疫性前列腺炎。
9.优选的,所述褐藻糖胶降低前列腺内中性粒细胞特异性的髓过氧化物酶的含量。
10.优选的,所述褐藻糖胶降低中性粒细胞在前列腺组织内的浸润。
11.优选的,所述褐藻糖胶减轻前列腺炎痛觉过敏反应。
12.本发明还提供了一种治疗前列腺炎的药物,所述药物包括活性成分褐藻糖胶及药学上可接受的辅料。
13.优选的,所述药物中褐藻糖胶的有效作用浓度为18~22mg/kg体重。
14.优选的,所述药物还添加有其他治疗前列腺炎的活性成分。
15.与现有技术相比,本发明具有如下有益效果:
16.本发明发现褐藻糖胶可以降低中性粒细胞在eap小鼠前列腺组织内的浸润,从而达到减轻前列腺炎症和痛觉过敏反应的效果,有可用于制备治疗慢性非细菌性前列腺炎的药物的潜在可能性。
附图说明
17.图1为小鼠实验性自身免疫性前列腺炎构建的结果检测,a为he染色图像,b为炎症评分,c为痛觉反应程度。
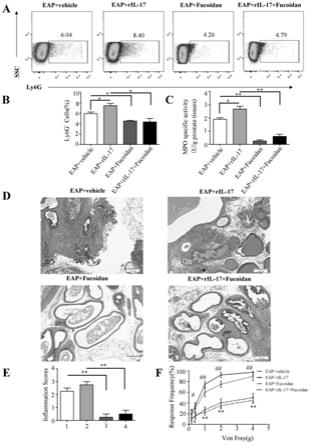
18.图2为小鼠实验性自身免疫性前列腺炎构建的结果检测,a为流式细胞术检测结果,b为免疫荧光图像和细胞数目统计结果,c为mpo活性。
19.图3为中性粒细胞与eap鼠的前列腺炎症和痛觉过敏反应关系的结果检测,a为血液学细胞计数器检测结果,b为he染色图像,c为炎症评分,d为痛觉反应程度。
20.图4为褐藻糖胶对中性粒细胞和eap鼠的前列腺炎症、痛觉过敏反应关系的结果检测,a~b为流式细胞术检测结果,c为mpo活性,d为he染色图像,e为炎症评分,f为痛觉反应程度。
具体实施方式
21.本发明提供了褐藻糖胶在制备治疗前列腺炎药物中的应用,所述前列腺炎包括小鼠实验性自身免疫性前列腺炎。
22.本发明构建了实验性自身免疫性前列腺炎(experimental autoimmune prostatitis,eap)小鼠动物模型,是利用小鼠对前列腺抗原的自身免疫构建的无菌性前列腺炎动物模型。在eap小鼠动物模型中,慢性非细菌性前列腺炎的特点—慢性盆腔疼痛和前列腺内炎性细胞浸润,均能完美体现,为研究慢性非细菌性前列腺炎的有效动物模型。
23.本发明发现,eap小鼠前列腺组织中有明显的中性粒细胞浸润,在使用抗ly6g特异性抗体对外周血中性粒细胞进行耗竭后,eap 抗ly6g小鼠前列腺组织炎性细胞浸润和盆腔痛觉过敏症状较eap igg组明显好转。由于全身性的耗竭中性粒细胞,可能造成生物体缺乏必要的对抗自然界细菌和病毒的免疫力,从而无法在自然界中生活。本发明的实验小鼠是在无菌环境饲养的,因此即使是中性粒细胞耗竭,尚未显现出对其寿命的影响。但是,若是在有细菌、病毒存在于周遭自然环境中的动物或人,耗竭中性粒细胞是不可行的。相反,减少前列腺组织内中性粒细胞的浸润,而不影响其外周血中的中性粒细胞,或许能实现治疗前列腺炎而不影响其在自然环境中的生存。因此,减少中性粒细胞从外周血迁移至前列腺,减少前列腺组织内中性粒细胞的浸润,可以成为治疗慢性非细菌性前列腺炎的可能治疗方式。
24.本发明提供了褐藻糖胶在制备治疗前列腺炎药物中的应用,所述前列腺炎包括慢性非细菌性前列腺炎。
25.褐藻糖胶是中性粒细胞迁移所必须的选择素(selectin)的竞争性抑制剂,因此,褐藻糖胶能够抑制中性粒细胞迁移至炎症部分。本发明发现,使用褐藻糖胶处理eap鼠后,通过流式细胞学证据和髓过氧化物酶检测双重方式,证实了褐藻糖胶处理组小鼠前列腺组织内中性粒细胞浸润含量减少,由此证实了褐藻糖胶处理能降低中性粒细胞在前列腺组织内的浸润。而褐藻糖胶的处理也造成小鼠前列腺组织炎性改变和痛觉过敏有效减轻。即使在使用小鼠重组il-17处理增强eap小鼠的前列腺炎表现后,再使用褐藻糖胶处理,同样能减轻前列腺组织的炎性改变和痛觉过敏症状。
26.本发明还提供了一种治疗前列腺炎的药物,所述药物包括活性成分褐藻糖胶及药学上可接受的辅料。
27.在本发明以褐藻糖胶为活性成分制备得到的治疗前列腺炎的药物中,褐藻糖胶的有效作用浓度为18~22mg/kg体重,优选为19~21mg/kg体重,更优选为20mg/kg体重。
28.本发明所述治疗前列腺炎的药物中还可以添加有其他治疗前列腺炎的活性成分,所述活性成分包括α受体阻滞剂、植物制剂、非甾体类抗炎镇痛药,能与褐藻糖胶共同起到治疗前列腺炎的作用。
29.本发明实施例中所使用的褐藻糖胶(fucoidan),也叫岩藻多糖,是由sigma-aldrich公司购买所得的化学品,产品编号是f5631,cas no.9072-19-9,是由位于上海市浦东新区仁庆路509号10幢的西格玛奥德里齐(上海)贸易有限公司生产。
30.下面结合实施例对本发明提供的技术方案进行详细的说明,但是不能把它们理解为对本发明保护范围的限定。
31.本发明实施例中动物实验经安徽医科大学动物中心动物伦理委员会批准(编号:llsc20190651)。
32.本发明实施例中所用试剂为:完全弗氏佐剂(cfa;sigma-aldrich)、水合氯醛(阿拉丁生物技术)、抗小鼠ly-6g抗体(bio-x-cell,clone 1a8)、大鼠igg(bio-x-cell,clone gl117)。
33.本发明实施例中所用检测方法为:
34.1.前列腺组织he染色和炎症评分。
35.前列腺组织用10%福尔马林固定,石蜡包埋。5μm切片用苏木精和eoxin(he)染色,并使用慢性前列腺炎的组织病理学分类系统进行盲法评分。
36.慢性炎症的程度从0~3分为:a)0分,无炎症;b)1分,轻度但明确的前列腺间质内炎性细胞浸润;c)2分,中度前列腺间质内炎性细胞浸润;d)3分,前列腺间质内炎性细胞浸润,前列腺实质内有大量单核细胞。
37.2.前列腺盆腔痛觉过敏行为学检测。
38.将vonfrey纤维细丝刺激前列腺附近的下腹部盆腔区域,小鼠的三种行为被认为是对vonfrey纤维丝刺激的阳性反应:1)腹部急剧收缩;2)立即舔或抓刺激丝的区域;或3)跳跃。
39.阳性反应率计算为阳性响应的百分比,以数据报告为平均值
±
sem。
40.3.前列腺组织内中性粒细胞流式细胞学计数分析。
41.新鲜采集的前列腺组织机械破坏,并在含有1mg/ml胶原酶d(sigma-aldrich,c9891)和0.05%dnasei(sigma-aldrich,d5025)的rpmi1640培养基中37℃酶解45分钟。消化后,悬浮液通过75μm细胞过滤器过滤,单细胞悬浮液用pbs洗涤。然后,用apc结合的抗ly6g(bd bioscience,560599)对细胞进行染色,以进行流式细胞仪细胞分选法(facs分析)。使用facs calibur流式细胞仪(bd bioscience)分析染色细胞,并使用flowjo软件x分析数据。
42.4.前列腺组织抗ly-6g免疫荧光染色。
43.前列腺组织用10%福尔马林固定,并用石蜡包埋。前列腺切片用5%牛血清白蛋白封闭,并在4℃下与兔抗鼠ly6g一级抗体(1:200,elabscience,e-ab-70094)孵育过夜。然后,在用tris缓冲盐水(tbs)清洗后,将切片与cy3结合的山羊抗兔igg(1:400,beyotime,a0516)和dapi(1:1000,beyotime,c1005)孵育。
44.使用蔡司lsm510共焦显微镜获取荧光图像。
45.5.中性粒细胞髓过氧化物酶活性检测。
46.根据mpo检测试剂盒制造商的说明,使用mpo活性测量试剂盒(elabscience,e-bc-k074)分析前列腺组织中的mpo活性。
47.用分光光度计在450nm处测定mpo活性,并以u/g前列腺组织表示。
48.实施例1
49.本实施例构建得到实验性自身免疫性前列腺炎的小鼠模型:
50.1、实验动物选择:从南京模型动物研究中心购买了6~8周龄的雄性nod小鼠。所有小鼠均在特定的无病原体条件下饲养。
51.2、小鼠模型构建
52.对照组:小鼠在第0天和第14天分别皮下注射0.1ml生理盐水。
53.eap组:小鼠在第0天和第14天分别皮下注射0.1ml由前列腺抗原和完全弗氏佐剂按照1:1混合得到的乳化液。
54.每组4只小鼠并进行了三个独立实验,数据为平均值
±
sem。
55.3、小鼠盆腔痛觉过敏行为学检测
56.对照组小鼠于第0天和第42天进行前列腺盆腔痛觉过敏行为学检测;eap组小鼠在前列腺抗原皮下注射构建eap模型前(基线检查,第0天)和eap诱导后第42天对小鼠进行测试,结果见图1-c。
57.4、小鼠前列腺组织he染色和炎症评分
58.第42天将对照组和eap组小鼠通过过量水合氯醛处死,并分别对小鼠第42天的前列腺组织进行切片he染色和炎症评分统计,结果见图1-a、1-b。
59.由图1可知,eap组小鼠前列腺组织内有大量炎性细胞浸润,无菌性的组织破坏也较对照组加重(图1-a);前列腺组织炎症评分较对照组增加(图1-b,p《0.05);针对von frey纤维丝刺激临近前列腺组织的下腹盆腔区域的痛觉反应程度较对照组增加(图1-c,p《0.05)。表明,小鼠eap模型具备人慢性非细菌性前列腺炎的特点—前列腺内炎性细胞浸润和慢性盆腔疼痛,该小鼠eap模型是研究人慢性非细菌性前列腺炎的可靠动物模型。
60.5、小鼠前列腺组织中中性粒细胞浸润检测
61.分别对eap组和对照组小鼠第42天的前列腺组织进行检测,通过流式细胞术分析前列腺组织中的ly6g
中性粒细胞,结果见图2-a;前列腺组织中性粒细胞浸润的免疫荧光染色结果见图2-b(图2-b中左侧为免疫荧光染色结果,右侧为基于免疫荧光染色结果统计得到的ly6g
细胞在每个高倍镜视野下(hp)的细胞数目);通过mpo比色分析试剂盒测定对照组和eap小鼠前列腺组织中的mpo活性,结果见图2-c。
62.由图2可知,eap小鼠前列腺组织中ly6g
细胞的百分比高于对照小鼠(图2-a,p《0.05);eap前列腺组织切片显示前列腺腺腔周围的ly6g阳性中性粒细胞水平显著升高(图2-b);eap小鼠前列腺组织中的mpo活性高于对照小鼠(图2-c,p《0.01)。表明,eap小鼠前列腺组织中中性粒细胞浸润增加。
63.实施例2
64.本实施例探究了中性粒细胞耗竭与eap鼠前列腺炎症和痛觉过敏反应的关系:
65.1、实验动物选择:从南京模型动物研究中心购买了6~8周龄的雄性nod小鼠。所有
小鼠均在特定的无病原体条件下饲养。
66.2、小鼠模型构建
67.对照组:eap igg同型对照抗体处理
68.试验组:eap 抗ly-6g抗体处理
69.eap小鼠模型采用实施例1中所述的诱导方式,在eap诱导前一天腹腔注射0.25mg抗小鼠ly-6g抗体或同型匹配的大鼠igg,并且每周重复注射一次。
70.每组4只小鼠并进行了三个独立实验,数据为平均值
±
sem。
71.3、eap鼠的前列腺炎症和痛觉过敏反应检测
72.在eap第1次诱导后42天,通过血液学细胞计数器测量eap igg和eap 抗ly6g小鼠外周血中的中性粒细胞、淋巴细胞和单核细胞数量,结果见图3-a。
73.在eap第1次诱导后42天,分别检测eap igg和eap 抗ly6g小鼠前列腺组织的代表性he染色图像(结果见图3-b)和炎症评分(结果见图3-c)。
74.在eap第1次诱导后第42天,分别检测eap igg和eap 抗ly6g小鼠在使用von frey纤维丝刺激临近前列腺的骨盆区域的痛觉反应频率,结果见图3-d。
75.由图3可知,抗ly6g治疗耗竭了外周循环血液的中性粒细胞,而不影响外周循环血液中的淋巴细胞和单核细胞(图3-a);与eap igg小鼠相比,eap 抗ly-6g处理小鼠的前列腺组织炎症性病理学改变显著减轻(图3b~3c);与eap igg小鼠相比,eap 抗ly-6g处理小鼠对vonfrey纤维丝刺激的痛觉反应程度也显著降低(图3d,p《0.05)。表明,中性粒细胞是eap发展的基础,减少中性粒细胞在前列腺组织的浸润可能成为eap的治疗策略之一。
76.实施例3
77.本实施例探究了褐藻糖胶对中性粒细胞在前列腺组织的浸润,前列腺炎症和痛觉过敏反应的影响:
78.1、实验动物选择:从南京模型动物研究中心购买了6~8周龄的雄性nod小鼠。所有小鼠均在特定的无病原体条件下饲养。
79.2、小鼠模型构建
80.对照组1:eap 生理盐水溶剂组
81.对照组2:eap 鼠重组il-17处理组
82.试验组1:eap 褐藻糖胶治疗组
83.试验组2:eap 鼠重组il-17 褐藻糖胶治疗组
84.eap小鼠模型采用实施例1中所述的诱导方式,在eap诱导后,第一次和第二次免疫后,对照组2和试验组2中eap小鼠每天腹腔注射重组小鼠il-17(ril-17,0.1mg/小鼠),持续1周。在eap诱导前一天,试验组1和试验组2中eap小鼠腹腔注射褐藻糖胶,剂量为20mg/kg体重,然后每周注射一次。在eap诱导前一天,对照组1中eap小鼠腹腔注射生理盐水,剂量为20mg/kg体重,然后每周注射一次。
85.用鼠重组il-17可增强中性粒细胞向前列腺组织的募集。
86.每组4只小鼠并进行了三个独立实验,数据为平均值
±
sem。
87.3、eap鼠的前列腺炎症检测
88.在eap第1次诱导后42天,通过流式细胞术分析各组前列腺组织中的ly6g
中性粒细胞,结果见图4-a、图4-b。
89.在eap第1次诱导后42天,通过mpo比色分析试剂盒分析各组前列腺组织的mpo活性,结果见图4-c。
90.在eap第1次诱导后42天,分别检测各组小鼠前列腺组织的代表性he染色图像(结果见图4-d)和炎症评分(结果见图4-e)。
91.在eap第1次诱导后第42天,分别检测各组小鼠在使用von frey纤维丝刺激临近前列腺的骨盆区域的痛觉反应频率,结果见图4-f。
92.四组前列腺组织中ly6g
细胞的百分比:eap 生理盐水溶剂组为5.92%
±
0.31%,eap 重组il-17组为7.45%
±
0.44%,eap 褐藻糖胶治疗组为4.50%
±
0.14%,eap 鼠重组il-17 褐藻糖胶治疗组为4.33%
±
0.67%。表明,褐藻糖胶治疗降低了前列腺组织中ly6g阳性中性粒细胞浸润的百分比(图4-a~4-b,p《0.05)。
93.四组前列腺组织中mpo活性为:eap 生理盐水溶剂组为1.90
±
0.24u/g前列腺组织,eap 重组il-17组为2.67
±
0.43u/g前列腺组织,eap 褐藻糖胶治疗组为0.26
±
0.18u/g前列腺组织,eap 鼠重组il-17 褐藻糖胶治疗组为0.61
±
0.32u/g前列腺组织。表明,褐藻糖胶治疗降低了前列腺组织中的mpo活性(图4-c,p《0.01)。
94.he染色结果显示,褐藻糖胶处理的eap小鼠前列腺组织的组织学外观减轻,前列腺间质内单核细胞浸润减少(图4-d~4-e,对照组1和试验组1分别为2.25
±
0.25vs 0.25
±
0.25,对照组2和试验组2分别为2.75
±
0.25vs0.50
±
0.29,p《0.01)。
95.慢性疼痛发展分析表明,与eap 生理盐水溶剂组(对照组1)相比,eap 褐藻糖胶组(试验组1)对von frey纤维丝刺激的的痛觉反应频率有所改善(p《0.05);与eap ril-17组(对照组2)相比,eap ril-17 褐藻糖胶组(试验组2)的对von frey纤维丝刺激的痛觉反应频率有所改善(p《0.05)。
96.由图4可知,褐藻糖胶能有效抑制前列腺组织内中性粒细胞浸润,可以减轻前列腺炎症和痛觉过敏反应。
97.以上所述仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。