1.本发明属于生物技术领域,具体涉及抑制结直肠癌增殖的新肿瘤标志物及新靶标发现与其应用,更具体涉及hsa_circ_0025367、hsa_circ_0087145、hsa_circ_0031408作为抑制结直肠癌增殖研究的新肿瘤标志物及新靶标与其应用。
背景技术:
2.结直肠癌(colorectal cancer,crc)是一种常见的消化道恶性肿瘤,与人类其他癌症相比,其发病率与死亡率逐年攀升,在全世界男性、女性中分别排名第3位及第2位,死亡病例在全世界男性、女性中分别排名第4位及第3位。相较于结直肠癌的严峻形势,目前结直肠癌的治疗仍然以手术切除为主,辅以放化疗以及中医药治疗,但效果并不理想,病人5年生存率仅为47.2%。近年来,靶向治疗越来越流行,已成为抗肿瘤治疗的主要手段之一,而靶向治疗也有一定的缺陷,基因调控网络复杂多样,靶向药的耐药现象是普遍存在的问题,一旦出现耐药情况,就要换新的靶向药物,虽然目前在包括结直肠癌在内的多种肿瘤中已有较多的作用靶标及其靶向药物,但是还远不能满足现有的临床治疗现状,因此发现新的分子靶标,阐明其发挥作用的分子机制,发展多样化的靶向药物,是目前基础科学与临床实践中的一大挑战。
3.过去人们对于癌症的治疗靶点主要聚焦于癌症进展过程中的关键蛋白质上。近年来,非编码rna作为肿瘤等疾病治疗的新靶标,新方法,变得越来越流行,越来越具有希望。大量的非编码rna已经被证实参与了肿瘤的发生发展过程,以反义寡核苷酸(asos)为例,多种核苷酸rna药物已进入临床的验证以及应用阶段。环状rna(circrna)是近年来发现的一种新型的长链非编码rna,因其结构稳定,序列保守,表达特异性等特点以及明确的生理学作用而有望成为新的癌症诊断标志物和治疗靶标。随着研究的深入,已有大量研究表明circrna在生物体的各项生命进程中发挥着极为关键的作用。而在结直肠癌进展过程,许多发挥关键作用的circrna其功能与作用机制还未被阐明,这显然不利于我们对结直肠癌疾病进展的理解,并基于此开发新的诊疗策略与手段。因此阐明结直肠癌生长过程中发挥关键作用的circrna的功能及其分子机制,基于此开发多样化的有效的诊断标志物及治疗靶点,对于我们更加合理和准确的诊断与治疗临床crc病人,具有积极的重要意义。
4.根据已公开发表的信息进行检索,人源基因环状rna hsa_circ_0025367;hsa_circ_0087145以及hsa_circ_0031408目前他们在人体中的功能与作用是完全未知的。
技术实现要素:
5.本发明要解决的技术问题是提供抑制结直肠癌增殖的靶标及其应用。
6.为解决上述技术问题,本发明提供hsa_circ_0025367、hsa_circ_0087145、hsa_circ_0031408在制备抑制结直肠癌增殖的药物中的应用。
7.本发明还同时提供了hsa_circ_0025367表达促进剂、hsa_circ_0087145表达促进剂、hsa_circ_0031408表达促进剂在制备抑制结直肠癌增殖的药物中的应用。
8.作为本发明应用的改进:抑制结直肠癌细胞体内增殖/体外增殖。
9.作为本发明应用的进一步改进:
10.所述hsa_circ_0025367表达促进剂为hsa_circ_0025367的过表达质粒;
11.所述hsa_circ_0087145表达促进剂为hsa_circ_0087145的过表达质粒;
12.所述hsa_circ_0031408表达促进剂为hsa_circ_0031408的过表达质粒。
13.作为本发明应用的进一步改进:
14.过表达hsa_circ_0025367能抑制结直肠癌细胞hct116、dld-1的体内外增殖能力;
15.过表达hsa_circ_0087145能抑制结直肠癌细胞sw480、sw620的体内外增殖能力;
16.过表达hsa_circ_0031408能抑制结直肠癌细胞hct116、sw620的体内外增殖能力。
17.本发明还同时提供了预防或/和治疗结直肠癌的组合物,组合物包含:
18.(1)hsa_circ_0025367的表达促进剂,或hsa_circ_0087145的表达促进剂,或hsa_circ_0031408的表达促进剂;
19.(2)药剂学上能够接受的载体。
20.作为本发明的预防或/和治疗结直肠癌的组合物的改进:
21.所述hsa_circ_0025367表达促进剂为hsa_circ_0025367的表达质粒;
22.所述hsa_circ_0087145表达促进剂为hsa_circ_0087145的表达质粒;
23.hsa_circ_0031408表达促进剂为hsa_circ_0031408的表达质粒。
24.本发明还提供了一种检测hsa_circ_0025367表达的试剂,所述hsa_circ_0025367表达的试剂包含基于荧光定量pcr定量检测方法的试剂,荧光定量pcr定量检测方法的试剂包含一对特异性引物,引物序列为:
25.hsa_circ_0025367forward primer 5
’‑
gatgtgactcaagcgactcca-3’;
26.hsa_circ_0025367reverse primer 5
’‑
actgagggaggccaagtcat-3’。
27.本发明还提供了一种检测hsa_circ_0087145表达的试剂,hsa_circ_0087145表达的试剂包含基于荧光定量pcr定量检测方法的试剂,荧光定量pcr定量检测方法的试剂包含一对特异性引物,引物序列为:
28.hsa_circ_0087145forward primer:5
’‑
ttcaatcgccgccctaa-3’;
29.hsa_circ_0087145reverse primer:5
’‑
ccttcagtcagcaaatccc-3’。
30.本发明还提供了一种检测hsa_circ_0031408表达的试剂,hsa_circ_0031408表达的试剂包含基于荧光定量pcr定量检测方法的试剂,荧光定量pcr定量检测方法的试剂包含一对特异性引物,
31.引物序列为:f(上游引物):5
’‑
gggagctgtccaagtcaaga-3’32.r(下游引物):5
’‑
attcgccttgacctccagttg-3’。
33.本发明所述的三个环状rna,hsa_circ_0025367的序列如seq id no:1所述,hsa_circ_0087145如seq id no:2所述,hsa_circ_0031408如seq id no:3所述。
34.本发明的目的之一:在于表明hsa_circ_0025367可以应用为结直肠癌的诊断标志物以及治疗靶标。
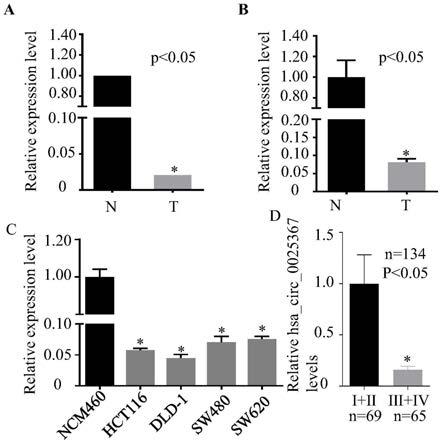
35.所采取的技术方案如下:通过对临床收集的配对的结直肠癌旁正常组织,原发灶癌组织进行转录组测序发现,相较于癌旁正常组织,hsa_circ_0025367在对配对的原发灶癌组织中表达显著下调(图1-1a),进一步采用rt-qpcr技术进行验证发现,结果与转录组结
果相一致(图1-1b)。检测了hsa_circ_0025367基因在细胞系中的表达情况,发现相较于正常结肠上皮细胞ncm460,hsa_circ_0025367在hct116等癌细胞系中表达显著下调(图1-1c)。并且hsa_circ_0025367的表达与crc病人的分期相关,中晚期病人hsa_circ_0025367的表达水平显著低于早期病人(图1-1d)。
36.更为关键的是,hsa_circ_0025367的表达与病人的预后相关。hsa_circ_0025367表达越高的病人,其总生存期和无病生存期均显著增加,即hsa_circ_0025367表达越高,病人预后相对越好(图1-2)。
37.成功构建hsa_circ_0025367过表达载体,建立hct116细胞和dld-1细胞稳转细胞株(图1-3a,图1-3d),通过soft agar与atp实验,发现过表达hsa_circ_0025367显著抑制了crc细胞的增殖能力(图1-3b~c,图1-3e~f)。
38.采取裸鼠皮下成瘤方式建立裸鼠异位移植瘤模型,观察hct116细胞在裸鼠皮下成瘤情况。研究发现,hsa_circ_0025367显著抑制了结直肠癌细胞hct116细胞的体内增殖能力(裸鼠皮下瘤生长体积,速度,重量显著降低)(图1-4a~d)。
39.本发明的目的之二:在于表明hsa_circ_0087145可以应用为结直肠癌的诊断标志物以及治疗靶标。
40.本发明所采取的技术方案如下:通过对临床收集的配对的结直肠癌旁正常组织,原发灶癌组织进行转录组测序发现,相较于癌旁正常组织,hsa_circ_0087145在对配对的原发灶癌组织中表达显著下调(图2-1a),进一步采用rt-qpcr技术进行验证发现,结果与转录组结果相一致(图2-1b)。检测了hsa_circ_0087145基因在细胞系中的表达情况,发现相较于正常结肠上皮细胞ncm460,hsa_circ_0087145在sw480等癌细胞系中表达显著下调(图1c)。并且hsa_circ_0087145的表达与crc病人的分期相关,中晚期病人hsa_circ_0087145的表达水平显著低于早期病人(图2-1d)。
41.更为关键的是,hsa_circ_0087145的表达与病人的预后相关。hsa_circ_0087145表达越高的病人,其总生存期和无病生存期均显著增加,即hsa_circ_0087145表达越高,病人预后相对越好(图2-2)。
42.成功构建hsa_circ_0087145过表达载体,建立sw480细胞和sw620细胞稳转细胞株(图2-3a,图2-3d),通过soft agar与atp实验,发现过表达hsa_circ_0087145显著抑制了crc细胞的增殖能力(图2-3b~c,图2-3e-f)。
43.采取裸鼠皮下成瘤方式建立裸鼠异位移植瘤模型,观察sw480细胞在裸鼠皮下成瘤情况。研究发现,hsa_circ_0087145显著抑制了结直肠癌细胞sw480细胞的体内增殖能力(裸鼠皮下瘤生长体积,速度,重量显著降低)(图2-4a~d)。
44.本发明的目的之三:在于表明hsa_circ_0031408可以应用为结直肠癌的诊断标志物以及治疗靶标。
45.本发明所采取的技术方案如下:通过对临床收集的配对的结直肠癌旁正常组织,原发灶癌组织进行转录组测序我们发现,相较于癌旁正常组织,hsa_circ_0031408在对配对的原发灶癌组织中表达显著下调(图3-1a),进一步采用rt-qpcr技术进行验证发现,结果与转录组结果相一致(图3-1b)。检测了hsa_circ_0031408基因在细胞系中的表达情况,发现相较于正常结肠上皮细胞ncm460,hsa_circ_0031408在hct116等癌细胞系中表达显著下调(图3-1c)。并且hsa_circ_0031408的表达与crc病人的分期相关,中晚期病人hsa_circ_
0031408的表达水平显著低于早期病人(图3-1d)。
46.更为关键的是,hsa_circ_0031408的表达与病人的预后相关。hsa_circ_0031408表达越高的病人,其总生存期和无病生存期均显著增加,即hsa_circ_0031408表达越高,病人预后相对越好(图3-2)。
47.成功构建hsa_circ_0031408过表达载体,建立hct116细胞和sw620细胞稳转细胞株(图3-3a,图3-3d),通过soft agar与atp实验,发现过表达hsa_circ_0031408显著抑制了crc细胞的增殖能力(图3-3b~c,图3-3e~f)。
48.采取裸鼠皮下成瘤方式建立裸鼠异位移植瘤模型,观察hct116细胞在裸鼠皮下成瘤情况。研究发现,hsa_circ_0031408显著抑制了结直肠癌细胞hct116细胞的体内增殖能力(裸鼠皮下瘤生长体积,速度,重量显著降低)(图3-4a~d)。
49.需要说明的是:目前,现有的抑制结直肠癌增殖和转移的靶标主要为her1(egfr/erbb1)、vegfr、braf、kras等,相关药物作用靶标主要为蛋白质;而本发明中的hsa_circ_0025367;hsa_circ_0087145以及hsa_circ_0031408为核酸靶点。
50.本发明的有益效果主要体现在:
51.1、通过转录组及rt-q-pcr等实验技术发现,相较于癌旁正常组织在癌组织中hsa_circ_0025367表达水平呈显著下调趋势,并且hsa_circ_0025367基因的表达高低与病人预后显著相关,表明hsa_circ_0025367可以作为结直肠癌增殖诊断标志物,并成为病人的预后指标之一。同时,本发明进一步以结直肠癌hct116、dld-1细胞为模型,过表达hsa_circ_0025367可显著抑制结直肠癌细胞hct116、dld-1的体内外增殖能力,表明hsa_circ_0025367可以作为抑制结直肠癌生长的潜在的治疗靶标。
52.2、通过转录组及rt-q-pcr等实验技术发现,相较于癌旁正常组织在癌组织中hsa_circ_0087145表达水平呈显著下调趋势,并且hsa_circ_0087145基因的表达高低与病人预后显著相关,表明hsa_circ_0087145可以作为结直肠癌增殖诊断标志物,并成为病人的预后指标之一。同时,本发明进一步以结直肠癌sw480、sw620细胞为模型,过表达hsa_circ_0087145可显著抑制结直肠癌细胞sw480、sw620的体内外增殖能力,表明hsa_circ_0087145可以作为抑制结直肠癌生长的潜在的治疗靶标。
53.3、通过转录组及rt-qpcr等实验技术发现,相较于癌旁正常组织在癌组织中hsa_circ_0031408表达水平呈显著下调趋势,并且hsa_circ_0031408基因的表达高低与病人预后显著相关,表明hsa_circ_0031408可以作为结直肠癌增殖诊断标志物,并成为病人的预后指标之一。同时,本发明进一步以结直肠癌hct116、sw620细胞为模型,过表达hsa_circ_0031408可显著抑制结直肠癌细胞hct116、sw620的体内外增殖能力,表明hsa_circ_0031408可以作为抑制结直肠癌生长的潜在的治疗靶标。
附图说明
54.下面结合附图对本发明的具体实施方式作进一步详细说明。
55.图1-1中:
56.图1-1a为通过转录组学高通量测序分析hsa_circ_0025367在结直肠癌相较于癌旁组织中转录水平的表达情况;图1-1b为hsa_circ_0025367在134对临床样本中转录水平表达情况;图1-1c为hsa_circ_0025367在细胞系中的表达情况。图1-1d为hsa_circ_
0025367蛋白在不同分期病人中的表达情况。
57.n代表癌旁正常组织;t代表癌组织。
58.图1-2为hsa_circ_0025367表达与病人预后的关系。
59.图1-3中:
60.图1-3a、图1-3d为在hct116与dld-1细胞中过表达hsa_circ_0025367后通过qpcr实验鉴定过表达效率;图1-3b、图1-3c为atp实验和softagar实验检测hsa_circ_0025367对crc细胞hct116增殖的影响;图1-3e、图1-3f为atp实验和soft agar实验检测hsa_circ_0025367对crc细胞dld-1增殖的影响。
61.图1-4为采取裸鼠皮下异位移植瘤模型验证hsa_circ_0025367对crc细胞增殖能力的影响;图1-4中:
62.图1-4a代表异源过表达hsa_circ_0025367后,对照组与实验组裸鼠皮下成瘤瘤体大小比较;图1-4b代表异源过表达hsa_circ_0025367后,对照组与实验组裸鼠皮下成瘤瘤体生长曲线;图1-4c代表异源过表达hsa_circ_0025367后,对照组与实验组裸鼠皮下成瘤瘤体重量称重;图1-4d代表异源过表达hsa_circ_0025367后,对照组与实验组裸鼠皮下成瘤瘤体rna提取验证hsa_circ_0025367是否在体内稳定过表达。
63.图2-1中:
64.图2-1a为通过转录组学高通量测序分析hsa_circ_0087145在结直肠癌相较于癌旁组织中转录水平的表达情况;图2-1b为hsa_circ_0087145在134对临床样本中转录水平表达情况;图2-1c为hsa_circ_0087145在细胞系中的表达情况;图2-1d为hsa_circ_0087145蛋白在不同分期病人中的表达情况。
65.n代表癌旁正常组织;t代表癌组织。
66.图2-2为hsa_circ_0087145表达与病人预后的关系。
67.图2-3中:
68.图2-3a,图2-3d为在sw480与sw620细胞中过表达hsa_circ_0087145后通过qpcr实验鉴定过表达效率;图2-3b~c为atp实验和softagar实验检测hsa_circ_0087145对crc细胞sw480增殖的影响;图2-3e~f为atp实验和soft agar实验检测hsa_circ_0087145对crc细胞sw620增殖的影响。
69.图2-4为采取裸鼠皮下异位移植瘤模型验证hsa_circ_0087145对crc细胞增殖能力的影响;图2-4中:
70.图2-4a代表异源过表达hsa_circ_0087145后,对照组与实验组裸鼠皮下成瘤瘤体大小比较;图2-4b代表异源过表达hsa_circ_0087145后,对照组与实验组裸鼠皮下成瘤瘤体生长曲线;图2-4c代表异源过表达hsa_circ_0087145后,对照组与实验组裸鼠皮下成瘤瘤体重量称重;图2-4d代表异源过表达hsa_circ_0087145后,对照组与实验组裸鼠皮下成瘤瘤体rna提取验证hsa_circ_0025367是否在体内稳定过表达。
71.图3-1中:
72.图3-1a为通过转录组学高通量测序分析hsa_circ_0031408在结直肠癌相较于癌旁组织中转录水平的表达情况;图3-1b为hsa_circ_0031408在134对临床样本中转录水平表达情况;图3-1c为hsa_circ_0031408在细胞系中的表达情况。图3-1d为hsa_circ_0031408蛋白在不同分期病人中的表达情况。
73.n代表癌旁正常组织;t代表癌组织。
74.图3-2为hsa_circ_0031408表达与病人预后的关系。
75.图3-3中:
76.图3-3a,图3-3d为在hct116与sw620细胞中过表达hsa_circ_0031408后通过qpcr实验鉴定过表达效率;图3-3b~c为atp实验和softagar实验检测hsa_circ_0031408对crc细胞hct116增殖的影响;图3-3e~f为atp实验和soft agar实验检测hsa_circ_0031408对crc细胞sw620增殖的影响。
77.图3-4为采取裸鼠皮下异位移植瘤模型验证hsa_circ_0031408对crc细胞增殖能力的影响;图3-4中:
78.图3-4a代表异源过表达hsa_circ_0031408后,对照组与实验组裸鼠皮下成瘤瘤体大小比较;图3-4b代表异源过表达hsa_circ_0031408后,对照组与实验组裸鼠皮下成瘤瘤体生长曲线;图3-4c代表异源过表达hsa_circ_0031408后,对照组与实验组裸鼠皮下成瘤瘤体重量称重;图3-4d代表异源过表达hsa_circ_0031408后,对照组与实验组裸鼠皮下成瘤瘤体rna提取验证hsa_circ_0031408是否在体内稳定过表达。
具体实施方式
79.下面结合具体实施例对本发明进行进一步描述,但本发明的保护范围并不仅限于此:
80.实施例一.1
81.通过转录组学手段,发现在临床样本中hsa_circ_0025367在癌组织中表达显著低于癌旁正常组织(图1-1a)。q-pcr检测了临床样本(图1-1b)以及在细胞系中hsa_circ_0025367的表达情况进一步验证了这一点(图1-1c)。同时q-pcr发现hsa_circ_0025367的表达与病人分期相关(图1-1d)。
82.具体如下:
83.1)组织样本
84.临床组织样本由温州医科大学附属第一医院采集,样本采集与利用已通过温州医科大学附属第一医院伦理委员会的伦理批准,严格按照相关制度与流程进行采集与利用。采集到样本后,一部分组织采取液氮速冻的方式保存于液氮罐中,一部分组织立即用4%的pfa固定24h-48h,具体处理流程如下:
85.a.组织脱水:组织经4%pfa固定后,流水过夜冲洗组织,除去残余的pfa固定液。之后按照30%酒精1h
→
50%酒精1h
→
70%酒精4℃过夜
→
80%酒精1h
→
90%酒精1h
→
95%酒精1h
→
100%酒精1h的顺序将组织梯度脱水。
86.b.组织透明:组织经梯度脱水后,将组织置入50%无水乙醇与50%二甲苯的混合液玻璃缸中5min,之后将组织转入二甲苯中5min。
87.c.组织浸蜡:组织透明后,将组织浸入软蜡中1h,之后浸入硬蜡中1h。
88.d.组织包埋:将组织从塑料包埋盒中取出,放入金属包埋盒中,将塑料包埋盒掩于其上,滴加适量的硬蜡,使硬蜡充分包裹塑料包埋盒,待硬蜡微凝固后将蜡块继续转入冰盒中,使蜡块与金属包埋盒脱离,取出蜡块,常温或4℃长期保存。
89.2)组织总rna提取
90.a.从超低温冰箱中取出步骤1)所得的结直肠癌临床样本,每个样本取样约50mg于ep管中,加入700μl的qiazol混匀,组织需要剪碎并用组织破碎仪充分破碎。
91.b.加入200μl的氯仿,剧烈震荡15s,冰上静置5min。提前预冷离心机至4℃。4℃离心,12000g,15min。
92.c.用200μl的去酶枪头吸取上清,移至新的ep管中,约400μl。加入等体积的400μl异丙醇,颠倒混匀,冰上静置10min。4℃离心,12000g,10min,弃去上清。
93.d.用depc水配制75%酒精,向上述沉淀中加入1ml配置好的75%酒精,吹打沉淀,4℃离心,12000g,5min,弃去上清,重复此步骤。
94.e.弃去上清后空离5min,用去酶小枪头吸取残留上清,留底部白色沉淀。开盖晾干,待底部白色沉淀透明后加入去酶水。4℃溶解2h,测定rna浓度,rna浓度为:癌旁正常组织:1777ug/ml;癌组织:2146ug/ml。
95.3)rt-qpcr
96.依照步骤2)提取并测定完成rna浓度后,使用购买于invitrogen公司的superscript
tm
iv逆转录试剂盒进行逆转录,根据试剂说明书逆转录反应体系及步骤如下:
[0097][0098]
按照说明书将各组分加入到pcr管中,振荡混匀,点离pcr管,之后将其置于pcr仪,设置pcr仪第一步反应程序:65℃,5min。反应完成后,冰上静置大于1min,加入如下表体系(rt反应体系)各组分进行第二步pcr反应。
[0099][0100]
上按照说明书将各组分加入到pcr管中,振荡混匀,点离pcr管,之后将其置于pcr仪,设置pcr仪第二步反应程序:50~55℃10min,80℃10min。得到cdna后,封口膜密封-80℃保存或完成下一步实验后再进行保存处理。将所需细胞获得cdna后,利用qiagen所购试剂盒进行pcr,pcr反应体系如下(4℃操作):
vector分别进行如下实验:
[0118]
1)采用atp实验检测肿瘤细胞生长活力变化
[0119]
具体步骤如下:用0.25%胰酶消化处于对数生长期的细胞,用培养基吹打成为单细胞悬液,计数后取相应悬液体积的细胞加入相应细胞数至96孔板中。细胞贴壁后从培养箱取出相应细胞,显微镜下观察状态。从-20℃取出atp检测试剂,室温溶解。甩去96孔板中的旧培养基,每孔加25μl的pbs,再加入每孔25μl的atp检测试剂,避光操作。避光,振荡器上震荡3min,室温静置10min。将96孔板中的西细胞裂解产物转移至避光板,每孔加40μl。上机检测。
[0120]
检测结果如图1-3b,图1-3e,随着时间的延长,实验组相对于对照组细胞的增殖活性逐渐降低。
[0121]
2)采用软琼脂克隆形成(soft agar)实验评价肿瘤细胞增殖能力
[0122]
hct116-hsa_circ_0025367、dld-1-hsa_circ_0025367相较于对照hct116-vector、dld-1-vector细胞锚定非依赖的恶性增殖能力。
[0123]
具体步骤如下:
[0124]
按照每孔取1.2ml的1.25%琼脂糖溶液与1.8ml配制的培养基(即:medium)于15ml离心管中,轻轻吹打混匀后加入6孔板的孔中,避免吹打出气泡,铺板要平而均匀,避免产生气泡。静置至少2h后,按照如下体系铺上层胶:
[0125][0126]
先将1.25%的琼脂糖凝胶与2
×
细胞培养基混匀后放入42℃水浴锅中预热,然后用0.25%胰酶消化处于对数生长期的细胞,用培养基吹打成为单细胞悬液,计数后取相应悬液体积的细胞加入相应细胞数至1.25%的琼脂糖凝胶与2
×
细胞培养基中,铺板。静置1-2小时后,用封口膜密封6孔板,之后放入37℃5%二氧化碳细胞培养箱中继续培养,7天左右开始观察克隆生长状态,待到克隆生长至合适大小时(为第10天),采用显微镜5倍镜拍照并计数,计算细胞集落数形成率(图1-3c,图1-3f)。
[0127]
所得结果为:hsa_circ_0025367显著抑制了结直肠癌细胞的体外增殖能力。根据该结果,可得知:hsa_circ_0025367可以作为结直肠癌的治疗靶标。
[0128]
实施例一.4
[0129]
过表达hsa_circ_0025367显著抑制结直肠癌细胞的体内增殖能力
[0130]
1)动物饲养
[0131]
balb/c-nu雌性裸鼠,周龄为3-4周,体重15
±
0.5克,实验动物由江苏集萃药康生物科技有限公司购入,并饲养于温州医科大学实验动物中心spf级实验区域。所进行动物实验的开展已通过温州医科大学实验动物伦理委员会的批准且实验过程符合伦理委员会的动物伦理要求。
[0132]
2)皮下注射
[0133]
0.25%胰酶消化处于对数生长期的hct116-vector细胞、hct116-hsa_circ_
0025367细胞,用培养基终止消化,将所有培养皿的细胞收集至50ml离心管中,1500rpm离心5min,之后弃去上清培养基,用pbs重悬细胞洗一次,再次1500rpm离心5min后弃去pbs,加入1ml pbs重悬,按照一定比例稀释细胞后充池计数,计算所需细胞量。每只裸鼠皮下注射100μl细胞悬液,其中包含300万细胞量。裸鼠皮下注射部位用75%酒精擦拭消毒处理,接种前将细胞充分混匀,用1ml无菌胰岛素注射器吸取100ul细胞悬液,均匀注射于小鼠右背部皮下位置,每组注射6只裸鼠。
[0134]
3)测定拍照
[0135]
1周左右pbs被裸鼠充分吸收,肿瘤细胞初步成瘤,此时用游标卡尺测肿瘤大小计算肿瘤体积(肿瘤体积v=0.52
×
(a
×
b2);待裸鼠接种肿瘤细胞生长4周左右时,用0.5%戊巴比妥钠麻醉裸鼠后处死,解剖取出瘤体,拍照并将瘤体称重(图1-4a~d)。
[0136]
所得结果为:hsa_circ_0025367显著抑制了结直肠癌细胞的体内增殖能力。根据该结果,可得知:在实施例一.3所得结论的基础上,进一步证实hsa_circ_0025367可以作为结直肠癌的治疗靶标。
[0137]
实施例二.1
[0138]
通过转录组学手段,发现在临床样本中hsa_circ_0087145在癌组织中表达显著低于癌旁正常组织(图2-1a)。q-pcr检测了临床样本(图2-1b)以及在细胞系中hsa_circ_0087145的表达情况进一步验证了这一点(图2-1c)。同时q-pcr发现hsa_circ_0087145的表达与病人分期相关(图2-1d)。
[0139]
1)、组织样本:等同于实施例一.1;
[0140]
2)、组织总rna提取:等同于实施例一.1;
[0141]
3)、rt-qpcr
[0142]
引物为:
[0143]
hsa_circ_0087145forward primer:5
’‑
ttcaatcgccgccctaa-3’;
[0144]
hsa_circ_0087145reverse primer:5
’‑
ccttcagtcagcaaatccc-3’;
[0145]
内参gapdh forward primer:5
’‑
ggagcgagatccctccaaaat-3’;
[0146]
内参gapdh reverse primer5
’‑
ggctgttgtcatacttctcatgg-3’;
[0147]
其余等同于实施例一.1。
[0148]
所得结果为:hsa_circ_0087145在结直肠癌组织与细胞(癌细胞系:hct116,dld-1,sw480,sw620)中表达显著低于正常组织与细胞(正常细胞系:ncm460)(图2-1b,c)。相较于早期(ⅰ期和ⅱ期)结直肠癌,hsa_circ_0087145在中晚期(ⅲ期和ⅳ期)结直肠癌中表达下降(图2-1d)。因此,可得知:hsa_circ_0087145可以作为结直肠癌的诊断标志物。
[0149]
实施例二.2
[0150]
hsa_circ_0087145高表达的患者预后要明显好hsa_circ_0087145低表达的患者(图2-2)整理预后相关临床信息,包括绘制生存曲线横坐标所需的病人的总生存时间(overall survival,os)、纵坐标生存率所需的生存状态(os status)。将hsa_circ_0087145的rna分别按照肿瘤组的表达水平将样本分为两组:高表达和低表达,并进行log-rank统计检验,设定p《0.05为统计学显著性阈值。分析hsa_circ_0087145与患者预后的关系并绘制k-m生存曲线。
[0151]
所得结果为:hsa_circ_0087145表达与结直肠癌病人的预后相关,hsa_circ_
0087145表达越低,结直肠癌病人的预后越差。根据该结果,可得知:hsa_circ_0087145可以作为结直肠癌的预后标志物。
[0152]
实施例二.3
[0153]
hsa_circ_0087145显著抑制结直肠癌细胞的体外增殖能力(图2-3的a~f)
[0154]
选用sw480细胞与sw620细胞,并采用常规质粒plenti-cmv-circrna-ef1-gfp-puro质粒在sw480与sw620细胞中过表达hsa_circ_0087145,建立稳定转染细胞sw480-hsa_circ_0087145,sw620-hsa_circ_0087145及其对照sw480-vector,sw620-vector,q-pcr实验验证过表达效率(图2-3a,3d)。
[0155]
说明:上述sw480-hsa_circ_0087145,sw620-hsa_circ_0087145参照本行业常规的质粒构建与合成方法,能轻易制备获得。
[0156]
sw480-hsa_circ_0087145,sw620-hsa_circ_0087145及其对照sw480-vector,sw620-vector分别进行如下实验:
[0157]
1)采用atp实验检测肿瘤细胞生长活力变化:
[0158]
实验步骤同实施例一.3;
[0159]
检测结果如图2-3b、图2-3e;随着时间的延长,实验组相对于对照组细胞的增殖活性逐渐降低。
[0160]
2)、采用软琼脂克隆形成(soft agar)实验评价肿瘤细胞增殖能力
[0161]
sw480-hsa_circ_0087145、sw620-hsa_circ_0087145相较于对照sw480-vector、sw620-vector细胞锚定非依赖的恶性增殖能力。实验方法参照实施例一.3。
[0162]
计算所得的细胞集落数形成率,如图2-3c,图2-3f。
[0163]
所得结果为:hsa_circ_0087145显著抑制了结直肠癌细胞的体外增殖能力。根据该结果,可得知:hsa_circ_0087145可以作为结直肠癌的治疗靶标。
[0164]
实施例二.4
[0165]
过表达hsa_circ_0087145显著抑制结直肠癌细胞的体内增殖能力
[0166]
1)动物饲养
[0167]
同实施例一.4。
[0168]
2)皮下注射
[0169]
0.25%胰酶消化处于对数生长期的sw480-vector细胞、sw480-hsa_circ_0087145细胞,每组注射5只裸鼠。其余同实施例一.4。
[0170]
3)测定拍照
[0171]
同实施例一.4。
[0172]
所得结果如图2-4a~d。
[0173]
所得结果为:hsa_circ_0087145显著抑制了结直肠癌细胞的体内增殖能力。根据该结果,可得知:在实施例二.3所得结论的基础上,进一步证实hsa_circ_0087145可以作为结直肠癌的治疗靶标。
[0174]
实施例三.1
[0175]
通过转录组学手段,发现在临床样本中hsa_circ_0031408在癌组织中表达显著低于癌旁正常组织(图3-1a)。q-pcr检测了临床样本(图3-1b)以及在细胞系中hsa_circ_0031408的表达情况进一步验证了这一点(图3-1c)。同时q-pcr发现hsa_circ_0031408的表
达与病人分期相关(图3-1d)。
[0176]
1)、组织样本:等同于实施例一.1;
[0177]
2)、组织总rna提取:等同于实施例一.1;
[0178]
3)、rt-qpcr
[0179]
引物为:
[0180]
hsa_circ_0031408forward primer5
’‑
gggagctgtccaagtcaaga-3’;
[0181]
hsa_circ_0031408reverse primer5
’‑
attcgccttgacctccagttg-3’;
[0182]
内参gapdh forward primer:5
’‑
ggagcgagatccctccaaaat-3’;
[0183]
内参gapdh reverse primer5
’‑
ggctgttgtcatacttctcatgg-3’;
[0184]
等同于实施例一.1。
[0185]
所得结果为:hsa_circ_0031408在结直肠癌组织与细胞(癌细胞系:hct116,dld-1,sw480,sw620)中表达显著低于正常组织与细胞(正常细胞系:ncm460)(图3-1b,c)。相较于早期(ⅰ期和ⅱ期)结直肠癌,hsa_circ_0031408在中晚期(ⅲ期和ⅳ期)结直肠癌中表达下降(图3-1d)。因此,可得知:hsa_circ_0031408可以作为结直肠癌的诊断标志物。
[0186]
实施例三.2
[0187]
hsa_circ_0031408高表达的患者预后要明显好hsa_circ_0031408低表达的患者(图3-2)整理预后相关临床信息,包括绘制生存曲线横坐标所需的病人的总生存时间(overall survival,os)、纵坐标生存率所需的生存状态(os status)。我们将hsa_circ_0031408的rna分别按照肿瘤组的表达水平将样本分为两组:高表达和低表达,并进行log-rank统计检验,设定p《0.05为统计学显著性阈值。分析hsa_circ_0031408与患者预后的关系并绘制k-m生存曲线。
[0188]
所得结果为:hsa_circ_0031408表达与结直肠癌病人的预后相关,hsa_circ_0031408表达越低,结直肠癌病人的预后越差。根据该结果,可得知:hsa_circ_0031408可以作为结直肠癌的预后标志物。
[0189]
实施例三.3
[0190]
hsa_circ_0031408显著抑制结直肠癌细胞的体外增殖能力(图3-3的a~f)
[0191]
选用hct116细胞与sw620细胞,并采用常规质粒plenti-cmv-circrna-ef1-gfp-puro质粒在hct116与sw620细胞中过表达hsa_circ_0031408,建立稳定转染细胞hct116-hsa_circ_0031408,sw620-hsa_circ_0031408及其对照hct116-vector,sw620-vector,q-pcr实验验证过表达效率(图3-3a,图3-3d)。
[0192]
说明:上述hct116-hsa_circ_0031408,sw620-hsa_circ_0031408参照本行业常规的质粒构建与合成方法,能轻易制备获得。
[0193]
hct116-hsa_circ_0031408,sw620-hsa_circ_0031408及其对照hct116-vector,sw620-vector,分别进行如下实验:
[0194]
1)、采用atp实验检测肿瘤细胞生长活力变化
[0195]
实验步骤同实施例一.3;
[0196]
检测结果如图3-3b、图3-3e;随着时间的延长,实验组相对于对照组细胞的增殖活性逐渐降低。
[0197]
2)、采用软琼脂克隆形成(soft agar)实验评价肿瘤细胞增殖能力
[0198]
hct116-hsa_circ_0031408、sw620-hsa_circ_0031408相较于对照hct116-vector、sw620-vector细胞锚定非依赖的恶性增殖能力。
[0199]
实验方法参照实施例一.3。
[0200]
计算所得的细胞集落数形成率,如图3-3c,图3-f。
[0201]
所得结果为:hsa_circ_0031408显著抑制了结直肠癌细胞的体外增殖能力。根据该结果,可得知:hsa_circ_0031408可以作为结直肠癌的治疗靶标。
[0202]
实施例三.4
[0203]
过表达hsa_circ_0031408显著抑制结直肠癌细胞的体内增殖能力
[0204]
1)动物饲养
[0205]
同实施例一.4。
[0206]
2)皮下注射
[0207]
0.25%胰酶消化处于对数生长期的hct116-vector细胞、hct116-hsa_circ_0031408细胞,其余同实施例一.4。
[0208]
3)测定拍照
[0209]
同实施例一.4。
[0210]
所得结果如图3-4a~d。
[0211]
所得结果为:hsa_circ_0031408显著抑制了结直肠癌细胞的体内增殖能力。根据该结果,可得知:在实施案例三所得结论的基础上,进一步证实hsa_circ_0031408可以作为结直肠癌的治疗靶标。
[0212]
最后,还需要注意的是,以上列举的仅是本发明的若干个具体实施例。显然,本发明不限于以上实施例,还可以有许多变形。本领域的普通技术人员能从本发明公开的内容直接导出或联想到的所有变形,均应认为是本发明的保护范围。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。