1.本发明涉及生物医药技术领域,具体涉及一种复合纳米药物载体及其制备方法和应用,特别是一种多聚唾液酸(psa)修饰的玉米醇溶蛋白纳米药物载体及其载药体系,特别是肿瘤靶向给药体系,以及二者的制备方法和应用。
背景技术:
2.随着社会经济发展和人民生活水平提高,受到饮食结构改变以及人口老龄化、城市化等因素的影响,世界范围内疾病谱和死亡谱发生显著变化,慢性非传染性疾病已经成为导致死亡的主要原因。其中,恶性肿瘤是目前全世界的主要死亡原因之一,已经成为严重危害人类生命健康、制约社会经济发展的一大类疾病。
3.化疗是目前肿瘤治疗中最常用的手段,化疗很大程度上取决于所施用的化学治疗剂是否可以安全有效地到达肿瘤部位,然而,这些化学治疗剂中的许多由于其在肿瘤部位的低浓度和对癌细胞和健康细胞两者的类似细胞毒性而经常导致疗效不佳和严重的副作用。
4.解决这些问题的方法之一是将化学治疗剂引入纳米药物载体中,所得载药体系可以持续释放药物,改善药代动力学分布,并通过通透性增强与滞留性(epr)而提高肿瘤积累。然而,药物的疗效仍然受到药物载体的一些限制,例如化学治疗剂的渗漏,res器官对化学治疗剂的摄取,通过epr效应纳米药物在肿瘤部位中渗透和积累不足。因此,迫切需要新的药物载体来解决这些问题。
技术实现要素:
5.为克服现有技术的不足,本发明提供一种psa修饰的玉米醇溶蛋白纳米药物载体及其载药体系,特别是肿瘤靶向给药体系,以及二者的制备方法和应用。
6.在本发明第一方面,提供一种具有核壳结构的纳米颗粒,其具有核心颗粒和包覆在核心颗粒外表面的包覆层,其中,核心颗粒包含玉米醇溶蛋白,包覆层包含psa。
7.在本发明的一个实施方式中,核心颗粒由玉米醇溶蛋白形成。
8.在本发明的一个实施方式中,包覆层由psa形成。
9.具体地,psa的平均分子量为5000-120000da(例如5000、10000、20000、40000、50000、60000、70000、80000、90000、100000、110000、120000da),特别是50000-80000da;在本发明的一些实施例中,psa的平均分子量为80000da。
10.具体地,该纳米颗粒的粒径可以为100-200nm(例如100、105、110、115、120、130、140、150、160、170、180、190、200nm),特别是100-120nm。
11.具体地,该纳米颗粒中包覆层的厚度可以为1-100nm(例如1、5、10、12、14、15、16、18、20、22、24、25、26、28、30、40、50、60、70、80、90、100nm),特别是10-30nm。
12.具体地,该纳米颗粒中核心颗粒的粒径可以为50-100nm(例如50、60、70、80、85、86、88、90、92、94、96、98、100nm),特别是85-95nm。
13.具体地,该纳米颗粒呈球形。
14.具体地,该纳米颗粒带负电荷。
15.在本发明第二方面,提供第一方面所述的纳米颗粒的制备方法,其包括如下步骤:
16.(1)形成核心颗粒;
17.(2)形成包覆层;
18.任选地,(3)除杂。
19.具体地,核心颗粒通过反溶剂沉淀法形成。
20.更具体地,步骤(1)包括:将玉米醇溶蛋白溶于乙醇水溶液中,调节ph至酸性,除去乙醇。
21.具体地,该乙醇水溶液可以为75-95%(v/v)乙醇水溶液,特别是85%乙醇水溶液。
22.具体地,调节ph至酸性为调节ph至4.5-6.5(例如4.5、5、5.2、5.5、5.7、6、6.5)。
23.具体地,调节ph至酸性所用试剂为无机酸溶液,例如盐酸溶液。
24.具体地,步骤(1)还包括搅拌步骤;更具体地,搅拌速度可以为500-5000rpm(例如500、1000、2000、3000、4000、5000rpm),搅拌时间可以为10-60分钟(例如10、20、30、40、50、60分钟)。
25.具体地,在调节ph至酸性后,步骤(1)还可以包括加入表面活性剂溶液的步骤。
26.具体地,上述表面活性剂可以为非离子型表面活性剂,例如吐温,特别是吐温80。
27.具体地,上述表面活性剂溶液的ph为酸性,例如ph 3.5-4。
28.具体地,上述表面活性剂溶液的浓度为0.01-1%(例如0.01%、0.05%、0.1%、0.2%、0.3%、0.4%、0.5%、1%),特别是0.01-0.1%。
29.在本发明的一个实施方式中,步骤(1)包括:将玉米醇溶蛋白溶于乙醇水溶液中,搅拌,调节ph至酸性,搅拌所得溶液,并加入表面活性剂,除去乙醇。
30.具体地,步骤(2)包括:将步骤(1)所得核心颗粒的分散体加入psa溶液中。
31.具体地,psa溶液的ph为酸性,例如为ph 2-6(例如2、3、4、5、6),ph 4。
32.具体地,psa溶液的浓度可以为0.05-10%(w/v)(例如0.01%、0.05%、0.075%、0.1%、0.2%、0.25%、0.4%、0.5%、0.6%、0.8%、1%、2.5%、5%、7.5%、10%),特别是0.1-1%,更特别是0.1-0.25%;在本发明的一些实施例中,psa溶液的浓度为0.1%。
33.具体地,psa的平均分子量为5000-120000da(例如5000、10000、20000、40000、50000、60000、70000、80000、90000、100000、110000、120000da),特别是50000-80000da;在本发明的一些实施例中,psa的平均分子量为80000da。
34.在本发明的一个实施例中,psa溶液的浓度为0.1%,其中psa的平均分子量为80000da。
35.具体地,步骤(2)还包括搅拌步骤;更具体地,搅拌速度可以为500-5000rpm(例如500、1000、2000、3000、4000、5000rpm),搅拌时间可以为0.5-5小时(例如0.5、1、2、3、4、5小时)。
36.具体地,步骤(3)可以包括:将步骤(2)所得体系离心,以除去杂质。
37.在本发明第三方面,提供第一方面所述的纳米颗粒在作为药物载体和制备药物中的应用。
38.在本发明第四方面,提供一种载药体系,其具有缓释和靶向性能,其为纳米颗粒,
该纳米颗粒具有核心颗粒和包覆在核心颗粒外表面的包覆层,其中,核心颗粒包含玉米醇溶蛋白,包覆层包含psa,并且,核心颗粒负载有一种或多种活性成分。
39.在本发明的一个实施方式中,核心颗粒由玉米醇溶蛋白和活性成分形成。
40.在本发明的一个实施方式中,包覆层由psa形成。
41.具体地,psa的平均分子量为5000-120000da(例如5000、10000、20000、40000、50000、60000、70000、80000、90000、100000、110000、120000da),特别是50000-80000da;优选地,psa的平均分子量为80000da。
42.具体地,该纳米颗粒的粒径可以为100-200nm(例如100、105、110、115、120、130、140、150、160、170、180、190、200nm),特别是100-120nm。
43.具体地,该纳米颗粒中包覆层的厚度可以为1-100nm(例如1、5、10、12、14、15、16、18、20、22、24、25、26、28、30、40、50、60、70、80、90、100nm),特别是10-30nm。
44.具体地,该纳米颗粒中核心颗粒的粒径可以为50-100nm(例如50、60、70、80、85、86、88、90、92、94、96、98、100nm),特别是85-95nm。
45.具体地,该纳米颗粒呈球形。
46.具体地,该纳米颗粒带负电荷。
47.在本发明的一个实施方式中,上述活性成分为药学活性成分,特别是抗肿瘤药物,例如,多柔比星、表柔比星、吡柔比星、伊达比星;米托蒽醌;拓扑替康、伊立替康、依喜替康、氨基喜树碱;紫杉醇、多西他赛;吉非替尼、伊马替尼、尼罗替尼、舒尼替尼、拉帕替尼、托法替尼、克里唑替尼、马赛替尼、恩曲替尼、依鲁替尼、阿法替尼、氟马替尼、厄洛替尼、来那替尼、艾乐替尼、阿帕替尼、talazoparib、lorlatinib、tpx-0005;顺铂、卡铂、奈达铂、环铂、奥沙利铂、洛铂;长春花碱、长春新碱、长春瑞滨、小檗碱、小檗胺;和厚朴酚(hnk);尿嘧啶氮芥、氮芥、异环磷酰胺、美法仑、苯丁酸氮芥、哌泊溴烷、曲他胺、三亚乙基硫代磷酰胺、白消安、卡莫司汀、洛莫司汀、链佐星、达卡巴嗪、氟脲嘧啶脱氧核苷、阿糖胞苷、6-巯嘌呤、6-硫鸟嘌呤、磷酸氟达拉滨;等等。
48.具体地,在核心颗粒中,玉米醇溶蛋白和活性成分的重量比可以为1:1至100:1(例如1:1、5:1、10:1、15:1、20:1、30:1、40:1、50:1、60:1、70:1、80:1、90:1、100:1),特别是5:1至20:1。
49.在本发明的一个实施例中,该活性成分为hnk;更具体地,在核心颗粒中,玉米醇溶蛋白和hnk的重量比为10:1。
50.在本发明第五方面,提供第四方面所述的载药体系的制备方法,其包括如下步骤:
51.(1)形成核心颗粒;
52.(2)形成包覆层;
53.任选地,(3)除杂。
54.具体地,核心颗粒通过反溶剂沉淀法形成。
55.更具体地,步骤(1)包括:将玉米醇溶蛋白与活性成分(分别或一起)溶于乙醇水溶液中,调节ph至酸性,除去乙醇。
56.具体地,该乙醇水溶液可以为75-95%(v/v)乙醇水溶液,特别是85%乙醇水溶液。
57.具体地,调节ph至酸性为调节ph至4.5-6.5(例如4.5、5、5.2、5.5、5.7、6、6.5)。
58.具体地,调节ph至酸性所用试剂为无机酸溶液,例如盐酸溶液。
59.具体地,步骤(1)还包括搅拌步骤;更具体地,搅拌速度可以为500-5000rpm(例如500、1000、2000、3000、4000、5000rpm),搅拌时间可以为10-60分钟(例如10、20、30、40、50、60分钟)。
60.具体地,在调节ph至酸性后,步骤(1)还可以包括加入表面活性剂溶液的步骤。
61.具体地,上述表面活性剂可以为非离子型表面活性剂,例如吐温,特别是吐温80。
62.具体地,上述表面活性剂溶液的ph为酸性,例如ph 3.5-4。
63.具体地,上述表面活性剂溶液的浓度为0.01-1%(例如0.01%、0.05%、0.1%、0.2%、0.3%、0.4%、0.5%、1%),特别是0.01-0.1%。
64.在本发明的一个实施方式中,步骤(1)包括:将玉米醇溶蛋白与活性成分(例如hnk)溶于乙醇水溶液中,搅拌,调节ph至酸性,搅拌所得溶液,并加入表面活性剂,除去乙醇。
65.具体地,步骤(2)包括:将步骤(1)所得核心颗粒的分散体加入psa溶液中。
66.具体地,psa溶液的ph为酸性,例如为ph 2-6(例如2、3、4、5、6),ph 4。
67.具体地,psa溶液的浓度可以为0.05-10%(w/v)(例如0.01%、0.05%、0.075%、0.1%、0.15%、0.2%、0.25%、0.4%、0.5%、0.6%、0.8%、1%、2.5%、5%、7.5%、10%),特别是0.1-1%,更特别是0.1-0.25%;在本发明的一些实施例中,psa溶液的浓度为0.1%。
68.具体地,psa的平均分子量为5000-120000da(例如5000、10000、20000、40000、50000、60000、70000、80000、90000、100000、110000、120000da),特别是50000-80000da;在本发明的一些实施例中,psa的平均分子量为80000da。
69.在本发明的一个实施例中,psa溶液的浓度为0.1%,其中psa的平均分子量为80000da。
70.具体地,步骤(2)还包括搅拌步骤;更具体地,搅拌速度可以为500-5000rpm(例如500、1000、2000、3000、4000、5000rpm),搅拌时间可以为0.5-5小时(例如0.5、1、2、3、4、5小时)。
71.具体地,步骤(3)可以包括:将步骤(2)所得体系离心,以除去未包封的活性成分等杂质。
72.在本发明第六方面,提供第四方面所述的载药体系在制备预防和/或治疗疾病的药物中的应用。
73.具体地,所述疾病可以为肿瘤、自身免疫疾病、感染性疾病等,特别是肿瘤。
74.具体地,上述肿瘤为恶性肿瘤,其包括但不限于:膀胱癌、乳腺癌、结肠直肠癌、肾癌、肝癌、肺癌(包括小细胞肺癌、非小细胞肺癌)、头和颈癌、食管癌、胆囊癌、卵巢癌、胰腺癌、胃癌、子宫颈癌、甲状腺癌、前列腺癌、皮肤癌、b细胞性慢性淋巴细胞白血病、急性淋巴细胞性白血病、非霍奇金淋巴瘤、霍奇金淋巴瘤、急性髓性白血病、弥漫性大b细胞淋巴瘤、多发性骨髓瘤等(包括原发性肿瘤和转移性肿瘤);特别是乳腺癌,包括原发性乳腺癌和转移性乳腺癌。
75.在本发明第七方面,提供一种药物组合物,其包含第四方面所述的载药体系,以及一种或多种药学上可接受的辅料。
76.具体地,所述药学上可接受的载体是指药学领域常规的药物载体,特别是药学上可接受的注射剂辅料,例如等渗的无菌盐溶液(磷酸二氢钠、磷酸氢二钠、氯化钠、氯化钾、
氯化钙、氯化镁等,或上述盐的混合物),或干燥的例如是冷冻干燥的组合物,其适当地通过加入无菌水或生理盐水形成可注射溶质。
77.具体地,该药物组合物可以采用任何合适的给药途径,例如胃肠道给药或非胃肠道给药(例如,静脉内、肌内、皮下、器官内、鼻内、皮内、滴注、脑内、直肠内等)途径;上述药物可以为任何合适的剂型,例如经胃肠道给药剂型,例如,包括,但不限于,片剂、丸剂、粉剂、颗粒剂、胶囊剂、锭剂、糖浆剂、液体、乳剂、混悬剂等;非经胃肠道给药剂型,例如,注射给药剂型:如注射剂(例如,用于皮下注射、静脉注射、肌内注射、腹膜内注射),呼吸道给药剂型:如喷雾剂、气雾剂、粉雾剂等,皮肤给药剂型,如外用溶液剂、洗剂、软膏剂、硬膏剂、糊剂、贴剂等,粘膜给药剂型:如滴眼剂、眼用软膏剂、滴鼻剂、含漱剂、舌下片剂等,腔道给药剂型:如栓剂、气雾剂、泡腾片、滴剂、滴丸剂等,用于直肠、阴道、尿道、鼻腔、耳道等。优选地,该药物组合物为注射剂。
78.具体地,该药物组合物的各种剂型可以按照药学领域的常规生产方法制备,例如使载药体系与一种或多种药学上可接受的辅料混合,然后将其制成所需的剂型。
79.在本发明第八方面,提供一种预防和/或治疗疾病的方法,其包括向有此需要的受试者施用第四方面所述的载药体系或第七方面所述的药物组合物的步骤。
80.具体地,所述疾病具有本发明第三、六方面所述的定义,特别是恶性肿瘤,例如乳腺癌,包括原发性乳腺癌和转移性乳腺癌。
81.在本发明的一个实施方式中,该方法为治疗恶性肿瘤的方法,其治疗作用不仅包括抑制肿瘤的生长,还可以包括抑制肿瘤转移。
82.具体地,受试者可以为哺乳动物,例如人类、猴、黑猩猩、犬、鼠、兔等,特别是人类。
83.本发明首次开发了一种多聚唾液酸(psa)修饰的玉米醇溶蛋白核/壳纳米颗粒,其可用于靶向递送药物(特别是抗肿瘤药物,如和厚朴酚(hnk)),可实现增强的药物递送效率、主动靶向能力、在肿瘤部位的特异性生物分布,从而抑制肿瘤的生长、迁移和侵袭。以hnk为例,实验证明,psa-玉米醇溶蛋白-hnk在携带4t1乳腺癌的小鼠模型中的增强的肿瘤积累,从而产生了理想的抗肿瘤功效和有利的生物安全性,并且,psa-玉米醇溶蛋白-hnk显著抑制了乳腺癌向肺和肝的转移。因此,本发明制备的纳米颗粒有望成为一种有效的肿瘤靶向药物载体用于药物开发和疾病治疗。
附图说明
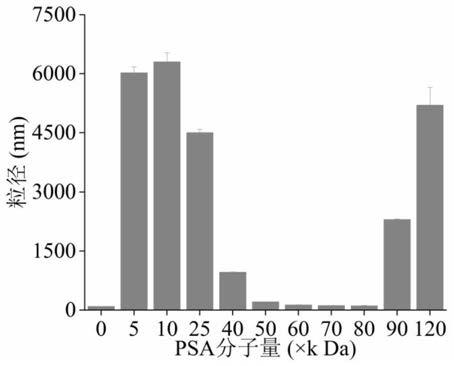
84.图1所示为不同psa分子量对纳米颗粒粒径的影响。
85.图2所示为不同psa溶液浓度对纳米颗粒粒径的影响。
86.图3所示为psa-zein-hnk纳米颗粒的表征。(a)粒度分布,通过dls方法测定;(b)psa-zein-hnk的形态,通过tem检测;比例尺,500nm;(c)不同制剂的hnk释放曲线。
87.图4所示为玉米醇溶蛋白和psa-玉米醇溶蛋白纳米颗粒在4t1细胞中的细胞摄取。(a)4t1细胞的cou6荧光强度,通过流式细胞术测量,温育1小时;(b)基于流式细胞术对cou6摄取的定量分析;(c)温育1小时后4t1细胞的共聚焦显微镜图像;比例尺,20μm。数据显示为平均值
±
sd(n=3),*p《0.05,**p《0.01。
88.图5所示为用不同hnk制剂温育小时的4t1细胞通过srb测定的细胞活力,各实验组三个条形分别代表zein-hnk、psa-zein-hnk、游离hnk。每个条形代表平均值
±
sd(n=6),*p
《0.05,**p《0.01。
89.图6所示为游离hnk、zein-hnk和psa-zein-hnk对4t1细胞的抗转移作用。(a)典型显微镜图像和(b、c、d)4t1细胞在伤口愈合、迁移和侵袭检测中与所有组预温育的定量分析。数据显示为平均值
±
sd(n=3),**p《0.01。
90.图7所示为4t1肿瘤球体的体外生长抑制试验。(a)用游离hnk、zein-hnk和psa-zein-hnk处理的肿瘤球体的典型图像,在rpmi-1640培养基中培养的肿瘤球体作为对照,比例尺,100μm;(b)各种hnk制剂处理后肿瘤球体的生长曲线。每个点代表平均值
±
sd(n=3),**p《0.01。
91.图8所示为dir标记的psa-zein纳米颗粒在4t1荷瘤小鼠体内的生物分布和体内肿瘤靶向特性。(a)4t1荷瘤小鼠在施用各种制剂后不同时间点的体内荧光图像;(b)48小时时主要器官和肿瘤的离体荧光图像。
92.图9所示为各种hnk制剂在4t1荷瘤小鼠模型中的体内抗肿瘤活性。(a)治疗期间肿瘤体积的变化曲线;(b)治疗期结束时肿瘤块的重量;(c)处死后观察到的肿瘤大小图像;(d)治疗期结束时肿瘤切片的h&e染色;(e)治疗期结束时肿瘤切片中凋亡细胞的tunel荧光染色;(f)tunel荧光染色的半定量结果。数据显示为平均值
±
sd(n=6),*p《0.05,**p《0.01。
93.图10所示为4t1荷瘤小鼠模型的体内抗转移和生物安全性研究。(a)4t1荷瘤小鼠在治疗期间的体重变化;(b)用各种hnk制剂处理后的肺转移性结节标本,红色箭头表示转移结节;(c)治疗期结束时主要器官切片的h&e染色,绿色箭头表示转移病灶,比例尺,50μm。
具体实施方式
94.除非另有定义,本发明中所使用的所有科学和技术术语具有与本发明涉及技术领域的技术人员通常理解的相同的含义。
95.本文所引用的各种出版物、专利和公开的专利说明书,其公开内容通过引用整体并入本文。
96.下面将结合本发明实施例,对本发明的技术方案进行清楚、完整地描述,显然,所描述的实施例仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有作出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
97.实施例的实验中所用部分试剂、材料、实验动物如下:
98.和厚朴酚(hnk,》98%)购自美伦生物技术有限公司(大连,中国)。玉米醇溶蛋白(》98%)和吐温80购自百灵威科技有限公司(北京,中国)。多聚唾液酸(psa)由镇江长兴制药有限公司生产(镇江,中国)。磺酰罗丹明b钠盐(srb)、香豆素-6(cou6)、hoechst 33258和基质胶均由sigma-aldrich(上海,中国)提供。annexin v-fitc/pi凋亡检测试剂盒购自碧云天生物科技有限公司(北京,中国)。兔多克隆抗人bcl-2、小鼠多克隆抗人bax、兔多克隆抗gapdh、兔抗小鼠免疫球蛋白g(igg)和山羊抗兔igg均获自cell signaling technology(danvers,usa)。抗e-钙粘蛋白和波形蛋白的兔多克隆抗体购自proteintech(chicago,usa)。除非另有说明,所有其它化学试剂均按原样使用。
99.鼠乳腺癌细胞系4t1获自中国医学科学院基础医学研究所(北京,中国),并在37
℃,含5%co2的湿润气氛下,在补充有10%胎牛血清(维森特生物技术有限公司,南京,中国)、100u/ml青霉素和100μg/ml链霉素的rpmi-1640培养基(迈晨科技有限公司,北京,中国)中培养。
100.雌性balb/c小鼠(4-6周龄)购自辽宁实验动物资源中心(本溪,中国)并在无特定病原体和温度控制条件下饲养。所有与动物有关的实验都得到了齐齐哈尔医学院伦理委员会的批准,并完全符合实验动物护理和使用的机构指南。
101.统计分析:
102.实施例中所有实验结果表示为平均值
±
标准偏差。使用学生t检验确定统计学差异。p《0.05被认为差异显著,p《0.01被认为差异极显著。
103.实施例1:psa分子量的考察
104.1、纳米颗粒的制备
105.分别使用不同分子量的psa制备psa-玉米醇溶蛋白纳米颗粒,具体步骤如下:
106.将玉米醇溶蛋白(100mg)溶于5.0ml乙醇/水(85:15,v/v)中。在1000rpm下搅拌1小时后,使用1mol/l hcl将上述混合溶液调节至ph 5.7,并在磁力搅拌(1000rpm)30min,同时滴加至20.0ml 0.05%吐温80溶液(调节至ph 4.0)中。然后,在37℃下通过旋转蒸发器除去剩余的乙醇。
107.对于用psa包覆玉米醇溶蛋白纳米颗粒的方法,将所得的玉米醇溶蛋白纳米颗粒分散体(5.0ml)注射到5.0ml psa溶液(调节至ph 4.0)中,持续搅拌(1000rpm)1小时。将所制备的样品以12000rpm离心以除去杂质。所得样品为玉米醇溶蛋白/psa核-壳纳米颗粒,并称为psa-玉米醇溶蛋白。
108.上述psa溶液浓度均为0.1%,其中,psa的分子量分别为5、10、25、40、50、60、70、80、90、120k da。
109.通过透射电子显微镜(tem,hitach ht-7700,日本)确认纳米颗粒的尺寸、结构和形态。
110.2、实验结果
111.实验结果如图1所示,当使用《50kda和》80kda的psa时,纳米颗粒发生广泛聚集。通常,psa的分子量决定了psa和阳离子玉米醇溶蛋白之间的吸附过程中向每个纳米颗粒表面提供的负电荷。对于50-80kda psa,几个psa分子可能足以逆转纳米粒的ζ电位。而对于《50kda的psa,相同的吸附发生次数正好接近等电点,这降低了静电排斥,导致纳米颗粒的团聚。至于》80kda的psa,可能的原因是,较大的psa尺寸导致单个psa分子吸附到两个或更多纳米粒表面,从而导致架桥絮凝。
112.实施例2:psa溶液浓度的考察
113.1、纳米颗粒的制备
114.分别使用不同浓度的psa溶液制备psa-玉米醇溶蛋白纳米颗粒,具体步骤如下:
115.将玉米醇溶蛋白(100mg)溶于5.0ml乙醇/水(85:15,v/v)中。在1000rpm下搅拌1小时后,使用1mol/l hcl将上述混合溶液调节至ph 5.7,并在磁力搅拌(1000rpm)30min,同时滴加至20.0ml 0.05%吐温80溶液(调节至ph 4.0)中。然后,在37℃下通过旋转蒸发器除去剩余的乙醇。
116.对于用psa包覆玉米醇溶蛋白纳米颗粒的方法,将所得的玉米醇溶蛋白纳米颗粒
分散体(5.0ml)注射到5.0ml psa溶液(调节至ph 4.0)中,持续搅拌(1000rpm)1小时。将所制备的样品以12000rpm离心以除去杂质。所得样品为玉米醇溶蛋白/psa核-壳纳米颗粒,并称为psa-玉米醇溶蛋白。
117.上述psa溶液浓度分别为0.05%、0.075%、0.1%、0.25%、0.5%、1%、2.5%、5%、7.5%、10%,各psa溶液中所用psa的分子量均为80k da。
118.通过透射电子显微镜(tem,hitach ht-7700,日本)确认纳米颗粒的尺寸、结构和形态。
119.2、实验结果
120.实验结果如图2所示,当使用小于0.1%的psa浓度时,纳米颗粒将迅速沉淀并形成大团聚体,当psa浓度在0.1%至1%之间时,可以得到分散性良好、粒径合适的纳米颗粒(100-200nm),而且随着psa浓度的增加,粒径稍微增大。但是当psa浓度进一步增加至超过1%时,纳米粒粒径急剧增大,达到1000nm以上。由于小粒径(100-200nm)的纳米颗粒,粒径小于脉管泄漏的孔径,再加上淋巴回流不良,可以为纳米颗粒在患者肿瘤部位的聚集和定位提供理想的治疗条件(ossipov,d.a.nanostructured hyaluronic acid-based materials for active delivery to cancer.expert opinion on drug delivery,2010,7(6):681
–
703.)。
121.实施例3:负载hnk的玉米醇溶蛋白/psa纳米颗粒的制备和表征
122.1、纳米颗粒的制备
123.将玉米醇溶蛋白(100mg)和hnk(10mg)溶于5.0ml乙醇/水(85:15,v/v)中。在1000rpm下搅拌1小时后,使用1mol/l hcl将上述混合溶液调节至ph 5.7,并在磁力搅拌(1000rpm)30min,同时滴加至20.0ml 0.05%吐温80溶液(调节至ph 4.0)中。然后,在37℃下通过旋转蒸发器除去剩余的乙醇。
124.对于用psa包覆玉米醇溶蛋白-hnk纳米颗粒的方法,将所得的玉米醇溶蛋白-hnk纳米颗粒分散体(5.0ml)注射到5.0ml 0.1%psa(psa分子量为80kda)(调节至ph 4.0)溶液中,持续搅拌(1000rpm)1小时。将新制备的样品以12000rpm离心以除去未包封的hnk。所得样品为负载hnk的玉米醇溶蛋白/psa核-壳纳米颗粒,并称为psa-玉米醇溶蛋白-hnk(在附图中简称为psa-zein-hnk)。
125.为了制备负载cou6或dir的纳米颗粒,以与上述制备psa-玉米醇溶蛋白-hnk相同的方式制备psa-玉米醇溶蛋白-cou6和psa-玉米醇溶蛋白-dir,仅用cou6或dir代替hnk。
126.2、纳米颗粒的表征
127.通过透射电子显微镜(tem,hitach ht-7700,日本)确认纳米颗粒的尺寸、结构和形态。将一滴这种稀释的纳米颗粒溶液置于铜载网上,随后使用2%乙酸双氧铀进行负染色,并在室温下干燥。然后在tem下在100kv下观察图像。通过nicomp 380zls particle sizing system(pss,usa)分析不同纳米颗粒的平均粒度、多分散性指数(pdi)和ζ电势值。通过hplc系统测定psa-玉米醇溶蛋白-hnk的药物包封效率。ee的计算公式如下:ee=(所负载的hnk的重量/进料hnk的重量)
×
100%。
128.使用动态透析方法在由具有0.2%吐温80的pbs(ph 7.4)组成的释放介质中测定不同hnk纳米颗粒的体外释放曲线。总共,将1ml各种制剂加入透析袋(mwco=12000-14000da)中,随后在37℃下以100rpm的速率水平振荡,在30ml释放介质中透析。在指定的时
间间隔,收集1ml体积的释放介质,并相应地补充等体积的新鲜介质。使用hplc系统在48小时内测定外部介质中的hnk含量。
129.3、实验结果
130.通过动态光散射检测获得的粒度分布显示psa-玉米醇溶蛋白-hnk具有窄的粒度分布,平均大小为107.2
±
10.1nm,pdi为0.23
±
0.05(图3a)。相比之下,未修饰的玉米醇溶蛋白-hnk分散体的平均大小为91.4
±
6.1nm。psa-玉米醇溶蛋白-hnk的平均粒径略大于未修饰的玉米醇溶蛋白-hnk的平均大小,表明psa成功引入玉米醇溶蛋白纳米颗粒的表面。如图3b所示,psa-玉米醇溶蛋白-hnk的tem图像呈明确的球形,平均大小为103.5nm(通过tem测量粒径与纳米粒度仪测得的粒径存在偏差,在合理误差范围内),与dls观察到的实验结果一致。
131.玉米醇溶蛋白-hnk的ζ电位测定为18.2
±
1.2mv。由于psa的化学结构中存在羧基,在用psa修饰后,psa-玉米醇溶蛋白-hnk的ζ电位急剧下降至-33.5
±
3.1mv。相对较高的ζ电势是通过静电排斥改善纳米颗粒在水性介质中的稳定性的关键因素。通常,与带正电荷的纳米颗粒相比,带负电荷的纳米颗粒可能表现出改善的胶体稳定性,增加血液循环时间,并降低对正常细胞的毒性(liang,h.s.;huang,q.r.;zhou,b.;he,l.;lin,l.f.;an,y.p.;li,y.;liu,s.l.;chen,y.j.;li,b.self-assembled zein-sodium carboxymethyl cellulose nanoparticles as an effective drug carrier and transporter.j.mater.chem.b 2015,3(16),3242-3253,doi:10.1039/c4tb01920b)。
132.包括尺寸增加和电荷逆转的上述结果证实psa在玉米醇溶蛋白纳米颗粒的表面上成功修饰。通过hplc测定,psa-玉米醇溶蛋白-hnk中的hnk负载率和包封效率分别为8.6%和86.3%。研究了玉米醇溶蛋白-hnk和psa-玉米醇溶蛋白-hnk的hnk释放曲线。如图3c所示,玉米醇溶蛋白-hnk和psa-玉米醇溶蛋白-hnk在含有0.2%吐温80的pbs(ph 7.4)中显示持续的hnk释放方式达48小时,表明可能降低给药频率。此外,psa修饰未导致玉米醇溶蛋白-hnk和psa-玉米醇溶蛋白-hnk之间的释放曲线之间存在显著差异。12小时后,两种纳米颗粒仅释放~50%的hnk,而在24小时内hnk增加至约65%。在48h时释放了接近75%的总hnk,这证实了psa-玉米醇溶蛋白-hnk在到达并积累到肿瘤部位之前具有稳定的负载和转运特性。
133.实施例4:体外细胞摄取
134.1、实验方法
135.(1)为了证明psa-玉米醇溶蛋白纳米颗粒通过配体-受体识别增强细胞内化,利用过表达选择蛋白(selectin)的4t1乳腺癌细胞并使用流式细胞术进行研究。将4t1细胞接种于6孔板(1
×
105个细胞/孔)中并培养过夜。然后,加入100ng/ml的载有cou6的psa-玉米醇溶蛋白纳米颗粒(psa-玉米醇溶蛋白-cou6,实施例3制备,在附图中简称为psa-zein-cou6),并将细胞在37℃下温育。1小时后,将细胞用冷pbs洗涤并用胰蛋白酶处理。然后将细胞离心并再分散于0.5ml pbs缓冲液中。
136.设置非靶向玉米醇溶蛋白-cou6组、游离cou6组,将上述实验条件中的psa-玉米醇溶蛋白-cou6分别替换为玉米醇溶蛋白-cou6(在附图中简称为zein-cou6)、游离cou6,其他实验条件相同。
137.设置psa psa-玉米醇溶蛋白-cou6组:将4t1细胞首先用2.0mg/ml psa培养1小时,
然后用psa-玉米醇溶蛋白-cou6再培养1小时,其他实验条件相同。
138.设置对照组,其不添加任何试剂处理,其他实验条件相同。
139.(2)对于选择受体竞争性抑制测定,各实验组的实验条件参照第(1)部分所述,然后通过facscan流式细胞仪(bd facscalibur,usa)直接测试细胞的平均cou6荧光强度。
140.(3)对于共聚焦激光扫描显微镜研究,将4t1细胞接种于玻璃底培养皿中并使其粘附过夜。与100ng/ml psa-玉米醇溶蛋白纳米颗粒温育1小时后,将细胞用冷pbs洗涤三次。随后,将细胞用4%多聚甲醛固定20min,随后将细胞核用5μg/ml hoechst 33258再染色20min。最后,使用lsm710激光共聚焦显微镜(zeiss,germany)观察经处理的细胞。
141.设置非靶向玉米醇溶蛋白-cou6组、游离cou6组、psa psa-玉米醇溶蛋白-cou6组和对照组,各实验组的实验条件参照第(1)部分所述。
142.2、实验结果
143.为了确定psa和选择蛋白受体在增强的摄取中的靶向作用,发明人首先比较了不同的负载cou6的玉米醇溶蛋白纳米颗粒的肿瘤靶向能力。通过流式细胞术定量测定不同纳米颗粒的细胞摄取。流式细胞术数据显示,荧光强度的顺序为对照《玉米醇溶蛋白-cou6《psa psa-玉米醇溶蛋白-cou6《psa-玉米醇溶蛋白-cou6《游离cou6(图4a和b)。与非靶向玉米醇溶蛋白-cou6组相比,psa-玉米醇溶蛋白-cou6组中的细胞摄取水平接近两倍。说明psa的引入对提高psa-玉米醇溶蛋白-cou6的摄取比电子吸附作用更大。此外,进行竞争性抑制测定以验证psa-选择蛋白受体介导的psa-玉米醇溶蛋白-cou6的细胞内化。与对照组相比,psa阻断选择蛋白受体后,psa-玉米醇溶蛋白-cou6的细胞摄取明显降低。这些发现为psa-玉米醇溶蛋白纳米颗粒经由psa-选择蛋白受体介导的途径内化到4t1细胞中提供了明确的支持。
144.通过共聚焦激光扫描显微镜收集的摄取图像与定量流式细胞术测定一致(图4c),在psa修饰的玉米醇溶蛋白纳米颗粒组中绿色荧光显著升高,但在玉米醇溶蛋白纳米颗粒组中cou6内化明显减弱。然而,psa预处理(psa psa-玉米醇溶蛋白-cou6)组绿色荧光强度增强,表明psa修饰可用于靶向给药的可行性和潜力。
145.实施例3:体外细胞毒性(srb)测定
146.1、实验方法
147.通过srb比色法测定各种hnk制剂对4t1的细胞活力。简言之,将4t1细胞以2
×
103个细胞/孔的密度接种于96孔板中并培养过夜。制备具有系列hnk浓度(0.3-20μg/ml)的玉米醇溶蛋白-hnk、psa-玉米醇溶蛋白-hnk(实施例3制备)和游离hnk溶液,并与4t1细胞一起温育48h。继续培养48小时后,将细胞用10%冷三氯乙酸固定,风干,并用0.4%srb染料染色,然后加入150μl tris碱溶液(10mm)以溶解srb染料。最后,用酶标仪(tecan safire2,switzerland)在540nm下测量代表细胞活力的最终溶液的吸光度。
148.2、实验结果
149.如图5所示,所有hnk制剂以浓度依赖性方式抑制细胞增殖。在所有组中,游离hnk对4t1细胞的抗增殖作用最强,表明更多的hnk通过被动扩散快速转移到细胞中。正如所预期的,psa-玉米醇溶蛋白-hnk表现出比玉米醇溶蛋白-hnk高得多的细胞毒性,这可能归因于通过psa修饰促进的细胞摄取的增加。psa-玉米醇溶蛋白-hnk(4.37μg/ml)在48h时的ic
50
值非常接近游离hnk(3.99μg/ml),并且显著高于玉米醇溶蛋白-hnk(7.74μg/ml)。这些结果
有力地证实了由psa-选择蛋白靶向递送介导的hnk的细胞毒性升高。
150.实施例4:体外细胞迁移和侵袭抑制测定
151.1、实验方法
152.使用简单的2d划痕伤口愈合划痕试验分析了对4t1细胞迁移的影响(liang,c.c.;park,a.y.;guan,j.l.in vitro scratch assay:a convenient and inexpensive method for analysis of cell migration in vitro.nat.protoc.2007,2(2),329-333,doi:10.1038/nprot.2007.30)。将4t1细胞在6孔板中培养过夜,直至形成汇合的单层。然后用无菌移液管尖端将划痕引入汇合单层,并用pbs洗涤以除去漂浮的细胞。然后将细胞与玉米醇溶蛋白-hnk、psa-玉米醇溶蛋白-hnk(实施例3制备)和游离hnk(5μg/ml hnk)在新鲜无血清rpmi-1640中一起温育。使用倒置显微镜(zeiss,axio observer a1)监测处理后0小时和24小时两个伤口边缘之间的距离。如前所述计算伤口愈合率(zhang,z.w.;cao,h.q.;jiang,s.j.;liu,z.y.;he,x.y.;yu,h.j.;li,y.p.nanoassembly of probucol enables novel therapeutic efficacy in the suppression of lung metastasis of breast cancer.small 2014,10(22),4735-4745,doi:10.1002/smll.201400799)。
153.使用24孔transwell板(8μm孔,costar,usa)进行transwell方法以进一步测量细胞迁移和侵入。对于细胞迁移测定,将4t1细胞与浓度为5.0μg/ml hnk的不同hnk溶液一起温育24h。然后将100μl不含fbs的rpmi 1640培养基中预处理的5
×
104个4t1细胞接种于24孔transwell的顶室中,并将600μl含10%fbs的培养基置于底室中。24小时后,将迁移至下层膜的细胞用4%多聚甲醛固定,并用0.4%结晶紫染色30分钟,然后在倒置显微镜下拍照。随后,将与细胞结合的结晶紫用33%乙酸溶液溶解用于定量分析。用酶标仪记录570nm处的光密度。
154.对于侵袭试验,将含有8
×
104预处理的4t1细胞的100μl无血清培养基接种于用稀释的matrigel(20μg/μl;cornig,usa)预包被的顶室中,并温育36小时。接下来的处理步骤与上述方法相对应。
155.2、实验结果
156.运动性增加是转移细胞的标志。伤口愈合划痕试验用于评估细胞的运动性。与对照组相比,所有hnk制剂在24小时后均能在一定程度上抑制划痕的愈合。psa-玉米醇溶蛋白-hnk显示出更强的抑制效果,伤口愈合率为13.33%,而玉米醇溶蛋白-hnk组的伤口愈合率增加到31.11%。游离hnk具有最强的抑制划痕愈合效果,伤口愈合率为6.67%(图6a和b)。此外,发明人在transwell模型上分析了4t1细胞的体外细胞迁移。观察到psa-玉米醇溶蛋白-hnk处理细胞的类似抑制作用。如图6a和c所示,psa-玉米醇溶蛋白-hnk组的迁移细胞数明显低于玉米醇溶蛋白-hnk组。与对照组相比,psa-玉米醇溶蛋白-hnk的细胞迁移率仅为20.05%,而玉米醇溶蛋白-hnk的细胞迁移率为54.5%。
157.接下来,发明人在transwell加基质胶试验中评估了psa-玉米醇溶蛋白-hnk对4t1细胞侵袭的影响。细胞侵袭是肿瘤转移的关键生物学过程,为启动肿瘤转移提供了先决条件(wang,j.;liu,d.;guan,s.;zhu,w.q.;fan,l.;zhang,q.;cai,d.f.hyaluronic acid-modified liposomal honokiol nanocarrier:enhance anti-metastasis and antitumor efficacy against breast cancer.carbohydr.polym.2020,235,doi:10.1016/j.carbpol.2020.115981)。如图6a和d所示,psa-玉米醇溶蛋白-hnk处理组的4t1细胞侵袭
显著低于玉米醇溶蛋白-hnk组。玉米醇溶蛋白-hnk、psa-玉米醇溶蛋白-hnk和游离hnk的细胞侵袭率分别为35.81%、16.59%和14.79%。这些结果证明psa-玉米醇溶蛋白-hnk的抗侵袭能力是玉米醇溶蛋白-hnk的2.15倍。基于上述结果,hnk处理可抑制4t1细胞的迁移和侵袭,并且与玉米醇溶蛋白-hnk相比,靶向psa-玉米醇溶蛋白-hnk抑制更高水平的迁移和侵袭细胞。因此,发明人推测psa-玉米醇溶蛋白-hnk可能对肿瘤的原发性转移具有优异的抑制作用。
158.实施例5:对肿瘤球体的体外细胞毒性
159.1、实验方法
160.在3d肿瘤球体(tumor spheroid)上进一步评估了不同的负载hnk的制剂的抗肿瘤活性。如前所述(del duca,d.;werbowetski,t.;del maestro,r.f.spheroid preparation from hanging drops:characterization of a model of brain tumor invasion.j.neurooncol.2004,67(3),295-303,doi:10.1023/b:neon.0000024220.07063.70),使用悬滴法支持3d细胞培养和球体形成。首先,将琼脂糖(2%,w/v)溶解于无血清rpmi-1640培养基中,并包被在48孔板的每个孔中以防止细胞粘附。接下来,将4t1细胞悬浮液(1
×
103/20μl)液滴悬挂在48孔板的盖子上。48小时后,将形成的肿瘤球体置于每个孔中,每孔中含0.9ml培养基。当肿瘤球体的大小为约100μm时,将均匀且致密的球体用于后续程序。将肿瘤球体分别与游离hnk、玉米醇溶蛋白-hnk和psa-玉米醇溶蛋白-hnk(实施例3制备)(10μg/ml hnk)一起温育。在确定的时间点(1、3、5和7天),监测肿瘤球体的生长抑制,并使用倒置显微镜(zeiss,axio observer a1)拍摄图像。
161.2、实验结果
162.如图7a和b所示,玉米醇溶蛋白-hnk、psa-玉米醇溶蛋白-hnk和游离hnk对4t1肿瘤球体的毒性高于对照,其体积表现出13.98倍的增加。由于扩散效应,游离hnk对肿瘤球体显示出最强的细胞毒性作用。此外,psa-玉米醇溶蛋白-hnk和玉米醇溶蛋白-hnk组中的球体体积分别降低至23.18%和44.23%。因此,表明psa-玉米醇溶蛋白-hnk比玉米醇溶蛋白-hnk具有甚至更高的细胞毒性。psa-玉米醇溶蛋白-hnk的细胞毒性增加被认为与psa修饰有关,这增强了纳米颗粒向肿瘤球体的渗透和积累。
163.实施例6:体内肿瘤靶向评估
164.1、实验方法
165.通过将1
×
106个4t1细胞悬液(100μl)皮下注射到balb/c小鼠的右腋窝中来建立皮下4t1肿瘤模型。在肿瘤体积达到300-400mm3后,将玉米醇溶蛋白-dir和psa-玉米醇溶蛋白-dir(实施例3制备,在附图中分别简称为zein-dir、psa-zein-dir)以500μg/kg dir的剂量经由尾静脉注射至皮下荷瘤小鼠中。在预定的时间点,通过体内成像系统(ivis lumina seriesⅲ,perkinelmer,usa)捕获麻醉小鼠的荧光图像。最后,在24小时拍摄解剖的肿瘤和主要器官的离体图像。
166.2、实验方法
167.如图8a所示,肿瘤中玉米醇溶蛋白-dir的积累迅速减少,并在48小时显著减弱。相比之下,psa-玉米醇溶蛋白-dir在肿瘤中从4小时直至48小时表现出强荧光。明显地,psa-玉米醇溶蛋白-dir显示出比非靶向玉米醇溶蛋白-dir高得多的肿瘤积累,证实psa修饰赋予玉米醇溶蛋白纳米颗粒具有肿瘤靶向作用并延长它们在肿瘤中的积累时间。最后,获得
肿瘤和主要器官,然后通过离体荧光成像进行评估。离体图像显示psa修饰导致玉米醇溶蛋白纳米颗粒在肺中的分布减少,并增强了肿瘤积累(图8b)。总之,这些体内数据表明,这种开发的psa-玉米醇溶蛋白纳米颗粒的改善的肿瘤积累将提供抗肿瘤剂(如hnk)的相当大且持久的效果。
168.实施例7:对4t1乳腺癌模型的体内抗肿瘤研究
169.如前所述建立皮下荷4t1乳腺癌模型,当肿瘤体积达到100mm3时,将其随机分成四组(n=6)。这些不同的组分别静脉内注射生理盐水、游离hnk、玉米醇溶蛋白-hnk和psa-玉米醇溶蛋白-hnk(实施例3制备),剂量为15mg/kg hnk,每两天一次,共4次。每隔一天测量肿瘤体积和小鼠体重。治疗24天后,收集肿瘤和主要器官。将肿瘤称重并成像以比较肿瘤生长抑制。将肺用4%多聚甲醛固定48小时,然后对肉眼检测的转移结节进行计数,以评估不同hnk制剂对癌症转移的抑制作用。将主要器官和肿瘤用4%多聚甲醛固定,随后用h&e(苏木精和曙红)染色用于进一步组织学分析。为了进一步在组织学上研究肿瘤细胞的凋亡,还对肿瘤样品进行了末端脱氧核苷酸转移酶脱氧尿苷三磷酸(dutp)切口末端标记(tunel)免疫荧光染色。
170.2、实验结果
171.在荷4t1乳腺癌的balb/c小鼠中测试了玉米醇溶蛋白-hnk、psa-玉米醇溶蛋白-hnk和游离hnk的体内抗肿瘤作用。抗肿瘤效果通过不同hnk制剂处理期间和之后的相对肿瘤体积、肿瘤重量和肿瘤图像来证明。如图9a所示,生理盐水组的4t1乳腺癌细胞在实验期间生长迅速,而不同的hnk制剂显著抑制了肿瘤生长。在实验期结束时,生理盐水处理对照组的平均肿瘤体积为1181.9
±
115.7mm3,游离hnk为965.9
±
88.3mm3,玉米醇溶蛋白-hnk为760.6
±
65.6mm3,psa-玉米醇溶蛋白-hnk处理组为619.1
±
62.9mm3。这表明与施用游离hnk相比,将hnk包封在玉米醇溶蛋白纳米颗粒中是绝对有益的。更重要的是,psa-玉米醇溶蛋白-hnk比玉米醇溶蛋白-hnk和游离hnk处理对肿瘤表现出更好的抑制作用,这反映了psa修饰对于靶向药物递送的优势。在不同hnk制剂处理后的肿瘤重量(图9b)和图像(图9c)中观察到类似的结果。所有的测量均证明psa-玉米醇溶蛋白-hnk具有最高的体内抗肿瘤效率,高于玉米醇溶蛋白-hnk的体内抗肿瘤效率,而玉米醇溶蛋白-hnk的体内抗肿瘤效率又高于游离hnk和生理盐水的体内抗肿瘤效率。总之,这些结果进一步证实了所提出的psa-玉米醇溶蛋白-hnk的特异性作用和最佳抗肿瘤作用。
172.为了进一步研究抗肿瘤效果,进行了组织学和免疫组织化学染色以评估主要器官和肿瘤的变化。如图9d所示,生理盐水组肿瘤的h&e染色图像充满紧密堆积的肿瘤细胞,并具有完整的形态,而psa-玉米醇溶蛋白-hnk组检测到肿瘤坏死,核碎裂和凝聚明显。tunel染色测定表明,与其他制剂处理相比,psa-玉米醇溶蛋白-hnk处理在肿瘤组织中产生最大数量的凋亡细胞(图9e和f),这与h&e的结果一致。psa-玉米醇溶蛋白-hnk的所有这些优异的结果均得益于psa修饰,这导致更高的细胞摄取效率、更强的细胞毒性和在肿瘤部位更多的药物积累。
173.为了评估与体内不同hnk制剂处理相关的可能的全身毒性,评估了体重变化和主要组织的h&e切片。如图10a所示,玉米醇溶蛋白-hnk、psa-玉米醇溶蛋白-hnk和游离hnk被小鼠良好耐受,因为与生理盐水组相比,它们在处理过程中没有表现出显著的体重减轻。对主要器官的组织学切片的组织学检查也证实了它们的体内生物安全性,因为在用不同hnk
制剂处理的小鼠中没有明显的病理学改变(图10c)。这些数据表明用于hnk的靶向递送的psa修饰的玉米醇溶蛋白核/壳纳米颗粒表现出优异的生物安全性,可以用作抗肿瘤治疗的安全制剂。
174.转移通常发生在晚期乳腺癌患者中。乳腺癌对于肺转移是众所周知的,导致患者快速死亡(liu,m.t.;ma,w.j.;zhao,d.;li,j.j.;li,q.r.;liu,y.h.;hao,l.y.;lin,y.f.enhanced penetrability of a tetrahedral framework nucleic acid by modification with irgd for dox-targeted delivery to triple-negative breast cancer.acs appl.mater.interfaces 2021,13(22),25825-25835,doi:10.1021/acsami.1c07297)。受到这些优异的抗肿瘤功效的鼓舞,发明人进一步检查了psa-玉米醇溶蛋白-hnk纳米颗粒的抗转移功效。拍摄肺的图像并在处理结束时计算转移性结节。如图10b所示,在生理盐水组中检测到许多转移性结节,表明乳腺肿瘤已转移至肺部。然而,在用不同hnk制剂处理的小鼠中观察到肺转移性结节的数量显著减少。游离hnk和玉米醇溶蛋白-hnk处理表现出对肺转移的中度抑制。而在psa-玉米醇溶蛋白-hnk处理中几乎没有发现肺结节,表明psa-玉米醇溶蛋白-hnk在抑制乳腺癌转移方面优于所有其他hnk制剂。与肺表面转移性结节的趋势相似,生理盐水组中肺和肝切片的h&e染色图像显示许多肿瘤细胞浸润(具有大细胞核)。而游离hnk和玉米醇溶蛋白-hnk处理组的肿瘤细胞浸润显著少于生理盐水组。更重要的是,通过psa-玉米醇溶蛋白-hnk将转移病灶控制到最小,没有肿瘤细胞浸润。这些结果表明psa-玉米醇溶蛋白-hnk不仅能有效抑制原发性肿瘤的生长,而且能抑制肿瘤转移的形成。
175.综上所述,发明人首次成功地使用反溶剂沉淀和静电沉积技术制备了一种psa修饰的玉米醇溶蛋白纳米颗粒,可用于hnk的靶向递送。psa修饰稳定了玉米醇溶蛋白纳米颗粒,并赋予它们在乳腺癌治疗中的主动靶向特性。psa-玉米醇溶蛋白-hnk是一种生物安全和生物相容的纳米药物递送系统,对选择蛋白阳性乳腺癌细胞表现出特异性结合和选择性毒性。在静脉内注射后,psa-玉米醇溶蛋白-hnk纳米颗粒表现出理想的肿瘤抑制效率,并且在整个处理期间没有引起明显的全身毒性,这可能是由于纳米颗粒在肿瘤部位积累增加所致。psa修饰改善肿瘤部位的hnk积累中起到重要作用。更重要的是,psa-玉米醇溶蛋白-hnk还在体外和体内模型中显示出对乳腺癌肺转移的更大抑制,进一步有助于改善乳腺癌治疗。这项工作为乳腺癌治疗提供了一个有前景的纳米平台,其具有增强的药物递送效率,可同时抑制原发性肿瘤和转移的侵袭性生长。
176.以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内,所作的任何修改、等同替换等,均应包含在本发明的保护范围之内。
177.本发明中描述的前述实施例和方法可以基于本领域技术人员的能力、经验和偏好而有所不同。
178.本发明中仅按一定顺序列出方法的步骤并不构成对方法步骤顺序的任何限制。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。