1.本发明属于药物技术领域,具体本发明涉及核酸药物技术领域。
背景技术:
2.mirna(micrornas)是一种20~23个核苷酸长的非编码的rna,具有调控基因表达和一系列生物学功能,与多种疾病的发病机制相关联,尤其是癌症。在细胞质中,mirna识别与其种子序列互补的mrna,随后诱导其翻译后降解和沉默,这为在转录水平上下调异常升高的致病相关蛋白提供了新的治疗手段。尽管已经发现了越来越多能够调节疾病过程的mirna,但它们的临床转化,特别是靶向肿瘤进展,一直受到核酸治疗的内在缺陷的阻碍,包括系统稳定性差、快速清除、膜通透性低和缺乏靶向能力。
3.为了改善这些技术障碍,现已开发了各种复杂的mirna修饰和/或传递方法,并在提高mirna治疗药物的药理潜力方面取得了重大进展。尽管化学修饰的mirna具有抗核酸酶的能力,并且延长在血流中半衰期,但脱靶效应严重限制了其临床应用,这可能是因为mirna在健康器官和组织中功能广泛。此外,对于mirnas载体,常用的脂类、阳离子聚合物和可生物降解聚合物往往会被网状内皮系统(res)快速清除,其中肝脏和脾脏巨噬细胞会从循环系统中迅速清除这些外源性颗粒,导致mirnas疗法的效力丧失或抑制。
4.纳米技术在克服mirna药理学缺陷方面有着巨大的前景。纳米载体介导的寡核苷酸递送能够在循环过程中保护“货物”不被核酸酶降解,并通过内吞作用促进寡核苷酸内化进入细胞质以避免遭受内吞体降解。无载体纳米药物为发展纳米医学提供了另一种可能,无载体纳米药物通过自组装和/或配位组装形成精细的纳米结构。无限配位聚合物(icp)是一类新兴的无载体纳米药物体系,药物通过配位键直接与离子连接,具有可调高载药量、成分可调、制备条件温和、无限可控的空间维数扩展等优点。因此,开发一种mirna来源的icp不仅能克服核酸疗法的药理学缺陷,而且在优化药效方面具有良好的药物优势,从而为包括癌症在内的多种人类疾病的rna衍生疗法提供新的思路。
技术实现要素:
5.本发明的目的在于克服现有核酸药物的缺陷和不足,提供用于癌症治疗的无限配位聚合物。
6.基于上述目的,本技术通过提供一种无限金-巯基配位聚合物来解决所属领域中的这种需要。
7.一方面,本发明涉及一种无限金-巯基配位聚合物,其包括:mirna、巯基、au
3
;其中,mirna的5’末端与所述巯基连接;au3 与所述巯基偶联形成-s-au
-s-。
8.进一步地,在本发明提供的一种无限金-巯基配位聚合物中,au
通过-s-au
-s-配位桥接mirna-sh。
9.进一步地,在本发明提供的一种无限金-巯基配位聚合物中,mirna为mir-30c。
10.进一步地,在本发明提供的一种无限金-巯基配位聚合物中,无限金-巯基配位聚
合物自组装成球形结构;这一自组装的驱动力来源于一种无限金-巯基配位聚合物内部的亲金性相互作用。
11.进一步地,在本发明提供的一种无限金-巯基配位聚合物中,以分子数量计,mirna、巯基、au
3
的配比为1:1:1。
12.另一方面,本发明提供了一种无限金-巯基配位聚合物在癌症治疗方面的用途。
13.进一步地,本发明提供的一种无限金-巯基配位聚合物用于抑制wnt/β-catenin信号通路。
14.进一步地,本发明提供的一种无限金-巯基配位聚合物用于增强抗肿瘤药物治疗效力。
15.另一方面,本发明提供了一种无限金-巯基配位聚合物的合成方法,其包括:
16.将mirna溶解于4mg/ml nh
2-peg-sh中,加入ddh2o,得到第一溶液,然后进行磁搅拌;mirna与nh
2-peg-sh的混合比例以od:μl计为1:250;ddh2o的加入量为1od mirna加入1.75ml ddh2o;磁搅拌的条件为50℃,550rpm;优选地,所述mirna为mir-30c;
17.将ddh2o加入hepes溶液中,得到第二溶液,然后进行磁搅拌;ddh2o与hepes溶液的混合比例以容积计为1:1;所用hepes溶液的ph为7.0;磁搅拌的条件为50℃,550rpm;
18.在第一溶液和第二溶液正在进行磁搅拌时,分别向第一溶液和第二溶液加入10mmhaucl4;在第一溶液中,mhaucl4的加入量为1μl nh
2-peg-sh加入1μl mhaucl4;在第二溶液中,mhaucl4的加入量为2.25ml ddh2o加入500μl mhaucl4;第一溶液与第二溶液的mhaucl4加入量相同;
19.当第一溶液与第二溶液变紫后,将第二溶液加入到第一溶液中,超声震荡5min,经两次超纯水离心洗涤,冷冻干燥得到所述无限金-巯基配位聚合物(iacsrna)。
20.本发明与现有技术相比具有以下有益效果或者优点:
21.(1)本发明提供的一种无限金-巯基配位聚合物克服了核酸治疗的内在弱点,包括全身稳定性差、清除快、膜通透性低和缺乏肿瘤靶向性等;
22.(2)本发明提供的一种无限金-巯基配位聚合物在抑制wnt/β-catenin信号通路方面表现出优异的效果,且没有表现出内脏和血液系统的毒性;
23.(3)本发明提供的一种无限金-巯基配位聚合物能有效地提高5-fu和anti-pd1等癌症治疗药物的效力。
附图说明
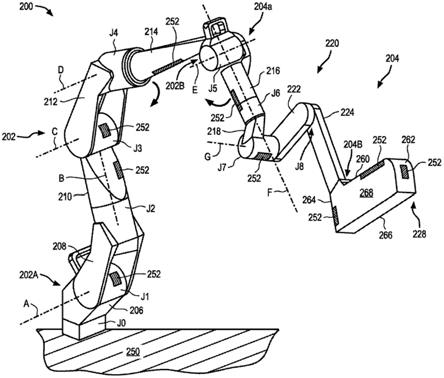
24.图1为iacs-mir-30c的结构示意图;
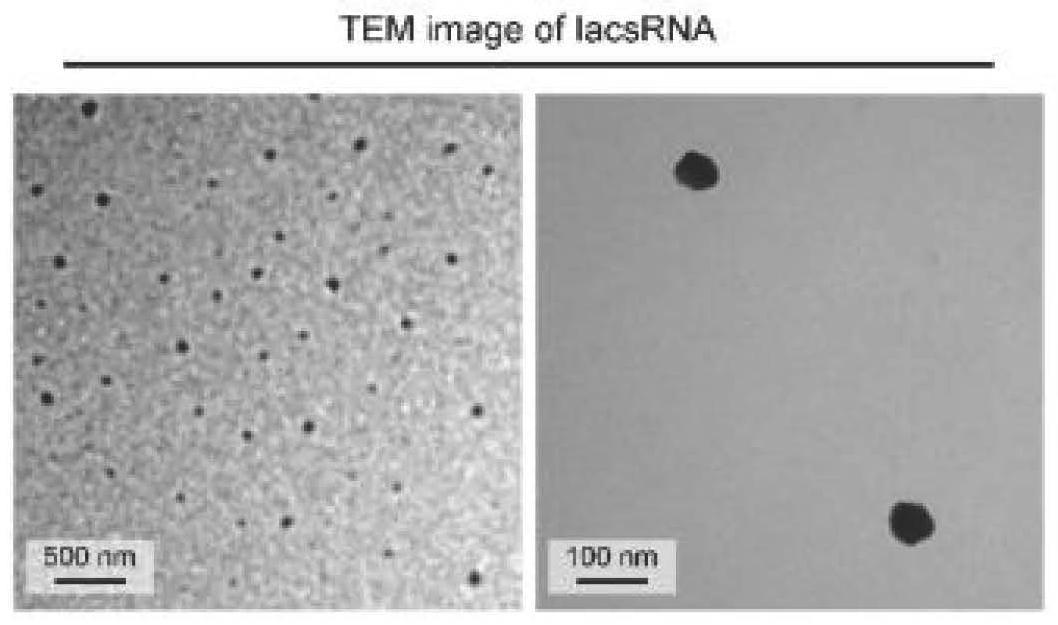
25.图2为iacsrna的tem图像;
26.图3为iacsrna在pbs缓冲液(ph=7.4)中的流体力学直径;
27.图4为iacsrna在pbs缓冲液(ph=7.4)中的zeta电位;
28.图5为iacsrna和mirna的ft-ir光谱;
29.图6为iacsrna的s 2p xps光谱;
30.图7为iacsrna的au 4fxps光谱;
31.图8-a为iacsrna和裸mirna的抗降解稳定性试验的凝胶电泳图;
32.图8-b为iacsrna和裸mirna的抗降解稳定性曲线图;
33.图8-c为孵育6h后不同细胞摄取1μm cy3标记的mirna和iacsrna流式细胞仪定性分析图;
34.图8-d为孵育6h后不同细胞摄取1μm cy3标记的mirna和iacsrna流式细胞仪定量分析图;
35.图8-e为不同ph下iacsrna的胶体稳定性变化图;
36.图8-f为健康c57/b6小鼠iacsrna和rna的血液循环曲线;
37.图8-g为不同时间下小鼠器官金属浓度;
38.图8-h为不同时间下小鼠肿瘤-器官浓度比;
39.图8-i为iacsrna的组织分布定性观察图;
40.图8-j为iacsrna的组织分布定量分析图;
41.图9-a为天冬氨酸转氨酶(alt)、丙氨酸氨基转移酶(ast)含量和肝脏病理切片图;
42.图9-b为血尿素氮(bun)、肌酐(cre)含量和肾脏病理切片图;
43.图9-c为小鼠血液中的红细胞(rbc)、白细胞(wbc)、淋巴细胞(lymph)、中性粒细胞(neut)、血小板(plt)和血红蛋白(hgb)含量图;
44.图9-d为小鼠体重变化图;
45.图9-e为小鼠心脏、肺和脾脏病理切片图;
46.图10-a为iacs-mir-30c表达水平图;
47.图10-b为bcl9表达水平图;
48.图10-c为暴露于50nm iacs-mir-30c 24h后b16f10细胞中差异表达基因的分层聚类图;
49.图10-d为wnt/β-catenin信号通路中基因的分层聚类图;
50.图10-e为st-wnt/β-catenin基因集富集分析图;
51.图10-f为pidβ-cateninnuc信号通路基因集富集分析图;
52.图10-g为wpwnt信号基因集富集分析图;
53.图10-h为实验组wnt/β-catenin信号通路基因集富集分析图;
54.图10-i为实验组肿瘤中wnt信号基因集富集分析图;
55.图10-j为实验组细胞有丝分裂基因集富集分析图;
56.图10-k为实验组细胞周期流式细胞仪分析图;
57.图11-a为pdx模型构建示意图;
58.图11-b为通过外显子测序检测肿瘤突变图;
59.图11-c为指定处理后通过免疫组织化学染色的代表性肿瘤切片;
60.图11-d为指定给药组pdx小鼠模型的肿瘤生长曲线图(n=5);
61.图11-e为第13天指定处理的肿瘤生长抑制(tgi)图;
62.图11-f为不同处理后的代表性照片;
63.图11-g为不同处理后的肿瘤重量图;
64.图11-h为不同处理小鼠肿瘤切片中的ki67染色图;
65.图11-i为不同处理后小鼠肿瘤切片中的tunel染色图;
66.图12-a为不同处理后cd3/cd8免疫荧光图;
67.图12-b为不同处理后cd4/cd25免疫荧光图;
68.图12-c为不同处理后cd3/cd8免疫荧光定量图;
69.图12-d为不同处理后cd4/cd25免疫荧光定量图;
70.图12-e为不同处理后小鼠肿瘤的ki67染色切片图;
71.图12-f为不同处理后小鼠肿瘤的tunel染色切片图;
72.图12-g为不同处理后小鼠b16f10肿瘤的生长曲线图(n=5);
73.图12-h为第9天指定处理的肿瘤生长抑制(tgi)图;
74.图12-i为第9天不同处理小鼠的代表肿瘤图片;
75.图12-j为第9天不同处理小鼠的肿瘤重量图。
76.图8-g和图8-h中,从左至右依次为注射后2h、24h、48h和72h处死,he为心脏,sp为脾,li为肝,lu为肺,ki为肾,tu为肿瘤;图8-j中,从左至右依次为ctrl、iacsrna和rna;图9-a、图9-b、图9-c的柱状图中,从左至右依次为control和iacs-mir-30c;图10-e~图10-j中kegg为京都基因和基因组百科全书,pid为通路相互作用数据库,nes为标准化富集评分;图10-k中从左至右依次为control、mir-30c和iacs-mir-30c;图12-a、图12-c、图12-e、图12-f中的比例尺为1:50μm;上述染色切片图中未进行额外标明的,其比例尺为1:100μm;上述图中数据表示为平均值
±
s.d,其中,*为p《0.05,**为p《0.01。
具体实施方式
77.下面,结合实施例对本发明的技术方案进行说明,但是,本发明并不限于下述的实施例。
78.实施例1
79.本实施例提供了一种无限金-巯基配位聚合物的制备过程。
80.将2od的mir-30c溶解于500μl nh
2-peg-sh(4mg/ml)中,加入1.75ml ddh2o,进行磁搅拌(50℃,550rpm)得到第一溶液。将2.25ml ddh2o加入2.25ml hepes(ph=7.0),进行磁搅拌(50℃,550rpm)得到第二溶液。在对两种溶液进行磁搅拌(50℃,550rpm)时,分别向两种溶液中加入500μl 10mmhaucl4。当溶液变紫后,将第二溶液加入第一溶液,超声震荡5min。经两次超纯水离心洗涤,冷冻干燥得到iacs-mir-30c,即所述无限金-巯基配位聚合物(iacsrna),其结果如图1所示。
81.实施例2
82.本实施例提供了一种无限金-巯基配位聚合物的物理性质试验。
83.图2为iacsrna的tem图像;图3为iacsrna在pbs缓冲液(ph=7.4)中的流体力学直径;图4为iacsrna在pbs缓冲液(ph=7.4)中的zeta电位;图5为iacsrna和mirna的ft-ir光谱;图6为iacsrna的s 2p xps光谱;图7为iacsrna的au 4fxps光谱。
84.基于上述结果可知,本发明提供的一种无限金-巯基配位聚合物([rna-s-au
]n)在au
间的亲油性驱动下,在小纳米尺度下自组装成近球形结构,通过iacsrna的透射电子显微镜(tem)图像和38.7nm附近iacsrna的流体力学直径支持,通过动态光散射分析测量的可接受多分散指数为0.265。此外,iacsrna的表面电荷为-11.1mv,这种电负性表明iacsrna在循环过程中可抵抗coronin并获得较长的半衰期。而且,uv-vis和ft-ir光谱进一步证实了iacsrna的成功组装,巯基修饰rna给出的特征吸光度亦证明了这一点。通过x射线光电子能谱(xps)分析探索了iacsrna中s和au的价态,其中s元素呈现 4价与[mirna-s-au
]n中预期
的分子组成一致(图1)。值得注意的是,iacsrna中au给出的电子能量信号低于au原子的基础电子能量,是由于共轭后电子从s迁移到au,从而进一步证明了无限金-巯基配位聚合物的构建。
[0085]
实施例3
[0086]
本实施例提供了一种无限金-巯基配位聚合物的理化和药学性质试验。
[0087]
将mirna及其相应的iacsrna在含有20%胎牛血清(fbs)的无菌pbs缓冲液中孵育,残基rna通过琼脂糖凝胶电泳进行半定量(图8-a)。试验结果表明,iacsrna将rna的半衰期从3.2
±
0.4h显著地延长到24h以上(图8-b),表明iacsrna可以克服核酸治疗药物的主要药学障碍——较差的全身稳定性。
[0088]
将sulfo-cyanine3(cy3)进行3
’‑
末端偶联,通过流式细胞仪分析进行细胞摄取检查。如图8-c和图8-d所示,孵育6h后,iacsrna(91.6%)比未转染的mirna(39.4%)显示出更多的内化进入b16f10黑色素瘤细胞。iacsrna阻止了巨噬细胞对mirna的摄取(图图8-c和图8-d),为本发明提供的无限金-巯基配位聚合物在体内的循环提供了非常有利的特征。
[0089]
在ph=7.4和ph=6.5条件下,在含20%血清的pbs中孵育不会改变iacsrna的流体力学直径(图8-e),表明coronin较低且胶体稳定性较高。结果与单独mirna相比,iacsrna通过mirna中标记的cy3荧光素的荧光信号定量系统注射后,显著改善了血液中的循环时间(图8-f)。
[0090]
根据纳米颗粒增强的渗透性和滞留性(epr)效应,显著延长的循环时间会促进其在肿瘤内的聚积。本实施例通过电感耦合等离子体质谱法(icp-ms)定量组织中的
197
au浓度测定了iacsrna在黑色素瘤b16f10同种移植模型中的生物分布。静脉注射2mg/kg iacsrna后,在生物分布结果(图8-g)和计算肿瘤与正常器官的蓄积比(图8-h)中可以发现肿瘤蓄积的时间依赖性趋势。为了直观地检测mirna和iacsrna之间不同的肿瘤积累,cy3标记的样本被静脉注射到荷瘤小鼠体内。注射后6h,离体荧光成像和定量(图8-i和图8-j)显示,与cys-mirna处理的小鼠相比,cys-iacsrna处理的小鼠肿瘤聚集超过4倍。
[0091]
综上所述,这些结果证明本实施例提供的无限金-巯基配位聚合物克服了核酸治疗的内在弱点,包括全身稳定性差、清除快、膜通透性低和缺乏肿瘤靶向性。
[0092]
实施例4
[0093]
本实施例提供了一种无限金-巯基配位聚合物的安全性试验。
[0094]
向健康的c57/bl6小鼠分别静脉注射生理盐水(control,对照组)或iacs-mir-30c(iacsrna组,实验组),隔天一次,剂量为10mg/kg,为治疗剂量的5倍(每组n=5),所用iacs-mir-30c来源于实施例1。给药9天后,用戊巴比妥钠对动物实施安乐死,取出器官,用去离子水冲洗,然后用4%多聚甲醛固定。收集小鼠内脏染色切片,观察病理形态学变化,统计小鼠体重和血常规数据。
[0095]
对照组和iacsrna组之间的天冬氨酸转氨酶(alt)、丙氨酸转氨酶(ast)和肝脏病理切片无差异,如图9-a所示。给药9天后,收集血尿素氮(bun)、肌酐(crea)和肾脏苏木精和伊红(h&e)染色切片无差异,其结果如图9-b所示。iacs-mir-30c治疗后未发现溶血、骨髓抑制、贫血、白细胞减少和血小板减少,其结果如图9-c所示。iacs-mir-30c处理对体重几乎没有影响,其结果如图9-d和图9-e所示。
[0096]
基于上述结果,iacs-mir-30c治疗未发现肝毒性,几乎无任何肾毒性,未发现溶
血、骨髓抑制、贫血、白细胞减少和血小板减少,对体重几乎没有影响,此外,在iacs-mir-30c处理的小鼠心脏、肺和脾脏中没有发现病理形态学变化。综上所述,iacs-mir-30c对于临床转化是足够安全的。
[0097]
实施例5
[0098]
本实施例提供了一种无限金-巯基配位聚合物强效抑制wnt/β-catenin通路的试验。
[0099]
mir-30c通过抑制bcl9的表达来抑制致癌性wnt/β-catenin的活化。比较iacs-mir-30c和mir-30c的效力,用b16f10细胞系,一种恶性和wnt过度活跃的黑色素瘤,在50nm浓度下孵育24小时来测验iacs-mir-30c和mir-30c的作用。
[0100]
b16f10细胞在接近100%的融合率下收获。细胞经离心制粒后再悬浮于无菌pbs中。5周龄野生型免疫c57/b6l小鼠皮下接种b16f10细胞(每个部位4
×
106)。当肿瘤达到平均体积为50mm3时,小鼠被随机分成不同的组(n=5),按照结果进行治疗。随后几天观察肿瘤生长和重量。第7天起,每隔2天尾静脉注射不同药物,共4次。肿瘤固定切片,进行ki67、tunel和免疫组织化学染色。
[0101]
实验结果表明,iacs-mir-30c增强了mir-30c在细胞中的聚积,并强效抑制了bcl9的表达,而无载体mir-30c在pbs模拟处理的对照组之间没有表现出差异(图10-a和图10-b)。在转录水平上,rna测序和随后的聚类分析证明iacs-mir-30c和b16f10细胞孵育24小时后导致360个基因差异表达(n=3)(图10-c)。
[0102]
基因集富集分析(gsea)显示,与对照模拟处理的细胞相比,iacs-mir-30c处理的细胞中β-catenin基因集富集了被抑制的特征基因(图10-d、图10-e和图10-f)。
[0103]
同时,wnt信号通路中呈现的被抑制的特征基因也显著富集(图10-g、图10-h和图10-i)。
[0104]
因此,反映在细胞周期、细胞周期检查点和细胞周期有丝分裂的gsea分析中,iacs-mir-30c诱导了癌细胞的细胞周期阻滞(图10-j)。pi染色发现细胞s期百分比显著降低再次证明了这一结论(图10-k)。
[0105]
综上所述,上述结果证明了iacsrna的构建方案在体外恢复了mir-30c的抗肿瘤作用,并强效抑制了wnt/β-catenin通路。
[0106]
实施例6
[0107]
本实施例提供了一种无限金-巯基配位聚合物抑制wnt/β-catenin通路并增强化疗疗效的试验。
[0108]
为了进一步检测iacs-mir-30c的体内效力,本实施例比较探索了其与化疗药物的抗癌作用,并进一步研究了其与化疗的协同增敏作用。
[0109]
为此,通过将手术获得的结肠肿瘤皮下移植到nod/scid小鼠的髂窝,建立了结肠癌患者来源的肿瘤异种移植(pdx)模型(图11-a)。在初次肿瘤切除手术时,将标本切成约5mm的小块,植入4~5周龄nod/scid小鼠的结肠内。通过全外显子组测序(wes)确定结肠肿瘤中的基因突变。肿瘤体积的计算公式为:体积=1/2长
×
宽2。当肿瘤长到约150mm3时,给小鼠静脉注射治疗剂/nacl,剂量为1.5mg/kg,每两天一次。收集异种移植物进行福尔马林固定石蜡包埋(ffpe),在液氮中快速冷冻或随后用同样的程序植入另一组小鼠。
[0110]
在该模型中,通过识别错义突变癌基因表征获得性结肠肿瘤,包括pik3ca(s66t)、
apc(v1822d)、egfr(r521k)、kras(g12d)(图11-b)。值得注意的是,apc的v1822d突变提示wnt信号通路的过度作用,kras的g12d突变意味着高度恶性和临床不治之症。当肿瘤体积达到100
±
30mm3时,荷瘤小鼠接受ns(control)、iacs-mir-30c、5-fu(结肠癌的一线化疗药物)或iacs-mir-30c/5-fu共同治疗,隔天一次,共13天,涉及静脉注射剂量为2mg/kg iacs-mir-30c和/或5mg/kg 5-fu(图11-a)。在第5天,肿瘤的免疫组织化学染色图像显示,iacs-mir-30c显著下调bcl9,并有效抑制β-catenin/wnt信号级联反应,bcl9、β-catenin和两种wnt-下游蛋白c-myc和cyclin d的蛋白水平下降支持了这一点(图11-c)。结果与模拟处理对照组相比,肿瘤体积曲线(图11-d)、肿瘤生长抑制(tgi)效应(图11-e)、肿瘤照片(图11-f)和肿瘤重量(图11-g)结果显示iacs-mir-30c在统计学上显著抑制肿瘤生长的作用强于5-fu。更重要的是,与iacs-mir-30c或5-fu的单药治疗相比,iacs-mir-30c和5-fu之间的联合治疗显示出显著增加的抗肿瘤作用(图11-d~图11-g)提示其协同致敏作用。此外,增殖细胞分析(ki67染色)和凋亡细胞分析(tunel染色)也支持这些结果(图11-h和图11-i)。
[0111]
综上所述,上述结果表明iacs-mir-30c在体内有效地抑制wnt/β-catenin通路,并增强化疗药物5-fu的抗肿瘤作用。
[0112]
实施例7
[0113]
本实施例提供了一种无限金-巯基配位聚合物增强pd-1疗效的试验。
[0114]
肿瘤细胞或肿瘤源性外泌体表达的程序性细胞死亡配体1(pd-l1)与t细胞表达的程序性细胞死亡蛋白1(pd-1)结合,有效刺激细胞毒性cd8
t细胞功能障碍和凋亡,使癌细胞逃避免疫攻击。因此,抗pd-1抗体或抗pd-l1抗体被认为是有效的抗肿瘤药物,但其抗肿瘤反应受到t细胞浸润的抑制。在肿瘤中,wnt信号传导导致t细胞排斥并使机体和对抗pd-l1抗体或抗pd-1抗体治疗耐药。
[0115]
本实施例验证通过lacs-mir-30c抑制wnt信号级联使pd1/pd-l1免疫检查点阻断治疗敏感。为了验证这一点,本实施例建立了一种免疫治疗模型,c57/b6l小鼠在胁腹部皮下接种b16f10细胞,并用iacs-mir-30c、抗pd-1抗体或iacs-mir-30c/抗pd-1抗体组合处理。如图s4和s5所示,iacs-mir-30c抑制b16f10肿瘤中β-catenin/wnt信号级联反应,bcl9、β-catenin、c-myc和cyclin d的蛋白水平下降支持了这一点。与anti-pd-1或iacs-mir-30c单药治疗相比,符合预期地,联合治疗导致调节性t淋巴细胞(cd4
/cd25
细胞,图12-a,图12-b)急剧减少,与肿瘤浸润细胞毒性t淋巴细胞(cd3
/cd8
细胞,图12-c,图12-d)数量增加形成鲜明对比。肿瘤细胞增殖的抑制(图12-e)和肿瘤细胞凋亡的增强(图12-f)也支持iacs-mir-30c对抗pd-1治疗的协同效应。因此,与抗pd-1治疗(37.5%tgi)或iacs-mir-30c治疗(62.7%tgi)相比,iacs-mir-30c/抗pd-1联合治疗导致tgi值显著增加(94.3%tgi)(图12-g和图12-h),与肿瘤照片(图12-i)和肿瘤重量(图12-j)的结果一致。
[0116]
综上所述,上述结果表明,iacs-mir-30c治疗可克服t细胞排斥,并通过抑制wnt信号级联放大抗pd-1抗体治疗中的抗肿瘤作用。
[0117]
基于实施例1~7的结果可见,本发明提供了一种通过温和简单的化学方法将治疗性mirna转化为稳定且生物可利用的iacsrna的通用方法。在自驱动下,iacsrna组装成具有高胶体、抗水解稳定性和低巨噬细胞摄取的球形纳米结构。因此,与正常mirna相比,iacsrna的循环半衰期延长并能在肿瘤部位积累。更重要的是,iacs-mir-30c在5倍治疗剂量注射下没有表现出内脏和血液系统的毒性。本发明提供的iacs-mir-30c在体外和体内有
效抑制wnt信号通路,并有效地提高结肠癌pdx模型中5-fu和黑色素瘤b16f10同种移植模型中anti-pd1的效力。
[0118]
如上所述,即可较好地实现本发明,上述的实施例仅仅是对本发明的优选实施方式进行描述,并非对本发明的范围进行限定,在不脱离本发明设计精神的前提下,本领域普通技术人员对本发明的技术方案做出的各种改变和改进,均应落入本发明确定的保护范围内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。