1.本发明属生物技术领域,具体涉及一种一种负载一氧化氮的靶向载药胶束。
背景技术:
2.肿瘤仍然是人类健康面临的最大问题之一。毋庸置疑,纳米药物的发展,为抗肿瘤的递送提供了革新性的方法,并且已有市售药物如doxil、onivyde、abraxane、vyxeos和genexol-pm等出现。通过调控药物的体内分布,纳米药物可提高临床给药效率,降低负作用。但是,纳米药物的临床收益,特别是针对实体瘤,却令人失望(nat.commun.2018,9,3390.)。例如,相比于母体药物,市售纳米药物不能明显提高病人的中位生存期(nat.rev.cancer 2017,17,20-37.)。纳米药物未能引起革新性转变,在近期引起了众多科学家的质疑(j.control.release 2019,305,221-222.)。
3.正常组织中的微血管内皮间隙致密、结构完整,大分子和脂质颗粒不易透过血管壁,而实体瘤组织中血管丰富、血管壁间隙较宽、结构完整性差,淋巴回流缺失,造成大分子类物质和脂质颗粒具有选择性高通透性和滞留性,这种现象被称作实体瘤组织的高通透性和滞留效应,简称epr效应。纳米药物主要依靠epr效应,在肿瘤组织的选择性分布,增加药效并减少系统副作用(cancer res.1986,46,6387-6392.)。但是由于血管功能不完善,同时也导致了通过血液运输的纳米药物在向肿瘤运输出现困难。同时,没有足够证据可以在临床上证明epr效应(j.control.release 2019,311-312,322
–
323.)。有临床证据证明doxil在肿瘤中的靶向蓄积不足,而长时间暴漏在低浓度的化疗药物下还容易使肿瘤出现耐药性。因此,仅依赖epr效应的纳米药物设计,需要从别的角度来考虑以提高其在肿瘤中的蓄积。
4.临床上为了提高药物在肿瘤中的蓄积,在介入治疗可通过热灌注方式给药,具体来讲是提前将药液加热至约50度,再灌注至肿瘤处以扩张血管、提高药物的蓄积和渗透(canc.j.2009,15,249-254.)。一氧化氮是一种重要的小分子信号分子,可扩张血管、整合血管上皮细胞、促进血液灌流和血管正常化。临床上目前也有在给化疗药的同时,尝试给予一氧化氮小分子前药,以提高化疗效果。
5.但是一氧化氮本身是一种气体分子,同时容易与血液中氧气发生淬灭作用,将一氧化氮直接递送至肿瘤处极其困难(chem.rev.2002,102,1091-1134.)。因此,一氧化氮供体(也称为一氧化氮前药)称为可能的策略(acsnano 2020,14,2024-2035.)。小分子供体如亚硝基硫醇或s-亚硝基化谷胱甘肽,在体内半衰期短并且难以蓄积于肿瘤处(mol.pharmaceutics 2019,16,409-421.);基于重金属配合物的供体可能带来潜在的生理毒性(chem.commun.2011,47,10776-10778.)。
6.因此,向肿瘤共递送化疗药物与一氧化氮成为一个在临床和医药工业中重要又有挑战性的课题,
技术实现要素:
7.本发明的目的提供一种负载一氧化氮的靶向载药胶束。
8.本发明提出的一种负载一氧化氮的靶向载药胶束,所述胶束由一氧化氮以前药形式储存在聚合物给药载体上组装而成,所述聚合物给药载体是基于聚乙二醇、聚赖氨酸和聚苯丙氨酸的三嵌段聚合物。
9.本发明中,所述聚合物给药载体上的10%聚合物材料由靶向功能基团修饰。
10.本发明中,所述靶向功能基团指的是由缬氨酸-精氨酸-甘氨酸-天冬氨酸-谷氨酸构建的环装多肽:crgd肽。
11.本发明中,所述胶束粒径为40-60纳米,z电势为 15-30毫伏。
12.本发明中,所述胶束粒径为43.9纳米,z电势为20.9毫伏。
13.本发明提出的负载一氧化氮的靶向载药胶束在肿瘤新生血管和肿瘤细胞中的应用,所述靶向载药胶束可以靶向分布在肿瘤细胞表面与新生血管表面的与肿瘤相关的整合素αvβ3。
14.本发明提出的负载一氧化氮的靶向载药胶束在化疗药物中的应用,其特征在于,所述化疗药物为疏水性药物(如阿霉素),或疏水性化疗药物。
15.本发明中,所述疏水性药物(如阿霉素)的载药量为10.8%,包封率为83.1%。
16.本发明中,该负载有一氧化氮靶向载药胶束可靶向肿瘤后、在肿瘤微环境下释放一氧化氮。
17.本发明中,该载药胶束可扩张肿瘤处毛细血管和促进新生血管熟化。
18.本发明中,可直接促进肿瘤细胞凋亡。
19.本发明中,该负载有一氧化氮靶向载药胶束可显著使肿瘤细胞凋亡和抑制肿瘤生长。
20.本发明的有益效果如下:
21.(1)一氧化氮的释放和药物的释放在同一个位置,起到良好的协同作用。
22.(2)本发明同时递送对肿瘤细胞杀伤的一氧化氮和细胞毒类化疗药,联合治疗肿瘤疗效达到1 1>2的效果。
23.(3)本发明中设计的基于聚乙二醇-聚赖氨酸-聚苯丙氨酸胶束系统,可体内长循环和体内降解能力,无生理毒性。
24.综上,本发明提供了一种可供临床或科研选择的向肿瘤共递送化疗药物与一氧化氮的方法,有望解决目前临床和纳米医药工业出现的问题。
附图说明
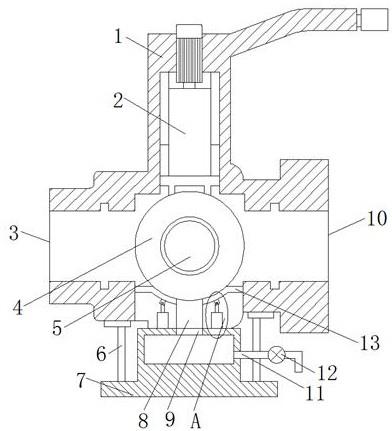
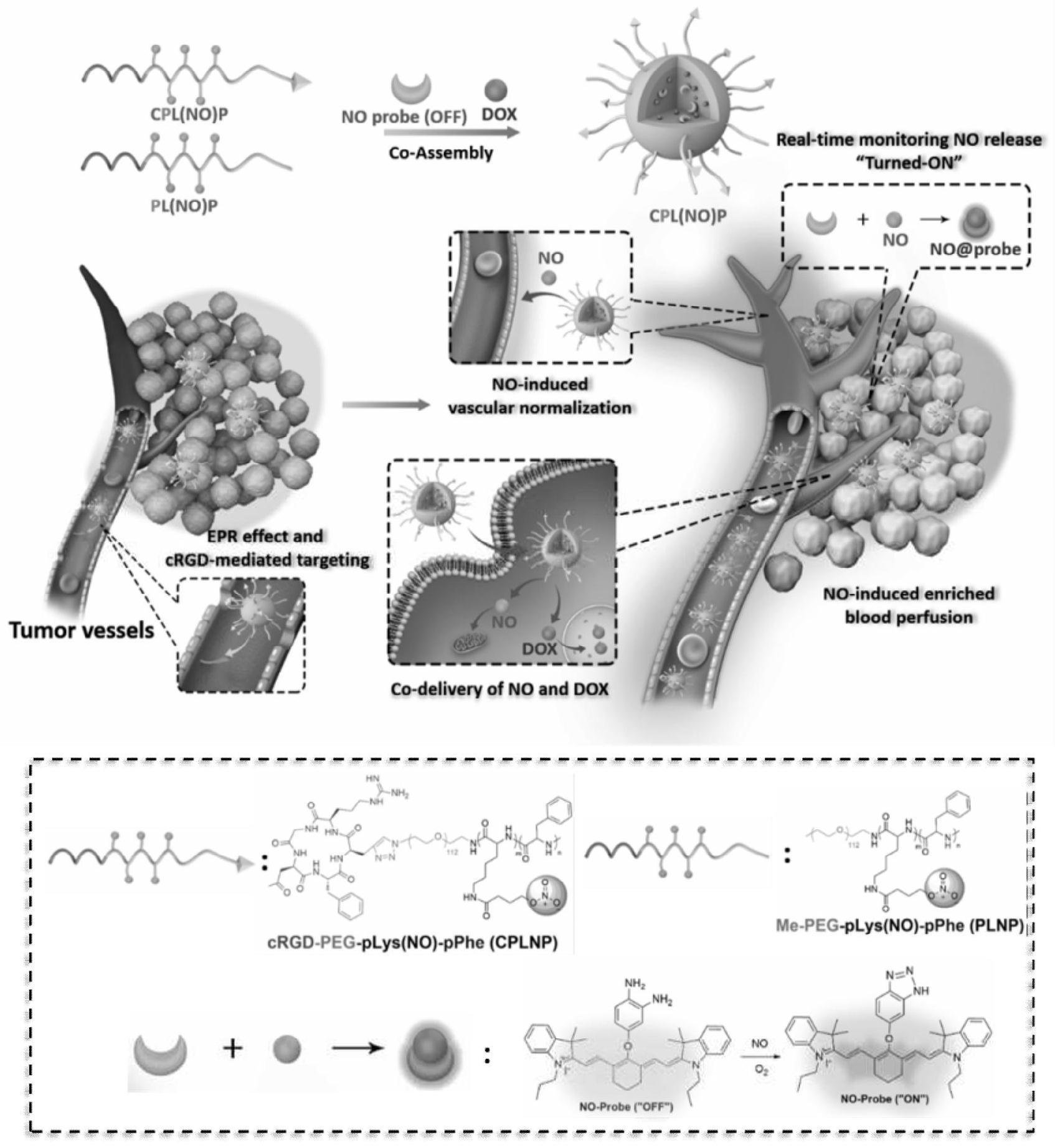
25.图1为向肿瘤共递送化疗药物与一氧化氮的方法和联合抗肿瘤的示意图;
26.图2为携带一氧化氮聚合物plnp及靶向聚合物cplnp的化学合成步骤;
27.图3为掺杂不同比例cplnp的靶向胶束的细胞摄取情况。a为在人脐静脉内皮huvec细胞和b为人三阴性乳腺癌md-mba-231细胞上的摄取情况;c为掺杂不同比例cplnp的靶向胶束被huvec细胞摄取的流式细胞术结果;d为利用流式细胞术检测掺杂10%的靶向胶束(简称cplnp)被不同抑制剂抑制的huvec细胞摄取情况;e为掺杂不同比例cplnp的靶向胶束被md-mba-231细胞摄取的流式细胞术结果;f为cplnp胶束被不同抑制剂抑制的md-mba-231
细胞摄取情况;g为cplnp胶束被huvec细胞摄取后荧光变化情况;h为cplnp胶束被md-mba-231细胞后激光扫描共聚焦显微镜下观察荧光变化情况;
28.图4中a为荷三阴性乳腺癌鼠尾静脉注射负载ir780不同制剂在不同时间下小动物活体成像仪观察结果;b为荷三阴性乳腺癌鼠尾静脉注射负载ir780不同制剂的离体器官及肿瘤在12小时下小动物活体成像仪观察结果;c为荷三阴性乳腺癌鼠尾静脉注射负载bodipy不同制剂的切片观察结果(cd31标定肿瘤新生血管;dapi标定细胞核;bodipy标定胶束);d为荷三阴性乳腺癌鼠尾静脉注射负载ir780不同制剂在12小时时小动物活体成像仪3d成像重构结果;e为荷三阴性乳腺癌鼠尾静脉注射负载一氧化氮近红外探针(off至on型)在不同时间下小动物活体成像仪观察结果;f为荷三阴性乳腺癌鼠尾静脉注射负载一氧化氮近红外探针(off至on型)在不同时间下小动物光声成像系统观察结果;
29.图5利用cck-8方法检测不同制剂组对md-mba-231细胞的a)细胞毒性和b)ic
50
数值(n=6);c为体内抗肿瘤实验策略(注射量为5mg dox/kg体重);不同制剂组处理后荷瘤鼠(n=6)的d为离体瘤;e为瘤重量;f为瘤体积;g为荷瘤鼠体重变化;h为离体瘤组织切片观测图(tunel结果);
30.图6中a为肿瘤区域扩张血管及新生血管机理示意图;b为利用光声成像观测含no纳米药物处理24小时后肿瘤区域血氧含量变化;c为不同制剂组处理荷瘤鼠离体瘤组织冰冻切片中代表性荧光图片(cd31代表肿瘤新生血管);d为不含化疗药物、仅用携带一氧化氮的纳米药物处理荷瘤鼠后离体瘤组织切片观测细胞凋亡情况(tunel结果);
31.图7为免疫组化法分析不同制剂组治疗荷瘤鼠后心肝脾肺肾的结果用于分析生理毒性;
32.图8为利用动态光散射仪分析25度下pbs7.4中cplnp/dox和plnp/dox的z电位结果;
33.图9为10毫摩尔谷胱甘肽存在与否下随时间cplnp/dox的粒径变化情况;
34.图10为掺杂不同比例cplnp的靶向胶束被huvec细胞摄取的流式细胞术结果(a:空白对照;b:掺杂0%;c:掺杂10%;d:掺杂20%;e:掺杂40%;f:掺杂80%;);
35.图11为掺杂不同比例cplnp的靶向胶束被md-mba-231细胞摄取的流式细胞术结果(a:空白对照;b:掺杂0%;c:掺杂10%;d:掺杂20%;e:掺杂40%;f:掺杂80%;);
36.图12为利用流式细胞术检测掺杂10%的靶向胶束(简称cplnp)被不同抑制剂抑制的huvec细胞摄取情况(a:靶向胶束为阳性对照;b:添加过量crgd用以饱和受体;c:4度处理;d:氧化苯胂处理;e:菲律平处理;f:秋水仙碱处理);
37.图13为利用流式细胞术检测掺杂10%的靶向胶束(简称cplnp)被不同抑制剂抑制的md-mba-231细胞摄取情况(a:靶向胶束为阳性对照;b:添加过量crgd用以饱和受体;c:4度处理;d:氧化苯胂处理;e:菲律平处理;f:秋水仙碱处理);
38.图14为氘代氯仿、室温下phe-nca的核磁共振氢谱(400mhz);
39.图15为氘代二甲亚砜、室温下n
3-peg-lys-phe(1:16:22)的核磁共振氢谱(400mhz);
40.图16为氘代二甲亚砜、室温下rgd-peg-lys-phe(1:16:20)的核磁共振氢谱(400mhz);
41.图17为氘代二甲亚砜、室温下ch3o-peg-lys-phe(1:7:11)的核磁共振氢谱
(400mhz);
42.图18为氘代二甲亚砜、室温下ch3o-peg-lys(no)-phe(1:10:10)的核磁共振氢谱(400mhz);
43.图19为氘代二甲亚砜、室温下ch3o-peg-lys(cbz)-phe(1:10:17)的核磁共振氢谱(400mhz);
44.图20为氘代二甲亚砜、室温下ch3o-peg-lys(br)-phe(1:12:15)的核磁共振氢谱(400mhz)。
具体实施方式
45.以下通过具体实施方式详细说明本发明的技术方案,应理解以下的具体实施方案仅为示例性,任何改动或变化只要不脱离本发明的技术方案设计,都应在本发明权利的要求保护范围之内。
46.实施例1:
47.胶束构建材料合成方法:开环聚合单体的制备:称取lys(z)3g(10.7mmol)和三光气1.27g(4.28mmol)于100ml两口瓶中,油泵抽真空,氮气保护,用注射器注入无水thf(30ml),50℃油浴中搅拌反应3h。反应结束后冷却至室温,将反应液滴入至无水正己烷(150ml)中并不断搅拌,析出白色结晶,-20℃中结晶过夜,抽滤干燥得到白色固体lys(z)-nca。同样,称取phe 3g(18.2mmol)和三光气2.69g(9.08mmol),按照上述操作得到白色固体phe-nca。利用1h nmr对上述两种活化单体的结构进行鉴定。
48.聚合物mpeg-plys-pphe和n
3-peg-plys-pphe的合成分别以ch3o-peg-nh2和n
3-peg-nh2为引发剂,按照开环聚合反应进行。称取ch3o-peg-nh2或n
3-peg-nh
2 1g(0.2mmol)于100ml两口瓶中,加入lys(z)-nca 735mg(2.4mmol),油泵抽真空,氮气保护,用注射器注入无水dmf(20ml),50℃油浴中搅拌反应48h。向反应液中加入phe-nca 1.15g(6.0mmol)和无水dmf(30ml),油泵抽真空,氮气保护,50℃油浴中继续反应48h。反应结束后冷却至室温,将反应液缓慢倒入至无水乙醚(500ml)中并不断搅拌,析出白色沉淀,-20℃中沉淀过夜,抽滤干燥得到白色固体peg-plys(z)-pphe。将此白色固体加入至tfa(10ml)和hbr/hoac(0.5ml)的混合体系中,室温搅拌反应3h后,将反应液转移至透析袋中(mw 1000),置于2l纯水中透析24h,每8h换一次水,冷冻干燥得到淡黄色固体peg-plys-pphe。利用1h nmr对上述聚合物的结构进行鉴定。
49.一氧化氮修饰的聚合物的合成:搅拌下peg-plys-pphe(1:6:20分子比,200mg,0.023mmol)和吡啶(7.1mg,2mmol,)溶解到无水dmf(10ml)中。4-溴丁酰氯(16.5mg,2mmol)溶解到无水dmf(2ml)中,在0度、氩气气氛下滴入到上述溶液中,并在0度、氩气气氛下搅拌4小时,室温、氩气气氛下搅拌20小时。之后利用减压蒸除dmf,残余物滴到0度乙醚(20ml)中,并重复三次,残余固体重溶于纯水(5ml)中并转移至透析袋中(mw 2000),置于4l纯水中透析24h,每8h换一次水,冷冻干燥得到淡黄色固体peg-plys(br)-pphe。利用1h nmr对上述聚合物的结构进行鉴定。peg-plys(br)-pphe(200mg,0.021mmol)和硝酸银(214mg,1.26mmol)溶解至无水乙腈(20ml)中,并在暗处搅拌24小时。之后利用减压蒸除乙腈,残余物滴到0度乙醚(20ml)中,并重复三次,残余固体重溶于纯水(5ml)中并转移至透析袋中(mw 2000),分别置于4l的edta(除去银离子)和纯水中透析24h,每8h换一次水,冷冻干燥得到淡黄色固体
peg-plys(no)-pphe(简称plnp)。利用1h nmr对上述聚合物的结构进行鉴定。
50.称取peg-plys(no)-pphe和炔丙基化的crgd(2equiv)于两口瓶中,油泵抽真空,氮气保护。称取cui(0.5equiv)和抗坏血酸钠(1equiv),溶于无水dmf中,加入dipea(1equiv)。将此混合溶液用注射器迅速加入至两口瓶中,30℃搅拌反应12h。将反应液转移至透析袋中(mw1000),置于2l 10mm edta-2na的水溶液(ph 7.0)中透析12h,转移至2l纯水中继续透析12h,冷冻干燥后得到白色固体crgd-peg-plys(no)-pphe(简称cplnp)。利用1h nmr对其结构进行鉴定。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。