一种定量检测gdf-15的试纸条和试剂盒
技术领域
1.本发明属于分子生物学技术领域,尤其涉及一种定量检测gdf-15的试纸条和试剂盒。
背景技术:
2.生长分化因子-15(growth differentiation factor-15,gdf-15)是转化生长因子β(transforming growth factorβ,tgf-β)超家族成员的一个远支,gdf-15是一种应激反应蛋白,生理情况下gdf-15在前列腺和胎盘中高表达,在多数其他组织中微弱表达,包括心脏组织。但是在病理和环境应激情况下,如缺血/再灌注损伤、心脏高压力负荷、心力衰竭和动脉粥样硬化等,gdf-15在心肌细胞中大量表达,对心肌细胞结构和凋亡程序发挥调节作用,特殊生理病理下,gdf-15表达量也显著上升,如手术、缺血、缺氧等引起的心肌、肾、肺或肝损伤,前列腺癌、乳腺癌、结肠癌等肿瘤病灶部位也存在高表达。大量临床与基础研究证实gdf-15是一个重要的心血管保护因子。作为新的标志物,gdf-15水平与多种心血管疾病的诊断、危险分层和预后判断有密切关系。gdf-15水平与多种肿瘤密切相关。尽管对各种肿瘤发生时gdf-15水平变化观点不一致,大多数研究表明gdf-15在多种肿瘤中表达升高。但从基因及细胞水平均能证实gdf-15能抑制肿瘤细胞生长、侵袭和转移,促进肿瘤细胞凋亡。
3.gdf-15能促进胚胎期鼠的多巴胺能神经元的生存和分化。在体内外都能促进损伤多巴胺能神经元的生存,并且伴随着皮质的损伤在神经元中被诱导。近年来,gdf-15水平与脑血管疾病的关系逐渐受到关注。脑血管疾病及脑损伤等情况下,血清gdf-15水平均升高,并能对疾病严重程度进行预测,然而其保护作用仍有争议。
4.时间分辨荧光免疫测定(trfia)是一种非同位素免疫分析技术,它用镧系元素标记抗原或抗体,根据镧系元素螯合物的发光特点,用时间分辨技术测量荧光,同时检测波长和时间两个参数进行信号分辨,可有效地排除非特异荧光的干扰,极大地提高了分析灵敏度。但是由于gdf-15检测在免疫层析试剂中实现性能的开发有较大难度,所以现有技术中还未有关于使用时间分辨荧光免疫测定样本中gdf-15的含量的报道。
技术实现要素:
5.有鉴于此,本发明的目的在于提供一种不具有结合垫的能够定量检测gdf-15的试纸条,在简化试纸条组分的基础上仍旧能够准确检测gdf-15,且检出限低,检测精密度、准确度高,能够达到临床诊断的需求。
6.为了实现上述发明目的,本发明提供了以下技术方案:
7.本发明提供了一种定量检测gdf-15的试纸条,所述试纸条由样品垫、层析膜和吸水纸组成;
8.所述样品垫上包被有荧光微球标记鼠抗人gdf-15单克隆抗体和荧光微球标记兔igg多克隆抗体;
9.所述层析膜上设置有t检测线和c质控线,所述t检测线上包被有鼠抗人gdf-15多
克隆抗体,所述c质控线上包被有羊抗兔igg多克隆抗体。
10.优选的,所述样品垫经样品垫处理溶液预处理后所得,所述样品垫处理溶液包括质量浓度为0.02%-0.04%抗红细胞抗体和质量浓度为0.01%-0.04%hbr阻断剂的0.1m-0.2m tris-hcl缓冲液,所述tris-hcl缓冲液的ph为8.0。
11.优选的,在样品垫上包被荧光微球标记鼠抗人gdf-15单克隆抗体时,所用的喷膜液为含有0.5%-1.5%tween20、0.25%-0.5%酪蛋白、2%-5%海藻糖、0.5%-0.75%的pvp 40000和0.9%nacl的0.05-0.1m硼酸-硼砂缓冲液,所述硼酸-硼砂缓冲液的ph为8.0。
12.优选的,制备荧光微球标记鼠抗人gdf-15单克隆抗体和制备荧光微球标记兔igg多克隆抗体时,所用封闭液为含有1%-2%bsa、1%-2%tween20的0.05-0.1m tris-hcl溶液,所述tris-hcl溶液的ph为8.0。
13.优选的,所述荧光微球标记鼠抗人gdf-15单克隆抗体的浓度为0.08~0.20mg/ml。
14.优选的,所述荧光微球标记兔igg多克隆抗体的浓度为0.08~0.20mg/ml。
15.优选的,所述鼠抗人gdf-15多克隆抗体的喷涂浓度为0.8~2.0mg/ml。
16.优选的,所述羊抗兔igg多克隆抗体的喷涂浓度为0.8~2.0mg/ml。
17.优选的,所述t检测线的宽度为0.5~1.5mm,所述c质控线的宽度为0.5~1.5mm。
18.本发明还提供了一种定量检测gdf-15的试剂盒,包括上述试纸条和稀释液;
19.所述稀释液为含质量浓度为0.2%-0.5%bsa、0.5%-1.0%pvp 40000、1.0-2.0%蔗糖和0.5%-1.0%吐温20的硼酸缓冲液溶液,所述硼酸缓冲液溶液的浓度为0.1~0.2m。
20.本发明的有益效果:
21.本发明首次提供了一种能够定量检测gdf-15的试纸条,简化了试纸条的组分,不含有结合垫。本发明对样品垫进行了特殊的预处理,在简化试纸条组分的基础上还提高了试纸条的性能。
22.本发明通过改进偶联过程配方、微球喷膜液配方、稀释液配方、标记浓度、包被浓度等,最终使试纸条的性能能够达到临床检测gdf-15的需求。本发明试纸条具有较好的线性范围,检出限低,精密度高和准确度高,稳定性好,在4-30℃保存18个月后,其性能还满足线性范围、最低检出限、精密度和准确度各项参数。
附图说明
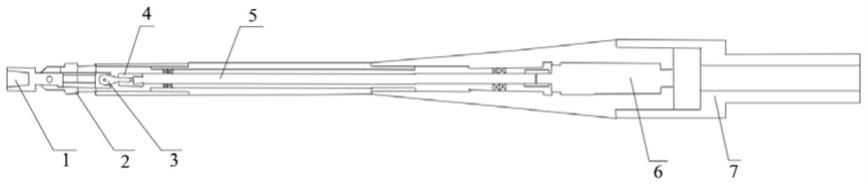
23.图1为本发明定量检测gdf-15试纸条的结构图。
具体实施方式
24.本发明提供了一种定量检测gdf-15的试纸条,所述试纸条由样品垫、层析膜和吸水纸组成;
25.所述样品垫上包被有荧光微球标记鼠抗人gdf-15单克隆抗体和荧光微球标记兔igg多克隆抗体;
26.所述层析膜上设置有t检测线和c质控线,所述t检测线上包被有鼠抗人gdf-15多克隆抗体,所述c质控线上包被有羊抗兔igg多克隆抗体。
27.本发明试纸条不具有结合垫,由样品垫、层析膜和吸水纸组成,将待测样本滴入样品垫,样本中的待测物在层析作用下与样品垫上荧光微球标记的抗体形成复合物,复合物
继续层析至层析膜的t检测线,被抗体捕获。样本中的待测物越多,在t检测线聚集的荧光微球越多,t检测线的荧光信号越强,检测线与c质控线的荧光信号比值与样本中的待测物量呈正相关关系。该荧光抗体的信号强度可通过荧光免疫检测仪检测和分析,进而准确的定量检测样本中gdf-15的含量。
28.本发明对于样品垫、层析膜和吸水纸的具体材质没有特殊要求,采用本领域常规制备试纸条使用的材质均可,在本发明具体实施例中,所述样品垫选择的是玻璃纤维,所述层析膜选择的是硝酸纤维素膜。在本发明中,所述样品垫上标记有荧光微球标记鼠抗人gdf-15单克隆抗体和荧光微球标记兔igg多克隆抗体,所述鼠抗人gdf-15抗体从abcam购买,所述兔igg多克隆抗体从长沙博优生物购买。在本发明中,所述荧光微球采用金属铕元素螯合物与苯乙烯单体共聚得到,生产厂家为bangs laboratories。
29.在本发明中,所述样品垫优选的是经样品垫处理溶液预处理后所得,所述样品垫处理溶液优选的包括质量浓度为0.02%-0.04%抗红细胞抗体和质量浓度为0.01%-0.04%hbr阻断剂的0.1-0.2m tris-hcl缓冲液,所述tris-hcl缓冲液的ph为8.0,更优选的包括质量浓度为0.03%抗红细胞抗体和质量浓度为0.02%-0.03%hbr阻断剂的0.15m tris-hcl缓冲液,所述tris-hcl缓冲液的ph为8.0,经本发明样品垫处理溶液预处理,使样品垫兼具样品垫和结合垫功能,简略了试纸条结构。
30.在本发明中,荧光微球标记鼠抗人gdf-15单克隆抗体的制备方法优选的包括如下步骤:将荧光微球溶液与硼酸-硼砂缓冲液混合、涡漩、超声、离心,得到第一沉淀;将第一沉淀用edc溶液进行活化、离心,得到第二沉淀;将第二沉淀与鼠抗人gdf-15单克隆抗体溶液、硼酸-硼砂缓冲液混合、反应,得到反应物,离心,得到第三沉淀;将第三沉淀经封闭液封闭过夜,得到鼠抗人gdf-15单克隆抗体。
31.在本发明中,所述荧光微球溶液的浓度优选为5-10mg/ml;所述硼酸-硼砂缓冲液的浓度优选为0.01-0.02mol/l,ph值优选为7.4-7.6。在本发明中,所述荧光微球溶液与硼酸-硼砂缓冲液的体积比优选为1:9-1:19。
32.本发明对于涡旋和超声的具体方式没有特殊限定,采用本领域常规涡旋、超声方式均可。在本发明中,所述漩涡的时间优选为20-30s,所述超声的时间优选为2~5min,所述超声的频率优选为50-100khz。在本发明中,所述离心的转速优选为14000-15000rpm,所述离心的温度优选为4-8℃,所述离心的时间优选为15-20min。
33.本发明对于edc溶液的具体来源没有特殊限定,采用本领域常规市售产品均可。在本发明中,所述edc溶液的浓度优选为20-30g/l,所述活化的时间优选为15~30min。在本发明中,每100μl的荧光微球溶液经处理后得到的第一沉淀优选用20-30μl的edc溶液进行活化。
34.在本发明中,所述鼠抗人gdf-15单克隆抗体溶液的浓度优选为80~200μg/ml。每100μl的荧光微球溶液经处理后得到的第二沉淀优选的与浓度为100-200μg/ml的gdf-15单克隆抗体溶液、900-1900ul的硼酸-硼砂缓冲液混合。在本发明中,所述反应的时间优选为2~4h,更优选为3h。
35.在本发明中,所述封闭液优选的为含有1%-2%bsa、1%-2%tween20的0.05-0.1m tris-hcl溶液,所述tris-hcl溶液的ph为8.0。
36.在本发明中,所述荧光微球标记兔igg多克隆抗体的制备方法同荧光微球鼠抗人
gdf-15单克隆抗体的制备方法,在此不再赘述。
37.在本发明中,将得到的荧光微球鼠抗人gdf-15单克隆抗体和荧光微球标记兔igg多克隆抗体分别溶于喷膜液中,再分别均匀地喷涂在样品垫上,37℃干燥3h,得到样品垫。所述喷膜液为含有0.5%-1.5%tween20、0.25%-0.5%酪蛋白、2%-5%海藻糖、0.5%-0.75%的pvp 40000和0.9%nacl的0.05-0.1m硼酸-硼砂缓冲液,所述硼酸-硼砂缓冲液的ph为8.0。
38.在本发明中,所述喷膜液中含标记有鼠抗人gdf-15单克隆抗体的荧光微球,所述鼠抗人gdf-15单克隆抗体标记的浓度优选为0.08~0.20mg/ml,更优选为0.1~0.15mg/ml;所述喷膜液中含标记有兔igg多克隆抗体的荧光微球,将荧光微球标记兔igg多克隆抗体溶于喷膜液后,所述兔igg多克隆抗体标记的浓度优选为0.08~0.20mg/ml,更优选为0.1~0.15mg/ml。
39.在本发明中,所述t检测线上包被有鼠抗人gdf-15多克隆抗体,所述鼠抗人gdf-15多克隆抗体的喷涂浓度优选为0.8~2.0mg/ml,更优选为1.5mg/ml;所述c质控线上包被有羊抗兔igg多克隆抗体,所述羊抗兔igg多克隆抗体的喷涂浓度优选为0.8~2.0mg/ml,更优选为1mg/ml。在本发明中,所述t检测线和c质控线的宽度独立的优选为0.5~1.5mm,更优选为1mm。在本发明中,所述c质控线距离吸水纸的距离优选为7.8~8.2mm,所述t检测线距离c质控线的距离优选为14.8~15.2mm。
40.本发明优选在硝酸纤维素膜上划t检测线和c质控线,划痕消失后,在37℃下避光干燥24h,得到层析膜。
41.本发明对于试纸条的具体制备方法没有特殊限定,采用本领域常规试纸条的制备方法均可,如将所述样品垫、层析膜和吸水纸依次搭接在pvc板上,进行裁剪,得到试纸条。在本发明具体实施例中,所述裁剪是按照4
±
0.1mm
×
75mm的规格进行。
42.本发明还提供了一种定量检测gdf-15的试剂盒,包括上述试纸条和稀释液;
43.所述稀释液为含质量浓度为0.2%-0.5%bsa、0.5%-1.0%pvp 40000、1.0-2.0%蔗糖和0.5%-1.0%吐温20的硼酸缓冲液溶液,所述硼酸缓冲液溶液的浓度为0.1~0.2m。
44.在本发明中,所述稀释液优选的为含质量浓度为0.3%-0.4%bsa、0.6%-0.9%pvp 40000、1.3-1.7%蔗糖和0.6%-0.8%吐温20的硼酸缓冲液溶液,所述硼酸缓冲液溶液的浓度优选为0.15~0.18m。
45.本发明对于bsa、pvp40000、蔗糖、吐温和硼酸的来源没有特殊限定,采用本领域常规市售产品均可。在本发明中,所述定量检测gdf-15的试剂盒优选的还包括sd卡,用于校准和质控,本发明对sd卡的来源没有特殊限定,采用本领域常规市售产品均可。
46.采用本发明试剂盒对待测样本中gdf-15的含量进行检测时,所述待测样本优选的为血清或血浆。本发明所述试剂盒的使用方法优选的包括如下步骤:吸取100μl血清或血浆样本,加入300-500ul的稀释液中,混匀后吸取100ul滴加至样品垫,反应10-15min。使用干式荧光免疫分析仪检测模块通过发光二极管发射特殊紫外光,当紫外光照射到层析膜上的t检测线和c质控线时,t检测线和c质控线位置的荧光微球双抗夹心复合物在紫外光的照射下呈现荧光条带,干式荧光免疫分析仪检测模块的光电二极管将检测到的荧光转化成电信号,测得t/c比值,通过干式荧光免疫分析仪的软件程序将t/c比值换算为gdf-15的浓度。
47.下面结合实施例对本发明提供的技术方案进行详细的说明,但是不能把它们理解
为对本发明保护范围的限定。
48.实施例1
49.样品垫的制备:
50.样品垫预处理:将样品垫处理溶液(含质量浓度为0.02%抗红细胞抗体、0.01%hbr阻断剂的浓度为0.1m的tris-hcl缓冲液(ph8.00)溶液)分别均匀地喷涂在玻璃纤维上,37℃干燥4h,得到处理的玻璃纤维。
51.荧光微球标记鼠抗人gdf-15单克隆抗体的制备:将100μl时间分辨荧光微球(10mg/ml)和900μlph=7.4的0.01mol/l的硼酸-硼砂缓冲液加入2ml的ep管中,涡旋20s,超声2min;将混合液在15000rpm、4℃下离心15min,弃去上清;沉淀使用1ml的ph=7.4的0.01mol/l的硼酸-硼砂缓冲液复溶后,加入20μl的30g/l的edc溶液进行活化,活化时间为15min。活化完成的混合液在15000rpm、4℃下离心15min后,弃去上清,取沉淀,在沉淀中加入100μg/ml的鼠抗人gdf-15单克隆抗体和1ml的ph=7.4的0.01mol/l的硼酸-硼砂缓冲液,反应时间为2h,反应完成后,直接向悬液中加入100μl的封闭液(含1%bsa、1%tween20的0.05m tris-hcl溶液,ph为8.0),封闭过夜,洗涤就可以得到荧光微球标记鼠抗人gdf-15单克隆抗体。
52.采用与荧光微球标记鼠抗人gdf-15单克隆抗体相同的制备方法制备荧光微球标记兔igg多克隆抗体。
53.将荧光微球标记鼠抗人gdf-15多克隆抗体、荧光微球标记兔igg多克隆抗体分别溶于含0.5%tween20、0.25%酪蛋白、2%海藻糖、0.5%的pvp 40000、0.9%nacl的0.05m硼酸-硼砂缓冲液(ph为8.0)的喷膜液中,使荧光微球标记鼠抗人gdf-15单克隆抗体的浓度为0.08mg/ml,使荧光微球标记兔igg多克隆抗体的浓度为0.08mg/ml,将得到的溶液分别均匀地喷涂在经处理的玻璃纤维上,37℃下干燥3h,得到样品垫。
54.层析膜的制备:
55.层析膜黏贴:将25
×
300mm的硝酸纤维素膜贴在78
×
300mm的pvc底板上;
56.包被液配制:使用磷酸缓冲液分别配置t线和c线包被液,t线gdf-15多克隆抗体浓度为1.5mg/ml,c线羊抗兔多抗浓度为1mg/ml;
57.层析膜包被与干燥:c线划在距离吸水纸端8mm处,t线划在距离吸水纸端15mm处,所述c线和t线的宽度均为0.5mm。室温放置至nc膜上划痕液消失后,放入烘箱中37℃下避光干燥24h,得层析膜。
58.将样品垫、层析膜和吸水纸依次搭接在pvc板上,按照4mm
×
75mm规格进行裁剪,得到试纸条,结构如图1所示。
59.实施例2
60.与实施例1的区别在于喷涂在经处理的玻璃纤维上的荧光微球标记鼠抗人gdf-15单克隆抗体的浓度为0.2mg/ml,荧光微球标记兔igg多克隆抗体的浓度为0.2mg/ml,其余均同实施例1。
61.实施例3
62.与实施例1的区别在于层析膜上t线gdf-15多克隆抗体浓度为0.8mg/ml,c线羊抗兔多抗浓度为0.8mg/ml,所述c线和t线的宽度均为1.5mm,其余均同实施例1。
63.实施例4
64.与实施例1的区别在于层析膜上t线gdf-15多克隆抗体浓度为2.0mg/ml,c线羊抗兔多抗浓度为2.0mg/ml,所述c线和t线的宽度均为1mm,其余均同实施例1。
65.实施例5
66.将实施例1制备得到的试纸条和稀释液组成能够定量检测gdf-15的试剂盒,其中稀释液为含质量浓度为0.5%bsa、0.5%pvp 40000、1.0%蔗糖、1.0%吐温的浓度为0.2m的硼酸缓冲液溶液。
67.实施例6
68.检测实施例5所得试剂盒的线性范围:
69.分别使用50pg/ml、100pg/ml、500pg/ml、1000pg/ml、2000pg/ml的参考品进行检测,每个样本检测三次,计算平均值后,将测定的平均值与理论浓度进行线性方程拟合,得到线性回归方程,并计算线性相关系数r,结果见表1。其中,参考品为含相应浓度的gdf-15抗原溶液,溶剂为含质量百分含量为1%bsa、含质量百分含量为10%甘露醇的0.01m pbs。
70.表1试剂盒的线性范围检测结果
[0071][0072]
由表1可以看出,本发明试剂盒检测gdf-15的线性范围为50pg/ml~2000pg/ml,线性相关系数r≥0.990。
[0073]
实施例7
[0074]
检测实施例5所得试剂盒的最低检出限
[0075]
用含质量浓度为0.5%bsa、0.5%pvp 40000、1.0%蔗糖、1.0%吐温的浓度为0.2m的硼酸缓冲液溶液作为空白样本重复检测10次,得出10次检测结果,计算其平均值(m)和标准差(sd),以空白均值加两倍标准差(m 2sd)报告最低检出限,结果见表2。
[0076]
表2试剂盒的最低检出限检测结果
[0077][0078][0079]
由表2可以得出,本发明试剂盒检测gdf-15的最低检出限满足小于或等于50pg/ml的技术标准要求。
[0080]
实施例8
[0081]
检测实施例5所得试剂盒的精密度
[0082]
分别使用200pg/ml和1000pg/ml的参考品重复检测10次,计算测量值的平均值m和标准差sd。按公式计算变异系数cv。式中:cv为变异系数;sd为10次测量结果的标准差;m为10次测量结果的平均值,结果见表3。其中,参考品为含相应浓度的gdf-15抗原溶液,溶剂为含质量百分含量为1%bsa、含质量百分含量为10%甘露醇的0.01mpbs。
[0083]
表3试剂盒的精密度检测结果
[0084][0085][0086]
由表3可以得出,本发明试剂盒的cv值满足不大于15%的技术标准要求。
[0087]
实施例9
[0088]
检测实施例5所得试剂盒的准确度
[0089]
用200pg/ml和2000pg/ml的参考品作为样本进行测试,重复测定3次,取平均值,计算其相对偏差,结果见表4。其中,参考品为含相应浓度的gdf-15抗原溶液,溶剂为含质量百分含量为1%bsa、含质量百分含量为10%甘露醇的0.01m pbs。
[0090]
表4试剂盒的准确度检测结果
[0091][0092]
由表4可以得出,本发明试剂盒的准确度相对偏差满足在
±
15%以内的技术标准要求。
[0093]
实施例10
[0094]
检测实施例5所得试剂盒的稳定性
[0095]
将实施例5所得试剂盒在25℃保存18个月后,分别对试剂盒的线性范围、最低检出限,精密度,准确度进行检测,具体步骤分别同实施例6-9。结果如表5-8所示。
[0096]
表5常温存放后试剂盒的线性范围检测结果
[0097][0098][0099]
由表5可以得出,常温长时间存放后试剂盒检测gdf-15的线性范围为50pg/ml~2000pg/ml,线性相关系数r≥0.990。
[0100]
表6常温存放后试剂盒的最低检出限检测结果
[0101][0102]
由表6可以得出,本发明试剂盒经常温长时间存放后,检测gdf-15的最低检出限也能满足小于或等于50pg/ml的技术标准要求。
[0103]
表7常温存放后试剂盒的精密度检测结果
[0104]
[0105][0106]
由表7可以得出,本发明试剂盒经常温长时间存放后,其cv值依旧满足不大于15%的技术标准要求。
[0107]
表8常温存放后试剂盒的准确度检测结果
[0108][0109]
由表8可以得出,本发明试剂盒经常温长时间存放后,其准确度的相对偏差仍在
±
15%的技术标准以内。
[0110]
将实施例5所得试剂盒分别在4℃、8℃、12℃、16℃、20℃、24℃、28℃、30℃温度条件下保存18个月,进行上述线性范围、最低检出限、精密度、准确度检测实验,其结果均符合线性范围:50-2000pg/ml、最低检出限≤50pg/ml、精密度不大于15%、准确度:测试值与理论值的相对偏差在
±
15%以内的技术标准。
[0111]
本发明试剂盒在4-30℃保存18个月后,试剂盒能够满足线性范围,最低检出限,精
密度,准确度等性能参数的要求,具有优异的稳定性。
[0112]
以上所述仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。