1.本发明涉及蛋白酪氨酸磷酸酶抑制的领域,具体涉及一种蛋白酪氨酸磷酸酶选择性抑制剂、用途、制备方法以及药物组合物。
背景技术:
2.蛋白酪氨酸磷酸酶(ptp)和蛋白酪氨酸激酶(ptk)共同调节体内蛋白磷酸化进程,ptp对细胞代谢、免疫、存活有重要作用,是众多疾病的药物设计的潜在靶点。其中酪氨酸磷酸酶1b(ptp1b)是糖尿病治疗的重要靶点之一。虽然ptp种类繁多,并且下游靶蛋白各异,但是其酶活性中心的相似度较高。目前基于ptp活性中心结构设计的ptp抑制剂,一般需以磷酸根或磷酸根类似物为活性基团,这些抑制剂在高浓度时将不可避免地影响细胞内其它磷酸根相关的代谢过程,造成药物不良反应。因此设计一种针对单一ptp酶的特异性抑制剂,能够在提高酶抑制活性的同时降低其有效使用浓度,是开发选择性ptp抑制剂的关键问题。
技术实现要素:
3.针对上述问题中存在的不足之处,本发明提供一种蛋白酪氨酸磷酸酶选择性抑制剂。
4.蛋白酪氨酸磷酸酶选择性抑制剂为功能化载体
‑
蛋白酪氨酸磷酸酶选择性配体
‑
钒配位复合物。
5.作为本发明的进一步改进,蛋白酪氨酸磷酸酶包括:酪氨酸磷酸酶1b、t细胞蛋白酪氨酸磷酸酶、(shp2)变构蛋白酪氨酸磷酸酶、(rptpσ)受体蛋白络氨酸磷酸酶σ、(cdc25b)细胞分裂周期因子25b、(mpk1)丝裂原活化蛋白激酶磷酸酶
‑
1、(prl3)促肝细胞再生磷酸酶
‑
3和(ptpmt1)线粒体蛋白酪氨酸磷酸酶1中的一种。
6.作为本发明的进一步改进,功能化载体包括:石墨烯量子点和石墨烯量子点功能类似物。
7.作为本发明的进一步改进,石墨烯量子点包括:o
‑
石墨烯量子点、n
‑
石墨烯量子点和f
‑
石墨烯量子点。
8.作为本发明的进一步改进,石墨烯量子点功能类似物包括:磁性纳米颗粒、金纳米颗粒、银纳米颗粒、纳米角、富勒烯、纳米管、碳点和石墨烯。
9.作为本发明的进一步改进,酪氨酸磷酸酶1b选择性配体的结构式为:
[0010][0011]
其中,x选自:饱和直链烷基、饱和支链烷基、环烷基、不饱和烷基或芳香基。
[0012]
作为本发明的进一步改进,酪氨酸磷酸酶1b选择性配体的结构式为:
[0013][0014]
作为本发明的进一步改进,t细胞蛋白酪氨酸磷酸酶选择性配体的结构式为:
[0015][0016]
本发明还提供一种上述蛋白酪氨酸磷酸酶选择性抑制剂的应用,上述蛋白酪氨酸磷酸酶选择性抑制剂用于制备治疗糖尿病、肿瘤或肥胖的药物。
[0017]
本发明还提供一种药物组合物,其包含上述蛋白酪氨酸磷酸酶选择性抑制剂和药学上可接受的辅料。
[0018]
本发明还提供一种蛋白酪氨酸磷酸酶选择性抑制剂的制备方法。该制备方法包括:将钒化合物与蛋白酪氨酸磷酸酶选择性配体混合,得到的化合物加载至功能化载体上,形成功能化载体
‑
蛋白酪氨酸磷酸酶选择性配体
‑
钒配位复合物。
[0019]
作为本发明的进一步改进,钒化合物包括无机钒化合物和有机钒化合物。
[0020]
作为本发明的进一步改进,无机钒化合物包括钒酸盐、偏钒酸盐、氧钒配合物、过氧钒配合物、羟胺钒配合物、钒的杂多酸配合物。
[0021]
作为本发明的进一步改进,有机钒化合物包括苯甲酸氧钒、阿司匹林氧钒、乙酰丙酮氧钒、双(2
‑
甲基
‑3‑
羟基
‑4‑
吡喃酮)氧钒(bmov)、3
‑
羟基
‑2‑
乙基
‑4‑
吡喃酮(beov)、3
‑
羟基
‑2‑
异丙基
‑4‑
吡喃酮(biov)、3
‑
羟基
‑2‑
正丁基
‑4‑
吡喃酮(bnbov)、二(吡啶2
‑
甲酸)氧钒(vo(pa)2)、吡啶二甲酸氧钒(vo
‑
dpa)、吡啶甲酸酞胺氧钒(vo
‑
pam)、甲基吡啶甲酸氧钒(vo
‑
mpa)、吡啶甲酸氧钒(vo
‑
pa)、丙二酸羟胺氧钒、草酸羟胺氧钒、缬氨酸羟胺氧钒、亮氨酸羟胺氧钒。
[0022]
本发明还提供一种基于gqds的具有ptp1b选择性抑制活性的钒配位复合物的制备方法。该制备方法包括:先分别制备gqds和ptp1b选择性配体;将ptp1b选择性配体混悬水溶液中,加入钒溶液,混匀;混合后,将化合物溶液滴加至gqds水溶液中,搅拌过夜;反应液过滤膜,得到基于gqds的具有ptp1b选择性抑制活性的钒配位复合物。
[0023]
作为本发明的进一步改进,基于gqds的具有ptp1b选择性抑制活性的钒配位复合物能够用于制备治疗糖尿病药物。钒配合物具有ptp1b抑制活性和抗糖尿病的效果,所以钒
配合物和ptp1b选择性配体具有相互促进作用。该复合物能够在提高钒配合物和ptp1b选择性配体抑制活性的同时降低钒配合物和ptp1b选择性配体有效使用浓度,从而避免钒配合物和ptp1b选择性配体对机体产生不良反应,最终提高了钒配合物和ptp1b选择性配体的生物利用度。
[0024]
本发明还提供一种基于gqds的具有tcptp选择性抑制活性的钒配位复合物的制备方法。该制备方法包括:先分别制备gqds和tcptp选择性配体;将tcptp选择性配体混悬水溶液中,加入钒溶液,混匀;混合后,将化合物溶液滴加至gqds水溶液中,搅拌过夜;反应液过滤膜,得到基于gqds的具有tcptp选择性抑制活性的钒配位复合物。
[0025]
本发明提供的蛋白酪氨酸磷酸酶选择性抑制剂能够对单一ptp酶产生特异性抑制作用,并且能够在提高酶抑制活性的同时降低其有效使用浓度,还不会对机体产生不良反应。
附图说明
[0026]
图1为本发明一种实施例公开的基于gqds的具有ptp1b选择性抑制活性的钒配位复合物对hepg2细胞中p
‑
src(y529)和p
‑
src(y418)表达作用结果图;
[0027]
图2为本发明一种实施例公开的基于gqds的具有tcptp选择性抑制活性的钒配位复合物对hepg2细胞中p
‑
src(y529)和p
‑
src(y418)表达作用结果图;
[0028]
图3为本发明一种实施例公开的基于gqds的具有ptp1b选择性抑制活性的钒配位复合物对糖尿病小鼠肝脏组织中p
‑
src(y529)和p
‑
src(y418)表达作用结果图;
[0029]
图4为本发明一种实施例公开的基于gqds的具有ptp1b选择性抑制活性的钒配位复合物对糖尿病小鼠脂肪组织中p
‑
src(y529)和p
‑
src(y418)表达作用结果图;
[0030]
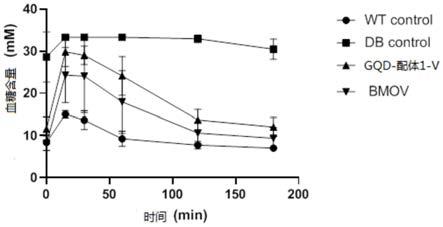
图5为本发明一种实施例公开的基于gqds的具有ptp1b选择性抑制活性的钒配位复合物对糖尿病小鼠进行口服糖耐量实验结果图。
具体实施方式
[0031]
为使本发明实施例的目的、技术方案和优点更加清楚,下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例是本发明的一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动的前提下所获得的所有其他实施例,都属于本发明保护的范围。
[0032]
下面结合附图对本发明做进一步的详细描述:
[0033]
本发明基于钒化合物对所有ptp酶具有较好的抑制作用,选择钒为活性基团。为进一步提高钒化合物选择性,设计并合成了一系列具有ptp1b选择性和tcptp选择性的配体,并利用gqds提高钒与选择性配体的结合强度,构建了以gqds为基础的ptp选择性配体
‑
钒配位复合物。
[0034]
本发明的目的在于提供一种制备不同ptp酶选择性抑制剂的通用方法,该方法包括:将ptp选择性配体与钒结合,将其结合后的产物共同加载到gqds上,构建gqds
‑
ptp选择性配体
‑
钒配位复合物。获得的配位复合物具有较好的ptp选择性抑制作用,且获得的基于gqds的具有ptp1b选择性抑制活性的钒配位复合物展现了良好的抗糖尿病效果。
[0035]
实施例一、gqds的制备方法
[0036]
将石墨烯(0.15g)加入到浓硫酸(30ml)和浓硝酸(10ml)的混合物中。将该混合溶液超声处理2h后,将混合物放入聚四氟乙烯内衬的反应釜中,120℃下反应5h。反应结束后,将反应液冷却到室温,用去离子水稀释至300ml。用无水碳酸钠固体调节其ph至8左右。将反应液放于4℃静置24h。其上清液经0.22μm的水系滤膜过滤后,用1000da透析袋在室温下透析2天(每天换水6次)去除无机盐离子,得到浅棕色澄清溶液,经冷冻干燥得到疏松棕黄色固体。
[0037]
实施例二、ptp1b选择性配体的制备方法
[0038][0039]
500mg 2,6
‑
二羟基苯甲酸溶于5ml甲醇中,冰浴下缓慢滴加含323.6μl氯化亚砜的甲醇溶液5ml。滴加完毕后,加热至60℃反应2h。tlc检测反应,待反应完毕后,旋转蒸发除去反应液,获得粗品,将粗品在甲醇中重结晶获得纯品中间体1。
[0040][0041]
400mg中间体1、342.8mg n
‑
boc
‑4‑
氨基丁醇、652.7mg三苯基膦混悬于20ml四氢呋喃中,氮气保护,冰浴下缓慢滴加偶氮二甲酸二乙酯(368μl稀释于2ml四氢呋喃中),反应1h,待反应结束后,用乙酸乙酯稀释反应液,反应液经水萃取3次,收集有机溶液,旋干,获得粗品,粗品经柱层析分离(石油醚:乙酸乙酯=10:1)获得纯品中间体2。
[0042][0043]
将获得的中间体2溶解于6ml 1m盐酸/二氧六环溶液中,氮气保护,冰浴下反应2h,反应完成后旋转蒸发除去反应液,得到的粗产物经柱层析分离(石油醚:乙酸乙酯=10:1)获得纯品中间体3。
[0044][0045]
将223mg中间体3、382mg o
‑
苯并三氮唑
‑
四甲基脲六氟磷酸盐(hbtu)、295mg(boc
‑
o
‑
tert
‑
butyl
‑
try)溶于25ml n,n
‑
二甲基甲酰胺中,缓慢加入n,n
‑
二异丙基乙胺(diea)溶液(200μl)。室温反应4h后,tlc监测反应结束,用乙酸乙酯稀释反应液,旋转蒸发除去反应液,将粗品溶于1m盐酸/二氧六环溶液中,反应结束后,旋转蒸发除去反应液,得到的粗产物经柱层析分离(石油醚:乙酸乙酯=5:1),获得纯品配体1,收率为32.5%。
[0046]
实施例三、基于gqds的具有ptp1b选择性抑制活性的钒配位复合物的制备方法
[0047]
取等体积0.012m配体1和0.024m navo3混合后,得到配体1
‑
v配合物,然后按每0.6mg配体1对应1mg gqds的比例gqds水溶液,搅拌过夜,反应液过0.02μm滤膜后,得到gqd
‑
配体1
‑
v溶液,收集制备好的gqd
‑
配体1
‑
v溶液,最后使用sephadex
tmg
‑
25m
(ge healthcare,usa)纯化,以除去未结合的配体1和v。
[0048]
实施例四、ptp1b选择性配体的制备方法
[0049]
1)树脂溶胀:称取1.8g 2
‑
ctc树脂于多肽合成反应瓶中,加入20ml n,n
‑
二甲基甲酰胺溶液浸泡并在摇床上振摇45min,使树脂充分溶胀后,用10ml n,n
‑
二甲基甲酰胺润洗3次;
[0050]
2)树脂键合亮氨酸:称取2.1g n
‑
芴甲氧羰基
‑
l
‑
亮氨酸(fmoc
‑
leu
‑
oh)溶于20mln,n
‑
二甲基甲酰胺溶液中加入1.5ml n,n
‑
二异丙基乙胺,充分混合后,加入至装有树脂的多肽合成反应瓶中,摇床振摇2h,反应完成后,n,n
‑
二甲基甲酰胺冲洗3次,加入10ml甲醇和1.5ml n,n
‑
二异丙基乙胺继续反应0.5h,封闭树脂未反应位点,抽掉反应液,n,n
‑
二甲基甲酰胺洗3次;
[0051]
3)脱fmoc保护:用20ml 20%的pip/dmf浸没反应树脂,摇床振摇30min,更换pip/dmf反应液,继续振摇30min。反应完全后,用dmf洗涤3次,抽干。
[0052]
4)肽链延长(以键合酪氨酸为例):将1.65g(fmoc
‑
o
‑
tert
‑
butyl
‑
try),1.5g hbtu,0.54g 1
‑
羟基苯并三唑(hobt),0.9ml diea溶于25ml n,n
‑
二甲基甲酰胺中,充分溶解混合后,加入到上述反应瓶中,摇床振摇4h,茚三酮法监测反应。反应完成后,抽去反应液,加入n,n
‑
二甲基甲酰胺洗涤三次,然后重复脱fmoc保护和肽链延长过程至键合所有氨基酸后用5%tfa/dmf切割多肽和树脂,并用水进行多肽沉淀获得粗品,然后用hplc进行纯化,得到配体2
[0053]
实施例五、基于gqds的具有ptp1b选择性抑制活性的钒配位复合物的制备方法
[0054]
取等体积0.012m配体2和0.012m navo3混合后,按每0.10mg配体2对应1mg gqds的比例加gqds水溶液,搅拌过夜,反应液过0.02μm滤膜后,得到gqd
‑
配体2
‑
v溶液,收集制备好的gqd
‑
配体2
‑
v溶液,最后使用sephadex
tmg
‑
25m
(ge healthcare,usa)纯化,以除去未结合的配体2和v。
[0055]
实施例六、tcptp选择性配体的制备方法
[0056]
[0057]2‑
ctc树脂(2
‑
ctc resin)(500mg,1mmol/g负载量)于20ml dmf活化后,dmf洗涤三次。将fmoc
‑
lys(alloc)
‑
oh(1.1g,2.4mmol)和diea(1.2ml,6.9mmol)溶于20ml dmf后,与树脂混合并振荡2小时,并用dmf再次洗涤树脂(3次)。加入含四(三苯基膦)
‑
钯(0)(50mg,0.04mmol)、乙醇(2.5ml)和diea(1.0ml,5.8mmol)的dmf溶液,脱去别构基团。采用相同方法结合4
‑
乙基苯甲酸(375mg,2.5mmol)后,用25ml 20%哌啶/dmf溶液振荡30mins脱去fmoc保护基团,并依次连接fmoc
‑
o
‑
tert
‑
tyr(1.2g,3.7mmol)、fmoc
‑
phe
‑
oh(968mg,2.5mmol)和(
‑
)
‑
薄荷氧乙酸(536mg,2.5mmol)。当肽序列完成后,用5%tfa/dmf处理1小时,将配体3从树脂上裂解。保留反应溶液,并在真空下蒸发三氟乙酸(tfa)。粗品经乙醚研磨后,用hplc纯化,得到最终产品配体3。
[0058]
实施例七、基于gqds的具有tcptp选择性抑制活性的钒配位复合物的制备方法
[0059]
取等体积0.012m配体3和0.012m navo3混合后,得到配体3
‑
v配合物,然后按每0.15mg配体3对应1mg gqds的比例加gqds水溶液,搅拌过夜,反应液过0.02μm滤膜后,得到gqd
‑
配体3
‑
v溶液,收集制备好的gqd
‑
配体3
‑
v溶液,最后使用sephadex
tmg
‑
25m
(ge healthcare,usa)纯化,以除去未结合的配体3溶液和v。
[0060]
实施例八、钒配合物进行体外酶抑制活性测试
[0061]
将实验实施例三和实施例七制备的钒配合物进行体外酶抑制活性测试。酶抑制活性反应体系ph=7.5,其中含25mm三羟甲基氨基甲烷(tris)、2mmβ
‑
巯基乙醇、2mm二硫苏糖醇(dtt)和1mm乙二胺四乙酸(edta)。取96孔板,每孔加入50μl含酶缓冲液后,加入不同浓度梯度的待测配合物(0、4nm、8nm和10nm),37℃孵育5min。然后加入100μl不同浓度对硝基苯酚磷酸酯二钠盐(p
‑
npp)(25mm、12.5mm和6.25mm)溶液,孵育25min。最终以50μl的3m naoh终止反应。测定反应液在405nm处吸光度。最终用graphpad prism 8作图求得ki值。
[0062]
结果如表1:
[0063]
表1
[0064][0065]
由表1结果可知,配体1
‑
v在溶液中展现了较好的ptp1b抑制活性和选择性。同时,配体3
‑
v展现了较好的tcptp抑制活性和选择性,而装载gqds后,不影响配合物抑制活性。
[0066]
实施例九、钒配合物进行细胞活性测试
[0067]
以每孔5
×
105个细胞的量将hepg2细胞接种于6孔板中,待细胞融合达到80%后,吸出培养基,磷酸盐缓冲盐溶液(pbs)清洗3次,加入不含fbs的dmem(高糖)培养基饥饿6h后,给药处理6h,其中navo3给药浓度为10μm,gqd
‑
配体1
‑
v给药浓度为0.05μm和0.25μm,gqd
‑
配体3
‑
v给药浓度为1μm和2.5μm,对照组用不含fbs的dmem(高糖)培养处理。药物处理后,进行蛋白提取,并用western blot技术,检测各组细胞中p
‑
src(y529)和p
‑
src(y418)含
量,判断gqd
‑
配体1
‑
v和gqd
‑
配体3
‑
v对ptp1b及tcptp的抑制活性及选择性。
[0068]
其中ptp1b选择性抑制能增加p
‑
src(y529)表达量,tcptp选择性抑制能增加p
‑
src(y418)含量,如图1所示,gqd
‑
配体1
‑
v能显著增高细胞中p
‑
src(y529)含量,同时对p
‑
src(y418)含量影响较小,说明gqd
‑
配体1
‑
v具有较好的ptp1b抑制活性和选择性。如图2所示,gqd
‑
配体3
‑
v能显著增高细胞中p
‑
src(y418)含量,同时对p
‑
src(y529)含量影响较小,说明gqd
‑
配体3
‑
v具有较好的tcptp抑制活性和选择性。
[0069]
实施例十、gqd
‑
配体1
‑
v进行系统的动物实验
[0070]
将bks
‑
db糖尿病小鼠及健康bks小鼠进行分组:
[0071]
(1)健康bks小鼠对照组(wt control,n=6),普通饲料喂养,持续喂养15周;
[0072]
(2)糖尿病对照组(db control,n=8),普通饲料喂养,持续喂养15周;
[0073]
(3)gqd
‑
配体1
‑
v给药组(gqd
‑
配体1
‑
v,n=8),普通饲料掺入gqd
‑
配体1
‑
v喂养,1
‑
2周:0.001mmol/kg/天;3
‑
5周:0.05mmol/kg/天;6
‑
9周:0.08mmol/kg/天;处死前:0.15mmol/kg/天;
[0074]
(4)双(2
‑
甲基
‑3‑
羟基
‑4‑
吡喃酮)氧钒治疗组(bmov组,n=8),将bmov掺杂在普通饲料中喂养,剂量为0.18mmol/kg/天。
[0075]
其中,每7天监测一次血糖,尾静脉取血,各组测得的血糖结果见表2:
[0076]
表2
[0077][0078]
由表2可见,bmov组和gqd
‑
配体1
‑
v组均能较好控制小鼠血糖,显示了优异的降糖效果;同时,gqd
‑
配体1
‑
v的给药浓度比bmov低,说明了gqd
‑
配体1
‑
v能够在提高酶抑制活性的同时降低其有效使用浓度。
[0079]
实施例十一、gqd
‑
配体1
‑
v对小鼠进行口服糖耐量实验
[0080]
将bks
‑
db糖尿病小鼠及健康bks小鼠进行分组:
[0081]
(1)健康bks小鼠对照组(wt control,n=6),普通饲料喂养,持续喂养9周;
[0082]
(2)糖尿病对照组(db control,n=8),普通饲料喂养,持续喂养9周;
[0083]
(3)gqd
‑
配体1
‑
v给药组(gqd
‑
配体1
‑
v,n=8),普通饲料掺入gqd
‑
配体1
‑
v喂养,1
‑
2周:0.001mmol/kg/天;3
‑
5周:0.05mmol/kg/天;6
‑
9周:0.08mmol/kg/天;
[0084]
(4)双(2
‑
甲基
‑3‑
羟基
‑4‑
吡喃酮)氧钒治疗组(bmov组,n=8),将bmov掺杂在普通饲料中喂养,剂量为0.18mmol/kg/天。
[0085]
给药9周后,进行口服糖耐量实验。实验开始前,将小鼠禁食不禁水12小时,而后测定小鼠空腹血糖,记为起始血糖值,而后按1g/kg的剂量对小鼠灌胃给药葡萄糖,分别测定灌胃后15min、30min、60min、120min和180min时小鼠血糖值,结果如图5所示,gqd
‑
配体1
‑
v口服给药浓度在0.08mmol/kg/天时,对bks
‑
db小鼠具有良好降糖效果。
[0086]
实施例十二、gqd
‑
配体1
‑
v对小鼠体内ptp1b抑制活性及选择性实验将bks
‑
db糖尿
病小鼠及健康bks小鼠进行分组:
[0087]
(1)健康bks小鼠对照组(wt control,n=6),普通饲料喂养,持续喂养15周;
[0088]
(2)糖尿病对照组(db control,n=8),普通饲料喂养,持续喂养15周;
[0089]
(3)gqd
‑
配体1
‑
v给药组(gqd
‑
配体1
‑
v,n=8),普通饲料掺入gqd
‑
配体1
‑
v喂养,1
‑
2周:0.001mmol/kg/天;3
‑
5周:0.05mmol/kg/天;6
‑
9周:0.08mmol/kg/天;处死前:0.15mmol/kg/天;
[0090]
(4)双(2
‑
甲基
‑3‑
羟基
‑4‑
吡喃酮)氧钒治疗组(bmov组,n=8),将bmov掺杂在普通饲料中喂养,剂量为0.18mmol/kg/天。
[0091]
给药15周处死后,分别取各小鼠肝脏和脂肪组织,研磨提取蛋白,通过western blot检测各小鼠肝脏和脂肪组织中p
‑
src(y529)和p
‑
src(y418)含量,判断gqd
‑
配体1
‑
v在小鼠体内对ptp1b的抑制活性及选择性,如图3、图4所示,gqd
‑
配体1
‑
v在小鼠体内仍具有较好的ptp1b抑制活性及选择性。
[0092]
结论:
[0093]
本发明提供的蛋白酪氨酸磷酸酶选择性抑制剂能够对单一ptp酶产生特异性抑制作用,并且能够在提高酶抑制活性的同时降低其有效使用浓度,还不会对机体产生不良反应。
[0094]
以上仅为本发明的优选实施例而已,并不用于限制本发明,对于本领域的技术人员来说,本发明可以有各种更改和变化。凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。