一种小分子抑制剂在制备靶向p2x7受体中的用途
技术领域
1.本发明属于p2x7r拮抗剂筛选技术领域,具体涉及一种小分子抑制剂在制备靶向p2x7受体中的用途。
背景技术:
2.嘌呤受体p2x7(p2x7r)是atp门控的离子通道,在人体的固有免疫中起重要作用,几乎在所有组织和器官的免疫细胞中普遍表达,如树突状细胞、t淋巴细胞、b淋巴细胞以及中性粒细胞,而在单核细胞或巨噬细胞上表达较高。p2x7r不仅可以被atp激活形成非选择性阳离子通道,引起na 和ca2 内流和k 外流导致细胞离子稳态的改变,并且在高浓度atp的刺激下具有形成多种非选择性膜孔的能力,足以允许分子量为900kda的物质通过巨噬细胞膜,导致细胞死亡。此外,p2x7r是p2x家族中与炎症反应最相关的受体,它通过激活nlrp3炎性小体的活化,并促进il
‑
1β的释放,被认为参与疼痛、神经退行性变和炎症性疾病等多种疾病发生,包括克罗恩病、痛风、类风湿关节炎和骨关节炎等。因此,拮抗p2x7r能够有效防治多种疾病发生发展,具有重要临床应用价值;
3.p2x7受体可以被特定的生物制剂阻断,包括小分子化合物、单克隆抗体、纳米体等。传统p2x7r特异性拮抗剂,如brilliant blue g会刺激某些细胞内信号酶,且存在致命毒性不宜用于人体研究;小分子化合物a438079会影响pannexin
‑
1通道,抑制胞内atp的输出;此外,许多抑制剂除抑制p2x7r外,还会影响其他p2受体,特异性较差,因此,筛选到特异性高、副作用低的小分子抑制剂意义重大。
技术实现要素:
4.本发明提供了一种小分子抑制剂在制备靶向p2x7受体中的用途,具体通过预测p2x7r蛋白结构建模及变构位点和筛选小分子变构抑制剂,获得的小分子抑制剂特异性高,安全性好,没有任何毒性,副作用低,是一种高效的针对atp受体p2x7r的变构抑制剂,通过变构效应阻断atp
‑
嘌呤受体p2x配体门控的离子通道7(p2x7r)信号通路,继而抑制nlrp3炎症小体活化。
5.本发明第一个目的是提供一种小分子抑制剂在制备靶向p2x7受体中的用途,所述小分子抑制剂的分子结构式如下(如图8所示):
[0006][0007]
进一步地,所述小分子抑制剂的筛选过程,包括如下步骤:
[0008]
第一步:预测p2x7r蛋白结构建模及变构位点:首先对p2x7r的蛋白结构进行建模,
然后预测变构位点,最后对变构位点进行评分,确定p2x7r蛋白变构抑制剂的候选位点;
[0009]
第二步:筛选小分子变构抑制剂:首先下载p2x7r蛋白的晶体复合物5u1x,采用glide蛋白预处理流程中的加氢、去水、蛋白结构优化;筛选小分子库,然后移除包含pains结构的分子,对小分子进行预处理和构象生成,使用schordinger软件进行对接获得对接构象,打分筛选小分子,挑选到打分在前2000名的小分子,并从中筛选出排名在前30名的小分子,分析其结合模式,然后通过最高精度对接筛选小分子并分析其结合模式,最终获得用于进行对接的小分子抑制剂。
[0010]
进一步地,第一步中,使用蛋白建模的程序i
‑
tessar对p2x7r的蛋白结构进行建模。
[0011]
进一步地,第一步中,使用蛋白变构位点预测程序allositepro软件对蛋白的变构位点进行预测。
[0012]
进一步地,第一步中,蛋白变构位点预测算法是基于目前已知所有被晶体实验证明的变构位点的特征提取与机器学习算法的预测程序。
[0013]
进一步地,第一步中,利用allosite程序对p2x7r蛋白三个变构位点进行评分。
[0014]
进一步地,第一步中,通过allosite程序对p2x7r蛋白三个变构位点进行评分的依据是pocket volume、allosite score和perturbation score;
[0015]
其中,当allosite程序得出pocket volume大于等于659.833,,allosite score大于等于0.630,,且perturbation score大于等于0.110,时该位点可以作为p2x7r蛋白变构抑制剂的候选位点。
[0016]
进一步地,第二步中,筛选小分子库是采用陶素化学提供的虚拟筛选进行的。
[0017]
进一步地,第二步中,使用薛定谔中的ligprep模块(epik模式)对小分子进行预处理和构象生成。
[0018]
进一步地,所述的小分子抑制剂用于制备治疗痛风关节炎的药物。
[0019]
与现有技术相比,本发明具有以下有益效果:
[0020]
1、本发明筛选获得的p2x7受体的小分子抑制剂特异性高,安全性好,没有任何毒性,副作用低,是一种高效的针对atp受体p2x7r的抑制剂,阻断atp
‑
嘌呤受体p2x配体门控的离子通道7(p2x7r)信号通路,继而抑制nlrp3炎症小体活化。
[0021]
2、本发明筛选获得的p2x7受体的小分子抑制剂能够应用于痛风关节炎的防治。
附图说明
[0022]
为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
[0023]
图1为本发明中p2x7r蛋白的三维建模结构图;
[0024]
图2为本发明中p2x7r蛋白预测得到的变构位点图;
[0025]
图3为本发明中小分子抑制剂与p2x7r蛋白的对接构象图;
[0026]
图4为本发明中小分子抑制剂与p2x7r蛋白的对接结构结合模式图;
[0027]
图5为本发明中小分子抑制剂对atp诱导转染野生型人p2x7r的hek
‑
293t细胞的通
道功能影响效果图;
[0028]
图6为本发明中不同剂量的小分子抑制剂对bzatp诱导thp
‑
1来源巨噬细胞产生炎症反应的影响效果图;
[0029]
图7为本发明中小分子抑制剂对atp诱导小鼠骨髓巨噬细胞产生炎症反应的影响效果图。
[0030]
图8为本发明中小分子抑制剂的结构式。
[0031]
图9为本发明中小分子抑制剂对痛风患者pbmc来源巨噬细胞产生炎症反应的影响。
[0032]
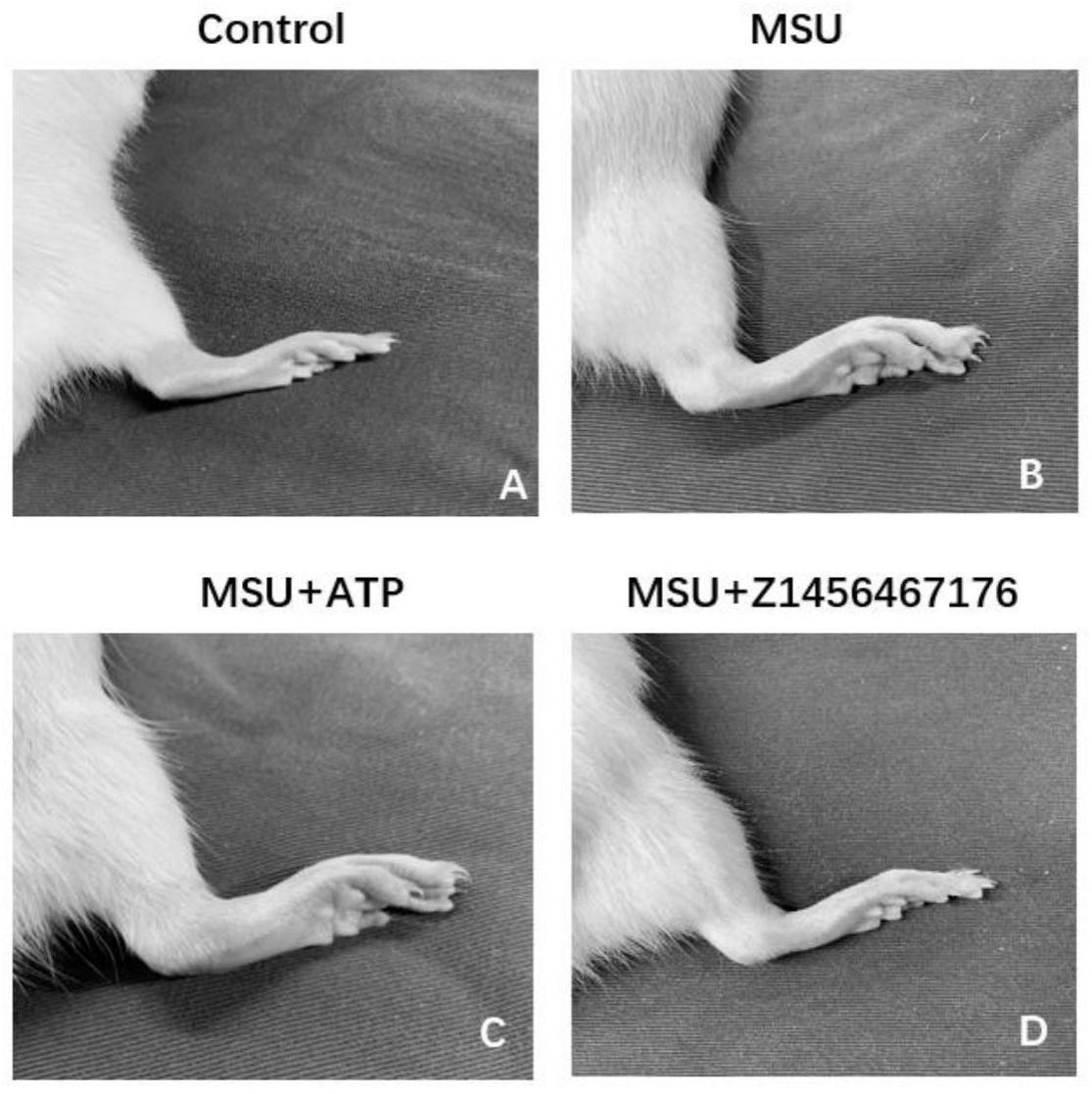
图10为发明中不同处理组对大鼠右踝关节及右足背的影响表观;
[0033]
其中,图a为注射pbs对大鼠右踝关节及右足背的影响表观;
[0034]
图b为注射msu对大鼠右踝关节及右足背的影响表观;
[0035]
图c为注射msu atp对大鼠右踝关节及右足背的影响表观;
[0036]
图d为注射z1456467176 msu对大鼠右踝关节及右足背的影响表观。
[0037]
图11为发明中小分子抑制剂对痛风大鼠模型中抗炎作用的影响;
[0038]
其中,图a表示大鼠踝关节周长;
[0039]
图b表示大鼠踝关节肿胀指数。
[0040]
图12为发明中不同处理组对大鼠血清il
‑
1β的影响。
[0041]
图13为不同处理组下的关节组织切片的光学显微图像;
[0042]
其中,图a为注射pbs的关节组织切片的光学显微图像;
[0043]
图b为注射msu的关节组织切片的光学显微图像;
[0044]
图c为注射atp msu的关节组织切片的光学显微图像;
[0045]
图d为注射z1456467176 msu的关节组织切片的光学显微图像。
具体实施方式
[0046]
下面结合具体实施例对本发明进行详细说明,但不应理解为本发明的限制。下列实施例中未注明具体条件的试验方法,通常按照常规条件操作,由于不涉及发明点,故不对其步骤进行详细描述。
[0047]
实施例1
[0048]
靶向p2x7受体的小分子抑制剂的筛选方法,包括如下步骤:
[0049]
步骤一、预测了p2x7r蛋白结构建模及变构位点
[0050]
p2x7r蛋白序列全长为595个氨基酸,该蛋白没有已知的晶体结构。发明人首先使用蛋白建模的程序i
‑
tessar对p2x7r的蛋白结构进行建模(如图1所示);
[0051]
然后,使用蛋白变构位点预测程序allositepro软件对蛋白的变构位点进行预测;该蛋白变构位点预测算法是基于目前已知所有被晶体实验证明的变构位点的特征提取与机器学习算法的预测程序,其可以对蛋白结构进行动态化处理,并识别出最有可能的变构位点(如图2所示)。使用该程序预测得到的三个变构位点,分别记为i,ii,iii。
[0052]
最后,利用allosite程序对p2x7r蛋白三个变构位点进行评分。allosite程序评价变构位点的主要依据为其pocket volume、allosite score和perturbation score。当allosite程序得出pocket volume大于等于659.833,allosite score大于等于0.630,且
perturbation score大于等于0.110,该位点可以作为p2x7r蛋白变构抑制剂的候选位点。
[0053]
结果表明,预测得到的变构位点i和ii均具有足够的大小,较高的变构概率及扰动强度(如表1),因此这两个位点可以作为p2x7r蛋白变构抑制剂的候选位点。
[0054]
表1预测到的变构位点及其属性
[0055]
变构位点pocke volumeallosite scoreperturbation scorei2735.1190.8021.000ii1978.6540.8300.887iii659.8330.6300.110
[0056]
步骤一的完成,为下一步小分子变构抑制剂进行高通量的筛选找到了作用靶点。
[0057]
步骤二、初步筛选靶向p2x7r小分子变构抑制剂
[0058]
虚拟筛选使用商业软件schordinger软件的glide模块进行。首先,我们从pbd数据库中下载p2x7r晶体5u1x,蛋白的处理采用glide蛋白预处理流程中的加氢
‑
>去水
‑
>蛋白结构优化。小分子的虚拟筛选采用陶素化学提供的虚拟筛选小分子库(个数200万 ),然后交由上海宇道生物技术有限公司操作,移除其中包含pains结构的分子,最终进行对接计算的分子个数为180万 。然后我们使用薛定谔中的ligprep模块(epik模式)对小分子进行预处理和构象生成。格点文件由f108为中心选取,选取其周围18埃的残基作为对接口袋。使用glide进行对接获取对接构象,其对接打分为:
‑
9.50271,其对接构象(图3),对小分子抑制剂与p2x7r蛋白的结合模式进行分析(图4),结合模式分析提示,小分子抑制剂与val,asp,lys之间形成了氢键作用。
[0059]
按照上述方法继续筛选,筛选打分在前2000名的小分子。然后对这2000个小分子再使用xp精度(最高精度对接)筛选出其中排名在前30名的小分子,分析其结合模式,最终得到的可进行对接的小分子文件,所述的小分子抑制剂编号为z1456467176,所述的小分子抑制剂的结构式如图8所示。
[0060]
所述小分子抑制剂的分子组成为:
[0061]
cl.cc(cc=1c=cc=c(c1)c(f)(f)f)c(=o)nc=2c=cc=c(c2)s(=o)(=o)nccn。
[0062]
结合图4分析的具体结果记录于表2
‑
表5中。
[0063]
表2疏水相互作用
[0064]
indexresidueaadistanceligand atomprotein atom188aphe3.354788798295aphe3.8547998953103aphe3.69479810194108aphe3.98478911035295atyr3.93479538326310aile3.8247904090
[0065]
表3氢键相互作用
[0066][0067]
表4π
‑
stacking
[0068][0069][0070]
表5π
‑
c ationinteractions
[0071][0072]
实施例2
[0073]
第一、探讨靶向p2x7受体的小分子抑制剂对atp诱导转染野生型p2x7r的hek
‑
293t细胞的通道功能影响。
[0074]
具体包括如下步骤:
[0075]
(1)构建过表达人p27xr的慢病毒载体:
[0076]
h
‑
p2rx7(野生型)和空病毒型过表达慢病毒载体均由上海汉恒生物科技有限公司直接合成。主要流程:选择慢病毒载体,并进行设计目的片段pcr引物,包括上游引物lv
‑
h
‑
p2rx7
‑
e/b
‑
f,其核苷酸序列如seq id no.1所示,下游引物lv
‑
h
‑
p2rx7
‑
e/b
‑
r的核苷酸序列如seq id no.2所示;选用限制性内切酶ecori和bamhi进行酶切载体,琼脂糖凝胶回收得到纯化的线性化载体;根据设计的引物进行目的片段pcr,琼脂糖凝胶回收得到正确大小的目的片段;将线性化载体和目的片段按照同源重组或者t4连接的方法进行连接;转化感受
态dh5a或者stbl3,菌液涂板,培养12
‑
16h;挑选单克隆行进菌落验证;选择菌落验证正确的阳性克隆进行测序;测序正确的克隆样品进行质粒抽提;
[0077]
lv
‑
h
‑
p2rx7
‑
e/b
‑
f(seq id no.1):
[0078]
tagaggatctatttccggtgaattcgccaccatgccggcctgctgcagc
[0079]
lv
‑
h
‑
p2rx7
‑
e/b
‑
r(seq id no.2)
[0080]
tcacttaagcttggtaccgaggatccgtaaggactcttgaagccactgt
[0081]
(2)建立表达野生型p2x7r的hek
‑
293t细胞:
[0082]
取培养生长良好的hek
‑
293t细胞,放37℃二氧化碳培养箱中培养24小时(2*105细胞/孔)。
[0083]
分别转染moi值为10的野生型p2x7r慢病毒,放37℃二氧化碳培养箱中培养24小时。转染24小时后添加小分子抑制剂(10,50μm)孵育30分钟,对照孔添加等体积的dmso孵育30分钟,收集hek
‑
293t细胞。
[0084]
吸取每孔的细胞,洗涤一次,并在37℃下重悬于含kcl的0.5ml hepes缓冲培养基中,用流式管收集;
[0085]
(3)添加溴化乙锭,刺激剂前和后检测hek
‑
293t对溴化乙锭摄取:
[0086]
在每管中添加溴化乙锭(25μm),用cytoflex流式细胞仪收集细胞,每秒1000个细胞数,每个样本5秒收集一次,收集40秒,之后加入atp(1.0mm)。每秒收集1000个细胞数,每个样本5秒收集一次,共收集5分钟(300秒);
[0087]
(4)小分子抑制剂对atp活化的通道功能的抑制作用:
[0088]
使用cytexpert软件对样本数据进行分析,读取每个样本平均荧光强度值,并对应时间作图。对比atp加入后hek
‑
293t对溴化乙锭摄取变化。
[0089]
结果如图5所示,将细胞对溴化乙锭的摄取量作为检测atp诱导下p2x7r孔通道开放功能强弱的方法。加入小分子抑制剂(z1456467176)后,转染了hp2x7r的293t细胞对atp诱导下溴化乙锭的摄取功能减弱,呈剂量依赖性发挥作用。
[0090]
图5中,control:转染了hp2x7r的293t细胞对atp诱导下溴化乙锭的摄取;
[0091]
z1456467176(10μm):转染了hp2x7r的293t细胞,加入抑制剂(10μm)孵育后,对atp诱导下溴化乙锭的摄取
[0092]
z1456467176(50μm):转染了hp2x7r的293t细胞,加入抑制剂(50μm)孵育后,对atp诱导下溴化乙锭的摄取。
[0093]
实验方法:流式细胞术
[0094]
横坐标:摄取时间
[0095]
纵坐标:溴化乙锭的平均荧光强度。
[0096]
第二、探讨小分子抑制剂对bzatp诱导thp
‑
1来源巨噬细胞产生炎症反应的影响。
[0097]
具体步骤如下:
[0098]
(1)建立thp
‑
1来源的人巨噬细胞模型:
[0099]
将thp
‑
1细胞以1
×
105/孔的密度接种在24孔板中。用100ng/ml丙二醇甲醚醋酸酯(phorbol
‑
12
‑
myristate
‑
13
‑
acetate,pma)刺激thp
‑
1细胞过夜,当thp
‑
1贴壁分化为巨噬细胞后,撤液,pbs洗涤一次,用50ng/ml脂多糖(lipopolysaccharide,lps)刺激3小时,撤液,pbs洗涤一次,进行后续实验;
[0100]
(2)添加小分子抑制剂和bzatp(100μm)后elisa检测thp
‑
1细胞培养上清il
‑
1β的表达:
[0101]
添加小分子抑制剂(1,10,50,100μm)孵育30分钟,对照孔添加等体积的dmso孵育30分钟,再加入100μm bzatp培养30分钟。收集培养液上清,400g离心5分钟,将elisa所需试剂置于室温平衡,按比例稀释,向样本孔每孔加入100μl稀释后的细胞上清。制作il
‑
1β标准曲线。将il
‑
1β标准品溶液以1:1的比例依次稀释6次,每次均需充分混匀。其浓度依次为250、125、62.5、31.25、15.63、7.81及3.91pg/ml,将稀释液设为标准曲线的基点。用封板膜封板,室温孵育2小时。加入200μl 1x洗液洗板4次,每次静置4分钟,然后用吸水纸拍干。向各孔加入200μl辣根过氧化物酶标记的链霉亲和素,用新封板膜封板,用封板膜封板,室温孵育2小时。重复步骤洗板步骤。向各孔加入显色底物tmb 200μl,室温避光孵育30min。向各孔加入终止液50μl终止反应。用多功能酶标仪分别测定450nm和570nm(参考波长)的吸光度值。各组od值为450nm吸光度值减去570nm吸光度值再减去空白对照组中的od值,通过标准曲线计算各组数值;
[0102]
结果图6显示,小分子抑制剂(z1456467176)能剂量依赖性的抑制thp
‑
1细胞中,bzatp诱导的巨噬细胞il
‑
1β的分泌。
[0103]
第二、探讨小分子抑制剂对atp诱导小鼠骨髓巨噬细胞产生炎症反应的影响。
[0104]
具体步骤如下:
[0105]
①
建立小鼠骨髓巨噬细胞模型:
[0106]
②
c57bl/6小鼠颈椎脱臼处死,浸泡于75%酒精消毒10min。
[0107]
③
无菌条件下分离小鼠双侧股骨和胫骨,除去附着的肌肉等组织,浸泡于75%酒精。
[0108]
④
剪去股骨和胫骨两端,用无菌pbs冲洗骨髓腔,将骨髓细胞冲洗至15ml离心管,400g离心5分钟,弃上清液,加入1ml红细胞裂解液,重悬后静置5分钟,加入pbs中止,400g离心5分钟,弃上清。
[0109]
⑤
加入含20%l929上清的dmem细胞培养基重悬细胞,按1*106细胞/孔铺板,每孔按1:100添加双抗。2
‑
3天后换液。
[0110]
⑥
第7天,彻液,pbs洗涤一次,用50ng/ml脂多糖(lipopolysaccharide,lps)刺激3小时,撤液,pbs洗涤一次,进行后续实验;
[0111]
⑦
添加z1456467176(1,10,50,100μm)孵育30分钟,对照孔添加等体积的dmso孵育30分钟,再加入1mm atp培养30分钟。
[0112]
⑧
收集培养液上清,400g离心5分钟,将elisa所需试剂置于室温平衡,按比例稀释,向样本孔每孔加入100μl稀释后3的细胞上清。制作il
‑
1β标准曲线。将il
‑
1β标准品溶液以1:1的比例依次稀释6次,每次均需充分混匀。其浓度依次为250、125、62.5、31.25、15.63、7.81及3.91pg/ml,将稀释液设为标准曲线的基点。用封板膜封板,室温孵育2小时。加入200μl 1x洗液洗板4次,每次静置4分钟,然后用吸水纸拍干。向各孔加入200μl辣根过氧化物酶标记的链霉亲和素,用新封板膜封板,用封板膜封板,室温孵育2小时。重复步骤洗板步骤。向各孔加入显色底物tmb 200μl,室温避光孵育30min。向各孔加入终止液50μl终止反应。用多功能酶标仪分别测定450nm和570nm(参考波长)的吸光度值。各组od值为450nm吸光度值减去570nm吸光度值再减去空白对照组中的od值,通过标准曲线计算各组数值;
[0113]
结果如图7所示,小分子抑制剂(z1456467176)能剂量依赖性的抑制bmdm细胞中,atp诱导的巨噬细胞il
‑
1β的分泌。
[0114]
第三、探讨小分子抑制剂对痛风患者pbmc来源巨噬细胞产生炎症反应的影响
[0115]
(1)建立痛风患者pbmc来源的巨噬细胞模型:a.提取将痛风患者2ml外周抗凝血pbmc,细胞以1
×
106/孔的密度接种在12孔板中过夜,撤液,pbs洗涤一次,用50ng/ml lps刺激3小时,撤液,pbs洗涤一次,进行后续实验;
[0116]
(2)添加小分子抑制剂变构抑制剂和bzatp(100μm)后elisa检测pbmc细胞培养上清il
‑
1β的表达:添加小分子抑制剂(1,10,50,100μm)孵育30分钟,对照孔添加等体积的dmso孵育30分钟,再加入100μm bzatp培养30分钟。后续elisa步骤同上;
[0117]
结果如图9所示,小分子抑制剂(z1456467176)抑制bzatp诱导的痛风患者外周血pbmc培养上清的il1β分泌。
[0118]
(3)建立大鼠痛风模型:a.将大鼠标记并且称重后,按照随机原则分为4组对照组msu(尿酸盐)组、atp msu(腺嘌呤核苷三磷酸 尿酸盐)组、抑制剂 msu(小分子抑制剂 尿酸盐)组、对照组,每组5
‑
7只。atp msu组腹腔注射生理盐水500μl含atp(10mm),抑制剂 msu组(z1456467176 msu)腹腔注射生理盐水500μl含小分子抑制剂(50mg/kg),msu组和对照组分别腹腔注射生理盐水500μl。半小时后腹腔注射水合氯醛(0.3ml/100g),10分钟后观察大鼠状态,待大鼠肌力下降,测量大鼠右踝关节及右足背初始周长。借鉴经典coderre造模法:将约4mg尿酸盐(msu)晶体溶解于100μl无菌pbs中,经皮下途径注入动物右踝关节腔内(msu组、atp msu组、抑制剂 msu组),对照组右踝关节腔内注射等体积pbs。12小时后用卷尺测量右踝关节及右足背周长,用踝关节肿胀指数来评估模型鼠右踝关节的临床表现。踝关节肿胀指数=(处理后踝关节的周长
‑
初始周长)/初始周长。b.采用摘眼球取血的方法获取大鼠的血标本,取大鼠眼球血1ml,室温静置30分钟,500g离心5分钟,留取上清,进行血清il
‑
1β的elisa检测。c.留取大鼠右踝关节置于10%福尔马林中固定1天,置于脱钙液中,脱钙1
‑
2周后延关节矢状面切开,石蜡包埋,制备大鼠踝关节组织切片,h&e染色,用光学显微镜(日本东京奥林巴斯)采集图像。
[0119]
结果如下:
[0120]
从图10可以看到,腹腔注射atp加重msu引起的局部关节肿胀,小分子抑制剂减轻atp诱导的关节症状。
[0121]
从图11可以看到,注射atp msu后,踝关节周长、踝关节肿胀指数较msu组加重,注射小分子抑制剂 msu后,踝关节周长、踝关节肿胀指数较msu组减轻。
[0122]
从图12可以看到,注射atp msu后,大鼠血清il
‑
1β水平较msu组升高,注射小分子抑制剂 msu后,il
‑
1β水平降低。
[0123]
从图13可以看到,注射atp msu后,大鼠踝关节组织切片炎症细胞浸润程度较msu组加重,注射小分子抑制剂 msu后,炎症细胞浸润程度减轻。
[0124]
需要说明的是,本发明中涉及数值范围时,应理解为每个数值范围的两个端点以及两个端点之间任何一个数值均可选用,为了防止赘述,本发明的描述了优选的实施例,但本领域内的技术人员一旦得知了基本创造性概念,则可对这些实施例作出另外的变更和修改。所以,所附权利要求意欲解释为包括优选实施例以及落入本发明范围的所有变更和修改。
[0125]
显然,本领域的技术人员可以对本发明进行各种改动和变型而不脱离本发明的精神和范围。这样,倘若本发明的这些修改和变型属于本发明权利要求及其等同技术的范围之内,则本发明也意图包含这些改动和变型在内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。