1.本发明涉及免疫芯片技术领域,尤其涉及一种检测芯片、设备及方法。
背景技术:
2.抗原与抗体的特异性结合是免疫反应的基础,一般采用酶或者荧光素等标记抗体以提供检测信号,常见的检测方法如酶联免疫、荧光免疫、化学发光等能满足大部分的检测需求,但有些标志物在血液中的浓度极低,一般方法很难检测到或者能检测到但结果不够准确。
3.相关技术中,将标记有荧光的抗体预埋在玻璃基板上,捕获抗体接枝到sio2阵列上,通过外接气动装置,将待检测样本依次通过芯片,反应完成后检测捕获区域的荧光信号,以此来反映样本中标志物的浓度,此种检测方法的劣势是检测芯片灵敏度偏低,对样本中浓度较低的物质检出率不高。
技术实现要素:
4.为了解决检测芯片灵敏度偏低,待检测样本中浓度较低的物质检出率不高的问题,本发明实施例提供一种检测芯片、设备及方法。
5.第一方面,本发明实施例提供一种检测芯片,包括:基板及位于所述基板上方的盖板;
6.所述盖板,包括:
7.第一进样口,用于注入待检测样本;
8.所述基板,包括:
9.第一反应区,预埋有已标记dna片段的第一抗体,所述第一反应区与所述第一进样口连通,用于进行所述待检测样本中的抗原与所述第一抗体的特异性结合,以形成抗原抗体对;
10.第二反应区,接枝有第二抗体,所述第二反应区与所述第一反应区远离所述第一进样口一侧连通,用于进行所述第二抗体捕获所述抗原抗体对以形成双抗夹心和进行pcr扩增,以通过pcr扩增后产物的荧光信号表征待检测样本中抗原的含量。
11.在一些实施方式中,所述盖板还包括:
12.至少一个第二进样口,与所述第二反应区连通,用于注入pcr扩增所需试剂。
13.在一些实施方式中,所述第一抗体包括:已标记dna片段且冻干于目标载体上的抗体。
14.在一些实施方式中,所述目标载体包括多孔载体。
15.在一些实施方式中,所述基板还包括:
16.第一流道,连接于所述第一进样口和所述第一反应区之间,用于将从所述第一进样口注入的所述待检测样本进行混匀后送入所述第一反应区;
17.第二流道,连接于所述第一反应区远离所述第一进样口一侧与所述第二反应区之
间,用于将所述抗原抗体对进行混匀后送入所述第二反应区。
18.在一些实施方式中,所述第一流道、所述第二流道为蛇形微流道。
19.在一些实施方式中,所述第二反应区沉积有二氧化硅阵列,所述第二抗体接枝于所述二氧化硅阵列。
20.在一些实施方式中,所述第二反应区呈凹槽状,凹槽的容积是根据pcr扩增所需反应物的总体积确定的。
21.在一些实施方式中,所述第一进样口还用于在形成双抗夹心后注入缓冲液,以对所述检测芯片进行清洗;
22.所述基板还包括:
23.废液池,与所述第二反应区远离所述第一反应区一侧连通,用于缓存清洗后的废液;
24.所述盖板还包括:
25.出样口,与所述废液池的远离所述第二反应区一侧连通,用于排出废液。
26.在一些实施方式中,所述盖板及所述基板的材质包括透明材质。
27.在一些实施方式中,所述透明材质包括:聚甲基丙烯酸甲酯或者玻璃。
28.第二方面,本发明实施例提供一种检测设备,包括第一方面所述的检测芯片。
29.在一些实施方式中,所述检测设备,还包括:
30.荧光显微镜,用于对pcr扩增后产物进行荧光信号检测,以确定待检测样本中抗原的含量。
31.第三方面,本发明实施例提供一种检测方法,基于第一方面所述的检测芯片或者基于第二方面所述的检测设备实现,所述检测方法包括:
32.待检测样本从第一进样口进入第一反应区,所述待检测样本中的抗原与预埋在所述第一反应区的第一抗体进行特异性结合,形成抗原抗体对;
33.所述抗原抗体对进入第二反应区,接枝于所述第二反应区的第二抗体捕获所述抗原抗体对,形成双抗夹心;
34.对所述双抗夹心进行pcr扩增;
35.对pcr扩增后产物进行荧光信号检测,以确定待检测样本中抗原的含量。
36.在一些实施方式中,所述待检测样本从第一进样口进入第一反应区,包括:
37.所述待检测样本从第一进样口进入所述检测芯片,经第一流道混匀后进入第一反应区;
38.所述抗原抗体对进入第二反应区,包括:
39.所述抗原抗体对经第二流道混匀后进入所述第二反应区。
40.在一些实施方式中,所述待检测样本从第一进样口进入所述检测芯片,经第一流道混匀后进入第一反应区之后,对所述待检测样本进行反复抽送,以使所述待检测样本中的抗原与所述第一抗体充分反应;和/或
41.所述抗原抗体对经第二流道混匀后进入所述第二反应区之后,对所述抗原抗体对进行反复抽送,以使所述抗原抗体对与所述第二抗体充分反应。
42.在一些实施方式中,所述第一抗体包括:已标记dna片段且冻干于目标载体上的抗体;
43.所述待检测样本从第一进样口进入第一反应区,所述待检测样本中的抗原与预埋在所述第一反应区的第一抗体进行特异性结合,包括:
44.待检测样本从第一进样口进入第一反应区,使所述第一反应区中预埋的所述第一抗体复溶;
45.所述待检测样本中的抗原与所述第一抗体进行特异性结合。
46.在一些实施方式中,所述对所述双抗夹心进行pcr扩增,包括:
47.通过至少一个第二进样口向第二反应区注入mix试剂、引物试剂及探针试剂,对所述双抗夹心进行pcr扩增。
48.在一些实施方式中,所述对所述双抗夹心进行pcr扩增,包括:
49.将所述检测芯片置于热板或pcr反应设备进行pcr扩增。
50.在一些实施方式中,在所述形成双抗夹心后,所述方法还包括:
51.通过第一进样口注入缓冲液,以对所述检测芯片进行清洗。
52.与现有技术相比,本发明实施例提供的技术方案至少能够带来如下有益效果:
53.采用dna片段对提供信号的第一抗体进行标记,并预埋于基板上形成的第一反应区,将第一进样口注入含有抗原的待检测样本时,待检测样本中的抗原与第一抗体发生特异性结合反应形成抗原抗体对,抗原抗体对被基板上形成的第二反应区中接枝的第二抗体捕获形成双抗夹心,进一步对双抗夹心进行pcr扩增,即使在待检测样本中抗原浓度极低的情况下,也能够检测出抗原并通过pcr扩增后产物的荧光信号来确定抗原的浓度,很好地解决了检测芯片灵敏度偏低,待检测样本中浓度较低的物质检出率不高的问题。
附图说明
54.图作简单地介绍,应当理解,以下附图仅示出了本发明的某些实施例,因此不应被看作是对范围的限定,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他相关的附图。
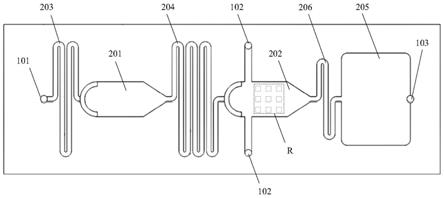
55.图1是本发明实施例提供的一种检测芯片结构示意图;
56.图2a是本发明实施例提供的盖板结构示意图;
57.图2b是本发明实施例提供的基板结构示意图。
具体实施方式
58.下面将结合本发明实施例中附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。通常在此处附图中描述和示出的本发明实施例的组件可以以各种不同的配置来布置和设计。因此,以下对在附图中提供的本发明的实施例的详细描述并非旨在限制要求保护的本发明的范围,而是仅仅表示本发明的选定实施例。基于本发明的实施例,本领域技术人员在没有做出创造性劳动的前提下所获得的所有其他实施例,都属于本发明保护的范围。
59.体外诊断行业按照原理主要分为生化诊断、分子诊断和免疫诊断,近年来免疫诊断成为体外诊断中规模最大的子领域。微孔板是目前免疫诊断中主要的耗材,与微孔板相比,微流控芯片具有缩短反应时间、减少试剂消耗、操作简便、集成化、自动化、便携化等优势,是新型的免疫诊断耗材。免疫微流控芯片,其原理是利用抗原
‑
抗体特异性结合,在微流
控芯片上完成反应并能体现检测结果的生物检测芯片,其优点就是只需少量病人标本或生物样品,通过一次检测便可获得多种相关生物信息或疾病的检测结果。与现行监测方法相比,具有通量高、快速、操作简便、自动化程度高等优点。相关技术中,免疫微流控芯片需要预埋标记荧光素的抗体,并将该抗体冻干到芯片上,将标记有荧光素的抗体冻干预存在玻璃基板上,捕获抗体接枝到sio2阵列上,通过外接气动装置,将待检测样本依次通过芯片,反应完成后检测捕获区域的荧光信号,以此来反映样本中标志物的浓度,然而,此种检测方法的劣势是检测灵敏度偏低,对样本中浓度较低的物质检出率不高。本发明实施例提供的检测芯片,是一种免疫pcr微流控芯片,不采用荧光素标记预埋的抗体,而是采用dna片段来标记预埋的抗体,在免疫反应完成后,在特定区域加入pcr扩增所需试剂进行pcr扩增,测得扩增后产物的荧光信号即可间接表征待检测样本中标志物的浓度,此芯片能够检测出样本中浓度极低的标志物,具有广泛应用前景。
60.实施例一
61.图1示出了一种检测芯片结构示意图,图2a、图2b分别示出了盖板结构示意图和基板结构示意图,如图1、图2a
‑
图2b所示,本实施例提供一种检测芯片,包括:基板2及位于基板2上方的盖板1;
62.盖板1,包括:
63.第一进样口101,用于注入待检测样本;
64.基板2,包括:
65.第一反应区201,预埋有已标记dna片段的第一抗体,第一反应区201与第一进样口101连通,用于进行待检测样本中的抗原与第一抗体的特异性结合,以形成抗原抗体对;
66.第二反应区202,接枝有第二抗体,第二反应区202与第一反应区201远离第一进样口101一侧连通,用于进行第二抗体捕获抗原抗体对以形成双抗夹心和进行pcr扩增,以通过pcr扩增后产物的荧光信号表征待检测样本中抗原的含量,以通过pcr扩增后产物的荧光信号表征待检测样本中抗原的含量。
67.本实施例中,采用dna片段对提供信号的第一抗体进行标记,并预埋于基板上形成的第一反应区,通过外接气动装置将第一进样口注入含有抗原的待检测样本时,待检测样本中的抗原与第一抗体发生特异性结合反应形成抗原抗体对,抗原抗体对被基板上形成的第二反应区中接枝的第二抗体捕获形成双抗夹心,进一步对双抗夹心进行pcr(聚合酶链式反应,polymerase chain reaction)扩增,即使在待检测样本中抗原浓度极低的情况下,也能够检测出抗原并通过pcr扩增后产物的荧光信号来确定抗原的浓度,很好地解决了检测芯片灵敏度偏低,待检测样本中浓度较低的物质检出率不高的问题,在一些疾病早期筛查领域有广泛应用前景。
68.在一些实施方式中,盖板及基板的材质包括但不限于透明材质,透明材质可以包括:聚甲基丙烯酸甲酯(pmma,polymethyl methacrylate)或者玻璃,可以通过将盖板用模切胶进行覆膜,将盖板封装于基板上方。
69.在一些实施方式中,盖板1还包括:
70.至少一个第二进样口102,与第二反应区202连通,用于注入pcr扩增所需试剂。在实际应用中,pcr扩增所需试剂包括但不限于mix试剂、引物试剂和探针试剂。在一些情形下,盖板包括一个第二进样口102,通过该第二进样口102注入pcr扩增所需试剂。另一些情
形下,盖板包括两个第二进样口102,分别用于注入pcr扩增所需的不同试剂,例如,一个进样口用于注入mix试剂,另一个第二进样口102用于注入引物试剂和探针试剂。另一些情形下,盖板包括三个第二进样口102,分别用于注入pcr扩增所需的不同试剂,例如,一个进样口用于注入mix试剂,另一个第二进样口102用于注入引物试剂,再一个第二进样口102用于注入探针试剂。图1所示为盖板包括两个第二进样口102的情形,仅为一种示例,并不能作为对本实施例提供的检测芯片结构的唯一限定,且两个第二进样口102也不限于图1所示的布设方式。
71.在一些情形下,将第一抗体冻干到基板的第一反应区处,在将盖板用模切胶进行覆膜并与基板封装时,冻干的第一抗体极易被破坏和污染,且冻干的抗体粉末可能高于pmma的沟道深度,容易造成抗体试剂的浪费,且在抗体复溶的过程中,冻干的第一抗体的复溶可能不完全,容易残留在基板上造成浓度的改变,复溶效果可能不理想。因此,在一些实施方式中,第一抗体包括:已标记dna片段且冻干于目标载体上的抗体,目标载体可以包括但不限于多孔载体,多孔载体可以为但不限于纸基。
72.在实际应用中,将标记有dna片段的抗体冻干于目标载体上,放置于基板2的第一反应区201,再将盖板1与基板2封装,实现第一抗体的预埋。一方面,采用dna片段对提供信号的第一抗体进行标记并在后续进行pcr扩增,可以很好地将待检测样本中浓度较低的物质检出,另一方面通过将预埋的第一抗体提前冻干到目标载体并封装于特定反应区,与直接冻干到检测芯片上的方式相比,可以有效减少抗体试剂在检测芯片上的残留,同时防止了冻干后的抗体试剂被破坏。
73.将标记有dna片段的抗体冻干于目标载体上,可以采用但不限于如下方式:吸取标记有dna片段的抗体,滴至目标载体以将目标载体浸润,使目标载体吸收该抗体,在
‑
40℃至
‑
80℃环境下对吸收有该抗体的目标载体进行冷冻,冷冻完成后进行干燥升华,使该抗体成为粉末状态实现冻干。
74.在一些情形下,可以根据检测所需第一抗体的试剂浓度,可对目标载体进行多次冻干
‑
复溶实验,以确定以固定工艺复溶后第一抗体的试剂成份。目标载体的大小可以为但不限于矩形,且尺寸略小于第一反应区201的尺寸,这样,在封装时可以直接将目标载体放进基板与盖板的夹层中,冻干的第一抗体不会受到破坏,且在复溶的时候,第一抗体不会残留在检测芯片上。
75.在一些实施方式中,基板2还包括:
76.第一流道203,连接于第一进样口101和第一反应区201之间,用于将从第一进样口101注入的待检测样本进行混匀后送入第一反应区201;
77.第二流道204,连接于第一反应区201远离第一进样口101一侧与第二反应区202之间,用于将抗原抗体对进行混匀后送入第二反应区202。
78.在一些实施方式中,第一流道203、第二流道204为蛇形微流道。第一流道203、第二流道204作为检测芯片的两个混匀区域,能够将进入流道的待检测样本/第一反应区所形成的抗原抗体对进行有效混匀,使得第一反应区201、第二反应区202内的反应更加充分。
79.在一些实施方式中,第二反应区202沉积有二氧化硅阵列r,第二抗体接枝于二氧化硅阵列r上,以与进入第二反应区202的抗原抗体对反应,形成双抗夹心。在实际应用中,基板经过羧基修饰后,将捕获用的第二抗体接枝到第二反应区202的sio2阵列上,4℃孵育
过夜,孵育完成。
80.在一些实施方式中,第二反应区202呈凹槽状,凹槽的容积是根据pcr扩增所需反应物的总体积确定的。在实际应用中,pcr扩增所需反应物可以包括但不限于双抗夹心及pcr扩增所需试剂,pcr扩增所需试剂包括但不限于mix试剂、引物试剂和探针试剂。根据pcr扩增所需反应物的总体积确定第二反应区202的凹槽容积,能够防止在后期pcr扩增过程中试剂溢出。
81.在一些实施方式中,第一进样口101还用于在形成双抗夹心后注入缓冲液,以对检测芯片进行清洗;
82.基板2还包括:
83.废液池205,与第二反应区202远离第一反应区201一侧连通,用于缓存清洗后的废液;
84.盖板还包括:
85.出样口103,与废液池205的远离第二反应区202一侧连通,用于排出废液。
86.在实际应用中,在抗原抗体对与第二抗体在第二反应区202反应完成后,可以从第一进样口101通过外接气动装置泵入缓冲液,对反应后的各区域(包括第一反应区210、第二反应区202及各流道等)进行冲洗,以清洗掉复溶后未特异性结合完的第一抗体、未被捕获的抗原抗体对等等,废液流入废液池,通过出样口103排出检测芯片,应当理解的是,在一些情况下,排出废液时可以通过在出样口103外接管路进行排出。前述缓冲液可以是但不限于pbs(磷酸盐缓冲盐溶液,phosphate buffered saline)。
87.在一些实施方式中,基板2还包括:
88.第三流道206,连接于第二反应区202远离第一反应区201一侧和废液池205之间。在实际应用中,第三流道206可以采用但不限于蛇形微流道。
89.在一些实施方式中,第一反应区201中与第一流道203连通的一侧、第二反应区202中与第二流道204连通的一侧可以设置台阶207,使进入第一反应区201、第二反应区202中的液体沿着台阶207所提供的平面向前流动,以使液面更加平缓地进入相应地反应区。
90.应当理解的是,图1、图2a及图2b仅为本实施例的检测芯片的示例,在实际应用中,第一反应区、第二反应区、废液池及各流道的具体形状及结构可根据需求调整,不限于图示的形状及结构。
91.实施例二
92.本发明实施例提供一种检测设备,包括:
93.实施例一的检测芯片。
94.在一些实施方式中,该检测设备还包括:
95.荧光显微镜,用于对pcr扩增后产物进行荧光信号检测,以确定待检测样本中抗原的含量。
96.在一些实施方式中,该检测设备还可以包括:
97.外接于第一进样口101的气泵装置,用于从第一进样口101注入待检测样本、缓冲液等,以及对待检测样本进行反复抽送,以使待检测样本中的抗原与第一抗体充分反应;和/或,对抗原抗体对进行反复抽送,以使抗原抗体对与第二抗体充分反应。
98.在一些实施方式中,该检测设备还包括:
99.热板或pcr反应设备,用于提供pcr扩增环境,使检测芯片置于热板或pcr反应设备上时,能够进行pcr扩增。
100.在一些情形下,根据pcr扩增环境的温度需求,配置多个热板,以实现pcr扩增所需的不同温度环境,在实际应用中,将检测芯片分别置于各温度的热板上反应即可实现pcr扩增,也可以是将检测芯片置于pcr反应设备,实现扩增所需的不同温度环境,完成pcr扩增。
101.本实施例中,采用dna片段对提供信号的第一抗体进行标记,并预埋于基板上形成的第一反应区,通过外接气动装置将第一进样口注入含有抗原的待检测样本时,待检测样本中的抗原与第一抗体发生特异性结合反应形成抗原抗体对,抗原抗体对被基板上形成的第二反应区中接枝的第二抗体捕获形成双抗夹心,进一步对双抗夹心进行pcr扩增,即使在待检测样本中抗原浓度极低的情况下,也能够利用荧光显微镜检测出抗原并通过pcr扩增后产物的荧光信号来确定抗原的浓度,很好地解决了检测芯片灵敏度偏低,待检测样本中浓度较低的物质检出率不高的问题。
102.实施例三
103.本实施例提供一种检测方法,基于实施例一的检测芯片或者基于实施例二的检测设备实现,该检测方法包括:
104.步骤s110、待检测样本从第一进样口进入第一反应区,待检测样本中的抗原与预埋在第一反应区的第一抗体进行特异性结合,形成抗原抗体对。
105.步骤s120、抗原抗体对进入第二反应区,接枝于第二反应区的第二抗体捕获抗原抗体对,形成双抗夹心。
106.步骤s130、对双抗夹心进行pcr扩增;
107.步骤s140、对pcr扩增后产物进行荧光信号检测,以确定待检测样本中抗原的含量。
108.本实施例中,将pcr扩增反应与免疫反应结合起来,预埋的第一抗体上标记有dna片段,与待检测样本中的抗原形成抗原抗体对后,由第二抗体捕获,形成双抗夹心,由于双抗夹心中的第一抗体上标记有dna片段,在免疫反应完成后对反应产物进行pcr扩增,也就对dna片段进行了pcr扩增,进而将检测芯片放置于荧光显微镜下进行光学信号检测,检测出的荧光信号能够间接表征待检测样本中的抗原含量,此方法能检测出待检测样本中浓度极低的标志物。
109.在一些实施方式中,待检测样本从第一进样口进入第一反应区,包括:
110.待检测样本从第一进样口进入检测芯片,经第一流道混匀后进入第一反应区;
111.抗原抗体对进入第二反应区,包括:
112.抗原抗体对经第二流道混匀后进入所述第二反应区。
113.第一流道、第二流道作为检测芯片的两个混匀区域,能够将进入流道的待检测样本/第一反应区所形成的抗原抗体对进行有效混匀,使得第一反应区、第二反应区内的反应更加充分。
114.在一些实施方式中,待检测样本从第一进样口进入检测芯片,经第一流道混匀后进入第一反应区之后,对待检测样本进行反复抽送,以使待检测样本中的抗原与第一抗体充分反应;和/或
115.抗原抗体对经第二流道混匀后进入第二反应区之后,对抗原抗体对进行反复抽
送,以使抗原抗体对与第二抗体充分反应。
116.在实际应用中,既可以只在待检测样本从第一进样口进入检测芯片,经第一流道混匀后进入第一反应区之后,对待检测样本进行反复抽送,也可以只在抗原抗体对经第二流道混匀后进入第二反应区之后,对抗原抗体对进行反复抽送,还可以在待检测样本从第一进样口进入检测芯片,经第一流道混匀后进入第一反应区之后和抗原抗体对经第二流道混匀后进入第二反应区之后,都进行反复抽送,本实施例不做唯一限定。应当理解的是,反复抽送的次数,可以根据实际情况而定,本实施例也不做任何限定。另外,反复抽送的过程中,液体还可以暂存于废液池,避免直接经出样口排出至外接的管路,避免液体进入外接的管路后再抽回而使反应物污染。
117.在一些实施方式中,第一抗体包括:已标记dna片段且冻干于目标载体上的抗体;
118.待检测样本从第一进样口进入第一反应区,待检测样本中的抗原与预埋在第一反应区的第一抗体进行特异性结合,包括:
119.待检测样本从第一进样口进入第一反应区,使第一反应区中预埋的第一抗体复溶;
120.待检测样本中的抗原与所述第一抗体进行特异性结合。
121.在实际应用中,在已标记dna片段的第一抗体冻干于目标载体的情形下,冻干完成后,目标载体放置于基板上的第一反应区,在抗原与第一抗体进行特异性结合时会先使第一抗体复溶,进而发生特异性结合。将标记有dna片段的抗体冻干于目标载体上,可以采用但不限于如下方式:吸取标记有dna片段的抗体,滴至目标载体以将目标载体浸润,使目标载体吸收该抗体,在
‑
40℃至
‑
80℃环境下对吸收有该抗体的目标载体进行冷冻,冷冻完成后进行干燥升华,使该抗体成为粉末状态实现冻干。
122.在一些实施方式中,对双抗夹心进行pcr扩增,包括:
123.通过至少一个第二进样口向第二反应区注入mix试剂、引物试剂及探针试剂,对双抗夹心进行pcr扩增。
124.在一些实施方式中,对双抗夹心进行pcr扩增,包括:
125.将检测芯片置于热板或pcr反应设备进行pcr扩增。
126.在一些实施方式中,在形成双抗夹心后、进行pcr扩增之前,该方法还包括:
127.通过第一进样口注入缓冲液,以对检测芯片进行清洗。
128.在实际应用中,注入缓冲液,能够清洗掉复溶后未特异性结合完的第一抗体、未被捕获的抗原抗体对等等,废液流入废液池,通过出样口排出检测芯片,避免废液对pcr扩增的干扰。
129.在本发明实施例所提供的几个实施例中,应该理解到,所揭露的系统和方法,也可以通过其它的方式实现。以上所描述的系统和方法实施例仅仅是示意性的。
130.需要说明的是,在本文中,术语“包括”、“包含”或者其任何其他变体意在涵盖非排他性的包含,从而使得包括一系列要素的过程、方法、物品或者设备不仅包括那些要素,而且还包括没有明确列出的其他要素,或者是还包括为这种过程、方法、物品或者设备所固有的要素。在没有更多限制的情况下,由语句“包括一个
……”
限定的要素,并不排除在包括所述要素的过程、方法、物品或者设备中还存在另外的相同要素。
131.虽然本发明所揭露的实施方式如上,但所述的内容只是为了便于理解本发明而采
用的实施方式,并非用以限定本发明。任何本发明所属技术领域内的技术人员,在不脱离本发明所揭露的精神和范围的前提下,可以在实施的形式上及细节上作任何的修改与变化,但本发明的专利保护范围,仍须以所附的权利要求书所界定的范围为准。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。