1.本发明属于废液分析检测领域,具体地说,涉及一种混合酸的废液或回收液中多组分的分析检测方法。
背景技术:
2.作为锂离子电池负极材料的石墨要求纯度高,杂质低,因此,需要有配套的提纯工艺来降低石墨中的杂质含量。目前,许多企业采用混酸法来除负极材料中的杂质,混酸法是负极材料提纯工艺中效果最好、成本最低、污染最大的方法。为了减少对环境的污染,同时最大限度的利用酸,申请人在混酸法提纯的基础上,拟采取膜分离技术来实现盐酸、氢氟酸回收再利用。但在实际操作中,存在废酸残液或回收酸组分复杂(主要包括游离酸、cl
‑
、f、si、al等)且含量不明的问题,故而,不能明确游离酸耗尽情况、回收酸组分和含量情况。因此,需要开发简单、方便,易于操作的检测方法来对此类溶液进行监测。
3.现有技术中,韩立斌等通过以百里香酚酞为第一级滴定指示剂,然后以氯化钙溶液作为沉淀剂,再以百里香酚酞作为第二级滴定指示剂对含磷酸、氢氟酸及硫酸的混酸体系组分含量进行了测试,并取得了比较准确的分析结果。扬州市卫生防疫站杨一超等研制了“空气中hf、hcl、h2so4共存时离子色谱测定”的方法。杨慧茹等报道了适用于氢氟酸和硫酸混合体系的电位滴定法、电极法、沉淀法、酸碱滴定法等。antje henβge等报道了用电位滴定法通过两步滴定确定了hno3、hf、h2sio4混酸中各组分含量。尽管有对简单混酸体系检测方法的探索,但是目前还没有关于检测含hcl、hf、si、al的溶液各组分含量的工业分析方法的报道。
4.目前,在较先进的分析测试手段中,阴离子虽可用离子色谱法对进行监测,但是该方法的仪器成本较高,对操作人员要求较高,操作过程繁杂且稀释过程易引入误差,不适用于工业现场分析。阳离子可用等离子体发射光谱法进行检测,但是该方法同样具有上述缺点。此外,由于氢氟酸会溶蚀管路(含硅),采用上述方法既损伤设备,又会增加对硅检测的不准确性。因此,需要提出一种简单、方便、快捷的对混合酸的废液或回收液中多组分的分析检测方法。
5.有鉴于此特提出本发明。
技术实现要素:
6.本发明要解决的技术问题在于克服现有技术的不足,提供一种混酸废液或回收液中多组分的分析检测方法。本发明采用(雷磁自动滴定仪)电位滴定法来测试废酸残液或回收酸中的各组分含量,在整个过程只需要两步滴定就可计算出cl
‑
、游离酸、si、铝、氟的含量。在整个过程中样品无需处理,一次出结果,简单快捷,可重复性好。
7.为解决上述技术问题,本发明采用技术方案的基本构思是:
8.本发明的第一目的是提供一种混合酸的废液或回收液中多组分的分析检测方法,包括:准备混合酸的废酸残液或回收酸,检测方法包括滴定并计算其中的氢氟酸、盐酸、硅、
铝的含量,步骤如下:
9.(1)测定废酸残液或回收酸中cl
‑
的含量;
10.(2)测定废酸残液或回收酸中游离酸、硅、铝的含量;
11.(3)根据电荷守恒原则计算氟的含量。
12.混酸提纯法是用一定浓度的盐酸和氢氟酸的混合溶液对负极材料前驱体进行酸洗提纯的方法。由于提纯后的混酸溶液中仍含有大量的盐酸、氢氟酸,为了降低生产成本,可以对废酸残液中的有效成分进行回收再利用。若回收酸中游离酸的浓度含量不明确,会影响回收酸的可重复利用性;回收酸中组分的含量不明确,则无法将回收酸调整为可用酸。通过离子色谱仪和电感耦合等离子发射光谱仪(icp)对废酸成分进行检验,得出经酸洗提纯后的混酸残液中,主要包含游离酸、cl
‑
、f、si、al等组分(需要说明的是,f、si、al在溶液中存在形式复杂,不仅以单离子形式存在,本技术中统一用元素的符号表示)。由于以上两种测试方法具有以下特点:1)仪器成本高;2)操作较为复杂,易引入误差;3)需要专人操作和维护,专业性较,使其不适用于非知识密集型企业。因此,迫切需要开发一套适用于多组分混合酸成分分析的工业分析方法。
13.基于开发适用于多组分混合酸成分分析方法的思路,本发明提供了一种可以准确检测废酸残液以及回收酸中氢氟酸、盐酸、硅、铝、氟各成分的含量的方法,一方面可以明确游离酸的浓度,便于回收酸进行重复利用;另一方面,可以明确各成分的含量,以便于调整为可用酸。本发明的分析检测方法,通过两次滴定便可计算出cl
‑
、游离酸、si、铝、氟的含量,整个过程中样品无需处理,一次出结果,简单快捷,重复性好,准确性高。
14.本发明的分析检测方法适用于各种含有氢氟酸、盐酸、硅、铝的混合溶液中各成分含量的检测,尤其特别适用于锂离子电池负极材料提纯用酸液组分检测。
15.进一步的方案,步骤(1)中,测定废酸残液或回收酸中cl
‑
含量的方法包括:
16.s1,配制nacl标准溶液和一定浓度的agno3溶液;
17.s2,用nacl标准液标定agno3溶液,计算硝酸银溶液的准确浓度;
18.s3,将定量的废酸残液或回收酸,加入去离子水,用已知浓度的agno3溶液进行滴定;
19.s4,计算废酸残液或回收酸中cl
‑1的浓度。
20.进一步具体的方案,
21.s1中,配制0.5mol/l nacl标准液溶液的方法,包括:1)取一定量nacl试剂于600℃烘箱中保温2小时恒重后,置于干燥器中,冷却至室温备用。2)称取一定量的已恒重的氯化钠于100ml烧杯中,加水溶解。3)转移到1000ml容量瓶,用去离子水冲洗小烧杯及转移的玻璃棒三次,定容容量瓶即可;
22.配制约为0.1m agno3溶液:称取一定量的硝酸银试剂溶于水中,稀释至1l,贮于棕色试剂瓶中,待标定后使用。
23.s2中,agno3的标定:吸取一定体积的0.5mol/l氯化钠标准溶液,于100ml烧杯中,加适量去离子水,加硝酸酸化,再加淀粉溶液(1g/100ml),再用待标定的硝酸银溶液进行滴定。
24.agno3溶液的浓度的计算公式为:
25.其中,v
终点
为滴定终点消耗的agno3溶液的体积。
26.s3中,对cl
‑1的滴定:吸取一定量的(v
废酸残液或回收酸
)的废酸残液或回收酸于100ml烧杯中,加去离子水,用标准硝酸银溶液进行滴定,滴定消耗agno3体积为
27.s4中,计算cl
‑1浓度的公式为即
28.进一步的方案,步骤(2)中,测定废酸残液或回收酸中游离酸、硅、铝的含量的方法包括:
29.s1,配制邻苯二甲酸氢钾标准溶液和一定浓度的氢氧化钠溶液;
30.s2,采用邻苯二甲酸氢钾标准溶液标定氢氧化钠溶液,计算氢氧化钠溶液的准确浓度;
31.s3,取一定体积的废酸残液或回收酸,用已知浓度的naoh溶液进行滴定,直至滴定出现三个滴定终点为止,记录达到三个滴定终点所消耗的naoh的体积v1,v2和v3;
32.s4,分别计算废酸残液或回收酸中游离酸、硅、铝的含量。
33.进一步的方案,
34.s1中,配制邻苯二甲酸氢钾标准溶液的方法包括:1)邻苯二甲酸氢钾试剂应在100
‑
125℃干燥1
‑
2h,2)在干燥器中冷却至室温备用,3)称取一定质量的邻苯二甲酸氢钾溶于去离子水中,制得0.1m的邻苯二甲酸标准溶液。
35.配制浓度约为0.5m naoh溶液:称取一定量naoh溶于去离子水中,定容后,制得浓度大概为0.5m的naoh溶液。
36.s2中,naoh标准溶液的标定:取一定体积的邻苯二甲酸氢钾溶液于烧杯中,加50ml去离子水,naoh溶液进行标定,滴定消耗naoh体积为v
naoh
,计算出naoh标准溶液的真实浓度。
37.s2中,计算氢氧化钠溶液浓度的公式为c
naoh
v
naoh
=c
邻苯二甲酸氢钾
v
邻苯二甲酸氢钾
,即
38.s3中,游离酸、硅、铝的滴定:取一定体积(v
废酸残液或回收酸
)的废酸残液或回收酸于烧杯中,加50ml去离子水,用naoh标准溶液进行滴定。调整v
废酸残液或回收酸
直至滴定出现三个滴定终点为止,记录达到三个滴定终点所消耗的naoh的体积v1,v2和v3。
39.本发明中通过雷磁自动滴定仪的计算机依据电位
‑
体积曲线确定拐点,即电位
‑
体积的偏导函数的最高点来确定滴定终点的,也就是说,滴定终点依据雷磁电位滴定仪自动读出的数据进行记录即可。
40.进一步的方案,
41.s4中,计算游离酸的含量的公式为c
游离酸
v
废酸残液或回收酸
=c
naoh
v1,即
42.计算废酸残液或回收酸中硅含量的公式为4c
si
v
废酸残液或回收酸
=(v2‑
v1)c
naoh
,即
43.计算废酸残液或回收酸中铝含量的公式为4c
al
v
废酸残液或回收酸
=(v3‑
v2)c
naoh
,即
44.本发明的检测的方法,通过一次滴定,便可以依次分析计算出废酸残液或回收酸中游离酸、硅、铝的含量,步骤简单,快捷,方便,适用于工业现场分析。
45.进一步的方案,步骤(3)中,根据电荷守恒原则计算氟的含量,公式为
46.c
f
=c
游离酸
4c
硅
3c
al
‑
c
cl
‑
。
47.本发明的第二目的是提供一种如上方案所述的混合酸的废液或回收液中多组分的分析检测方法在锂离子电池负极材料提纯用酸液组分检测中的应用。
48.采用上述技术方案后,本发明与现有技术相比具有以下有益效果:
49.1、采用本发明的电位滴定方法分析检测混合酸的废液或回收液中的多种组分,整个过程只需要两次滴定便可以计算出cl
‑
、游离酸、si、铝、氟的含量,整个过程中样品不需要额外处理,一次出结果,简单快捷,重复性好,适用于工业现场分析。
50.2、本发明的分析检测方法适用于对各种混合酸的废液或回收液中多种组分的检测,尤其特别适用于锂离子电池负极材料提纯用酸液组分检测。
51.下面结合附图对本发明的具体实施方式作进一步详细的描述。
附图说明
52.附图作为本发明的一部分,用来提供对本发明的进一步的理解,本发明的示意性实施例及其说明用于解释本发明,但不构成对本发明的不当限定。显然,下面描述中的附图仅仅是一些实施例,对于本领域普通技术人员来说,在不付出创造性劳动的前提下,还可以根据这些附图获得其他附图。在附图中:
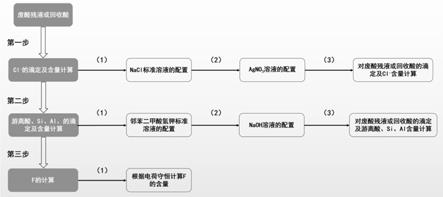
53.图1是本发明分析检测方法的过程示意图。
54.需要说明的是,这些附图和文字描述并不旨在以任何方式限制本发明的构思范围,而是通过参考特定实施例为本领域技术人员说明本发明的概念。
具体实施方式
55.为使本发明实施例的目的、技术方案和优点更加清楚,下面将结合本发明实施例中的附图,对实施例中的技术方案进行清楚、完整地描述,以下实施例用于说明本发明,但不用来限制本发明的范围。
56.需要说明的是,本发明中所述“滴定”,指通过两种溶液的定量反应来确定某种溶质的含量,可以采用现有技术中已有的具体方法实施。
57.本发明具体提供一种混合酸的废液或回收液中多组分的分析检测方法,准备混合酸的废酸残液或回收酸,废液或回收液中包含氢氟酸、盐酸、硅、铝组分,检测方法包括滴定并计算其中的氢氟酸、盐酸、硅、铝的含量,步骤如下:
58.第一步:对废酸残液或回收酸中游离cl
‑
的滴定,具体包括:
59.(1)配制0.5m nacl溶液:1)取一定量nacl试剂于600℃烘箱中保温2小时恒重后,置于干燥器中,冷却至室温备用。2)称取一定量的已恒重的氯化钠于100ml烧杯中,加水溶解。3)转移到1000ml容量瓶,用去离子水冲洗小烧杯及转移的玻璃棒三次,定容容量瓶即可;
60.(2)配制约为0.1m agno3溶液:称取一定量的硝酸银溶于水中,稀释至1l,贮于棕色试剂瓶中,待标定后使用;
61.(3)agno3的标定:吸取一定体积的0.5mol/l氯化钠标准溶液,于100ml烧杯中,加适量去离子水,加硝酸酸化,再加淀粉溶液(1g/100ml),再用待标定的硝酸银溶液进行滴定;
62.(4)计算硝酸银溶液的浓度,公式为
63.(5)对cl
‑1的滴定:吸取一定量的(v
废酸残液或回收酸
)的废酸残液或回收酸于100ml烧杯中,加去离子水,用标准硝酸银溶液进行滴定,滴定消耗agno3体积为
64.(6)计算废酸残液或回收酸中cl
‑1的浓度:公式为的浓度:公式为
65.涉及到的离子反应式如下:
66.nacl agno3=agcl
↓
nano367.第二步:对废酸残液或回收酸中游离酸、硅、铝的滴定,具体包括,
68.(1)配制邻苯二甲酸氢钾标准溶液:1)邻苯二甲酸氢钾试剂应在100
‑
125℃干燥1
‑
2h,2)在干燥器中冷却至室温备用,3)称取一定质量的邻苯二甲酸氢钾溶于去离子水中,制得0.1mol/l的邻苯二甲酸标准溶液。
69.(2)配制浓度约为0.5mol/l naoh溶液:称取一定量naoh溶于去离子水中,定容后,制得浓度大概为0.5mol/l的naoh溶液;
70.(3)naoh标准溶液的标定:取一定体积的邻苯二甲酸氢钾溶液于烧杯中,加50ml去离子水,naoh溶液进行标定,滴定消耗naoh体积为v
naoh
,计算出naoh标准溶液的真实浓度;
71.计算氢氧化钠溶液浓度的公式为c
naoh
v
naoh
=c
邻苯二甲酸氢钾
v
邻苯二甲酸氢钾
,即
72.(4)游离酸、硅、铝的滴定:取一定体积(v
废酸残液或回收酸
)的废酸残液或回收酸于烧杯中,加50ml去离子水,用naoh标准溶液进行滴定。调整v
废酸残液或回收酸
直至滴定出现三个滴定终点为止,记录达到三个滴定终点所消耗的naoh的体积v1,v2和v3;
73.本发明中,需要调整摸索使废酸残液或回收酸的体积适量,以便于采用naoh标准溶液滴定时,可以间隔出现三个滴定终点。若废酸残液或回收酸的体积过小,则少量氢氧化钠滴入后,反应连续完成,间隔时间过小,无法分辨出三个滴定终点;若废酸残液或回收酸的体积过大,则耗费naoh溶液过多,耗费时间过长,则造成浪费。
74.具体的,取0.2ml(v
废酸残液或回收酸
)的废酸残液或回收酸于烧杯中,加50ml去离子水,将naoh标准溶液滴入烧杯中;
75.首先,oh
‑
与废酸残液或回收酸中的游离酸反应,当游离酸与氢氧化钠反应完全时,达到第一个滴定终点,记录所消耗的naoh的体积v1;
76.涉及的化学反应式为:
77.a.hcl naoh=nacl h2o
78.b.hf naoh=naf h2o
79.c.h2sif6 2naoh=na2sif6 2h2o
80.然后,继续滴加naoh标准溶液,oh
‑
与废酸残液或回收酸中的si反应,当溶液中的硅元素全部转化为si(oh)4时,达到第二个滴定终点,记录所消耗的naoh的体积v2;
81.涉及的化学反应式为:
82.na2sif6 4naoh=si(oh)4 6naf=sio2 6naf h2o
83.最后,继续滴加naoh标准溶液,oh
‑
与废酸残液或回收酸中的al元素反应,当al元素全部转化为alo2‑
时,达到第三个滴定终点,记录所消耗的naoh的体积v3;
84.涉及的化学反应式为:
[0085][0086]
(5)游离酸、硅、铝浓度的计算:
[0087]
1)c
游离酸
v
废酸残液或回收酸
=c
naoh
v1,
[0088]
2)4c
si
v
废酸残液或回收酸
=(v2‑
v1)c
naoh
,
[0089]
3)4c
al
v
废酸残液或回收酸
=(v3‑
v2)c
naoh
,
[0090]
那么,
[0091]
第三步根据电荷守恒计算氟的含量,公式为c
f
=c
游离氢
4c
硅
3c
al
‑
c
cl
‑
。
[0092]
本发明的方法可以通过现有技术的方法实现,可以手动检测,也可以采用仪器检测,均可以实现,差异在于精确度的差别。为了使检测结果更加精确,可以采用仪器检测。作为一种优选的方案,本发明的滴定过程通过雷磁自动滴定仪的电位滴定模式进行检测的,滴定终点由计算机通过计算得出。作为一种具体的方案,通过雷磁自动滴定仪的电位滴定模式进行检测的装置及参数如下:
[0093]
采用的装置
[0094][0095]
装置参数设置
[0096]
(1)在滴定过程中始终打开搅拌器,转速为20r/min;
[0097]
(2)在正式滴定前要先进行空白滴定;
[0098]
(3)滴定的参数设置一般有:
[0099]
1)滴定类型:本发明用邻苯二甲酸标定氢氧化钠溶液和用氢氧化钠滴定游离酸的滴定类型选“ph”,其余的滴定选“mv”;
[0100]
2)稳定时间设置6s;
[0101]
3)添加体积的方式的选择,如果可以判断物质的大概浓度,可以选择预加一定体积已知浓度的溶液,如果不确定,则不选预加;
[0102]
4)每次添加体积:需要根据滴定误差预判评估。eg:要控制滴定误差在1%,则滴定过程要滴定100滴已知溶液,若到滴定过程预计滴4ml,则可设置每次添加体积为0.04ml。
[0103]
5)终点个数不需设置;
[0104]
6)突跃量设置为1。
[0105]
实施例1
[0106]
如图1所示,本实施例提供了一种检测锂离子电池负极材料混酸法提纯后的废酸残液中的各成分的含量的方法。采用上述所述雷磁自动滴定仪进行检测。废酸残液中的成分主要包括游离酸、cl
‑
、f、si、al。具体测试步骤如下,
[0107]
第一步:对废酸残液或回收酸中游离cl
‑
的滴定,具体包括:
[0108]
(1)配制0.5m nacl溶液:1)取一定量nacl试剂于600℃烘箱中保温2小时恒重后,置于干燥器中冷却至室温备用;2)称取29.250g的已恒重的氯化钠nacl于100ml小烧杯中,加水溶解。3)转移到1l容量瓶,用去离子水冲洗小烧杯及转移的玻璃棒三次,定容容量瓶即可;
[0109]
(2)配制约为0.1m agno3溶液:称取16.987g的硝酸银溶于水中,稀释至1l,贮于棕色试剂瓶中,待标定后使用;
[0110]
(3)agno3的标定:吸取1ml的0.5mol/l氯化钠标准溶液,于100ml烧杯中,加适量去离子水,加硝酸酸化,再加淀粉溶液(1g/100ml),再用待标定的硝酸银溶液进行滴定,直到滴定终点共计消耗agno3溶液4.971ml;
[0111]
(4)计算硝酸银溶液的浓度,公式为(4)计算硝酸银溶液的浓度,公式为
[0112]
(5)对cl
‑1的滴定:吸取50ml的(v
废酸残液或回收酸
)的废酸残液或回收酸于100ml烧杯中,用标准硝酸银溶液进行滴定,滴定消耗agno3体积为
[0113]
(6)计算废酸残液或回收酸中cl
‑1的浓度:公式为的浓度:公式为
[0114]
第二步:对废酸残液或回收酸中游离酸、硅、铝的滴定,具体包括,
[0115]
(1)配制邻苯二甲酸氢钾标准溶液:邻苯二甲酸氢钾试剂应在100
‑
125℃干燥1
‑
2h,然后于干燥器中冷却至室温。称取20.422g的邻苯二甲酸氢钾溶于1l去离子水中,制得0.1m的邻苯二甲酸标准溶液;
[0116]
(2)配制约为0.5m naoh溶液:称取19.998g naoh溶于去离子水中,定容后,制得1l
浓度大概为0.5m的naoh溶液;
[0117]
(3)naoh标准溶液的标定:取10ml的邻苯二甲酸氢钾溶液于烧杯中,加40ml去离子水,naoh溶液进行标定,滴定消耗naoh体积v
naoh
为2ml,计算出naoh标准溶液的真实浓度,
[0118]
(4)游离酸、硅、铝的滴定:取0.2ml(v
废酸残液或回收酸
)的废酸残液或回收酸于烧杯中,加50ml去离子水,用naoh标准溶液进行滴定。调整v
废酸残液或回收酸
直至滴定出现三个滴定终点为止,记录达到三个滴定终点所消耗的naoh的体积分别是:v1为2.946ml、v2为4.345ml、v3为4.700ml;
[0119]
利用下述公式计算游离酸、硅、铝的浓度:
[0120][0121]
计算得废酸中游离酸、si、al的含量分别依次是7.365mol/l、0.874mol/l、0.222mol/l。
[0122]
第三步根据电荷守恒计算氟的含量,公式为c
f
=c
游离氢
4c
硅
3c
al
‑
c
cl
‑
,计算氟的含量为11.482mol/l。
[0123]
实施例2
[0124]
作为本发明的另一实施例,本实施例提供了一种检测锂离子电池负极材料混酸法提纯后的废酸残液中的各成分的含量的方法,其检测方法与实施例1所述方法相同,区别在于,在本实施例中,选取的废酸残液不同。具体检测步骤如下:
[0125]
第一步:对废酸残液中游离cl
‑
的滴定,具体包括:
[0126]
(1)配置0.5mol/l nacl溶液、0.1mol/l agno3溶液,对agno3溶液进行标定、计算硝酸银溶液浓度与实施例1对应步骤完全一致。
[0127]
(2)对cl
‑1的滴定:吸取0.2ml的(v
废酸残液或回收酸
)的废酸残液或回收酸于100ml烧杯中,用标准硝酸银溶液进行滴定,滴定消耗agno3体积为为6.266ml。
[0128]
(3)计算废酸残液或回收酸中cl
‑1的浓度:公式为的浓度:公式为
[0129]
第二步:对废酸残液或回收酸中游离酸、硅、铝的滴定,具体包括,
[0130]
(1)邻苯二甲酸氢钾标准溶液、naoh溶液配置,对naoh溶液的标定与实施例1对应步骤完全一致;
[0131]
(2)游离酸、硅、铝的滴定:取0.2ml(v
废酸残液或回收酸
)的废酸残液或回收酸于烧杯中,加50ml去离子水,用naoh标准溶液进行滴定。调整v
废酸残液或回收酸
直至滴定出现三个滴定终点为止,记录达到三个滴定终点所消耗的naoh的体积分别是:v1为2.113ml、v2为3.121ml、v3为5.323ml;
[0132]
利用下述公式计算游离酸、硅、铝的浓度:
[0133][0134]
根据电荷守恒计算氟的含量,公式为c
f
=c
游离氢
4c
硅
3c
al
‑
c
cl
‑
,计算氟的含量。
[0135]
(3)计算得废酸中游离酸、si、al以及f的含量分别是5.282mol/l、0.63mol/l、1.376mol/l、8.778mol/l。
[0136]
以上所述仅是本发明的较佳实施例而已,并非对本发明作任何形式上的限制,虽然本发明已以较佳实施例揭露如上,然而并非用以限定本发明,任何熟悉本专利的技术人员在不脱离本发明技术方案范围内,当可利用上述提示的技术内容作出些许更动或修饰为等同变化的等效实施例,但凡是未脱离本发明技术方案的内容,依据本发明的技术实质对以上实施例所作的任何简单修改、等同变化与修饰,均仍属于本发明方案的范围内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。