1.本发明涉及免疫学技术、血清抗体组学技术及疾病诊断领域,更具体地,本发明涉及辅助诊断桥本甲状腺炎的血清相关自身抗体标志物及其应用。
背景技术:
2.桥本甲状腺炎(hashimoto's thyroiditis,ht)又称桥本氏病(hashimoto's disease,hd)或慢性淋巴细胞性甲状腺炎(chronic lymphocytic thyroiditis,clt),是目前最常见的自身免疫性甲状腺疾病,也是导致甲状腺功能减退最常见的原因。据文献报道约20%
‑
30%的患者会出现甲状腺功能减退。当前ht发病率逐年快速增加,已成为严重威胁人们健康和生活质量的一类常见疾病。有数据指出全世界有13.8%
‑
38%的人患有ht,女性患病率为男性的4
‑
10倍。我国目前尚缺乏大规模的ht流行病学调查研究,对不同地方的ht患病率相关报道1.03%
‑
23.08%不等。ht常起病隐匿,早期无特异临床症状,因此易被漏诊、误诊,多数病例在常规体检时被发现,而大部分患者处于未知晓状态。目前对ht治疗固有地缺少有效药物,尤其发病早期缺少有效的治疗药物。因此提高桥本甲状腺炎的早期诊断率和研制更加高效安全的治疗药物是其治疗的关键。
3.桥本甲状腺炎的病因被认为是遗传易感性和环境因素相结合,导致免疫耐受丧失,进而对甲状腺组织进行自身免疫攻击而发生疾病,其中79%的易感性由遗传因素造成,21%是环境和其他因素影响,如吸烟、碘摄入、硒缺乏、维生素d缺乏、干扰素α类药物治疗、放射暴露、胎儿微嵌合体、怀孕、更年期等。ht发病机制至今尚未完全阐明,根据已有研究主要与细胞免疫、抑制和调节性t细胞缺陷、细胞毒性和细胞凋亡、体液免疫、甲状腺自身抗体、钠碘转运体和pendrin抗体、细胞因子、趋化因子作用有关。其病理过程包括形成甲状腺自身抗体,损伤甲状腺细胞,破坏甲状腺组织。目前常用于临床诊断的甲状腺自身抗体包括抗甲状腺球蛋白抗体(tgab)、甲状腺过氧化物酶抗体(tpoab)或甲状腺微粒体抗体(tmab)、tsh受体抗体(trab)(包括tsh受体刺激性抗体(tsab)、tsh刺激阻断性抗体(tsbab)和tsh受体结合抑制免疫球蛋白(tbii))。其中tpoab被认为是ht最重要的特征,约95%的患者存在tpoab,而tgab诊断的可靠性较tpoab低,在60%
‑
80%的病例中存在。自身抗体的产生是自身免疫性疾病的基本特征之一,除上述甲状腺相关自身抗体,桥本甲状腺炎患者血清中可能还存在许多针对其他特异性和非特异性抗原产生的自身抗体,然而目前鲜有关于ht相关自身抗体及血清诊断标志物的筛选和研究。
4.huprot
tm
人类蛋白质组芯片含有>20000个新测序的全长人类重组蛋白,对应16152个独特的蛋白编码基因,覆盖率高达81%,是迄今为止世界上最高通量的人重组蛋白质组芯片,与其他蛋白质组芯片相比具有高灵敏度、特异度,可以对各种蛋白质、抗体以及配体进行检测。该芯片已应用于标志物筛选鉴定、小分子靶标、蛋白与蛋白相互作用、核酸与蛋白相互作用、病原菌与宿主相互作用、抗体特异性研究等,正在成为一种在癌症和自身免疫性疾病中发现新的自身抗体和生物标志物的高效方法。目前国内外学者应用该蛋白质组芯片在肺癌、胃癌、卵巢癌、结直肠癌、胶质瘤、神经精神性狼疮、白塞病等疾病生物标志物的
研究中均有新的发现。但目前尚未有应用此技术筛选桥本甲状腺炎诊断标志物的研究。
技术实现要素:
5.针对现有技术的不足,本发明的目的是提供辅助诊断桥本甲状腺炎的血清相关自身抗体标志物及其应用,该抗体标志物能够有效、准确地辅助诊断桥本甲状腺炎。
6.为了实现上述目的,本发明的技术方案之一是:
7.辅助诊断桥本甲状腺炎的血清相关自身抗体标志物,该抗体标志物为nc2b、kras、tmem243、cdc42相关自身抗体中至少一种。
8.优选的,该抗体标志物为nc2b、kras、tmem243、cdc42四种相关自身抗体的组合。
9.本发明的技术方案之一是:一种上述血清相关自身抗体标志物在制备桥本甲状腺炎辅助诊断相关试剂、试剂盒中的应用。
10.本发明的技术方案之一是:一种上述血清相关自身抗体标志物在制备桥本甲状腺炎治疗药物中的应用。
11.本发明的技术方案之一是:一种桥本甲状腺炎辅助诊断试剂盒,包括elisa技术所用的nc2b、kras、tmem243、cdc42人重组蛋白中至少一种。
12.进一步,该桥本甲状腺炎辅助诊断试剂盒,还包括人源igg标准品、辣根过氧化物酶标记的山羊抗人igg以及elisa技术常用的试剂。
13.上述试剂盒用于检测血清中nc2b、kras、tmem243、cdc42四种相关自身抗体中至少一种。
14.本发明的技术方案之一是:一种上述试剂盒在辅助诊断桥本甲状腺炎中的应用。
15.自身抗体是引发自身免疫反应的重要因素,也是自身免疫性疾病的重要标志,不同的自身免疫性疾病有不同的自身抗体谱。患者血液中存在高效价自身抗体是自身免疫性疾病的特点之一,也是临床确诊自身免疫性疾病的重要依据。筛选出的相关自身抗体有助于进一步深入研究桥本甲状腺炎的发病机制。
16.血清相关自身抗体作为诊断标志物,具有稳定性好、易获取、灵敏度和特异性高的特点。筛选出具有诊断价值的血清相关自身抗体的开发利用将为包括桥本甲状腺炎在内的同类自身免疫性疾病的诊断和治疗提供新的范例。
17.本发明的有益效果:
18.本发明运用huprot
tm
人类蛋白质组芯片从桥本甲状腺炎患者血清样本中筛选出具有显著差异的相关自身抗体,进而采用elisa法在更多样本中对筛选出的自身抗体进行验证,旨在寻找新的对桥本甲状腺炎具有潜在诊断价值的血清标志物。并根据此类血清标志物设计出对桥本甲状腺炎的诊断试剂盒,将有助于提高桥本甲状腺炎的早期诊断和诊治水平,也将为桥本甲状腺炎的进一步研究和治疗提供新的思路。
19.具体地说,本发明技术方案包括:(1)建立统一标准的标本库和数据库:系统收集完整的患者基本信息和临床病例资料,以标准操作程序采集符合标准的血液样本。(2)运用高通量huprot
tm
人类蛋白质组芯片技术分析桥本甲状腺炎和正常对照人群中差异表达的血清相关自身抗体,运用统计学和生物信息学方法筛选差异表达的有意义的相关自身抗体。(3)进一步大样本验证,明确这些相关自身抗体诊断桥本甲状腺炎灵敏性、特异性。(4)血清相关自身抗体诊断试剂盒的研制:根据桥本甲状腺炎与正常人群血清中差异表达的相关自
身抗体开发诊断试剂盒,实现对桥本甲状腺炎患者的早期辅助诊断,为将来研制可能与这些相关自身抗体治疗有关的桥本甲状腺炎药物提供依据。
20.本发明通过huprot
tm
人类蛋白质组芯片以及elisa法,对桥本甲状腺炎和正常对照者血清中的差异表达相关自身抗体进行严格的、多阶段的验证和评价,证实了nc2b、kras、tmem243、cdc42四种相关自身抗体及其组合物作为新的辅助诊断桥本甲状腺炎标记物的可靠性以及可重复性。运用高通量蛋白质组芯片技术筛选出桥本甲状腺炎血清相关自身抗体标志物有助于桥本甲状腺炎的早期辅助诊断,以早发现、早治疗。
附图说明
21.图1为蛋白质芯片检测原理。
22.图2为芯片扫描质量评估结果(蛋白点样)。
23.注:图a为芯片扫描图:分别展示为整体扫描(左)和局部放大图(右),其中从左至右第1
‑
4个箭头所指为阳性对照(gst,浓度从左至右分别为10ng/μl、50ng/μl、100ng/μl、200ng/μl),最右侧箭头为阴性对照(bsa蛋白);图b为芯片制备重复性评价结果。
24.图3为桥本甲状腺炎血清样本的芯片扫描结果图。
25.注:左一图为芯片全局扫描图,右一图为芯片局部放大图,中间为merge合成图。右一图上下两个激光通道和通道分别为532nm
‑
igg通道、635nm
‑
igm通道;merge图下方从左至右第1
‑
2个箭头指示为阳性对照点(分别为human igg、human igm),最右侧箭头指示为阴性对照点(bsa);右—图中的箭头指示为阳性点,其中右上图箭头所示点表示532nm通道即igg响应,右下图箭头所示点表示635nm通道即igm响应,白色点表示igm和igg均有响应。
26.图4为桥本甲状腺炎组具有显著差异的76个相关自身抗体的snr聚类分析。
27.注:横向为样本,纵向为该样本对应的蛋白(igg或igm响应类型)。
28.图5为桥本甲状腺炎组相关自身抗体蛋白互作网路图。
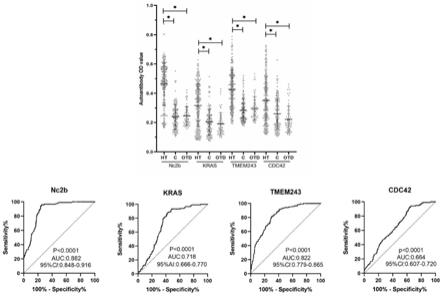
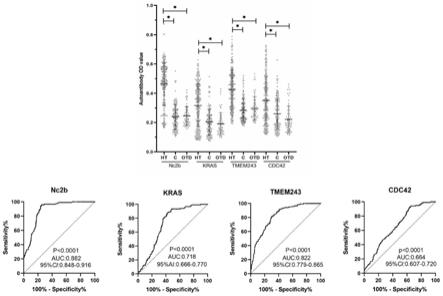
29.图6为桥本甲状腺炎疾病特征性相关自身抗体的散点图和roc曲线图。
30.注:ht:桥本甲状腺炎组,c:正常对照组,otd:其他甲状腺疾病组。
31.图7为四种相关自身抗体单独诊断和联合诊断roc曲线图。
具体实施方式
32.以下结合实施例对本发明的具体实施方式作进一步详细说明。
33.实施例1、蛋白质芯片筛选桥本甲状腺炎相关自身抗体
34.1、血清标本来源
35.2017年1月至2019年12月从河南中医药大学第一附属医院、第三附属医院、郑州大学第一附属医院收集门诊和住院初诊的未经治疗的桥本甲状腺炎患者,从中国人民解放军第988医院收集健康体检人群的静脉血清样本。从中选取15例桥本甲状腺炎患者(甲状腺功能正常、甲状腺功能亢进、甲状腺功能减退患者各5例)和5例正常(健康)对照者血清样本作为huprot
tm
蛋白质组芯片检测样本,各组患者性别、年龄比较均无统计学差异。
36.2、蛋白芯片实验主要仪器设备
37.120090型晶芯slidewasher
tm
芯片洗干仪(北京博奥晶典生物技术有限公司)、晶芯luxscan
tm 10k
‑
a型微阵列芯片扫描仪(北京博奥晶典生物技术有限公司)、cytm3
‑
conjugated affinipure goat anti
‑
human igg(美国jackson公司)、alexa fluor 647
‑
conjugated affinipure donkey anti
‑
human igm(美国jackson公司)、multifuge x1r冷冻高速离心机(美国thermo公司)。
38.3、蛋白质芯片检测原理
39.每一个样品使用1张huprot
tm
蛋白质芯片进行检测,特异性的抗体(包括igg、igm或其它类型抗体)与固定于芯片上的蛋白进行结合,清洗去除未结合的抗体和其它蛋白质,再通过荧光标记二抗anti
‑
human igm(cy5标记,波长635nm)和anti
‑
human igg荧光二抗(cy3标记,波长532nm)并借助荧光扫描仪数据化信号。信号的强弱与抗体的亲和力、数量呈正相关。芯片检测原理图如图1所示。
40.4、蛋白芯片质量控制
41.在高通量芯片实验前通过对芯片进行质量检测以保证标志物筛选的可靠性。蛋白芯片上的蛋白n端均带有用于该蛋白纯化的gst(谷胱甘肽s
‑
转移酶)标签,因此利用抗gst抗体与蛋白质芯片杂交可以评估高密度蛋白质组芯片的质量。蛋白融合gst进行表达纯化,纯化后制备成芯片,并且每个蛋白重复2个点。芯片制备完成后通过anti
‑
gst进行芯片质量检测,蛋白点样结果展示如图2所示。从图2可知,以重复蛋白anti
‑
gst杂交产生的前景值为对象,通过散点图分析,线性拟合后的r2为0.98,说明芯片制备整体重复性良好;以anti
‑
gst杂交产生的信噪比为计算对象,通过阴性对照来评价蛋白点的检出率,由结果可知,蛋白检出率>99%,说明芯片制备合格。
42.5、蛋白芯片检测实验步骤
43.(1)封闭:将保存的蛋白芯片从
‑
80℃取出,置于侧摆摇床,加入封闭液,室温封闭3h;
44.(2)血清样本孵育:弃尽封闭液,迅速加入血清孵育液(血清用孵育液稀释200倍),置于侧摆摇床,4℃过夜孵育;
45.(3)清洗:用镊子将芯片取出(注意不能触及或划破芯片的上表面),置于水平摇床,清洗液室温清洗3次,10min/次;
46.(4)二抗孵育:置于侧摆摇床,二抗孵育液(二抗用孵育液稀释1000倍)室温孵育1h(从此步骤开始,注意避光操作);
47.(5)清洗:置于水平摇床,清洗液室温清洗3次,10min/次,完成后用超纯水室温清洗2次,10min/次;
48.(6)干燥:将芯片置于芯片干燥机离心干燥;
49.(7)扫描:按照扫描仪的操作规范和使用说明操作。设置参数为:power 90%,pmt value650,若存在爆点,调节pmt或者power至扫描无爆点。
50.6、蛋白芯片实验数据处理与统计分析
51.通过genepix pro v6.0软件读取芯片扫描结果,获取原始数据。运用r语言limma程序包对芯片数据进行处理。为消除同一张芯片内不同蛋白点之间由于背景值不一致导致的信号不均一的情况,故通过背景校正方法进行处理。实现方式为每个蛋白的前景值与背景值比值,即f/b,并此基础上定义snr(signal noise ratio,信噪比),即两个重复蛋白的f/b的均值。为了减少不同样品、不同芯片之间及实验操作等系统性差异带来的误差,在数据比对前对样本snr进行归一化处理,基于归一化后的数据进行统计学分析以筛选出实验
组区分于对照组的特异性响应抗体。
52.采用spss 22.0统计软件进行数据处理与统计分析。对连续型变量采用kolomogorov
‑
smirnov test进行正态性检验,符合正态分布的变量用表示;对于符合正态分布的连续型变量,采用t检验或单因素方差分析进行组间比较,多组间的两两比较采用dunnett检验;对于非正态分布的连续型变量,两组间比较采用mann
‑
whitney u秩和检验,分类变量间比较采用χ2检验,不满足χ2检验条件的资料采用fisher精确检验。检验水准α=0.05,以p<0.05为差异有统计学意义。
53.7、抗体标志物筛选
54.每个芯片的23034的蛋白位点,去除芯片上nd、control点,保留23032个蛋白位点。以归一化后的snr值为计算对象,基于统计学方法筛选潜在的特异性高响应抗体标志物,具体分析如下:
55.(1)对于任意一个蛋白,假设需要比对的样本来自完全相同的两个总体,并通过mann
‑
whitney u秩和检验,单尾,进行检验,并以p
‑
value进行表征。定义,当p
‑
value<0.05时,拒绝原假设,即两者存在显著性差异。
56.(2)对于任意一个蛋白,计算疾病组与健康对照组的差异表达倍数,即fold change=疾病组均值/健康对照组均值,用以表示疾病组高于健康对照组的程度;定义,fold change≥1.5即为潜在差异,一般认为差异倍数越大,两组间区别越明显。
57.(3)对于不同样本组,为避免出现阴性蛋白之间的比较,在进行样本比对前,根据归一化之后芯片上蛋白点信号snr值的分布设置阳性蛋白判断阈值,定义igg
‑
snr>4、igm
‑
snr>5时判断该蛋白为阳性蛋白。在此基础上,以对照组在该蛋白上的snr为计算对象设定cutoff阈值(cutoff
‑
igg≥4,cutoff
‑
igm≥5),分别计算疾病组与健康对照组的阳性率,并定义疾病组最低阳性率为50%,即在该蛋白上疾病组的阳性样本个数不低于3/5或8/15个;健康对照组的最高阳性率为0%,即在该蛋白上健康对照组阳性样本个数0/5个,分别计算疾病组的阳性率(sensitivity)和健康对照组的阳性率(1
‑
specificity)。
58.8、结果
59.8.1蛋白芯片扫描结果
60.每一个样本使用1张huprot
tm
蛋白质芯片进行检测,特异性的抗体(包括igg、igm或其它类型抗体)与固定于芯片上的蛋白相结合,清洗去除未结合的抗体和其它蛋白质,再通过荧光标记二抗anti
‑
human igm(cy5标记,波长635nm)和anti
‑
human igg荧光二抗(cy3标记,波长532nm),并借助荧光扫描仪数据化信号。信号的强弱与抗体的亲和力、数量呈正相关。芯片扫面结果示例如图3所示。从图3可知,检测分析得所有对照点均正常,本研究中实验样品芯片合格。
61.8.2筛选出的桥本甲状腺炎相关自身抗体
62.通过比较桥本甲状腺炎组(ht)与正常健康对照组(nc),筛选出具有显著差异的特异性免疫高响应相关自身抗体76个,其中igg响应类型49个,igm响应类型27个(fold change≥1.5,p
‑
value<0.05),见表1。
63.表1桥本甲状腺炎组(ht)与健康对照组(nc)比较具有显著差异的相关自身抗体
64.65.[0066][0067]
对筛选出的具有显著差异的76个相关自身抗体进行snr聚类分析如图4所示,从无监督学习聚类结果来看,ht组样本与nc组样本能通过两步聚类被区分。因此,可知所筛选出的蛋白在整体区分桥本甲状腺炎组与健康对照组中,分类正确率为100%。
[0068]
利用string蛋白互作数据库分析桥本甲状腺炎组筛选得出的差异蛋白之间的互作关系,构建蛋白互作网络,以综合评分(combination score)大于0.4为阈值条件,将string中所得蛋白互作网络数据导入cytoscape3.8.0软件,运用其网络分析(networkanalyzer)工具筛选蛋白互作网络的中心节点,得出桥本甲状腺炎组具有重要调节功能的节点蛋白有cdc42、kras等,见图5,涉及的主要分子功能为gtp酶活性、gpt结合,主要信号传导通路为肌动蛋白细胞骨架调节通路。
[0069]
9、筛选出的桥本甲状腺炎相关自身抗体
[0070]
从上述筛选出的76个桥本甲状腺炎相关自身抗体中,选取在桥本甲状腺炎甲状腺功能正常、甲状腺功能亢进和甲状腺功能减退患者中均有差异表达,且经genbank数据库检索在甲状腺组织和细胞中均高表达的蛋白,在更多血清样本中进行验证。待验证相关自身抗体为nc2b、kras、tmem243、cdc42、rasl11b,见表2。
[0071]
表2筛选出的待验证桥本甲状腺炎不同甲状腺功能状态共有的差异显著的相关自
身抗体
[0072][0073]
实施例2、间接elisa实验验证筛选出的桥本甲状腺炎相关自身抗体
[0074]
选取待验证相关自身抗体nc2b、kras、tmem243、cdc42、rasl11b,通过间接elisa实验在大样本中检测nc2b、kras、tmem243、cdc42、rasl11b五种相关自身抗体的含量,验证相关自身抗体作为诊断标志物的特异性、灵敏性。
[0075]
2.1血清标本来源
[0076]
2017年1月至2019年12月从河南中医药大学第一附属医院、第三附属医院、郑州大学第一附属医院收集门诊和住院初诊的未经治疗的桥本甲状腺炎患者及非桥本甲状腺炎的甲状腺疾病患者,从中国人民解放军第988医院收集健康体检人群的静脉血清样本。运用pass 15.0软件估算所需的样本量。根据本研究需求,桥本甲状腺炎患者组是正常对照组的样本量的2倍,按α=0.05,1
‑
β=0.90,患者组sensitivity最低证型p1=70%,正常对照组sensitivity p2=10%,将正常对照组均值 2sd作为截断值,根据截断值计算研究因素在桥本甲状腺炎组与正常对照组的阳性率,二者差值应大于10%。计算得桥本甲状腺炎组约需216例病人,正常对照组约需108例,考虑脱落及失访病例,需增加10%病例,最终桥本甲状腺炎组约需240例病人,正常对照组约需120例。
[0077]
从收集的血清样本中选取240例桥本甲状腺炎患者(其中甲状腺功能正常患者95例、甲状腺功能亢进患者60例、甲状腺功能减退患者85例)、60例非桥本甲状腺炎的甲状腺疾病患者、120例健康对照者血清样本作为elisa验证实验检测样本,各组患者性别、年龄比较均无统计学差异。
[0078]
2.2实验步骤
[0079]
(1)从生物公司购买的nc2b、kras、tmem243、cdc42、rasl11b商品化人重组蛋白分别用蛋白稀释液稀释至250μg/ml,用包被液将各重组蛋白按照表3所示分别稀释至合适的浓度,用移液枪加入至96孔酶标板中,100μl/孔,加样时要注意避免气泡并避免液体粘附于孔壁。另用包被液将人源igg标准品稀释8个梯度浓度(640ng/ml、320ng/ml、160ng/ml、80ng/ml、40ng/ml、20ng/ml、10ng/ml、0ng/ml)作为质控用来调节板与板之间的差异,100μl/孔,用封板膜封好后置于4℃冰箱,包被过夜。
[0080]
(2)封闭:弃去酶标板中包被液,在吸水纸上拍干,每孔内加入200μl 2%bsa进行封闭,用封板膜封好后置于4℃冰箱,封闭过夜。
[0081]
(3)洗板:将封闭过夜的酶标板取出,甩去板内封闭液,拍干,用96孔全自动洗板机
上1
×
pbst溶液洗板3次,拍干。
[0082]
(4)一抗(血清)孵育:用含1%bsa的1
×
pbst抗体稀释液以1:100(v/v)的比例在96孔深孔板中稀释血清样本(现用现稀释),用12孔道移液枪把稀释好的血清样本加入酶标板内,100μl/孔,空白对照孔加入100μl不含血清的抗体稀释液,封板膜封口,在37℃恒温水浴锅中半水浴孵育1h。
[0083]
(5)洗板:弃去酶标板内的血清稀释液,拍干,用96孔全自动洗板机上1
×
pbst溶液洗板5次,并在吸水纸上拍干酶标板。
[0084]
(6)二抗孵育:用含1%bsa的1
×
pbst抗体稀释液以1:10000(v/v)的比例稀释辣根过氧化物酶标记的山羊抗人igg二抗(现配现用),用12孔道移液枪向酶标板内加入稀释好的二抗,100μl/孔,封板膜封好后,37℃半水浴孵育1h。
[0085]
(7)洗板:弃去酶标板每孔内的二抗稀释液,拍干,用96孔全自动洗板机上1
×
pbst溶液洗板5次,并在吸水纸上拍干酶标板。
[0086]
(8)显色反应:提前30min打开酶标仪预热,设置好标本布局和测量双波长(450nm和620nm)。取出4℃冰箱里的底物液a和底物液b按1:1(v/v)比例混匀(现用现配),用12孔道移液枪向酶标板加入显色液,100μl/孔,室温避光反应5
‑
10min。
[0087]
(9)终止反应:肉眼观察出现颜色变化后,及时用12孔道移液枪向酶标板内加入终止液,50μl/孔,使反应终止,终止完全后放入酶标仪内检测,保存实验数据。
[0088]
表3各蛋白包被浓度
[0089][0090]
2.3数据处理与统计分析
[0091]
使用spss 22.0、graphpad prism 8.0对获取的实验数据进行统计学分析。通过roc曲线计算各相关自身抗体的auc、灵敏度、特异度以及95%置信度区间(95%ci),筛选标准定义为auc>0.5且p<0.05。选取特异度大于90%时的最大约登指数(灵敏度 特异度
‑
1)并定义为截断值。所有分析均采取双侧检验,当p值小于0.05时,认为差异具有统计学意义。
[0092]
2.4结果
[0093]
结果如表4所示,根据auc>0.5且p<0.05剔除rasl11b,其在桥本甲状腺炎患者血清和正常对照血清中的浓度差异无统计学意义,其余相关自身抗体nc2b、kras、tmem243、cdc42在桥本甲状腺炎患者血清中的抗体浓度均显著高于正常对照血清中的水平,且差异具有统计学意义(p<0.05)。
[0094]
表4 5种桥本甲状腺炎相关自身抗体的诊断价值
[0095]
[0096]
nc2b、kras、tmem243、cdc42四种相关自身抗体在桥本甲状腺炎患者、非桥本甲状腺炎的其他甲状腺疾病患者和健康对照者中表达的散点图和roc曲线图见图6。由图6可知,ht组相关自身抗体表达量显著高于健康对照组和其他甲状腺疾病患者组。
[0097]
经elisa验证得出的nc2b、kras、tmem243、cdc42四种相关自身抗体在桥本甲状腺炎患者中,单个抗体诊断和四种抗体联合诊断的roc曲线图见图7,可以看出四种相关自身抗体联合诊断的auc值最高(0.992),表明nc2b、kras、tmem243、cdc42四种相关自身抗体联合诊断具有较高的诊断价值。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。