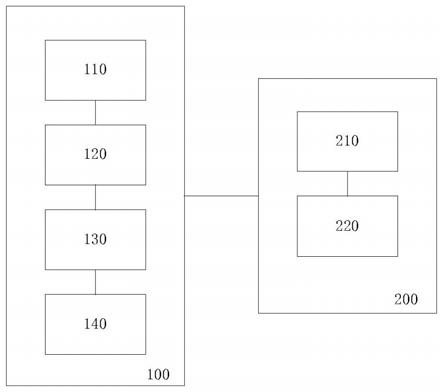
6
‑
氯甲基
‑2‑
吡啶甲醇的检测方法和应用
技术领域
1.本发明属于检测技术领域,具体涉及6
‑
氯甲基
‑2‑
吡啶甲醇的检测方法和应用。
背景技术:
2.抗体药物偶联物(antibody drug conjugate,adc)是将单克隆抗体与药物进行偶联所获得的偶联产物。通过化学键将细胞毒药物与单克隆抗体进行偶联,利用抗体可特异性识别肿瘤细胞的特性,可以“精确”地把毒性小分子运送到肿瘤细胞,在提高肿瘤部位药物浓度的同时降低正常组织、器官的药物浓度,达到高效低毒的抗肿瘤效果。
3.式(1)所示的化合物(其中r1为(ch2)
n
或peg),是实现对生物分子定点偶联修饰的重要化合物。该化合物在用于偶联生物分子与修饰物时,生物分子的活性和亲和力更好。在制备抗癌药物中显示出极大的优势,如曲妥珠单抗等抗癌药物。
[0004][0005]6‑
氯甲基
‑2‑
吡啶甲醇是该化合物合成中的重要中间体,与该化合物具有相同的官能团吡啶环,且取代位置存在一致性。合成式(1)所示的化合物的过程中,6
‑
氯甲基
‑2‑
吡啶甲醇的纯度将直接影响式(1)所示的化合物以及抗体药物偶联物的纯度,从而影响抗癌药物的疗效。对6
‑
氯甲基吡啶
‑2‑
甲酸甲醇的检测,对控制式(1)所示的化合物以及抗体药物偶联物纯度和质量至关重要。
[0006]
已知在制备6
‑
氯甲基吡啶
‑2‑
甲酸甲醇中,6
‑
氯甲基吡啶
‑2‑
甲酸甲酯是最大的杂质。采用液相色谱对6
‑
氯甲基吡啶
‑2‑
甲酸甲醇进行检测,6
‑
氯甲基吡啶
‑2‑
甲酸甲醇很难与杂质实现有效分离,尤其是与已知杂质6
‑
氯甲基吡啶
‑2‑
甲酸甲酯。
[0007]
因此,亟需提供6
‑
氯甲基
‑2‑
吡啶甲醇的检测方法,能够使6
‑
氯甲基
‑2‑
吡啶甲醇与已知杂质、未知杂质均能实现有效分离,能够实现其纯度的检测。
技术实现要素:
[0008]
本发明旨在至少解决上述现有技术中存在的技术问题之一。为此,本发明提出6
‑
氯甲基
‑2‑
吡啶甲醇的检测方法,能够使6
‑
氯甲基
‑2‑
吡啶甲醇与已知杂质、未知杂质均能实现有效分离,其纯度检测的重复性好,准确率高。
[0009]
本发明第一方面提供了6
‑
氯甲基
‑2‑
吡啶甲醇的检测方法。
[0010]
具体的,6
‑
氯甲基
‑2‑
吡啶甲醇的检测方法,采用液相色谱进行检测;
[0011]
所述液相色谱的条件包括:采用流动相梯度洗脱;
[0012]
所述流动相包括流动相a和流动相b;所述流动相a为甲酸水溶液,所述流动相b为
乙腈。
[0013]
优选的,所述检测方法,包括以下步骤:
[0014]
(1)称量6
‑
氯甲基
‑2‑
吡啶甲醇,溶于稀释液中,制得系统适应性试验溶液;
[0015]
(2)取待测样品,溶于稀释液中,制得待测样品溶液;
[0016]
(3)取稀释液采用液相色谱进行检测,记录色谱图a;取所述系统适应性试验溶液,采用液相色谱进行检测,记录色谱图b;取所述待测样品溶液,以液相色谱进行检测,记录色谱图c;
[0017]
(4)在所述色谱图c中扣除所述色谱峰a,根据所述色谱图b、c,按峰面积归一化法计算所述6
‑
氯甲基
‑2‑
吡啶甲醇的纯度;
[0018]
所述液相色谱的条件包括:采用流动相梯度洗脱;
[0019]
所述流动相包括流动相a和流动相b;所述流动相a为甲酸水溶液,所述流动相b为乙腈。采用流动相为甲酸水溶液与乙腈进行梯度洗脱,能够改善分离效果;其中,甲酸水溶液还能够改善主峰及杂质峰的峰型。所述流动相不含盐,易配制、易平衡、易冲洗,能够减少分析时间,提高检测效率。
[0020]
优选的,所述甲酸水溶液的质量浓度为0.01%
‑
0.05%;进一步优选的,所述甲酸水溶液的质量浓度为0.01%
‑
0.03%。甲酸浓度越高酸性越大,对色谱柱寿命有影响,优选低浓度的甲酸水溶液为流动相。
[0021]
优选的,所述流动相梯度洗脱的条件为:
[0022]0‑
3分钟,所述流动相中流动相a的体积百分数为85%
‑
95%;
[0023]3‑
13分钟,所述流动相中流动相a的体积百分数由85%
‑
95%变化至5%
‑
15%;
[0024]
13
‑
23分钟,所述流动相中流动相a的体积百分数为5%
‑
15%;
[0025]
23
‑
24分钟,所述流动相中流动相a的体积百分数由5%
‑
15%变化至85%
‑
95%;
[0026]
24
‑
30分钟,所述流动相中流动相a的体积百分数为85%
‑
95%。
[0027]
进一步优选的,所述梯度洗脱的条件为:
[0028]0‑
3分钟,所述流动相中流动相a的体积百分数为87%
‑
93%;
[0029]3‑
13分钟,所述流动相中流动相a的体积百分数由87%
‑
93%变化至7%
‑
13%;
[0030]
13
‑
23分钟,所述流动相中流动相a的体积百分数为7%
‑
13%;
[0031]
23
‑
24分钟,所述流动相中流动相a的体积百分数由7%
‑
13%变化至87%
‑
93%;
[0032]
24
‑
30分钟,所述流动相中流动相a的体积百分数为87%
‑
93%。
[0033]
更优选的,所述梯度洗脱的条件为:
[0034]0‑
3分钟,所述流动相中流动相a的体积百分数为90%;
[0035]3‑
13分钟,所述流动相中流动相a的体积百分数由90%变化至10%;
[0036]
13
‑
23分钟,所述流动相中流动相a的体积百分数为10%;
[0037]
23
‑
24分钟,所述流动相中流动相a的体积百分数由10%变化至90%;
[0038]
24
‑
30分钟,所述流动相中流动相a的体积百分数为90%。
[0039]
优选的,所述液相色谱的条件还包括:检测波长:269nm
±
5nm;柱温:25
±
5℃;进样量:10
‑
30μl;流速:0.7
‑
1.2ml/min;检测器:紫外检测器;色谱柱为:c18色谱柱。
[0040]
优选的,所述色谱柱为wondasil c18 superb 5um 4.6*250mm(w)。
[0041]
优选的,在步骤(1)中,所述系统适应性试验溶液中所述6
‑
氯甲基
‑2‑
吡啶甲醇的
质量浓度为0.25
‑
1.0mg/ml。
[0042]
优选的,在步骤(1)
‑
(3)中,所述稀释液包括水和乙腈;进一步优选的,在所述稀释液中所述乙腈与水的体积比为(1
‑
2):(1
‑
2)。
[0043]
优选的,在步骤(3)中,所述色谱图b中,所述6
‑
氯甲基
‑2‑
吡啶甲醇的理论板数≥2000。
[0044]
本发明第二方面提供了6
‑
氯甲基
‑2‑
吡啶甲醇的检测方法的应用。
[0045]
具体的,所述检测方法在制备6
‑
氯甲基
‑2‑
吡啶甲醇中的应用。
[0046]
具体的,所述检测方法在制备抗体药物偶联物中的应用。
[0047]
采用所述检测方法检测6
‑
氯甲基
‑2‑
吡啶甲醇,从而对6
‑
氯甲基
‑2‑
吡啶甲醇、式(1)所示的化合物或抗体药物偶联物的质量进行监控。
[0048]
相对于现有技术,本发明的有益效果如下:
[0049]
(1)本发明提供的检测方法,以甲酸水溶液与乙腈为流动相,进行梯度洗脱,能够改善分离效果,使6
‑
氯甲基
‑2‑
吡啶甲醇及其已知杂质、未知杂质均能实现有效分离;且所述流动相不含盐,易配制、易平衡、易冲洗,可减少分析时间,提高检测效率。
[0050]
(2)本发明提供的检测方法,简便、快速、准确率高、重复性好,有利于6
‑
氯甲基
‑2‑
吡啶甲醇工业化生产和质量控制;进而有利于有效控制式(1)所示的化合物或抗体药物偶联物的纯的和质量,有利于对抗体药物偶联物进行更为深入的质量研究工作。
附图说明
[0051]
图1为实施例1中已知杂质6
‑
氯甲基吡啶
‑2‑
甲酸甲酯的高效液相色谱图;
[0052]
图2为实施例1中系统适应性溶液的高效液相色谱图;
[0053]
图3为实施例1中第1批待测样品第一次测试的高效液相色谱图;
[0054]
图4为实施例1中第1批待测样品第二次测试的高效液相色谱图;
[0055]
图5为实施例2中第2批待测样品溶液的高效液相色谱图;
[0056]
图6为实施例3中第3批待测样品溶液的高效液相色谱图;
[0057]
图7为实施例4中第4批待测样品溶液的高效液相色谱图;
[0058]
图8为对比例1中第1批待测样品溶液的高效液相色谱图。
具体实施方式
[0059]
为了让本领域技术人员更加清楚明白本发明所述技术方案,现列举以下实施例进行说明。需要指出的是,以下实施例对本发明要求的保护范围不构成限制作用。
[0060]
以下实施例中所用的原料、试剂或装置如无特殊说明,均可从常规商业途径得到,或者可以通过现有已知方法得到。
[0061]
实施例1
[0062]
(1)设置液相色谱条件:
[0063]
色谱柱:wondasil c18 superb 5um 4.6*250mm(w);
[0064]
进样量:20μl;
[0065]
流速:1.0ml/min;
[0066]
柱温:25℃;
[0067]
检测波长:269nm;
[0068]
流动相a:0.01%甲酸水溶液;
[0069]
流动相b:乙腈;
[0070]
稀释液:水与乙腈的体积比为1:1;
[0071]
检测器:紫外检测器;
[0072]
定量方法:面积归一化法;
[0073]
流动相梯度见表1;
[0074]
表1流动相梯度表
[0075]
时间(min)流动相a(%)流动相b(%)0901039010131090231090249010309010
[0076]
(2)空白试验:精密量取稀释液20μl,注入液相色谱仪进行检测,记录色谱图a。空白不得有干扰。
[0077]
(3)系统适应性溶液配制:取6
‑
氯甲基
‑2‑
吡啶甲醇的工作对照品适量置于容量瓶中,用稀释液溶解浓度约为0.5mg/ml液体,作为系统适应性试验溶液。已知杂质溶液配制:取6
‑
氯甲基吡啶
‑2‑
甲酸甲酯适量置于容量瓶中,用稀释液溶解定容;取第1批待测样品(批号为ilx04
‑
210101)适量,精密称定,加稀释液稀释制成浓度为0.5mg/ml的待测样品溶液。
[0078]
(4)系统适用性试验:精密量取系统适应性试验溶液20μl,注入液相色谱仪,记录色谱图b。理论板数按6
‑
氯甲基
‑2‑
吡啶甲醇计算应不低于2000。
[0079]
(5)精密量取已知杂质溶液和待测样品溶液各20μl,注入液相色谱仪,记录色谱图c1和c2。对获得的色谱图进行分析,其中已知杂质(6
‑
氯甲基吡啶
‑2‑
甲酸甲酯)的色图谱c1见图1,在图1中,横坐标为时间(time),纵坐标为吸光值(absorbance/mau),由图1可知表1所示的信息。
[0080]
表1
[0081] 出峰时间(min)峰面积峰面积占比(%)主峰分离度理论塔板数已知杂质12.407191.70298.973.6686333
[0082]
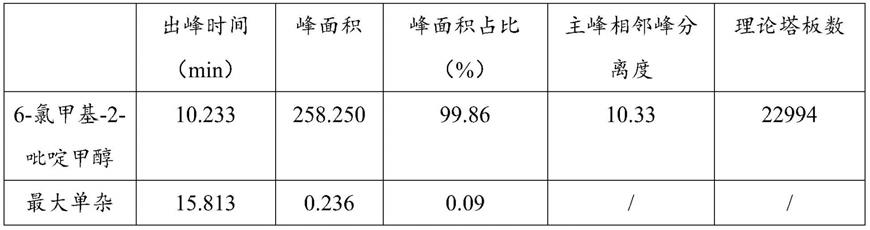
系统适应性溶液色谱图b见图2,在图2中,横坐标为时间(time),纵坐标为吸光值(absorbance/mau),由图2可知表2所示的信息。
[0083]
表2
[0084][0085]
待测样品溶液的色谱图c2见图3,在图3中,横坐标为时间(time),纵坐标为吸光值(absorbance/mau),由图3可知表3所示的信息。
[0086]
表3
[0087][0088]
在待测样品溶液的色谱图中扣除空白试验色谱峰a,按面积归一化法计算待测样品溶液中6
‑
氯甲基
‑2‑
吡啶甲醇的纯度为99.51%。
[0089]
对上述待测样品溶液((批号为ilx04
‑
210101))按照相同的检测方法进行第二次检测,待测样品溶液第二次测试的高效液相色谱图见图4,在图4中,横坐标为时间(time),纵坐标为吸光值(absorbance/mau),由图4可知表4所示的信息。6
‑
氯甲基
‑2‑
吡啶甲醇及其已知杂质(6
‑
氯甲基吡啶
‑2‑
甲酸甲酯)、未知杂质均能实现有效分离。
[0090]
表4
[0091][0092]
通过分析两次测定的峰面积,计算其相对标准偏差(rsd)为:0.02%,重复性好。在待测样品溶液的色谱图中扣除空白试验色谱峰a,按面积归一化法计算待测样品溶液中6
‑
氯甲基
‑2‑
吡啶甲醇的纯度为99.51%,计算两次测定的纯度的相对标准偏差(rsd),rsd为0.0%,该检测方法重复性好。
[0093]
实施例2
[0094]
与实施例1采用相同的检测方法对第2批待测样品(批号为ilx04
‑
210102)进行检测。
[0095]
待测样品的高效液相色谱图见图5,在图5中,横坐标为时间(time),纵坐标为吸光值(absorbance/mau),由图5可知表5所示的信息。6
‑
氯甲基
‑2‑
吡啶甲醇及其已知杂质(6
‑
氯甲基吡啶
‑2‑
甲酸甲酯)、未知杂质均能实现有效分离。待测样品中6
‑
氯甲基
‑2‑
吡啶甲醇的纯度为98.43%。
[0096]
表5
[0097][0098][0099]
实施例3
[0100]
与实施例1采用相同的检测方法对第3批待测样品(批号为ilx04
‑
210104)进行检测。
[0101]
待测样品的高效液相色谱图见图6,在图6中,横坐标为时间(time),纵坐标为吸光值(absorbance/mau),由图6可知表6所示的信息。6
‑
氯甲基
‑2‑
吡啶甲醇及其已知杂质(6
‑
氯甲基吡啶
‑2‑
甲酸甲酯)、未知杂质均能实现有效分离。待测样品中6
‑
氯甲基
‑2‑
吡啶甲醇的纯度为99.77%。
[0102]
表6
[0103]
[0104]
实施例4
[0105]
与实施例1采用相同的检测方法对第4批待测样品(批号为ilx04
‑
210105)进行检测。
[0106]
待测样品的高效液相色谱图见图7,在图7中,横坐标为时间(time),纵坐标为吸光值(absorbance/mau),由图7可知表7所示的信息。6
‑
氯甲基
‑2‑
吡啶甲醇及其已知杂质(6
‑
氯甲基吡啶
‑2‑
甲酸甲酯)、未知杂质均能实现有效分离。待测样品中6
‑
氯甲基
‑2‑
吡啶甲醇的纯度为99.76%。
[0107]
表7
[0108][0109][0110]
对比例1
[0111]
对比例1与实施例1的区别在于,采用0.01%磷酸水溶液(质量浓度)替代0.01%甲酸水溶液,其余检测方法同实施例1。
[0112]
待测样品的高效液相色谱图见图8,在图8中,横坐标为时间(time),纵坐标为吸光值(absorbance/mau),由图8可知,以0.01%磷酸水溶液作为流动相a时,主峰旁边的杂质无法得到良好的分离,无法检测其纯度,其效果明显不如甲酸溶液。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。