一种评估实体肿瘤claudin18.2蛋白表达的方法和应用
技术领域
1.本发明属于生物医学检测领域,具体涉及一种评估实体肿瘤claudin18.2蛋白表达的方法和应用。
背景技术:
2.claudins是一个紧密连接蛋白质家族,其中claudin18.2是一种胃特异性亚型,高度选择性表达于人正常胃粘膜上皮,但通常埋藏在胃粘膜中,正常情况下claudin18.2单克隆抗体难以结合claudin18.2的位点。近期研究表明,claudin18.2在胃癌、胰腺癌和胆管癌等实体肿瘤中存在不同程度的表达,且实体肿瘤会破坏紧密连接结构,导致肿瘤细胞的claudin18.2表位暴露,使claudin18.2成为实体肿瘤潜在的治疗靶点。以claudin18.2为靶点的抗肿瘤药物陆续在不同类型晚期实体肿瘤中开展早期临床研究,但目前尚无评估实体肿瘤中claudin18.2表达的有效手段,迫切需要开发一种能够快速、便捷且准确地评估实体肿瘤中claudin18.2蛋白表达的检测方法。
3.免疫组织化学是利用抗体特异性结合抗原的特性,通过抗体上标记物的显色部位及强度,来检测组织或细胞中某种蛋白质的定位和表达强度的技术,是检测实体肿瘤claudin18.2表达的可靠方法。但免疫组化检测存在一定的假阳性、假阴性,同一组织相同抗原在不同批次实验中的结果可能存在差异。因此,需要优化现有免疫组化技术及评估手段,提高免疫组化检测的稳定性和准确性,用于筛选claudin18.2阳性表达实体肿瘤,服务于靶向claudin18.2治疗。
技术实现要素:
4.本发明的主要目的是提供一种能够快速、准确且稳定地评估实体肿瘤claudin18.2蛋白表达的方法。
5.本发明的另一目的是提供上述评估实体肿瘤claudin18.2蛋白表达的方法在以claudin18.2蛋白为靶点的抗肿瘤药物筛选中的应用。
6.为实现上述目的,本发明采用如下技术方案:
7.本发明提供了claudin18.2蛋白在制备实体肿瘤诊断或预后评估的试剂盒中的应用。
8.优选地,所述试剂盒以claudin18.2蛋白作为诊断或预后评估的标记物。
9.优选地,所述实体肿瘤包括上皮来源的实体肿瘤。
10.优选地,所述试剂盒是通过免疫组化染色技术体外检测实体肿瘤患者的手术切除组织中claudin18.2蛋白的表达情况。
11.优选地,所述试剂盒包括如下试剂:
12.试剂a:claudin18.2单克隆抗体
×
1;
13.试剂b:hrp标记的igg二抗
×
1;
14.试剂c:pbs缓冲液
×
1;
15.试剂d:抗原修复液
×
1;
16.试剂e:3%过氧化氢溶液
×
1;
17.试剂f:山羊血清封闭液
×
1;
18.试剂g:dab浓缩液
×
1;
19.试剂h:dab缓冲液
×
1;
20.试剂i:苏木素染液
×
1;
21.其中,所述claudin18.2单克隆抗体可以特异性结合实体肿瘤细胞上的claudin18.2抗原。
22.优选地,所述免疫组化染色技术包括脱蜡、抗原修复、内源性过氧化物酶失活、封闭、一抗孵育、二抗孵育、dab显色、复染、脱水、封片和镜检的步骤。
23.本发明还提供了一种评估实体肿瘤claudin18.2蛋白表达的方法,包括以下步骤:
24.(1)将claudin18.2蛋白的质控、高表达、低表达、中表达和阴性对照切片,与实体肿瘤细胞膜的待检测切片一起进行免疫组化染色,镜下观察并机器采集图像;
25.(2)采用免疫组化分析软件分析上述图像,如所述claudin18.2蛋白质控对照切片、阴性对照切片的染色无假阳性或假阴性,用上述软件分别获取待检测切片和上述质控、高表达、低表达、中表达和阴性的对照切片claudin18.2蛋白染色的平均灰度值作为强度指标,阳性细胞比例作为占比指标,
26.(3)结合步骤(2)中强度指标按照如下标准进行打分,具体为:待检测切片的染色强度以对照切片的平均灰度值为判定标准,0表示待检测切片平均灰度值<低表达对照切片平均灰度值;1 表示低表达对照切片平均灰度值≤待检测切片平均灰度值<中表达对照切片平均灰度值;2 表示中表达对照切片平均灰度值≤待检测切片平均灰度值<高表达对照切片平均灰度值;3 表示待检测切片平均灰度值≥高表达对照切片平均灰度值;
27.同时使用免疫组化分析软件如image j获取待检测切片的阳性细胞占比值,综合待检测切片的强度指标和占比指标进行claudin18.2蛋白表达结果判定,标准为:
28.若待检测切片的染色强度≥2 ,且阳性细胞占比≥40%,认为实体肿瘤细胞膜中claudin18.2蛋白呈阳性;
29.若待检测切片的染色强度<2 ,或阳性细胞占比<40%,认为实体肿瘤细胞膜中claudin18.2蛋白呈阴性。
30.优选地,所述claudin18.2蛋白质控对照切片含有人正常胃粘膜上皮组织切片;
31.所述claudin18.2蛋白高表达对照切片为claudin18.2蛋白染色的平均灰度值接近参照样本最高灰度值70%对应的实体肿瘤组织切片;
32.所述claudin18.2蛋白中表达对照切片为claudin18.2蛋白染色的平均灰度值接近参照样本最高灰度值40%对应的实体肿瘤组织切片;
33.所述claudin18.2蛋白低表达对照切片为claudin18.2蛋白染色的平均灰度值接近参照样本最高灰度值10%对应的实体肿瘤组织切片;
34.所述claudin18.2蛋白阴性对照切片为参照样本中claudin18.2蛋白染色的平均灰度值最低对应的实体肿瘤组织切片;
35.其中,所述参照样本为待检测实体肿瘤组织标本库中100例以上不同病人来源的肿瘤组织切片或组织芯片。
36.更优选地,所述claudin18.2蛋白的质控、高表达、低表达、中表达和阴性对照切片均为石蜡包埋的切片,厚度均为4μm。
37.更优选地,所述claudin18.2蛋白的高表达、低表达、中表达和阴性对照切片实体肿瘤组织均来自待检测患者同一类型的肿瘤组织。
38.本发明还提供了所述评估实体肿瘤claudin18.2蛋白表达的方法在以claudin18.2蛋白为靶点的抗肿瘤药物筛选中的应用。
39.有益效果
40.本发明首次公开一种可准确评估实体肿瘤组织中claudin18.2蛋白表达的方法,通过提供不同表达水平的对照切片提高判读的可操作性和一致性,降低人工判读主观性对结果判断的影响,为实体肿瘤claudin18.2蛋白检测提供高灵敏度、高特异性和标准化的评判标准,具有操作简便、便于推广、结果可靠和可重复性高等优点,可准确评估不同患者实体肿瘤组织中claudin18.2的表达水平,并作为筛选靶向claudin18.2相关药物治疗实体肿瘤的诊断依据,指导临床相关药物的使用。
附图说明
41.为了更清楚地说明本发明中的技术方案,下面将对实施例描述中所需要的附图作简单的介绍,显而易见地,下面描述的附图仅仅是本发明的一些实施例,对于本领域普通技术人员来说,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图,其中:
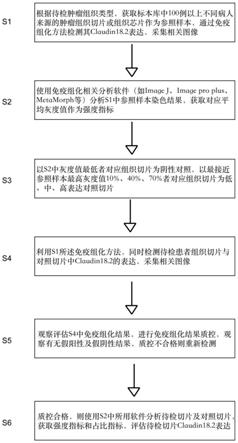
42.图1是本发明中评估实体肿瘤claudin18.2蛋白表达的方法流程示意图。
43.图2是claudin18.2蛋白表达质控切片和claudin18.2蛋白不同表达水平组织切片的免疫组化染色结果;21:claudin18.2表达质控切片染色结果;22:claudin18.2高表达对照切片染色结果;23:claudin18.2中表达对照切片染色结果;24:claudin18.2低表达对照切片染色结果;25:claudin18.2阴性对照切片染色结果。
具体实施方式
44.下面结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性的劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
45.如图1所示,本发明中评估实体肿瘤claudin18.2蛋白表达的方法,流程为:
46.步骤s1:根据待检肿瘤组织类型,获取标本库中100例以上不同病人来源的肿瘤组织切片或组织芯片作为参照样本,通过免疫组化方法(如本发明中试剂盒)检测其claudin18.2表达,采集相关图像;
47.步骤s2:使用免疫组化分析软件(如image j、image pro plus、meta morph)分析s1中参照样本染色结果,获取对应平均灰度值作为染色强度指标;
48.步骤s3:以s2中灰度值最低者对应组织切片为阴性对照,以最接近最高灰度值10%、40%、70%者对应组织切片为低、中、高表达对照切片;
49.步骤s4:利用s1所述免疫组化方法,同时检测待检测患者组织切片与对照切片中claudin18.2的表达,采集相关图像;
50.步骤s5:观察评估s4中免疫组化结果,进行免疫组化结果质控,观察有无假阳性和假阴性结果,质控不合格则重新检测;
51.步骤s6:若s5质控合格,则使用s2中软件分析待检测切片和对照切片染色结果,获取平均灰度值及和阳性细胞占比,待检测切片平均灰度值小于低、中、高表达对照切片以及大于高表达对照切片的,表达强度分别评定为0、1 、2 、3 ;结合占比指标,综合评估待检测切片的claudin18.2表达。
52.本发明的具体方案中,claudin18.2单克隆抗体能够特异性结合claudin18.2抗原分子。
53.本发明具体的方案中,待检测样本为实体肿瘤组织,如实体肿瘤细胞。
54.以下实施例中采用免疫组化染色方法检测实体肿瘤组织中claudin18.2表达,该方法涉及以下试剂:claudin18.2单克隆抗体、hrp标记的igg二抗、pbs缓冲液、抗原修复液、3%过氧化氢溶液、山羊血清封闭液、dab浓缩液、dab缓冲液以及苏木素染液;具体过程包括脱蜡、抗原修复、内源性过氧化物酶失活、封闭、一抗孵育、二抗孵育、dab显色、复染、脱水及封片、镜检评估。
55.以下实施例中检测实体肿瘤组织中claudin18.2表达的对照切片包括:
56.1)claudin18.2表达质控对照切片设有人正常胃粘膜上皮组织切片;
57.2)claudin18.2高表达对照切片为参照样本中经免疫组化分析软件(如image j、image pro plus、meta morph等)分析,claudin18.2染色平均灰度值最接近参照样本最高灰度值70%者对应的实体肿瘤组织切片;
58.3)claudin18.2中表达对照切片为参照样本中经免疫组化分析软件分析,claudin18.2染色平均灰度值最接近参照样本最高灰度值40%者对应的实体肿瘤组织切片;
59.4)claudin18.2低表达对照切片为参照样本中经免疫组化分析软件分析,claudin18.2染色平均灰度值最接近参照样本最高灰度值10%者对应的实体肿瘤组织切片;
60.5)claudin18.2阴性对照切片为参照样本中经免疫组化分析软件分析,claudin18.2染色平均灰度值最低者对应的实体肿瘤组织切片;
61.作为一个优选例,检测实体肿瘤claudin18.2表达的对照切片中,除claudin18.2表达质控切片外的实体肿瘤切片均来自待检测患者同一类型的肿瘤组织。
62.作为一个优选例,检测实体肿瘤claudin18.2表达的对照切片均为石蜡包埋的切片。
63.作为一个优选例,检测实体肿瘤claudin18.2表达的对照切片厚度均为4μm。
64.以下实施例中,通过比对对照切片染色结果对免疫组化结果进行质控并准确判断实体肿瘤中claudin18.2表达水平的方法,步骤为:
65.1)取出预先准备好的对照切片,与待检测切片一同进行免疫组化染色,镜下观察、机器采集图像并使用软件进行分析评估;
66.2)若claudin18.2表达质控切片及阴性对照切片染色无明显假阳性、假阴性结果,则进行下一步的分析评估;
67.3)使用免疫组化分析软件分别获取待检测切片与对照切片claudin18.2染色的平
均灰度值作为强度指标,阳性细胞比例作为占比指标。
68.其中,待检测切片的染色强度以对照切片的平均灰度值为判定标准,即:
69.1)0:待检测切片平均灰度值<低表达对照切片平均灰度值;
70.2)1 :低表达对照切片平均灰度值≤待检测切片平均灰度值<中表达对照切片平均灰度值;
71.3)2 :中表达对照切片平均灰度值≤待检测切片平均灰度值<高表达对照切片平均灰度值;
72.4)3 :待检测切片平均灰度值≥高表达对照切片平均灰度值;
73.同时,使用image j获取待检测切片阳性细胞占比值,综合待检测切片的强度指标和占比指标进行claudin18.2表达结果判定。标准即:
74.若待检肿瘤细胞膜染色强度≥2 且阳性细胞占比≥40%即认为claudin18.2阳性;
75.若待检肿瘤细胞膜染色强度<2 或阳性细胞占比<40%即认为claudin18.2阴性。
76.实施例1
77.claudin18.2不同表达水平实体肿瘤组织的选择及对照切片的制备,步骤如下:
78.检测实体肿瘤claudin18.2表达的对照切片需要从已有的实体肿瘤组织样本中选择。获取样本库中100例以上不同病人来源的实体肿瘤组织切片或组织芯片,使用免疫组织化学染色方法检测claudin18.2表达,具体如下:
79.1)石蜡切片脱蜡:将实体肿瘤组织切片置于烘片机上,65℃烘片30min后,置于新鲜二甲苯中浸泡5min,两次;依次浸泡于100%、95%、75%乙醇中各5min;用双蒸水浸泡5min,pbs清洗5min,3次,得到脱蜡切片。
80.2)抗原修复:向耐高温金属容器中注入抗原修复液,放入上述脱蜡切片,保证切片中组织完全浸没,而后放置于高压锅中,97℃保持25min,然后取出,室温下冷却20min,双蒸水清洗5min,3遍。
81.3)内源性过氧化物酶失活:向修复后切片上滴加3%过氧化氢溶液100
–
200ul,覆盖切片上组织,10min后用pbs清洗5min,3遍;
82.4)封闭:向步骤3中所得切片滴加封闭用山羊血清100
–
200ul,常温封闭15min。
83.5)一抗孵育:将步骤4中所得切片甩去封闭液,不清洗,直接滴加100
–
200ul稀释后的鼠抗人claudin18.2单克隆抗体,室温湿盒孵育1h或4℃过夜,而后pbs清洗5min,3遍。
84.6)二抗孵育:向步骤5中所得切片上滴加100
–
200ul hrp标记的山羊抗鼠igg二抗,覆盖切片上组织,室温湿盒孵育1h,而后甩去切片上液体,置于pbs中清洗5min,3遍。
85.7)dab显色:将dab溶液与pbs缓冲液以1:50的比例配置成dab显色液,将新鲜的dab显色液滴加在二抗孵育后的切片上,室温静置10min,而后甩去dab显色液,pbs清洗5min,3遍。
86.8)复染:向步骤7中所得切片滴加苏木素复染液,1min30s后用自来水冲洗5min返蓝。
87.9)脱水及封片:将切片依次浸泡于75%、95%、100%乙醇及二甲苯中,各浸泡5min,晾干后滴加中性树胶一滴,将盖玻片置于组织上,得到检测后切片,显微镜下观察。
88.10)结果判读及对照切片制备:claudin18.2是一种膜蛋白,通常表达于实体肿瘤
细胞表面,根据切片上实体肿瘤细胞的染色强度,可将其分为4级:
89.0,无染色,表现为无棕色着色;
90.1 ,低表达,表现为淡黄色;
91.2 ,中表达,表现为棕黄色;
92.3 ,高表达,表现为棕褐色。
93.依据上述标准,使用免疫组化分析软件如image j进行评估,以灰度值最低者对应组织切片为阴性对照,以最接近最高灰度值的10%、40%、70%者对应的组织切片为低、中、高表达对照切片。
94.11)claudin18.2表达质控对照切片制备:根据既往研究结果和预实验结果可知,claudin18.2在人正常胃粘膜上皮中表达,本发明所采用的claudin18.2表达质控切片为人正常胃粘膜上皮组织切片。
95.实施例2
96.待检测标本中claudin18.2表达的判定,具体如下:
97.制备好待检测实体肿瘤组织切片后,取出实施例1中所制备的对照切片,使用实施例1中的免疫组化检测方法同时检测待检测切片与对照切片,并采集染色结果图像,如图2所示。如果claudin18.2表达质控对照切片染色结果无假阳性及假阴性结果,则使用免疫组化分析软件image j评估待检测片与对照切片染色结果,获取平均灰度值与阳性细胞占比。
98.其中,待检测切片claudin18.2染色强度判断标准为:
99.1)0:待检测切片平均灰度值<低表达对照切片平均灰度值;
100.2)1 :低表达对照切片平均灰度值≤待检测切片平均灰度值<中表达对照切片平均灰度值;
101.3)2 :中表达对照切片平均灰度值≤待检测切片平均灰度值<高表达对照切片平均灰度值;
102.4)3 :待检测切片平均灰度值≥高表达对照切片平均灰度值;
103.同时,使用image j获取待检测切片阳性细胞占比值,综合待检测切片的强度指标和占比指标进行claudin18.2表达结果判定。结果判定标准:
104.实体肿瘤细胞膜染色强度≥2 且阳性细胞占比≥40%即认为claudin18.2阳性;
105.实体肿瘤细胞膜染色强度<2 或阳性细胞占比<40%即认为claudin18.2阴性。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。