基于上转发光免疫层析技术的crp和saa的联合定量检测方法
技术领域
1.本发明涉及免疫技术诊断领域,具体涉及基于上转发光免疫层析技术的crp和saa的联合定量检测方法。
背景技术:
2.感染性疾病检测标志物在感染引起的炎症反应早期已有不同程度的升高,对判断感染及其类型具有重要的作用,这些检测标志物包括c
‑
反应蛋白(c
‑
reactive protein,crp)、血清淀粉样蛋白a(serum amyloid aprotein,saa)、降钙素原(procalcitonin,pct)等。crp是由肝细胞合成的一种急性时相反应蛋白,任何侵袭性感染或组织损伤等原因引起的炎症发生后的6~8小时内都会引起血清中的浓度明显升高,24~48小时达到顶峰,升高幅度与感染程度呈正相关,被誉为炎症标志物;crp的半衰期为19小时,病毒感染时升高不明显,正常值为0~10mg/l。saa是一种非特异性急性时相反应蛋白,由104个氨基酸组成,在多种病毒感染急性期(数小时内)都有显著的升高,如流感病毒、呼吸道合胞病毒等。健康人群大多处于3mg/l以下,96%小于10mg/l;浓度为10~100mg/l时提示病毒感染可能性大,100~500mg/l提示细菌感染急性期可能性大,≥500mg/l则提示病毒感染(重症)或细菌感染。对感染性疾病标志物的联合检测,能够提高准确性和特异性,从而实现及时精准诊断。
3.多重检测能够同时分析一个样本中的多个指标从而提高准确性和判断是否存在多种感染,能够有效的节约样本量从而减轻病人的痛苦,并能提高检测效率。通过集成化的酶联免疫分析平台实现多重检测,成本较高且较耗时,主要应用于医院的检验科。多重免疫poct检测方法主要分别基于纸层析、芯片、磁珠、微流控和免疫层析等方法。其中免疫层析是目前单靶标最常用的poct方法,因此多重免疫层析方法将会是最实用的poct方法。
4.目前免疫层析多重检测主要通过基于单靶标试纸组合或在分析膜上喷多条检测带等方法实现。(1)基于单靶标试纸组合的多重免疫层析检测,主要是将多个单靶标以横向或纵向排列集合。其原理是将多个单靶标试纸的样品垫联合共用一个加样孔,样品加入后会分配给各个项目,其缺点是因各个试纸成分不同带来阻力不同而使得样品很难被均匀分配。(2)在分析膜上喷多个条带实现多重检测,是在分析膜上分布多个前后平行的检测带实现同时检测多个项目。基于多条带的试纸,因前方条带完全挡住了层析的液体,后方条带的反应容易受到前方的干扰,这使得利用多条带实现双靶标检测较容易,但是四个或更多条带排布于同一试纸条上时则很难成功制备,即三靶标或更多靶标检测很难被实现。
5.稀土纳米上转发光颗粒(ucp颗粒)具有独特的发光特性,能够实现高灵敏和零背景检测,并具有高稳定性和安全性等特性。将ucp颗粒作为芯片的生物标记物,将在多重检测中具有广阔的应用前景。因此,研制一种基于上转发光技术的横向芯片,并用于感染性疾病标志物saa和crp的检测,具有重要的临床应用价值。
技术实现要素:
6.本发明所要解决的技术问题是如何基于上转发光免疫层析技术准确定量检测c
‑
反应蛋白和/或血清淀粉样蛋白a。
7.为了解决上述技术问题,本发明首先提供了检测a蛋白和/或b蛋白的免疫层析芯片。所述免疫层析芯片包含结合垫和分析膜。
8.上文所述结合垫上可含有被生物标记物标记的抗a抗体1、抗b抗体1和质控物。
9.上文所述分析膜上可含有a检测点、b检测点和质控检测点。所述a检测点上可固定有抗a抗体2,所述b检测点上可固定有抗b抗体2。所述质控检测点上可固定有抗质控物的抗体。所述抗a抗体1与所述抗a抗体2可为不同或相同的抗a抗体。所述抗b抗体1与所述抗b抗体2可为不同或相同的抗b抗体。所述a检测点、所述b检测点和所述质控检测点这三个点的中心的连线是一条直线,该连线可与待测样品前进的方向(层析方向)垂直。
10.上文所述免疫层析芯片中,所述质控物可为已知蛋白。所述分析膜上的a检测点、b检测点和质控检测点可为横向排布的。所述横向为与待测样品前进的方向(层析方向)垂直。
11.上文所述免疫层析芯片中,所述a检测点、b检测点和质控检测点均可为圆形检测点。所述圆形检测点的直径可为1mm。
12.上文所述a蛋白可为c
‑
反应蛋白(crp),所述b蛋白可为血清淀粉样蛋白a(saa)。所述a蛋白还可为其他蛋白,如saa或pct等。所述b蛋白还可为其他蛋白,如crp或pct等。
13.上文所述生物标记物可为稀土纳米上转发光颗粒。
14.上文所述免疫层析芯片中,所述抗体为单克隆抗体。
15.上文所述分析膜上的所述a检测点、所述b检测点和所述质控检测点的制备过程可包括在所述a检测点点样所述抗a抗体2、在所述b检测点点样所述抗b抗体2、在所述质控检测点点样所述抗质控物的抗体的过程。所述点样体积可为40nl。
16.上文所述质控物可为羊igg。所述抗质控物的抗体可为兔抗羊igg的抗体。
17.上文所述免疫层析芯片还可包含样品垫、吸水垫和粘性底衬。
18.上文所述免疫层析芯片的层析方向可为由所述样品垫到所述结合垫,由所述结合垫到所述分析膜,由所述分析膜到所述吸水垫。
19.所述样品垫和结合垫可部分重叠,所述重叠部分为样品垫在上方。所述分析膜与结合垫及吸水垫可有重叠,所述重叠部分为分析膜位于结合垫和吸水垫的下方。
20.所述粘性底衬可为单面涂有压力敏感胶的硬体材质。所述粘性底衬可为pvc板。
21.所述样品垫为添加液体样品的位置。所述样品垫可为具有较大床体积且微观结构均匀的物质。所述样品垫可为玻璃纤维或聚醋膜。
22.所述为分析膜可为检测所述生物标记物的信号的位置。所述分析膜可为微观结构均匀的物质。所述分析膜可为硝酸纤维素膜或尼龙膜。
23.所述吸水垫可为具有较大床体积的物质。所述吸水垫可为吸水纸或纤维素膜。
24.上文所述免疫层析芯片中,所述样品垫可为玻璃纤维。所述分析膜可为硝酸纤维素膜。所述吸水垫可为吸水纸。
25.上文所述的免疫层析芯片中,可通过检测所述免疫层析芯片上的生物标记物的信号值,确定a和/或b浓度:包括检测所述分析膜上所述a检测点、b检测点和质控检测点的生物标记物的信号值得到检测峰,通过计算所述a检测点与所述质控检测点的检测峰面积的比值确定a的浓度,通过计算所述b检测点与所述质控检测点的检测峰面积的比值确定b的
浓度。所述a可为c
‑
反应蛋白(crp)。所述可b为血清淀粉样蛋白a(saa)。所述质控物可为羊igg。
26.为了解决上述技术问题,本发明还提供了上文所述的免疫层析芯片在制备检测crp和/或saa产品(试纸)中的应用。
27.使用上文所述的免疫层析芯片制备的检测crp和/或saa的产品(试纸)也属于本发明的保护范围。
28.上文所述产品(试纸)对所述crp的浓度检测范围可为0.5~150mg/l。上文所述产品(试纸)对saa的浓度检测范围可为2.5~200mg/l。
29.本发明提供一种基于上转发光法的crp/saa联合定量检测的横向免疫层析芯片,该芯片具有体积小、快速、准确定量、背景干扰较小、各检测项目间相互干扰较少等优点。该芯片克服了纵向芯片中分析膜上靠样品垫较远的检测项目的免疫反应易受前方反应干扰、不能精确定量等缺点,提供了基于上转发光的crp/saa定量检测试剂,可对crp、saa进行快速、准确、定量检测。
30.本发明的有益效果在于:
31.本发明所制备的检测crp和/或saa的横向点阵免疫层析芯片,将现有技术中免疫层析分析膜上的检测条带改为横向点阵,可以克服纵向条带式多重检测试纸条上前面条带对后面条带的影响,使得每个检测项目具有各自的通道,最大限度的减少各项目之间的相互干扰。同时,本专利基于稀土纳米上转发光颗粒(ucp颗粒)的新型标记物制备芯片的结合垫,ucp颗粒具有独特的发光特性,能够实现高灵敏和零背景检测,并具有高稳定性和安全性等特性。将ucp颗粒作为芯片的生物标记物,将在多重检测中具有广阔的应用前景。
附图说明
32.图1为芯片的结构组成及反应示意图。(a)芯片的结构组成。(b)阴性和阳性反应的结果示意图。c为质控点,t1为crp检测点,t2和t3为saa检测点。
具体实施方式
33.下面结合具体实施方式对本发明进行进一步的详细描述,给出的实施例仅为了阐明本发明,而不是为了限制本发明的范围。以下提供的实施例可作为本技术领域普通技术人员进行进一步改进的指南,并不以任何方式构成对本发明的限制。
34.下述实施例中的实验方法,如无特殊说明,均为常规方法,按照本领域内的文献所描述的技术或条件或者按照产品说明书进行。下述实施例中所用的材料、试剂等,如无特殊说明,均可从商业途径得到。
35.实施例一、应用于crp和saa的上转发光免疫层析芯片的联合定量检测方法
36.1.应用于crp和saa的上转发光免疫层析芯片制备的方法
37.1.1试剂
38.a)用于免疫层析试纸条制备的ucp颗粒。
39.b)抗saa抗体(包括抗saa单抗1(杭州伊佰新生物技术有限公司,货号mxd01)和抗saa单抗2(杭州伊佰新生物技术有限公司,货号mxd06))、抗crp抗体(抗crp单抗1(厦门万泰沧海生物技术有限公司,货号1284)和抗crp单抗2(厦门万泰沧海生物技术有限公司,货号
1745)),兔抗羊igg(本实验室制备),羊igg(本实验室制备),saa标准品(杭州伊佰新生物技术有限公司,货号xd01),crp标准品(北京霍尔姆斯生物技术有限公司,货号hao12an);
40.c)其他tris
‑
hcl(包被缓冲液)、磷酸缓冲液(pb)、bsa(封闭)、冻干液(0.20mpb缓冲液,含2%bsa,3%蔗糖)、样本稀释液(0.2m pb缓冲液,1%tween20,)。
41.1.2芯片的结构组成
42.1.1.1芯片整体结构:芯片是由样品垫、结合垫、分析膜和吸水垫依次排布在粘性底衬上(图1)。样品垫和结合垫部分重叠,重叠部分样品垫在上方;分析膜与结合垫及吸水垫有重叠,分析膜位于结合垫和吸水垫的下方。
43.1.1.2结合垫:结合垫中含有抗saa抗体标记的ucp颗粒(ucp
‑
抗saa单抗1)、抗crp抗体标记的ucp颗粒(ucp
‑
抗crp单抗1)、和作为质控物的羊igg标记的ucp颗粒(ucp
‑
羊igg)。
44.1.1.3分析膜组成:分析膜上横向依次排列有抗saa单抗2、抗saa单抗2、抗质控物抗体(兔抗羊igg)、抗crp单抗2。
45.1.3应用于crp和saa的上转发光免疫层析芯片制备的方法
46.采用双抗体夹心方式建立能够对crp和/或saa进行快速定量检测的上转发光免疫层析方法(crp/saa
‑
upt
‑
lf)。
47.检测原理为:(1)阳性标准品样品:样品在加入免疫层析芯片的样品垫后,在虹吸作用下向前(由样品垫向吸水垫方向)涌动,分别经过结合垫和分析膜,阳性样品中的crp和/或saa首先与结合垫中的ucp
‑
抗saa单抗1和/或ucp
‑
抗crp单抗1相结合,形成ucp
‑
抗saa单抗1
‑
saa复合物和/或ucp
‑
抗crp单抗1
‑
crp复合物。该形成复合物和游离的ucp
‑
抗crp单抗1和/或ucp
‑
抗saa单抗1继续向前层析到达分析膜:在分析膜上的t1位置,固定在分析膜上的抗crp单抗2捕获ucp
‑
抗crp单抗1
‑
crp复合物形成固相
‑
抗crp单抗2
‑
crp
‑
抗crp单抗1
‑
ucp新复合物;在分析膜上的t2和t3位置,固定在分析膜上的抗saa单抗2捕获ucp
‑
抗saa单抗1
‑
saa复合物形成固相
‑
抗saa单抗2
‑
saa
‑
抗saa单抗1
‑
ucp新复合物;质控位置c捕获游离质控物ucp
‑
羊igg形成固相兔抗羊igg
‑
羊igg
‑
ucp。(2)阴性样品:样品和ucp
‑
抗saa单抗1、ucp
‑
抗crp单抗1以及ucp
‑
羊igg一起进入分析膜,只在质控带上形成固相兔抗羊igg
‑
羊igg
‑
ucp。因此,在此免疫层析芯片检测模式中,阳性样品在检测点与质控点上都有特异性的信号峰出现,而阴性样品只在质控点上有特异的信号峰。
48.1.3.1结合垫的制备
49.将表面修饰过的ucp颗粒(北京开景基因技术有限公司)使用0.02mpb重悬至1mg/ml,配置3支于1ml离心管并放置于恒温振荡器上振荡,在3支离心管内分别加入抗saa单抗1、抗crp单抗1和作为质控物的羊igg,持续搅拌1h;分别加入bsa封闭10min,4℃、12000rpm、30min离心,分别获得ucp
‑
抗saa单抗1、ucp
‑
抗crp单抗1和ucp
‑
羊igg这三种ucp单抗复合物。将这三种ucp单抗复合物分别用冻干液重悬后混匀浇于玻璃纤维(购置德国默克公司默克密理博公司,货号gfcp203000)上,于
‑
80℃冰箱预冻2h后再放置冻干机内冻干3h,制备成结合垫,置于干燥柜内保存。
50.1.3.2试纸组装与切割
51.将吸水纸剪裁为3cm
×
20cm,作为吸水垫。将玻璃纤维裁剪为宽度为1.5cm
×
20cm的细长条作为样品垫。将样品垫、结合垫、硝酸纤维素膜(分析膜,简称nc膜,购自德国默克
公司默克密理博公司,货号hf09002s25)、吸水垫依次粘贴在粘性底衬(上海金标生物科技有限公司,sm31
‑
40)上,用高速数控斩切机斩切为10mm宽的试纸条,并装配于塑料卡壳中制备为检测试纸条。
52.1.3.3分析膜上点样得到用于crp和saa的上转发光免疫层析芯片
53.点样样品分别为抗crp单抗2、兔抗羊igg(抗质控物抗体)和抗saa单抗2。将1.3.2得到的10mm宽的试纸条置于点样仪上,在试纸条上硝酸纤维素膜中间位置附近横向(与层析方向垂直)点样,点样方法为横向(与层析方向垂直)点喷四个相互分离的圆点。抗crp单抗2、兔抗羊igg和抗saa单抗2依次各点样40nl,分别得到检测点1(t1)、质控点(c)、检测点2(t2)和检测点3(t3),即t1(样品为抗crp单抗2)为crp检测点,t2和t3(样品均为抗saa单抗2)为saa检测点,c(样品为兔抗羊igg)为质控点。检测点1(t1)、质控点(c)、检测点2(t2)和检测点3(t3)这四个点的中心的连线是一条直线,该连线与待测样品前进的方向(层析方向)垂直。这四个点均为直径为1mm的圆形。
54.点样后将10mm宽的试纸条置于电热恒温鼓风干燥箱内37℃干燥1h即得到用于crp和saa的上转发光免疫层析芯片。
55.2.利用芯片检测crp和saa及结果分析
56.2.1检测方法
57.将saa标准品、crp标准品使用0.2m pb稀释,其中crp样品分别稀释成crp含量为0.5、1、4、10、40、100、150mg/l七个浓度梯度的样品;saa样品分别稀释成saa含量为2.5、5、12.5、50、100、200mg/l六个浓度梯度的样品。将上述稀释得到的不同浓度梯度的样品与样本稀释液(0.2m pb,1%tween20)以体积比为1:99的比例混合,混匀后得到待检测样品。取250μl待检测样品加入至用于crp和saa联合检测的上转发光免疫层析芯片的样品垫上,静置15min。使用upt生物传感器(热景(廊坊)生物技术有限公司,型号为upt芯片传感器)扫描,分析膜上nc膜的检测点(t1、t2和t3)和质控点(c)上的信号被扫描出现检测峰,将各检测点的峰面积与质控点峰面积比值(t/c值)作为检测结果。t1/c为crp检测结果,t2/c和t3/c分别为saa检测结果。
58.2.2crp检测结果
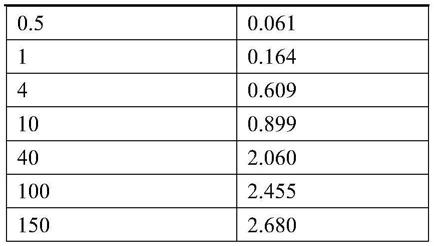
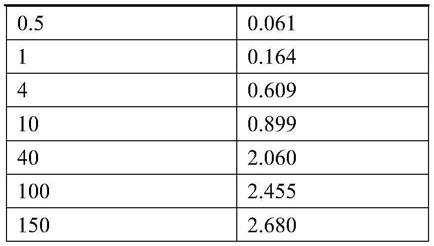
59.本发明制备的检测芯片对crp的检测范围为0.5~150mg/l。步骤2.1中crp七个浓度梯度样品使用本发明制备的检测芯片得到的t/c值、t/c值对应的crp浓度(mg/l)见表1,通过检测待测样品的t/c值,可根据t/c值确定crp的浓度范围。
60.表1.crp浓度与其对应检测得到的t/c值
61.[0062][0063]
2.3saa检测结果
[0064]
本发明制备的检测芯片对saa的检测范围为2.5~200mg/l。步骤2.1中saa六个浓度梯度样品使用本发明制备的检测芯片得到的t/c值、t/c值对应的saa浓度(mg/l)见表2,通过检测待测样品的t/c值,可根据t/c值确定saa的浓度范围。
[0065]
表2.saa浓度与其对应检测得到的t/c值
[0066]
saa浓度(mg/l)t/c值00.1952.50.29350.66312.50.842501.2671001.6522001.805
[0067]
实施例二、芯片分析膜点样体积的筛选
[0068]
在实施例一制备得到的应用于crp和saa的上转发光免疫层析芯片的分析膜上上t1、t3和t4点样位置都点样不同体积抗saa单抗2,测试芯片分析膜上不同检测点的点样体积对saa检测结果的影响。
[0069]
具体为将芯片分析膜上抗saa单抗2点样体积分别设置为t1检测点40nl、t3检测点50nl和t4检测点60nl,芯片样品垫分别加入0、2、4、40、200、400mg/l六个saa标准品稀释后得到的saa的梯度浓度样品进行免疫层析检测。同时在芯片分析膜上包含c质控点(点样体积40nl),将t1/c、t3/c和t4/c值作为检测值。将包含不同浓度梯度的saa标准品定义为阳性样本p,将用于稀释标准品的样本稀释液(0.2m pb,1%tween20)定义为阴性样本n。将阳性样本p的检测值和阴性样本n的检测值的差值,再和阴性样本n的检测值做比值,即(p
‑
n)/n,作为判断各点样体积效果的标准。结果发现40nl结果最好(表3)。所以选用40nl作为芯片的点样体积。
[0070]
表3.不同检测点的点样体积对应的检测t/c值和saa浓度
[0071][0072]
备注:na为不适用。
[0073]
以上对本发明进行了详述。对于本领域技术人员来说,在不脱离本发明的宗旨和范围,以及无需进行不必要的实验情况下,可在等同参数、浓度和条件下,在较宽范围内实施本发明。虽然本发明给出了特殊的实施例,应该理解为,可以对本发明作进一步的改进。总之,按本发明的原理,本技术欲包括任何变更、用途或对本发明的改进,包括脱离了本技术中已公开范围,而用本领域已知的常规技术进行的改变。按以下附带的权利要求的范围,可以进行一些基本特征的应用。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。