1.本发明属于医药领域,涉及肉苁蓉提取物的一种新用途,具体涉及肉苁蓉提取物及松果菊苷在制备具有胃粘膜保护作用的药物中的应用。
背景技术:
2.胃溃疡是全球范围内最常见的慢性胃肠道功能紊乱性疾病之一,发病率高达10%。胃溃疡是一种多因素、多途径参与的多发性疾病,其主要临床表现有长期发作的周期性,节律性上腹部疼痛,并伴有恶心、呕吐、反胃、嗳气、泛酸等一系列胃肠道症状。
3.另外,过量饮酒也会导致胃粘膜损伤、胃溃疡。酒中的主要成分乙醇可溶于脂质进入胃壁,导致胃粘膜损伤、通透性增加,出现胃粘膜充血、胃粘膜糜烂出血等,严重者会导致胃穿孔、消化道大出血等,严重威胁患者的生命安全。
4.胃溃疡、胃粘膜损伤的治疗以药物为主,包括化学药物和中药,但治疗难度大。化学药物主要有甲硝唑、西咪替丁、硫酸铝、阿莫西林、奥美拉唑等,中药则多为复方制剂。其中,相对于化学药,中药复方治疗胃溃疡有更高的安全性。对中药天然产物进行提取、分离,用于酒精性胃损伤的治疗,是开发护胃、抗胃溃疡药物和保健品的重要方法。但是,目前天然产物在治疗胃溃疡、胃粘膜损伤方面的疗效不够显著。因此,以中药为原料,开发对胃溃疡、胃粘膜损伤具有显著治疗效果的药物具有重要的应用价值和经济效益。
5.肉苁蓉为列当科肉苁蓉属多年寄生性药用植物,具有极高的药用价值,素有“沙漠人参”的美誉。在我国,肉苁蓉主要分布于新疆、内蒙古地区,甘肃和宁夏也有分布。我国肉苁蓉属植物有4种,分别为荒漠肉苁蓉c.deserticolay.c.ma、盐生肉苁蓉c.salsa(c.a.mey.)g.beck、管花肉苁蓉c.tubulosa(schenk)r.wight及沙苁蓉c.sinensisg.beck(屠鹏飞等,中国现代中药,2015,17(4):297-301)。其中,荒漠肉苁蓉和管花肉苁蓉为官方认可作为中药肉苁蓉的基原植物收录入《中国药典》。有研究表明,荒漠肉苁蓉的多糖提取物和苯乙醇苷均能改善酒精诱导的肝损伤模型小鼠的血清和肝脏指标的恢复,提高hepg2细胞的存活,减轻模型动物肝组织中脂肪微泡和坏死细胞,可见荒漠肉苁蓉的多糖提取物和苯乙醇苷对乙醇诱导的慢性肝损伤有显著的保护作用。还有研究表明,富含多糖的荒漠肉苁蓉提取物能够通过激活免疫系统,减少小鼠的炎性粘膜增生和肠内幽门螺杆菌感染,具有预防结直肠癌、肠道炎症的作用(参见,侯蕾等,“肉苁蓉研究进展与产业化现状”,山东农业科学,第52卷第12期,2020年,第133-140页)。
6.松果菊苷(echinacoside,ech)是从肉苁蓉中提取的天然化合物,性状为白色结晶粉末。松果菊苷具有很多生物学效应,如神经保护作用、肝脏的保护作用、抗肿瘤、抗凋亡、抗衰老、免疫调节和促进生殖的作用,同时还具有降糖、降脂、促进骨形成以及抗肺动脉高压和预防动脉粥样硬化的作用。此前,有研究表明,松果菊苷能够缓解酒精诱导的氧化应激和肝硬化(参见,zhitao,etal.“echinacosideameliorates alcohol-inducedoxidativestressandhepaticsteatosisbyaffecting srebp1c/fasnpathwayviapparα”,
foodandchemical toxicology,vol148,2021,111956)。另外,还有研究报道,富含松果菊苷的管花肉苁蓉提取物能够减轻葡聚糖硫酸钠诱导的小鼠结肠炎(参见,yaminjia,etal.“ameliorationof dextransulphatesodium-inducedcolitisinmiceby echinacoside-enrichedextractofcistanchetubulosa”,phytotherapyresearch,vol28,2014,110-119)。肉苁蓉总苷和松果菊苷还能够用于预防和治疗酒精性肝损伤伴随肠道损伤(参见cn113425764a)。
7.从上述对现有技术的综述可知,目前尚无对肉苁蓉提取物以及松果菊苷对胃粘膜保护作用方面的研究报道,本发明刚好填补了这一技术空白。
技术实现要素:
8.本发明的目的是为了解决现有技术的不足,实现采用现代药物研究方法对天然产物进行开发利用,结合大量药效学实验筛选,提供了肉苁蓉提取物及松果菊苷在制备具有胃粘膜保护作用的药物中的应用。
9.为达到本发明的目的,本发明采用了如下技术方案:
10.在第一个方面中,本发明提供了肉苁蓉提取物在制备具有胃粘膜保护作用的药物中的应用。
11.在第一个方面中,本发明提供了肉苁蓉提取物在制备预防或治疗胃粘膜损伤或胃溃疡的药物中的应用。
12.作为可选的方式,在上述应用中,所述肉苁蓉提取物是从荒漠肉苁蓉(cistanchedeserticola)或管花肉苁蓉(cistanche tubulosa)中提取得到的。
13.作为可选的方式,在上述应用中,所述肉苁蓉提取物是从管花肉苁蓉或荒漠肉苁蓉中提取得到的管花肉苁蓉总苷或荒漠肉苁蓉总苷、管花肉苁蓉多糖或荒漠肉苁蓉多糖、管花肉苁蓉寡糖或荒漠肉苁蓉寡糖。
14.优选地,所述肉苁蓉总苷、所述肉苁蓉多糖或所述肉苁蓉寡糖的制备方法包括以下步骤:
15.将管花肉苁蓉或荒漠肉苁蓉饮片粉碎成粗粉,加6-10倍量水加热回流提取三次,每次1.5-3h,合并滤液,减压浓缩至相对密度1.15,50℃测定,加85%-95%乙醇至含醇量达50-70%,低温沉淀10-15小时,滤过,沉淀即为肉苁蓉总多糖部位;滤液减压浓缩至相对密度1.15,50℃测定,再经大孔树脂纯化,依次用水和不同浓度的乙醇洗脱,收集水洗脱液,减压浓缩至稠膏,即得肉苁蓉总寡糖;再用30-50%乙醇洗脱,收集洗脱液,减压浓缩,干燥,即得肉苁蓉总苷。
16.更优选地,所述肉苁蓉总苷、所述肉苁蓉多糖或所述肉苁蓉寡糖的制备方法包括以下步骤:
17.将管花肉苁蓉或荒漠肉苁蓉饮片粉碎成粗粉,加8倍量水加热回流提取三次,每次2h,合并滤液,减压浓缩至相对密度1.15,50℃测定,加95%乙醇至含醇量达60%,低温沉淀12小时,滤过,沉淀即为肉苁蓉总多糖部位;滤液减压浓缩至相对密度1.15,50℃测定,再经大孔树脂纯化,依次用水和不同浓度的乙醇洗脱,收集水洗脱液,减压浓缩至稠膏,即得肉苁蓉总寡糖;再用40%乙醇洗脱,收集洗脱液,减压浓缩,干燥,即得肉苁蓉总苷。
18.作为可选的方式,在上述应用中,所述肉苁蓉提取物是天然产物单体。
19.优选地,所述天然产物单体是从肉苁蓉总苷中制备得到的。
20.优选地,所述天然产物单体选自以下一种或多种:红景天苷、毛蕊花糖苷、2
’‑
乙酰基毛蕊花糖苷、管花苷a、松果菊苷或异毛蕊花糖苷。
21.优选地,所述天然产物单体的制备方法包括以下步骤:
22.取肉苁蓉总苷,加6-10倍量水溶解,经ods柱层析,洗脱液为甲醇-水,梯度洗脱得16个流份fr.i-xvi。fr.iv经sephadexlh-20柱层析洗脱,洗脱液为甲醇-水,得到10个主要流分fr.1-fr.10,fr.5经hplc半制备分离,洗脱液为甲醇-水,得到化合物松果菊苷和管花苷a。fr.vii经sephadexlh-20柱层析洗脱,洗脱液为甲醇-水,得到12个主要流分fr.1-fr.12,fr.8经hplc制备分离,洗脱液为水-甲醇-乙腈,得化合物毛蕊花糖苷和2
’‑
乙酰基毛蕊花糖苷;fr.10经hplc制备分离,洗脱液为甲醇-水,得到化合物异毛蕊花糖苷。fr.viii经sephadexlh-20柱层析洗脱,洗脱液为甲醇-水,得到8个主要流分fr.1-fr.8,fr.3经硅胶ptlc,硅胶h,展开剂氯仿-甲醇,得化合物红景天苷。
23.更优选地,所述天然产物单体的制备方法包括以下步骤:
24.取肉苁蓉总苷,加8倍量水溶解,经ods柱层析(100-120目,甲醇-水,25:75-75:25)梯度洗脱得16个流份(fr.i-xvi)。fr.iv经sephadexlh-20柱层析(甲醇-水,50:50)洗脱,得到10个主要流分fr.1-fr.10,fr.5经hplc半制备分离(甲醇-水,30:70)得到化合物松果菊苷和管花苷a。fr.vii经sephadexlh-20柱层析(甲醇-水,50:50)洗脱,得到12个主要流分fr.1-fr.12,fr.8经hplc制备分离(水-甲醇-乙腈,62:29:9)得化合物毛蕊花糖苷和2
’‑
乙酰基毛蕊花糖苷;fr.10经hplc制备分离(甲醇-水,40:60)得到化合物异毛蕊花糖苷。fr.viii经sephadexlh-20柱层析(甲醇-水,50:50)洗脱,得到8个主要流分fr.1-fr.8,fr.3经硅胶ptlc(硅胶h,氯仿-甲醇,3:1)得化合物红景天苷。
25.更优选地,所述天然产物单体为松果菊苷。
26.作为可选的方式,在上述应用中,松果菊苷剂量依赖性降低ldh释放率,抑制胆汁酸诱导的自噬过度激活,剂量依赖性显著下调il-6、il-1β、tnfα的含量。
27.作为可选的方式,在上述应用中,所述药物中仅包含肉苁蓉提取物作为活性成分,另外还包含药学上可接受的载体。
28.作为可选的方式,在上述应用中,所述药物的剂型为口服剂型。
29.作为可选的方式,在上述应用中,所述口服剂型为胶囊剂、片剂、颗粒剂或口服液。
30.本发明相对于现有技术,具有以下有益效果:
31.本发明结合我国在天然产物研究方面的优势,筛选出肉苁蓉提取物及包括松果菊苷在内的多种天然产物单体在胃粘膜保护以及预防和治疗胃粘膜损伤和胃溃疡等方面的新用途。本发明具有开发成用于治疗相关适应症的药物的前景,具有重要的临床意义和商业价值。
附图说明
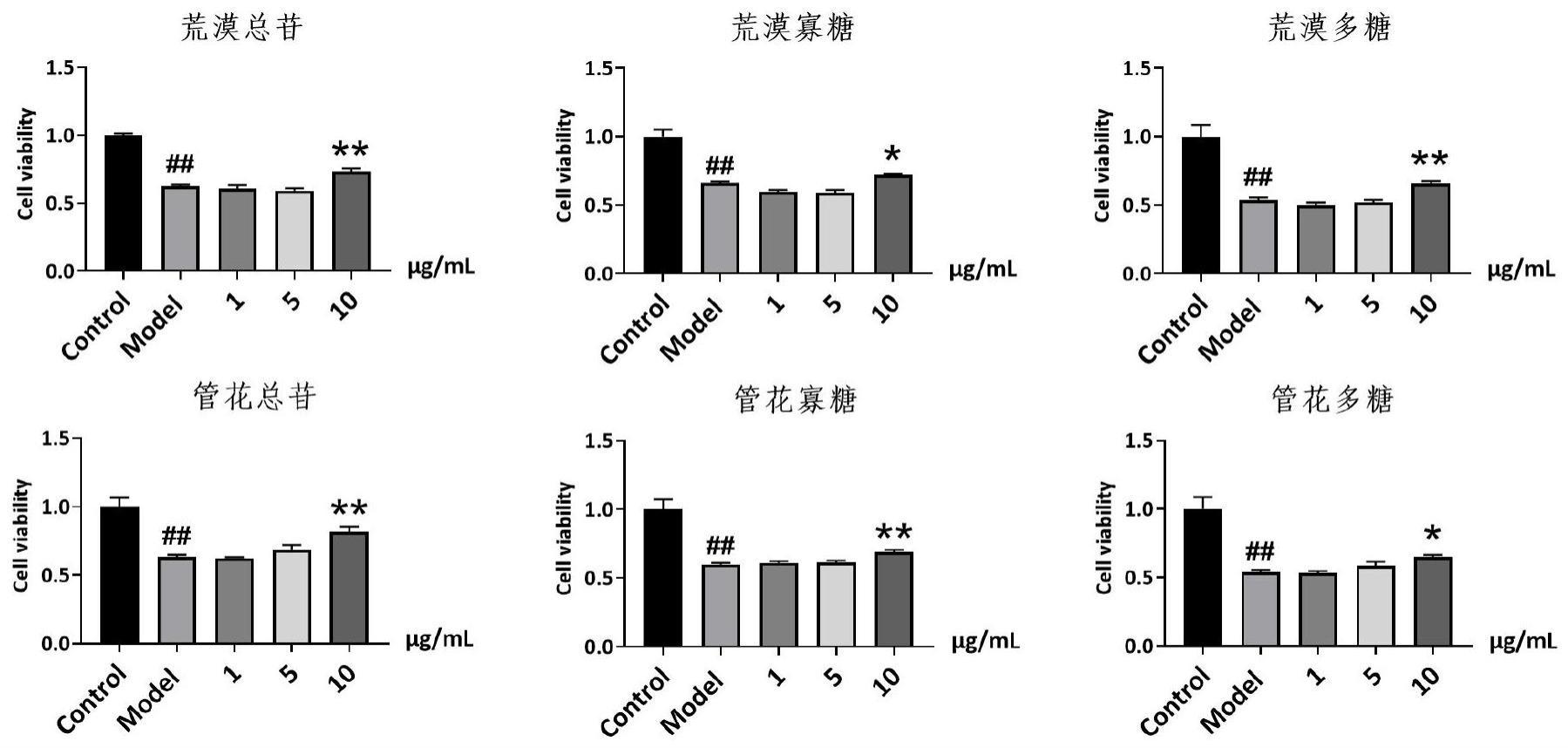
32.图1:各提取物组分在tca诱导的ges-1细胞损伤模型上的活性。采用t-test分析两组之间的差异,数据以mean
±
sem表示,n=6。相比于正常对照组,
##
p《0.01;相比于模型组,*p《0.05,**p《0.01。
33.图2:单体成分在tca诱导的ges-1细胞损伤模型上的活性。采用t-test分析两组之
间的差异,数据以mean
±
sem表示,n=6。相比于正常对照组,
##
p《0.01;相比于模型组,*p《0.05,**p《0.01,***p《0.001。
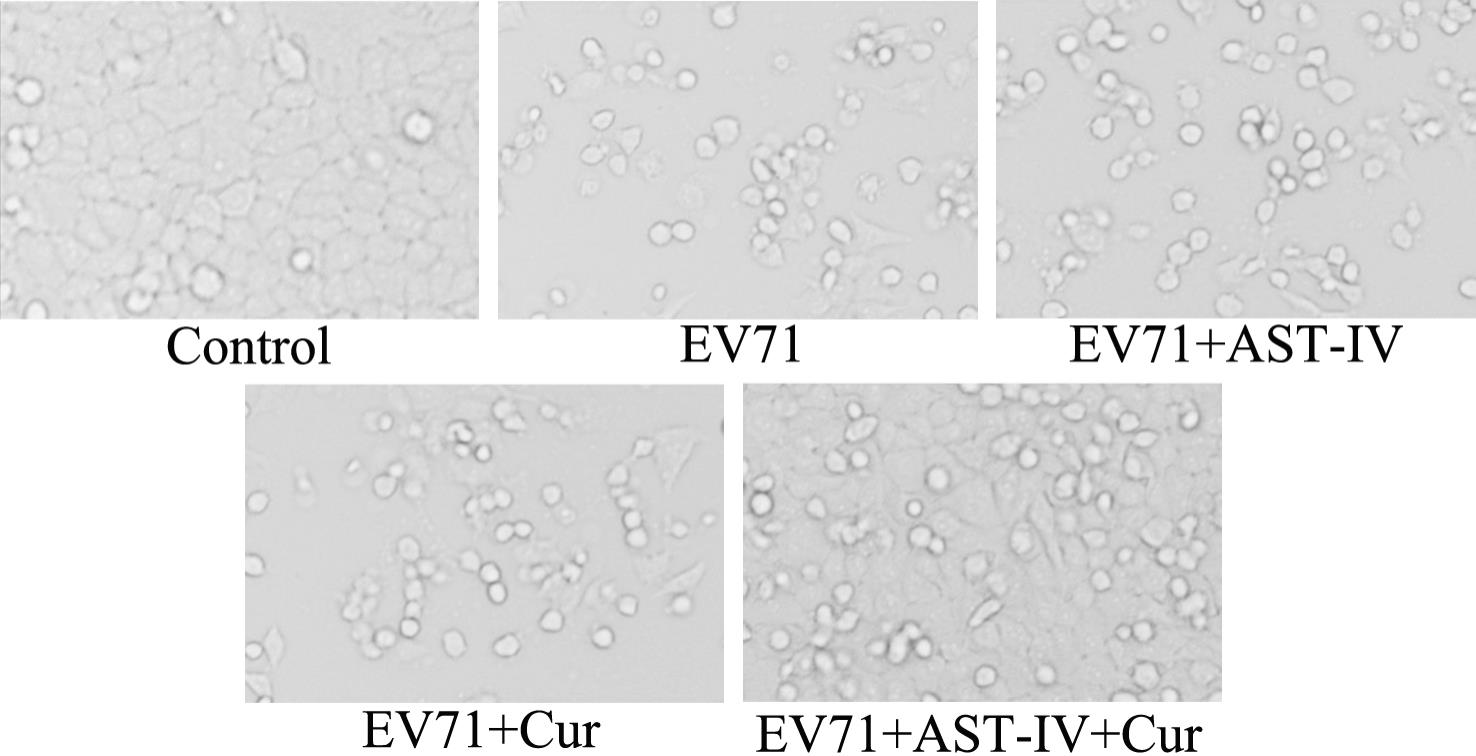
34.图3:松果菊苷改善胃粘膜损伤的体外活性筛选。其中,a为ech为对乙醇诱导的ges-1细胞存活率的影响;b为ech对胆汁酸诱导的ges-1细胞存活率的影响;c为ech对乙酰水杨酸诱导的细胞存活率的影响。ech:松果菊苷。采用t-test分析两组之间的差异,数据以mean
±
sem表示,n=6。相比于正常对照组,
##
p《0.01;相比于模型组,*p《0.05,**p《0.01。
35.图4:松果菊苷对胆汁酸诱导ges-1细胞损伤模型ldh释放率的影响。其中,ech:松果菊苷。采用t-test分析两组之间的差异,数据以mean
±
sem表示,n=6。相比于正常对照组,
##
p《0.01;相比于模型组,*p《0.05。
36.图5:松果菊苷对胆汁酸诱导ges-1细胞自噬的影响。
37.图6:松果菊苷对各组小鼠胃组织大体观的影响。其中,cg:正常对照组,sg:阳性对照硫糖铝,ech25:25mg/kg松果菊苷,ech50:50mg/kg松果菊苷。红色箭头指示为胃粘膜出血部位。
38.图7:松果菊苷对各组小鼠胃组织病理形态的的影响。其中,cg:正常对照组,sg:阳性对照硫糖铝,ech25:25mg/kg松果菊苷,ech50:50mg/kg松果菊苷。黑色箭头指示为胃粘膜细胞的坏死和紊乱。h&e染色结果(
×
200),标尺=50μm。
39.图8:松果菊苷对各组icr小鼠血浆il-1β,il-6,tnfα水平的影响。其中,a为icr小鼠血浆il-6水平;b为icr小鼠血浆il-1β水平;c为icr小鼠血浆tnfα水平。cg:正常组;mg:模型组;sg:阳性药硫糖铝组;ech25:25mg/kg松果菊苷,ech50:50mg/kg松果菊苷。采用t-test分析两组之间的差异,数据以mean
±
sem表示,n=7。相比于cg组,
#
p《0.05,
##
p《0.01;相比于mg组,*p《0.05,**p《0.01。
具体实施方式
40.下面参照具体的实施例对本发明做进一步说明。应当理解,此处所描述的具体实施例仅用于解释本发明,并不用于限定本发明的范围。
41.本发明所述药学上可接受的载体是指药物制剂领域常规的药物载体,选自填充剂、粘合剂、崩解剂、润滑剂、助悬剂、润湿剂、色素、矫味剂、溶剂、表面活性剂中的一种或几种。
42.本发明所述填充剂包括但不限于淀粉、微晶纤维素、蔗糖、糊精、乳糖、糖粉、葡萄糖等;所述润滑剂包括但不限于硬脂酸镁、硬脂酸、氯化钠、油酸钠、月桂醇硫酸钠、泊洛沙姆等;所述粘合剂包括但不限于水、乙醇、淀粉浆、糖浆、羟丙基甲基纤维素、羧甲基纤维素钠、海藻酸钠、聚乙烯吡咯烷酮等;所述崩解剂包括但不限于淀粉泡腾混合物即碳酸氢钠和枸橼酸、酒石酸、低取代羟丙基纤维素等;所述助悬剂包括但不限于多糖如金合欢胶、琼脂、藻酸、纤维素醚和羧甲基甲壳酯等;所述溶剂包括但不限于水、平衡的盐溶液等。
43.可以将所述药物制成各种固体口服制剂、液体口服制剂等。药剂学可接受的口服剂固体制剂有:普通片剂、分散片、肠溶片、颗粒剂、胶囊剂、滴丸、散剂等,口服液体制剂有口服液、乳剂等。上述各种剂型可以根据药物制剂领域的常规工艺制备而成。
44.本发明中使用的肉苁蓉提取物及包括松果菊苷在内的各种天然产物单体可以采用本发明所述的提取分离方法或文献中报道的其他生物提取方法从肉苁蓉中提取分离得
到,也可以购自市售产品。
45.在上文所述的医药用途中,对于肉苁蓉提取物以及包括松果菊苷在内的各种天然产物单体的给药时间、给药次数和给药频率等等,需要根据病情的具体诊断结果而定,这在本领域技术人员掌握的技术范围之内。
46.为了更好地理解本发明的实质,在下文具体实施方式部分用药效学实验及其结果来进一步说明肉苁蓉提取物及松果菊苷在制药领域中的新用途。
47.实施例中未注明具体技术或条件者,按照本领域内的文献所描述的技术或条件,或者按照产品说明书进行。所用试剂或仪器未注明生产厂商者,均为可通过正规渠道购买得到的常规产品。
48.下面实施例中的实验方法,如无特殊说明,均为常规方法。下述实施例中所用的试验材料,如无特殊说明,均为市售产品。
49.除非另外说明,否则本发明中涉及的百分比和份数均为重量百分比和重量份数。
50.实施例1:肉苁蓉总苷、肉苁蓉多糖和肉苁蓉寡糖的提取方法1.管花肉苁蓉或荒漠肉苁蓉各部位提取物的制备(仅为示例性方法,也可以通过其他途径获得):
51.管花肉苁蓉或荒漠肉苁蓉饮片粉碎成粗粉,加8倍量水加热回流提取三次,每次2h,合并滤液,减压浓缩至相对密度1.15(50℃测定),加95%乙醇至含醇量达60%,低温沉淀12小时,滤过,沉淀即为肉苁蓉总多糖部位;滤液减压浓缩至相对密度1.15(50℃测定),再经大孔树脂纯化,依次用水和不同浓度的乙醇洗脱,收集水洗脱液,减压浓缩至稠膏,即得肉苁蓉总寡糖;再用40%乙醇洗脱,收集洗脱液,减压浓缩,干燥,即得肉苁蓉总苷。
52.2.管花肉苁蓉或荒漠肉苁蓉各单体化合物的制备(仅为示例性方法,也可以通过其他途径获得):
53.取肉苁蓉总苷,加8倍量水溶解,经ods柱层析(100-120目,甲醇-水,25:75-75:25)梯度洗脱得16个流份(fr.i-xvi)。fr.iv经sephadexlh-20柱层析(甲醇-水,50:50)洗脱,得到10个主要流分fr.1-fr.10,fr.5经hplc半制备分离(甲醇-水,30:70)得到化合物松果菊苷和管花苷a。fr.vii经sephadexlh-20柱层析(甲醇-水,50:50)洗脱,得到12个主要流分fr.1-fr.12,fr.8经hplc制备分离(水-甲醇-乙腈,62:29:9)得化合物毛蕊花糖苷和2
’‑
乙酰基毛蕊花糖苷;fr.10经hplc制备分离(甲醇-水,40:60)得到化合物异毛蕊花糖苷。fr.viii经sephadexlh-20柱层析(甲醇-水,50:50)洗脱,得到8个主要流分fr.1-fr.8,fr.3经硅胶ptlc(硅胶h,氯仿-甲醇,3:1)得化合物红景天苷。
54.实施例2:肉苁蓉各提取物对牛磺胆酸诱导的ges-1细胞损伤模型的药效活性筛选
55.采用牛磺胆酸(taurocholicacid,tca)诱导的人胃粘膜上皮细胞系ges-1细胞建立胃粘膜损伤模型,评价荒漠肉苁蓉(简称荒漠)和管花肉苁蓉(简称管花)各提取物及其主要单体的胃粘膜保护活性。前期实验结果显示,tca对ges-1细胞损伤的ic50是1.47mm,因此本研究采用1.5mm的tca作为细胞损伤的造模剂量。各提取物均采用1,5,10μg/ml的浓度评价其在tca诱导的ges-1细胞损伤模型上的活性。
56.实验结果显示,模型组细胞存活率相较于对照组显著降低(p《0.01);而相较于模型组,管花总苷、管花多糖、管花寡糖均在10μg/ml浓度下,细胞活度有显著提高(p《0.05),提示管花总苷、管花多糖具有显著的胃粘膜保护活性。荒漠总苷、荒漠寡糖、荒漠多糖在10μg/ml浓度下,细胞活度有显著提高(p《0.05),提示荒漠总苷、荒漠寡糖、荒漠多糖具有显著
的胃粘膜保护活性(图1)。
57.实施例3:肉苁蓉单体成分对牛磺胆酸诱导的ges-1细胞损伤模型的药效活性筛选
58.肉苁蓉主要单体活性筛选均采用1,5,10μm的浓度评价其在tca诱导的ges-1细胞损伤模型上的活性。结果显示,模型组细胞存活率相对于对照组显著降低(p《0.01);而相对于模型组,红景天苷和毛蕊花糖苷细胞活度在1,5,10μm浓度下均能显著提高细胞活度,且具有剂量依赖性,在10μm时细胞活度的提高率最高(p《0.01),提示红景天苷和毛蕊花糖苷能够剂量依赖性的保护胃粘膜细胞。2
’‑
乙酰基毛蕊花糖苷、松果菊苷、异毛蕊花糖苷均在10μm时显著提高细胞活度,提示2
’‑
乙酰基毛蕊花糖苷、松果菊苷和异毛蕊花糖苷具有显著的胃粘膜保护活性。管花苷a在10μm浓度下能显著提高细胞活度(p《0.05),提示管花苷a有显著的胃粘膜保护活性(图2)。
59.实施例4:松果菊苷对不同ges-1细胞损伤模型的药效活性
60.由于肉苁蓉的特征性成分松果菊苷药效活性最为显著,因此本研究再次利用三种体外ges-1细胞损伤模型评价松果菊苷的体外胃粘膜保护的药效活性。
61.在8%的乙醇诱导的细胞损伤模型中,松果菊苷1,5,10μm三个浓度下均可显著提高乙醇损伤的细胞存活率且呈剂量依赖性(p《0.01),其中10μm的松果菊苷药效最佳。在1.5mm胆汁酸(bileacid,ba)诱导的ges-1细胞损伤模型中,松果菊苷1,5,10μm三个浓度下同样均能显著提高胆汁酸诱导的ges-1细胞损伤存活率。在5mm乙酰水杨酸诱导的ges-1细胞损伤模型中,松果菊苷在10μm浓度下具有显著的胃粘膜细胞保护活性(p《0.05)。在三种不同的胃粘膜细胞损伤模型中,松果菊苷均显示出良好的药效活性,为本研究进一步的机制探索和体外药效验证奠定了基础(图3)。
62.实施例5:松果菊苷对胆汁酸诱导ges-1细胞损伤模型ldh释放率的影响
63.细胞损伤会释放大量乳酸脱氢酶,因此检测ldh释放率可以评价松果菊苷的细胞保护作用。
64.结果显示,胆汁酸处理后细胞内ldh释放率显著增加(p《0.01),而松果菊苷处理后,剂量依赖性降低了ldh释放率(p《0.05),说明松果菊苷具有一定的细胞保护作用(图4)。
65.实施例6:松果菊苷对胆汁酸诱导ges-1细胞自噬的影响
66.细胞自噬是细胞损伤常见的应激机制也是多种消化系统疾病的病理基础。自噬是一种程序化的自我分解代谢调节过程,当细胞自噬过程被启动后,待分解的细胞碎片、受损细胞器及异常蛋白质等会被包裹形成囊泡,通过胞浆运输过程中逐渐成熟酸化,与溶酶体结合形成自噬溶酶体,并最终被消化、降解和再利用。吖啶橙染料能够渗入自噬溶酶体中,在荧光显微镜下呈现红黄色荧光,进而反应细胞的自噬水平。
67.为了探究松果菊苷对胆汁酸诱导ges-1细胞自噬水平的影响,采用吖啶橙染色对其进行分析。结果显示,胆汁酸处理细胞后内红绿色荧光水平增强,说明细胞自噬被显著激活。松果菊苷处理后,红绿色荧光水平有所改善,说明松果菊苷抑制了胆汁酸诱导的自噬过度激活,松果菊苷的胃保护作用与细胞自噬的调控相关(图5)。
68.实施例7:松果菊苷对各组小鼠胃组织大体观的影响
69.健康雄性spf级icr小鼠,体重20-25g,饲养在屏障环境中普通饲料适应性喂养1周,然后随机分成5组(每组10只),分别为正常对照组(controlgroup,cg)、模型组(model group,mg)、阳性药硫糖铝组(sucralfate-treatedgroup,sg)、ech25组(25mg/
kgdoseofech-treatedgroup,ech25)、ech50组(50mg/kgdoseofech-treatedgroup,ech50)。除cg组外,其余各组小鼠灌胃反流液(2.5%tca、1.5%胰蛋白酶、0.25%卵磷脂)建立胆汁反流性胃炎模型,每日2次,剂量为15ml/kg。小鼠在灌胃反流液3天后,各组开始给药处理,给药处理持续2周,每日在灌胃反流液6h后,ech组灌胃不同剂量的ech25mg/kg和50mg/kg,阳性药硫糖铝组剂量为120mg/kg。
70.胆汁反流造成胃损伤时,胃镜下可见慢性胃炎或胃溃疡的表现,如胃粘膜颜色不均匀、充血质脆,有出血点或溃疡点,胃黏液中存在绿色或黄色的胆汁样液体等。
71.给药2周动物取材时,对小鼠胃粘膜大体观进行拍照观察,可以初步判断胃粘膜的损伤程度。如图6所示,正常组小鼠胃粘膜粘膜完整红润,褶皱正常无红肿,表面无溃疡点和出血点。模型组胃粘膜出现明显的出血点,胃粘膜红肿,褶皱消失。ech高剂量组和阳性药硫糖铝组胃粘膜出血点和红肿均有所改善。
72.实施例8:松果菊苷对各组小鼠胃组织病理形态的影响
73.动物实验方法如实施例8所示。通过h&e染色对胆汁反流性胃粘膜损伤模型小鼠胃组织切片进行病理形态学观察,并显微镜下观察各组胃粘膜上皮细胞的病理形态。如图7所示,cg组胃粘膜结构完整,上皮细胞呈单柱状,排列整齐,几乎未见缺损、脱落。与cg组相比,mg组胃粘膜上皮细胞脱落、缺损,固有腺体排列紊乱,这些特征与胆汁反流性胃炎患者中观察到的特征相似。ech给药治疗后,上述改变明显较模型组轻,胃粘膜结构基本完整,胃粘膜上皮细胞排列相对整齐规则,说明ech治疗可明显减轻胃组织的病理损伤。
74.实施例9:松果菊苷对各组小鼠血浆il-1β,il-6,tnfα水平的影响
75.动物实验方法如实施例7所示。胃粘膜遭受胆汁等刺激因素的攻击,防御因子受损,导致胃粘膜慢性炎症并造成组织损伤。il-1β,il-6,tnfα均为炎症反应的标志因子,为了进一步研究ech在胆汁反流性胃炎中的作用,检测了血浆中的炎症因子il-6、il-1β和tnfα的水平。
76.如图8所示,在胆汁反流2周后,上述三种炎症因子均显著上调(p《0.01),而ech则显著下调il-6、il-1β、tnfα的含量,且呈剂量依赖关系。
77.显然,本领域的技术人员可以对本发明进行各种改动和变型而不脱离本发明的精神和范围。这样,倘若本发明的这些修改和变型属于本发明权利要求及其等同技术的范围之内,则本发明也意图包含这些改动和变型在内。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。