by blocking a conformational change of the unphosphorylated form[j].nature,1979,282(5736):333
–
335.
[0008]
[3]evangelou a m.vanadium in cancer treatment[j].critical reviews in oncology/hematology,2002,42(3):249
–
265.
[0009]
[4]li y,yang l,xu x,et al.multifunctional size-expandable nanomedicines enhance tumor accumulation and penetration for synergistic chemo-photothermal therapy[j].acs applied materials and interfaces,2021,13(39):46361
–
46374.
[0010]
[5]ware m j,nguyen l p,law j j,et al.a new mild hyperthermia device to treat vascular involvement in cancer surgery[j].scientific reports,springer us,2017,7(1):1
–
14.
[0011]
[6]zhou j,lin z,ju y,et al.polyphenol-mediated assembly for particle engineering[j].accounts of chemical research,2020,53(7):1269
–
1278.
[0012]
[7]song x r,li s h,dai j,et al.polyphenol-inspired facile construction of smart assemblies for atp-and ph-responsive tumor mr/optical imaging and photothermal therapy[j].small,2017,13(20):1
–
8.
技术实现要素:
[0013]
在本发明中,我们设计合成了一种超小钒酸基纳米颗粒,用于钒酸盐的体内递送。该设计以牛血清白蛋白(bsa)为模板,在其表面利用单宁酸(ta)和fe之间的配位效应形成包封,最终合成了粒径小而均匀,稳定性高的纳米材料ta-v@bsa,具有较好的生物安全性。其中,钒酸盐具有atp酶抑制活性,材料整体具有光热转化能力(808nm光激发),并基于热效应增强抑制效果,产生联合增强作用,因此,ta-v@bsa能够实现对肿瘤细胞的有效杀伤。此外,该材料具有浓度依赖的光声成像能力,可以用于指导治疗。
[0014]
具体合成步骤如下:
[0015]
(1)活化并配置钒(v)母液:取一定量的钒酸盐类加入离子水,优选钒浓度为200mm,用氢氧化钠调节ph至碱性,加热煮沸,至溶液无色透明,保证所有固体充分溶解,然后静置冷却至室温,并重复上述调节ph、加热、冷却至室温,直至溶液保持无色透明且ph值稳定为固定值,从而完成钒酸盐的活化成为v母液;每次ph调节的固定值依据不同种类的钒酸盐的特性调整,优选调节为10.0;完成活化后的钒酸盐应分装后-20℃保存,避免反复冻融;
[0016]
可供选择的钒酸盐类包括:原钒酸钠,偏钒酸钾,偏钒酸钠等,其中优选原钒酸钠;
[0017]
所用氢氧化钠的浓度为0.1-10m,1m为宜;若ph高于10.0可用0.1-10m盐酸回调,1m为宜;加热温度为90-100℃;溶解过程可以通过磁力搅拌、涡旋震荡辅助;
[0018]
(2)取bsa置于反应容器a中,加入去离子水溶解,得到bsa溶液;bsa溶液的浓度为1-100mg/ml(0.015-1.5mm),10mg/ml(0.15mm)为宜;通过超声辅助、搅拌、轻微加热等手段辅助溶解,确保溶解充分、溶液浓度均匀;
[0019]
(3)取步骤(1)中v母液,用去离子水稀释,得到v溶液;v溶液的浓度为1-100mm,优选10mm为宜;
[0020]
通过超声、搅拌等手段辅助,保证溶液浓度均匀;
[0021]
(4)取ta置于反应容器b中,加入去离子水溶解,得到ta溶液;ta溶液的浓度为1-100mm,优选40mm为宜;
[0022]
通过超声、搅拌、轻微加热等手段辅助溶解,确保溶解充分、溶液浓度均匀;
[0023]
(5)取步骤(2)的bsa溶液v1ml和步骤(3)的v溶液v2ml优先混合均匀后,边搅拌边加入ta溶液v3ml,再次混合均匀,持续搅拌并反应一段时间;最终混合溶液中钒与bsa的摩尔比为20:1-50:1优选33.3:1,钒与ta的摩尔比为1:0.5-1:10优选1:4为宜,可以通过控制ta:v的比例控制对bsa的包封效果;
[0024]
反应时间为20-50min,30min左右颜色不继续变化为宜;
[0025]
一般如溶液体积用量关系为v1=2v2=2v3。
[0026]
(6)将步骤(5)合成产物转移至透析袋中,用去离子水透析过夜;透析袋的截留分子量为100kda;
[0027]
透析袋外去离子水的体积与透析袋中溶液体积的比例为1:60-1:200,1:100为宜;通过磁力搅拌确保透析充分,转速为300-800r,优选600r为宜;透析总时间为18-72h,48h为宜;每隔12h更换透析袋外去离子水一次;
[0028]
(7)将步骤(6)中透析袋中产物取出后转移至离心管中,离心去除沉淀,合成的ta-v@bsa。
[0029]
离心转速为6000-10000rpm,8000rpm为宜;离心时间为15-30min,20min为宜。
[0030]
本发明所得ta-v@bsa作为制备治疗肿瘤的药剂,ta-v@bsa作为制备抑制atp酶活性的药剂,通过光激活或热来增强抑制效果,作为光热材料实用,通过光来加强atp酶活性的抑制效果和肿瘤细胞的杀伤;作为光声成像材料,用于指导治疗。
[0031]
本发明具有如下优势:
[0032]
1.以bsa为模板,ta为交联介质合成的钒酸盐递送体系,生物安全性高,稳定性好,能够实现钒的体内递送。
[0033]
2.ta-v@bsa整体尺寸较小,能够深入肿瘤组织内部,并基于肿瘤部位氧化应激态特征,实现钒酸响应释放,发挥其atp酶抑制剂活性,能够发挥肿瘤杀伤效果。
[0034]
3.ta-v@bsa具有光热转化能力,能够在808nm近红外光照射下升温,并通过温度控制产生温热效应,联合促进钒酸的药效活性。
[0035]
4.ta-v@bsa经光热转化产生的热信号可以进一步转化为声信号,故具有光声成像的功能,用以指导治疗进程。
附图说明
[0036]
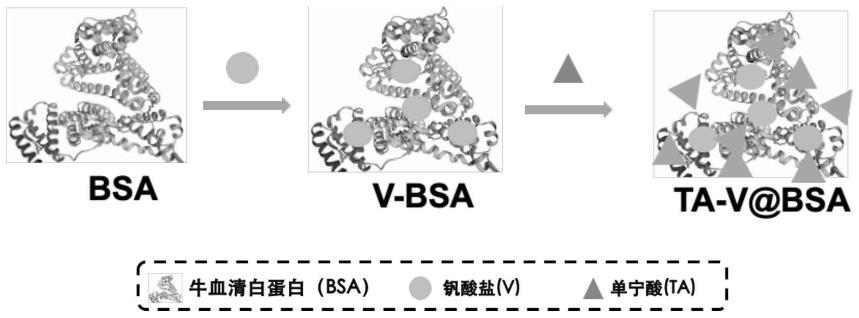
图1:ta-v@bsa合成步骤示意图。
[0037]
图2:ta-v@bsa功能示意图。
[0038]
图3:包封效率与ta:v比例的关系图。a)sds-page电泳结果;b)包封率统计结果。
[0039]
图4:ta-v@bsa的粒径电位表征结果图。a)透射电镜图;b)动态光散射粒径测试结果;c)动态光散射电位测试结果。
[0040]
图5:ta-v@bsa的x射线光电子能谱测试结果图。
[0041]
图6:ta-v@bsa的响应释放行为表征结果图。
[0042]
图7:不同浓度ta-v@bsa的500-850nm波段吸收光谱。
[0043]
图8:光激发光热转化能力评价。a)不同浓度ta-v@bsa在808nm(1w/cm2,10min)光照后升温曲线;b)不同组别热成像图片;c)光稳定性测试结果。
[0044]
图9:细胞毒性实验测试结果。a)不同浓度ta-v@bsa的细胞毒性;b)光激发下的联合细胞毒性比较。
[0045]
图10:atp酶活测试结果。
[0046]
图11:光声成像效果评价。
具体实施方式
[0047]
下面结合实施例对本发明做进一步说明,但本发明并不限于以下实施例。
[0048]
实施例1
[0049]
(1)原钒酸钠活化:将原钒酸钠溶解在原地烧瓶中配置成200mm的溶液,使用1m氢氧化钠调节ph至10.0,100℃加热同时磁力搅拌,直到煮沸至无色透明,确保所有固体溶解。冷却至室温后,重复调ph、加热、冷却步骤3次,直至溶液保持无色并且ph稳定在10.0,得到成功活化的钒酸钠母液。
[0050]
(2)取200mm活化的钒酸钠母液5ml,加入去离子水稀释,得到最终浓度10mm的v溶液,具体稀释倍数根据母液icp测试结果确定。将不同质量的ta溶解在去离子水中,超声至所有固体物溶解,分别配置成1.25,2.5,5,10,20,40mm的溶液备用。
[0051]
(3)各取100mg的bsa分别置于6个圆底烧瓶中,并加入10ml去离子水,超声至所有固体物溶解。各取5ml浓度为10mm的v溶液加入每个圆底烧瓶,混合均匀后边搅拌边在各个烧瓶中添加不同浓度的ta溶液5ml,400r搅拌反应30min至溶液颜色不再变化。混合后bsa终浓度为0.075mm,v的终浓度为2.5mm,ta的终浓度分别为0.3125,0.625,1.25,2.5,5,10mm,bsa:v摩尔比为1:33.3,ta:v的摩尔比依次为1:8,1:4,1:2,1:1,2:1,4:1。
[0052]
(4)将以上产物加入到100kda截留分子量的透析袋中,在2l的去离子水中透析,每隔12h换一次液,共透析48h,最后将透析袋中的溶液在8000rpm下离心20min去除不溶物,最终在上清液中获得超小粒径的ta-v@bsa,使用icp对最终合成的钒浓度进行定量。
[0053]
以上针对ta-v@bsa的合成流程(1)-(3)总结如图1所示。
[0054]
ta-v@bsa的功能总结如图2所示。ta-v@bsa整体尺寸较小,能够深入肿瘤组织内部,基于h2o2模拟的肿瘤部位氧化应激态特征,实现钒的响应释放,发挥其atp酶抑制剂活性,从而发挥肿瘤杀伤效果。同时,ta-v@bsa具有光热转化能力,能够在808nm近红外光照射下升温,从而产生温热效应,增强钒酸的抑制剂活性,从而联合增强发挥抗癌效果。同时,基于热信号到声信号的进一步转化,ta-v@bsa具有光声成像能力,能够用以指导治疗。
[0055]
不同ta:v比例下对bsa的包封结果如图3所示。a图中sds-page结果显示,对比bsa的对照和bsa和v的简单混合物,当ta的比例增加,对bsa的包封效果增加,表现为bsa蛋白的对应条带宽度下降,更多的bsa由于被包封后分子量的进一步增加从而滞留在孔洞中。表明当ta:v达到4:1时,能够实现对bsa的完全包封。b图针对包封率的统计结果与a图相符。后续的实验我们使用ta:v=4:1完成。
[0056]
ta-v@bsa的透射电镜的结果(图4中a)显示:ta-v@bsa具有很好的单分散性,平均粒径小于20nm。动态光散射(dls)的结果(图4中b、c)显示:ta-v@bsa的水合粒径为55.31nm
±
6.31nm,zeta电位为-15.3
±
1.52ev。
[0057]
ta-v@bsa的x射线光电子颜色测试v 2p结果如图5所示。能谱可以被分为513.61ev,515.70ev两个峰,占比分别为89.8%与11.2%,分别为v(iv)与v(v)的特征峰,意味着ta-v@bsa中钒主要存在的价态为 4价,其在合成过程中被还原,导致毒性降低。
[0058]
图6是我们针对ta-v@bsa中钒的释放能力进行的测试,结果发现:在pbs中ta-v@bsa中钒无明显的释放,而在过氧化氢条件下(模拟的肿瘤氧化应激态),复合结构则会被氧化破坏,从而导致钒逐渐从体系中释放,并在24h小时累积释放率达到45%
±
2.94%。
[0059]
通过紫外可见光谱显示(图7,图中线上数字代表ta-v@bsa浓度,单位:mg/ml),较大浓度的ta-v@bsa在500-850nm有很强的吸收,并且这种吸收随着浓度呈现线性增加,证实了ta-v@bsa具有对nir光的吸收能力。基于其穿透深度深的特性,808nm激光是目前应用广泛的激光,基于ta-v@bsa在808nm处的吸光能力也非常可观,因此我们选择808nm激光作为后续实验的激发光。
[0060]
光热转化能力评价实验结果如图8所示,图8中a、b结果显示,不同浓度的ta-v@bsa在经过808nm激光(1w/cm2,10min)照射后的升温曲线与最终温度不同,浓度越高,升温效果越好。同时,我们进行了光热转化稳定性测试,用以评价ta-v@bsa在经历多次光激发后的光热转化能力,实验结果如图8中c所示。图中的阴影区域代表给与光照(808nm激光,1w/cm2,5min),由于光热转化,溶液温度上升;图中的空白区域代表撤掉光照,由于向周围环境的热辐射,温度自然下降。对比第一次升温和第五次升温的过程我们发现,当经历照射-降温各5min的5个循环后,ta-v@bsa的升温速度和最终达到温度并无明显下降,即其光热转化能力在有限次的光照下并不受影响,具有较好的光热转化稳定性。
[0061]
随后,我们使用小鼠乳腺癌细胞(4t1)验证了ta-v@bsa的肿瘤杀伤效果。每孔加入5
×
104个4t1细胞,待细胞贴壁后,加入5,12.5,25,50,100ug/ml ta-v@bsa,孵育24h后,用mtt法检测。实验结果如图9中a所示,随着ta-v@bsa浓度的增加,细胞活力也逐渐下降,这是由于肿瘤细胞的氧化应激状态诱发部分钒的释放,从而导致了细胞凋亡。此外,另一组对比实验结果显示(图9中b),pbs l组没有明显的细胞活率降低,证明单独激光照射没有肿瘤细胞杀伤效果;而在控制ta-v的浓度均为60ug/ml后,激光光照联合组ta-v@bsa l组(808nm,1w/cm2,10min)相比ta-v@bsa组对肿瘤细胞的杀伤进一步增加,显示了光激发后的联合增强抗肿瘤效果。
[0062]
对上述图9b中不同组别的atpase酶活测试结果如图10所示,实验结果显示,ta-v@bsa l组atpase酶活最低,验证了前述我们的设想,即基于光照后产生的温热效应,增强了钒酸盐的atp酶抑制效果,从而增强了对肿瘤的杀伤。
[0063]
紧接着我们使用高分辨光声成像仪对ta-v@bsa的光声成像能力进行了测试。图11中a圈中灰色部分代表了光声信号。将不同浓度的ta-v@bsa加入到塑料软管后,使用650nm-850nm间隔5nm对不同浓度的样品进行成像,然后利用800nm光声信号与浓度关系进行相关性分析。结果显示:随着ta-v@bsa的浓度增加,光声信号也逐渐增强,两者呈现线性相关(图11中b)。在荷瘤小鼠(4t1)上,尾静脉注射ta-v@bsa后肿瘤部位的光声成像结果显示:随着ta-v@bsa在体内的循环后在肿瘤部位逐渐富集,小鼠肿瘤部位的光声信号逐渐增强,并且在4h达到峰值后逐渐降低。证实了ta-v@bsa能够实现肿瘤集聚的同时,再次证明了其通过光声成像指导治疗的可行性。
[0064]
综上所述,我们以bsa为模板合成了超小的、具有atp酶抑制活性的钒基纳米材料ta-v@bsa,该材料具有氧化响应性钒释放和光热转化能力,可以通过钒酸盐的atp酶抑制活性和光激活、热增强的抑制效果来实现对肿瘤细胞的有效杀伤,同时该材料具有浓度依赖的光声成像能力,可以用于指导治疗。
[0065]
本文应用了具体个例对本发明的原理及实施方式进行了阐述,以上实施例的说明只是用于帮助理解本发明的核心思想,在不脱离本发明原理的情况下,还可对本发明进行若干改进和修饰,这些改进和修饰也落入本发明的保护范围内。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。