一种抗flt3-itd耐药突变型急性髓系白血病药物
技术领域
1.本发明涉及生物医药领域,具体地,涉及一种抗flt3-itd耐药突变型急性髓系白血病的药物。
背景技术:
2.急性髓系白血病(aml)是一种造血干细胞的恶性疾病,其特征是髓系异常分化的原始细胞克隆性扩增。这种未成熟骨髓细胞增殖的后果包括未成熟祖细胞的累积和正常造血功能的损害,导致严重的感染,贫血和出血。一些患者还可能出现髓外疾病,包括中枢神经系统受累。一直以来aml的标准治疗方案是以阿糖胞苷和柔红霉素为主的化疗,但是多数老年aml患者无法承受高强度的化疗,因此急需新的治疗方案来改善aml患者尤其老年患者的生存率。
3.fms样酪氨酸激酶3(flt3)是一种受体酪氨酸激酶,通常在急性髓细胞性白血病(aml)中发生突变。约23%aml患者在flt3的近膜结构域获得内部串联复制(flt3-itd),这是预后不良的标志。众所周知,itd突变会导致flt3受体的自身磷酸化和组成性激活,从而通过激活aml细胞中的flt3/stat5/mapk信号导致细胞恶性增殖、分化和存活。
4.目前已有若干个flt3抑制剂被批准用于临床,但长期治疗效果不尽人意,多数aml患者会在短期内产生耐药,主要机制是flt3激酶区域中与药物结合重要位点的获得性继发突变,二次突变位点集中在f691或d835残基处;还有一些aml的亚克隆中存在flt3-itd-tkd双重突变,并通过索拉非尼治疗选择出来。因此针对flt3-itd-tkd耐药突变的靶向药物研发再一次成为aml的研究热点。
技术实现要素:
5.本发明的目的在于提供一种针对flt3-itd耐药突变型急性髓系白血病的药物。
6.本发明的第一方面,提供了一种小分子化合物的用途,用于制备一组合物或制剂,所述组合物或制剂用于:
7.(a)抑制flt3-itd突变的白血病细胞生长;
8.(b)抑制flt3-itd-tkd突变的白血病细胞的生长;
9.(c)促进细胞凋亡,其中所述细胞为flt3-itd突变或flt3-itd-tkd突变的白血病细胞;
10.(d)抑制flt3蛋白磷酸化,其中所述flt3蛋白为flt3-itd突变或flt3-itd-tkd突变的flt3蛋白;和
11.(e)治疗急性髓系白血病(aml);
12.其中,所述小分子化合物为kx02或其药学上可接受的盐,所述的kx02具有式i所示的结构:
d835y、flt3-itd-d835v、flt3-itd-d835f或其组合。
32.在另一优选例中,所述白血病细胞为人类或非人类哺乳动物细胞。
33.在另一优选例中,所述白血病细胞是分离自aml患者的骨髓样本的白血病细胞。
34.在另一优选例中,所述aml患者具有flt3-itd突变,较佳地具有flt3-itd-tkd突变,更佳地具有flt3-itd-f691l、flt3-itd-d835y、flt3-itd-d835v、flt3-itd-d835f突变或其组合,最佳地具有flt3-itd-f691l突变。
35.本发明的第三方面,提供了一种体外非治疗性抑制flt3蛋白磷酸化的方法,所述方法包括:将flt3蛋白与小分子化合物kx02或其药学上可接受的盐接触,从而抑制所述flt3蛋白的磷酸化,其中所述flt3蛋白为flt3-itd突变或flt3-itd-tkd突变的flt3蛋白。
36.本发明的第四方面,提供了一种治疗急性髓系白血病(aml)的方法,所述方法包括:向需要的对象施用安全有效量的小分子化合物kx02或其药学上可接受的盐,或含有其的药物组合物。
37.在另一优选例中,所述需要的对象为人类或非人类哺乳动物。
38.在另一优选例中,所述需要的对象患有急性髓系白血病(aml)。
39.在另一优选例中,所述在另一优选例中,所述急性髓系白血病(aml)是具有flt3-itd突变,较佳地具有flt3-itd-tkd突变,更佳地具有flt3-itd-f691l、flt3-itd-d835y、flt3-itd-d835v、flt3-itd-d835f突变或其组合,最佳地具有flt3-itd-f691l突变的aml。
40.在另一优选例中,所述安全有效量是指:0.001-50mg/kg(体重),较佳地0.1-25mg/kg(体重),更佳地1-10mg/kg(体重),最佳地7.5-10mg/kg(体重)。
41.应理解,在本发明范围内中,本发明的上述各技术特征和在下文(如实施例)中具体描述的各技术特征之间都可以互相组合,从而构成新的或优选的技术方案。限于篇幅,在此不再一一累述。
附图说明
42.图1显示了筛选得到的包括kx02在内的5种小分子抑制剂,以及目前已应用于临床的flt3-itd靶向抑制剂crenolanib、ac220(quizartinib)和giltertinib的结构式。
43.图2显示了在flt3-itd突变的人类白血病细胞株molm13以及mv4-11中以不同浓度的kx02和ac220处理48小时后使用cell titer-glo检测细胞的活率。以上实验均重复三次且能得到接近的效果,图中为取其中一次实验中三个重复样本的统计结果。
44.图3显示了小鼠正常细胞ba/f3、ba/f3-flt3-itd、itd-f691l、itd-d835y、itd-d835v和itd-d835f细胞株使用flt3抑制剂ac220(a)、flt3抑制剂glitertinib(b)、或小分子化合物kx02(c)处理48小时细胞的增殖情况。以上实验皆重复三次且能得到接近的效果,图中为取其中一次实验中三个重复样本的统计结果。
45.图4显示了kx02对flt3-itd突变细胞有促凋亡的作用。mv4-11以及molm13以不同的浓度的kx02处理24小时后,使用annexin v-apc/pi流式检测凋亡细胞比例。以上实验均重复三次且能得到接近的效果,图中为取其中一次实验中三个重复的样本统计的结果。
46.图5显示了kx02对flt3-itd突变细胞及其相关的耐药突变的细胞株具有促进凋亡的效果。在ba/f3上突变的细胞用不同浓度的kx02处理24小时后,流式检测凋亡细胞比例。以上实验均重复三次且能得到接近的效果,图中为取其中一次实验中三个重复的样本统计
的结果。
47.图6显示了kx02使flt3-itd突变细胞株的周期阻滞在g2/m期。以上实验均重复三次且能得到接近的效果,图中为取其中一次实验中三个重复的样本统计的结果。
48.图7显示了kx02使flt3-itd-tkd双重突变细胞株的周期阻滞在g2/m期。以上实验均重复三次且能得到接近的效果,图中为取其中一次实验中三个重复的样本统计的结果。
49.图8显示了人白血病细胞株mv4-11以及molm13用不同浓度的kx02(0、25nm、50nm、100nm)处理12小时后通过western blot检测p-flt3、flt3、p-stat5、stat5、p-erk、erk、p-src、scr以及内参gapdh蛋白的表达。
50.图9显示了小鼠细胞baf3上构建了flt3突变体的细胞系,用不同浓度的kx02处理12小时后通过western blot检测p-flt3、flt3、p-stat5、stat5、p-erk、erk、p-src、scr以及内参gapdh蛋白的表达。
51.图10显示了人白血病细胞株mv4-11及molm13用不同浓度的长春新碱(0、25nm、50nm、100nm)处理12小时后通过western blot检测p-flt3、flt3、p-stat5、stat5、p-erk、erk以及内参gapdh蛋白的表达。
52.图11显示了用小鼠细胞baf3上构建了flt3突变体的细胞系,包括baf3 ft3-itd、baf3 itd-f691l、baf3 itd-d835y用不同浓度的长春新碱处理12小时后通过western blot检测p-flt3、flt3、p-stat5、stat5、p-erk、erk以及内参gapdh蛋白的表达。
53.图12显示了kx02抑制微管蛋白聚合而破坏了微管网络结构。在molm13细胞中用100nmol/l紫杉醇,100nmol/l长春新碱,100nmol/l秋水仙碱,100nmol/l kx02,200nmol/l kx02处理4小时,微管形态通过免疫荧光监测。用药处理后,与抗α/β-微管蛋白抗体和alexa fluor488偶联抗兔抗体(绿色)一起孵育。核染色(蓝色)是用dapi染色的。共聚焦显微镜(60x)成像。
54.图13显示了在molm13和mv4-11细胞使用不同浓度梯度的ac220合加50nμ、100nμmp-hj-1b处理48小时后用celltiter-glo检测细胞活率。以上实验均重复三次且能得到接近的效果,图中为取其中一次实验中三个重复的样本统计的结果。
55.图14显示了(a)kx02与flt3(蛋白质数据库:5x02)对接结果概述;显示两个不同角度的视图。(b)kx02-flt3模型特写,残基leu-616和glu-661的氢键。
56.图15显示了(a)kx02与flt3(蛋白质数据库:4rt7)对接结果概述;显示两个不同角度的视图。(b)kx02-flt3模型特写,残基cys-694的氢键。
57.图16显示了4例诊断明确的flt3-itd阳性aml患者的骨髓细胞样本和两例flt3-itd,flt3-d835y的aml患者的骨髓细胞分别经3倍浓度梯度递增添加药物kx02以及ac220处理,48小时后应用celltiter-glo检测细胞活率情况。以上实验均重复三次且能得到接近的效果,图中为取其中一次实验中三个重复的样本统计的结果。
58.图17显示了flt3-itd阳性aml患者的骨髓细胞样本使用不同浓度的kx02(0、25nm、50nm、100nm)处理12小时后通过western blot检测p-flt3、flt3以及内参gapdh蛋白的表达。
59.图18显示了baf3 flt3/itd-f691l白血病模型小鼠发病模型建立后第4天开始灌胃给药处理,在给药治疗的第4天(a)和第8天外周血检测白血病细胞的比例(即gfp阳性细胞所占的比率)*表示p《0.05,**表示p《0.01,***表示p《0.001。
60.图19显示了baf3 flt3/itd-f691l白血病模型小鼠模型给药期间,每组小鼠称量体重结果统计。
61.图20显示了baf3 flt3/itd-f691l白血病模型小鼠发病模型在小鼠注射白血病细胞的第10天,从三组中每组随机抽取一只小鼠被安乐死并解剖,取出脾脏和肝脏称重并拍照。*表示p《0.05,**表示p《0.01,***表示p《0.001。
62.图21显示了baf3 flt3/itd-f691l白血病模型小鼠发病模型将小鼠脾脏和肝脏进行伊红(h&e)染色并于镜下观察白血病细胞的浸润情况。
63.图22显示了在小鼠注射白血病细胞的第10天,从三组(包括对照组、ac220组(10mg/kg)、kx02组(10mg/kg))中随机抽取一只小鼠被安乐死并解剖。然后取出脾脏和骨髓,通过流式细胞术检测骨髓和脾脏中的白血病细胞(即gfp阳性细胞比例)。
64.图23显示了三组小鼠每天持续灌胃给药,直到对照组小鼠开始死亡,然后停止继续给药以观察小鼠的生存和死亡情况并做生存期统计。*表示p《0.05,**表示p《0.01,***表示p《0.001。
具体实施方式
65.本发明人经过广泛而深入的研究,首次意外地发现小分子化合物kx02可以作为flt3激酶的抑制剂,发挥抗flt3-itd耐药突变型急性髓系白血病作用。实验证明,kx02在体外可以抑制flt3-itd突变以及flt3-itd耐药突变型(flt3-itd-tkd双重突变,尤其是flt3-itd-f691l突变)的白血病细胞的生长,促进细胞凋亡。进一步的实验证明,kx02是通过抑制白血病细胞内flt3蛋白激酶的磷酸化,同时破坏细胞内微管结构来发挥抑制作用。此外,动物实验证明,kx02可以延缓flt3-itd-f691l白血病小鼠的发病,并延长患病小鼠的生存时间。因此,kx02可以作为急性髓系白血病,尤其是带有的flt3-itd耐药突变的aml的治疗剂。
66.在此基础上,完成了本发明。
67.术语
68.为了可以更容易地理解本公开,首先定义某些术语。如本技术中所使用的,除非本文另有明确规定,否则以下术语中的每一个应具有下面给出的含义。在整个申请中阐述了其它定义。
69.flt3蛋白和突变
70.flt3基因其定位于13q12染色体。人类和鼠类flt3基因均由24个外显子(3,848bp)组成。flt3与iii类受体酪氨酸激酶(rtkiii)受体家族的其他成员基因的序列具有很强相似性。iii类受体酪氨酸激酶家族包括flt3,fms,血小板衍生的生长因子受体(pdgfr)和kit。flt3包含四个区域,分别为:由五个免疫球蛋白样亚结构域组成的n末端细胞外区域;一个跨膜结构域;一个近膜(juxtamembrane domain,jm)结构域以及细胞内c末端激酶结构域。
71.flt3突变中的大多数是框内编码近膜区域的插入突变,称为内部串联重复(itd)突变,大多数itd突变发生在富含酪氨酸的区域,对应的密码子为589至599。flt3-itd突变是aml中最常见的突变,约占25%。flt3-itd是常见的驱动突变,并赋予aml患者不良的预后。itd突变会导致flt3受体的自身磷酸化和组成性激活,从而通过激活aml细胞中的flt3/stat5/mapk信号导致细胞恶性增殖、分化和存活。flt3突变在酪氨酸激酶域(flt3-tkd)在
aml中的发生率较低(约占所有病例的7-10%),其预后价值尚不确定。flt3-itd高阳性为aml患者预后不良风险类别,该突变引起对常规化疗耐药。
72.flt3抑制剂
73.flt3是aml中最重要的靶标之一,自发现flt3突变以来,人们一直在努力开发flt3抑制剂。flt3抑制剂是与atp竞争结合激酶域活性口袋的小分子,可抑制自身磷酸化和下游靶标的磷酸化。flt3抑制剂可大致分为第一代和第二代抑制剂。第一代flt3抑制剂是多激酶抑制剂,对flt3没有选择性,包括midostaurin,索拉非尼,舒尼替尼和ponatinib。第二代flt3抑制剂可以选择性抑制flt3,其中包括quizartinib,gilteritinib和crenolanib。
74.使用flt3抑制剂治疗的aml患者容易产生耐药,主要机制是flt3激酶区域中与药物结合重要位点的获得性继发突变,二次突变位点集中在f691或d835残基处,从而形成flt3-itd-tkd双重突变。
75.微管蛋白及其抑制剂
76.微管(microtube)是由α
–
β微管蛋白组成的异二聚体动态结构,作为细胞骨架的重要组成部分,在细胞分裂中必不可少,微管蛋白是抗癌药物的重要靶标。通过结合微管不同位点,微管靶向抑制剂破坏了微管蛋白动力学。微管抑制剂干扰微管功能并将细胞停滞在有丝分裂中,最终通过凋亡和坏死导致细胞死亡,微管抑制剂在抗肿瘤药物的发展中有着重要地位。
77.根据与微管位点结合的不一样,微管蛋白抑制剂大致分为稳定微管的药物和破坏微管的药物。秋水仙碱和长春新碱等微管蛋白抑制剂可抑制微管蛋白聚合从而稳定微管,微管蛋白稳定剂紫杉醇(紫杉醇)可增强微管蛋白聚合从而破坏微管。
78.kx02
79.kx2-391(即kx02)是靶向src激酶家族和微管蛋白的双重抑制剂,可在新的α,β微管蛋白异二聚体结合位点结合并抑制微管蛋白聚合。kx02对多种肿瘤细胞系(包括几种前列腺癌细胞小鼠模型)表现出显著的细胞毒性。已经证实kx02是一种临床有效的低毒性微管抑制剂。它具有很强的微管蛋白抑制活性,可以在低纳摩尔水平上显著抑制微管蛋白的聚合。与传统的微管抑制剂相比,临床前和临床试验已证实kx02的毒性非常低。
80.本发明提供了一种kx02的用途,用于用于制备一化学组合物或制剂,所述组合物或制剂用于:
81.(a)抑制flt3-itd突变的白血病细胞生长;
82.(b)抑制flt3-itd-tkd突变的白血病细胞的生长;
83.(c)促进细胞凋亡,其中所述细胞为flt3-itd突变或flt3-itd-tkd突变的白血病细胞;
84.(d)抑制细胞内flt3蛋白磷酸化,其中所述细胞为flt3-itd突变或flt3-itd-tkd突变的白血病细胞;和
85.(e)治疗急性髓系白血病(aml)。
86.其中,所述组合物或制剂不影响细胞内src蛋白的磷酸化,所述细胞为flt3-itd突变或flt3-itd-tkd突变的白血病细胞。
87.在另一优选例中,所述flt3-itd-tkd突变选自下组:flt3-itd-f691l、flt3-itd-d835y、flt3-itd-d835v、flt3-itd-d835f或其组合。
88.在另一优选例中,所述flt3-itd-tkd突变为flt3-itd-f691l。
89.在另一优选例中,所述急性髓系白血病(aml)是具有flt3-itd突变,较佳地具有flt3-itd-tkd突变,更佳地具有flt3-itd-f691l、flt3-itd-d835y、flt3-itd-d835v、flt3-itd-d835f突变或其组合,最佳地具有flt3-itd-f691l突变的aml。
90.在另一优选例中,所述flt3-itd-tkd突变是由ac220(quizartinib)或giltertinib治疗引起的耐药性突变。
91.药物组合物
92.如本文所用,术语“药物组合物”是指将用于特定目的而被施用的组合物。
93.为了本发明目的,药物组合物含有kx02或其药学上可接受的盐作为活性成分,以及药学上可接受的载体并用于治疗急性髓系白血病(aml)。
94.术语“药学上可接受的”是指政府药品管理机构或在药典上列出并认可的可以用于脊椎动物、尤其用于人类的物质。通常,药学上可接受的载体指的是一种或多种相容性固体或液体填料或凝胶物质,它们适合于人使用,而且必须有足够的纯度和足够低的毒性。“相容性”在此指的是组合物中各组份能和本发明的活性成分以及它们之间相互掺和,而不明显降低活性成分的药效。药学上可以接受的载体部分例子有纤维素及其衍生物(如羧甲基纤维素钠、乙基纤维素钠、纤维素乙酸酯等)、明胶、滑石、固体润滑剂(如硬脂酸、硬脂酸镁)、硫酸钙、植物油(如豆油、芝麻油、花生油、橄榄油等)、多元醇(如丙二醇、甘油、甘露醇、山梨醇等)、乳化剂(如)、润湿剂(如十二烷基硫酸钠)、着色剂、调味剂、稳定剂、抗氧化剂、防腐剂、无热原水等。
95.本发明活性成分或药物组合物的施用方式没有特别限制,代表性的施用方式包括(但并不限于):口服、肌肉注射、静脉注射、静脉滴注、瘤内注射、灌肠、喷雾、外敷、或腹腔注射。
96.用于口服给药的固体剂型包括片剂、丸剂、散剂、颗粒剂、或胶囊剂。在这些固体剂型中,活性成分与至少一种常规惰性赋形剂(或载体)混合,如柠檬酸钠或磷酸二钙,或与下述成分混合:(a)填料或增容剂,例如,淀粉、乳糖、蔗糖、葡萄糖、甘露醇和硅酸;(b)粘合剂,例如,羟甲基纤维素、藻酸盐、明胶、聚乙烯基吡咯烷酮、蔗糖和阿拉伯胶;(c)保湿剂,例如,甘油;(d)崩解剂,例如,琼脂、碳酸钙、马铃薯淀粉或木薯淀粉、藻酸、某些复合硅酸盐、和碳酸钠;(e)缓溶剂,例如石蜡;(f)吸收加速剂,例如,季胺化合物;(g)润湿剂,例如鲸蜡醇和单硬脂酸甘油酯;(h)吸附剂,例如,高岭土;和(i)润滑剂,例如,滑石、硬脂酸钙、硬脂酸镁、固体聚乙二醇、十二烷基硫酸钠,或其混合物。胶囊剂、片剂和丸剂中,剂型也可包含缓冲剂。
97.固体剂型如片剂、糖丸、胶囊剂、丸剂和颗粒剂可采用包衣和壳材制备,如肠衣和其它本领域公知的材料。它们可包含不透明剂,并且,这种组合物中活性成分或化合物的释放可以延迟的方式在消化道内的某一部分中释放。可采用的包埋组分的实例是聚合物质和蜡类物质。必要时,活性成分也可与上述赋形剂中的一种或多种形成微胶囊形式。
98.用于口服给药的液体剂型包括药学上可接受的乳剂、溶液、悬浮剂、糖浆或酊剂。除了活性成分外,液体剂型可包含本领域中常规采用的惰性稀释剂,如水或其它溶剂,增溶剂和乳化剂,例知,乙醇、异丙醇、碳酸乙酯、乙酸乙酯、丙二醇、1,3-丁二醇、二甲基甲酰胺以及油,特别是棉籽油、花生油、玉米胚油、橄榄油、蓖麻油和芝麻油或这些物质的混合物
等。
99.除了这些惰性稀释剂外,组合物也可包含助剂,如润湿剂、乳化剂和悬浮剂、甜味剂、矫味剂和香料。
100.除了活性成分外,悬浮液可包含悬浮剂,例如,乙氧基化异十八烷醇、聚氧乙烯山梨醇和脱水山梨醇酯、微晶纤维素、甲醇铝和琼脂或这些物质的混合物等。
101.用于肠胃外注射的组合物可包含生理上可接受的无菌含水或无水溶液、分散液、悬浮液或乳液,和用于重新溶解成无菌的可注射溶液或分散液的无菌粉末。适宜的含水和非水载体、稀释剂、溶剂或赋形剂包括水、乙醇、多元醇及其适宜的混合物。
102.用于局部给药的本发明药物组合物的剂型包括软膏剂、散剂、贴剂、喷雾剂和吸入剂。活性成分在无菌条件下与生理上可接受的载体及任何防腐剂、缓冲剂,或必要时可能需要的推进剂一起混合。
103.使用药物组合物,是将安全有效量的本发明化合物适用于需要治疗的哺乳动物(如人),其中施用时剂量为药学上认为的有效给药剂量,对于60kg体重的人而言,日给药剂量通常为1~2000mg,优选6~600mg。当然,具体剂量还应考虑给药途径、病人健康状况等因素,这些都是熟练医师技能范围之内的。通常其中“安全有效量”指的是:化合物的量足以明显改善病情,而不至于产生严重的副作用。
104.本发明药物组合物可以单独给药,或者与其他药学上可接受的化合物联合给药。例如,本发明药物组合物可以和其他抗白血病药物联用。
105.本发明的主要优点在于:
106.(1)本发明首次提出微管蛋白抑制剂kx02具有抑制flt3蛋白磷酸化的活性,可以作为flt3激酶的抑制剂。
107.(2)本发明提供了一种抗flt3-itd耐药突变型急性髓系白血病的药物kx02,为在使用现有flt3抑制剂后出现耐药性的患者提供了治疗选择。
108.(3)本发明为将来的临床转化提供重要的理论依据与实验基础,同时也为设计flt3靶点提供了新的思路。
109.下面结合具体实施例,进一步阐述本发明。应理解,这些实施例仅用于说明本发明而不用于限制本发明的范围。下列实施例中未注明具体条件的实验方法,通常按照常规条件,例如sambrook等人,分子克隆:实验室手册(new york:cold spring harbor laboratory press,1989)中所述的条件,或按照制造厂商所建议的条件。除非另外说明,否则百分比和份数是重量百分比和重量份数。
110.实验材料和方法
111.实验细胞:
112.人molm-13、mv4-11、293t细胞与小鼠baf3、3t3细胞均购自american type culture collection(atcc)公司(manassas,va,usa)。小鼠baf3-flt3-itd、baf3-flt3-itd-f691l、baf3-flt3-itd-d835y、baf3-flt3-itd-d835v、baf3-flt3-itd-d835f细胞为内部构建。
113.实验试剂:
114.quizartinib(ac220)、长春新碱、紫杉醇、kx02购于selleck chemicals公司(houston,tx,usa)。gitertinib购于targetmol公司(boston,ma,usa)。
115.aml患者临床样本:
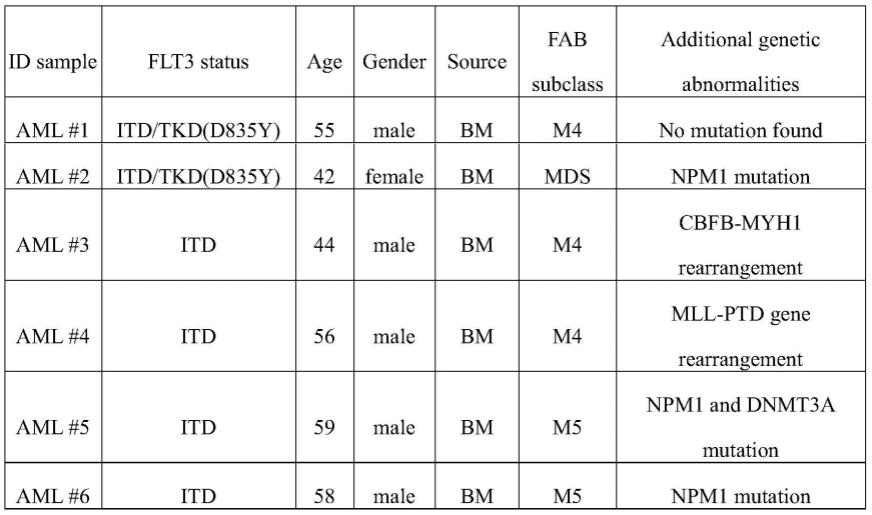
116.aml患者临床样本来源于就诊于上海交通大学医学院附属瑞金医院血液科患者的临床检测剩余样品。该研究得到上海交通大学医学院附属瑞金医院伦理委员会的批准。根据上海交通大学医学院附属瑞金医院规定,获得了患者体外药物测试研究的知情同意。所用aml患者临床信息见下表:
[0117][0118]
实验动物:
[0119]
6-8周龄balb/c小鼠购于斯莱克实验动物有限责任公司(上海,中国)。
[0120]
实验方法:
[0121]
1.flt3-itd与flt3-itd-tkd突变质粒构建
[0122]
根据trizol rna提取方法提取molm13细胞的rna,并反转录所得rna从而获得cdna。以cdna作为模板,以migr1为载体,设计flt3-itd片段的引物,构建migr1-flt3-itd突变质粒。
[0123]
flt3-itd片段的引物如下:
[0124]
primer-f:gccggaattagatctctcgagatgccggcgttggcgcgc(seq id no:1);
[0125]
primer-r:tagggggggggggcggaattcctacgaatcttcgacctgagcc(seq id no:2)。
[0126]
以migr1-flt3-itd为模板,设计flt3-itd-tkd突变目的片段引物,构建flt3-itd-tkd突变质粒。
[0127]
flt3-itd-tkd突变目的片段引物如下:
[0128]
f691l/fttttggaatactgttgctatggtgatcttctc(seq id no:3)f691l/rgcaacagtattccaaaatcaagtaaattggtcctga(seq id no:4)d835v/fggctcgagttatcatgagtgattccaactatgttgtc(seq id no:5)d835v/rtcatgataactcgagccaatccaaagtcacat(seq id no:6)d835y/fggctcgatatatcatgagtgattccaactatgttgtc(seq id no:7)d835y/rtcatgatatatcgagccaatccaaagtcacat(seq id no:8)d835f/fggctcgatttatcatgagtgattccaactatgttgtc(seq id no:9)
d835f/rtcatgataaatcgagccaatccaaagtcacat(seq id no:10)
[0129]
2.带有flt3-itd与flt3-itd-tkd突变的baf3细胞的构建
[0130]
使用构建的flt3-itd与flt3-itd-tkd突变质粒转染293t细胞,包装flt3-itd与flt3-itd-tkd逆转录病毒。使用flt3-itd与flt3-itd-tkd逆转录病毒感染baf3细胞,使用流式分选仪分选gfp阳性细胞即携带flt3-itd或flt3-itd-tkd突变的细胞。
[0131]
3.虚拟筛选与分子对接
[0132]
配体与受体结构处理:使用autodock vina版本1.1.2、autodock工具版本1.5.6和pymol版本2.3.3完成计算建模研究。flt3(pdb accession numbe 5x02)蛋白三维立体结构来源于proteindatabank数据库。蛋白结果处理由pymol软件处理,对原始结果进行加氢原子以及去除水分子,去掉原来的小分子化合物。另存为的.pdbt格式文件。通过pymol软件口袋模块识别结合位点。l3400临床化合物库(1481个分子)通过targetmol官方获取,导出mol格式后,通过open babel软件,把小分子化合物二维结构转换成三维结构,再进行加氢键,加电荷,然后另存为的.pdbt格式文件。
[0133]
分子对接:使用autodock vina 1.1.2对接到flt3的atp结合位点。每个配体对接5次,每次重复模拟产生20个姿势,每个配体总共产生100个姿势。从这些中,选择最高得分姿势(根据autodock vina估计的结合自由能)进行进一步分析。
[0134]
4.kx02与flt3分子对接
[0135]
使用autodock vina版本1.1.2、autodock工具版本1.5.6和pymol版本2.3.3完成计算建模研究[25]。flt-itd(残基587-947)的结构是根据蛋白质数据库登录号5x02[26]的序列制备。在制备大分子时,去除了所有的水分子,并在结构中加入了所有的极性氢。选择flt3的整个atp结合位点作为可能的配体结合位点地点kx02的坐标是使用dundee progrd2服务器生成的,它的初始配置通过gromacs力场最小化了能量。adt被用来给配体分配一个gasteiger电荷。在对接过程中,9个扭键被定义为可旋转的。autodock vina用于定义配体与flt-itd的对接。autodock vina根据δg值提供对接分数。在模型研究之后,排名最高的平均能量为-9.8kcal/mol。仅选取排名最高的分数进行可视化和pymol分析。
[0136]
5.celltiter-glo检测细胞活力
[0137]
celltiter-glo发光活细胞检测系统是一种可靠而灵敏检测细胞活力的方法。活细胞中存在atp,其含量直接反映了细胞数量和细胞状态。向细胞培养基加入celltiter-glo试剂,荧光素酶在细胞中atp的作用下催化荧光素发出荧光(波长为562nm),在光信号检测体系中,发光值与atp量成正比,atp含量与活细胞数成正比,因此检测到的荧光强度可以反映细胞活力。
[0138]
测量细胞活力时,将80ul浓度为6.25
×
10*4/ml生长状态良好的molm-13、mv4-11、baf3-flt3-itd、baf3-flt3-itd-691l、baf3-flt3-itd-d835y,baf3-flt3-itd-d835v,baf3-flt3-itd-d835f细胞种于96孔细胞培养板(每孔5000个细胞),然后加入20ul不同浓度的quizartinib(ac220)、kx02、gitertinib处理48小时。在每个培养孔中加入100ul celltiter-glo。室温孵育30分钟后,充分混匀取50ul转移至384孔板(每个96孔取2个重复)中于酶标仪检测荧光强度。
[0139]
6.临床样本的分离与培养
[0140]
取新鲜置于肝素抗凝管中的aml病人骨髓标本,用pbs稀释一倍。在15ml离心管中
加入与pbs稀释的骨髓样本等体积的ficoll分离液。然后用1ml移液枪将稀释好的骨髓样本沿管壁缓慢滴入ficoll页面上,注意不要破坏分层。然后于水平低温高速离心机2000rpm离心20分钟。离心后管内液体分为三层,上层为血浆和血小板,下层主要为红细胞。单个核细胞包括淋巴细胞和单核细胞位于中层界面处的白色混浊狭窄带。用1ml移液枪缓慢吸取至新的无菌15ml离心管,加入5倍液体体积的rpmi-1640培养液,混匀之后1500rpm离心10分钟。弃上清之后加入适量体积的1
×
红细胞裂解液,混匀之后室温静置5分钟,1500rpm离心5分钟,管底白色沉淀即为单个核细胞。使用适量rpmi-1640培养基重悬细胞沉淀,吸取20ul用countstar计算细胞密度及细胞活率,根据细胞密度及细胞活力进行冻存或用于后续实验。人单个核细胞于含5%二氧化碳的37℃恒温培养箱中使用补充了10ng/ml人干细胞因子,10ng/ml人il-3、10ng/ml人il-6的stemspan基本培养基中培养,并加入相应体积的100
×
青霉素链霉素双抗预防污染。
[0141]
7.flt3突变aml小鼠模型的建立与体内实验
[0142]
(1)flt3突变aml小鼠模型的建立:收集baf3-flt3-itd-691l细胞,调整细胞浓度为2
×
10^5/200ul,然后给每只balb/c小鼠尾静脉注射200ul(2
×
10^5个)baf3-flt3-itd-691l细胞。所有小鼠随机分为四组,包括甲基纤维素溶剂对照组、ac220组、kx02组,每组15只。
[0143]
(2)在注射细胞后的第四天,开始对小鼠进行给药。ac220使用5%甲基纤维素溶解,kx02使用30%peg300 5%dmso 65%水溶解,均使用灌胃法每天给药一次,给药剂量分别为ac220 10mg/kg,kx02 10mg/kg。
[0144]
(3)在给药的第四天和第八天,每只小鼠眼眶采血50ul于1.5ml ep管中。加入1ml 1
×
红细胞裂解液混匀,室温裂解红细胞5分钟。300rcf离心5分钟,弃去上层液体,用300ul pbs重悬细胞沉淀转移至流式管中,使用流式细胞仪分析gfp阳性细胞即白血病细胞baf3-flt3-itd-691l细胞的比例,以评估药物疗效。
[0145]
(4)在细胞注射后9天,每组小鼠各采用颈椎脱臼法处死三只。取出一侧胫骨,使用1ml注射针头吹出骨髓细胞,裂解红细胞后流式分析骨髓中gfp阳性细胞即白血病细胞baf3-flt3-itd-691l细胞的比例。同时取出小鼠的脾脏和肝脏做石蜡切片进行he染色,镜下观察脾脏中白血病细胞的浸润情况并拍照。
[0146]
(5)给药后每天称量各组小鼠体重。在溶剂对照组出现第一只死亡小鼠后所有分组停止给药,随访观察各组小鼠的生存状况并进行生存期统计分析。
[0147]
使用graphpad prism绘制kaplan-meier生存曲线并进行统计学分析。骨髓细胞及外周细胞阳性率均使用graphpad prism采取student's t检验进行统计学分析,统计学差异的大小用*表示如下:*表示p《0.05,**表示p《0.01,***表示p《0.001,****表示p《0.0001。
[0148]
实施例1
[0149]
kx02能抑制flt3-itd白血病细胞及耐药突变细胞的生长
[0150]
1.1 docking计算小分子化合物库与flt3的结合能力
[0151]
通过对l3400临床化合物库(1481个分子,来源于targetmol)与flt3(残基587-947)催化位点进行了分子对接模拟(抑制剂和亲和力见表1)筛选靶向flt3的化合物。flt3(pdb accession numbe 5x02)蛋白三维立体结构来源于proteindatabank数据库。使用autodock vina 1.1.2对接到flt3的atp结合位点。
[0152]
在制备大分子时,去除了所有的水分子,并在结构中加入了所有的极性氢。每个配体对接5次,每次重复模拟产生20个姿势,每个配体总共产生100个姿势。从这些中,选择最高得分姿势(根据autodock vina估计的结合自由能)进行进一步分析,对接结果按结合亲和力排序。
[0153]
使用flt3抑制剂crenolanib(-9.6kcal/umol)的结合能力作为临界值,发现有136种抑制剂的结合亲和力小于-9.6kcal/umol。值得注意的是,在这些抑制剂中,有13种小分子抑制剂被批准用于治疗白血病或白血病的临床试验(表2-1),其中8种已被证明是flt3抑制剂,包括crenolanib和sorafenib已被fda批准使用的药物。这一结果进一步证明了此筛选方法的可靠性。在其余5种抑制剂(即icg001(分子量548.6)、ly2090314(分子量512.5)、kx02(分子量431.5)、bemcentinib(分子量506.6)、idasanutlin(分子量616.5)5个化合物)中,kx02相对分子量较小,结构较简单(如图1所示),因此选择src/微管蛋白双重抑制剂kx02做进一步研究。
[0154]
表1. 13种候选小分子化合物与flt3的结合能力
[0155][0156]
[0157]
1.2 kx02对flt3-itd突变aml细胞的抑制作用
[0158]
为了探究kx02是否对flt3-itd突变细胞株具有杀伤作用,我们首先在携带flt3-itd突变的人类白血病细胞株molm13和mv4-11中使用cell titer-glo检测kx02和ac220用药48小时后细胞增殖的情况。
[0159]
结果显示,在这两株细胞中,kx02能显著抑制细胞增殖,从而诱导flt-itd突变的aml细胞株凋亡。kx02对flt3-itd的抑制作用逊于经典药物ac220(图2)。
[0160]
1.3 kx02对ac220耐药flt3突变细胞系的抑制作用
[0161]
如何克服flt3抑制剂治疗产生进一步的突变耐药是目前临床上比较突出的问题。通过对携带flt3-itd aml患者使用ac220后产生耐药后的基因组测序已经鉴定出各种的活化flt3-itd-tkd双重突变。发明人设计了临床鉴定的主要flt-itd-tkd突变体,包括ba/f3 flt3-itd、itd-f691l、itd-d835y、itd-d835v和itd-d835f,这些突变体均能转化小鼠细胞ba/f3使其不依赖il-3生存。
[0162]
接下来,用cell titer-glo评估了kx02在缺乏il-3的培养基中对转化细胞系在48小时的生长抑制作用。用il-3培养的正常ba/f3细胞系进行比较来评价药物的安全性。结果发现,ba/f3 flt3-itd对ac220和glitertinib高度敏感,但ba/f3 flt3-itd-f691l、ba/f3 flt3-itd-d835y、ba/f3 flt3-itd-d835v和ba/f3 flt3-itd-d835f对ac220均表现出明显耐药(图3a)。giltertinib作为临床上常用的第二代flt3抑制剂,临床证实对flt3-itd有效,但对flt3-itd-tkd的作用有限,尤其针对flt3-itd-f691l突变体,这与先前的研究一致(图3b)。
[0163]
图3c显示,kx02能显著抑制所有表达flt3-itd-tkd突变且对ii型flt3抑制剂(如ac220)耐药的ba/f3细胞生长,对flt3-itd表达ba/f3细胞也有抑制作用。作为评价kx02治疗效果的对照,ba/f3-itd-f691l细胞对kx02的敏感性是亲本细胞ba/f3的10倍(37nm vs 372nm)。更为重要的是,kx02对flt-itd-tkd突变耐药(ba/f3 flt3-itd-f691l、ba/f3 flt3-itd-d835y、ba/f3 flt3-itd-d835v和ba/f3 flt3-itd-d835f)的作用效果均明显优于ac220,在ba/f3 flt3-itd-f691l突变细胞株中,kx02的药效也优于giltertinib。
[0164]
kx02与ac220及glitertinib对flt3-itd-tkd突变细胞株的作用见下表2:
[0165]
表2.kx02与ac220及glitertinib对flt3-itd-tkd突变细胞株的作用
[0166][0167]
1.4 kx02对flt3突变的aml细胞及耐药突变的凋亡影响
[0168]
诱导肿瘤细胞凋亡是抗肿瘤药物的主要作用方式之一,为了探究kx02对携带flt3突变aml细胞的凋亡作用的影响,首先在人白血病细胞molm-13和mv4-11中使用浓度为0、25nm、50nm、100nm的kx02处理,使用annexin v-apc/pi流式细胞术检测kx02对细胞的促凋亡作用。
[0169]
流式结果显示,在kx02对molm13和mv4-11细胞的促凋亡作用均呈现剂量依赖性。在mv4-11中凋亡细胞的比例分别是8.12%、19.37%、23.75%、27.4%,而在molm13细胞比例则为3.12%、7.91%、18.9%、24.1%(图4)。
[0170]
接下来观察了kx02对ac220耐药的flt3-itd-tkd双重突变的作用效果,包括ba/f3 flt3-itd、ba/f3 itd-f691l、ba/f3 itd-d835y、ba/f3 itd-d835v和ba/f3 itd-d835f,同时以il-3培养的ba/f3细胞系进行对比来评估其安全性。kx02的浓度依次为0、25nm、50nm、100nm,使用annexin v-apc/pi流式细胞术检测kx02在诱导耐药突变细胞凋亡的作用。
[0171]
流式结果显示(图5),kx02对上述耐药细胞株均有促凋亡作用,且呈现剂量依赖性。在ba/f3中凋亡细胞的比例分别是6.13%、7.13%、10.60%、11.30%,在flt3-itd细胞的凋亡细胞比例则为4.49%、6.17%、14.70%、17.10%,而在耐药突变flt3-itd-d835y细胞的比例为6.61%、11.10%、16.70%、23.10%以及flt3-itd-df691l细胞的比例为7.12%、10.70%、17.90%、22.30%。kx02只对突变细胞株有促凋亡作用,而对ba/f3正常的小鼠细胞基本没有促进凋亡的作用。这些结果表明,kx02可能特异针对flt3靶点,从而起到抗肿瘤的作用。
[0172]
1.5kx02对flt3突变的aml细胞及耐药突变的细胞周期影响
[0173]
kx02作为一个双靶点药物,在高浓度时具有抑制微管蛋白的作用,微管蛋白聚合受阻后会导致细胞周期阻滞,因此检测了kx02对flt3-itd突变细胞株mv4-11和molom13细胞周期的影响。
[0174]
结果发现,在kx02处理后,两株细胞均呈现g0/g1期、s期细胞比例减少,g2/m期细胞比例增加,并呈现剂量效应关系,说明kx02能使flt3-itd突变细胞发生g2/m期阻滞(图
d835y细胞系)12小时后的flt3相关信号通路关键分子检测,结果与molm13、mv4-11一致(图11),由此可见微管抑制剂并不能改变flt3及其下游通路。进一步证明kx02可以特异性靶向flt3蛋白,从而抑制flt3及其下游通路。而不是抑制微管蛋白的靶点起作用。
[0188]
2.3 kx02破坏了molm13细胞的微管
[0189]
除了src抑制,kx02被证实抑制微管聚合。为了测试kx02是否可以直接影响微管蛋白的结构,同时微管蛋白聚合剂(紫杉醇)和微管蛋白解聚剂(秋水仙碱和长春新碱)用作阳性对照。用浓度100nmol/l的kx02、100nmol/l紫杉醇、100nmol/l长春新碱以及100nmol/l秋水仙素或dmso处理了molm13细胞4小时,然后固定和染色α/β-微管蛋白抗体alexa fluor-488偶联的抗兔抗体和dapi,通过荧光显微镜观察微管蛋白结构和细胞核。
[0190]
图12显示,对照细胞中的微管网络表现出正常的排列,微管在整个细胞中遍历,细胞核完整且外观正常。秋水仙碱和长春碱会抑制微管蛋白的聚合,紫杉醇会促进其过度聚合成异常的微管。而用kx02处理的细胞具有较小的微管网络,在整个细胞质中可见弥漫性染色,kx02在体外显著抑制了molm13细胞中微管的形成。这和微管蛋白解聚剂秋水仙碱和长春新碱结果相似,与紫杉醇导致染色更深的微管阵列相反。
[0191]
上述试验证实,kx02以秋水仙碱或长春碱样的方式抑制微管蛋白的聚合,证实kx02是在人白血病细胞molm13也起到微管抑制的作用,从而和flt3抑制共同组成双靶点抑制剂,共同发挥抗肿瘤的作用。
[0192]
2.4微管抑制剂可在体外增强flt3抑制剂抑制白血病细胞的生长的效果
[0193]
为探究kx02对flt3-itd flt3抑制剂ac220与微管抑制剂联合应用对flt3突变型aml的杀伤作用,首先使用跟kx02作用靶点相似的微管抑制剂mp-hj-1b作为参考,然后在两株flt3-itd阳性aml细胞株molm-13和mv4-11分别观察微管抑制剂mp-hj-1b和flt3抑制剂ac220单独使用或联合用药诱导细胞杀伤的情况。将细胞均匀种于96孔板中,然后以不同浓度的ac220加dsam0、50nμ、100nμmp-hj-1b处理48小时后用celltiter-glo检测两药合加的细胞生长情况并且统计两药合加的协同指数。
[0194]
实验结果发现,应用微管抑制剂mp-hj-1b可以增强对ac220在flt3-itd阳性aml细胞株molm-13和mv4-11的杀伤作用(图13)。
[0195]
实施例3
[0196]
分子对接研究揭示了kx02与flt3的分子相互作用
[0197]
为了进一步了解kx02在结构水平上对突变flt3的抑制活性,对flt3(5x02)进行了计算建模。与flt3(残基587-947)催化位点)进行了分子对接模拟,kx02被用来与atp结合位点对接。flt3(pdb accession numbe 5x02)蛋白三维立体结构来源于proteindatabank数据库。使用autodock vina 1.1.2对接到flt3的atp结合位点。在制备大分子时,去除了所有的水分子,并在结构中加入了所有的极性氢。对接研究显示kx02在atp结合位点有9个不同的结合位置。选择结合能最低的位置(-9.8kcal/mol)进行分析。
[0198]
对接结果表明(图14),kx02与flt3蛋白结合良好,可能的结合位点包括leu-616、val-624和glu-661等氨基酸残基。kx02的非极性氢原子与leu-616和glu-661残基的活性基团之间的氢键为和远小于传统氢键的进一步发现val-624氨基酸的r基团能与kx02六元环吡啶形成p-π共轭结构,这对提高kx02在蛋白质囊中的稳定性有重要作用。此外,化合物和蛋白质的活性口袋也具有较强的疏水作用和范德华力。这些相互作用力能
有效地提高化合物kx02在flt3蛋白活性囊中的稳定性,是一种潜在的抑制剂。
[0199]
为了进一步明确flt3与kx02相互作用,选择来源于proteindatabank数据库另外的flt3(pdb accession numbe 4r 4rt7)蛋白三维立体结构,按照上述同样的方法,对接研究显示kx02在atp结合位点有9个不同的结合位置。选择结合能最低的位置(-9.1kcal/mol)进行分析。
[0200]
对接结果表明(图15),kx02与flt3蛋白结合良好,可能的结合位点包括cys-694等氨基酸残基。kx02的非极性氢原子与leu-694残基的活性基团之间的氢键为远小于传统氢键的此外,化合物和蛋白质的活性口袋也具有较强的疏水作用和范德华力。通过两种不同的结晶与kx02都结合,这更加验证了kx02是一种潜在的抑制剂
[0201]
实施例4
[0202]
kx02显著抑制flt3-itd原代细胞的作用
[0203]
4.1 kx02对flt3-itd白血病患者的原代骨髓细胞抑制作用
[0204]
收集了瑞金医院4例诊断明确的flt3-itd阳性aml患者骨髓细胞样本和两例flt3-itd,flt3-d835y的aml患者骨髓细胞样本,随后分离得到骨髓单个核细胞后,将细胞均匀的铺于96孔板上,随后以不同浓度的kx02处理48小时后celltiter-glo实验检测细胞活率,同时以ac220作为阳性对照。
[0205]
这些结果显示(图16),kx02可以显著的抑制flt3-itd阳性aml患者的骨髓细胞生长,起到杀伤肿瘤细胞的作用,且呈剂量效应关系,达到与ac220相当的治疗水平。值得注意的是,两例flt3-itd,flt3-d835y的aml患者的骨髓细胞样本对ac220反应性差,但能被kx02显著抑制。这也说明kx02在携带flt3-itd突变的患者可以达到ac220的治疗效果,而当患者其同时携带flt3-d835y突变,则ac220的效果远不如kx02。
[0206]
4.2 kx02对flt3-itd白血病患者原代骨髓细胞的磷酸化flt3影响
[0207]
使用三例收集的骨髓细胞样本来验证kx02是否可以在携带flt3-itd突变的原代骨髓白血病细胞起到同样的作用。分别使用不同浓度的kx02(0、25nm、50nm、100nm)处理骨髓样本,12小时后,收集蛋白后通过western blot检测磷酸化flt3以及总的flt3蛋白水平。
[0208]
结果显示,随着药物浓度的递增,磷酸化flt3逐渐减弱(图17)。上述结果提示,kx02在原代细胞也可以抑制flt3磷酸化水平,从而抑制其下游信号通路在诱导细胞凋亡中起到重要作用。
[0209]
实施例5
[0210]
kx02显著延长flt3-itd-f691l白血病模型小鼠的生存时间
[0211]
5.1 kx02显著延缓flt3-itd-f691l白血病小鼠发病
[0212]
在动物研究中使用了baf3 flt3/itd-f691l急性白血病小鼠模型。
[0213]
收集baf3-flt3-itd-691l细胞,然后给每只balb/c小鼠尾静脉注射200ul(2
×
10^5个细胞)。将所有小鼠随机分为3组,注射细胞后的第4天开始每天对小鼠进行灌胃给药,包括甲基纤维素溶剂对照组、ac220组(10mg/kg)、kx02组(10mg/kg),对照组第一只小鼠死亡后各组小鼠均停止给药。在给药后的第4天和第8天分别采集小鼠的外周血,通过流式检测gfp阳性细胞的比率来确定小鼠白血病负荷。
[0214]
结果显示,治疗4天后,对照组和ac220组的gfp率分别为8.5%和7.0%,但kx02治疗组的外周血中几乎没有白血病细胞。同样,在治疗第8天,对照组(38.9%)和ac220组
(30.1%)的gfp率显著增加。重要的是,两次随访外周血,kx02治疗组的外周血中几乎没有白血病细胞(图18,p《0.001),kx02能明显延长白血病小鼠模型的发病。
[0215]
整个治疗过程中,随访每只小鼠体重,发现在治疗期间小鼠体重没有明显改变,后期体重略有所增加(图19),说明对该剂量kx02小分子药物对小鼠的副作用不大。
[0216]
在小鼠注射白血病细胞的第10天(用药1周),从三组中每组随机抽取一只小鼠安乐死并解剖,取出脾脏和肝脏称重并拍照。与对照组和ac220组相比,kx02治疗组的脾脏和肝脏都比较正常,而其他两组脾脏和肝脏明显增大以及体重增加(图20)。
[0217]
随后将注射白血病细胞第10天处死的各组小鼠脾脏和肝脏进行伊红(h&e)染色并于镜下观察白血病细胞的浸润情况。结果发现kx02处理组脾脏和肝脏中白血病细胞的浸润均要明显少于对照组和ac220组(图21),相比于ac220,kx02更能延缓双突变白血病小鼠的发病。
[0218]
此外,还通过流式细胞术检测骨髓和脾脏中的白血病细胞(即gfp阳性细胞比例)。结果显示,kx02治疗后,骨髓中白血病细胞占3%,而对照组为62.8%,ac220组为53.3%;与骨髓样本相似,kx02组脾脏中未检出白血病细胞,对照组为62.8%,ac220组为54%(图22)。说明此时kx02处理组小鼠尚未明显发病,亦无肝脾浸润。
[0219]
5.2 kx02显著延长flt3-itd-f691l白血病模型小鼠的生存期
[0220]
三个给药组的小鼠每天持续灌胃给药,直到对照组小鼠开始死亡,然后停止继续给药以观察小鼠的生存和死亡情况并做生存期统计。
[0221]
结果显示,与对照组给药组相比,ac220单独治疗并未延长中位生存期(13天vs 12天),这也与之前相关文献报道一致,该结果表明ac220对itd-f691l具有耐药性。kx02在中位生存期方面显示出显著的治疗效果,从对照组的12天显著延长到23天(图23,p《0.0001)。kx02治疗效果明显优于其他两组。
[0222]
体内小鼠实验证明,kx02化合物在动物体内也具有不错的治疗效果,能克服目前flt3抑制剂治疗后产生的二次突变的耐药。具有一定的临床转化的意义。
[0223]
讨论
[0224]
flt3是在急性髓系白血病最有希望的靶点之一,flt3突变是aml中最常见的基因改变,且预后不良相关,因此flt3抑制剂一直在积极的临床开发中。在目前临床上的多种flt3抑制剂中,主要分为第一代和第二代flt3抑制剂。
[0225]
然而不管是第一代还是第二代flt3抑制剂,它们所面临的共同的主要问题是绝大部分患者在使用不到半年的时间会产生进一步的耐药突变。已经明确的索拉菲尼和奎扎替尼产生最常见的耐药突变主要是f691l、d835y/f/v和y842c等,而giltertinib则会产生f691l的突变从而导致耐药。由于tkd获得性点突变导致对flt3抑制剂的耐药性限制了疗效,并且“看门人”突变f691l对所有现有的flt3抑制剂都具有耐药性。因此,寻找有效、安全的药物克服f691l等突变引起的耐药性仍是临床亟待解决的问题。
[0226]
本发明中,发明人确定kx02具有有效的抗flt3-itd突变白血病细胞作用。在细胞、整体动物及临床标本证实kx02是一种有效的flt3抑制剂,尤其针对flt3-itd-tkd双重耐药突变。它能有效抑制flt3自身磷酸化及其下游信号通路,包括stat5和mapk在aml细胞系和携带flt3-itd突变的患者源性aml细胞中的表达。分子对接研究表明kx02直接与flt3结合抑制其活性。更重要的是,发明人发现kx02对表达flt3-itd-d835y/v/f-和flt3-itd-f691l
的baf3细胞也有很强的抑制作用,这些细胞具有ac220抗性。使用小鼠模型进行的体内研究表明,口服kx02可保持其抗flt3-itd-f691l突变的活性,并显著延长flt3-itd-f691l细胞移植白血病小鼠的存活时间。
[0227]
除了开发新一代的flt3抑制剂解决目前面临的耐药性的问题之外。在临床试验中,将flt3抑制剂与其他药物组合使用是克服目前对flt3 tki耐药性的主要解决方案之一。在本发明中,kx02同时作为微管抑制剂,通过免疫荧光等实验方法证明,抑制微管的一个靶点也起到了重要作用,因此kx02作为一个flt3和微管双靶点抑制剂,可能在耐药突变起到重要作用。
[0228]
自从flt3抑制剂应用于临床以来,耐药突变已成为flt3抑制剂治疗的关键问题。在这项发明中,证明kx02是一种有效的、选择性和口服生物利用度好的flt3激酶抑制剂。在小鼠模型中,它显示出显著的抗肿瘤活性,尤其针对flt3-itd-tkd耐药突变,在体内表现出良好的耐受性。kx02目前处于临床前开发的晚期。未来的临床实验有可能会验证该化合物治疗flt3突变型aml的疗效。kx02可作为一种治疗选择,尤其是在使用现有flt3抑制剂后出现耐药性的患者。本发明为将来的临床转化提供重要的理论依据与实验基础,同时也为设计flt3靶点提供了新的思路。
[0229]
在本发明提及的所有文献都在本技术中引用作为参考,就如同每一篇文献被单独引用作为参考那样。此外应理解,在阅读了本发明的上述讲授内容之后,本领域技术人员可以对本发明作各种改动或修改,这些等价形式同样落于本技术所附权利要求书所限定的范围。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。