rab 35或其下游调控分子在治疗骨折后慢性疼痛中的应用
技术领域
1.本发明属于生物医药领域,涉及rab 35或其下游调控分子在治疗骨折后慢性疼痛中的应用。
背景技术:
2.随着我国工业、建筑、交通等行业高速发展及人口老龄化加剧,导致工业意外事故、建筑伤、交通伤和老年骨质疏松性骨折的发生也随之增加。据统计,我国每年发生创伤性骨折的人数已超过440万, 全世界每年患骨质疏松性骨折的人数约为900万。骨折后慢性疼痛是继发于骨折后的一种慢性疼痛状态,不仅症状严重,而且发病率高,尚无有效的治疗措施。有报道,踝关节和腕关节骨折后慢性疼痛的发生率高达61.7%,胫骨骨折后慢性疼痛的发生率为55.1%。严重的疼痛不仅妨碍患者早期复健和骨骼肌肉功能恢复,还将增加患者心脑血管意外、抑郁症、急性创伤后认知功能障碍(post-traumatic cognitive dysfunction)和慢性复杂区域疼痛综合征(complex regional pain syndrome)发生的风险,严重影响患者生活质量,加重患者家庭及社会经济负担,已成为亟待解决的重要公共健康问题。而骨折后慢性疼痛的发生机理尚不清楚,是当今疼痛领域的研究热点之一。
3.研究表明,rab gtpases 作为分子开关,在gtp结合的活性形式和gdp结合的非活性形式之间转换,能够调节神经元细胞的内吞和轴突运输,参与多种神经类疾病的病理进程,如阿尔兹海默病(alzheimer’s disease,ad)、帕金森病(parkinson’s disease,pd)等疾病,但在骨折后慢性疼痛中未见研究。本研究通过vivo-morpholino干扰,行为学测定等手段,围绕调控膜泡运输的rab gtp酶家族蛋白rab35,研究其在骨折后慢性疼痛中的作用。
技术实现要素:
4.根据本发明的一个方面,本发明提供了一种药物组合物,所述药物组合物包括rab 35或其下游调控分子功能性表达的抑制剂。
5.进一步,所述抑制剂包括降低rab 35或其下游调控分子mrna或蛋白水平,或降低rab 35蛋白或其下游调控分子蛋白活性的试剂。
6.进一步,所述抑制剂包括核酸抑制剂,蛋白抑制剂,蛋白水解酶,蛋白结合分子;优选地,所述抑制剂为核酸抑制剂。
7.进一步,所述核酸抑制剂选自shrna、小干扰rna、dsrna、微小rna、反义核酸或其构建物。
8.进一步,所述药物组合物包括药学上可接受的载体。
9.进一步,rab 35的下游调控分子是secretogranin ii。
10.根据本发明的另一个方面,本发明还提供了rab 35或其下游调控分子功能性表达的抑制剂在制备预防或治疗骨折后慢性疼痛的药物中的应用。
11.进一步,所述抑制剂包括降低rab 35或其下游调控分子mrna或蛋白水平,或降低rab 35蛋白或其下游调控分子蛋白活性的试剂;
进一步,所述抑制剂包括核酸抑制剂,蛋白抑制剂,蛋白水解酶,蛋白结合分子;优选地,所述抑制剂为核酸抑制剂。
12.进一步,所述核酸抑制剂选自shrna、小干扰rna、dsrna、微小rna、反义核酸或其构建物。
13.进一步,所述药物组合物包括药学上可接受的载体。
14.进一步,rab 35的下游调控分子是secretogranin ii。
附图说明
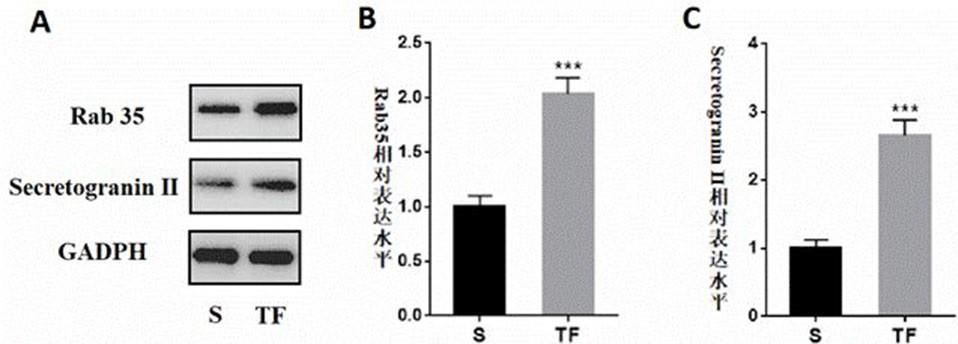
15.图1显示骨折后慢性疼痛小鼠脊髓rab 35及secretogranin ii表达结果图,其中a:免疫印迹图;b:柱状统计图。***p《0 .001,与s组相比;图2注射rab 35 morpholino缓解小鼠骨折后导致机械痛和热痛的结果图,其中a:机械缩足反应阈(mwf(%));b:热缩足潜伏期(twl);***p《0 .001;
&&& p《0 .001;图3显示secretogranin ii表达结果图,其中a:免疫印迹图;b:柱状统计图;***p《0 .001;
&&& p《0 .001。
具体实施方式
16.下面结合附图和实施例对本发明作进一步详细的说明。以下实施例仅用于说明本发明而不用于限制本发明的范围。实施例中未注明具体条件的实验方法,通常按照常规条件,例如sambrook 等人,分子克隆:实验室手册(new york: cold spring harborlaboratory press, 1989)中所述的条件,或按照制造厂商所建议的条件。
17.本发明公开了一种药物组合物,所述药物组合物包括rab 35或其下游调控分子功能性表达的抑制剂;所述抑制剂是指任何可降低rab 35或其下游调控分子基因或表达产物稳定性、下调rab 35或其下游调控分子的表达、降低rab 35或其下游调控分子的有效作用时间或抑制rab 35或其下游调控分子基因的转录的物质,这些物质均可用于本发明,作为对于下调rab 35或其下游调控分子的表达有用的物质,从而可用于疾骨折后慢性疼痛治疗。
18.作为本发明的一种选择方式,所述的rab 35或其下游调控分子的抑制剂是一种特异性与rab 35或其下游调控分子结合的抗体。所述特异性抗体包括单克隆抗体、多克隆抗体;本发明不仅包括完整的抗体分子,也包括抗体的任何片段或修饰,例如,嵌合抗体、scfv、fab、f(ab’)2、fv等。只要所述片段能够保留与rab 35或其下游调控分子蛋白的结合能力即可。用于蛋白质水平的抗体的制备时本领域技术人员公知的,并且本发明可以使用任何方法来制备所述抗体。
19.作为本发明的一种优选方式,所述rab 35或其下游调控分子的抑制剂是一种rab 35或其下游调控分子特异性的小干扰rna分子。如本文所用,所述的“小干扰rna”是指一种短片段双链rna分子,能够以同源互补序列的mrna为靶目标降解特定的mrna,这个过程就是rna干扰(rna interference)过程。小干扰rna可以制备成双链核酸的形式,它含有一个正义链和一个反义链,这两条链仅在杂交的条件下形成双链。一个双链rna复合物可以由相互分离的正义链和反义链来制备。因此,举例来讲,互补的正义链和反义链是化学合成的,其后可通过退火杂交,产生合成的双链rna复合物。
20.本发明的核酸抑制物如sirna可以化学合成,也可以通过一个重组核酸结构里的表达盒转录成单链rna之后进行制备。sirna等核酸抑制物,可通过采用适当的转染试剂被输送到细胞内,或还可采用本领域已知的多种技术被输送到细胞内。
21.作为本发明的一种可选方式,所述的rab 35或其下游调控分子的抑制剂也可以是一种“小发夹rna(small hairpin rna,shrna)”,其是能够形成发夹结构的非编码小rna分子,小发夹rna能够通过rna干扰途径来抑制基因的表达。如上述,shrna可以由双链dna模板来表达。双链dna模板被插进一个载体,例如质粒或病毒载体,然后在体外或体内连接到一个启动子进行表达。shrna在真核细胞内dicer酶的作用下,可被切割成小干扰rna分子,从而进入rnai途径。“shrna表达载体”是指一些本领域常规用于构建shrna结构的质粒,通常该质粒上存在“间隔序列”以及位于“间隔序列”两边的多克隆位点或供替换序列,从而人们可以将shrna(或类似物)相应的dna序列通过正向和反向的方式插入多克隆位点或替换其上的供替换序列,该dna序列转录后的rna可形成shrna(short hairpin)结构。所述的“shrna表达载体”目前已经完全可以通过商购的途径购买获得,例如一些病毒载体。
22.作为本发明的一种优选地实施方式,所述rab 35或其下游调控分子的抑制剂是反义寡核苷酸。所述反义寡核苷酸具有与目的序列互补的序列,并且通过所述互补序列,可以实现目的基因的抑制,所述反义寡核苷酸是核糖核酸或dna。作为一种优选地实施方式,反义寡核苷酸包含至少一个化学改性。反义寡核苷酸能包含一个或一个以上的锁核酸(lnas,locked nucleicacids)。锁核酸为改性核糖核酸,在核糖部位的2’至4’碳之间包含额外的桥键,来具有锁定(locked)形态,并以此具有锁核酸的寡核苷酸具有改善的热稳定性。择一性地,反义寡核苷酸可包含肽核酸(pna,peptide nucleic acids),并且反义寡核苷酸包含基于肽的主链来代替糖-磷酸主链。反义寡核苷酸能包含的其他化学改性包括:如2
’‑
o-烷基(例如,2
’‑
o-甲基,2
’‑
o-甲氧基乙基)、2
’‑
氟及4
’‑
硫氧改性一样的糖改性;硫代磷酸、吗啉代或磷羧酸键之类的主链改性。反义寡核苷酸的长度为7-50核苷酸,优选为10-40核苷酸,更优选为15-30核苷酸,最优选为20-25核苷酸。
23.本发明的具体实施方案中,所述rab 35或其下游调控分子的抑制剂是反义寡核苷酸技术改进后的morpholino技术中使用的试剂。
24.本发明所涉及的药物组合物除了包括活性成分,还包括药学上可接受的载体。所述药学上可接受的载体,包括(但不限于)稀释剂、粘合剂、表面活性剂、致湿剂、吸附载体、润滑剂、填充剂、崩解剂。
25.其中,稀释剂如乳糖、氯化钠、葡萄糖、尿素、淀粉、水等;粘合剂如淀粉、预胶化淀粉、糊精、麦芽糖糊精、蔗糖、阿拉伯胶、明胶、甲基纤维素、羧甲基纤维素、乙基纤维素、聚乙烯醇、聚乙二醇、聚乙烯比咯烷酮、海藻酸及海藻酸盐、黄原胶、羟丙基纤维素和羟丙基甲基纤维素等;表面活性剂如聚氧化乙烯山梨聚糖脂肪酸酯、十二烷基硫酸钠、硬脂酸单甘油酯、十六烷醇等;致湿剂如甘油、淀粉等;吸附载体如淀粉、乳糖、斑脱土、硅胶、高岭土和皂粘土等;润滑剂如硬脂酸锌、单硬脂酸甘油酯、聚乙二醇、滑石粉、硬脂酸钙和镁、聚乙二醇、硼酸粉末、氢化植物油、硬脂富马酸钠、聚氧乙烯单硬脂酸酯、单月桂蔗糖酸酯、月桂醇硫酸钠、月桂醇硫酸镁、十二烷基硫酸镁等;填充剂如甘露醇(粒状或粉状)、木糖醇、山梨醇、麦芽糖、赤藓糖、微晶纤维素、聚合糖、偶合糖、葡萄糖、乳糖、蔗糖、糊精、淀粉、海藻酸钠、海带多糖粉末、琼脂粉末、碳酸钙和碳酸氢钠等;崩解剂如交联乙烯吡咯烷酮、羧甲基淀粉钠、低
取代羟丙基甲基、交联羧甲基纤维素钠、大豆多糖等。
26.本发明中的药物组合物还可以包括稳定剂、杀菌剂、缓冲剂、等渗剂、螯合剂、ph控制剂及表面活性剂等添加剂。
27.其中,稳定剂包括人类血清蛋白、l-氨基酸、糖及纤维素衍生物。l-氨基酸还可以包括甘氨酸、半胱氨酸及谷氨酸中的任意一个。糖类包括单糖,例如葡萄糖、甘露糖、半乳糖、果糖等;糖醇,例如甘露醇、纤维醇、木糖醇等;二糖,例如蔗糖、麦芽糖、乳糖等;多聚糖,例如葡聚糖、羟丙基淀粉、硫化软骨素、透明质酸等及它们的衍生物。纤维素衍生物包括甲基纤维素、乙基纤维素、羟乙基纤维素、羟丙基纤维素、羟丙甲基纤维素及羟甲基纤维素钠。表面活性剂包括离子或非离子表面活性剂,例如聚氧化乙烯烷基酯、山梨聚糖单酰基酯、脂肪酸甘油酯。添加剂缓冲剂可以包括硼酸、磷酸、乙酸、柠檬酸、谷氨酸及相应的盐(它们的碱金属或碱性稀土金属盐,例如钠盐、钾盐、钙盐及镁盐)。等渗剂包括氯化钾、氯化钠、糖及甘油。螯合剂包括乙二胺四乙酸钠及柠檬酸。
28.本发明所述药物组合物可口服给药、非胃肠道给药、通过吸入喷雾给药、局部给药、直肠给药、鼻给药、颊给药、阴道给药或通过植入的贮药装置给药。优选口服给药或注射给药。本发明药物组合物可含有任何常用的无毒可药用载体、辅料或赋形剂。
29.在治疗过程中,可以根据症状的严重程度、复发的频率和治疗方案的生理应答,调整本发明药物组合物的剂量。
30.实施例 rab35在骨折后慢性疼痛中的应用一、实验步骤(1)实验分组:健康雄性c57bl6小鼠18只,2月龄,由中国北京军事医学科学院实验动物中心提供。采用随机数字表法分为3组(n=6):假手术组(s组):小鼠麻醉后,备皮,消毒,铺巾,切皮,拨开软组织,不行胫骨骨折,逐层缝合伤口;胫骨骨折慢性疼痛模型(tf组) :按照下述方法制作模型;rab 35 morpholino 胫骨骨折慢性疼痛模型(rmo tf组) :在制作胫骨骨折慢性疼痛模型前24h,经l5-6椎间隙穿刺注射,注射rab 35 morpholino 10μl。rab 35 morpholino: 5
′‑
tccacttcccgaacaaacagccgga-3
′
(gene tools, philomath,or,usa),按照说明书稀释成1 mm 母液,分装储存。
31.(2)小鼠胫骨骨折慢性疼痛模型:选取健康成年雄性 c57bl/6 小鼠(购自中国人民解放军军事医学科学院实验动物中心),使用七氟醚(麻醉诱导 3%;麻醉维持 1.5%)吸入麻醉,将动物侧卧位固定于手术台上,常规备皮,消毒,铺巾,于小鼠右膝下切开皮肤,逐层剥离软组织,暴露胫骨,于骨髓腔内插入0.7mm 不锈钢针,固定后用手术钳于胫骨中段断裂,术毕缝合伤口。
32.(3)鞘内给药:使用七氟醚(麻醉诱导3%;麻醉维持1.5%)吸入麻醉,将大鼠俯卧,备皮,消毒,以微量注射器从椎间隙垂直缓慢进针,直接用微量注射器连接30g针头经l5-6椎间隙穿刺注射,注射rab 35 morpholino,可特异性敲低rab 35 表达。
33.(4)行为学实验:于模型前24 h(t0)、制作骨折模型后1、3、7和14d(t1-4)时测定机械缩足频率(the frequency of the mechanical foot contraction response, mwf(%))和热缩足潜伏期(thermal foot contraction latency,twl),测试前使小鼠适应15 min。
采用bsevf3电子von frey纤维丝(harvard apparatus公司,美国)测定mwf(%)。以von frey纤维丝对大鼠右后足2、3趾骨间垂直施加刺激,记录出现阳性反应(如快速缩足反应、舔舐右足或嘶叫)的刺激力度,连续测定10次,间隔1 min,取缩足频率为mwf(%)。
34.采用红外足底测痛仪(iict life science 390)测定twl,记录从左后足接触热板至出现回缩、踮脚、挣扎、嘶叫、舐足任一反应的时间为twl,连续测定3次,间隔5min,取平均值作为pwl(sec)。为防止烫伤鼠爪,twl上限定设置为20s。
35.(5)western blot:采用western blot法测定蛋白的表达。于最后1次行为学测定结束后,处死大鼠,取脊髓l4-6节段,加入预冷的组织蛋白裂解液,研磨成组织匀浆。将匀浆液4℃离心5min,12000rpm,离心半径10cm,上清液即为脊髓组织总蛋白。使用rab35(abcam,英国),secretogranin ii(leading biology公司,美国),gadph一抗(abcam,英国),按照说明书的指南进行实验测定rab35,secretogranin ii, gadph的相对表达。
36.(6)统计学分析:采用spss 18 .0统计学软件进行分析,正态分布的计量资料以均数
±ꢀ
标准差(
±ꢀ
s)表示,随机区组设计的计量资料比较采用单因素方差分析,重复测量设计的计量资料比较采用重复测量设计的方差分析,p《0.05为差异具有统计学意义。
37.二、实验结果(1) 骨折后慢性疼痛小鼠脊髓rab 35及secretogranin ii表达增加。
38.结果如图1所示,在骨折后14天最后一次行为学后,处死小鼠取脊髓l4-6,在western blot结果发现:与生理盐水组(c组)相比,骨折后慢性疼痛小鼠脊髓rab 35及secretogranin ii表达增加,证明rab 35及secretogranin ii参与骨折后小鼠发生慢性疼痛的过程。
39.(2) 注射rab 35 morpholino缓解了小鼠骨折后导致机械痛和热痛结果如图2所示,与假手术组(s组)相比,胫骨骨折组 (tf组) 小鼠术后1、3、7和14d(t1-4)mwf(%)显著增加,热缩足潜伏期(twl)缩短(***p《0 .001)。这些结果表明,小鼠胫骨骨折所致机械性触诱发痛(图2a)和热刺激诱发痛(图2b)发生于术后3天,于7~14天达高峰,证实胫骨骨折能诱发慢性疼痛。
40.与tf组比较,注射rab 35 morpholino组(rmo tf组)的mwf(%)显著降低,twl显著延长(&&&p《0 .001),说明抑制rab 35的表达可以缓解小鼠骨折后导致机械痛和热痛。
41.3) rab 35通过secretogranin ii缓解小鼠骨折后导致机械痛和热痛在骨折后14天最后一次行为学后,处死小鼠取脊髓l4-6,在western blot结果发现:与tf组比较,注射rab 35 morpholino组(rmo tf组)的secretogranin ii表达减低,证明rab 35通过secretogranin ii缓解小鼠骨折后导致机械痛和热痛(图3)。
42.尽管本发明的具体实施方式已经得到详细的描述,但本领域技术人员将理解:根据已经公布的所有教导,可以对细节进行各种修改和变动,并且这些改变均在本发明的保护范围之内。本发明的全部分为由所附权利要求及其任何等同物给出。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。